修饰核酸缀合物
1.本发明涉及一种核酸缀合物,其包含至少一个2’,3
’‑
o缩酮部分。该缀合物适合用于以高功效将核酸分子的靶标特异性或靶标选择性递送到细胞(诸如哺乳动物细胞,包括人细胞)中。因此,提供了用于治疗性核酸分子(包括反义分子和sirna分子或前体或此类分子的修饰)的新的递送媒介物。
2.wo 2014/048969描述了核脂质(nucleolipid)和用于制备核脂质的方法。特别地,描述了包含脂质2’,3
’‑
o缩酮部分的核苷酸。发现这些核苷酸在某些癌细胞中具有药物活性。然而,未公开将包含2’,3
’‑
o缩酮部分的核酸分子递送到靶细胞中。
3.本发明的目的是提供核酸分子,其可以以高功效被递送到靶细胞中。
4.本发明人已经发现,将2’,3
’‑
o缩酮部分附接至核酸分子、特别是附接至核酸链的3
’‑
端和/或5
’‑
端可以增加向靶细胞中的递送、特别是向靶细胞或靶生物体中的体内递送。因此,提供了具有改进的特性的治疗性或诊断性核酸缀合物。
5.本发明的第一方面是式(i)的核酸缀合物,其包含至少一个2’,3
’‑
o-缩酮部分:
[0006][0007]
其中
[0008]
x是核酸分子,
[0009]
b是核碱基,和
[0010]
r1和r2彼此独立地是烃基团,其中所述烃基团任选地包含一个或多个杂原子,诸如n、o、p、s、或卤素。
[0011]
应理解,本发明还包括式(i)和本文的任何其他式中所描绘的化合物的任何立体异构体、盐和溶剂化物。
[0012]
式(i)的核酸缀合物包含核酸分子x,其中至少一个2’,3
’‑
o-缩酮部分附接至该核酸分子x。
[0013]
术语“核酸分子”是指包含至少两个核苷酸构建单元的任何类型的寡核苷酸或多核苷酸。核酸分子可以包含核糖核苷酸构建单元、2
’‑
脱氧核糖核苷酸构建单元、修饰核苷酸构建单元或其任何组合。在某些实施方案中,核酸分子是任选地包含至少一个修饰核苷酸构建单元和/或至少一个2
’‑
脱氧核糖核苷酸构建单元的rna分子、任选地包含至少一个修饰核苷酸构建单元和/或至少一个核糖核苷酸构建单元的dna分子、或由修饰核苷酸构建单元组成的核酸类似物分子。
[0014]
如本文所用,术语“核酸类似物分子”、特别是dna或rna分子类似物,是指作为类似物(即在结构上类似于天然存在的rna或dna分子)的分子。通常,天然存在的核酸是核苷酸
链,其由三种要素组成:骨架部分(特别是磷酸骨架),戊糖(核糖或脱氧核糖),以及四种核碱基之一。类似物可以具有改变的任何这些要素,诸如修饰核碱基或锁核酸(lna)。相应的类似物是本领域技术人员已知的。特别地,类似物可以赋予不同的碱基配对和碱基堆积特性。
[0015]2’
,3
’‑
o缩酮部分包含核碱基b。术语“核碱基”典型地是指包含至少一个n原子的环状(例如单环或双环)、饱和、不饱和、芳族或杂芳族碱基,其中核碱基能够经由与互补核碱基、特别是与天然存在的核碱基的氢键形成碱基对。核碱基可以是任何天然存在或非天然存在的核碱基,例如任何天然存在或非天然存在的嘌呤或嘧啶碱基,诸如腺嘌呤、胞嘧啶、鸟嘌呤、胸腺嘧啶或尿嘧啶,或修饰核碱基,例如修饰的腺嘌呤、胞嘧啶、鸟嘌呤、胸腺嘧啶、或尿嘧啶碱基。
[0016]2’
,3
’‑
o缩酮部分的核碱基可以是“修饰核碱基”。该术语包括任何类型的修饰核碱基,例如被疏水部分取代的核碱基、被碳水化合物部分取代的核碱基和/或被官能部分取代的核碱基。
[0017]
疏水部分可以选自具有至少5个c-原子、特别是至少10个c-原子的部分。
[0018]
在某些实施方案中,疏水部分选自取代或未取代的非环状或环状萜烯部分。例如,疏水部分可以是c
5-c
30
萜烯部分、特别是c
5-c
20
萜烯部分、并且更特别是c
15
萜烯部分,其可以是环状或非环状的,其可以是饱和或不饱和的,和/或任选地被一个或多个杂原子或一个或多个官能团取代或间断,或是甾醇部分,例如胆固醇部分。
[0019]
此外,疏水部分可以选自取代或未取代、环状或非环状、饱和、不饱和、或多不饱和羧酸部分,包括其盐或衍生物,诸如酯或酰胺。例如,疏水部分可以是c
5-c
30
羧酸部分,例如二十二碳六烯酸部分、二十碳五烯酸部分、二十二烷酸部分、石胆酸部分、或视黄酸或视黄酸酯部分。
[0020]
此外,疏水部分可以选自取代或未取代、环状或非环状、饱和、不饱和或多不饱和醇、酮、醛、或胺。例如,疏水部分可以是c
5-c
30
醇、酮、或酰胺部分,例如生育酚部分、生育酚琥珀酸酯部分、视黄醇部分、视黄醛部分、精胺部分、或亚精胺部分。
[0021]
在某些实施方案中,疏水部分选自
[0022][0023]
和/或
[0024][0025]
其中
[0026]
r和r’独立地选自c
1-c
30
烷基、优选地c5至c
25-烷基,n是1至6的整数,优选地n是1或2,并且a是1至20、优选地2至18、更优选地6至16的整数。
[0027]
碳水化合物部分可以是单糖、寡糖或多糖部分,包括修饰碳水化合物,例如乙酰化
碳水化合物部分。例如,碳水化合物部分可以是galnac部分。
[0028]
官能部分可以是点击官能部分,诸如炔烃基团或叠氮化物基团,或醚、酯、酰胺、羧酸、硫酯、硫代酰胺、或硫代醚基团。
[0029]
式(i)的缀合物包含2’,3
’‑
o-缩酮部分,其中核糖部分的2
’‑
oh基团和3
’‑
oh基团已经被转化为包含取代基r1和r2的缩酮基团。
[0030]
r1和r2彼此独立地是烃基团,其中所述烃基团任选地包含一个或多个杂原子,诸如n、o、p、s、或卤素。
[0031]
r1和r2可以是饱和、单不饱和或多不饱和非环状直链或支链烃基团,或饱和、单不饱和或多不饱和、芳族或杂芳族环状烃基团,其可以被一个或多个杂原子间断或取代。
[0032]
在某些实施方案中,r1和/或r2彼此独立地是c
5-21
烃基团、特别是c
5-11
烃基团并且更特别是c9烃基团,其中所述烃基团任选地包含一个或多个杂原子,诸如n、o、p、s、或卤素,例如f、cl、br、或i。
[0033]
在另外的实施方案中,r1和/或r2彼此独立地是直链或支链烷基、直链或支链烯基以及直链或支链炔基,其中所述烷基、烯基或炔基任选地包含一个或多个杂原子,诸如n、o、p、s、或卤素。
[0034]
在还另外的实施方案中,r1和/或r2彼此独立地是环状部分,即包含至少一个环状结构的部分,例如单环、双环或三环结构。环状部分可以是碳环或杂环部分,例如5-18个环原子,其中至少一个c-原子可以被至少一个选自n、o和s的杂原子替代。
[0035]
在还另外的实施方案中,r1和/或r2彼此独立地包含官能团,例如选自醚、酯、酰胺、羧酸、硫酯、硫代酰胺、或硫代醚基团的官能团。
[0036]
在还另外的实施方案中,r1和/或r2彼此独立地包含标志物基团,例如荧光、发光、或放射性标志物基团。
[0037]
在还另外的实施方案中,r1和/或r2彼此独立地包含如本文所定义的核酸分子,例如具有至多50个并且特别是5至25个核苷酸构建单元的核酸分子。
[0038]
在具体实施方案中,r1和r2是直链或支链c9烷基、更特别是直链c9烷基。
[0039]
在具体实施方案中,缀合物包含核碱基b,其是式(iia)的尿嘧啶碱基:
[0040][0041]
其中z是ch或n并且r3是h。
[0042]
在该实施方案中,r1和r2优选地是直链c9烷基。
[0043]
在另外的具体实施方案中,缀合物包含核碱基b,其是式(iib)的尿嘧啶碱基:
[0044][0045]
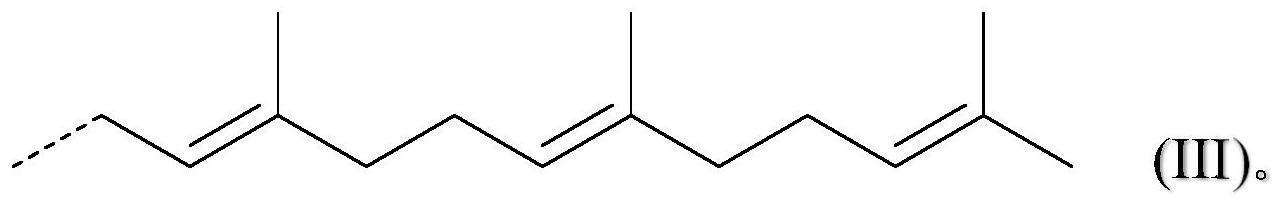
其中z是ch或n并且r3是疏水部分,例如萜烯部分、特别是c
5-c
30
萜烯部分、更特别是c
5-c
20
萜烯部分、并且甚至更特别是c
15
萜烯部分,例如式(iii)的萜烯部分:
[0046][0047]
在该实施方案中,r1和r2优选地是直链c9烷基。
[0048]
在某些实施方案中,核酸分子x具有至少约5个核苷酸构建单元和至多1,000个或更多个核苷酸构建单元的链长度。在另外的实施方案中,核酸分子x具有约5至约100个核苷酸构建单元、约10至约50个核苷酸构建单元、约12至约40个核苷酸构建单元以及特别地约15至约30个核苷酸构建单元的链长度。
[0049]
术语“核酸分子”包括单链、双链、三链和四链核酸分子,例如dna分子或rna分子及其类似物。此外,核酸分子可以包含至少一个如以下所描述的修饰核苷酸构建单元。
[0050]
在一个实施方案中,核酸分子是dna分子,其可以包含至少一个修饰核苷酸构建单元。术语“dna分子”包括单链和多链,例如双链、三链、或四链dna分子、特别是单链或双链dna分子。多链,例如双链dna分子可以包含具有相同长度的链或具有不同长度的链。在多链,例如双链dna分子中,单个链可以作为单独分子存在或经由单链环或经由异源连接基共价连接。
[0051]
术语“dna分子”包括由天然dna构建单元(即2'-脱氧核糖核苷酸构建单元)组成的分子,以及包含至少一个2'-脱氧核糖核苷酸构建单元和至少一个修饰核苷酸构建单元和/或至少一个核糖核苷酸构建单元的分子。
[0052]
在另外的实施方案中,核酸分子是rna分子,其可以包含至少一个修饰的构建单元和/或至少一个2
′‑
脱氧核糖核苷构建单元。术语“rna分子”包括单链或多链,例如双链、三链和四链rna分子、特别是单链或双链rna分子。多链rna分子可以包含具有相同长度的链或具有不同长度的链。例如,双链rna分子可以是平末端的或可以具有至少一个突出端(overhang),例如至少一个3'-突出端。在多链,例如双链rna分子中,单个链可以作为单独分子存在或经由单链环或经由异源连接基共价连接。
[0053]
术语“rna分子”包括由天然rna构建单元(即核糖核苷酸构建单元)组成的分子,以及包含天然rna构建单元和至少一个修饰核苷酸构建单元和/或至少一个2
′‑
脱氧核糖核苷酸构建单元的分子。
[0054]
术语“核苷酸构建单元”是指可以掺入如本文所描述的核酸分子中并且形成所述核酸分子的一部分的部分。典型地,核苷酸构建单元包含核碱基部分、糖部分和骨架部分。术语“核碱基”可以包括如以上对于式(i)的核碱基b所描述的任何类型的核碱基。糖部分可以包括核糖部分或2
’‑
脱氧核糖部分,包括其任何修饰。骨架部分可以包括在两个核苷酸构
建单元(包括其任何修饰)之间形成核苷间键的磷酸酯基团。核酸分子x可以包含修饰的核苷酸类似物单元,该修饰的核苷酸类似物单元包含核碱基修饰、糖修饰和/或骨架修饰。
[0055]
在某些实施方案中,核酸分子x包含至少一个修饰核苷酸构建单元,特别地选自:
[0056]
(a)核碱基修饰的构建单元;
[0057]
(b)糖修饰的构建单元;
[0058]
(c)骨架修饰的构建单元,和
[0059]
(d)其任何组合。
[0060]
术语“核碱基修饰的构建单元”是指包含修饰的核碱基的核苷酸构建单元。术语“修饰核碱基”可以包括如以上对于式(i)的核碱基b所描述的任何类型的修饰核碱基。
[0061]
术语“糖修饰的构建单元”是指包含修饰的糖的核苷酸构建单元。术语“糖”典型地是指核糖或2
’‑
脱氧核糖部分并且包括任何类型的修饰的糖部分。在某些实施方案中,糖修饰的核苷酸构建单元选自核苷酸构建单元,其中核糖部分的环和/或环上的取代基被修饰。
[0062]
在某些实施方案中,修饰核苷酸构建单元是2
’‑
修饰核苷酸构建单元,其中核糖部分的2
′‑
oh取代基被2
′‑
r4取代,其中r4是卤素(例如,氟)、c
1-c5烷基、o-c
1-c5烷基、s-c
1-c5烷基、c
2-c5烯基、o-c
2-c5烯基、s-c
2-c5烯基、c
2-c5炔基、o-c
2-c5炔基、s-c
2-c5炔基、氨基(包括单取代-或二取代的氨基),例如,c
1-c5烷基、c
2-c5烯基或c
2-c5炔基取代的氨基,其中每个烷基、烯基或炔基任选地被oh、卤素、环烷基、环烯基、(杂)芳基(例如苯基)、o-烷基、s-烷基、和/或氨基取代。
[0063]
在某些实施方案中,修饰核苷酸构建单元是桥接的,例如2
’‑4′‑
桥接的修饰核苷酸构建单元,其中桥典型地具有2-5个原子、特别是2-3个原子的长度,包括c-原子和任选地杂原子,诸如o、n或s。在具体实施方案中,修饰的构建单元是具有2
′‑
o-ch
2-4
′
桥的锁核酸构建单元。
[0064]
在某些实施方案中,修饰核苷酸构建单元是其中核糖部分的环被修饰的构建单元,例如吗啉基构建单元、硫代核糖构建单元、6元吡喃糖构建单元或肽核酸(pna)构建单元。
[0065]
术语“骨架修饰的构建单元”是指包含修饰的核苷间键的核苷酸构建单元。在骨架修饰的核苷酸构建单元中,连接相邻构建单元的磷酸酯基团被修饰的核苷间键替代,例如硫代磷酸酯键、膦酸烷基酯(例如膦酸甲酯键)和硼代磷酸酯键(borano phosphate)。
[0066]
核酸分子优选地选自适用于药物应用的核酸分子。优选的核酸分子包括包含编码序列的mrna分子,特别是包含蛋白质编码序列的mrna分子、能够rna干扰的rna分子(诸如16-27聚体sirna,特别是21聚体sirna)、平端sirna、sisirna、shrna、asirna、airna、叉sirna、27聚体sirna、哑铃型sirna、16聚体sirna、ss-sirna;微小rna分子及其antagomir,例如前体mirna模拟物;能够基因编辑的rna分子,例如crispr/cas复合物的组分,诸如tracrrna、crrna、sgrna;反义dna或rna;形成核酸分子的三链体或四链体;cpg-寡核苷酸、ttaggg-寡核苷酸、适配体、核糖酶或dna酶或此类分子的前体或修饰。
[0067]
在某些实施方案中,核酸分子x是任选地包含至少一个修饰的构建单元和/或至少一个dna构建单元的rna分子、任选地包含至少一个修饰的构建单元和/或至少一个rna构建单元的dna分子、或由修饰的构建单元组成的核酸类似物分子。
[0068]
在另外的实施方案中,核酸分子x是双链rna分子,其任选地包含至少一个修饰的
构建单元并且任选地具有至少一个突出端,例如5
’‑
突出端和/或3'-突出端,例如1、2或3个核苷酸构建单元的突出端。在具体实施方案中,rna分子是sirna分子。
[0069]
在另外的实施方案中,核酸分子x是任选地包含至少一个修饰的构建单元和/或至少一个核糖构建单元的单链dna分子,特别是反义分子。
[0070]
式(i)的核酸缀合物可以通过将2
’‑3’‑
o-缩酮部分(iv)附接至核酸分子x来制备,其中2
’‑3’‑
o-缩酮部分具有式(iv):
[0071][0072]
其中
[0073]
y是反应性官能部分,例如氨基磷酸酯(phosphoramidate)基团或适合于核酸分子、特别是核酸分子骨架的化学合成中的另一基团,
[0074]
b是核碱基,和
[0075]
r1和r2彼此独立地是烃基团,其中所述烃基团任选地包含一个或多个杂原子,诸如n、o、p、s、或卤素。
[0076]
如本文所用,术语“氨基磷酸酯”还可以包含用于核酸分子合成并且技术人员已知的“氨基磷酸酯变体”。
[0077]2’‑3’‑
o-缩酮部分(iv)的合成描述于wo 2014/048969中,其公开内容通过引用并入本文。2
’‑3’‑
o-缩酮部分(iv)与核酸分子x的附接可以在核酸分子x的合成期间或之后例如根据固相核酸合成中的标准方法进行。
[0078]
在某些实施方案中,2’,3
’‑
o-缩酮构建单元附接至核酸分子x的至少一个链的5
′‑
端和/或3
′‑
端。
[0079]
在具体实施方案中,2’,3
’‑
o-缩酮构建单元附接至双链sirna分子的有义链的5
′‑
端或反义分子的5
′‑
端。
[0080]
在另外的实施方案中,2’,3
’‑
o-缩酮构建单元附接至核酸分子x的链内的核碱基。
[0081]
在另外的实施方案中,存在附接至核酸分子x的多个、例如2个2’,3
’‑
o-缩酮构建单元。
[0082]
本发明的另外的方面涉及式(i)的缀合物在医学中的用途,例如用于人类医学或兽医学中的用途,特别是用于人类医学和体内动物研究中的用途。在某些实施方案中,医学用途包括向有需要的受试者、特别是向人受试者给予缀合物。在另外的实施方案中,将缀合物离体给予靶细胞或靶器官,并且随后将靶细胞或靶器官引入有需要的受试者中、特别是引入人受试者中。在还另外的实施方案中,将缀合物给予卵母细胞或胚胎,其中排除将人干细胞或人胚胎用于工业商业目的。如果将本发明的缀合物给予卵母细胞或胚胎,则优选的是,卵母细胞或胚胎的生殖系不被遗传修饰,而是仅治疗疾病,诸如遗传疾病。根据优选实施方案,将本发明的缀合物给予非人卵母细胞或非人胚胎。
[0083]
本发明提供了介导细胞、组织、器官、或生物体中靶标特异性核酸修饰的有效方法,其包括以下步骤:
[0084]
(a)使细胞、组织、器官、或生物体与本发明的缀合物接触,和
[0085]
(b)介导由缀合物的核苷组分对靶核酸实现的靶标特异性核酸修饰。
[0086]
接触步骤(a)可以包括将缀合物引入靶细胞(例如,可以存在于细胞培养物、单细胞微生物、或靶细胞中的分离的靶细胞)或多细胞生物体(诸如靶组织和/或靶器官)内的多个靶细胞中。靶细胞、靶组织和/或靶器官优选地是哺乳动物,包括人。靶生物体优选地是哺乳动物生物体,例如人体。靶细胞优选地是哺乳动物细胞,包括人细胞。靶组织优选是哺乳动物组织,包括人组织。靶器官优选地是哺乳动物器官,包括人器官。
[0087]
引入生物体中可以包括任何类型的给药,包括全身给药或局部给药,例如通过注射或输注。示例性给药类型包括经耳、经颊、支气管内、肠内、硬膜外、吸入、灌注到膀胱中、动脉内、关节内、胃内、臀肌内、心内、皮内、腰髓内、淋巴管内、乳房内、肌内、鼻内、神经内、眼内、骨内、腹膜内、胸膜内、肺内、肠内、鞘内、气管内、尿道内、宫内、静脉内、心室内、玻璃体内、口服、经口、肠胃外、硬膜外、神经周围、经皮、直肠、球后、结膜下、皮下、舌下、局部、经皮、经粘膜和/或阴道给药。
[0088]
介导步骤(b)优选地包括靶核酸的修饰,例如,当使用sirna缀合物时通过rna干扰,或当使用反义分子缀合物时通过抑制mrna转录。
[0089]
本发明还提供了包含如上所述的作为活性剂的缀合物以及合适的载体的药物组合物。对于诊断或治疗性应用,药物组合物可以呈溶液剂(例如用于输注或注射的溶液剂)、乳膏剂、软膏剂、片剂、混悬剂、粉剂等的形式。组合物可以以任何合适的方式给予,例如通过肠胃外给药,例如注射或输注,通过经粘膜施用,或通过透皮施用,或通过口服、局部、鼻、直肠给药等。局部施用是特别优选的,诸如在手术期间在腹腔中或在腹膜中。进一步优选的是在肿瘤附近或眼睛中的应用,特别是根据本发明的sirna缀合物的应用。
[0090]
药物组合物可以包含呈适用于递送到生物体中、特别是递送到人体中的任何形式的作为活性剂或前药的缀合物。例如,组合物可以包含呈包封形式或呈非包封形式的活性剂,连同递送媒介物诸如脂质体和/或连同转染试剂,或不含递送媒介物和/或不含转染试剂。
[0091]
在某些实施方案中,本发明的缀合物可以用于调节中,例如,靶细胞、靶组织、靶器官或靶生物体中目的基因的下调或上调。目的基因可以是内源性基因或来自外源性病原体的基因,特别是病毒或细菌基因或与内源性疾病相关的基因,诸如致癌基因,或与自身免疫性疾病相关的基因或与过敏性疾病相关的基因。
[0092]
在另外的实施方案中,本发明的缀合物可以用于编码核酸分子的引入和任选的表达中,例如靶细胞或靶生物体中的蛋白质编码核酸分子,诸如mrna分子。
[0093]
本发明的具体方面涉及缀合物用于核酸分子、特别是如本文所描述的治疗性核酸分子的靶细胞特异性、靶组织特异性和/或靶器官特异性递送的用途。本发明的尤其优选的实施方案涉及如本文所描述的附接至双链sirna分子的有义链的5
′‑
端或反义分子的5
′‑
端的2’,3
’‑
o-缩酮构建单元用于靶细胞、靶组织和/或靶器官特异性递送、特别是体内递送的用途。因此,sirna缀合物用于sirna分子、特别是治疗性sirna分子的靶细胞、靶组织和/或靶器官特异性递送的用途是特别优选的。
[0094]
例如,靶细胞可以是肺细胞、心脏细胞、肾细胞、肝细胞、胰腺细胞、结肠细胞、肌肉细胞、神经细胞、胃细胞、小肠细胞、大肠细胞、直肠细胞、膀胱细胞、骨细胞、肾上腺细胞、眼细胞、皮肤细胞、或脑细胞。如本文所用,“组织”是指由共享共同官能或结构的一组类似或不同分化的细胞(诸如靶细胞)组成的有机材料。
[0095]
本发明的还另外的方面涉及缀合物用于将核酸分子递送到靶细胞、靶组织、或靶器官中的体外用途。靶细胞可以选自可以将核酸分子递送到其中的任何类型的细胞,例如动物细胞,诸如哺乳动物细胞、鸟细胞或昆虫细胞、植物细胞、真菌细胞、原生动物细胞、细菌细胞和古细菌细胞。在具体实施方案中,靶细胞是人细胞。
[0096]
该方面的具体实施方案涉及缀合物在靶细胞、靶组织和/或靶器官中基因的下调中的用途。
[0097]
特别地,本发明提供了体外核酸分子的靶细胞特异性递送、靶组织特异性递送和/或靶器官特异性递送。例如,靶细胞可以是肺细胞、心脏细胞、肾细胞、肝细胞、胰腺细胞、结肠细胞、肌肉细胞、神经细胞、胃细胞、小肠细胞、大肠细胞、直肠细胞、膀胱细胞、骨细胞、肾上腺细胞、眼细胞、皮肤细胞、或脑细胞。
[0098]
本发明的还另外的方面涉及如本文所描述的2’,3
’‑
o-缩酮部分(iv)用于附接至核酸分子的用途。
[0099]
本发明的另外的方面如本说明书的以下条目中所描述。
[0100]
条目
[0101]
1.一种式(i)的核酸缀合物,其包含至少一个2’,3
’‑
o-缩酮部分:
[0102][0103]
其中
[0104]
x是核酸分子,
[0105]
b是核碱基,且
[0106]
r1和r2彼此独立地是烃基团,其中所述烃基团任选地包含一个或多个杂原子,诸如n、o、p、s、或卤素。
[0107]
2.如条目1所述的缀合物,
[0108]
其中r1和r2彼此独立地是c
5-21
烃基团、特别是c
5-11
烃基团并且更特别是c9烃基团,其中所述烃基团任选地包含一个或多个杂原子,诸如n、o、p、s、或卤素。
[0109]
3.如条目1或2所述的缀合物,
[0110]
其中r1和r2彼此独立地是直链或支链烷基、直链或支链烯基以及直链或支链炔基,其中所述烷基、烯基或炔基任选地包含一个或多个杂原子,诸如n、o、p、s、或卤素。
[0111]
4.如前述条目中任一项所述的缀合物,
[0112]
其中r1和r2是直链或支链c9烷基。
[0113]
5.如前述条目中任一项所述的缀合物,
[0114]
其中所述核碱基b是包含至少一个n原子的单环-或双环芳族或杂芳族碱基。
[0115]
6.如前述条目中任一项所述的缀合物,
[0116]
其中所述核碱基b是杂环碱基,例如嘌呤或嘧啶碱基,特别地选自尿嘧啶、胸腺嘧啶、或其类似物。
[0117]
7.如前述条目中任一项所述的缀合物,
[0118]
其中所述核碱基b是修饰碱基,例如被疏水部分取代的碱基、被碳水化合物部分取代的碱基或被官能部分取代的碱基。
[0119]
8.如条目7所述的缀合物,
[0120]
其中所述疏水部分是萜烯部分、特别是c
5-c
30
萜烯部分、更特别是c
5-c
20
萜烯部分、并且甚至更特别是c
15
萜烯部分,或甾醇部分,例如胆固醇部分。
[0121]
9.如条目7所述的缀合物,
[0122]
其中所述碳水化合物部分是galnac基团。
[0123]
10.如条目7所述的缀合物,
[0124]
其中所述官能部分是点击官能部分,诸如炔烃基团或叠氮化物基团,或诸如炔烃基团或叠氮化物基团,或醚、酯、酰胺、羧酸、硫酯、硫代酰胺、或硫代醚基团。
[0125]
11.如条目1-6中任一项所述的缀合物,
[0126]
其中b是式(iia)的核碱基:
[0127]
(iia)
[0128]
其中z是ch或n并且r3是h。
[0129]
12.如条目1-8中任一项所述的缀合物,
[0130]
其中b是式(iib)的核碱基:
[0131][0132]
其中z是ch或n并且r3是萜烯部分、特别是c
5-c
30
萜烯部分、更特别是c
5-c
20
萜烯部分、并且甚至更特别是c
15
萜烯部分,例如式(iii)的萜烯部分:
[0133][0134]
13.如前述条目中任一项所述的缀合物,
[0135]
其中所述核酸分子x具有至少5个核苷酸构建单元和最多达1,000个或更多个核苷酸构建单元、5至100个核苷酸构建单元、10至50个核苷酸构建单元、12至40个核苷酸构建单元并且特别是15至30个核苷酸构建单元的链长度。
[0136]
14.如前述条目中任一项所述的缀合物,
[0137]
其中所述核酸分子x包含至少一个修饰核苷酸构建单元,其特别地选自:
[0138]
(a)碱基修饰的核苷酸构建单元;
[0139]
(b)糖修饰的核苷酸构建单元;
[0140]
(c)骨架修饰的核苷酸构建单元,和
[0141]
(d)其任何组合。
[0142]
15.如条目14所述的缀合物,
[0143]
其中所述碱基修饰的核苷酸构建单元选自包含被疏水部分取代的碱基的构建单元、包含被碳水化合物部分取代的碱基的核苷酸构建单元和包含被官能部分取代的碱基的核苷酸构建单元。
[0144]
16.如条目14所述的缀合物,
[0145]
其中所述糖修饰的核苷酸构建单元选自2
’‑
修饰的核糖构建单元、2
’‑4′‑
桥接修饰的核糖构建单元(例如锁核苷酸(lna)构建单元)、吗啉基构建单元和肽核酸(pna)构建单元。
[0146]
17.如条目14所述的缀合物,
[0147]
其中所述骨架修饰的核苷酸构建单元包含修饰的核苷间键,例如,硫代磷酸酯键、膦酸烷基酯(例如,膦酸甲酯键)和硼代磷酸酯键。
[0148]
18.如前述条目中任一项所述的缀合物,
[0149]
其中所述核酸分子x是单链核酸分子或双链核酸分子。
[0150]
19.如条目1-18中任一项所述的缀合物,
[0151]
其中所述核酸分子x是(i)任选地包含至少一个修饰核苷酸构建单元和/或至少一个dna构建单元的rna分子、或(ii)任选地包含至少一个修饰核苷酸构建单元和/或至少一个rna构建单元的dna分子、或(iii)核酸类似物分子。
[0152]
20.如条目19所述的缀合物,
[0153]
其中所述核酸分子x是单链、双链、三链、或四链rna分子,特别是单链或双链rna分子,其中所述rna分子任选地包含至少一个脱氧核糖核苷酸构建单元、至少一个修饰的构建单元并且任选地具有至少一个3'-突出端,特别是sirna分子。
[0154]
21.如条目19所述的缀合物,
[0155]
其中所述核酸分子x是单链、双链、三链、或四链rna分子,特别是单链或双链dna分子,其中所述dna分子任选地包含至少一个核糖核苷酸构建单元、至少一个修饰的构建单元,特别是反义分子。
[0156]
22.如前述条目中任一项所述的缀合物,
[0157]
其中所述2’,3
’‑
o-缩酮构建单元附接至所述核酸分子x的链的5
′‑
端和/或3
′‑
端。
[0158]
23.如条目22所述的缀合物,
[0159]
其中所述2’,3
’‑
o-缩酮构建单元附接至双链sirna分子的有义链的5
′‑
端或反义分子的5
′‑
端。
[0160]
24.如前述条目中任一项所述的缀合物,
[0161]
其中所述2’,3
’‑
o-缩酮构建单元附接至所述核酸分子x的链内的碱基。
[0162]
25.如前述条目中任一项所述的缀合物,其用于医学,例如用于人类医学或兽医学,特别是用于人类医学。
[0163]
26.用于根据条目25的用途的条目1-24中任一项所述的缀合物,其中将所述缀合
物给予有需要的受试者、特别是给予人受试者。
[0164]
27.用于根据条目25的用途的条目1-24中任一项所述的缀合物,其中将所述缀合物离体给予靶细胞或靶器官,并且其中随后将所述靶细胞或靶器官引入有需要的受试者中、特别是引入人受试者中。
[0165]
28.用于根据条目25的用途的条目1-24中任一项所述的缀合物,其中将所述缀合物给予卵母细胞或胚胎,其中排除将人干细胞或人胚胎用于工业商业目的。
[0166]
29.用于根据条目25-28中任一项的用途的条目1-24中任一项所述的缀合物,其中所述给予包括靶细胞和/或靶器官特异性递送。
[0167]
30.用于根据条目25-29中任一项的用途的条目1-24中任一项所述的缀合物,其用于靶细胞或靶生物体中的基因的上调或下调,所述基因例如内源性基因或来自外源性病原体的基因,特别是病毒或细菌基因,或与内源性疾病相关的基因,诸如致癌基因,或与自身免疫性疾病相关的基因,或与过敏性疾病相关的基因。
[0168]
31.用于根据条目25-29中任一项的用途的条目1-24中任一项所述的缀合物,其用于在靶细胞或靶生物体中引入和任选地表达编码核酸分子基因。
[0169]
32.用于根据条目25-31中任一项的用途的条目1-24中任一项所述的缀合物,其中所述靶细胞是肺细胞、心脏细胞、肾细胞、肝细胞、胰腺细胞、结肠细胞、肌肉细胞、神经细胞、胃细胞、小肠细胞、大肠细胞、直肠细胞、膀胱细胞、骨细胞、肾上腺细胞、眼细胞、皮肤细胞、或脑细胞。
[0170]
33.如条目1-24中任一项所述的缀合物用于将核酸分子递送到靶细胞中的体外用途。
[0171]
34.如条目33所述的用途,
[0172]
其中所述靶细胞选自动物细胞,诸如哺乳动物细胞、鸟细胞或昆虫细胞,植物细胞,真菌细胞,原生动物细胞,细菌细胞和古细菌细胞。
[0173]
35.如条目33或34所述的用途,
[0174]
其中所述靶细胞是人细胞。
[0175]
36.如条目33-35中任一项所述的用途,其用于靶细胞中基因的上调或下调。
[0176]
37.如条目33-35中任一项所述的用途,其用于在靶细胞或靶生物体中引入和任选地表达编码核酸分子基因。
[0177]
38.如条目33-37中任一项所述的用途,其包括靶细胞特异性递送。
[0178]
39.如条目33-38中任一项所述的用途,
[0179]
其中所述靶细胞是肺细胞、心脏细胞、肾细胞、肝细胞、胰腺细胞、结肠细胞、肌肉细胞、神经细胞、胃细胞、小肠细胞、大肠细胞、直肠细胞、膀胱细胞、骨细胞、肾上腺细胞、眼细胞、皮肤细胞、或脑细胞。
[0180]
40.2’,3
’‑
o-缩酮部分(iv)用于附接至核酸分子的用途:
[0181][0182]
其中
[0183]
y是反应性官能部分,
[0184]
b是核碱基,和
[0185]
r1和r2彼此独立地是烃基团,其中所述烃基团任选地包含一个或多个杂原子,诸如n、o、p、s或卤素。
[0186]
41.如条目40所述的用途,
[0187]
其中所述2’,3
’‑
o-缩酮部分(iv)包含条目2-12中任一项的至少一个特征。
[0188]
42.如条目40或41所述的用途,
[0189]
其中所述核酸分子包含条目13-21中任一项的至少一个特征。
[0190]
43.如条目40-42中任一项所述的用途,
[0191]
其中所述2’,3
’‑
o-缩酮部分(iv)附接至所述核酸分子包含条目22-24中任一项的至少一个特征。
[0192]
44.如条目40-43中任一项所述的用途,其中所述反应性官能部分y是氨基磷酸酯基团。
[0193]
本发明应当通过以下附图和实施例更详细地概述。
附图说明:
[0194]
图1:a.作为氨基亚磷酸酯(phosphoramidite)的2
′
,3
′‑
o-缩酮部分pramo01和pramo02的结构和摩尔质量。b.寡核苷酸gapdh-反义和gapdh-有义(一起形成靶向双链sirna分子sigapdh)以及scr-反义和scr-有义(一起形成非靶向双链sirna分子scrambled sirna)作为裸rna分子或作为与pramo01或pramo02的缀合物的序列和分子质量。*意指硫代磷酸酯核苷间键。dt意指2
′‑
脱氧核糖核苷酸t构建单元。
[0195]
图2:静脉内注射3.75、10、或25mg/kg的裸sirna(sigapdh)、pramo01缀合的sirna、pramo02缀合的sirna或pbs/葡萄糖(n=3/组)的balb/c小鼠(6-8周)的肺(a)、肝(b)、心脏(c)、胰腺(d)和肾(e)中的gapdh mrna水平的测量。在注射后72小时之后收集组织。gapdh mrna水平使用归一化为管家基因(肌动蛋白b)的δδc
t
测量,并且表示为磷酸盐缓冲盐水(pbs)/葡萄糖的百分比(平均值
±
sd)。
[0196]
图3:静脉内注射3.75、10、或25mg/kg的裸sirna(sigapdh)、pramo01缀合的sirna、pramo02缀合的sirna、非靶向对照sirna(scrambled sirna)(n=3/组)的balb/c小鼠(6-8周)的肺(a)、肝(b)、心脏(c)、胰腺(d)和肾(e)中的gapdh mrna水平的测量。在注射后72小时之后收集组织。gapdh mrna水平使用归一化为管家基因(肌动蛋白b)的δδc
t
测量,并且表示为非靶向sirna的百分比(平均值
±
sd)。
[0197]
图4:用kras g12c-肺癌细胞在肺部3d器官模型中测量kras mrna水平,所述kras g12c-肺癌细胞在用pbs处理48h之后,用针对kras g12c的pramo01-缀合的sirna转染,并且使用转染试剂rnaimax(10μm sirna)。kras mrna水平使用归一化为管家基因(肌动蛋白b)的δδct测量,并且表示为阴性对照pbs(n=2)的百分比,(平均值
±
sd)。
实施例
[0198]
结果
[0199]
将两种不同的基于脂质的载体分子pramo01和pramo02(图1)附接至针对甘油醛3-磷酸脱氢酶(gapdh)基因的双链sirna分子sigapdh的有义链。修饰的sirna分子在体内被转移到不同的器官中并且分析了gapdh基因的下调。
[0200]
将pramo01和pramo02合成为修饰的氨基亚磷酸酯并且共价偶联至有义rna链的5'端。
[0201]
图2-3示出将脂质修饰的寡核苷酸静脉内注射到balb/c小鼠的尾静脉中的结果。实验动物的靶器官中gapdh基因表达被特异性地改变。注射之后72小时将动物处死,并且检查5个不同的组织。使用肺中的pram01修饰的sirna检测到gapdh基因下调(基因沉默)至58%(n=3)。使用pram02修饰的sirna在肝脏、心脏和胰腺中也可以检测到下调(n=3)。
[0202]
在3d肺器官芯片(具有突变kras g12c的人肺癌细胞)中进一步测试pramo01的递送效率。在该实验中,用pbs和针对突变kras g12c的pramo01-缀合-sirna连同rnaimax转染试剂处理两个额外的芯片,分别作为阴性对照和阳性对照。每个芯片含有两个独立的隔室;因此,产生了两个生理学独立的重复。用10μm sirna转染3d模型并且在转染后48h分析。可以在用pramo01-缀合的sirna处理并且使用和不使用转染试剂的3d模型中看到kras基因的下调(分别下调至70%和78%)。
[0203]
所使用的sirna-序列:
[0204]5′
gugguaguuggagcuugug dtdt 3
′
有义
[0205]5′
cacaagcuccaacuaccac dtdt 3
′
反义
[0206]
材料和方法
[0207]
脂质和寡核苷酸的合成
[0208]
脂质合成根据标准方法进行。寡核苷酸的合成和寡核苷酸与脂质的缀合根据标准方法进行。
[0209]
向小鼠中注射裸sirna和脂质缀合的sirna
[0210]
向6周龄的雌性balb/c小鼠静脉内注射葡萄糖或3.75、10、或25mg/kg的sirna(溶解在注射用水中的裸的或脂质-缀合的)。通常,每种物质注射三只小鼠(n=33,包括对照)。注射后第3天将动物处死。
[0211]
体内mrna沉默的测量
[0212]
收集组织,急速冷冻并且在-80℃下储存。rna提取使用qiagen tissuelyser和rneasy试剂盒(qiagen)在trizol rna分离试剂(thermofisher scientific,germany)中进行。使用revertaid hminus first strand cdna合成试剂盒和随机六聚体引物(mbi ferments,st.leon-rot,germany),转录cdna。对于qpcr,根据制造商的说明书使用taqman gapdh测定、taqman actinb测定和taqman mastermix(thermofischer scientific,
germany)。将相对gapdh表达归一化为肌动蛋白b并且通过δδct方法确定。
[0213]
在3d器官模型中测量mrna沉默
[0214]
在转染后48h收集含有具有kras g12c-突变的人肺癌细胞系的3d器官模型并且使用rneasy试剂盒(qiagen)分离rna。使用revertaid h minus first strand cdna合成试剂盒和随机六聚体引物(mbi ferments,st.leon-rot,germany),转录cdna。对于qpcr,根据制造商的说明书使用taqman kras测定、taqman actinb测定和taqman mastermix(thermofischer scientific,germany)。将相对kras表达归一化为肌动蛋白b并且通过δδct方法确定。
[0215]
茎环pcr
[0216]
为了扩增sirna,使用revertaid h minus first strand cdna合成试剂盒(thermofisher scientific,germany)将分离的rna转录成cdna。对于sirna的定量,使用基于cybergreen的qpcr测定(biorad)。所有程序均根据制造商的说明书进行。
[0217]
统计分析
[0218]
使用graphpad prism 8软件(graphpad software,inc.,san diego,ca,usa)分析数据。在三个独立的体内实验的每个中,将沉默水平归一化为非靶向对照(相应的scrambled sirna)的平均值。使用t-检验和anova分析数据用于多重比较。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。