1.本发明涉及抗菌材料技术领域,具体涉及一种由长链叔胺季铵化制得的壳聚糖季铵盐及其制备方法。
背景技术:
2.壳聚糖(chitosan)是自然界中唯一的阳离子碱性多糖,可经甲壳素脱乙酰化得到。壳聚糖含量丰富,作为一种可再生、无毒副作用、生物相容性和降解性良好的多糖,具有一定的杀菌、抑菌活性,被广泛应用于医药、食品、农业、日化、环保等多种行业领域中。壳聚糖的分子间和分子内存在很强的氢键作用,结晶度高,使其难溶于水及多数有机溶剂中,只能溶于盐酸、多元羧酸等酸性溶液,限制了其应用,但其含有活泼的-oh、-nh2,可引入其他活性基团,进而能够改善其生物活性,甚至产生新的活性功能。
3.在壳聚糖众多的衍生物中,壳聚糖季铵盐是重要的衍生物之一,壳聚糖季铵化扩大了壳聚糖衍生物的应用领域,具有较高的研究价值。壳聚糖通过季铵化改性不但能够提高壳聚糖衍生物的水溶性,而且合成的壳聚糖季铵盐还具有更强的抗菌抑菌性能。目前,壳聚糖的季铵化改性方法主要有两种:直接季铵化法和接技季铵化法。壳聚糖的直接季铵化改性根据完成的途径可以分为两种:一是利用壳聚糖分子结构中的氨基与烷基化试剂作用并使伯胺基团转化为叔胺基团,然后再与卤代烃作用而在其分子链中形成季铵基团;二是通过壳聚糖的氨基先与羰基化合物作用并生成schiff碱,然后再经还原生成n-烃基化壳聚糖,最后通过与卤代烃的作用而在壳聚糖分子链中形成季铵基团。壳聚糖接枝季铵化的本质是利用壳聚糖分子中含活泼h的基团(包括c3位和c6位上的羟基及c2位上的氨基),与含活泼反应性基团的季铵化试剂之间的缩合反应或加成反应,向壳聚糖分子结构中引进季铵基团,从而生成壳聚糖季铵化产物。
4.但是,目前常见的壳聚糖季铵化的改性方法中存在操作复杂、溶剂消耗量大、改性路线单一等问题。
技术实现要素:
5.针对现有壳聚糖季铵化方法中存在的操作复杂、溶剂消耗量大、改性线路单一等问题,本发明提供了一种由长链叔胺季铵化制得的壳聚糖季铵盐及其制备方法,其具有增强的抗菌性能和良好的生物相容性,可以广泛用作临床医用抗菌材料。
6.为了解决上述技术问题,本发明采用如下技术方案:
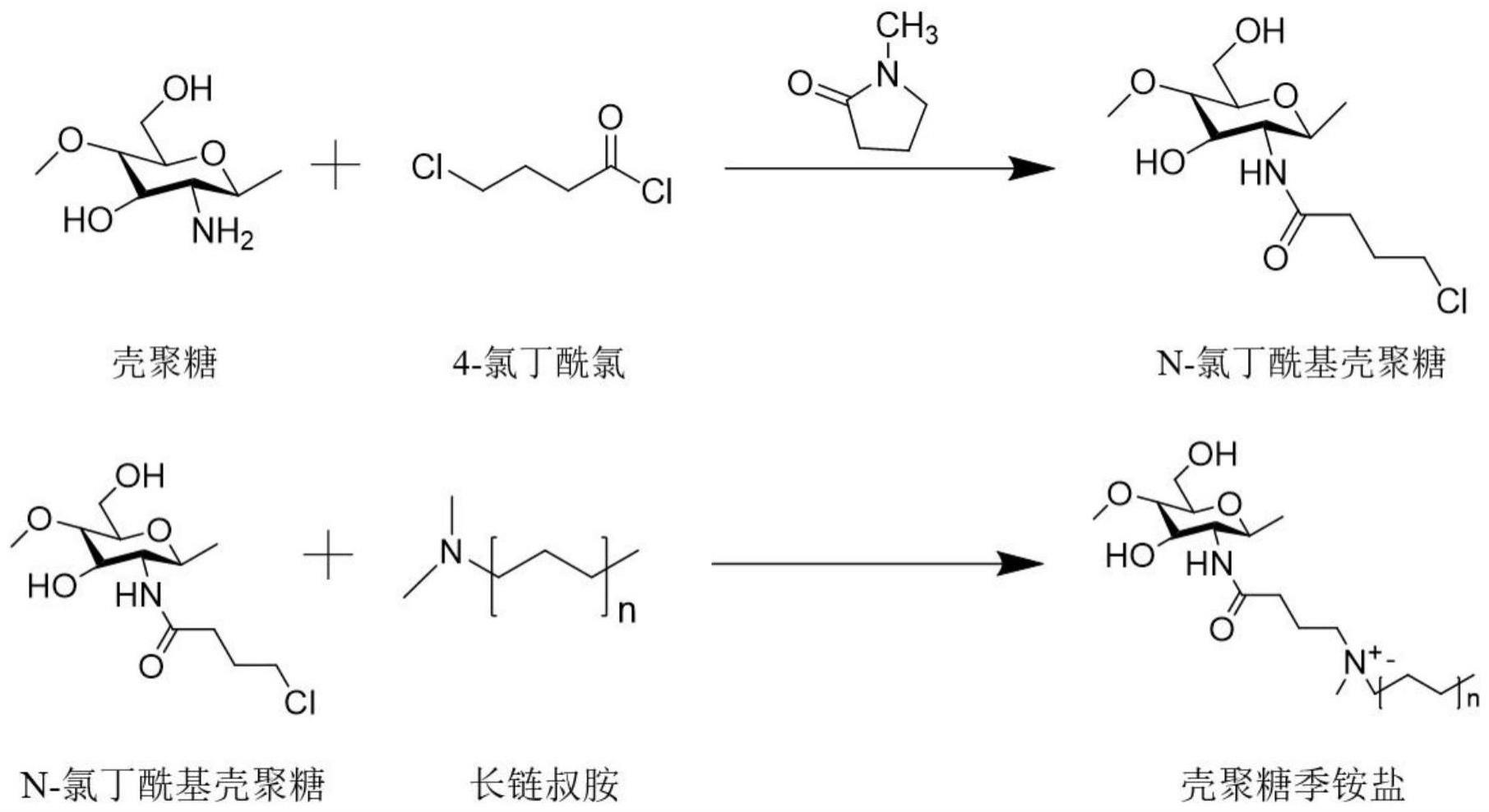
7.本发明公开了一种由长链叔胺季铵化制得的壳聚糖季铵盐,其特点在于:由脱乙酰壳聚糖与4-氯丁酰氯在n-甲基吡咯烷酮中反应获得n-氯丁酰基壳聚糖后,再与长链叔胺反应制得壳聚糖季铵盐;所述n-氯丁酰基壳聚糖的结构式如式(1)所示,所述长链叔胺的结构式如式(2)所示,所述壳聚糖季铵盐的结构式如式(3)所示,其中n为长链叔胺的叔胺链长度,具体反应式如图1所示:
[0008][0009]
进一步地,所述长链叔胺为n=10的n,n-二甲基正辛胺、n=12的n,n-二甲基癸胺或n=14的十二烷基二甲基叔胺。
[0010]
本发明所述的壳聚糖季铵盐的制备方法,包括以下步骤:
[0011]
(1)将脱乙酰壳聚糖溶解在n-甲基吡咯烷酮中,然后逐滴加入溶解在n-甲基吡咯烷酮中的4-氯丁酰氯,常温下搅拌反应5-6小时;反应结束后,将反应体系倒入乙醚中沉淀出聚合物,然后依次用甲醇和乙醚洗涤并抽滤,得到n-氯丁酰基壳聚糖;
[0012]
(2)将步骤(1)所得n-氯丁酰基壳聚糖溶解在稀盐酸溶液中,再加入长链叔胺,55-60℃下搅拌反应20-24h;反应结束后,将反应体系倒入无水乙醇中沉淀出聚合物,然后离心、用无水乙醇洗涤并抽滤,最后真空干燥、研磨,得到目标产物壳聚糖季铵盐。
[0013]
进一步地,步骤(1)中,脱乙酰壳聚糖与4-氯丁酰氯的用量比为2-2.05g:2.78ml。
[0014]
进一步地,步骤(1)中,搅拌反应在氮气气氛下进行。
[0015]
进一步地,步骤(2)中,所述稀盐酸溶液的浓度为0.1mol/l,n-氯丁酰基壳聚糖、稀盐酸溶液与长链叔胺的用量比为1-1.05g:65-75ml:10ml。
[0016]
进一步地,步骤(2)中所述真空干燥是在40℃下真空干燥18-24h。
[0017]
与现有技术相比,本发明的有益效果体现在:
[0018]
本发明提供了一种新的壳聚糖季铵化的合成路线,是通过将不同链长的叔胺(n,n-二甲基正辛胺、n,n-二甲基癸胺、十二烷基二甲基叔胺)与酰化壳聚糖直接进行反应,发生季铵化。本发明的制备方法操作简单、反应条件温和、溶剂消耗量较低,所得壳聚糖季铵盐具有很强的抗菌抑菌活性,可广泛应用于日常抗菌材料或医学抗菌材料的制备。
附图说明
[0019]
图1为本发明的合成路线图。
[0020]
图2为实施例1、2、3、4所得产物cs-中、cs-12、cs-10、cs-8的红外光谱图。
[0021]
图3为壳聚糖和对比例所得对比样1与对比样2的红外光谱图。
[0022]
图4为壳聚糖在20min内对金黄色葡萄球菌的杀菌效果平板涂布照片;
[0023]
图5为实施例1中产物cs-中在20min内对金黄色葡萄球菌的杀菌效果平板涂布照片;
[0024]
图6为实施例2中产物壳聚糖季铵盐cs-12在20min内对金黄色葡萄球菌的杀菌效果平板涂布照片;
[0025]
图7为实施例3中产物壳聚糖季铵盐cs-10在20min内对金黄色葡萄球菌的杀菌效果平板涂布照片。
[0026]
图8为实施例3中产物壳聚糖季铵盐cs-8在20min内对金黄色葡萄球菌的杀菌效果
平板涂布照片。
具体实施方式
[0027]
下面对本发明的实施例作详细说明,本实施例在以本发明技术方案为前提下进行实施,给出了详细的实施方式和具体的操作过程,但本发明的保护范围不限于下述的实施例。
[0028]
一、中间体产物n-氯丁酰基壳聚糖的制备
[0029]
实施例1
[0030]
本实施例按如下步骤制备n-氯丁酰基壳聚糖(cs-中):
[0031]
量取60ml的n-甲基吡咯烷酮加入到三颈烧瓶中,加入2.0015g的脱乙酰壳聚糖并溶解,然后将溶解在5mln-甲基吡咯烷酮的2.78ml4-氯丁酰氯逐滴加到该溶液中。在氮气气氛下,将反应混合物在常温下搅拌反应6h。
[0032]
反应结束后,将反应体系倒入乙醚中沉淀,得到聚合物为粗品,之后依次用甲醇和乙醚洗涤样品并进行抽滤,最后40℃真空烘干,得到中间体产物n-氯丁酰基壳聚糖1.6979g。
[0033]
二、壳聚糖季铵盐反应条件的优化
[0034]
实施例2
[0035]
本实施例以叔胺链长度n=14的十二烷基二甲基叔胺为原料,按如下步骤制备碳链长度为12的壳聚糖季铵盐(cs-12):
[0036]
通风橱内取发烟盐酸0.6ml,溶解于70ml超纯水中,即得到0.1mol/l的盐酸溶液,无菌过滤后加入到三颈烧瓶中,取1.0048g实施例1所得n-氯丁酰基壳聚糖加入并溶解,再向三颈烧瓶逐滴加入10ml十二烷基二甲基叔胺。之后将三颈烧瓶放置于油浴锅中60℃搅拌反应24h。反应结束后,将反应体系倒入无水乙醇中沉淀出聚合物,放入转速为8000rpm的离心机中离心5min,之后用无水乙醇洗涤并抽滤产物。最后40℃下真空干燥24h,产物研磨成粉末,即得到壳聚糖季铵盐cs-12共0.9188g。
[0037]
实施例3
[0038]
本实施例以叔胺链长度n=12的n,n-二甲基癸胺为原料,按如下步骤制备碳链长度为10的壳聚糖季铵盐(cs-10):
[0039]
通风橱内取发烟盐酸0.6ml,溶解于70ml超纯水中,即得到0.1mol/l的盐酸溶液,无菌过滤后加入到三颈烧瓶中,取1.0021g实施例1所得n-氯丁酰基壳聚糖加入并溶解,再向三颈烧瓶逐滴加入10ml n,n-二甲基癸胺。之后将三颈烧瓶放置于油浴锅中60℃搅拌反应24h。反应结束后,将反应体系倒入无水乙醇中沉淀出聚合物,放入转速为8000rpm的离心机中离心5min,之后用无水乙醇洗涤并抽滤产物。最后40℃下真空干燥24h,产物研磨成粉末,即得到壳聚糖季铵盐cs-10共0.9011g。
[0040]
实施例4
[0041]
本实施例以n=10的n,n-二甲基正辛胺为原料,按如下步骤制备碳链长度为8的壳聚糖季铵盐cs-8:
[0042]
通风橱内取发烟盐酸0.6ml,溶解于70ml超纯水中,即得到0.1mol/l的盐酸溶液,无菌过滤后加入到三颈烧瓶中,取1.0007g实施例1所得n-氯丁酰基壳聚糖加入并溶解,再
向三颈烧瓶逐滴加入10mln,n-二甲基正辛胺。之后将三颈烧瓶放置于油浴锅中55℃搅拌反应24h。反应结束后,将反应体系倒入无水乙醇中沉淀出聚合物,放入转速为8000rpm的离心机中离心5min,之后用无水乙醇洗涤并抽滤产物。最后40℃下真空干燥24h,产物研磨成粉末,即得到壳聚糖季铵盐cs-8共0.8761g。
[0043]
图2为壳聚糖和实施例1、2、3、4所得产物cs-中、cs-12、cs-10、cs-8的红外光谱图。壳聚糖在1600cm-1
处有较强的吸收峰,这是壳聚糖分子中-nh2的变形振动吸收峰,而由图可以看见,cs-中的红外光谱图中该峰消失,说明壳聚糖分子链中的-nh2被反应取代,壳聚糖酰化成功。而cs-12、cs-10、cs-8出现在1463.89cm-1
处较强的吸收峰,这是-n
(ch3)3的弯曲振动吸收峰,证明几种链段长度不同的壳聚糖季铵盐都成功合成。
[0044]
对比例
[0045]
在壳聚糖季铵盐的制备工艺摸索过程中,本发明进行了大量实验,包括溶剂体系、反应温度与后处理条件等,部分实验列举如下:
[0046]
1、以n-甲基吡咯烷酮为溶剂
[0047]
量取60ml的n-甲基吡咯烷酮加入至三颈烧瓶中,取1.0159g实施例1所得n-氯丁酰基壳聚糖加入并溶解,再向三颈烧瓶逐滴加入10ml十二烷基二甲基叔胺。之后将三颈烧瓶放置于油浴锅中60℃搅拌反应24h。反应结束后,反应体系中存在沉淀物,依次用乙醚和甲醇洗涤并抽滤产物,最后40℃下真空干燥24h,得到最终产物(命名为对比样1)。
[0048]
2、以二甲基亚砜(dmso)为溶剂
[0049]
量取60mldmso加入至三颈烧瓶中,取1.0015g实施例1所得n-氯丁酰基壳聚糖加入并溶解,再向三颈烧瓶逐滴加入10ml十二烷基二甲基叔胺。之后将三颈烧瓶放置于油浴锅中60℃搅拌反应24h。反应结束后,将反应体系倒入乙醚中,发现并未沉淀出聚合物。之后将反应体系倒入丙酮中,发现沉淀出聚合物,然后继续用丙酮洗涤并抽滤产物。最后40℃下真空干燥24h,得到最终产物(命名为对比样2)。
[0050]
由图3的红外光谱图可知,所得对比样1与对比样2不存在-n
(ch3)3的弯曲振动吸收峰,表明n-氯丁酰基壳聚糖与十二烷基二甲基叔胺未发生季铵化反应。
[0051]
3、制备碳链长度为8的壳聚糖季铵盐cs-8时,将反应温度分别设定为60℃、45℃,反应结束后,反应体系呈浑浊沉淀状态,且经后续测试证明所得产物(60℃所得产物命名为对比样3、45℃所得产物命名为对比样4)无抗菌抑菌性能。
[0052]
三、壳聚糖季铵盐抗菌性能的验证
[0053]
按如下步骤测试上述各实施例、对比例所得样品的杀菌效果:
[0054]
a、实验前准备:准备100ml锥形瓶,10ml离心管若干、5ml离心管若干、胰酪大豆胨液体培养基(tsb)、胰酪大豆胨琼脂发酵固体培养基(tsb),全部进行高压蒸汽灭菌(121℃、40min)、备用。胰酪大豆胨琼脂发酵固体培养基冷却到60℃,倾倒平板,等待凝固,形成固体培养皿。
[0055]
b、摇菌:取15ml玻璃试管,加入10-12ml的胰酪大豆胨液体培养基(tsb),接种金黄色葡萄球菌,然后置于恒温振荡器,37℃、160r/min培养18-20小时,使得菌落计数达到约5
×
108cfu/ml。
[0056]
c、使用移液枪吸取100μl步骤b获得的菌液添加于3.9ml去离子水中,摇晃均匀。
[0057]
d、取400μl步骤c获得的细菌悬浮液于9.6ml去离子水中,混匀后得到细菌稀释液;
分别取0.05g各实施例与对比例所制得的样品加入到细菌稀释液中,磁子搅拌充分接触。
[0058]
e、在各实施例所制得的样品与细菌稀释液充分接触之后,分别在0min、5min、10min、20min取20μl细菌稀释液滴入固体培养基中,涂布平板,将培养皿放置恒温培养箱中培养(培养温度为30-37℃,培养时间为24-36h),记录细菌数目。
[0059]
各实施例、对比例所得的样品的杀菌性能测试结果如表1所示。
[0060]
表1对金黄色葡萄球菌的杀菌测试
[0061][0062][0063]
对比可知,实施例2、3、4所得的cs-12、cs-10、cs-8的抗菌性能显著优于壳聚糖、实施例1所得的cs-中和对比例中合成的产物。cs-12在5min时就可将金黄色葡萄球菌完全杀灭;cs-10在5min时杀菌率也达到98.02%,在10min也达到近100%;cs-8在5min时杀菌率达到94.31%,10min也达到99.07%,20min时达到100%。而对比例中合成的产物,抗菌性能与壳聚糖并无太大差别,甚至对比样3还远不如壳聚糖本身的抗菌效果,说明本发明中的壳聚糖季铵化的反应需在合适的溶剂和反应温度中进行。n-氯丁酰基壳聚糖即实施例1中所得产物cs-中的抗菌性能对比壳聚糖有明显提升,但是与壳聚糖季铵盐的抗菌速度和抗菌性能相比仍有显著的差别。从抗菌效果的对比也可以证明壳聚糖季铵盐的成功合成。
[0064]
显然,上述实施例仅仅是为清楚地说明所作的举例,而并非对实施方式的限定。任何熟悉本专业的技术人员可能利用上述揭示的技术内容加以变更或改型为等同变化的等效实施例。但是凡是未脱离本发明技术方案内容,依据本发明的技术实质对以上实施例所作的任何简单修改、等同变化与改型,仍属于本发明技术方案的保护范围。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。
