用于治疗rna病毒诱导的疾病的方法和组合物
技术领域
1.本发明涉及用于治疗或减轻rna病毒诱导的疾病的症状或预防rna病毒诱导的疾病的方法,更具体地,涉及一种施用环己烯酮化合物的方法。
背景技术:
2.rna病毒是一种以rna(核糖核酸)为其遗传物质的病毒。这种核酸通常是单链rna(ssrna)但可能是双链rna(dsrna)。由rna病毒引起的值得注意的人类疾病包括普通感冒、流行性感冒、sars、mers、covid-19、登革热病毒、丙型肝炎、戊型肝炎、西尼罗河热、埃博拉病毒疾病、狂犬病、脊髓灰质炎、流行性腮腺炎和麻疹。
3.rna病毒诱导的疾病(诸如rna病毒性肺炎)是导致许多死亡的常见原因。每年大约有4.5亿例肺炎病例。在这些病例中,病毒性肺炎占约2亿病例,其包括约1亿儿童和1亿成人。病毒性肺炎是由病毒引起的肺炎。肺炎是一种引起一侧或两侧肺部炎症的感染。肺泡充有液体或脓液,使呼吸困难。
4.冠状病毒是引起哺乳动物和鸟类疾病的一组相关rna病毒。在人类中,这些病毒会引起呼吸道感染,该呼吸道感染可从轻度到致命。轻度病状包括一些普通感冒病例(该普通感冒病例也由某些其他病毒引起,主要是鼻病毒),而更致命的变体能够导致sars、mers和covid-19。
技术实现要素:
5.在一个方面,本文提供了用于治疗或减轻受试者中rna病毒诱导的疾病(诸如rna病毒诱导的肺炎)的症状和/或预防rna病毒诱导的疾病(如rna病毒诱导的肺炎)的方法,其包括向所述受试者施用治疗有效量的具有以下结构的环己烯酮化合物:其中,x和y中的每个独立地为氧、nr5或硫;r为氢或c(=o)c
1-c8烷基;r1、r2和r3中的每个独立地为氢、任选地为取代的甲基或(ch2)
m-ch3;r4为nr5r6、or5、oc(=o)r7、c(=o)or5、c(=o)r5、c(=o)nr5r6、卤素、5或6元内酯、c
1-c8烷基、c
2-c8烯基、c
2-c8炔基、芳基、葡糖基,其中,所述5或6元内酯、c
1-c8烷基、c
2-c8烯基、c
2-c8炔基、芳基和葡糖基任选地被选自以下的一个或多个取代基取代:nr5r6、or5、oc(=o)r7、c(=o)or5、c(=o)r5、c(=o)nr5r6、c
1-c8烷基、c
2-c8烯基、c
2-c8炔基、c
3-c8环烷基和c
1-c8卤代烷基;
r5和r6中的每个独立地为氢或c
1-c8烷基;r7为c
1-c8烷基、or5或nr5r6;m=1-12;并且n=1-12;或其药学上可接受的盐、代谢物、溶剂化物或前药。援引并入
6.在本说明书中提及的所有出版物、专利和专利申请都通过引用并入本文,其程度就好像各单独出版物、专利或专利申请都被具体地和单独地指出通过引用并入。
附图说明
7.本发明的新颖特征在所附权利要求中具体阐述。通过参考下面对利用了本发明的原理的说明性实施方案加以阐述详细描述和附图,将获得对本发明的特征和优点的更好理解,在附图中:
8.图1a/b示出了示例性化合物1降低hbeag(1a)和hbsag(1b)表达水平的研究结果。
9.图2a/b示出了示例性化合物1降低hbv nda表达水平(2a)和hcv rna活性(2b)的研究结果。
10.图3说明了sars-cov-2的潜在临床进展。
11.图4提供了通过示例性化合物1的抗病毒、抗炎症和抗纤维化的多种途径。
12.图5提供了示例性化合物1与水飞蓟素比较的nrf-2核转位研究结果。
13.图6提供了示例性化合物1的氧化应激的研究结果。
14.图7提供了示例性化合物1的nf-kb激活模型的肾脏炎症的研究结果。
15.图8提供了用示例性化合物1在mcp-1、il-6和cd3标志物情况下对于局部肾脏炎症的研究结果。
16.图9a/b提供了示例性化合物1的通过tgf-β1抑制(9a)和纤维化相关蛋白(9b)的抗纤维化活性的研究结果。
17.图10提供了通过示例性化合物1的抑制sars的研究结果。
18.图11提供了示例性化合物1与对照组(仅dmso)比较的细胞培养研究结果。
19.图12a-c分别提供了cxcl10(12a)、il6(12b)、和il18(12c)的基因表达水平。
20.图13a-b分别提供了tgfb1(13a)和col4a1(13b)的基因表达水平。
具体实施方式
21.虽然已经开发了许多用于治疗冠状病毒诱导的疾病(诸如sars和mers)的治疗剂,但迄今为止开发的药物没有发现显著效果。
22.在一些实施方案中,环己烯酮化合物从天然产物的提取物中获得或通过合成或半合成来制备。在一些实施方案中,本发明提供了用于治疗或减轻受试者中rna病毒诱导的疾病的症状或预防受试者中rna病毒诱导的疾病的示例性环己烯酮化合物(例如化合物1)的治疗和预防潜力。
23.在一些实施方案中,提供了用于治疗或减轻受试者中rna病毒诱导的疾病(诸如rna病毒诱导的肺炎)的症状和/或预防rna病毒诱导的疾病(诸如rna病毒诱导的肺炎)的方法,其包括向所述受试者施用治疗有效量的具有以下结构的环己烯酮化合物:
其中,x和y中的每个独立地为氧、nr5或硫;r为氢或c(=o)c
1-c8烷基;r1、r2和r3中的每个独立地为氢、任选地为取代的甲基或(ch2)
m-ch3;r4为nr5r6、or5、oc(=o)r7、c(=o)or5、c(=o)r5、c(=o)nr5r6、卤素、5或6元内酯、c
1-c8烷基、c
2-c8烯基、c
2-c8炔基、芳基、葡糖基,其中,所述5或6元内酯、c
1-c8烷基、c
2-c8烯基、c
2-c8炔基、芳基和葡糖基任选地被选自以下的一个或多个取代基取代:nr5r6、or5、oc(=o)r7、c(=o)or5、c(=o)r5、c(=o)nr5r6、c
1-c8烷基、c
2-c8烯基、c
2-c8炔基、c
3-c8环烷基和c
1-c8卤代烷基;r5和r6中的每个独立地为氢或c
1-c8烷基;r7为c
1-c8烷基、or5或nr5r6;m=1-12;并且n=1-12;或其药学上可接受的盐、代谢物、溶剂化物或前药。
24.在一些实施方案中,提供了包括治疗有效量的具有以下结构的环己烯酮化合物的药物组合物:其中,x和y中的每个独立地为氧、nr5或硫;r为氢或c(=o)c
1-c8烷基;r1、r2和r3中的每个独立地为氢、任选地为取代的甲基或(ch2)
m-ch3;r4为nr5r6、or5、oc(=o)r7、c(=o)or5、c(=o)r5、c(=o)nr5r6、卤素、5或6元内酯、c
1-c8烷基、c
2-c8烯基、c
2-c8炔基、芳基、葡糖基,其中,所述5或6元内酯、c
1-c8烷基、c
2-c8烯基、c
2-c8炔基、芳基和葡糖基任选地被选自以下的一个或多个取代基取代:nr5r6、or5、oc(=o)r7、c(=o)or5、c(=o)r5、c(=o)nr5r6、c
1-c8烷基、c
2-c8烯基、c
2-c8炔基、c
3-c8环烷基和c
1-c8卤代烷基;r5和r6中的每个独立地为氢或c
1-c8烷基;r7为c
1-c8烷基、or5或nr5r6;m=1-12;并且n=1-12;或其药学上可接受的盐、代谢物、溶剂化物或前药;其用于治疗或减轻受试者中rna病毒诱导的疾病(诸如病毒诱导的肺炎)的症状和/或预防受试者中rna病毒诱导的疾病(诸如病毒诱导的肺炎)。
25.在一些实施方案中,提供了治疗有效量的具有以下结构的环己烯酮化合物或其药学上可接受的盐、代谢物、溶剂化物或前药在制备用于治疗、减轻受试者中rna病毒诱导的疾病(诸如rna病毒诱导的肺炎)的症状和/或预防受试者中rna病毒诱导的疾病(诸如rna病毒诱导的肺炎)的药物中的用途,其中,x和y中的每个独立地为氧、nr5或硫;r为氢或c(=o)c
1-c8烷基;r1、r2和r3中的每个独立地为氢、任选地为取代的甲基或(ch2)
m-ch3;r4为nr5r6、or5、oc(=o)r7、c(=o)or5、c(=o)r5、c(=o)nr5r6、卤素、5或6元内酯、c
1-c8烷基、c
2-c8烯基、c
2-c8炔基、芳基、葡糖基,其中,所述5或6元内酯、c
1-c8烷基、c
2-c8烯基、c
2-c8炔基、芳基和葡糖基任选地被选自以下的一个或多个取代基取代:nr5r6、or5、oc(=o)r7、c(=o)or5、c(=o)r5、c(=o)nr5r6、c
1-c8烷基、c
2-c8烯基、c
2-c8炔基、c
3-c8环烷基和c
1-c8卤代烷基;r5和r6中的每个独立地为氢或c
1-c8烷基;r7为c
1-c8烷基、or5或nr5r6;m=1-12;并且n=1-12。
26.在一些实施方案中,所述rna病毒诱导的疾病为rna病毒诱导的肺炎、冠状病毒诱导的肺炎、或sars-cov-2诱导的肺炎等。在某些实施方案中,rna病毒是冠状病毒。在一些实施方案中,rna病毒诱导的疾病是由冠状病毒科感染引起或诱导的。在一些实施方案中,在某些实施方案中,所述冠状病毒科感染由α冠状病毒229e(hcov-229e)、nl63(hcov-nl63,纽黑文冠状病毒)、β冠状病毒oc43(hcov-oc43)、hku1、mers-cov(导致中东呼吸综合征的冠状病毒)、sars-cov(导致严重急性呼吸综合征的冠状病毒)或sars-cov-2(导致严重急性呼吸系统综合征的冠状病毒,以前在2019年被称为新型冠状病毒,或2019-ncov)等引起或与之相关。在某些实施方案中,所述冠状病毒科感染是由严重急性呼吸系统综合征冠状病毒2(sars-cov-2)引起或与之相关。在一些实施方案中,所述rna病毒诱导的疾病是rna病毒诱导的肺炎。在某些实施方案中,所述冠状病毒科感染是由严重急性呼吸系统综合征冠状病毒2(sars-cov-2)引起或与之相关。在一些实施方案中,环己烯酮化合物降低rna病毒浓度或预防rna病毒复制。在某些实施方案中,环己烯酮化合物降低以下rna病毒浓度或预防以下rna病毒复制:α冠状病毒229e(hcov-229e)、nl63(hcov-nl63,纽黑文冠状病毒)、β冠状病毒oc43(hcov-oc43)、hku1、mers-cov(导致中东呼吸综合征的冠状病毒)、sars-cov(导致严重急性呼吸综合征的冠状病毒)或sars-cov-2(导致严重急性呼吸系统综合征的冠状病毒,以前在2019年被称为新型冠状病毒,或2019-ncov)等。在一些实施方案中,受试者为人类。
27.在一些实施方案中,提供了一种用于在有需要的受试者中治疗、抑制和/或预防冠状病毒诱导的肺炎的方法,该方法包括向所述受试者施用有效量的下式(i)的环己烯酮化合物。
28.在一些实施方案中,提供了一种用于在有需要的受试者中治疗、抑制和/或预防rna病毒复制(例如冠状病毒复制)的方法,该方法包括向受试者施用有效量的本文公开的环己烯酮化合物。
29.在一些实施方案中,提供了一种用于降低有需要的受试者中rna病毒浓度的方法,该方法包括向受试者施用有效量的本文公开的环己烯酮化合物。
30.在一些实施方案中,提供了一种用于在有需要的受试者中抑制和/或预防rna病毒感染的方法,该方法包括向受试者施用有效量的本文公开的环己烯酮化合物。
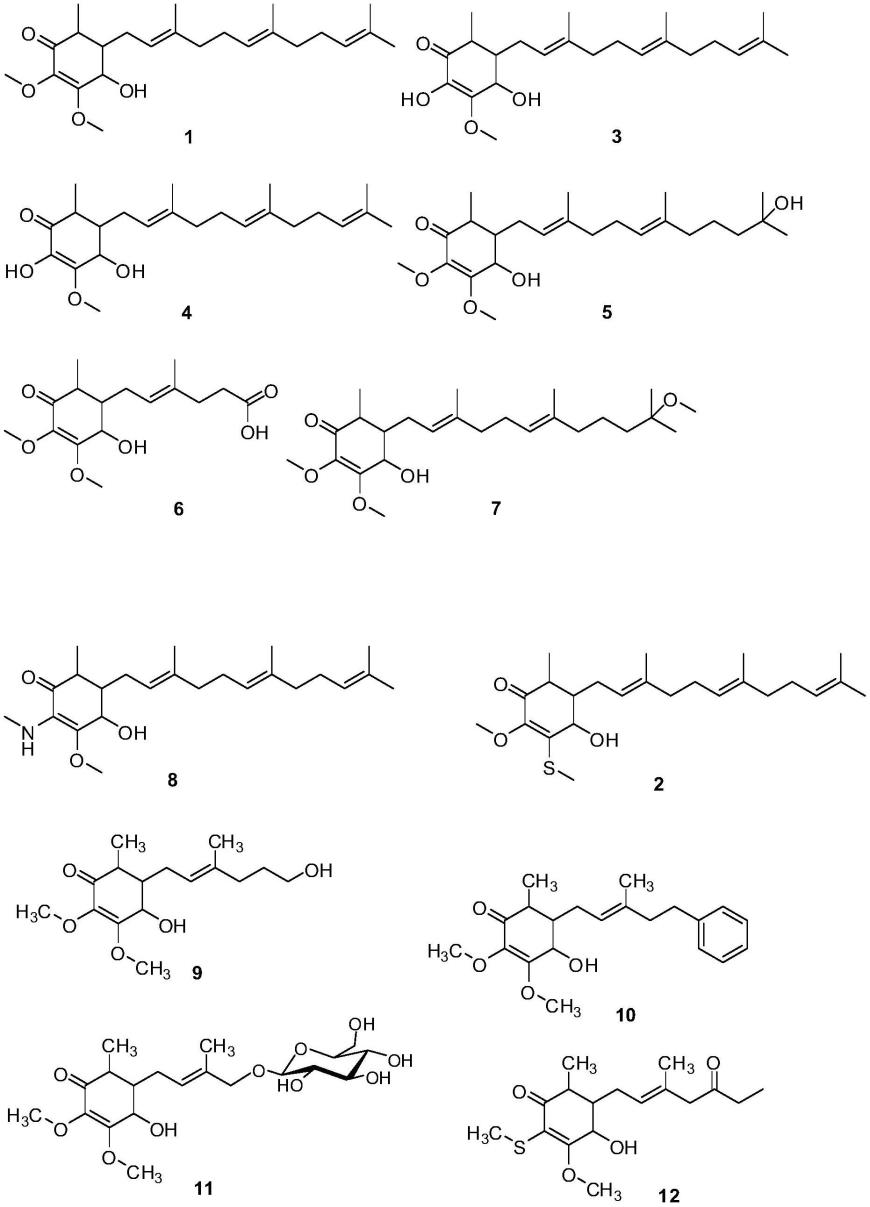
31.在一些实施方案中,具有以下结构的环己烯酮化合物由任何合适的起始材料通过合成或半合成制备,在其他实施方案中,环己烯酮化合物通过发酵等制备。例如,化合物1和3-7是从有机溶剂提取物中分离出来的。非限制性示例性化合物如下说明。
32.在其他实施方案中,具有以下结构的环己烯酮化合物是从牛樟芝的有机溶剂提取物中分离出来的在一些实施方案中,有机溶剂选自醇(例如甲醇、乙醇、丙醇等)、酯(例如乙酸甲酯、乙酸乙酯等)、烷烃(例如戊烷、己烷、庚烷等)、卤代烷烃(例如氯甲烷、氯乙烷、氯仿、二氯甲烷等)等。例如,示例性化合物1-7是从有机溶剂提取物中分离出来的。在某些实施方案中,有机溶剂是醇。在某些实施方案中,醇为乙醇。在一些实施方案中,环己烯酮化合物是从牛樟芝的水性提取物中分离出来的。在某些实施方案中,本文公开的环己烯酮化合物是通过合成或半合成制备的。
33.在一些实施方案中,x和y中的每个独立地为氧或硫。本领域已知,其中x和y中的每个独立地为硫的化合物可以通过与其中x和y中的每个独立地为氧的化合物相似或相同的途径制备,因为氧和硫在结构中具有相似的化学性质。在一些实施方案中,通过合适的保护基团,其中x和y中的每个独立地为nr5的化合物可以通过与其中x和y中的每个独立地为氧或硫的化合物相似的途径制备。
34.在一些实施方案中,r为氢、c(=o)c3h8、c(=o)c2h5或c(=o)ch3。在一些实施方案中,r1为氢、甲基、乙基、丙基、丁基、戊基或己基。在某些实施方案中,r1为氢或甲基。在一些
实施方案中,r2为氢、甲基、乙基、丙基、丁基、戊基或己基。在某些实施方案中,r2为氢或甲基。在一些实施方案中,r3为氢、甲基、乙基、丙基、丁基、戊基或己基。在一些实施方案中,r4为卤素、nh2、nhch3、n(ch3)2、och3、oc2h5、c(=o)ch3、c(=o)c2h5、c(=o)och3、c(=o)oc2h5、c(=o)nhch3、c(=o)nhc2h5、c(=o)nh2、oc(=o)ch3、oc(=o)c2h5、oc(=o)och3、oc(=o)oc2h5、oc(=o)nhch3、oc(=o)nhc2h5、或oc(=o)nh2。在一些实施方案中,r4为c2h5c(ch3)2oh、c2h5c(ch3)2och3、ch2cooh、c2h5cooh、ch2oh、c2h5oh、ch2ph,c2h5ph、ch2ch=c(ch3)(cho)、ch2ch=c(ch3)(c(=o)ch3)、5或6元内酯、c
2-c8烯基、c
2-c8炔基、芳基或葡糖基,其中所述5或6元内酯、c
2-c8烯基、c
2-c8炔基、芳基和葡糖基任选地被选自以下的一个或多个取代基取代:nr5r6、or5、oc(=o)r7、c(=o)or5、c(=o)r5、c(=o)nr5r6、c
1-c8烷基、c
2-c8烯基、c
2-c8炔基、c
3-c8环烷基和c
1-c8卤代烷基。在某些实施方案中,r4为任选地被一个或多个选自以下的取代基取代的5或6元内酯、c
2-c8烯基、c
2-c8炔基、芳基和葡糖基:nr5r6、or5、oc(=o)r7、c(=o)or5、c(=o)r5、c(=o)nr5r6、c
1-c8烷基、c
2-c8烯基、c
2-c8炔基、c
3-c8环烷基和c
1-c8卤代烷基。在某些实施方案中,r4为ch2ch=c(ch3)2。在某些实施方案中,化合物为某些药物和医学术语
35.除非另有说明,否则本技术(包括说明书和权利要求书)中使用的下列术语具有以下给出的定义。必须注意,除非上下文另有明确说明,否则如说明书和所附权利要求中所使用的,单数形式“一”、“一个”和“该”包括复数个指代物。除非另有说明,否则采用质谱、nmr、hplc、蛋白质化学、生物化学、重组dna技术和药理学的常规方法。在本技术中,除非另有说明,否则使用“或”或“和”表示“和/或”。此外,术语“包括(including)”以及诸如“包括有(include)”、“包括了(includes)”和“被包括(included)”等其他形式的使用不是限制性的。本文使用的章节标题仅用于组织目的,不应解释为限制所描述的主题。
[0036]“烷基”基团是指脂肪族烃基。烷基可以是饱和烷基(意味着它不包含任何碳-碳双键或碳-碳三键)或烷基可以是不饱和烷基(意味着它包含至少一个碳-碳双键或碳-碳三键)。烷基部分,无论是饱和的还是不饱和的,可以是支链或直链的。
[0037]“烷基”基团可以具有1至12个碳原子(无论何时出现在本文中,数值范围例如“1至12”是指给定范围内的每个整数;例如,“1至12个碳原子”是指烷基可由1个碳原子、2个碳原子、3个碳原子等组成,最多包括12个碳原子,但本定义还涵盖其中未指定数值范围的术语“烷基”的出现)。本文所述化合物的烷基基团可指定为“c
1-c8烷基”或类似指定物。仅作为示例,“c
1-c8烷基”表示烷基链中有1、2、3、4、5、6、7或8个碳原子。在一方面,烷基选自甲基、乙基、丙基、异丙基、正丁基、异丁基、仲丁基和叔丁基。典型的烷基基团包括但不限于甲基、乙基、丙基、异丙基、丁基、异丁基、仲丁基、叔丁基、戊基、新戊基、己基、烯丙基、丁-2-烯基、丁-3-烯基、环丙基甲基、环丁基甲基、环戊基甲基、环己基甲基等。在一方面,烷基为c
1-c8烷基。
[0038]
术语“亚烷基”是指二价烷基。任何上述一价烷基基团可以通过从烷基中夺取第二
个氢原子而成为亚烷基。在一方面,亚烷基是c
1-c
12
亚烷基。在另一方面,亚烷基是c
1-c8亚烷基。典型的亚烷基包括但不限于-ch
2-、-ch(ch3)-、-c(ch3)
2-、-ch2ch
2-、-ch2ch(ch3)-、-ch2c(ch3)
2-、-ch2ch2ch
2-、-ch2ch2ch2ch
2-、-ch2(ch2)3ch
2-等。
[0039]
如本文所用,术语“芳基”是指其中形成环的每个原子是碳原子的芳环。芳基环由5、6、7、8、9或多于9个碳原子形成。芳基任选地被取代。在一方面,芳基是苯基或萘基。在一方面,芳基是苯基。在一方面,芳基是c
6-c
10
芳基。根据结构,芳基可以是单价基或二价基(即亚芳基)。在一方面,亚芳基是c
6-c
10
亚芳基。示例性亚芳基包括但不限于苯基-1,2-亚基(phenyl-1,2-ene)、苯基-1,3-亚基和苯基-1,4-亚基。
[0040]
术语“芳烃”是指具有包含4n 2π电子的离域π-电子体系的平面环,其中n是整数。芳环可由5、6、7、8、9、10或多于10个的原子形成。芳烃任选地被取代。术语“芳烃”包括碳环芳基(“芳基”、例如,苯基)和杂环芳基(或“杂芳基”或“杂芳烃”)基团(例如,吡啶)。该术语包括单环或稠环多环(即,共享相邻碳原子对的环)基团。
[0041]
术语“卤代(halo)”或“卤素”或“卤化物”是指氟、氯、溴或碘。
[0042]
术语“内酯”是指环状酯,其可以看作是同一分子中的醇基-oh和羧酸基-cooh的缩合产物。其特征是由两个或更多个碳原子和单个氧原子组成的闭环,其中酮基=o在与另一个氧相邻的一个碳中。
[0043]
术语“杂环”或“杂环的”是指环中含有1到4个杂原子的杂芳环(也称为杂芳基)和杂环烷基环(也称为杂脂环基团),其中环中的每个杂原子选自o、s和n,其中每个杂环基团在其环体系中具有4至10个原子,并且条件是任何环不包含两个相邻的o或s原子。非芳族杂环基团(也称为杂环烷基)包括在其环体系中仅具有3个原子的基团,但芳族杂环基团在其环体系中必须具有至少5个原子。杂环基团包括苯并稠环体系。3元杂环基团的示例是吖丙啶基。4元杂环基团的示例是氮杂环丁烷基(azetidinyl)。5元杂环基团的示例是噻唑基。6元杂环基团的示例是吡啶基,10元杂环基团的示例是喹啉基(quinolinyl)。非芳族杂环基团的示例是吡咯烷基、四氢呋喃基、二氢呋喃基、四氢噻吩基、噁唑烷酮基(oxazolidinonyl)、四氢吡喃基、二氢吡喃基、四氢硫代吡喃基、哌啶基、吗啉基、硫代吗啉基、噻噁烷基(thioxanyl)、哌嗪基、吖丙啶基、氮杂环丁烷基、氧杂环丁基(oxetanyl)、硫杂环丁基(thietanyl)、高哌啶基、氧杂环庚烷基(oxepanyl)、硫杂环庚烷基(thiepanyl)、氧氮杂卓基(oxazepinyl)、二氮杂卓基(diazepinyl)、硫氮杂卓基(thiazepinyl)、1,2,3,6-四氢吡啶基、吡咯啉-2-基、吡咯啉-3-基、二氢吲哚基、2h-吡喃基、4h-吡喃基、二恶烷基(dioxanyl)、1,3-二氧戊环基、吡唑啉基、二噻烷基、二硫戊环基(dithiolanyl)、二氢吡喃基、二氢噻吩基、二氢呋喃基、吡唑烷基、咪唑啉基、咪唑烷基、3-氮杂双环[3.1.0]己烷基、3-氮杂双环[4.1.0]庚烷基、3h-吲哚基和喹啉基。芳族杂环基团的示例是吡啶基、咪唑基、嘧啶基、吡唑基、三唑基、吡嗪基、四唑基、呋喃基、噻吩基、异恶唑基、噻唑基、恶唑基、异噻唑基、吡咯基、喹啉基、异喹啉基、吲哚基、苯并咪唑基、苯并呋喃基、噌啉基、吲唑基、吲嗪基、酞嗪基、哒嗪基、三嗪基、异吲哚基、蝶啶基、嘌呤基、恶二唑基、噻二唑基、呋咱基、苯并呋咱基、苯并噻吩基、苯并噻唑基、苯并恶唑基、喹唑啉基、喹喔啉基、萘啶基和呋喃并吡啶基(furopyridinyl)。如果可能的话,上述基团可以是c-连接的或n-连接的。例如,衍生自吡咯的基团可以是吡咯-1-基(n-连接的)或吡咯-3-基(c-连接的)。此外,衍生自咪唑的基团可以是咪唑-1-基或咪唑-3-基(两者均为n-连接的)或咪唑-2-基、咪唑-4-基或咪唑-5-基
(所有都是c-连接的)。杂环基团包括苯并稠环系统。非芳族杂环可以被一个或两个氧代(=o)部分取代,例如吡咯烷-2-酮。
[0044]
如本文所用的术语“烯基”是指含有2-10个碳并含有至少一个通过去除两个氢形成的碳-碳双链的直链、支链或环状(在这种情况下,它也称为“环烯基”)烃。在一些实施方案中,根据结构,烯基是单价基或二价基(即,亚烯基)。在一些实施方案中,烯基任选地被取代。烯基的说明性示例包括但不限于乙烯基、2-丙烯基、2-甲基-2-丙烯基、3-丁烯基、4-戊烯基、5-己烯基、2-庚烯基、2-甲基-1-庚烯基和3-癸烯基(cecenyl)。
[0045]
如本文所用的术语“炔基”是指含有2-10个碳并含有至少一个通过去除四个氢形成的碳-碳三链的直链、支链或环状(在这种情况下,它也称为“环炔基”)烃。在一些实施方案中,根据结构,炔基是单价基或二价基(即,亚炔基)。在一些实施方案中,炔基任选地被取代。炔基的说明性示例包括但不限于乙炔基、丙炔基、丁炔基、戊炔基、己炔基、庚炔基等。
[0046]
如本文所用的术语“烷氧基”是指通过氧原子与母分子部分附接的如本文所定义的烷基基团。烷氧基的说明性示例包括但不限于甲氧基、乙氧基、丙氧基、2-丙氧基、丁氧基、叔丁氧基、戊氧基和己氧基。
[0047]
如本文所用的术语“环烷基”是指仅包含碳和氢的单环或多环基团,包括饱和、部分不饱和或完全不饱和的那些单环或多环基团。环烷基基团包括具有3至10个环原子的基团。环状的代表性示例包括但不限于以下部分:团。环状的代表性示例包括但不限于以下部分:在一些实施方案中,根据结构,环烷基基团是单价基或二价基(即,亚环烷基)。
[0048]
如本文所用的术语“卤代烷基”、“卤代烯基”、“卤代炔基”和“卤代烷氧基”包括其中至少一个氢被卤素原子取代的烷基、烯基、炔基和烷氧基结构。在其中两个或更多个氢原子被卤素原子取代的某些实施方案中,卤素原子彼此完全相同。在其中两个或更多个氢原子被卤素原子取代的其他实施方案中,卤素原子彼此不完全相同。术语“氟烷基”和“氟烷氧基”分别包括其中卤素是氟的卤代烷基和卤代烷氧基。在某些实施方案中,卤代烷基任选地被取代。
[0049]
如本文所用的术语“葡糖基”包括d-或l-型葡糖基基团,其中葡糖基基团通过葡萄糖环上的任何羟基附接。
[0050]
如本文所用的关于制剂、组合物或成分的术语“可接受的”是指对被治疗的受试者的总体健康没有持续的有害影响。
[0051]
薄孔菌属(antrodia)是薄孔菌科中真菌的属。薄孔菌属物种的子实体通常平放或展开在生长表面,其中子实层暴露在外面;边缘可以转动以形成窄托架(bracket)。大多数物种存在于温带和北方森林中,并导致褐腐病。
[0052]
牛樟芝又名粗樟菌(stout camphor fungus)、灵芝,是一种台湾地方特有的薄孔菌属菌类,它只生长在地方特有的牛樟上,导致褐色心腐病。这种台湾独特的蘑菇已被用作保护不同疾病状况的传统药物。
[0053]
本领域已知的是从牛樟芝不同部位分离的活性成分因不同的培养介质和方法而变化。例如,本文公开的某些环己烯酮化合物只能从用于培养牛樟芝的独特的固态发酵工艺中分离出来,这与其他已知方法不同。
[0054]
如本文所用的术语“载体”是指相对无毒的化学化合物或试剂,其有助于将化合物整合入细胞或组织中。
[0055]
如本文所用的术语“共同施用”等是指包括向单个患者施用选定的治疗剂,并旨在包括通过相同或不同的施用途径或在相同或不同的时间施用药剂的治疗方案。
[0056]
术语“稀释剂”是指用于在递送前稀释目标化合物的化合物。稀释剂还可用于稳定化合物,因为它们可以提供更稳定的环境。溶解在缓冲溶液中的盐(其也可以提供ph控制或维持)在本领域中用作稀释剂,包括但不限于磷酸盐缓冲盐溶液。
[0057]
如本文所用的术语“有效量”或“治疗有效量”是指施用足量的药剂或化合物,其将在一定程度上缓解所治疗的疾病或病况的一种或多种症状。结果可以是减少和/或减轻疾病的体征、症状或起因,或生物系统的任何其他期望的改变。例如,用于治疗用途的“有效量”是提供疾病症状的临床显著减少所需的包含本文公开的化合物的组合物的量。在任何个别情况下,适当的“有效”量可以使用技术来确定,例如剂量递增研究。
[0058]
如本文所用的术语“增强(enhance)”或“增强了(enhancing)”是指在效力或持续时间方面增加或延长所期望的效果。因此,关于增强治疗剂的效果,术语“增强”是指在效力或持续时间方面增加或延长其他治疗剂对系统的效果的能力。如本文所用的“增强有效量”是指足以增强期望系统中另一种治疗剂效果的量。
[0059]
本文公开的化合物的“代谢物”是当该化合物代谢时形成的该化合物的衍生物。术语“活性代谢物”是指化合物代谢时形成的化合物的生物活性衍生物。如本文所用的术语“代谢”是指生物体改变特定物质的过程(包括但不限于水解反应和通过酶催化的反应)的总和。因此,酶可以对化合物产生特定的结构变化。例如,细胞色素p450催化多种氧化和还原反应,而尿苷二磷酸葡萄糖醛酸转移酶催化活化的葡萄糖醛酸分子向芳醇、脂肪醇、羧酸、胺和游离巯基的转移。本文公开的化合物的代谢物任选地通过将化合物施用于宿主并分析来自宿主的组织样品,或通过在体外将化合物与肝细胞温育并分析所得化合物来鉴定。
[0060]
如本文所用的术语“药物组合”是指由多于一种活性成分的混合或组合而成的产品,包括活性成分的固定组合和非固定组合。术语“固定组合”是指活性成分(例如化合物(即,本文所述的环己烯酮化合物))和助剂两者以单一实体或剂量的形式同时施用于患者。术语“非固定组合”是指将活性成分(例如化合物(即,本文所述的环己烯酮化合物))和助剂作为单独的实体同时、并行或顺序施用于患者,而没有特定的干预时间限制,其中这种施用在患者体内提供了两种化合物的有效水平。后者也适用于鸡尾酒疗法,例如施用三种或更
多种活性成分。
[0061]
术语“药物组合物”是指化合物(即本文所述的环己烯酮化合物)与其他化学组分(诸如载体、稳定剂、稀释剂、分散剂、悬浮剂、增稠剂和/或赋形剂)的混合物。药物组合物有助于将化合物施用于生物体。本领域存在多种施用化合物的技术,包括但不限于:经静脉内、口服、气雾、肠胃外、眼部、肺部和局部施用。
[0062]
术语“受试者”或“患者”包括哺乳动物和鸟类。哺乳动物的示例包括但不限于哺乳动物类的任何成员:人类、非人类灵长类动物(诸如黑猩猩)、以及其他猿类和猴类物种;农场动物,诸如牛、马、绵羊、山羊、猪;家养动物,诸如兔、狗和猫;实验室动物,包括啮齿类动物,例如大鼠、小鼠和豚鼠等。在一实施方案中,哺乳动物是人类。
[0063]
如本文所用的术语“治疗(treat)”、“治疗(treating)”或“治疗(treatment)”包括缓解、降低或减轻疾病或病况的至少一种症状,预防额外的症状,抑制疾病或病况,例如阻止疾病或病况的发展、缓解疾病或病况、引起疾病或病况消退、缓解由疾病或病况引起的状况、或预防性和/或治疗性地停止疾病或病况的症状。特别地,术语“治疗(treat)”、“治疗(treatment)”或“治疗(treating)”是指减少受试者(例如,患者)经历冠状病毒诱导的疾病症状的频率、程度、严重性和/或持续时间。
[0064]
术语“预防(prevent)”、“预防(prevention)”或“预防(preventing)”是指抑制、降低风险、减少冠状病毒诱导的疾病相关症状的发作或避免冠状病毒诱导的疾病的相关病症。施用途径和剂量
[0065]
合适的施用途径包括但不限于经口服、静脉内、直肠、气雾、肠胃外、眼部、肺部、经粘膜、经皮、阴道、耳部、鼻部和局部施用。此外,仅作为示例,肠胃外递送包括肌内、皮下、静脉内、髓内注射、以及鞘内、直接心室内、腹膜内、淋巴管内和鼻内注射。
[0066]
在某些实施方案中,如本文所述的化合物以局部而非全身方式施用,例如通过将化合物直接注射到器官中,通常以贮库制剂或缓释制剂的形式。在具体实施方案中,长效制剂通过植入(例如皮下或肌内)或通过肌内注射施用。此外,在其他实施方案中,药物在靶向药物递送系统(例如,在用器官特异性抗体包被的脂质体中)中递送。在此类实施方案中,脂质体靶向器官并被器官选择性吸收。在又一些其他实施方案中,如本文所述的化合物以快速释放制剂的形式、以延长释放制剂的形式或以中等释放制剂的形式提供。在又一些其他实施方案中,本文所述的化合物是局部施用。
[0067]
在一些实施方案中,环己烯酮化合物或其药学上可接受的盐、代谢物、溶剂化物或前药被经肠胃外或静脉内施用。在其他实施方案中,环己烯酮化合物或其药学上可接受的盐、代谢物、溶剂化物或前药通过注射施用。在一些实施方案中,环己烯酮化合物或其药学上可接受的盐、代谢物、溶剂化物或前药是口服施用。
[0068]
在患者病况没有改善的情况下,根据医生的判断,化合物的施用可以长期施用,即持续延长的时间段(包括在患者的整个生命期间),以改善或以其他方式控制或限制患者疾病或病况的症状。在患者状态改善的情况下,根据医生的判断,化合物的施用可以连续或暂时暂停一段时间(即,“药物假期”)。
[0069]
上述范围仅是建议性的,因为关于个体治疗方案变量的数量很大,并且从这些推荐值的相当大的偏离并不少见。这种剂量可以根据许多变量而改变,不限于所用化合物的
活性、待治疗的疾病或病况、施用方式、个体受试者的要求、治疗的疾病或病况的严重程度和执业医生的判断。
[0070]
此类治疗方案的毒性和治疗功效可以通过细胞培养物或实验动物中的标准制药程序来确定,包括但不限于用于确定ld
50
(50%的人群的致死剂量)和ed
50
(50%的人群的治疗有效的剂量)。毒效与治疗效果之间的剂量比为治疗指数,可表达为ld
50
和ed
50
之间的比值。优选显示出高治疗指数的化合物。从细胞培养试验和动物研究中获得的数据可用于制定用于人类的剂量的范围。此类化合物的剂量优选在包括ed
50
且毒性最小的循环浓度范围内。根据所采用的剂型和所采用的施用途径,剂量可在此范围内变化。
[0071]
应理解,在一些实施方案中,根据多种因素修改用于治疗、预防或改善寻求缓解的病况的剂量方案。这些因素包括受试者所患的病症,以及受试者的年龄、体重、性别、饮食和医疗状况。因此,在其他实施方案中,实际采用的剂量方案变化宽泛,因此偏离了本文所述的剂量方案。
[0072]
药物制剂
[0073]
一些实施方案中提供了药物组合物,其包括:治疗有效量的具有以下结构的环己烯酮化合物:其中,x和y中的每个独立地为氧、nr5或硫;r为氢或c(=o)c
1-c8烷基;r1、r2和r3中的每个独立地为氢、任选地为取代的甲基或(ch2)
m-ch3;r4为nr5r6、or5、oc(=o)r7、c(=o)or5、c(=o)r5、c(=o)nr5r6、卤素、5或6元内酯、c
1-c8烷基、c
2-c8烯基、c
2-c8炔基、芳基、葡糖基,其中,所述5或6元内酯、c
1-c8烷基、c
2-c8烯基、c
2-c8炔基、芳基和葡糖基任选地被选自以下的一个或多个取代基取代:nr5r6、or5、oc(=o)r7、c(=o)or5、c(=o)r5、c(=o)nr5r6、c
1-c8烷基、c
2-c8烯基、c
2-c8炔基、c
3-c8环烷基和c
1-c8卤代烷基;r5和r6中的每个独立地为氢或c
1-c8烷基;r7为c
1-c8烷基、or5或nr5r6;m=1-12;并且n=1-12;或其药学上可接受的盐、代谢物、溶剂化物或前药;和药学上可接受的赋形剂。
[0074]
在一些实施方案中,药物组合物的环己烯酮化合物具有以下结构:其中,x和y中的每个独立地为氧、nr5或硫;
r为氢或c(=o)c
1-c8烷基;r1、r2和r3中的每个独立地为氢、任选地为取代的甲基或(ch2)
m-ch3;r4为nr5r6、or5、oc(=o)r7、c(=o)or5、c(=o)r5、c(=o)nr5r6、卤素、5或6元内酯、c
1-c8烷基、c
2-c8烯基、c
2-c8炔基、芳基、葡糖基,其中,所述5或6元内酯、c
1-c8烷基、c
2-c8烯基、c
2-c8炔基、芳基和葡糖基任选地被选自以下的一个或多个取代基取代:nr5r6、or5、oc(=o)r7、c(=o)or5、c(=o)r5、c(=o)nr5r6、c
1-c8烷基、c
2-c8烯基、c
2-c8炔基、c
3-c8环烷基和c
1-c8卤代烷基;r5和r6中的每个独立地为氢或c
1-c8烷基;r7为c
1-c8烷基、or5或nr5r6;m=1-12;并且n=1-12;或其药学上可接受的盐、代谢物、溶剂化物或前药。
[0075]
在一些实施方案中,r为氢、c(=o)c3h8、c(=o)c2h5或c(=o)ch3。在一些实施方案中,r1、r2和r3中的每个独立地是氢、甲基、乙基、丙基、丁基、戊基、己基、庚基或辛基。在某些实施方案中,r1为氢或甲基。在某些实施方案中,r2为氢、甲基、乙基、丙基、丁基、戊基或己基。在某些实施方案中,r3为氢、甲基、乙基、丙基、丁基、戊基或己基。在一些实施方案中,r4为卤素、nh2、nhch3、n(ch3)2、och3、oc2h5、c(=o)ch3、c(=o)c2h5、c(=o)och3、c(=o)oc2h5、c(=o)nhch3、c(=o)nhc2h5、c(=o)nh2、oc(=o)ch3、oc(=o)c2h5、oc(=o)och3、oc(=o)oc2h5、oc(=o)nhch3、oc(=o)nhc2h5或oc(=o)nh2。在某些实施方案中,r4为c2h5c(ch3)2oh、c2h5c(ch3)2och3、ch2cooh,c2h5cooh、ch2oh、c2h5oh、ch2ph、c2h5ph、ch2ch=c(ch3)(cho)、ch2ch=c(ch3)(c(=o)ch3)、5或6元内酯、芳基、或葡糖基,其中所述5或6元内酯、芳基和葡糖基任选地被选自以下的一个或多个取代基取代:nr5r6、or5、oc(=o)r7、c(=o)or5、c(=o)r5、c(=o)nr5r6、c
1-c8烷基、c
2-c8烯基、c
2-c8炔基、c
3-c8环烷基和c
1-c8卤代烷基。在某些实施方案中,r4是ch2cooh、c2h5cooh、ch2oh、c2h5oh、ch2ph、c2h5ph、ch2ch=c(ch3)(cho)、ch2ch=c(ch3)(c(=o)ch3)、5或6元内酯、芳基、或葡糖基,其中所述5或6元内酯、芳基和葡糖基任选地被选自以下一个或多个取代基取代:nr5r6、or5、oc(=o)r7、c(=o)or5、c(=o)r5、c(=o)nr5r6、c
1-c8烷基、c
2-c8烯基、c
2-c8炔基、c
3-c8环烷基和c
1-c8卤代烷基。在某些实施方案中,r4为任选地被选自以下的一个或多个取代基取代的5或6元内酯:nr5r6、or5、oc(=o)r7、c(=o)or5、c(=o)r5、c(=o)nr5r6、c
1-c8烷基、c
2-c8烯基、c
2-c8炔基、c
3-c8环烷基和c
1-c8卤代烷基。
[0076]
在某些实施方案中,化合物选自:
[0077]
在某些实施方案中,化合物选自:
[0078]
在一些实施方案中,本文所述的化合物被配制成药物组合物。在特定实施方案中,药物组合物以常规方式使用一种或多种生理学可接受的载体配制,该载体包括促进将活性化合物加工成可药用的制剂的赋形剂和助剂。适当的制剂取决于所选择的施用途径。任何药学上可接受的技术、载体和赋形剂都适用于配制本文所述的药物组合物:雷明顿:药学科
学与实践,第十九版(宾夕法尼亚州伊斯顿:麦克出版公司,1995)(remington:the science and practice of pharmacy,nineteenth ed(easton,pa.:mack publishing company,1995));hoover,john e.,雷明顿药物科学,麦克出版公司,宾夕法尼亚州伊斯顿1975(hoover,john e.,remington’s pharmaceutical sciences,mackpublishing co.,easton,pennsylvania 1975);liberman,h.a.和lachman,l.编著,药物剂型,marcel decker,纽约,n.y.,1980(liberman,h.a.and lachman,l.,eds.,pharmaceutical dosage forms,marcel decker,new york,n.y.,1980);和药用剂型和递送系统,第七版(pharmaceutical dosage forms and drug delivery systems,seventh ed.)(lippincott williams&wilkins1999)。
[0079]
本文提供包含化合物(即本文所述的环己烯酮化合物)和药学上可接受的稀释剂、赋形剂或载体的药物组合物。在某些实施方案中,如在联合疗法中,所述的化合物作为其中化合物(即,本文所述的环己烯酮化合物)与其他活性成分混合的药物组合物施用。本文涵盖以下联合疗法部分和本公开全文中阐述的活性物质的所有组合。在具体实施方案中,药物组合物包括一种或多种化合物(即,本文所述的环己烯酮化合物)。
[0080]
本文所用的术语“药物组合物”是指化合物(即本文所述的环己烯酮化合物)与其他化学组分(诸如载体、稳定剂、稀释剂、分散剂、悬浮剂、增稠剂和/或赋形剂)的混合物。在某些实施方案中,药物组合物有助于将化合物施用于生物体。在一些实施方案中,实施本文提供的治疗方法或用途时,将治疗有效量的化合物(即,本文所述的环己烯酮化合物)以药物组合的物形式施用于患有待治疗的疾病或病况的哺乳动物。在具体实施方案中,哺乳动物是人类。在某些实施方案中,治疗有效量根据疾病的严重程度、受试者的年龄和相对健康状况、所用化合物的效力和其他因素而变化。本文所述的化合物单独使用或与一种或多种治疗剂组合作为混合物的组分使用。
[0081]
在一实施方案中,将化合物(即,本文所述的环己烯酮化合物)配制成水溶液。在具体实施方案中,水溶液选自,仅作为示例,生理相容性缓冲液(诸如汉克氏溶液(hank’s solution)、林格氏溶液(ringer’s solution))或生理盐水缓冲液。在其他实施方案中,化合物(即,本文所述的环己烯酮化合物)被配制为经粘膜施用。在具体的实施方案中,经粘膜制剂包括适合待渗透的屏障的渗透剂。在其中将本文所述的化合物配制用于其他肠胃外注射的又一些其他实施方案中,合适的制剂包括水溶液或非水溶液。在具体实施方案中,此类溶液包含生理相容性缓冲液和/或赋形剂。
[0082]
在另一个实施方案中,本文所述的化合物被配制用于口服施用。本文所述的化合物,包括化合物(即,本文所述的环己烯酮化合物),通过将活性化合物与例如药学上可接受的载体或赋形剂组合来配制。在各种实施方案中,将本文所述的化合物配制成口服剂型,包括,仅作为示例,片剂、粉剂、丸剂、糖衣丸、胶囊、液体、凝胶、糖浆、酏剂、浆液、悬浮液等。
[0083]
在某些实施方案中,用于口服使用的药物制剂通过如下获得:将一种或多种固体赋形剂与一种或多种本文所述的化合物混合,任选地研磨所得混合物,并在添加合适的助剂后加工颗粒剂混合物(如果需要),以获得片剂或糖衣丸芯。合适的赋形剂,尤其是填充剂,例如糖类,包括乳糖、蔗糖、甘露醇或山梨糖醇;纤维素制剂,诸如:例如玉米淀粉、小麦淀粉、大米淀粉、马铃薯淀粉、明胶、黄蓍胶、甲基纤维素、微晶纤维素、羟丙基甲基纤维素、羧甲基纤维素钠;或其他,诸如:聚乙烯吡咯烷酮(pvp或聚维酮)或磷酸钙。在具体实施方案
中,任选地添加崩解剂。崩解剂包括,仅作为示例,交联的交联羧甲基纤维素钠、聚乙烯吡咯烷酮、琼脂或海藻酸或其盐诸如海藻酸钠。
[0084]
在一实施方案中,诸如糖衣丸芯和片剂的剂型具有一种或多种合适的包衣。在具体实施方案中,浓缩糖溶液用于对该剂型包衣。糖溶液任选地包含附加组分,诸如仅作为示例,阿拉伯树胶、滑石、聚乙烯吡咯烷酮、卡波姆凝胶、聚乙二醇和/或二氧化钛、漆溶液和合适的有机溶剂或溶剂混合物。染料和/或颜料也可选地添加到包衣中以用于识别目的。此外,染料和/或颜料可选地用于表征活性化合物剂量的不同组合。
[0085]
在某些实施方案中,将治疗有效量的至少一种本文所述的化合物配制成其他口服剂型。口服剂型包括由明胶制成的推入配合式胶囊,以及由明胶和增塑剂(诸如甘油或山梨糖醇)制成的软密封胶囊。在具体实施方案中,推入配合式胶囊含有与一种或多种填充剂混合的活性成分。填充剂包括,仅作为示例,乳糖、粘合剂(诸如淀粉)和/或润滑剂(诸如滑石或硬脂酸镁)和任选的稳定剂。在其他实施方案中,软胶囊含有一种或多种溶解或悬浮在合适液体中的活性化合物。合适的液体包括,仅作为示例,一种或多种脂肪油、液体石蜡或液体聚乙二醇。此外,任选地加入稳定剂。
[0086]
在其他实施方案中,治疗有效量的至少一种本文所述的化合物被配制用于经口腔或舌下施用。适合于经口腔或舌下施用的制剂包括,仅作为示例,片剂、锭剂或凝胶剂。在又一些其他实施方案中,本文所述的化合物被配制用于肠胃外注射,包括适用于大剂量注射或连续输注的制剂。在具体的实施方案中,注射用制剂以单位剂型(例如,在安瓿中)或在多剂量容器中。任选地将防腐剂添加到注射制剂中。在又一些其他实施方案中,化合物(即,本文所述的环己烯酮化合物)的药物组合物以适合肠胃外注射的形式被配制为在油性或水性媒介物中的无菌悬浮液、溶液或乳液。肠胃外注射制剂任选地包含配制剂,例如悬浮剂、稳定剂和/或分散剂。在具体的实施方案中,用于肠胃外施用的药物制剂包括以水溶性形式的活性化合物的水溶液。在另外的实施方案中,活性化合物的悬浮液被制备成合适的油性注射悬浮液。用于本文所述的药物组合物的合适的亲脂性溶剂或媒介物包括,仅作为示例,诸如芝麻油的脂肪油、或诸如油酸乙酯或甘油三酯的合成脂肪酸酯、或脂质体。在某些具体实施方案中,水性注射悬浮液含有增加悬浮液粘度的物质,例如羧甲基纤维素钠、山梨糖醇或葡聚糖。任选地,悬浮液包含合适的稳定剂或增加化合物溶解度以允许制备高浓度溶液的试剂。或者,在其他实施方案中,活性成分为粉末形式,用于在使用前与合适的媒介物(例如,无菌无热原水)一起配成。
[0087]
在一方面,将化合物(即,本文所述的环己烯酮化合物)制备为如本文所述或本领域已知的肠胃外注射用溶液并用自动注射器进行施用。自动注射器,诸如在美国专利号4,031,893、5,358,489;5,540,664;5,665,071、5,695,472和wo/2005/087297(对于这些公开,其每一个都通过引用并入本文)中公开的那些自动注射器,是已知的。通常,所有自动注射器都包含一定体积的溶液,该溶液包含待注射的化合物(即,本文所述的环己烯酮化合物)。通常,自动注射器包括用于保持溶液的储器,该储器与用于递送药物的针流体连通;以及用于自动展开针、将针插入患者体内并将剂量递送到患者体内的机构。示例性注射器以每1ml溶液约0.5mg至50mg化合物(即,本文所述的环己烯酮化合物)的浓度提供约0.3ml、0.6ml、1.0ml或其他合适体积的溶液。每个注射器只能递送一剂量的化合物。
[0088]
在又一些其他实施方案中,化合物(即,本文所述的环己烯酮化合物)被局部施用。
本文所述的化合物被配制成多种可局部施用的组合物,例如溶液、悬浮液、洗剂、凝胶、糊剂、药棒、香膏、乳膏或软膏。这种药物组合物任选地包含增溶剂、稳定剂、张力增强剂、缓冲剂和防腐剂。
[0089]
在又一些其他实施方案中,化合物(即,本文所述的环己烯酮化合物)被配制用于经皮施用。在具体实施方案中,经皮制剂采用经皮递送装置和经皮递送贴剂并且可以是溶解和/或分散在聚合物或粘合剂中的亲脂性乳液或缓冲水溶液。在各种实施方案中,此类贴剂被构造用于药剂的连续、脉动式或按需递送。在另外的实施方案中,化合物(即,本文所述的环己烯酮化合物)的经皮递送是通过离子电渗贴剂等实现的。在某些实施方案中,经皮贴剂提供化合物(即,本文所述的环己烯酮化合物)的受控递送。在具体实施方案中,通过使用速率控制膜或通过将化合物捕获在聚合物基质或凝胶内来减慢吸收速率。在替代实施方案中,吸收促进剂用于增加吸收。吸收促进剂或载体包括辅助通过皮肤的可吸收的药学上可接受的溶剂。例如,在一实施方案中,经皮装置呈绷带形式,该经皮装置包括背衬构件;储器,该储器含有任选具有载体的化合物;任选的速率控制屏障物,用于在长的时间段内以受控的和预定的速率将化合物递送至宿主的皮肤;以及将装置固定到皮肤上的用具。
[0090]
可以使用本领域已经描述的各种装置来施用本文所述的经皮制剂。例如,这样的装置包括但不限于美国专利号3,598,122、3,598,123、3,710,795、3,731,683、3,742,951、3,814,097、3,921,636、3,972,995、3,993,072、3,993,073、3,996,934、4,031,894、4,060,084、4,069,307、4,077,407、4,201,211、4,230,105、4,292,299、4,292,303、5,336,168、5,665,378、5,837,280、5,869,090、6,923,983、6,929,801和6,946,144。
[0091]
本文所述的经皮剂型可包含本领域常规的某些药学上可接受的赋形剂。在一个实施方案中,本文所述的经皮制剂包括至少三种组分:(1)化合物(即,本文所述的环己烯酮化合物)的制剂;(2)渗透增强剂;(3)水性佐剂。此外,经皮制剂可包括附加组分,例如但不限于胶凝剂、乳膏和软膏基材等。在一些实施方案中,经皮制剂还包括织造或非织造背衬材料以增强吸收并防止经皮制剂从皮肤上去除。在其他实施方案中,本文所述的经皮制剂保持饱和或过饱和状态以促进扩散到皮肤中。
[0092]
在其他实施方案中,化合物(即,本文所述的环己烯酮化合物)被配制为用于通过吸入施用。适合通过吸入施用的各种形式包括但不限于气雾剂、雾剂或粉剂。化合物(即,本文所述的环己烯酮化合物)的药物组合物方便地以气雾剂喷雾形式从加压包装物或喷雾器、使用合适的推进剂(例如,二氯二氟甲烷、三氯氟甲烷、二氯四氟乙烷、二氧化碳或其他合适的气体)来递送。在具体的实施方案中,加压气雾剂的剂量单位是通过提供递送计量的量的阀来确定。在某些实施方案中,例如,仅作为示例,用于吸入器或吹药器中的明胶的胶囊和药筒被配制为含有化合物和合适的粉末基材(例如乳糖或淀粉)的粉末混合物。
[0093]
鼻内制剂是本领域中已知的,且描述于例如美国专利号4,476,116、5,116,817和6,391,452中,其中每一个都通过引用具体并入本文。使用苯甲醇或其他合适的防腐剂、碳氟化合物和/或本领域已知的其他增溶剂或分散剂,将包括化合物(即,本文所述的环己烯酮化合物)的制剂根据这些和本领域公知的其他技术制备成在盐水中的溶液。参见,例如,ansel,h.c.等,药物剂型和药物递送系统,第六版(1995)(ansel,h.c.et al.,pharmaceutical dosage forms and drug delivery systems,sixth ed.(1995))。优选地,这些组合物和制剂用合适的无毒药学上可接受的成分制备。这些成分诸如在该领域的
标准参考:雷明顿:药剂学的科学和实践,第21版,2005(remington:the science and practice of pharmacy,21st edition,2005)中找到。合适载体的选择高度依赖于所需鼻用剂型(例如溶液、悬浮液、软膏或凝胶)的确切性质。除活性成分外,鼻用剂型通常含有大量的水。也可以存在少量其他成分,例如ph调节剂、乳化剂或分散剂、防腐剂、表面活性剂、胶凝剂或缓冲剂和其他稳定剂和增溶剂。优选地,鼻用剂型应与鼻分泌物等渗。
[0094]
对于吸入施用,本文所述的化合物可以是气雾剂、雾剂或粉剂形式。本文所述的药物组合物方便地以气雾剂喷雾形式从加压包装物或喷雾器、使用合适的推进剂(例如,二氯二氟甲烷、三氯氟甲烷、二氯四氟乙烷、二氧化碳或其他合适的气体)来递送。在加压气雾剂的情况下,剂量单位可通过设置递送计量的量的阀门来确定。诸如仅作为示例,用于吸入器或吹药器中的明胶的胶囊和药筒可以被配制为含有本文所述的化合物和合适的粉末基材(例如乳糖或淀粉)的粉末混合物。
[0095]
在其他实施方案中,化合物(即,本文所述的环己烯酮化合物)被配制成直肠组合物,诸如灌肠剂、直肠凝胶剂、直肠泡沫剂、直肠气雾剂、栓剂、胶状栓剂或保留灌肠剂,其含有常规栓剂基材(诸如可可脂或其他甘油酯),以及合成聚合物(诸如聚乙烯吡咯烷酮、peg等)。在组合物的栓剂形式中,首先熔化任选地与可可脂组合的低熔点蜡(诸如但不限于脂肪酸甘油酯的混合物)。
[0096]
在某些实施方案中,以任何常规方式使用一种或多种生理学上可接受的载体配制药物组合物,所述生理学上可接受的载体包括促进将活性化合物加工成可药用的制剂的赋形剂和助剂。适当的制剂取决于所选择的施用途径。如本领域合适的且所理解的,任选地使用任何药学上可接受的技术、载体和赋形剂。包含化合物(即,本文所述的环己烯酮化合物)的药物组合物可以以常规方式制造,诸如,仅作为示例,通过常规混合、溶解、制粒、糖衣丸制造、磨细、乳化、封装、包埋或压缩工艺制造。
[0097]
药物组合物包括至少一种药学上可接受的载体、稀释剂或赋形剂和作为活性成分的至少一种本文所述的化合物(即,本文所述的环己烯酮化合物)。活性成分呈游离酸或游离碱形式,或呈药学上可接受的盐形式。此外,本文所述的方法和药物组合物包括使用结晶形式(也称为多晶型物),以及具有相同类型活性的这些化合物的活性代谢物。本文所述化合物的所有互变异构体均包括在本文所述化合物的范围内。术语“药学上可接受的盐”是指保留游离碱的生物有效性和性质并且通过与无机酸或有机酸反应获得的那些盐,所述无机酸或有机酸诸如盐酸、氢溴酸、硫酸、硝酸、磷酸、甲磺酸、乙磺酸、对甲苯磺酸、水杨酸、苹果酸、马来酸、琥珀酸、酒石酸、柠檬酸等。
[0098]
此外,本文所述的化合物包括非溶剂化形式以及与药学上可接受的溶剂(例如水、乙醇等)形成的溶剂化形式。本文中呈现的化合物的溶剂化形式也被认为是在本文中公开的。此外,药物组合物任选地包括其他药用制剂或药物制剂、载体、佐剂(诸如防腐剂、稳定剂、润湿剂或乳化剂)、溶液促进剂、用于调节渗透压的盐、缓冲剂和/或其他有治疗价值的物质。
[0099]
用于制备包括本文所述化合物的组合物的方法包括将化合物与一种或多种惰性、药学上可接受的赋形剂或载体一起配制以形成固体、半固体或液体。固体组合物包括但不限于粉剂、片剂、可分散颗粒剂、胶囊剂、扁囊剂和栓剂。液体组合物包括其中溶解有化合物的溶液、包含化合物的乳液、或含有包括本文公开的化合物的脂质体、胶束或纳米颗粒的溶
液。半固体组合物包括但不限于凝胶、悬浮液和乳膏剂。本文所述的药物组合物的形式包括液体溶液或悬浮液、适用于在使用前在液体中溶解或悬浮的固体形式,或作为乳液。这些组合物还任选地包含少量无毒的辅助物质,例如润湿剂或乳化剂、ph缓冲剂等。
[0100]
在一些实施方案中,至少包含化合物(即,本文所述的环己烯酮化合物)的药物组合物说明性地采取液体形式,其中所述药剂存在于溶液、悬浮液或两者中。通常,当组合物作为溶液或悬浮液施用时,第一部分药剂存在于溶液中,而第二部分药剂以颗粒形式存在于液体基质中的悬浮液中。在一些实施方案中,液体组合物包括凝胶制剂。在其他实施方案中,液体组合物是水性的。
[0101]
在某些实施方案中,药物水性悬浮液包含一种或多种聚合物作为悬浮剂。聚合物包括水溶性聚合物(诸如纤维素聚合物,例如、羟丙基甲基纤维素)和水不溶性聚合物(诸如交联的含羧基聚合物)。本文所述的某些药物组合物包括粘膜粘附聚合物,选自例如羧甲基纤维素、卡波姆(丙烯酸聚合物)、聚(甲基丙烯酸甲酯)、聚丙烯酰胺、聚卡波非、丙烯酸/丙烯酸丁酯共聚物、海藻酸钠和葡聚糖。
[0102]
药物组合物还任选地包含增溶剂以促进化合物(即,本文所述的环己烯酮化合物)的溶解度。术语“增溶剂”通常包括导致形成试剂的胶束溶液或真溶液的试剂。某些可接受的非离子表面活性剂(例如聚山梨醇酯80)可用作增溶剂,眼部可接受的乙二醇、聚乙二醇(例如,聚乙二醇400和乙二醇醚)也可作为增溶剂。
[0103]
此外,药物组合物任选地包含一种或多种ph调节剂或缓冲剂,包括酸,诸如乙酸、硼酸、柠檬酸、乳酸、磷酸和盐酸;碱,诸如氢氧化钠、磷酸钠、硼酸钠、柠檬酸钠、醋酸钠、乳酸钠、三羟甲基氨基甲烷;和缓冲液,诸如柠檬酸盐/葡萄糖、碳酸氢钠和氯化铵。这些酸、碱和缓冲液以将组合物的ph保持在可接受范围内所需的量内被包含。
[0104]
此外,药物组合物任选地包含一种或多种盐,该一种或多种盐以使组合物的克分子渗透压浓度达到可接受范围所需的量被包含。此类盐包括具有钠阳离子、钾阳离子或铵阳离子和盐酸根、柠檬酸根、抗坏血酸根、硼酸根、磷酸根、碳酸氢根、硫酸根、硫代硫酸根或亚硫酸氢根阴离子的那些盐;合适的盐包括氯化钠、氯化钾、硫代硫酸钠、亚硫酸氢钠和硫酸铵。
[0105]
其他药物组合物任选地包含一种或多种防腐剂以抑制微生物活性。合适的防腐剂包括含汞物质,诸如硼酸苯汞(merfen)和硫柳汞;稳定二氧化氯;和季铵化合物,诸如苯扎氯铵、十六烷基三甲基溴化铵和十六烷基氯化吡啶鎓。
[0106]
又一些其他药物组合物包含一种或多种表面活性剂以增强物理稳定性或用于其他目的。合适的非离子表面活性剂包括聚氧乙烯脂肪酸甘油酯和植物油,例如,聚氧乙烯(60)氢化蓖麻油;和聚氧乙烯烷基醚和烷基苯基醚,例如,辛基酚聚醚(octoxynol)10、辛基酚聚醚40。
[0107]
又一些其他药物组合物可包含一种或多种抗氧化剂以在需要时增强化学稳定性。合适的抗氧化剂包括,仅作为示例,抗坏血酸和焦亚硫酸钠。
[0108]
在某些实施方案中,药物水性悬浮液组合物被封装在单剂量不可重新封闭的容器中。或者,使用多剂量可重新封闭的容器,在这种情况下,通常在组合物中包含防腐剂。
[0109]
在替代实施方案中,采用用于疏水性药物化合物的其他递送系统。脂质体和乳液是本文中递送媒介物或载体的示例。在某些实施方案中,也采用有机溶剂,诸如n-甲基吡咯
烷酮。在额外的实施方案中,本文所述的化合物使用缓释系统来递送,例如含有治疗剂的固体疏水聚合物的半透性基质。在本文中可用各种缓释材料。在一些实施方案中,缓释胶囊释放化合物持续数小时至超过24小时。根据治疗试剂的化学性质和生物稳定性,可以采用额外的蛋白质稳定策略。
[0110]
在某些实施方案中,本文所述的制剂包含一种或多种抗氧化剂、金属螯合剂、含硫醇的化合物和/或其他通用稳定剂。此类稳定剂的示例包括但不限于:(a)约0.5%至约2%w/v的甘油、(b)约0.1%至约1%w/v的甲硫氨酸、(c)约0.1%至约2%w/v的单硫代甘油、(d)约1mm至约10mm的edta、(e)约0.01%至约2%w/v的抗坏血酸、(f)0.003%至约0.02%w/v的聚山梨醇酯80、(g)0.001%至约0.05%w/v的聚山梨醇酯20、(h)精氨酸、(i)肝素、(j)硫酸葡聚糖、(k)环糊精、(l)戊聚糖多硫酸酯和其他类肝素、(m)二价阳离子诸如镁和锌,或(n)它们的组合。实施例实施例1:示例性环己烯酮化合物的制备
[0111]
将100g来自牛樟芝的菌丝体放入烧瓶中。将适量的水和酒精(70-100%的乙醇溶液)添加至烧瓶中并在20-25℃下搅拌至少1小时。将溶液通过过滤器和0.45μm膜过滤,并收集滤液作为提取物。在一个实例中,例如,提取物通过在lee,t-h.等,planta med 2007;73:1412-1415中公开的固态发酵菌丝体条件和组合物来制备。
[0112]
将牛樟芝的滤液进行高效液相色谱(hplc)分析。在rp18柱上进行分离,流动相由甲醇(a)和0.3%乙酸(b)组成,其中梯度条件为:95%-20%b中0-10min,20%-10%b中10-20min,10%-10%b中20-35min,10%-95%b中35-40min,流速为1ml/min。用紫外-可见检测器监测柱流出物。
[0113]
对在21.2至21.4min收集的级分进行收集并浓缩以产生化合物5,为淡黄色液体产物。化合物5经分析为4-羟基-5-(11-羟基-3,7,11-三甲基十二碳-2,6-二烯基)-2,3-二甲氧基-6-甲基环己-2-烯酮,分子量为408(分子式:c
24h40
o5)。1h-nmr(cdcl3)δ(ppm)=1.21,1.36,1.67,1.71,1.75,1.94,2.03,2.07,2.22,2.25,3.68,4.05,5.71和5.56。
13
c-nmr(cdcl3)δ(ppm):12.31,16.1,16.12,17.67,25.67,26.44,26.74,27.00,30.10,40.27,43.34,59.22,60.59,71.8,120.97,123.84,124.30,131.32,134.61,135.92,138.05,160.45和197.11。化合物5:4-羟基-5-(11-羟基-3,7,11-三甲基十二碳-2,6-二烯基)-2,3-二甲氧基-6-甲基环己-2-烯酮
[0114]
对在23.7至24.0min收集的级分进行收集并浓缩以产生化合物7,为淡黄色液体产物。化合物7经分析为4-羟基-2,3-二甲氧基-5-(11-甲氧基-3,7,11-三甲基十二碳-2,6-二烯基)-6-甲基环己-2-烯酮,分子量为422(c
25 h
42
o5)。1h-nmr(cdcl3)δ(ppm)=1.21,1.36,1.71,1.75,1.94,2.03,2.07,2.22,2.25,3.24,3.68,4.05,5.12,5.50和5.61。
13
c-nmr
(cdcl3)δ(ppm):12.31,16.1,16.12,17.67,24.44,26.44,26.74,27.00,37.81,39.81,40.27,43.34,49.00,59.22,60.59,120.97,123.84,124.30,135.92,138.05,160.45和197.12。化合物7:4-羟基-2,3-二甲氧基-5-(11-甲氧基-3,7,11-三甲基十二碳-2,6-二烯基)-6-甲基环己-2-烯酮
[0115]
对在25至30min收集的级分进行收集并浓缩,得到4-羟基-2,3-二甲氧基-6-甲基-5-(3,7,11-三甲基十二碳-2,6,10-三烯基)环己-2-烯酮(化合物1,也称为安卓奎诺尔),为淡黄棕色液体产物。化合物1的分析显示了c
24h38
o4的分子式,分子量为390,熔点为48至52℃。核磁共振谱表明,1h-nmr(cdcl3)δ(ppm)=1.51,1.67,1.71,1.75,1.94,2.03,2.07,2.22,2.25,3.68,4.05,5.07和5.14;
13
c-nmr(cdcl3)δ(ppm)=12.31,16.1,16.12,17.67,25.67,26.44,26.74,27.00,39.71,39.81,40.27,43.34,59.22,60.59,120.97,123.84,124.30,131.32,135.35,135.92,138.05,160.45和197.12。化合物1:4-羟基-2,3-二甲氧基-6-甲基-5-(3,7,11-三甲基十二碳-2,6,10-三烯基)环己-2-烯酮
[0116]
化合物27(化合物1的代谢物)是从动物研究中进食了化合物1的大鼠的尿样本中获得的。化合物27经测定为4-羟基-2,3-二甲氧基-6-甲基-5-(3-甲基-2-己烯酸)环己-2-烯酮,分子量为312(c
16h24
o6)。测定为2,3-二甲氧基-5-甲基-6-((2e,6e)-3,7,11-三甲基十二碳-2,6,10-三烯基)环己-2,5-二烯-1,4-二酮(分子量为386.52,c
24h34
o4)的化合物25是从纯化工艺中获得的。
[0117]
化合物26,4-羟基-2-甲氧基-6-甲基-5-((2e,6e)-3,7,11-三甲基十二碳-2,6,10-三烯基)环己-2-烯酮,也是通过纯化工艺制备的,分子量为350.53(c
23h36
o3)。也制备了化合物28。
[0118]
或者,示例性化合物可由4-羟基-2,3-二甲氧基-6-甲基环己-2,5-二烯酮等制备。例如,参见美国专利号9,365,481和美国专利公开号2016-0237012中的示例。类似地,具有结构的其他环己烯酮化合物从牛樟芝分离或由合适的原料经合成或半合成制备。本领域普通技术人员将容易地利用合适的条件进行此类合成。实施例2:化合物1(安卓奎诺尔)的抗病毒、抗炎症、抗纤维化活性研究
[0119]
对示例性化合物(化合物1)进行抗病毒、抗炎症和抗纤维化活性研究。
[0120]
材料和方法
[0121]
细胞培养。将hepg2.2.15细胞系在37℃下,在5%co2培养箱中,在mem培养基中培养,培养基补充有10%胎牛血清、青霉素(100iu/ml;gibco,美国)和链霉素(100ug/ml;gibco,美国)。这是一种源自人肝母细胞瘤细胞系hepg2的细胞系,其特征在于具有稳定的hbv表达。qs5是产生hbv的大鼠肝癌细胞系。
[0122]
购得拉米夫定(3tc)和阿德福韦酯(adv)作为阳性对照用于hbv治疗。将安卓奎诺尔(g4)和拉米夫定(3tc)溶于二甲亚砜(dmso),仅用于储备溶液并在培养基中稀释。细胞中dmso的最终浓度低于0.1%。将药物用2x104细胞在96孔板中处理72小时。
[0123]
hepg2.2.15上清液中hbsag和hbeag水平用他们的商业酶联免疫吸附测定(elisa)试剂盒按照制造商的说明进行测量。
[0124]
mtt测定。将1.25x105细胞/孔接种到24孔板上。将细胞与不同浓度的g4和3tc(1、5、25、50、100和200um)一起温育72小时。将1mg/ml 3-(4,5-二甲基噻唑-2-基)-2,5-二苯基四唑鎓-溴化物(mtt)添加到每个孔中,并在37℃温育2小时,以形成有色晶体。用dmso代替培养基并将板在室温振荡温育15分钟以溶解晶体。通过酶标仪测量吸光度。在490nm处测量光密度。
[0125]
病毒dna的southern印迹分析。将与hbv核心颗粒相关的dna在1.2%天然琼脂糖凝胶上解析,并使用特异性hbv dna探针通过southern印迹分析进行检测。southern印迹凝胶的每个泳道上装载有从每个处理培养皿中提取的与核心颗粒相关的病毒dna的总量,在转染前一晚以相同的细胞密度接种。结果
[0126]
为了检查安卓奎诺尔对hbv蛋白表达(包括表面抗原(hbsag)和e抗原(hbeag))的影响,使用elisa测定来量化hbv复制。研究结果表明,化合物1(即,安卓奎诺尔)降低hbeag(见图1a)和hbsag(见图1b)表达水平。与拉米夫定相比,化合物1显示了两种主要的hbv生物
标志物hbeag和hbsag的表达水平分别降低了50%和40%。因此,简而言之,示例性化合物1在不同剂量不仅对hbeag而且对hbsag显示出显著的抑制作用。
[0127]
为了评价示例性化合物1对病毒复制的效果,分离和分析了与细胞内hbv核心颗粒相关的dna。通过southern印迹,示例性化合物1(安卓奎诺尔)显示显著地抑制了hbv复制中间体(松弛环状、线性和单链dna)。如图2a/b显示,化合物1(安卓奎诺尔)降低了hbv dna表达水平(2a),并降低了hcv rna活性(2b)。特别是,与拉米夫定和阿德福韦酯相比,化合物1在降低hbv dna表达水平方面显示出更明显的结果。化合物1还显示hcv rna活性显著降低95%。
[0128]
安卓奎诺尔抑制hbv的产生可能是其细胞毒性的结果,并且通过使用mtt测定检查了这种可能性。在暴露于高达5um安卓奎诺尔时未检测到明显的细胞毒性,表明安卓奎诺尔对上清液病毒蛋白和dna水平的抑制作用不是由其细胞毒性引起的。值得注意的是,超过25um的安卓奎诺尔对hepg2.2.15细胞具有细胞毒性作用。
[0129]
为了治疗、减轻受试者中冠状病毒感染(例如sars-cov-2)的症状或预防受试者中冠状病毒感染(例如sars-cov-2)的病程,应理解,除抗病毒活性外,还需要多种方法,如图3所示。病毒感染后,病毒会复制且病毒数量增加,发生炎症引起细胞因子风暴,导致肿块纤维化。因此,具有抗病毒、抗炎症甚至抗纤维化能力的化合物(诸如示例性化合物1)是对抗冠状病毒感染的合适药物,如图4所示。例如,这表明化合物1抑制mtor的功能并抑制内吞作用。
[0130]
尤其是,研究结果(参见图5)提供了化合物1与水飞蓟素相比,在较低的施用浓度下显示出nrf-2核转位的有效增加。图6提供了化合物1显著降低乙醇诱导的alt和ast升高并抑制氧化应激。化合物1的其他抗炎症结果包括将nf-kb表达抑制36%,以及将核nrf-2表达增强2倍,如图7所示。在图8中,化合物1还显示分别有效抑制mcp-1、il-6和cd3表达约50%、57%和66%。以上所有研究结果均表明化合物1在抗炎症活性中的有效性。
[0131]
还发现示例性化合物1提供抗纤维化活性。图9a说明了示例性化合物1有效抑制tgf-β1的表达约64%。在利用纤维化相关蛋白(col 1和col iii)的研究中,化合物1还显示了如图9b所示的抗纤维化特性。因此,数据清楚地表明化合物1消除了病毒活性、炎症效应子的蛋白表达和tgfβ1信号介导的纤维化。实施例3:示例性化合物1对covid-19进展的影响研究
[0132]
该研究旨在评价示例性化合物1通过抗sars-cov-2(特异性目标1)、抗sars-cov-2诱导的细胞因子风暴和抗sars-cov-2诱导的纤维化(特异性目标2)对covid-19(即sars-cov-2)进展的影响。总体目标是确认示例性化合物1(即、安卓奎诺尔)是否为covid-19治疗提供了潜在的三重作用,并为sars-cov-2患者提供了一种新的治疗方案。
[0133]
特异性目标1.研究安卓奎诺尔对抗sars-cov-2的功能效果
[0134]
产率降低测定用于确定安卓奎诺尔对sars-cov-2的抑制率(ec
50
)。简而言之,将vero e6细胞接种到含有2%fbs的dmem的24孔培养板中,并用化合物1(即、安卓奎诺尔,10或20μm)处理1小时。将在dmso中的没有任何处理的平板用作对照。然后,将所得细胞用sars-cov-2(感染复数,moi=0.1)感染1小时。去除安卓奎诺尔和病毒后,将细胞用pbs洗涤一次,并用含有不同浓度安卓奎诺尔的覆盖培养基覆盖24小时。收集细胞培养基用于病毒噬菌斑测定以确定噬菌斑形成单位的数量。在感染前1天,将vero e6细胞接种到含有10%
fbs和抗生素的dmem的24孔培养板中。将细胞培养基添加到细胞单层中,并在37℃下温育1小时。随后,除去细胞培养基,并将细胞单层用pbs洗涤一次,然后用含有1%甲基纤维素的培养基覆盖5天。将细胞用10%甲醛固定1小时。去除覆盖培养基后,用0.5%结晶紫染色细胞,将噬菌斑计数。分别通过amresco的ripa细胞裂解缓冲液和nucleospin rna试剂盒(macherey-nagel)收集细胞用于蛋白质和rna提取。然后,分别通过蛋白质印迹(抗体目录号40143-r019)和定量实时pcr(qrt-pcr)检测核衣壳蛋白和e基因的表达水平。此外,将分离的rna用于特异性目标2。此外,安卓奎诺尔对vero e6细胞的细胞毒性(即ic
50
)将通过酸性磷酸酶测定进行测量。本文中,瑞德西韦(1μm)治疗将用作对照。所有结果将显示为来自至少三个独立实验的平均值
±
s.d.。
[0135]
研究结果表明,20和10μm的化合物1均显著降低了sars-cov-2浓度(20μm为99.93%,10μm为91.20%)。参见图10。图11还提供了细胞培养结果,显示了来自安卓奎诺尔和对照(dmso板)处理的细胞培养板。
[0136]
特异性目标2.探索安卓奎诺尔对sars-cov-2诱导的细胞因子风暴和对sars-cov-2诱导的纤维化的影响
[0137]
目前的研究表明,多种细胞因子/趋化因子与covid-19疾病显著相关。例如,血浆ip-10(也称为cxcl10)与疾病严重程度高度相关,可预测covid-19的进展。il-6还可以作为进展为严重covid-19的预测因子,这表明靶向细胞因子作为covid-19患者的治疗选项。关于covid-19的长期影响,tgf-β介导的胶原沉积可能是造成不可逆肺纤维化的重要因素。
[0138]
为了揭示安卓奎诺尔对sars-cov-2诱导的细胞因子风暴和对sars-cov-2诱导的纤维化的影响,将特异性目标1中描述的rna用于检测细胞因子/趋化因子(诸如cxcl10、il6、和il18,见图12a-c)、促纤维化生长因子(诸如tgfb1,见图13a)和胶原(诸如col1a1、col3a1和col4a1)的基因表达。简而言之,通过m-mlv逆转录酶试剂盒将5.4μgrna逆转录为cdna。使用sybr
tm
green master mix试剂盒建立实时pcr分析,并在quantstudio
tm 5实时pcr系统中进行。通过归一化肌动蛋白rrna确定目标mrna的相对水平。研究结果:
[0139]
图12a-c分别提供了cxcl10(12a)、il6(12b)、和il18(12c)的基因表达水平。使用20μm的安卓奎诺尔,cxcl10表达发生1.01倍变化,而使用10μm的安卓奎诺尔和dmso分别观察到3.40倍和9.04倍变化。使用10μm安卓奎诺尔,il6表达发生11.88倍变化,而使用dmso观察到47.81倍变化。使用20μm安卓奎诺尔,il18表达发生0.89倍变化,而使用dmso观察到1.36倍变化。
[0140]
图13a-b分别提供了tgfb1(13a)和col4a1(13b)的基因表达水平。使用20μm安卓奎诺尔,tgfb1表达发生0.99倍变化,而使用dmso观察到2.59倍变化。使用20μm安卓奎诺尔,col4a1表达发生0.65倍变化,而使用dmso观察到2.37倍变化。
[0141]
因此,清楚地表明示例性化合物安卓奎诺尔对sars-cov-2诱导的细胞因子风暴和对sars-cov-2诱导的纤维化提供了优异的效果。实施例4:用于评价化合物1在患有因covid 19引起的轻度至中度肺炎住院患者中的安全性和有效性的2期研究临床试验
[0142]
这项研究的主要目标是:
·
评价对因covid-19引起的轻度至中度肺炎的安卓奎诺尔治疗的功效,如通过以
下测量:o 临床改善时间o 疾病的进展。
·
评价患有因covid-19引起的轻度至中度肺炎的患者中安卓奎诺尔治疗的安全性。次要目标是:
·
进一步评价在该患者群体中与安慰剂相比,安卓奎诺尔的功效,通过以下测量:o 住院持续时间o 病毒学清除o 生命状态(死亡)
·
评估该患者群体中安卓奎诺尔的药代动力学(pk)血浆浓度。
·
评估该患者群体中安卓奎诺尔的安全性。研究设计:
[0143]
这是一项2期临床试验,旨在评价安卓奎诺尔在因covid-19引起的轻度至中度肺炎住院患者中的安全性和功效。
[0144]
本研究中包括的住院患者的主要特征是:在筛查之前5天内发热发作且呼吸频率>24/分钟的成人患者。必须存在由covid 19引起的轻度至中度肺炎的症状(通过胸部x光或计算机扫描[ct]扫描确认结果)。计划治疗持续时间为结合当地soc政策的护理标准(soc)疗法施用安卓奎诺尔或安慰剂10天。
[0145]
计划招募一共166名患者并以1:1的安卓奎诺尔与安慰剂比例随机分组。
[0146]
由于安卓奎诺尔在前期临床研究中已显示出抗病毒和抗炎症活性,因此计划将其用于治疗患有covid-19感染的患者。因此,计划对初始标记同生群(initial sentinel cohort)患者进行治疗,以评估安卓奎诺尔的安全性。该标记同生群将包括首次20名患者(10名患者被分配以安卓奎诺尔,10名患者被分配以安慰剂)。一旦首次20名患者开始治疗,招募将暂停。
[0147]
一旦首次20名患者已完成至少10天的疗法,数据监测委员会(data monitoring committee,dmc)将评估该标记同生群中安卓奎诺尔的安全性和耐受性。dmc可能会揭露该评估的数据。一旦标记同生群中的20名患者已治疗至少10天,并且研究已被dmc评估为安全地继续进行,则将恢复招募。
[0148]
研究中所有招募的患者(包括标记同生群)都将被包括在研究治疗的有效性和安全性的主要分析中。dmc将持续审查安全性并评估风险/益处概况。一旦所有患者都实现临床改善,或从疗法开始后已被随访28天,将进行主要功效分析。患者人数:
[0149]
该研究计划招募一共166名患者(安卓奎诺尔组83名患者和安慰剂组83名患者)。此招募水平确保了大约135个改善事件。招募将基于以下假设:安卓奎诺尔组与安慰剂组的随机分配比例为1:1;
·
临床改善定义为中值从7天变为4天。
·
每位患者将被随访长达28天
·
90%的性能
·
双侧α为0.05。诊断、以及入选和排除的主要标准:
[0150]
除非另有说明,否则患者在筛查就诊时必须满足以下所有入选标准:1.愿意并能够提供知情同意书。2.≥18岁且≤80岁的男性或女性患者。3.因发烧(定义为口腔温度≥38.6℃)和呼吸频率》24/分钟而住院。发烧(腋窝≥36.6℃,或口腔≥37.2℃,或肛门或耳朵≥37.8℃
……
吉利德(gilead))注意:住院患者还可以包括入住用于治疗covid-19患者的以医院为条件的中心的患者。4.胸部x光或ct扫描符合肺炎。状态:单侧和双侧肺炎(浸润/间质)5.筛查前5天内开始发烧。6.经鼻咽样本pcr检验(非血清学检验)证实的sars cov 2感染。7.有生育潜能的男性患者和女性患者必须同意使用协议规定的避孕方法。8.有生育能力的女性患者在第1天的筛查和治疗前必须有阴性妊娠检验。9.男性患者必须同意从研究药物的第一剂到最后一剂后90天内不捐献精子。10.研究人员认为,患者愿意并能够遵守研究药物方案和所有其他研究要求。11.住院《48小时和在满足入选标准48小时内随机化。
[0151]
除非另有说明,否则如果患者在筛查就诊时满足以下任何排除标准,他们将被排除在研究之外:1.女性患者怀孕或哺乳。2.任何患者伴随的危及生命的病况,包括但不限于:需要机械通气、急性呼吸窘迫综合征(ards)、休克或心力衰竭。患者需要侵入性机械通气;或其他器官衰竭需要icu监测面罩氧疗(o2吸入)是否可以接受?3.在胸部x光上的肺叶或亚肺叶实变的证据。4.室内空气中的血氧饱和度(spo2)《90%,或动脉氧分压(pao2)/吸入氧百分比(fio2)《200mmhg,严重呼吸困难或需要正压通气(有或没有插管)5.根据研究者的判断,可能会干扰对研究要求的依从性的药物或酒精的滥用。6.招募前7天内使用被认为可能对covid 19具有活性的其他药物的治疗。7.在给药后30天内使用其他研究药物,或计划在参与本研究的同时招募到另一项研究药物的临床试验。8.由研究者确定的筛查时有临床显著的异常ecg。9.患者需要频繁或长期使用全身性皮质类固醇或其他免疫抑制药物(例如,用于器官移植或自身免疫病况)。10.筛查时的异常实验室值:a.估计的肾小球滤过率(gfr)《50ml/min。
b.丙氨酸氨基转移酶(alt)或天冬氨酸氨基转移酶(ast)》5
×
正常上限(uln),或alt/ast》3
×
uln加上总胆红素》2
×
uln。c.血小板计数《100
×
109/l。d.总胆红素》1.5
×
uln,除非患者患有已知吉尔伯特综合征。e.女性血红蛋白《9g/dl或男性《11g/dl。f.总白细胞(wbc)计数《3,500/mm3或绝对嗜中性粒细胞计数(anc)《1,500/mm3。11.在研究治疗开始前14天内,使用任何抗病毒药物或任何已知是cyp2c19、cyp3a4、cyp2c8和cyp2e1的强诱导剂或抑制剂的药物进行治疗。12.在研究者看来,会危及患者安全或潜在影响患者依从性或研究中的安全性/功效观察的任何其他临床显著的医学状况或实验室异常。13.除2019-ncov之外的其他病毒的病毒性肺炎14.患者不能口服药物15.随机化时已插管或需要立即插管的患者16.严重的认知和精神障碍检验品、剂量和施用方式:
[0152]
每天两次(bid)以200mg(2粒胶囊)的剂量口服施用安卓奎诺尔(100mg胶囊),持续10天。
[0153]
参考疗法、剂量、剂型和施用方式:安慰剂(胶囊)bid口服施用10天。
[0154]
研究中患者参与的持续时间:总研究持续时间计划为最多28
±
2天。筛查期计划为最多2天。计划的治疗持续时间为10天。后续安全评价将在第14天和第28天(
±
2天)进行。
[0155]
研究人群:全分析集(full analysis set,fas):所有接受过至少1个剂量研究药物的随机化患者。将根据随机分配给患者的治疗对患者进行分析。
[0156]
符合方案集(per protocol set,pps):在研究期间没有重大研究方案偏差的所有来自fas的患者。在数据库锁定之前,应将有任何重大方案偏差的患者排除在pps之外。
[0157]
安全性集(safety set,ss):所有接受过至少1个剂量研究药物的患者。将根据患者实际接受的研究治疗对患者进行分析。
[0158]
药代动力学集(pharmacokinetic set,pks):所有已接受至少1个剂量的研究药物并且具有至少1个可评价血浆浓度的患者,其没有重大方案偏差或被认为显著影响pk的事件。终点:
[0159]
主要功效终点是:临床改善时间[时间范围:开始服药后28天内]临床改善被定义为从研究治疗开始到发烧正常化≤37.2℃口腔、室内空气中呼吸频率≤24/分钟、室内空气中血氧饱和度(spo2)》94%的时间(天数)。(个人或全部)消除缺氧(定义为室内空气中spo2≥93%或pa02/fi02≥300mmhg)。
·
疾病缓解速率[时间范围:开始用药后的第14天和第28天]
·
疾病的进展
疾病的进展被定义为需要正压通气(插管或不插管)、或需要icu护理。对于仍然住院并作为soc的一部分进行动脉血气(abg)检验的患者亚组,pao2/fio2《200mmhg也将用作疾病进展的量度。发生呼吸衰竭时侵入性机械通气速率[时间范围:10天]
[0160]
次要功效终点是:
·
住院时间(天数)。
·
从鼻咽或呼吸道样本中病毒学清除o病毒学清除时间,测量未从治疗开始到第一次阴性sars-cov-2 pcr检验的研究天数o病毒载量的变化速率将根据定量分析的有效性进行评价。(实时rt-pcr检验)
·
生命状态(死亡)将收集直到第14天和第28天
·
肺部影像改善时间[时间范围:服药后10天内]安全性终点包括以下变量:
·
不良事件(ae)。
·
胸部影像(x光或ct扫描)结果。
·
生命体征:血压、脉搏速率。
·
体检:一般外观、heent、淋巴、心血管、呼吸、胃肠、骨骼肌、神经、皮肤病学。
·
12导联心电图(ecg)。
·
标准安全性实验室检验(血液学、化学和尿分析)。
[0161]
药代动力学评价
[0162]
从血浆样品中评估的pk参数是:
·
谷值(初始剂量)血浆浓度(ctrough)
·
最大血浆浓度(cmax)。统计方法:
[0163]
一般原则:
[0164]
连续变量将通过标准描述性统计概括:患者数(n)、平均值、标准偏差(sd)、中值、最小值(min)和最大值(max)。患者或事件的频率和百分比将在分类变量中概括。在0.025的一侧α的结果将被视为统计学显著的,在0.2的一侧α的结果将被视为指示了有希望的趋势。功效分析:
[0165]
主要功效分析
[0166]
临床恢复时间的风险比(hr)及其95%置信区间(ci)将通过cox比例风险模型估计,患者在死亡时、在向他们提供任何非研究抗-病毒治疗时,或者在第28天如果他们尚未康复,则对患者进行数据截尾。将通过kaplan-meier(km)方法估计临床改善的中值时间,并将提供km曲线。用于组间比较的p-值将根据对数秩检验获得。
[0167]
对于疾病的进展,使用逻辑回归计算在两组中需要正压通气和需要icu护理的患者的比例和组间差异以及95%ci。p-值将基于卡方检验。对于具有作为soc的一部分收集的abg数据的患者亚组,还将评价pao2/fio2。
[0168]
次要功效分析
·
住院时间、病毒学清除(病毒学清除时间、病毒载量的变化率)和生命状态将使用与主要功效终点类似的统计方法进行分析。安全性分析:
[0169]
不良事件将根据监管活动医学词典(medical dictionary for regulatory activities,meddra)进行编码。
[0170]
按照系统器官分类(soc)、优选术语(pt)和治疗组总结了患有治疗紧急ae(teae)、严重ae(sae)、与研究治疗相关的teae、与导致治疗中断的研究治疗teae相关的sae、导致研究中断的teae和导致死亡的teae的患者的数量和百分比。此外,teae的严重程度以及与研究治疗的关系将按soc、pt和治疗组概括。
[0171]
以下标准化meddra查询(smq)标识特殊关注的ae(aesi),并将被报告:
·
呼吸衰竭
·
机会性感染
[0172]
将描述性地概括特定实验室检验结果、生命体征、spo2、体检和egg结果的检验值和相对于基线的变化。在适用的情况下,将呈现按治疗组的转移附表。药代动力学分析:
[0173]
将提供对安卓奎诺尔血浆浓度和/或pk参数的描述性统计。表1:评估时间表
缩略语:ae=不良事件;c
max
=最大血浆浓度;c
trough
=谷值(给药前(pre dose))血浆浓度;ct=计算机化扫描;dmc=数据监测委员会;ecg=心电图;eos=研究结束;eot=治疗结束;fio2=吸入氧的百分比;heent=头、眼、耳、鼻和喉;icu=重症监护室;pao2=动脉氧分压;pcr=聚合酶链反应;pd=药效动力学;pk=药代动力学;spo2=血氧饱和度/脉搏血氧测量。脚注:a患者在达到临床康复(定义为从研究治疗开始到发烧、呼吸频率和氧合正常化的时间[天数])后可以在治疗开始后在第2至10天期间的任何时间出院。然后将要求患者在家接受治疗(按所开处方),并在第14天和第28天通过电话进行随访以评估症状。出院患者需要到医院/站点完成第10天的评估/eot访视。b招募20名患者的初始同生群以评估安全性和耐受性。一旦dmc确认没有安全性问题,研究将恢复招募剩余的患者。c筛查前5天内体温(口腔、额头、腋窝、鼓室)≥38.6℃且呼吸频率》24/分钟。筛查时将进行完整的体检(一般外观、heent、淋巴、心血管、呼吸、胃肠、骨骼肌、神经和皮肤系统)。住院期间将进行靶向covid-19症状的体检。住院期间每天要评估生命体征(呼吸频率、血压和脉搏速率)。身高和体重将仅在筛查时测量。d胸部x光或ct扫描应显示与covid-19肺炎一致的结果,并将在筛查和出院时进行。e在当地(站点)实验室对生育潜能的女性患者进行尿妊娠检验。f功效参数评估:[1]筛查和后续访视时,在当地实验室进行covid-19的pcr检验
(直到阴性结果)。该检验可在中心实验室进行,供出院患者进行其后续检测;[2]如果患者需要延长住院或疾病进展(定义为需要正压通气(插管或不插管),或需要icu护理),则可以评估为临床恶化状态。对于仍然住院且作为soc的一部分进行动脉血气(abg)检验的患者亚组,pao2/fio2还将用作疾病进展的量度;[3]第1天每日spo2监测:5分钟内3次连续读数的平均值;[4]在筛查和住院期间进行pao2/fio2的动脉血气评价(直至出院)。g安全性参数评估:[1]将从治疗开始(住院期间和出院后在家中)直到eos对ae进行评估;[5]标准安全性实验室检验将包括血液学、化学和尿分析的所有参数,并将在第1、5和10天在给药前进行;[6]当患者处于仰卧位时,在筛选时进行12-导联egg;[7]从筛查直到eos记录既往和伴随药物。h药代动力学参数包括ctrough和cmax。这些参数的血液样本将在第5天和第10天(如果患者仍在住院)、给药前和给药后2小时进行评估。实施例5:口服制剂。
[0174]
为了制备用于口服递送的药物组合物,将等重量的示例性化合物1与等重量的玉米油(例如,25mg、50mg、100mg、200mg)混合。将该混合物并入胶囊中的口服剂量单位中,该胶囊适合于口服施用。
[0175]
在一些情况下,将100mg的本文描述的化合物与750mg的淀粉混合。将该混合物并入诸如硬明胶胶囊中的口服剂量单位中,该硬明胶胶囊适合于口服施用。实施例6:舌下(硬锭剂)制剂
[0176]
为了制备用于口腔递送的药物组合物,例如硬锭剂,将一份本文所述的化合物与4-5份混合有适量的淡玉米糖浆、蒸馏水和薄荷提取物的糖粉混合。将混合物轻轻混合并倒入模具中以形成适合口腔施用的锭剂。实施例7:吸入组合物
[0177]
为了制备用于吸入递送的药物组合物,将20mg本文所述的化合物与50mg无水柠檬酸和100ml 0.9%氯化钠溶液混合。将混合物并入诸如雾化器的吸入递送单元中,该吸入递送单元适合用于吸入施用。
[0178]
虽然本文已经示出和描述了本发明的优选实施方案,但是对于本领域技术人员来说,显然这些实施方案仅作为示例而提供。在不脱离本发明的情况下,本领域技术人员将会想到许多变化、改变和替换。应当理解,在实践本发明时可以采用本文描述的本发明的实施方案的各种替代方案。所附权利要求旨在限定本发明的范围,并且由此涵盖在这些权利要求范围内的方法和结构及其等同方案。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。
