1.本技术涉及新的耐辐射奇球菌菌株、源自于该菌株的胞外多糖和包含该胞外多糖的组合物,并且更具体地,本技术涉及产生显著增加量的胞外多糖的新的耐辐射奇球菌菌株,该胞外多糖提供优异的抗氧化性能并为细胞和生物体提供针对紫外线/x射线/伽马射线的保护作用;并且涉及胞外多糖相关的技术。
背景技术:
2.耐辐射奇球菌(deinococcus radiodurans)是一种革兰氏阳性细菌,几乎是不仅可以在干涸条件下,而且可以在紫外线和电离辐射条件下存活的唯一微生物;并且,据报道,其能够在这些条件生长是因为该菌株自身的dna修复系统以及细胞膜中的特定疏水性物质和类胡萝卜素均优于其他生物体的细胞。
3.韩国专利注册号kr10-1776586b1等公开了源自于在如上文所描述的可在极端环境下存活的耐辐射奇球菌的胞外多糖表现出诸如皮肤衰老抑制、皮肤恢复等作用。
4.另一方面,反复和长期暴露于环境中的刺激物会使皮肤蛋白变性,劣化脂质层(lipid lamella layer),去除保护性细胞间脂质,导致失去天然保湿因子并降低细胞间粘附。例如,暴露于紫外线会导致表皮和真皮受损,而持续暴露于紫外线会引起皮肤生物力学特性变化,从而导致皱纹。源自于耐辐射奇球菌的胞外多糖可应用于多种类型的组合物,例如具有抗衰老和皮肤恢复作用的化妆品组合物。
5.然而,为了以这种方式来商业应用源自于耐辐射奇球菌的胞外多糖,应当获得足够产量的胞外多糖生产,并且进一步要求胞外多糖能够发挥改进的功效。
6.因此,本发明人研究了新的耐辐射奇球菌菌株,并且尤其证实了耐辐射奇球菌,其以显著提高的产率产生具有优异的抗氧化功效的胞外多糖,并且所产生的胞外多糖提供优异的抗氧化性能以及针对紫外线/x射线/伽马射线的细胞和生物保护作用,从而完成本技术。
技术实现要素:
7.技术问题
8.本技术的一个方面是提供新的耐辐射奇球菌菌株,该菌株以显著提高的产量产生具有优异的抗氧化功效的胞外多糖。
9.本技术的另一方面是提供具有优异的抗氧化和辐射防护功效的胞外多糖。
10.本技术的另一方面是提供包含具有优异的抗氧化和辐射防护功效的胞外多糖的组合物。
11.本技术的另一方面是提供从耐辐射奇球菌提取具有优异的抗氧化和辐射防护功效的胞外多糖的方法。
12.问题的解决方案
13.根据本技术的一个方面,提供了特征在于以保藏号kctc 13955bp保藏的耐辐射奇球菌brd125菌株。
14.根据本技术的一个方面,提供了源自于以保藏号kctc 13955bp保藏的耐辐射奇球菌brd125菌株的胞外多糖。
15.根据本技术的另一方面,提供了化妆品组合物、用于抑制皮肤衰老的药物组合物、用于皮肤恢复的药物组合物以及抗氧化食品,它们包括源自于耐辐射奇球菌brd125菌株的胞外多糖。
16.根据本技术的另一方面,提取源自于耐辐射奇球菌的胞外多糖的方法包括:通过培养耐辐射奇球菌brd125菌株获得培养基;使用乙醇浓度为50%或更高的乙醇水性溶液来沉淀培养基中的胞外多糖;从该沉淀的沉淀物中以沉淀物的形式去除蛋白质、脂质和核酸的杂质去除操作;以及纯化该杂质去除操作中所得到的上清液。
17.发明的有益效果
18.与相关技术中的菌株相比,在根据本技术的示例性实施方式提供的新的耐辐射奇球菌菌株的情况下,胞外多糖的产量可以是显著提高的,并且进一步地,源自于根据示例性实施方式的新的耐辐射奇球菌菌株的胞外多糖具有优异的抗氧化作用和针对紫外线/x射线/伽马射线的优异细胞和生物保护作用,从而有望在工业上广泛应用到多个领域。
附图说明
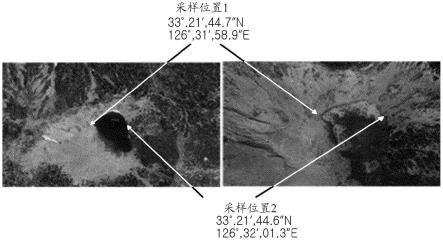
19.图1示出了用于分离耐辐射微生物的土壤收集点的卫星图像。
20.图2示意性地示出了根据本技术的示例性实施方式的耐辐射微生物分离过程。
21.图3示出了每种耐辐射奇球菌菌株产生的deinopol的量。
22.图4示意性地示出了根据本技术的示例性实施方式的deinopol产生过程。
23.图5示出了deinopol brd125和deinopol r1的抗氧化作用的比较结果。
24.图6示出了deinopol brd125和deinopol r1针对紫外线的防护作用的比较结果。
25.图7a和图7b示出了deinopol brd125在cho细胞中辐射(x射线)诱导的活性氧物质清除能力(图7a)和细胞抗辐射活力(图7b)的结果。
26.图8a至图8c示出了新的菌株brd125的deinopol针对辐射引起的骨髓细胞和脾脏中的免疫细胞的细胞死亡的抑制能力,并且更详细地示出了辐射(x射线)照射在骨髓细胞和脾脏中的免疫细胞中引起的细胞周期比率的变化(图8a、图8b)以及deinopol使bcl-2(一种细胞死亡抑制因子)表达增加的结果(图8c)。
27.图9a至图9c示出了新的菌株brd125的deinopol对经辐照小鼠(伽马射线)的骨髓细胞(图9a)和脾免疫细胞(图9b)的死亡抑制能力,以及deinopol对经照射小鼠的骨髓细胞的dna片段化的抑制作用(图9c)。
28.图10示出了新的菌株brd125的deinopol在经照射小鼠(伽马射线)中提高内源性脾集落形成的结果。
29.图11示出了新的菌株brd125的deinopol在经照射小鼠(伽马射线)中相对提高脾脏中造血细胞因子的表达。
30.图12a至图12c示出了验证新的菌株brd125的deinopol在经照射小鼠(伽马射线)中使外周血中的白细胞(图12a)、外周血中的淋巴细胞(图12b)和脾脏中的免疫细胞(图
12c)再生增强功效的结果。
具体实施方式
31.下文中,将参照所附附图对本技术的示例性实施方式进行描述。然而,本技术的实施方式可以修改为各种其他形式,并且本技术的范围不限于以下描述的实施方式。
32.本发明人已经鉴定了新的耐辐射奇球菌菌株,与相关技术中的耐辐射奇球菌相比,其具有显著改进的胞外多糖生产能力,并且证实了由这种新的菌株产生的胞外多糖具有优异的抗氧化保护作用和紫外线防护作用,即使基于与相同量的源自于相关技术的耐辐射奇球菌的胞外多糖进行比较时也是如此。
33.因此,根据本技术的示例性实施方式,提供了新的耐辐射奇球菌菌株,其可以改进的生产力来产生胞外多糖,并且进一步产生具有优异抗氧化保护作用和紫外线防护作用的胞外多糖。更详细地,根据本技术的示例性实施方式,提供了特征在于以保藏号kctc 13955bp保藏的耐辐射奇球菌brd125菌株。
34.在本技术中,“源自于耐辐射奇球菌的胞外多糖(deinococcus radiodurans-derived exopolysaccharide(eps))”与“deinopol”可互换指代。
35.进一步地,根据本技术的示例性实施方式,提供了源自于本技术的以保藏号kctc 13955bp保藏的耐辐射奇球菌brd125菌株的胞外多糖。
36.根据示例性实施方式的源自于耐辐射奇球菌brd125菌株的胞外多糖包含阿拉伯糖、半乳糖、葡萄糖和木糖。
37.更详细地,胞外多糖包含:基于总胞外多糖的重量,9重量%的阿拉伯糖、10重量%的半乳糖、15重量%的葡萄糖、18重量%的木糖和48总量%的其他未知糖。在这种情况下,未知其他糖包括32重量%的其他糖1和16重量%的其他糖2。上述其他糖1和2表示检测到的峰不是岩藻糖、鼠李糖、阿拉伯糖、半乳糖、葡萄糖、木糖和甘露糖的峰的未知糖,其中岩藻糖、鼠李糖、阿拉伯糖、半乳糖、葡萄糖、木糖和甘露糖这些糖是通过lc/ms进行的糖检测实验中的标准糖。更详细地,在本技术中,基于通过lc/ms进行的糖检测实验中的保留时间,其他糖1位于岩藻糖和鼠李糖之间,而其他糖2在相同基础下位于阿拉伯糖和半乳糖之间。通过改变现有糖中糖自身的结构或残基,这些其他糖可以被分析为新型的未知糖。
38.本技术胞外多糖的这种糖组合是以前未知的新的糖组合,并且更详细地,其没有从耐辐射奇球菌r1(相关技术中已知的菌株)分离的胞外多糖中存在的岩藻糖和鼠李糖,而是包含如上文所述的两种其他类型的糖。
39.此外,根据本技术的示例性实施方式,提供了化妆品组合物,其包含源自于上述耐辐射奇球菌brd125菌株的胞外多糖。
40.化妆品组合物可包括:基于总化妆品组合物的体积,浓度为0.8μg/ml至50μg/ml的根据本技术的示例性实施方式的胞外多糖作为有效成分,并且更详细地,包含浓度为3μg/ml至10μg/ml的根据本技术的示例性实施方式的胞外多糖。
41.如果基于总化妆品组合物的体积,所包含的胞外多糖的量低于0.8μg/ml,则衰老抑制和皮肤恢复作用不充分,并且甚至在100μg/ml或更高的情况下,由于不会发生细胞毒性的变化,其使用仍是可能的,但是从工艺经济性的角度来看,可包含浓度为50μg/ml或更低的胞外多糖,这是因为含量增加带来的效果提升并不显著。
42.根据本技术的示例性实施方式的化妆品组合物可用于抗氧化、衰老抑制、辐射防护和/或皮肤恢复。在这种情况下,衰老抑制既包括防止衰老的作用,还包括减缓或延缓衰老进程的作用,皮肤恢复包括保护皮肤免受紫外光等外界刺激以及修复由此受损的皮肤的一系列过程。
43.例如,当根据本技术的示例性实施方式的组合物是化妆品组合物时,可以将化妆品组合物制备成各种形式,例如乳液、洗剂、霜剂(水包油、油包水、多相)、溶液、悬浮液(无水和水性)、无水产品(油和二醇体系)、凝胶、面膜(mask)、剥撕式化妆膏(pack)或散剂。
44.除了活性成分之外,根据本技术的实施方式的组合物可以根据需要包含额外的成分,该额外的成分包括化妆品制剂中可接受的载体和/或化妆品中通常配制的其他添加剂。
45.在这种情况下,“化妆品配方中可接受的载体”是指已知并使用的并且可能包含在化妆品配方中的化合物或组合物或者未来将开发的化合物或组合物,其毒性不超过与皮肤接触后人体可适应于毒性。载体可以以组合物总重量的约1重量%至约99.99重量%,详细地,约50重量%至约99重量%的量包含在根据示例性实施方式的组合物中。
46.然而,由于该比例依据上述的化妆品配方而变化,并且还根据详细的施用部位或优选的施用量而变化,因此该比例不应被理解为在任何方面限制本技术的范围。
47.另一方面,作为额外的成分,可提供的示例为醇、油、表面活性剂、脂肪酸、硅油、润湿剂、保湿剂、粘度调节剂、乳剂、稳定剂、防晒剂、显色剂、香料、抗氧化剂、植物提取物、ph调节剂或颜料等。可用作醇、油、表面活性剂、脂肪酸、硅油、润湿剂、保湿剂、粘度调节剂、乳剂、稳定剂、防晒剂、显色剂或香料等的化合物或组合物在本领域中是已知的,并且因此,可以选择并使用适当的相应材料或组合物。
48.此外,根据本技术的示例性实施方式,提供了用于预防和抑制皮肤衰老的药物组合物以及用于皮肤恢复和皮肤保护的药物组合物,其包含源自于耐辐射奇球菌brd125菌株的胞外多糖。
49.更详细地,所提供的用于预防和抑制皮肤衰老的药物组合物包含:基于药物组合物的体积,0.8μg/ml至50μg/ml的源自于耐辐射奇球菌brd125菌株的胞外多糖作为活性成分;以及所提供的用于皮肤恢复、辐射防护和皮肤保护的药物组合物包含:基于药物组合物的体积,0.8μg/ml至50μg/ml的源自于耐辐射奇球菌brd125菌株的胞外多糖作为活性成分。
50.例如,根据示例性实施方式的药物组合物可用作用于治疗衰老相关疾病、辐射防护和皮肤损伤疾病,例如皱纹、皮肤光老化、色素沉着、雀斑、黄褐斑和辐射(诸如紫外线)引起的皮肤损伤的药物组合物。
51.基于其用途的常规方法,根据示例性实施方式的药物组合物可以以各种形式配制和使用,例如,口服制剂,诸如散剂、颗粒剂、片剂、胶囊剂、混悬剂、乳液、糖浆剂和气雾剂,或者无菌注射溶液的形式;并且可以口服或通过各种途径给药,包括静脉内、腹膜内、皮下、直肠和局部给药等。
52.可包含在上述药物组合物中的合适载体、赋形剂和稀释剂的示例可包括乳糖、右旋糖、蔗糖、山梨糖醇、甘露糖醇、木糖醇、赤藓糖醇、麦芽糖醇、淀粉、阿拉伯树胶、藻酸盐、明胶、磷酸钙、硅酸钙、纤维素、甲基纤维素、无定形纤维素、聚乙烯吡咯烷酮、水、羟基苯甲酸甲酯、羟基苯甲酸丙酯、滑石粉、硬脂酸镁和矿物油等。
53.此外,治疗性药物组合物可进一步包含填充剂、抗凝集剂、润滑剂、润湿剂、调味
剂、乳化剂和防腐剂等。
54.用于口服给药的固体制剂包括片剂、丸剂、散剂、颗粒剂、胶囊剂等,这些固体制剂可以通过在药物组合物中混合至少一种赋形剂,诸如淀粉、碳酸钙、蔗糖、乳糖或明胶等来配制。此外,除了简单的赋形剂外,还可以使用润滑剂,诸如硬脂酸镁和滑石粉。
55.用于口服使用的液体制剂包括混悬剂、液体溶液、乳液和糖浆剂等,并且除为常规使用的简单稀释剂的水和液体石蜡外,还可包括各种赋形剂,诸如润湿剂、甜味剂、香料和防腐剂。
56.用于肠胃外给药的制剂包括无菌水性溶液、非水性溶剂、混悬剂、乳液、冻干制剂和栓剂。作为非水性溶剂和悬浮剂,可以使用丙二醇、聚乙二醇、植物油(诸如橄榄油)和注射用酯(诸如油酸乙酯)。注射剂的基质可以包括相关技术的添加剂,例如增溶剂、等渗剂、悬浮剂、乳化剂、稳定剂和防腐剂。
57.根据示例性实施方式的药物组合物以药学有效量给药或施用于需要治疗衰老相关疾病和皮肤损伤疾病的受试者。
58.根据示例性实施方式的组合物可以作为单独的治疗剂给用或者与其他治疗剂组合给药,可以与相关领域的治疗剂依次给药或同时给药,并且可以单次或多次给药。在考虑到所有上述因素的情况下,重要的是,给药能够以最小量获得最大效果而没有副作用的量,这可由本领域技术人员容易地确定。然而,由于根据示例性实施方式的组合物的增加或减少取决于给药途径、疾病的严重程度、性别、体重、年龄等而增加或减少,因此剂量并不以任何方式来限制本技术的范围。
59.此外,根据本技术的示例性实施方式,提供了抗氧化食品,其含有源自于耐辐射奇球菌brd125菌株的胞外多糖作为活性成分。
60.根据示例性实施方式的抗氧化食品是包括所有健康功能食品和健康补充剂等的食品组合物,并且食品组合物的形式没有特别限制,并且旨在包括被制成为诸如液体、固体或其他流体的任意形式的任何食品。
61.例如,当根据示例性实施方式的食品组合物是诸如功能饮料的食品组合物时,除了活性成分之外,该食品组合物可含有甜味剂、调味剂、生理学上的活性成分和矿物质等。
62.甜味剂可以以使食品具有合适的甜味的量来使用,并且可以是天然的或合成的。详细地说,可以使用天然甜味剂,并且天然甜味剂的示例可包括糖甜味剂,诸如玉米糖浆固体、蜂蜜、蔗糖、果糖、乳糖和麦芽糖。
63.调味剂可用于增强味道或香气,天然香料和合成香料均可使用,并且详细地说,可使用天然香料。在使用天然成分的情况下,除了调味之外,还可以获得营养增强。天然调味剂可得自于苹果、柠檬、柑橘、葡萄、草莓或桃等,或者得自于绿茶叶、玉竹(solomon’s seal)、竹叶、肉桂、菊花叶和茉莉等。此外,可以使用得自于人参(红参)、竹笋、芦荟和银杏的天然调味剂。天然调味剂可以是液体浓缩物或固体提取物。在一些情况下,可以使用合成调味剂,并且合成调味剂可以包括酯、醇、醛和萜烯等。
64.作为生理学上的活性物质,可使用儿茶素类(诸如儿茶素、表儿茶素、没食子儿茶素和表没食子儿茶素)以及维生素类(诸如视黄醇、抗坏血酸、生育酚、钙化醇、硫胺素、核黄素等)。作为矿物质,可使用钙、镁、铬、钴、铜、氟化物、锗、碘、铁、锂、镁、锰、钼、磷、钾、硒、硅、钠、硫、钒和锌等。
65.此外,除了甜味剂之外,如果需要,根据示例性实施方式的食品组合物还可含有防腐剂、乳化剂、酸化剂和增稠剂等。这些防腐剂和乳化剂等可以以极少量地添加和使用,只要可以获得其添加的用途即可。当用数值表示时,极少量表示基于食品组合物的总重量,0.0005重量%至约0.5重量%的范围。
66.可使用的防腐剂包括山梨酸钙钠、山梨酸钠、山梨酸钾、苯甲酸钙、苯甲酸钠、苯甲酸钾和乙二胺四乙酸(edta)等。可使用的乳化剂的示例包括阿拉伯树胶、羧甲基纤维素、黄原胶和果胶。可使用的酸化剂的示例可包括柠檬酸、苹果酸、富马酸、己二酸、磷酸、葡糖酸、酒石酸、抗坏血酸和乙酸等。除了用于增强味道之外,可添加这些酸化剂来使食品组合物具有适当的酸度以抑制微生物的生长。作为可使用的增稠剂,可以使用悬浮剂、沉降剂、凝胶形成剂和溶胀剂等。
67.另一方面,根据本技术的另一实施方式,提供了提取源自于耐辐射奇球菌brd125的胞外多糖的方法。该提取方法包括:通过培养耐辐射奇球菌brd125菌株获得培养基;使用50%或更高的乙醇来沉淀培养基中的胞外多糖;从沉淀的沉淀物中去除作为沉淀物的蛋白质、脂质和核酸的杂质去除操作;以及,对在杂质去除操作中得到的上清液进行纯化。
68.在通过培养耐辐射奇球菌获得培养基的操作中,培养温度可为28℃至38℃,具体为30℃至35℃,更具体为约30℃的温度。
69.获得培养基的操作可例如通过以下来进行:将耐辐射奇球菌接种到2l胰蛋白胨-葡萄糖-酵母提取物(tgy)中,然后在约30℃的温度下振荡孵育48小时,然后用伽马射线以17kgy照射悬浮液2小时以对培养基中的耐辐射奇球菌的细胞壁的eps进行分离和灭菌,然后通过离心去除被杀死的耐辐射奇球菌。
70.此外,在获得培养基的操作之后,提取方法中可进一步包括使用超滤系统将获得的培养基浓缩50倍至200倍,具体浓缩80倍至130倍的操作。在如上所述进行浓缩的情况下,可以更有效地提取相对大量的胞外多糖。
71.随后,可进行使用50%或更高乙醇浓度的乙醇水性溶液在培养基中沉淀胞外多糖的操作。例如,将培养基与浓度为50%或更高的乙醇混合,具体地,与浓度为50%或更高且小于80%的乙醇水性溶液混合,然后在0℃至4℃下经过约1小时至24小时,具体经过10小时至14小时后,核酸和高分子量物质被沉淀,并可被通过离心去除。
72.此外,在如上获得的上清液中,可以将水性乙醇溶液中的乙醇浓度提高到80%或更高,然后在0℃至4℃下沉淀约1小时至24小时,具体沉淀10小时至14小时,从而使得上清液中的胞外多糖可以进一步沉淀。如果培养基的乙醇浓度低于80%,则存在低分子量eps不沉淀的问题。
73.通过上述方法沉淀的胞外多糖可以与水混合以制备水性胞外多糖溶液。该水性溶液具有胞外多糖溶解在水中的形式。不溶性物质不是水溶性胞外多糖,因此可以通过固-液分离(例如使用过滤器)来去除。在这种情况下,可使用的过滤器没有特别限制,只要它们可以去除不溶性物质即可,例如,可以使用0.22μm的过滤器来去除不溶性物质。
74.沉淀物不仅包括胞外多糖,还包括其他蛋白质或脂质,为了去除这些沉淀物而进行的杂质去除操作可通过以下来进行:将含有重量比为4:1的氯仿和丁醇的水性混合醇溶液加入到沉淀物中以获得作为上清液的胞外多糖。在这种情况下,水性混合醇溶液可以是混合醇和水以3:7至7:3的重量比混合,具体地,以5:5的重量比混合的混合物。
75.另一方面,纯化上清液的操作可通过透析来进行。例如,可以使用10kda的透析管在三级无菌蒸馏水中来透析分离的上清液。
76.可替代地,纯化操作可以通过凝胶过滤来进行。应用于纯化操作的凝胶过滤方法没有特别限制。例如,在4℃的冰箱中用二级蒸馏水稳定sephacryl s-300hr柱后,向柱内注入5ml沉淀的胞外多糖,并且注入后,以5ml/min的速率连续注入二级蒸馏水以获得通过柱分离的洗脱液。此时,洗脱液可以通过使用例如蒽酮反应糖分析法等测量糖浓度来确认为其为产生胞外多糖的洗脱液。
77.根据本技术的示例性实施方式的提取胞外多糖的方法可以简化纯化过程并提高纯化效率。
78.此外,还可进一步包括对经纯化的胞外多糖进行干燥的操作。在这种情况下,干燥方法没有特别限制,例如可通过冷冻干燥来进行。
79.如上所述,根据本技术的示例性实施方式,提供了从耐辐射奇球菌brd125菌株中提取胞外多糖的方法,并且通过上述过程,以高产率获得了源自于新的耐辐射奇球菌brd125菌株的具有新的多糖组成的胞外多糖(eps),并且此外,可以实现具有显著改善的皮肤衰老预防和皮肤恢复作用的组合物。
80.在下文中,将通过具体实施例来更详细地描述本技术。以下实施例仅为帮助理解本技术内容,本技术的范围并不限于此。
81.本发明的方式
82.实施例
83.1.来自汉拿山白鹿潭的耐辐射微生物的分离
84.从汉拿山白鹿潭(参见图1,表1)的两个地方采集约30g土壤,使用韩国原子能研究所高级辐射研究所的高水平辐射照射设备照射5kgy的伽马射线。将30ml的r2a液体介质加入到经伽马射线照射的土壤中,然后在30℃下孵育(富集)2小时,随后分别将约0.5ml涂抹在r2a固体介质中,然后在孵育箱中于30℃下孵育3天。选择出现在r2a固体介质上的菌落并在r2a液体培养基中孵育两天。部分经培养的液体介质产生贮藏菌株(storage strain),剩余部分再次铺在r2a固体介质上,在孵育箱于30℃下孵育两天,在r2a固体介质上确认菌落(参见图2)。
85.通过16s rrna分析,分离并鉴定来自土壤的58种(species)耐辐射微生物、来自粘土的49种耐辐射微生物和来自淡水的3种耐辐射微生物。最终分离出110种耐辐射微生物。
86.[表1]
[0087]
土壤采集坐标
[0088] 坐标采样位置133
°
,21',44.7"n 126
°
,31'58.9"e采样位置233
°
,21',44.6"n 126
°
,32'01.3"e
[0089]
2.通过16s rrna分析鉴定耐辐射奇球菌
[0090]
为了鉴定通过上述1的过程所分离的110种耐辐射微生物(110radiation-r esistant microoganisms),分离了基因组dna,并分析16s rrna基因(参见表2)。使用27f(5'-agagtttgatcmtggctcag-3)和1492r引物(5'-tacggyt accttgttacgactt-3')进行16s rrna基因序列分析,以分析扩增约1350b p或更高的pcr产物的碱基序列。为了确认碱基序
列之间的相似性,使用nc bi的blast数据库鉴定分离的抗辐射微生物。结果,在110种菌株(110str ains)中,鉴定出30种(30species)与耐辐射奇球菌(d.radiodurans)具有99%同源性。
[0091]
结果,在110种菌株中,鉴定出30种耐辐射奇球菌,其中3种被确认很有可能是新物种(species)。
[0092]
[表2]
[0093]
16s mrna分析结果及经鉴定的微生物名称
[0094]
[0095][0096]
3.耐辐射奇球菌的胞外多糖生产的确认(deinopol生产的比较)
[0097]
将采用上述1中的方法分离并经上述2中的方法鉴定的耐辐射奇球菌菌株和耐辐射奇球菌r1菌株(来自us atcc)分别接种于ty液体介质中,并在30℃和200rpm的条件下培养,并进行离心以分离通过培养耐辐射奇球菌菌株获得的培养基。进行蒽酮反应以确认在所分离的培养基中的源自于耐辐射奇球菌的胞外多糖(eps)(可与“deinopol”互换指代)。图3的每个条形图像表示源自于名称包括相应条形图下端数字的菌株的deinopol的od630值,
△
eps表示不能产生deinopol的突变菌株。
[0098]
据此确认了在耐辐射奇球菌r1、br9、br11、br15、br22和brd125菌株中产生大量的eps,并且在耐辐射奇球菌brd125菌株中产生相对最大量的eps。结果示于图3的图示中,并且在图3的图示中,在与菌株名相关的数字前省略了“br”,对于125,则是省略了“brd”。
[0099]
如此获得的耐辐射奇球菌brd125菌株于2019年9月17日以保藏号kctc13955bp保藏在韩国生物科学与生物技术研究所生物资源中心(korea research institute of bioscience and biotechnology,biological resource center)。
[0100]
4.来自耐辐射奇球菌brd125的deinopol的分离和纯化
[0101]
为了分离出上述3中产生胞外多糖最多的耐辐射奇球菌brd125的deinopol,在tgy液体介质中于30℃和200rpm下孵育2天,进行离心以获得培养基。将所获得的培养基用旋转
蒸发仪在65℃下浓缩10倍至20倍。经浓缩的培养基为50%乙醇水性溶液,使deinopol在4℃下沉淀12小时,以通过离心去除核酸和部分蛋白沉淀物来获得上清液。
[0102]
将上清液中的乙醇浓度由50%升高至80%,并在4℃下沉淀12小时,所沉淀的deinopol沉淀物经离心分离,然后使其溶解在三级蒸馏水中。
[0103]
沉淀物不仅包含deinopol,还含有其他蛋白质或脂质,并且为了去除其他蛋白质或脂质,将4:1=氯仿:丁醇的混合醇溶液与溶解有deinopol的三级灭菌蒸馏水以1:1混合,然后通过离心分离含有deinopol的上清液。
[0104]
使用10kda透析管在三级灭菌蒸馏水中对经分离的上清液进行透析,然后冷冻干燥以获得最终的deinopol。
[0105]
上述过程示意性地示出在图4中,并且所得到的deinopol粉末纯化良好,具有94.7%的纯度。(参见表3)
[0106]
[表3]
[0107]
经纯化的deinopol的纯度
[0108] epsdna蛋白eps纯度耐辐射奇球菌brd12594.75mg/l0.125mg/l1.967mg/l94.7%
[0109]
5.源自耐辐射奇球菌brd125的小多糖的糖组成的确认
[0110]
采用bio-lc对上述4的过程中提取的源自于耐辐射奇球菌brd125的eps的糖组成进行分析,结果如下表4所示。下表4所示的其他糖是检测到的除了为lc/ms进行糖检测实验期间的标准糖的岩藻糖、鼠李糖、阿拉伯糖、半乳糖、葡萄糖、木糖和甘露糖的峰以外的未知糖。更详细地说,在本技术中,基于lc/ms糖检测实验中的保留时间,其他糖(1)位于岩藻糖和鼠李糖之间,而其他糖(2)在相同基础下位于阿拉伯糖和半乳糖之间。通过改变现有糖中糖自身的结构或残基,这些其他糖可分析为新型的未知糖。
[0111]
如下表4所示,源自于耐辐射奇球菌brd125的eps的糖组成如下:
[0112]
[表4]
[0113]
糖的类型含量(wt%)阿拉伯糖9半乳糖10葡萄糖15木糖18未知的其他糖132未知的其他糖216总和100
[0114]
分析的结果如表4所示,确认了源自于耐辐射奇球菌brd125的eps的糖组成是以前未知的糖组成。
[0115]
6.耐辐射奇球菌brd125的deinopol的抗氧化功效的比较
[0116]
(1)通过dpph实验比较抗氧化活性
[0117]
进行dpph实验以比较植物乳球菌(lactococcus plantarum,l.p)的胞外多糖(l.p eps)与经纯化的deinopol brd125(brd125 eps)和deinopol r1(r1 eps)的抗氧化能力,其中植物乳球菌是已知具有抗氧化能力的对照组,结果示出在图5中。
[0118]
此外,接种heka细胞并使之稳定18小时,用deinopol处理并培养12小时以确认每种deinopol针对紫外线的保护作用。在紫外线照射前30分钟,为heka细胞更换不含fbs的新鲜培养基,并用紫外线照射。照射4小时后,更换成含fbs的新鲜培养基,并且3天后利用cck-8计算细胞活力,结果示出在图6中。
[0119]
结果,如可在图5和图6中分别看到的那样,根据相同量的胞外多糖的功效的比较结果,确认了deinopol brd125(brd125 eps)具有显著高的抗氧化作用,并且具有针对紫外线的优异保护作用。
[0120]
(2)检查去除活性氧(ros)的有效性
[0121]
为了确认新的菌株brd125的deinopol去除辐射诱导的活性氧(ros)的有效性,接种cho细胞并使之稳定18小时,然后用浓度为50μg/ml的deinopol处理。在deinopol处理后4小时,用与活性氧反应的试剂dcf-da以20μm的浓度处理1小时,然后分离细胞并立即用x射线照射。使用流式细胞仪分析细胞中活性氧的浓度。结果,确认了在照射的对照组中测量到相对极高的活性氧,而通过deinopol的处理,活性氧显著减少(参见图7a)。
[0122]
为了确认新的菌株brd125的deinopol的辐射防护功效,在6孔板的每孔中接种200至500个cho细胞并使之稳定3小时,然后用浓度为50μg/ml的deinopol处理。在deinopol处理后2小时,在160kv和1ma的x射线条件下分别照射2gy、3gy、4gy和6gy。x射线照射后第7天,弃去培养基,用甲醇固定细胞,然后用0.5%结晶紫对菌落进行染色并计数。在这种情况下,cho细胞活力计算方法如下:
[0123]
存活分数=试验组的pe/正常对照组的pe
[0124]
*pe(平板效率)=计数的菌落/起始细胞
×
100
[0125]
结果证实,与照射的对照组相比,通过deinopol处理,在x射线照射后cho细胞中的存活分数在统计学上显著增加(图7b)。
[0126]
7.耐辐射奇球菌brd125的deinopol的辐射防护功效的确认
[0127]
(1)体外抑制辐射引起的造血细胞和免疫细胞凋亡的功效确认
[0128]
为了确认新的菌株brd125的deinopol对辐射敏感的造血细胞和免疫细胞的辐射防护功效,采集了小鼠的骨髓(造血细胞)和脾脏(免疫细胞),并分别从中分离出细胞。将每种细胞接种在12孔板中,并用浓度为50μg/ml的deinopol处理3小时,然后在160kv和1ma条件下用x射线以3gy的剂量照射骨髓细胞,并且以1gy的剂量照射脾脏中的免疫细胞。在x射线照射后24小时,收集所有细胞,固定在70%乙醇中,并用碘化丙啶(pi)试剂染色,利用流式细胞仪分析细胞周期和死亡细胞的百分比。结果,照射后骨髓细胞和脾细胞的细胞死亡率均显著增加,而处于g1期的细胞减少。经证实,在骨髓细胞和脾细胞中,与辐照对照组相比,deinopol处理组的细胞死亡率在统计学上显著降低,而与辐照对照组相比,处于g1期增加(图8a和图8b)。通过该实验证实,deinopol处理使bcl-2的表达(一种细胞死亡抑制因子)增加,而bcl-2的表达会因辐射而在骨髓细胞和脾细胞中降低(图8c)。
[0129]
(2)体内抑制辐射引起的造血细胞和免疫细胞死亡的功效确认
[0130]
为了确认新的菌株brd125的deinpol对造血系统和免疫细胞的辐射防护功效,在辐照(伽马射线)照射前48小时和24小时以及紧接照射后30分钟内,将deinopol以50μg/kg bw腹膜内注射至小鼠,并且辐射暴露以4gy的剂量单次全身照射的形式来进行。照射后4小时,处死所有的小鼠,然后收集骨髓细胞和脾细胞,用70%乙醇固定,pi(碘化丙啶)试剂染
色,流式细胞仪分析凋亡细胞的百分比。此外,收集来自骨髓细胞的片段化dna,然后在2%琼脂糖凝胶中进行电泳,以确认辐射引起的凋亡造血细胞的dna片段化程度。结果证实,在骨髓细胞和脾细胞中,辐射引起细胞死亡率的显著增加,但通过施用deinopol,辐射引起的死亡率在统计学上显著降低(参见图9a和图9b)。此外,证实了,通过辐射,骨髓细胞的dna片段化显著高于正常对照组的dna片段化,但在施用deinopol的小鼠的骨髓细胞中dna片段化现象减少(图9c)。因此,发现deinopol对经照射小鼠的造血干细胞和免疫细胞具有优异防护作用。
[0131]
(3)deinopol在经照射小鼠中使内源性脾集落形成增加的确认
[0132]
照射后迅速失去对辐射敏感的造血干细胞,然后在脾脏发生紧急造血行为以补充血液中的细胞数量,并且在脾脏表面可观察到造血细胞集落。为了证实新的菌株brd125的deinopol在经照射小鼠中增加内源性脾集落形成,在辐照(伽马射线)照射前48小时和24小时以及紧接照射后30分钟内和24小时和48小时后,以50μg/kgbw腹膜内注射deinopol,并且照射以6.5gy的剂量单次全身照射的形式来进行。照射后第9天,处死所有小鼠,收集脾脏,固定并用波恩氏(bouin’s)溶液染色。对在脾脏表面形成的集落数进行计数。结果证实,照射对照组的脾脏上的造血细胞集落数平均为1.5,而施用deinopol的经照射小鼠的平均数为22.8(参见图10)。因此,发现deinopol具有促进经照射小鼠造血干细胞保护和再生的优异作用。
[0133]
(4)辐射对体内造血因子表达的影响的确认
[0134]
为了证实deinopol在经照射小鼠中造血因子gm-csf和scf表达的增加,在辐射(伽马射线)暴露前48小时和24小时以及照射后30分钟内和24小时和48小时后,以50μg/kgbw腹膜内注射deinopol,并且照射以3gy的剂量单次全身照射的形式来进行。照射后第7天,处死所有小鼠,从脾脏收集细胞,并提取rna。提取的rna通过rt过程合成为cdna,并通过进行pcr过程来比较gm-csf和scf的表达水平。结果证实,与照射对照组相比,注射了deinopol的经照射小鼠中gm-csf和scf的表达分别增加至1.5倍和2倍(图11)。
[0135]
(5)照射后体内外周血细胞数和脾免疫细胞数恢复效果的确认
[0136]
照射后,外周血中的白细胞的数量和淋巴细胞的数量以及脾脏中的免疫细胞的数量迅速减少。在这种情况下,通过免疫细胞的再生来恢复免疫细胞的数量在照射后的恢复中起着重要作用。因此,在以3gy的剂量(次致死量)照射后,观察到deinopol对外周血和脾免疫细胞数量恢复的作用。为了证实新的菌株brd125的deinopol在经照射小鼠使(a)外周血中白细胞的数量、(b)外周血中淋巴细胞的数量和(c)脾脏中免疫细胞的数量的恢复增加,在照射前48小时和24小时以及以3gy的剂量辐射(伽马射线)暴露后30分钟内和24小时和48小时后,以50μg/kgbw腹膜内注射deinopol。照射后第7天、第14天、第21天通过小鼠眼眶静脉采血,使用自动血细胞计数器测定外周血中白细胞和淋巴细胞的数量,收集脾脏中的免疫细胞并进行计数。结果观察到,在照射对照组中,照射后第7天,外周血中白细胞和淋巴细胞急剧下降至正常对照组的约20%的水平,随后逐渐恢复,并在照射后3周回到照射前水平。另一方面,在施用deinopol的照射组中,白细胞和淋巴细胞的数量在统计学上显著高于照射对照组的白细胞和淋巴细胞的数量,并且再生也增加(图12a和图12b)。此外,根据脾脏中免疫细胞的数量的计数结果,在照射对照组中,免疫细胞的数量在照射后第7天迅速减少并逐渐恢复,而在施用deinopol的经照射小鼠中,照射后第7天免疫细胞的数量略有下
降,但第14天与正常对照组几乎没有差异(图12c)。根据这些结果,确认了deinopol具有促进照射后免疫细胞数恢复的效果。
[0137]
尽管上文已经详细描述了本技术的实施方式,但是本技术的范围并不限于此,并且在不背离权利要求中描述的本技术的技术精神的情况下,可以进行各种修改和变化,这对于本领域普通技术人员来说是显而易见的。
[0138]
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。