1.本发明涉及有机合成技术领域,特别是涉及一种电化学氧化合成含氟异噁唑衍生物的方法。
背景技术:
2.肟是一种迷人的分子,广泛存在于有机化学和生物化学中。β,γ-不饱和肟的环化反应是一种常用的构建异噁唑啉和硝酮化合物的合成方法,且异噁唑啉和硝酮化合物是有机合成中重要的结构单元。不饱和酮肟的邻位氧化三氟甲基化反应引起了有机科学家的极大关注,该特色反应可以快速有效地在酮肟的分子内烯烃上构建邻位氧化酰化或氧化氟化等重要结构分子。然而,目前合成获得所需要的产物主要是通过金属催化、光催化或过氧化物导向的方式实现的,而采用新的电化学氧化的合成技术来构建官能团化的异噁唑结构研究的比较少,目前只有两例被报道。同时电化学合成技术是近年来发展比较迅猛的研究领域,在有机合成中更是一种绿色,高效清洁的合成手段。
3.目前,基于分子内烯烃的肟实现自由基环化反应的方式主要取决于底物本身,无论是双自由基,小分子催化,金属催化或光催化都需要从底物启动自由基发生环化反应。因此,发展温和高效的电化学氧化合成异噁唑啉的方法具有深远的基础研究价值。
技术实现要素:
4.本发明致力于发展一种绿色、高效清洁的电化学氧化合成含氟异噁唑衍生物的方法,本发明电化学氧化β,γ-不饱和肟和三氟亚磺酸钠的自由基环化反应构建氟化的异噁唑环骨架,该方法在无需任何金属和氧化剂的参与下,以较温和的条件,高效地合成含氟异噁唑衍生物,能获得较好的收率。
5.为实现上述目的,本发明提供了如下方案:
6.本发明提供一种电化学氧化合成含氟异噁唑衍生物的方法,包括以下步骤:
7.1)合成三氟取代异噁唑衍生物
8.将β,γ-不饱和酮肟和三氟甲基亚磺酸钠混合,控制温度在25℃,选用c( )/pt(-)作为电极,加入四乙基六氟磷酸铵和六氟异丙醇/乙腈(指的是六氟异丙醇和乙腈),室温反应3.0h;
9.2)反应结束后,旋蒸除去六氟异丙醇/乙腈,加水淬灭,乙酸乙酯萃取,合并有机相,减压蒸馏去除大部分溶剂,柱层析分离提纯,得到含氟异噁唑衍生物。
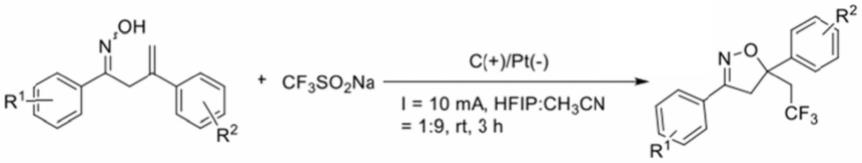
10.本发明电化学氧化合成含氟异噁唑衍生物的方法的反应路线如下:
[0011][0012]
r1、r2独立地选自卤素、烷基、甲氧基或三氟甲基,r1、r2优选独立地选自f、cl、br、
ch3、och3或cf3。
[0013]
本发明公开了一种温和条件下电化学氧化含氟异噁唑啉衍生物的绿色合成方法。该方法利用β,γ-不饱和酮肟和无机盐三氟甲基亚磺酸钠为起始原料,在c( )/pt(-)作为电极的条件下,i=10ma的电流,室温反应3h,便能顺利地将无机盐中的三氟甲基基团成功引入到有机底物中,再通过分子内的亲核环化反应生成了三氟甲基化的异噁唑产物,本发明在无需金属和额外氧化剂的条件下巧妙地将无机氟化物引入到异噁唑环的骨架中,既丰富了氟化学的研究,又为有机化合物与无机化合物的自由基串联组合反应提供了新的途径,并且本发明在放大规模的情况下,在药物、农药的应用上也体现了一定的潜在价值。
[0014]
优选地,β,γ-不饱和酮肟与三氟甲基亚磺酸钠的摩尔比为1:2。。
[0015]
优选地,所述β,γ-不饱和酮肟的结构式如下:
[0016][0017]
r1、r2独立地选自卤素、烷基、甲氧基或三氟甲基。
[0018]
优选地,r1、r2独立地选自f、cl、br、ch3、och3或cf3。更优选,r1=f、cl、br、ch3、och3或cf3,r2=f、cl、br或ch3。
[0019]
优选地,六氟异丙醇(hfip)与乙腈(ch3cn)的体积比为1:9。
[0020]
优选地,柱层析分离提纯过程中,以乙酸乙酯和石油醚作为洗脱剂。
[0021]
优选地,石油醚与乙酸乙酯的体积比为10:1~30:1。
[0022]
本发明电化学氧化合成含氟异噁唑衍生物的方法优选如下:
[0023]
1)将β,γ-不饱和酮肟和三氟甲基亚磺酸钠(摩尔比为1:2)加入到反应器中反应,控制温度在25℃,选用c( )/pt(-)作为电极,四乙基六氟磷酸铵(276mg,0.1m),六氟异丙醇/乙腈(10ml),室温反应3.0h;
[0024]
2)反应结束后,旋蒸除去六氟异丙醇/乙腈,加水淬灭,乙酸乙酯萃取,合并有机相,减压蒸馏去除大部分溶剂,以乙酸乙酯和石油醚作为洗脱剂(体积比为10:1~30:1)对粗产品进行柱层析分离提纯,得到目标产物含氟异噁唑衍生物。
[0025]
本发明发展了无需外加氧化剂或铜催化剂的电化学体系,直接向反应体系中引入含三氟取代的无机亚磺酸盐,成功将氟原子引入到异噁唑环中,反应条件温和,绿色高效,可持续性且经济效益高,同时合成的氟化异噁唑啉衍生物也是护心药和除草剂的活性分子骨架。并且在放大规模的情况下,在药物、农药的应用上也体现了一定的潜在价值。
[0026]
本发明公开了以下技术效果:
[0027]
1)本发明使用含氟的无机盐,既可以引入合成意义上重要的氟原子,又可以充当电解质的作用,不仅拓展了成本经济效益,同时也成功实现了烯丙基肟分子内的氧化三氟甲基化反应,收益可观;
[0028]
2)本发明含有三氟甲基的异噁唑骨架,可作为有机合成中间体,该方法有着良好的官能团耐受性和宽广的底物范围等优势,可广泛用于药物,农药的新型合成提供有效片段;
[0029]
3)本发明采用电化学的催化方式,将清洁廉价的电能应用于化学反应,高效地构
建氟化异噁唑结构,提高了产物收率,并大大缩短了化学反应的时间。
附图说明
[0030]
为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
[0031]
图1为实施例1制备的3,5-二苯基-5-(2,2,2-三氟乙基)-4,5-二氢异噁唑的1h-nmr核磁共振谱;
[0032]
图2为实施例2制备的5-苯基-3-(对甲苯基)-5-(2,2,2-三氟乙基)-4,5-二氢异噁唑的1h-nmr核磁共振谱;
[0033]
图3为实施例3制备的3-(4-溴苯基)-5-苯基-5-(2,2,2-三氟乙基)-4,5-二氢异噁唑的1h-nmr核磁共振谱;
[0034]
图4为实施例4制备的3-(4-氯苯基)-5-苯基-5-(2,2,2-三氟乙基)-4,5-二氢异噁唑的1h-nmr核磁共振谱;
[0035]
图5为实施例5制备的3-(4-叔丁基苯基)-5-苯基-5-(2,2,2-三氟乙基)-4,5-二氢异噁唑的1h-nmr核磁共振谱;
[0036]
图6为实施例6制备的5-苯基-5-(2,2,2-三氟乙基)-3-(4-三氟甲基苯基)-4,5-二氢异噁唑的1h-nmr核磁共振谱。
具体实施方式
[0037]
现详细说明本发明的多种示例性实施方式,该详细说明不应认为是对本发明的限制,而应理解为是对本发明的某些方面、特性和实施方案的更详细的描述。
[0038]
应理解本发明中所述的术语仅仅是为描述特别的实施方式,并非用于限制本发明。另外,对于本发明中的数值范围,应理解为还具体公开了该范围的上限和下限之间的每个中间值。在任何陈述值或陈述范围内的中间值,以及任何其他陈述值或在所述范围内的中间值之间的每个较小的范围也包括在本发明内。这些较小范围的上限和下限可独立地包括或排除在范围内。
[0039]
除非另有说明,否则本文使用的所有技术和科学术语具有本发明所述领域的常规技术人员通常理解的相同含义。虽然本发明仅描述了优选的方法和材料,但是在本发明的实施或测试中也可以使用与本文所述相似或等同的任何方法和材料。本说明书中提到的所有文献通过引用并入,用以公开和描述与所述文献相关的方法和/或材料。在与任何并入的文献冲突时,以本说明书的内容为准。
[0040]
在不背离本发明的范围或精神的情况下,可对本发明说明书的具体实施方式做多种改进和变化,这对本领域技术人员而言是显而易见的。由本发明的说明书得到的其他实施方式对技术人员而言是显而易见得的。本发明说明书和实施例仅是示例性的。
[0041]
关于本文中所使用的“包含”、“包括”、“具有”、“含有”等等,均为开放性的用语,即意指包含但不限于。
[0042]
本发明利用β,γ-不饱和酮肟,三氟甲基亚磺酸钠为起始原料,在c( )/pt(-)作为
电极的条件下,i=10ma的电流,室温反应3h,其中β,γ-不饱和酮肟与三氟甲基亚磺酸钠的摩尔比为1:2,实现了不饱和酮肟分子内烯烃的双官能团化反应,高效合成了三氟甲基化的异噁唑衍生物。
[0043]
实施例1:3,5-二苯基-5-(2,2,2-三氟乙基)-4,5-二氢异噁唑的合成
[0044][0045]
向25ml的电化学反应池中加入1,3-二苯基-丁-3-烯-1-酮肟(0.2mmol,47.4mg)、三氟亚磺酸钠(0.4mmol,62.4mg),四乙基六氟磷酸铵(276mg,0.1m),hfip:ch3cn=1:9(v:v,10ml),在c( )/pt(-)作为电极的条件下,i=10ma的恒定电流下,25℃磁力搅拌反应5h;反应完毕后,减压蒸馏除去六氟异丙醇和乙腈,加水淬灭,乙酸乙酯萃取三次,合并有机相,减压浓缩得到粗品,粗品用石油醚:乙酸乙酯(30:1,v:v)作为淋洗剂洗脱,经柱层析分离提纯后得到目标产物3,5-二苯基-5-(2,2,2-三氟乙基)-4,5-二氢异噁唑,为白色固体,收率72%。
[0046]
本实施例制备的3,5-二苯基-5-(2,2,2-三氟乙基)-4,5-二氢异噁唑的1h-nmr核磁共振谱见图1,其核磁数据如下:
[0047]1h-nmr(300mhz,cdcl3)δ7.58-7.55(m,2h),7.44-7.41(m,2h),7.32-7.23(m,6h),3.65(dd,j=41.7hz,j=16.5hz,2h),2.85(dd,j=20.4hz,j=10.2hz,2h).
[0048]
实施例2:5-苯基-3-(对甲苯基)-5-(2,2,2-三氟乙基)-4,5-二氢异噁唑的合成
[0049][0050]
向25ml的电化学反应池中加入3-苯基-1-(对甲苯基)-丁-3-烯-1-酮肟(0.2mmol,50.3mg)、三氟亚磺酸钠(0.4mmol,62.4mg),四乙基六氟磷酸铵(276mg,0.1m),hfip:ch3cn=1:9(v:v,10ml),在c( )/pt(-)作为电极的条件下,i=10ma的恒定电流下,30℃磁力搅拌反应3h;反应完毕后,减压蒸馏除去六氟异丙醇和乙腈,加水淬灭,乙酸乙酯萃取三次,合并有机相,减压浓缩得到粗品,粗品用石油醚:乙酸乙酯(30:1,v:v)作为淋洗剂洗脱,经柱层析分离提纯后得到目标产物5-苯基-3-(对甲苯基)-5-(2,2,2-三氟乙基)-4,5-二氢异噁唑,为白色固体,收率58%。
[0051]
本实施例制备的5-苯基-3-(对甲苯基)-5-(2,2,2-三氟乙基)-4,5-二氢异噁唑的1h-nmr核磁共振谱见图2,其核磁数据如下:
[0052]1h nmr(300mhz,cdcl3)δ7.48
–
7.41(m,4h),7.34
–
7.23(m,3h),7.19
–
7.10(m,2h),3.63(dd,j=40.2hz,j=16.8hz,2h),2.84(dd,j=20.7hz,j=10.5hz,2h),2.29(s,3h).
[0053]
实施例3:3-(4-溴苯基)-5-苯基-5-(2,2,2-三氟乙基)-4,5-二氢异噁唑的合成
[0054][0055]
向25ml的电化学反应池中加入1-(4-溴苯基)-3-苯基丁-3-烯-1-酮肟(0.2mmol,63.2mg)、三氟亚磺酸钠(0.4mmol,62.4mg),四乙基六氟磷酸铵(276mg,0.1m),hfip:ch3cn=1:9(v:v,10ml),在c( )/pt(-)作为电极的条件下,i=10ma的恒定电流下,30℃磁力搅拌反应4h;反应完毕后,减压蒸馏除去六氟异丙醇和乙腈,加水淬灭,乙酸乙酯萃取三次,合并有机相,减压浓缩得到粗品,粗品用石油醚:乙酸乙酯(30:1,v:v)作为淋洗剂洗脱,经柱层析分离提纯后得到目标产物3-(4-溴苯基)-5-苯基-5-(2,2,2-三氟乙基)-4,5-二氢异噁唑,为淡黄色固体,收率60%。
[0056]
本实施例制备的3-(4-溴苯基)-5-苯基-5-(2,2,2-三氟乙基)-4,5-二氢异噁唑的1h-nmr核磁共振谱见图3,其核磁数据如下:
[0057]1h nmr(300mhz,cdcl3)δ7.26
–
7.21(m,5h),7.17
–
6.99(m,4h),3.51(dd,j=43.2hz,j=16.8hz 2h),2.67(dd,j=20.7hz,j=10.2hz,2h).
[0058]
实施例4:3-(4-氯苯基)-5-苯基-5-(2,2,2-三氟乙基)-4,5-二氢异噁唑的合成
[0059][0060]
向25ml的电化学反应池中加入1-(4-氯苯基)-3-苯基丁-3-烯-1-酮肟(0.2mmol,63.2mg)、三氟亚磺酸钠(0.4mmol,62.4mg),四乙基六氟磷酸铵(276mg,0.1m),hfip:ch3cn=1:9(v:v,10ml),在c( )/pt(-)作为电极的条件下,i=10ma的恒定电流下,30℃磁力搅拌反应3h;反应完毕后,减压蒸馏除去六氟异丙醇和乙腈,加水淬灭,乙酸乙酯萃取三次,合并有机相,减压浓缩得到粗品,粗品用石油醚:乙酸乙酯(30:1,v:v)作为淋洗剂洗脱,经柱层析分离提纯后得到目标产物3-(4-氯苯基)-5-苯基-5-(2,2,2-三氟乙基)-4,5-二氢异噁唑,为白色固体,收率78%。
[0061]
本实施例制备的3-(4-氯苯基)-5-苯基-5-(2,2,2-三氟乙基)-4,5-二氢异噁唑的1h-nmr核磁共振谱见图4,其核磁数据如下:
[0062]1h nmr(300mhz,cdcl3)δ7.59(d,j=8.6hz,2h),7.51
–
7.48(m,2h),7.43
–
7.32(m,5h),3.71(dd,j=43.1hz,j=16.8hz,2h),2.93(dd,j=20.7hz,j=10.3hz,2h).
[0063]
实施例5:3-(4-叔丁基苯基)-5-苯基-5-(2,2,2-三氟乙基)-4,5-二氢异噁唑的合成
[0064][0065]
向25ml的电化学反应池中加入1-(4-叔丁基苯基)-3-苯基丁-3-烯-1-酮肟
(0.2mmol,58.7mg)、三氟亚磺酸钠(0.4mmol,62.4mg),四乙基六氟磷酸铵(276mg,0.1m),hfip:ch3cn=1:9(v:v,10ml),在c( )/pt(-)作为电极的条件下,i=10ma的恒定电流下,25℃磁力搅拌反应3h;反应完毕后,减压蒸馏除去六氟异丙醇和乙腈,加水淬灭,乙酸乙酯萃取三次,合并有机相,减压浓缩得到粗品,粗品用石油醚:乙酸乙酯(30:1,v:v)作为淋洗剂洗脱,经柱层析分离提纯后得到目标产物3-(4-叔丁基苯基)-5-苯基-5-(2,2,2-三氟乙基)-4,5-二氢异噁唑,为白色固体,收率54%。
[0066]
本实施例制备的3-(4-叔丁基苯基)-5-苯基-5-(2,2,2-三氟乙基)-4,5-二氢异噁唑的1h-nmr核磁共振谱见图5,其核磁数据如下:
[0067]1h nmr(300mhz,cdcl3)δ7.60(d,j=8.5hz,2h),7.52
–
7.49(m,2h),7.44
–
7.31(m,5h),3.72(dd,j=42.2,j=16.7hz,2h),2.93(dd,j=21.0hz,j=10.4hz,2h),1.32(s,9h).
[0068]
实施例6:5-苯基-5-(2,2,2-三氟乙基)-3-(4-三氟甲基苯基)-4,5-二氢异噁唑的合成
[0069][0070]
向25ml的电化学反应池中加入3-苯基-1-(4-三氟甲基苯基)丁-3-烯-1-酮肟(0.2mmol,61.0mg)、三氟亚磺酸钠(0.4mmol,62.4mg),四乙基六氟磷酸铵(276mg,0.1m),hfip:ch3cn=1:9(v:v,10ml),在c( )/pt(-)作为电极的条件下,i=10ma的恒定电流下,25℃磁力搅拌反应6h;反应完毕后,减压蒸馏除去六氟异丙醇和乙腈,加水淬灭,乙酸乙酯萃取三次,合并有机相,减压浓缩得到粗品,粗品用石油醚:乙酸乙酯(30:1,v:v)作为淋洗剂洗脱,经柱层析分离提纯后得到目标产物5-苯基-5-(2,2,2-三氟乙基)-3-(4-三氟甲基苯基)-4,5-二氢异噁唑,为淡黄色固体,收率72%。
[0071]
本实施例制备的5-苯基-5-(2,2,2-三氟乙基)-3-(4-三氟甲基苯基)-4,5-二氢异噁唑的1h-nmr核磁共振谱见图6,其核磁数据如下:
[0072]1h nmr(300mhz,cdcl3)δ7.77(d,j=8.2hz,2h),7.65(d,j=8.3hz,2h),7.52
–
7.49(m,2h),7.44-7.31(m,3h),3.75(dd,j=45.1,16.8hz,2h),2.95(dd,j=20.7hz,j=10.3hz,2h).
[0073]
本发明在医药,农药,有机合成等诸多领域有着广泛的应用,另外,本发明操作简单,绿色清洁,反应条件温和,成本低,反应高效,拥有广阔的应用前景。
[0074]
例如,实施例1的目标产物可作为磺胺异噁唑,氯洒西林等抗菌,抗过敏药物的合成中间体。
[0075]
实施例1的目标产物可作为中间体合成具有防虫功效的化合物以及具有除草功效的化合物,作为木材防虫剂和除草剂使用。
[0076]
实施例1的目标产物可进一步衍生还原生成β-氨基醇化合物,是制备氨基醇衍生物的重要中间体。
[0077]
以上所述的实施例仅是对本发明的优选方式进行描述,并非对本发明的范围进行限定,在不脱离本发明设计精神的前提下,本领域普通技术人员对本发明的技术方案做出的各种变形和改进,均应落入本发明权利要求书确定的保护范围内。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。