用嵌合抗原受体治疗癌症的组合物和方法
1.发明背景
技术领域
2.本披露涉及使用嵌合抗原受体t细胞来治疗癌症。
背景技术:
3.1.嵌合抗原受钵t细胞疗法
4.嵌合抗原受体(car)t细胞疗法是特定形式的基于细胞的免疫疗法,该免疫疗法使用工程化的t细胞对抗癌症。在car t细胞疗法中,将t细胞从患者血液中收获,离体工程化以表达含有抗原结合结构域和t细胞激活结构域的car,扩增至更大的群体并且施用至患者。car t细胞用作结合至癌细胞并引起这些癌细胞的破坏的活的药物。当成功时,car t细胞治疗的作用往往会持续很长时间,如通过在临床缓解后很长时间在患者中检测car t细胞的持久性和扩增所证明的。
5.2.car结构和功能
6.car的抗原结合结构域是靶向肿瘤细胞上的表面抗原的细胞外区域。合适的靶抗原可以是蛋白质、磷酸化蛋白质、肽-mhc、碳水化合物、或糖脂分子。理想的靶抗原在肿瘤细胞上广泛表达以使得能够靶向高百分比的癌细胞。理想的候选靶抗原也在正常组织上最低限度地表达,从而限制了肿瘤外的中靶毒性。car的抗原结合结构域包含针对靶抗原的靶向部分,如抗体单链可变片段(scfv)。
7.car的t细胞激活结构域在细胞内,并激活t细胞以响应于与其靶抗原相互作用的抗原结合结构域。t细胞激活结构域可以含有一个或多个共刺激结构域,这些共刺激结构域是已知的激活t细胞受体的细胞内结构域。由于共刺激结构域对car t细胞动力学、细胞毒性功能、和安全特性具有不同的影响,因此car构建体内的共刺激结构域的选择和位置会影响car t细胞的功能和命运。
8.car的细胞外抗原结合结构域和细胞内t细胞激活结构域通过跨膜结构域、铰链、和任选地间隔子区连接。铰链结构域是提供构象自由度以促进与肿瘤细胞上的靶抗原结合的短肽片段。它可单独使用或与设计scfv远离t细胞表面的间隔子结构域结合使用。间隔子的最佳长度取决于结合表位与细胞表面的接近度。
9.针对b淋巴细胞抗原cd19的car t疗法(诺华公司(novartis))在小儿急性淋巴细胞性白血病中显示出前景,并且针对b细胞成熟抗原的car t疗法(“bb2121”,和合作)针对复发性/难治性多发性骨髓瘤显示出前景。最近的数据表明,car方法可对实体瘤有效。gd2 car自然杀伤t细胞(nkt)疗法在神经母细胞瘤中显示出活性(heczey a等人invariant nkt cells with chimeric antigen receptor provide a novel platform for safe and effective cancer immunotherapy[具有嵌合抗原受体的恒定nkt细胞为安全且有效的癌症免疫疗法提供新的平台].blood[血液];124
(18):2824-33,2014),并且具有派姆单抗(pembrolizumab)的间皮素car t已证明在间皮瘤中具有抗肿瘤活性。然而,需要用于治疗实体瘤的另外的靶标。
[0010]
3.car t细胞疗法的挑战
[0011]
不幸的是,基于car t细胞的疗法的复杂性可能导致不希望的和不安全的作用。毒性作用,如神经毒性和急性呼吸窘迫综合征,是car t细胞疗法的潜在不良作用并且可能致命。细胞因子释放综合征(crs)是与car t细胞相关的最常见的急性毒性。当淋巴细胞被高度激活并释放出过量的炎性细胞因子时,发生crs。当测定这些因子时,有时在患有crs的患者中观察到白介素2、白介素6、白介素1β、gm-csf和/或c反应蛋白的血清升高。crs按严重性分级并诊断为1-4级(轻度至重度)之一,其中更严重的病例的临床特征为患者出现高烧、低血压、缺氧和/或多器官毒性。一项研究报道,用抗cd19car-t细胞疗法治疗的急性淋巴细胞性白血病患者中有92%经历crs,并且50%的这些患者出现了3-4级的症状(fitzgerald等人,crit care med.[危重病急救医学]45(2):e124-e131(2017))。
[0012]
成功的car t细胞免疫疗法的另一个挑战是由实体瘤的肿瘤微环境(tme)的特征引起的免疫抑制。由于营养供应有限,实体瘤的肿瘤微环境(tme)可在代谢上对car t细胞不利。这种不利导致营养竞争、t细胞代谢适应性丧失和氧含量降低(即,“缺氧”)。缺氧降低t细胞激活和增殖,而且减少细胞因子和裂解酶产生。这些作用中的关键角色是缺氧诱导因子-1α(hif-1α),其是转录因子缺氧诱导因子-1(hif-1)的α亚基。hif-1α是对缺氧的细胞和系统稳态反应的主要调节因子,这使其成为氧稳态的关键因素。hif-1α还控制参与能量代谢、血管生成、细胞凋亡的基因,以及促进对缺氧的代谢适应的其他基因的转录。hif-1α还在t细胞激活中起重要作用。它导致t细胞表现出完全效应表型,包括细胞因子和裂解颗粒产生、高糖酵解、高代谢活性和高活性氧物质(ros)产生。这样的表型导致作为肿瘤位点的效应t细胞的数量减少、效应特征的维持减少和低持久性。已经表明,低效应表型导致增加数量的效应细胞,其在肿瘤位点具有增加的活性和更大的持久性(kishton,r.j.,sukumar,m.,和restifo,n.p.(2017).metabolic regulation of t cell longevity and function in tumor immnunotherapy[肿瘤免疫疗法中t细胞寿命和功能的代谢调节].cell metab[细胞代谢],26(1),94-109)。因此,hif-1α介导的免疫抑制也是为了获得针对实体瘤的有效且持久的car t细胞疗法所必须克服的重要障碍。
[0013]
4.装甲
[0014]
制备更加抵抗肿瘤相关的免疫抑制的car t细胞的最新方法称为“装甲”。装甲是对car t细胞进行分子操作,以表达一种或多种可以抵抗免疫抑制的“装甲分子”。例如,显性负性hif-1α(hif1αdn)装甲分子在对hif-1α引起的缺氧和葡萄糖剥夺诱导的细胞凋亡有抗性的胰腺癌细胞中的表达使细胞对缺氧和葡萄糖剥夺诱导的细胞凋亡和生长抑制敏感。(che等人,dominant-negative hypoxia-inducible factor-1αreduces tumorigenicity of pancreatic cancer cells through the suppression of glucose metabolism[显性负性缺氧诱导因子-1α通过抑制葡萄糖代谢降低胰腺癌细胞的致瘤性],am j pathol[美国病理学杂志],162(4),1283-1291(2003))。
[0015]
因此,需要另外的car t细胞疗法以增强有效癌症治疗的医疗设备。这样的疗法应包括有效治疗癌症、同时将发生危险炎性反应(如crs)的风险降至最低的car t细胞。此外,这样的疗法应包括可在实体瘤的免疫抑制性tme中持续存在的car t细胞。
技术实现要素:
[0016]
本披露描述了使用car t细胞来治疗癌症的组合物和方法。如下所述,在第一方面,一种分离的核酸序列,该分离的核酸序列编码(a)嵌合抗原受体(car),其中该car包含对细胞表面抗原具有特异性的抗原结合结构域;和(b)装甲分子,其中该装甲分子在肿瘤微环境中的细胞表面上表达时抵抗对该细胞的免疫抑制。
[0017]
在另一方面,本披露描述了一种细胞,该细胞包含核酸序列,该核酸序列编码嵌合抗原受体(car)和在该细胞表面上表达的hif1αdn装甲分子。
[0018]
在另一个方面,本披露描述了一种细胞,该细胞包含:含有抗原结合结构域的抗gpc3嵌合抗原受体(car),其中该抗原结合结构域包含含有重链可变区(vh)和轻链可变区(vl)的抗体、fab、或scfv,其中该vh包含含有seq id no:37的氨基酸序列的cdr1、含有seq id no:38的氨基酸序列的cdr2、以及含有seq id no:39的氨基酸序列的cdr3,并且其中该vl包含含有seq id no:40或seq id no:43的氨基酸序列的cdr1、含有seq id no:41或seq id no:44的氨基酸序列的cdr2、以及含有seq id no:42或seq id no:45的氨基酸序列的cdr3;和hif1αdn装甲分子。
[0019]
在又一个方面,本披露描述了一种治疗癌症的方法,该方法包括:向有需要的受试者施用细胞,其中该细胞包含(a)对细胞表面抗原具有特异性的嵌合抗原受体(car),和(b)装甲分子,其中该装甲分子在该癌症的肿瘤微环境中抵抗对该细胞的免疫抑制。
[0020]
根据以下的详细描述以及所附权利要求,将更全面地理解本发明的这些和其他特征以及优点。应注意权利要求的范围由其中的叙述定义,而不是由本说明书中阐述的特征和优点的具体讨论定义。
附图说明
[0021]
包括附图以提供对本披露的方法和组合物的进一步理解。附图展示了本披露的一个或多个实施例,并且与说明书一起用于解释本披露的原理和操作。
[0022]
图1.用hif1αdn对gpc3 car-t进行装甲。hif1adn结构的示意图。
[0023]
图2a-2c.hif1αdn相对于内源性hif1α过表达。
[0024]
在常氧(20%o2)或缺氧(1%o2)条件下扩增未转导的(ut)细胞、未装甲的gpc3 car t细胞和gpc3 hif1 αdn car t细胞。2a.图显示了每个样品的内源性hif1αmrna的表达,表示为相对于在(20%o2)下扩增的ut的倍数诱导。2b.在常氧(20%o2)和缺氧(1%o2)下,在未转导的、未装甲的gpc3 car t细胞和gpc3hif1αdn car t细胞中的内源性hif1α蛋白表达。β-肌动蛋白用作上样对照。2c.在常氧(20%o2)和缺氧(1%o2)下扩增的未转导的(ut)、gpc3 car t细胞和gpc3 hif1αdn car t细胞中hif1αdn相对于内源性hif1αmrna表达的倍数诱导。
[0025]
图3.表达hif1αdn的car-t分化程度较低。通过流式细胞术分析在常氧或缺氧条件下未转导的(ut)、gpc3和gpc3 hif1αdn car t细胞分化。条形图表示通过流式细胞术评估的cd62l
低
cd45ro
高
效应记忆t细胞(t
em
)的频率。
[0026]
图4.hif1αdn car t细胞干性的nanostring分析。与干性(上部箭头)和效应子功能(下部)相关的基因的表达。基因表示为相对于gpc3的gpc3 hif1αdn。
[0027]
图5.表达显性负性hif1a的gpc3-car修饰的t细胞在急性激活后表现出增强的氧
化磷酸化。(a)上小图显示了gpc3-car修饰的和显性负性hif1a gpc3-car修饰的t细胞在基础培养条件下并响应于激活的cd3/cd28包被珠和寡霉素的ocr。下小图显示了静息t细胞的基础ocr和急性激活后的ocr增益。数据显示为平均值
±
sd。(b)上小图显示了gpc3-car修饰的和显性负性hif1a gpc3-car修饰的t细胞在基础培养条件下并响应于激活的cd3/cd28包被珠和外源性葡萄糖的ecar。下小图显示了静息t细胞的基础ecar和急性激活后的ecar增益。数据显示为平均值
±
sd。(**p<.01,***p<.001;威氏配对符号秩次检验(wilcoxon matched pairs signed rank test))。
[0028]
图6.hif1αdn car t细胞在抗原接触后脱粒。在常氧(左)和缺氧(右)培养条件下扩增car-t细胞后,在hep3b(gpc3
)或snu182(gpc3-)细胞存在下,对ut、gpc3、gpc3 hif1αdn car t细胞的cd107a表达(脱粒和毒性的标记)进行流式细胞术分析。即使在缺氧下扩增,car-t细胞也会在体外响应于抗原接触而脱粒。hif1αdn car t细胞即使在静止状态下激活和分化程度较低,也能有效脱粒。
[0029]
图7.hif1αdn car t细胞在抗原接触后产生较少的ifnγ和il-2,但产生相似的tnfα。在常氧条件下抗原(gpc3)接触后24小时,在常氧或缺氧条件下扩增的ut、gpc3和gpc3 hif1αdn car t细胞的培养上清液中ifnγ、il-2和tnfa的浓度。
[0030]
图8.在低氧条件下刺激后,异位显性负性hif1a产生多功能t细胞。(a)用pma和离子霉素刺激6小时后,gpc3-car修饰的和显性负性hif1a gpc3-car修饰的t细胞的ifn-γ、il-2、tnf-α细胞内细胞因子染色的代表性流式图。(b)描绘cd4
和cd8
t细胞的细胞因子反应质量的条形图,如通过识别ifn-γ
、il-2
和tnf-α
细胞的门的布尔组合(boolean combination)确定的。y轴上的数字表示细胞百分比。
[0031]
图9.hif1αdn car t细胞快速且有效地杀伤靶细胞。在常氧和缺氧条件下,测量未转导的(ut)细胞、gpc3和gpc3 hif1αdn car t细胞通过细胞溶解对hep3b靶细胞的靶向和杀伤。使用基于实时阻抗的杀伤测定(rtca)测量hep3b细胞随时间的%细胞溶解。ut细胞对靶细胞的细胞溶解作用最小,而gpc3和hif1αdn car t细胞均具有显著的细胞溶解作用。出乎意料的是,在常氧和缺氧条件下,与未装甲的car t细胞相比,hif1αdn car t细胞表现出更快的靶细胞杀伤。这些令人惊讶的结果表明,用hif1αdn装甲car t细胞为car t细胞提供了除耐缺氧之外的额外优点,并且表明hif1αdn可用于提高其他car t细胞的效率,而与car靶抗原无关。
[0032]
图10.在常氧和缺氧条件下,按e:t比率的靶细胞细胞溶解的速率和效率。在不同的效应子与靶标比率(e∶t)下,在常氧(左)和缺氧(右)条件下扩增的ut、gpc3和gpc3 hif1αdn car t细胞对hep3b细胞的细胞溶解能力。使用基于实时阻抗的杀伤测定(rtca)测量值,并将这些值表示为kt80(杀伤80%靶标所需的时间)。
[0033]
图11.hep3b靶细胞细胞溶解的可视化。在常氧条件下引入细胞后3小时(下小图),ut、gpc3和gpc3 hif1αdn car t细胞对hep3b靶细胞的细胞溶解的显微照片。上小图显示不存在靶细胞时的t细胞。
[0034]
图12.靶细胞的细胞溶解。在e∶t为1∶1的常氧条件下,ut、gpc3和gpc3 hif1αdn car t细胞对huh7和plc-prf15靶细胞的细胞溶解。gpc3和gpc3 hif1αdn car t细胞对每种细胞类型表现出相似的细胞溶解速率。
[0035]
图13.存在靶抗原时的细胞增殖。通过羧基荧光素二乙酸琥珀酰亚胺酯(cfse)稀释液测量的抗原依赖性细胞增殖。
[0036]
图14.hif1αdn的表达增强car-t体内功效(huh7),用huh7细胞皮下接种nsg小鼠,并且当肿瘤体积达到大约150mm3时,静脉内(i.v.)输注7
×
106个ut、gpc3或gpc3 hif1αdn car t细胞。每周两次测量肿瘤体积。
[0037]
图15.hif1αdn的表达增强car-t体内功效(hep3b)。用hep3b细胞皮下接种nsg小鼠,并且当肿瘤体积达到大约150mm3时,静脉内输注7
×
106个ut、gpc3或gpc3 hif1αdn car t细胞。每周两次测量肿瘤体积。
[0038]
图16.hif1αdn的表达增加car-t浸润实体瘤的能力。用hep3b细胞皮下接种nsg小鼠,并且当肿瘤体积达到大约175mm3时,静脉内输注7
×
106个ut、gpc3或gpc3 hif1αdn car t细胞。输注后7天通过流式细胞术评估肿瘤中t细胞的频率和数量。
[0039]
图17.用hif1αdn car-t治疗的小鼠血清中高水平的ifnγ。在携带hep3b肿瘤并用未转导的t细胞、未装甲的或装甲的gpc3car-t细胞输注的小鼠血清中检测到的ifn-γ浓度。
[0040]
图18.hif1αdn car-t在外周保持分化程度较低的表型。在携带hep3b肿瘤并用未转导的t细胞、未装甲的或装甲的gpc3 car-t细胞输注的小鼠脾脏中cd70
cd27-car-t细胞的频率。
具体实施方式
[0041]
1.定义
[0042]
除非另有定义,本文使用的所有技术和科学术语具有本发明所属领域的技术人员通常理解的含义。以下的参考文献为技术人员提供了本发明所用的多个术语的通用定义:singleton等人,dictionary of microbiology and molecular biology[微生物学和分子生物学词典](第2版1994);the cambridge dictionary of science and technology[剑桥科技词典](walker编著,1988);the glossary of genetics[遗传学词汇],第5版,r.rieger等人(编著),斯普林格出版社(springer verlag)(1991);以及hale和marham,the harper collins dictionary of biology[哈珀科林斯生物学词典](1991)。除非另有指明,否则如本文所用的以下术语具有以下赋予它们的含义。
[0043]
如本文所用的,术语“包含(comprise)”和“包括(include)”及其变体(例如,“包含(comprises/comprising)”、“包括(includes/including)”)应理解为表示包括陈述的组分、特征、元素或步骤,或一组组分、特征、元素或步骤,但不排除任何其他组分、特征、元素或步骤,或一组组分、特征、元素或步骤。术语“包含”、“基本上由......组成”和“由......组成”中的任何一个可以用其他两个术语中的任一个替换,同时保留其普通含义。
[0044]
除非上下文另有明确指明,否则如本文所用的单数形式“一个/种(a/an)”和“该”包括复数指示物。
[0045]
本文披露的百分比可以与披露的值相差
±
10%、20%或30%的量,并且仍在预期披露的范围内。
[0046]
除非另作说明或另外从上下文和本领域的普通技术人员所理解的明显可见,在本披露的不同实施例中表示为范围的本文的值可以采取所陈述范围内的任何具体值或子范
围,至该范围的下限单位的十分之一,除非上下文另外明确指明。
[0047]
如本文所用的,范围和量可表示为“约”某个特定值或范围。术语“约”还包括该精确量。例如,“约5%”意指“约5%”并且也指“5%”。术语“约”还可以指给定值或值的范围的
±
10%。因此,例如,约5%也指4.5%-5.5%。除非另外从上下文显而易见,本文提供的所有数值被该术语“约”修饰。
[0048]
如本文所用的,术语“或”和“和/或”可描述彼此组合或排斥的多个组分。例如,“x、y、和/或z”可指单独的“x”、单独的“y”、单独的“z”、“x、y、和z”、“(x和y)或z”、“x或(y和z)”、或“x或y或z”。
[0049]
如本文所用的,术语“多肽”是指由通过酰胺键(也称为肽键)线性连接的单体(氨基酸)构成的分子。术语“多肽”指两个或更多个氨基酸的任何一条链或多条链。因此,肽、二肽、三肽、寡肽、“蛋白质”、“氨基酸链”或用于指具有两个或更多个氨基酸的一条链或多条链的任何其他术语被包括在“多肽”的定义中,并且术语“多肽”可以代替这些术语中的任何一个、或可与其互换使用。
[0050]
如本文所用的,“蛋白质”可指单个多肽,即,如上所定义的单个氨基酸链,而且还可以指相关联的两个或更多个多肽,例如,通过二硫键、氢键、或疏水相互作用来产生多聚体蛋白。
[0051]“分离的”物质,例如分离的核酸,是不在其天然环境中的物质,尽管该分离的物质不一定是纯化的。例如,分离的核酸是不会产生于或位于其天然或自然环境(如细胞)中的核酸。分离的物质可以通过任何合适的技术分离、分馏、或至少部分纯化。
[0052]
如本文所用的,术语“抗体”和“其抗原结合片段”是指能够结合至抗体靶向的指定抗原的抗体的至少最小部分,例如在由b细胞产生的典型抗体的上下文中,重链(vh)的可变结构域和轻链(vl)的可变结构域的至少一些互补决定区(cdr)。抗体或其抗原结合片段可以是或源自多克隆抗体、单克隆抗体、人抗体、人源化抗体、或嵌合抗体、单链抗体、表位结合片段,例如,fab、fab
′
和f(ab
′
)2、fd、fv、单链fv(scfv)、单链抗体、二硫键连接的fv(sdfv)、包含单独的或与相反结构域的一部分结合的vl或vh结构域(例如,整个vl结构域以及具有一个、两个或三个cdr的部分vh结构域)的片段、以及通过fab表达文库产生的片段。scfv分子在本领域是已知的,并且描述于例如美国专利号5,892,019中。本披露涵盖的抗体分子可以是或源自免疫球蛋白分子的任何类型(例如,igg、ige、igm、igd、iga以及igy)、类别(例如,igg1、igg2、igg3、igg4、iga1以及iga2)或子类。
[0053]
如本文所用的,术语“多核苷酸”包括单个核酸以及多个核酸,并且指分离的核酸分子或构建体,例如信使rna(mrna)或质粒dna(pdna)。术语“核酸”包括任何核酸类型,如dna或rna。
[0054]
如本文所用的,术语“载体”可指引入宿主细胞的核酸分子,从而产生转化的宿主细胞。载体可包括允许其在宿主细胞中复制的核酸序列,如复制起点。载体还可以包括一种或多种可选择的标记基因和本领域已知的其他遗传元件。此处设想的特定类型的载体可以与病毒缔合或掺入病毒中,以促进细胞转化。
[0055]“转化的”细胞或“宿主”细胞是已经通过分子生物学技术将核酸分子引入的细胞。本文考虑了可将核酸分子引入这样的细胞的所有技术,这些技术包括用病毒载体转染,用质粒载体转化,以及通过电穿孔、脂转染、和粒子枪加速引入裸dna。
[0056]
如本文所用的,术语“亲和力(affinity)”指抗原或靶标(如表位)与其同源结合结构域(如互补位)的结合强度的量度。如本文所用的,术语“亲合力(avidity)”指表位与互补位(即抗原与抗原结合结构域)的群体之间的复合物的总体稳定性。
[0057]
如本文所用的,当在治疗癌症的上下文中使用时,术语“治疗(treat/treatment/treatment of)”指减轻疾病病理、减轻或消除疾病症状、促进存活率提高、和/或减轻不适。例如,治疗可以是指当向受试者施用疗法时该疗法减少疾病症状、体征或病因的能力。治疗还指缓和或减少至少一种临床症状和/或抑制或延迟病症的进展和/或预防或延迟疾病或疾患的发作。
[0058]
如本文所用的,术语“受试者”、“个体”或“患者”指希望诊断、预后或治疗的任何受试者,特别是哺乳动物受试者。哺乳动物受试者包括例如人、非人灵长类动物、狗、猫、豚鼠、兔子、大鼠、小鼠、马、牛、熊等。
[0059]
如本文所用的,术语施用的治疗性物质(如car t细胞)的“有效量”或“治疗有效量”是足以进行特别说明或预期目的,如治疗癌症的量。“有效量”可以根据所述目的凭经验以常规方式确定。
[0060]
2.综述
[0061]
本披露涉及使用嵌合抗原受体(car)细胞疗法来治疗癌症的组合物和方法。更特别地,本披露涉及car细胞疗法,其中转化的细胞(如t细胞)表达例如靶向磷脂酰肌醇蛋白聚糖-3(gpc3)的car。本文披露的car构建体、表达这些构建体的转化的细胞、以及利用这些转化的细胞的疗法可提供稳健的癌症治疗,该癌症治疗具有细胞因子释放综合征(crs)或在非gpc3表达细胞中不加选择的细胞因子释放的最小化的风险。
[0062]
不希望受理论的束缚,gpc3被认为是以多种形态可行的癌症靶标,这些形态包括双特异性t细胞接合子、car细胞、以及单克隆抗体和抗体-药物缀合物(adc)。gpc3是一种癌胚抗原,是gpi连接的硫酸肝素蛋白聚糖。gpc3稳定wnt-fzd相互作用,从而刺激wnt信号传导。gpc3与patched竞争对hh的结合,这缓解了smoothened抑制并诱导gpc3降解。这两种途径均显示刺激肝细胞癌(hcc)生长。并且,gpc3表达水平显示与hcc的分期和分级相关。
[0063]
此外,据信gpc3是car细胞疗法的有希望的靶标。因此,已经如本文所述开发了抗体和源自这些抗体的car构建体。
[0064]
本披露的另外的方面包括car t细胞,如靶向gpc3的那些以及用hif1αdn装甲以保护car t细胞免受与例如实体瘤的缺氧肿瘤微环境(tme)相关的免疫抑制的其他那些。
[0065]
3.car构建体设计
[0066]
本披露的car构建体可具有几种组分,其中许多组分可以基于所得car构建体的希望的或精确的功能来选择。除了抗原结合结构域,car构建体还可具有间隔子结构域、铰链结构域、信号肽结构域、跨膜结构域、以及一种或多种共刺激结构域。选择一种组分而不是另一种(即选择来自一种受体的特定共刺激结构域,相对于来自不同受体的共刺激结构域)可影响临床疗效和安全特性。
[0067]
4.抗原结合结构域
[0068]
本文预期的抗原结合结构域可包括抗体或其一个或多个抗原结合片段。一种预期的靶向gpc3的car构建体包含单链可变片段(scfv),该scfv含有来自对gpc3具有特异性的一种或多种抗体的轻链和重链可变区,这些可变区直接连接在一起或经柔性接头(例如,具
有1、2、3或更多个重复序列的ggggs的重复序列)连接在一起。
[0069]
如本文披露的car的抗原结合结构域对靶蛋白的结合亲和力可以变化。与抗体(通常希望这些抗体具有更高亲和力)相比,在car的上下文中,结合亲和力与疗效之间的关系可能更细微。例如,当与低亲和力的变体相比时,对源自高亲和力scfv(具有0.56nm的解离常数)的受体酪氨酸激酶样孤儿受体1(ror1)-car的临床前研究导致治疗指数增加。相反地,已经报道了其他实例,其中,针对较低亲和力而工程化scfv改善了具有不同抗原密度的细胞之间的区别。这可用于提高肿瘤组织与正常组织上差异表达的抗原的治疗特异性。
[0070]
可以使用多种方法确定抗原结合结构域的结合亲和力。在一些实施例中,可以使用排除亲合力作用的方法。亲合力作用涉及与多个靶表位同时相互作用的多个抗原结合位点,通常涉及多聚结构。因此,亲合力在功能上代表多种相互作用的累积强度。排除亲合力作用的方法的一个实例是其中相互作用蛋白质的一种或两种是单体的/单价的任何方法,因为如果一个或两个配偶体仅含有单个相互作用位点,则多个同时相互作用是不可能的。
[0071]
5.间隔子结构域
[0072]
本披露的car构建体可具有间隔子结构域,以提供构象自由度,从而促进与靶细胞上的靶抗原结合。间隔子结构域的最佳长度可以取决于结合表位与靶细胞表面的接近度。例如,近端表位可能需要较长间隔子,而远端表位可能需要较短间隔子。除了促进car与靶抗原的结合以外,实现car细胞与癌细胞之间的最佳距离还可以有助于空间上阻塞大抑制分子进入car细胞和靶癌细胞之间形成的免疫突触。car可具有长间隔子、中等间隔子或较短间隔子。长间隔子可包括免疫球蛋白g1(igg1)或igg4(天然的,或具有治疗性抗体中常见的修饰,如s228p突变)的ch2ch3结构域(约220个氨基酸),而ch3区可单独用于构建中等间隔子(约120个氨基酸)。较短间隔子可源自cd28、cd8α、cd3或cd4的区段(<60个氨基酸)。短间隔子也可源自igg分子的铰链区。这些铰链区可源自任何igg同种型,并且可以含有或可以不含有在治疗性抗体中常见的突变,如以上提及的s228p突变。
[0073]
6.铰链结构域
[0074]
car也可具有铰链结构域。柔性铰链结构域是提供构象自由度以促进与肿瘤细胞上的靶抗原结合的短肽片段。它可单独使用或与间隔子序列结合使用。术语“铰链”和“间隔子”经常可互换使用-例如,可将igg4序列视为“铰链”序列和“间隔子”序列(即,铰链/间隔子序列)。
[0075]
car可进一步包括包含信号肽的序列。信号肽的功能是促进细胞将car转移至细胞膜。实例包括igg1重链信号多肽、igκ或λ轻链信号肽、粒细胞-巨噬细胞集落刺激因子受体2(gm-csfr2或csfr2)信号肽、cd8a信号多肽、或cd33信号肽。
[0076]
7.跨膜结构域
[0077]
car可进一步包括包含跨膜结构域的序列。跨膜结构域可包括跨细胞膜的疏水α螺旋。跨膜结构域的特性没有如car构建体的其他方面一样经过细致地研究,但其可潜在地影响car表达并且与内源性膜蛋白的缔合。跨膜结构域可源自例如cd4、cd8α、或cd28。
[0078]
8.共刺激结构域
[0079]
car可进一步包括形成共刺激结构域的一个或多个序列。共刺激结构域是能够增强或调节免疫效应细胞的反应的结构域。共刺激结构域可包括例如来自cd3ξ(或cd3z)、cd28、4-1bb、ox-40、icos、cd27、gitr、cd2、il-2rβ和myd88/cd40中的一种或多种的序列。共
a1、mage-a3、mage-a4、间皮素(msln)、muc1、muc16、ny-eso-1、wt1、pdl1、caix、cd70、psma、和psca。本文还预期了其他细胞表面抗原。
[0090]
在一些实施例中,本披露提供了一种分离的核酸序列,该分离的核酸序列编码嵌合抗原受体(car),该嵌合抗原受体包含对磷脂酰肌醇蛋白聚糖3(gpc3)具有特异性的抗原结合结构域。抗原结合结构域具有约100纳摩尔(nm)或更少的平衡解离常数(kd),并且car构建体不诱导gpc3-细胞中细胞因子的产生。在一些实施例中,抗原结合结构域包括抗体或其抗原结合片段。抗原结合结构域可以是fab或单链可变片段(scfv)。在一些实施例中,抗原结合结构域是包含seq id no:33或seq id no:34的核酸序列的scfv。
[0091]
在一些实施例中,car进一步包括跨膜结构域、共刺激结构域、和信号结构域。跨膜结构域可以是cd28跨膜结构域。共刺激结构域可以是cd3ζ(或cd3z)、cd28、4-1bb、ox-40、icos、cd27、gitr、cd2、il-2rβ和myd88/cd40共刺激结构域中的一个或多个。在一个特定的实施例中,共刺激结构域是cd28、4-1bb、和cd3ζ共刺激结构域中的一个或多个。信号结构域可以是编码csfr2信号肽的序列。
[0092]
在一些实施例中,分离的核酸序列可包括铰链/间隔子结构域。铰链/间隔子结构域可以是igg4p铰链/间隔子。
[0093]
在一些特定的实施例中,编码嵌合抗原受体(car)的分离的核酸序列可具有seq id no:11、seq id no:12、seq id no:13、seq id no:14、seq id no:15、seq id no:16、seq id no:17、seq id no:18、或seq id no:26的序列。
[0094]
在其他实施例中,本披露提供了一种包括抗原结合结构域的抗gpc3嵌合抗原受体(car)。抗原结合结构域可以是包含重链可变区(vh)和轻链可变区(vl)的抗体、fab、或scfv。在一些实施例中,vh可具有含有seq id no:37的氨基酸序列的cdr1、含有seq id no:38的氨基酸序列的cdr2、以及含有seq id no:39的氨基酸序列的cdr3。在一些实施例中,vl可具有含有seq id no:40或seq id no:43的氨基酸序列的cdr1、含有seq id no:41或seq id no:44的氨基酸序列的cdr2、以及含有seq id no:42或seq id no:45的氨基酸序列的cdr3。
[0095]
在一些实施例中,vh可以是seq id no:27或seq id no:29的氨基酸序列,并且vl可以是seq id no:28或seq id no:30的氨基酸序列。在一些实施例中,car可进一步具有跨膜结构域、共刺激结构域、和信号结构域。
[0096]
在一些特定的实施例中,抗gpc3 car可具有seq id no:3、seq id no:4、seq id no:5、seq id no:6、seq id no:7、seq id no:8、seq id no:9、seq id no:10、或seq id no:25的氨基酸序列。
[0097]
在其他实施例中,本披露提供了一种包含编码嵌合抗原受体(car)的核酸序列的载体。核酸序列可以是seq id no:11、seq id no:12、seq id no:13、seq id no:14、seq id no:15、seq id no:16、seq id no:17、seq id no:18、seq id no:26、seq id no:33、或seq id no:34。
[0098]
在其他实施例中,本披露提供了一种包含载体的细胞,该载体具有seq id no:11、seq id no:12、seq id no:13、seq id no:14、seq id no:15、seq id no:16、seq id no:17、seq id no:18、seq id no:26、seq id no:33、或seq id no:34的核酸序列。
[0099]
在其他实施例中,本披露提供了一种细胞,该细胞具有编码嵌合抗原受体(car)的
核酸序列,其中该car包含对磷脂酰肌醇蛋白聚糖3(gpc3)具有特异性的抗原结合结构域,其中该抗原结合结构域具有约100纳摩尔(nm)或更少的平衡解离常数(kd),并且其中该car构建体不诱导gpc3-细胞中细胞因子的产生。例如,核酸序列可以是seq id no:11、seq id no:12、seq id no:13、seq id no:14、seq id no:15、seq id no:16、seq id no:17、seq id no:18、seq id no:26、seq id no:33、或seq id no:34。
[0100]
在其他实施例中,本披露提供了一种细胞,该细胞在其细胞外表面上表达抗gpc3嵌合抗原受体(car)。car可具有抗原结合结构域,该抗原结合结构域可以是各自具有重链可变区(vh)和轻链可变区(vl)的抗体、fab、或scfv。vh可包括含有seq id no:37的氨基酸序列的cdr1、含有seq id no:38的氨基酸序列的cdr2、以及含有seq id no:39的氨基酸序列的cdr3。vl可包括含有seq id no:40或seq id no:43的氨基酸序列的cdr1、含有seq id no:41或seq id no:44的氨基酸序列的cdr2、以及含有seq id no:42或seq id no:45的氨基酸序列的cdr3。
[0101]
在一些实施例中,vh可具有seq id no:27或seq id no:29的氨基酸序列。在一些实施例中,vl可具有seq id no:28或seq id no:30的氨基酸序列。car可进一步包括跨膜结构域、共刺激结构域、和信号结构域。该细胞表达car,该car具有seq id no:3、seq id no:4、seq id no:5、seq id no:6、seq id no:7、seq id no:8、seq id no:9、seq id no:10、或seq id no:25的氨基酸序列。
[0102]
在一些实施例中,本披露提供了在其细胞外表面上表达car的t细胞、自然杀伤(nk)细胞、细胞毒性t淋巴细胞(ctl)、和/或调节性t细胞,并且该car可具有seq id no:3、seq id no:4、seq id no:5、seq id no:6、seq id no:7、seq id no:8、seq id no:9、seq id no:10、或seq id no:25的氨基酸序列。这样的细胞可在与表达gpc3的肿瘤细胞接触后表现出抗肿瘤免疫。
[0103]
13.用car治疗癌症
[0104]
在一些实施例中,本披露提供了用于治疗癌症的car细胞。具有本文所述用途的组合物(例如,抗体、car构建体、和car细胞)和方法尤其可用于抑制赘生性细胞的生长或扩散。在一些方面,它们特别可用于抑制其中gpc3发挥作用的赘生性细胞的生长。
[0105]
可通过本披露的组合物治疗的赘生物包括实体瘤,例如,肝、肺或卵巢的实体瘤。然而,本文列出的癌症不旨在进行限制。例如,预期用于本文的治疗的癌症类型包括例如nsclc、晚期实体恶性肿瘤、胆道肿瘤、膀胱癌、结直肠癌、弥漫性大b细胞淋巴瘤、食管肿瘤、食道鳞状细胞癌、广泛期小细胞肺癌、胃腺癌、胃癌、胃食管连接部癌、头颈癌、头颈部鳞状细胞癌(head and neck squamous cell carcinoma)、肝细胞癌、霍奇金淋巴瘤、肺癌、黑素瘤、间皮瘤、转移性肾透明细胞癌、转移性黑素瘤、转移性非皮肤黑素瘤、多发性骨髓瘤、鼻咽肿瘤、非霍奇金淋巴瘤、卵巢癌、输卵管癌、腹膜肿瘤、胸膜间皮瘤、前列腺肿瘤、复发性或转移性pd-l1阳性或阴性scchn、复发性鳞状细胞肺癌、肾细胞癌(renal cell cancer/renal cell carcinoma)、scchn、下咽鳞状细胞癌、喉鳞状细胞癌、小细胞肺癌、头颈部鳞状细胞癌(squamous cell carcinoma of the head and neck)、鳞状细胞肺癌、tnbc、移行细胞癌、不可切除性或转移性黑素瘤、尿路上皮癌(urothelial cancer/urothelial carcinoma)。
[0106]
在一个实施例中,此处预期用于治疗的癌症包括在癌细胞的细胞表面上表达gpc3
的任何癌症。在一个特定的实例中,预期用于本文的治疗的癌症包括肝细胞癌、非小细胞肺癌、卵巢癌和鳞状细胞肺癌。
[0107]
14.装甲
[0108]
在一些实施例中,本披露提供了“装甲的”细胞,如car t细胞,其具有通过保护细胞免受环境损害(如免疫抑制性细胞因子或免疫抑制性tme)来增强或优化细胞功能的一种或多种遗传修饰。遗传修饰包括但不限于细胞因子的分泌增加,与免疫细胞(如t细胞、巨噬细胞和调节性t细胞)相互作用的配体的表达,或功能特性的改变。本领域技术人员将理解,对细胞(如t细胞)进行装甲可以提供本文未描述的许多另外的益处,这些益处允许t细胞在免疫抑制性tme中存活。
[0109]
在一些实施例中,细胞可以包括含有肿瘤特异性抗原结合结构域的嵌合抗原受体(car),其中该抗原结合结构域包含含有重链可变区(vh)和轻链可变区(vl)的抗体、fab、或scfv;和缺氧诱导因子1α(hif-1α)显性负性(hif1αdn)装甲分子。
[0110]
在一些实施例中,装甲的细胞可以包括编码嵌合抗原受体(car)的核酸序列,其中该car包含对磷脂酰肌醇蛋白聚糖3(gpc3)具有特异性的抗原结合结构域,其中该抗原结合结构域具有约100纳摩尔(nm)或更少的平衡解离常数(kd),并且其中该car构建体不诱导gpc3-细胞中细胞因子的产生,并且其中该细胞表达hif1αdn装甲分子。
[0111]
在一些实施例中,装甲的细胞可以包括包含抗原结合结构域的抗gpc3嵌合抗原受体(car),其中该抗原结合结构域包含含有重链可变区(vh)和轻链可变区(vl)的抗体、fab、或scfv,其中该vh包含含有seq id no:37的氨基酸序列的cdr1、含有seq id no:38的氨基酸序列的cdr2、以及含有seq id no:39的氨基酸序列的cdr3,并且其中该vl包含含有seq id no:40或seq id no:43的氨基酸序列的cdr1、含有seq id no:41或seq id no:44的氨基酸序列的cdr2、以及含有seq id no:42或seq id no:45的氨基酸序列的cdr3;hif1αdn装甲分子。
[0112]
15.治疗方法
[0113]
本发明的car修饰的细胞(如car t细胞)可单独施用或作为具有稀释剂和/或与细胞因子或细胞群体缔合的其他组分的药物组合物施用。简言之,本发明的药物组合物可包括例如如本文所述的car t细胞、以及一种或多种药学上或生理学上可接受的载体、稀释剂或赋形剂。这样的组合物可以包含缓冲液,如中性缓冲盐水、缓冲盐水等;硫酸盐;碳水化合物,如葡萄糖、甘露糖、蔗糖或右旋糖酐、甘露醇;蛋白质、多肽或氨基酸,如甘氨酸;抗氧化剂;螯合剂,如edta或谷胱甘肽;辅助剂(例如氢氧化铝);以及防腐剂。本发明的药物组合物可适于治疗(或预防)。
[0114]
还可以将car修饰的细胞与一种或多种另外的疗法结合施用。在一个实施例中,另外的疗法可包括抗细胞因子抗体。例如,一种或多种抗tnfα可被用于在较高的car t剂量(其可能与crs样症状和体重减轻相关)下减弱毒性并促进抗肿瘤活性。
[0115]
每剂量施用的car细胞的数目、剂量的数目和给药频率将取决于不同的参数,如患者的年龄、体重、临床评价、肿瘤类型、肿瘤负荷和/或其他因素(包括主治医生的判断)。考虑任何可接受的施用途径,例如但不限于静脉内施用(例如静脉内输注)、肠胃外或皮下施用途径。
[0116]
在一个特定实施例中,预期的治疗方案可包括一种或多种生物组分,如car t细胞
和抗癌症抗体和/或化学治疗组分。例如,预期治疗方案可另外包括免疫检查点抑制剂(ici),如靶向pd-1/pd-l1轴(pdx)的免疫检查点抑制剂,以及其他免疫肿瘤学(io)治疗,如免疫系统激动剂。
[0117]
预期的抗体包括抗pd-l1抗体(如度伐鲁单抗(durvalumab)(medi4736)、阿维鲁单抗(avelumab)、阿特珠单抗(atezolizumab)、kno35),抗pd-1抗体(如纳武单抗(nivolumab)、派姆单抗、regn2810、shr1210、ibi308、pdr001、抗pd-1、bgb-a317、bcd-100、和js001),以及抗ctla4抗体(如曲美木单抗(tremelimumab)或伊匹单抗(ipilimumab))。本文还预期了另外的抗体。本文还预期了任何治疗有效的抗体子部分。
[0118]
关于用于本文提供的方法中的度伐鲁单抗(或其片段)的信息可以见于美国专利号8,779,108;9,493,565;和10,400,039中,将其披露内容通过引用以其全文并入本文。在一个特定的方面,用于本文提供的方法中的度伐鲁单抗或其抗原结合片段包含如在前述美国专利中披露的2.14h9opt抗体的可变重链和可变轻链cdr序列。
[0119]
关于用于本文提供的方法中的曲美木单抗(或其抗原结合片段)的信息可以见于美国专利号6,682,736(其中曲美木单抗被称为11.2.1)中,将其披露内容通过引用以其全文并入本文。
[0120]
本文预期的另外的治疗剂(化疗剂或生物制剂)包括但不限于顺铂/吉西他滨(gemcitabine)或甲氨蝶呤(methotrexate)、长春花碱(vinblastine)、adriamycin
tm
(阿霉素(doxorubicin))、顺铂(mvac)、基于卡铂的方案、或单剂紫杉烷(taxane)或吉西他滨、替莫唑胺(temozolomide)、或达卡巴嗪(dacarbazine)、长春氟宁(vinflunine)、多西他赛(docetaxel)、紫杉醇(paclitaxel)、白蛋白结合紫杉醇(nab-paclitaxel)、维莫非尼(vemurafenib)、厄洛替尼(erlotinib)、阿法替尼(afatinib)、西妥昔单抗(cetuximab)、贝伐单抗(bevacizumab)、厄洛替尼(erlotinib)、吉非替尼(gefitinib)、和/或培美曲塞(pemetrexed)。另外的实例包括靶向dna损伤修复系统的药物,如聚(adp-核糖)聚合酶1(parp1)抑制剂以及抑制wee1蛋白激酶活性、atr蛋白激酶活性、atm蛋白激酶活性、极光蛋白激酶b活性、和dna-pk活性的治疗剂。
[0121]
可以将本文预期的任何治疗性组合物或方法与本文提供的任何其他治疗性组合物和方法中的一种或多种进行组合。
[0122]
在一些实施例中,本披露提供了一种治疗癌症的方法,该方法包括向有需要的受试者施用有效量的细胞,该细胞包含含有抗原结合结构域的抗gpc3嵌合抗原受体(car)以及在肿瘤微环境中的细胞表面上表达时抵抗对该细胞的免疫抑制的装甲分子。在另一方面,本披露描述了抗原结合结构域,该抗原结合结构域可以是包含重链可变区(vh)和轻链可变区(vl)的抗体、fab、或scfv。vh可包括含有seq id no:37的氨基酸序列的cdr1、含有seq id no:38的氨基酸序列的cdr2、以及含有seq id no:39的氨基酸序列的cdr3。vl可包括含有seq id no:40或seq id no:43的氨基酸序列的cdr1、含有seq id no:41或seq id no:44的氨基酸序列的cdr2、以及含有seq id no:42或seq id no:45的氨基酸序列的cdr3。在一些实施例中,该方法进一步抑制肿瘤生长、诱导肿瘤消退、和/或延长受试者的存活。
[0123]
在一些实施例中,该装甲分子是hif1αdn。
[0124]
在一些实施例中,该细胞是自体细胞。例如,该自体细胞可以选自由以下组成的组:t细胞、自然杀伤(nk)细胞、细胞毒性t淋巴细胞(ctl)、和调节性t细胞。
[0125]
在一些实施例中,通过该方法治疗的癌症是实体瘤。例如,癌症可以是肝细胞癌、非小细胞肺癌、卵巢癌、和/或鳞状细胞肺癌。在一个特定的实施例中,癌症是肝细胞癌。
[0126]
应理解,本文所述的说明书的特定方面不限于呈现的特定实施例,并且可以变化。还应理解的是,本文使用的术语仅用于描述特定方面的目的,并且并不旨在进行限制,除非本文特别定义。此外,如技术人员将认识到的,本文披露的特定实施例可与本文披露的其他实施例结合而不受限制。
[0127]
实例
[0128]
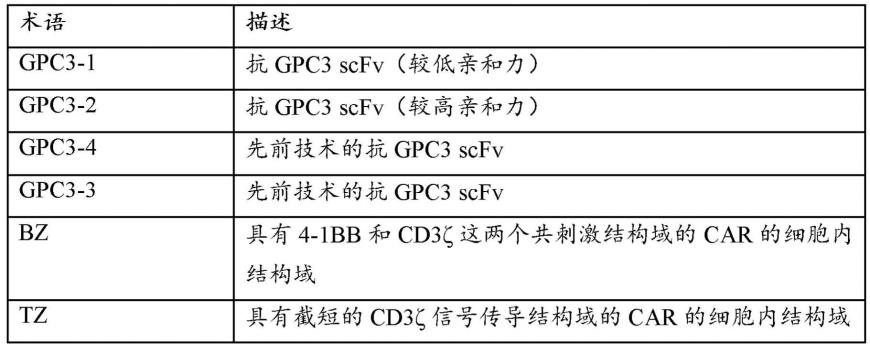
以下实例说明了本披露的特定实施例及其各种用途。阐述它们仅出于解释目的并且不应以任何方式解释为限制本披露的范围。表1提供了术语的描述。
[0129]
表1.术语的描述
[0130][0131]
[0132]
实例1:用hif1αdn对gpc3 car t细胞进行装甲
[0133]
产生分化程度较低细胞
[0134]
概要
[0135]
在本实例中,将用显性负性hif-1α(hif1αdn)分子装甲gpc3bz car t细胞作为保护car t细胞免受缺氧相关的免疫抑制以改善car t效应子功能和肿瘤控制的潜在方法进行调查。
[0136]
方法
[0137]
图1.hif1αdn:通过在n末端和c末端截短野生型hif1α蛋白使得该蛋白质缺少dna结合结构域、氧依赖性降解结构域和反式激活结构域来制备显性负性hif-1α分子。(chen j,zhao s,nakada k,等人dominant-negative hypoxia-inducible factor-1 alpha reduces tumorigenicity of pancreatic cancer cells through the suppression of glucose metabolism[显性负性缺氧诱导因子-1α通过抑制葡萄糖代谢降低胰腺癌细胞的致瘤性].am j pathol[美国病理学杂志].2003;162(4):1283-1291.doi:10.1016/s0002-9440(10)63924-7)。截短的hif1αdn序列(seq id no:49)对应于野生型hif1α序列的残基30-389。装甲的car t细胞:通过将hif1αdn表达为与gpc3 bz car的c末端融合物(其中t2a肽分隔gpc3 bz car和hif1αdn)来用hif1αdn装甲gpc3 bz car t细胞。在hif1αdn装甲的gpc3bz car-t构建体中,cd33信号肽用于指导car的分泌,并且car被n末端ha表位标签修饰以促进检测细胞表面上的car表达。
[0138]
图2.t细胞是未转导的(ut)或用gpc3-1或gpc3-1hif1αdn构建体转导,并在常氧(20%o2)或缺氧(1%o2)条件下扩增11天。图2a和2c.按照制造商的说明用rneasy微型试剂盒(凯杰公司(qiagen))从冷冻沉淀中提取mrna并逆转录为cdna。通过实时pcr扩增内源性或显性负性hif1α,并表示为通过比较c(t)方法计算的倍数诱导(schmittgen td,livak kj.analyzing real-time pcr data by the comparative c(t)method[通过比较c(t)方法分析实时pcr数据].natprotoc[自然-实验室指南].2008;3(6):1101-1108)。图2b.通过蛋白质印迹检测内源性hif1α的表达。如图2a和2c所述扩增细胞并在含有蛋白酶和磷酸酶抑制剂的ripa缓冲液中裂解。
[0139]
图3.在转导后7天,通过流式细胞术分析在常氧(20%o2)或缺氧(1%o2)下扩增的ut、gpc3-1或gpc3-1hif1αdn car-t细胞的表面上cd62l
低
cd45ro
高
t效应记忆细胞的频率。
[0140]
图4.将ut、gpc3-1或gpc3-1hif1adn car-t在常氧条件下扩增11天。用rneasy微型试剂盒(凯杰公司)从冷冻细胞沉淀中提取细胞mrna。按照制造商的说明用nanostring car-t表征面板进行基因表达分析。图将基因表达描绘为相对于ut的log2倍数变化。
[0141]
图5.将gpc3-car修饰的t细胞产物重悬于无血清的未缓冲的dmem培养基中,该培养基补充有l-谷氨酰胺(200mm)和nacl(143mm)用于糖酵解应激试验或补充有d-葡萄糖(25mm)和丙酮酸钠(1mm)用于线粒体应激试验。然后将细胞铺在seahorse细胞板上(1
×
106个细胞/孔),用cell-tak(康宁公司(corning))包被以促进t细胞附着。糖酵解应激试验通过在稳态下和在依次注射抗cd3/cd28珠(细胞与珠的比率为1∶1),随后注射d-葡萄糖(10mm)后测量ecar(mph/min)来进行。线粒体应激试验通过在稳态下和在依次注射抗cd3/cd28珠(细胞与珠的比率为1∶1),随后注射寡霉素(0.5μm)后测量ocr(pmol/min)来进行。使用seahorse系统的实验采用以下测定条件:2分钟混合;2分钟等待;和3分钟测量。
[0142]
结果
[0143]
通过实时pcr证实显性负性hif1α的表达,而通过蛋白质印迹研究内源性hif1α的表达。与内源性hif1α相比,显性负性hif1a过表达。此外,dn的表达不改变通过蛋白质印迹检测的缺氧诱导的内源性hif1α的稳定(图2)。
[0144]
肿瘤微环境中的t细胞适应性和持久性与其分化状态有关(kishton,r.j.,sukumar,m.,和restifo,n.p.(2017).metabolic regulation of t cell longevity and function in tumor immunotherapy[肿瘤免疫疗法中t细胞寿命和功能的代谢调节].cell metab[细胞代谢],26(1),94-109.)。为了研究hif1αdn表达对t细胞分化的影响,我们分析了常氧(20%o2)或缺氧(1%o2)扩增6天后gpc3-1或gpc3-1hif1αdn car-t中cd62l
低
cd45ro
高
t效应记忆细胞的频率。gpc3-1hif1αdn保持了分化程度较低的表型,如通过与未装甲的car-t相比在缺氧和常氧条件下t
em
频率的降低判断的(参见图3)。值得注意的是,在缺氧下扩增的细胞比在常氧下扩增的细胞的分化程度更高,然而即使在这种条件下,hif1αdn的表达也赋予了类似于ut t细胞的分化程度较低的表型。
[0145]
hif1α不仅是缺氧反应的主要调节因子,也是常氧下t细胞激活的关键中间物,并且与多种信号转导和代谢途径的调节有关。为了全面了解由hif1αdn的表达诱导的遗传变化,我们对在常氧(20%o2)条件下扩增的纯化的gpc3-1或gpc3-1hif1αdn car-t进行了nanostring分析。与未装甲的car t细胞相比,hif1αdn car t细胞具有与干性相关的基因的增加的表达和效应子功能相关的基因的减少的表达。因此,该结果证实hif1αdn的表达与激活和分化程度较低的表型相关(参见图4)。
[0146]
静息t细胞利用能量有效的氧化代谢,但当刺激生长时或在病原体接触后转换为高度糖酵解代谢(michalek,r.d.,和rathmell,j.c.(2010).the metabolic life and times of a t-cell[t细胞的代谢寿命和时间].immunol rev[免疫学评论],236,190-202.)。为了研究hif1αdn表达对car-t细胞代谢状态的影响,我们通过在基础条件下和抗原暴露后的实时活细胞分析(seahorse xf),在耗氧率(ocr)的基础上分析细胞外酸化率(ecar)和线粒体氧化磷酸化来评估糖酵解。在基础条件下,hif1αdn car t细胞表现出较低的ocr和较高的ecar,表明它们更容易糖酵解。相比之下,在抗原暴露后,hif1αdn获得60%的ocr,而未装甲的只有20%。相反,未装甲的ecar激活后的增益为340%,而装甲的car-t仅为100%。因此,hif1αdn的表达恢复细胞代谢并赋予car-t响应于应激下增加的能量需求的能力(参见图5)。
[0147]
结论
[0148]
用于产生抗癌免疫反应的t细胞的特征是决定临床结果的关键因素。特别地,使用具有细胞寿命延长特征的t细胞治疗癌症与改善的抗肿瘤反应相关(kishton,r.j.,sukumar,m.,和restifo,n.p.(2017).metabolic regulation of t cell longevity and function in tumor immunotherapy[肿瘤免疫疗法中t细胞寿命和功能的代谢调节].cell metab[细胞代谢],26(1),94-109)。缺氧和hif信号传导途径影响免疫细胞的命运和功能,包括糖酵解基因表达的上调。因此,缺氧驱动细胞朝向分化程度更高的状态,这与肿瘤中短暂的持久性和不良结果相关。(kishton,r.j.,sukumar,m.,和restifo,n.p.(2017).metabolic regulation of t cell longevity and function in tumor immunotherapy[肿瘤免疫疗法中t细胞寿命和功能的代谢调节].cell metab[细胞代谢],26(1),94-109.;
krzywinska,e.,和stockmann,c.(2018).hypoxia,metabolism and immune cell function[缺氧、代谢和免疫细胞功能].biomedicines[生物医学],6(2))。我们的数据表明,与未装甲的car t细胞相比,表达hif1αdn的car-t保持幼稚且激活程度较低的表型,如通过表面标记、基因表达和线粒体功能的分析所显示的。这些观察结果表明,hif1αdn car t细胞很好地适应于耐受与实体瘤的严重缺氧tme相关的免疫抑制性作用。
[0149]
实例2hif1αdn car t细胞在靶标暴露后的功能反应
[0150]
概要
[0151]
在本实例中,在与暴露于靶抗原gpc3相关的hif1αdn car t细胞中测定脱粒、细胞毒性、效应细胞因子产生、离体杀伤和增殖反应。
[0152]
方法
[0153]
图6.响应于gpc3的car t细胞脱粒。将所示的car-t细胞与hep3b或a375在golgi stop和针对直接用荧光染料标记的脱粒标记cd107a的抗体存在下共培养6小时。靶标接合诱导car-t脱粒,并且随后结合培养基中存在的荧光标记的抗cd107。通过流式细胞术检测的cd107累积与脱粒的程度成正比,并且该累积表明了靶细胞的裂解。孵育后6小时,通过流式细胞术分析细胞。
[0154]
图7.响应于gpc3的hif1αdn car t细胞效应细胞因子产生:将5
×
104个car-t细胞与靶细胞以1∶1的比率在rpmi 10%fcs中共培养。24小时后,收集上清液并通过meso scale discovery 4-plex试剂盒分析细胞因子。
[0155]
图8.将gpc3-1或gpc3-1hif1αdn car-t在缺氧或常氧下暴露于表达gpc3的靶细胞。在pma和离子霉素存在下培养6小时后,进行gpc3-car修饰的和显性负性hif1a gpc3-car修饰的t细胞的细胞内细胞因子染色。然后将细胞用蓝色live/dead可固定染料和cd3抗体染色,随后按照制造商的方案用bd固定和透化缓冲液(ebioscience公司)固定和透化。然后随后将细胞与ifn-γ、il-2和tnf-α(ebioscience公司)抗体在4℃下一起孵育30分钟。用flowjo软件(树星公司(treestar))补偿并分析流式细胞术分析数据。使用的抗体:抗cd3(sk7)、抗il-2(mq1-17h12)、抗ifn-γ(4s.b3)、抗tnfα(mab11)购自ebioscience公司。
[0156]
图9.car-t杀伤靶表达细胞。用细胞阻抗监测技术(xcelligence)进行细胞毒性研究。将3
×
104个靶细胞铺板,并将在缺氧和常氧条件下培养的car-t细胞在24小时后以指定的效应子:靶标(e∶t)比率添加。用rtca软件pro计算细胞溶解百分比和kt80。用rtca esight(配备有活细胞成像能力的xcelligence仪器)获得图像。使用的靶细胞:hep3b:gpc3
高
;huh7:gpc3
中等
;plc-prf-15:gpc3
低
;snu-182gpc3-。
[0157]
图10.用rdca软件pro对在常氧或缺氧下按照指定的e:t比率如图9所示进行的研究计算杀伤时间80(kt)。
[0158]
图11.在与gpc3 肿瘤细胞共培养期间,car-t介导的细胞毒性的实时监测的明视场像。共培养3小时后拍摄照片。在装甲的car-t细胞存在下,细胞凋亡特征已经很清楚。上图表示不存在靶细胞时的t细胞。
[0159]
图12.用rdca软件pro对如图9所示进行的细胞毒性研究计算细胞溶解百分比。使用指定的靶细胞(huh7和plc/prf/5)。
[0160]
图13.按照制造商的说明用cfse标记car-t,并将其与指定的细胞系一起孵育。3天后,通过流式细胞术分析cfse的稀释度。
[0161]
图14.将huh7细胞植入nsg小鼠(10只小鼠/组)的侧腹中。当肿瘤达到150mm3的平均体积时,向小鼠给予700万个指定的car-t。图表示在指定时间测量的肿瘤体积。
[0162]
图15.将hep3b细胞植入nsg小鼠(9只小鼠/组)的侧腹中。当肿瘤达到150mm3的平均体积时,向小鼠给予700万个指定的car-t。图表示在指定时间测量的肿瘤体积。
[0163]
结果
[0164]
hif1αdn car t具有分化和激活程度较低的表型,因此我们想要测试它们是否能够产生有效的抗原特异性免疫反应。在常氧下扩增的gpc3-1car-t细胞在暴露于gpc3
hep3b后不久脱粒,并且如果细胞在缺氧条件下扩增,则脱粒程度略微降低。在常氧条件下扩增的hif1αdn car t细胞能够类似于未装甲的car-t而进行脱粒;然而,如果在缺氧条件下扩增,则脱粒没有减少。脱粒具有抗原特异性,如通过与snu-182一起孵育后不存在cd107
细胞所显示的。该结果表明,即使在缺氧下扩增,hif1αdn car t也可以响应于抗原接触而有效且特异性地脱粒(参见图6)。
[0165]
细胞因子分泌是t细胞激活的标志;因此,我们想要研究hif1αdn表达对抗原依赖性效应细胞因子产生的影响。与未装甲的car t细胞相比,hif1αdn car t细胞在常氧和缺氧条件下暴露于gpc3后产生较少的ifnγ和il-2,但产生相似量的tnf-α。这些数据表明,即使hif1αtdn car t具有分化程度较低的表型,它们也能以抗原依赖性方式分泌大量的效应细胞因子。参见图7。
[0166]
产生多种细胞因子的t细胞,即所谓的“多功能”t细胞,提供比仅产生单一细胞因子的细胞更有效的免疫反应。当细胞在常氧条件下暴露于抗原时,在抗原刺激后产生三种主要效应细胞因子ifn-γ
/il-2
/tnfa
的未装甲的和装甲的cd4和cd8 t细胞的频率在未装甲的和装甲的之间是相似的。缺氧下的刺激显著降低了未装甲的多功能t细胞的频率。相比之下,多功能hif1αdn car-t的频率仅受到缺氧的轻微影响(参见图8),表明hif1αdn的表达保护car-t免受缺氧驱动的免疫抑制。
[0167]
杀伤靶细胞是car-t细胞最重要的特征;因此,我们分析了gpc3hif1αdn car t杀伤表达各种水平gpc3的靶细胞的能力。hif1αdn的表达与分化程度较低的表型相关;因此,我们假设hif1αdn将比它们的未装甲的对应物持续更长时间,但也将更慢地杀伤靶细胞。出乎意料的是,hif1αdn car t细胞在常氧或缺氧条件下杀伤hep3b细胞快于未装甲的car t细胞。hep3b靶细胞在暴露于hif1αdn car t仅3小时后显示出明显且显著的细胞凋亡前外观(参见图9-11)。gpc3 hif1αdn car t杀伤具有较低gpc3表达的其他gpc3
细胞系huh7和plc-prf15的能力与未装甲的对应物相似,图12。这些结果表明,gpc3 hif1αdn car t以比未装甲的car t更快的速率杀伤表达更高水平的gpc3的细胞。
[0168]
hif1α在抗原识别后在t细胞中稳定,并且它是t细胞激活的重要介质,因此我们询问dn的表达是否导致t细胞增殖改变。使cfse标记的ut、gpc3和gpc3 hif1αdn car t细胞不受刺激或与hep3b或huh7共培养。cfse在每次细胞分裂后在子细胞内逐渐稀释,稀释度与增殖程度成正比。3天后的流式细胞术分析显示,hif1αdn car t细胞响应于表达高和低gpc3的靶细胞而与未修饰的car t细胞类似地增殖。hif1αdn的表达在抗原不存在的情况下恢复了未修饰的car t细胞的非特异性增殖,与其分化程度较低的表型一致。该结果表明,用显性负性分子的异位表达阻断hif1α途径不损害抗原诱导的car-t细胞增殖(参见图13)。
[0169]
结论
[0170]
hif1αdn car t细胞能够杀伤gpc3 癌细胞,同时保持活性较低且更幼稚的表型。此外,hif1αdn的表达部分保护了car-t细胞免于缺氧诱导的多功能性丧失。令人惊讶的是,在常氧和缺氧条件下,与未装甲的car t细胞相比,hif1αdn car t细胞在体外表现出增强的杀伤某些靶细胞的能力。这些令人惊讶的结果表明,用hif1αdn装甲car t细胞能以与提供缺氧抗性无关的方式向car t细胞提供改善的细胞溶解功效。
[0171]
实例3:hif1αdn的表达提高了car-t体内功效
[0172]
概要
[0173]
在本实例中,在两种不同的异种移植模型中,在体内测定hif1αdn装甲的car-t细胞对抗gpc3
肿瘤细胞的有效性。
[0174]
方法
[0175]
使用肝细胞癌huh7来测试hif1adn装甲的car-t细胞在减小肿瘤体积方面的体内有效性。将肿瘤细胞植入nsg小鼠(10只小鼠/组)的侧腹中。当肿瘤达到150mm3的平均体积时,向小鼠给予7
×
106个指定的car-t或700万个未转导的t细胞,并且每两周一次测量肿瘤(参见图14)。
[0176]
使用肝细胞癌hep3b来测试hif1αdn装甲的car-t细胞在减小肿瘤体积方面的体内有效性。将肿瘤细胞植入nsg小鼠(10只小鼠/组)的侧腹中。当肿瘤达到150mm3的平均体积时,向小鼠给予7
×
106个指定的car-t或700万个未转导的t细胞,并且每两周一次测量肿瘤(参见图15)。
[0177]
对给予7
×
106个car-t的携带huh7肿瘤的小鼠进行离体分析。输注后四天,从每组5只小鼠收集肿瘤。使用accuchec计数珠通过流式细胞术计算cd45 细胞的数量。(参见图16)。
[0178]
向携带hep3b肿瘤的小鼠给予7
×
106个car-t细胞。对于ifnγ分析,在car-t输注后七天以小体积收获血液并使用bd microtainer血清分离管分离血清。使用msd测定确定ifnγ水平(参见图17)。
[0179]
向携带hep3b肿瘤的小鼠给予7
×
106个car-t细胞。输注后四天,收集脾脏和肿瘤,并通过流式细胞术染色评估cd27和cd70的表达。(参见图18)。
[0180]
结果
[0181]
与它们的未装甲的对应物相比,gpc3 hif1αdn car-t细胞能够更有效地控制huh7,并且更快地诱导hep3b肿瘤消退(参见图14和15)。我们假设hif1αdn的表达赋予car-t细胞增加的浸润缺氧实体瘤的能力。t细胞输注后四天对hep3b肿瘤的分析显示在hif1αdn治疗的小鼠中t细胞的数量确实增加了2-3倍,表明hif1αdn的表达允许car-t细胞在实体瘤中更好地浸润和增殖(参见图16)。与肿瘤中细胞数量的增加一致,我们也在输注了hif1αdn装甲的gpc3 car-t的小鼠血清中检测到更多的ifn-γ。值得注意的是,尽管在肿瘤中,装甲的和未装甲的car-t细胞显示cd70 激活表型,但hif1αdn在具有na表达的脾脏中的激活程度较低。cd70与ut细胞相似。
[0182]
结论与未装甲的gpc3 car-t相比,表达hif1αdn的gpc3car-t诱导更快的肿瘤消退。肿瘤消退与细胞在肿瘤中浸润和增殖的能力的显著增加相关。此外,尽管装甲的细胞在肿瘤中被完全激活,但它们在脾脏中比未装甲的car-t表达更少的cd70,表明它们即使在体内也能保持激活程度较低的状态。总之,这些观察结果表明,通过显性负性hif1α的表达阻
断hif1α途径提高了car-t细胞体内功效,同时保持了激活和分化程度较低的表型。
[0183]
本文描述的实施例可以在不存在本文未具体披露的任何一个或多个元素、一个或多个限制的情况下实践。将已经采用的术语和表达用作描述性术语,而不是限制性的,并且不意图在使用这样的术语和表达时排除所示出和描述的特征或其部分的任何等同物,但是应当认识到,在所要求保护的实施例的范围内可以进行各种修改。因此,应当理解,尽管已经通过实施例、任选特征具体披露了本发明,但是本领域技术人员可以对本文披露的概念进行修改和变化,并且认为这样的修改和变化可以处于由说明书和所附权利要求书限定的这些实施例的范围内。尽管本披露的一些方面可被视为特别有利,但是预期本披露不限于本披露的这些特定方面。
[0184]
如果组的一个、多于一个或全部成员存在于、使用于或以其他方式相关于给出的产品或方法,则在该组的一个或多个成员之间包括“或”的权利要求或说明书被认为是满意的,除非有相反的指明或另外从上下文明显可见。本披露包括实施例,在这些实施例中,组中的恰好一个成员存在于、使用于或以其他方式相关于给出的产品或方法。本披露包括实施例,在这些实施例中,组中的多于一个或全部成员存在于、使用于或以其他方式相关于给出的产品或方法。
[0185]
此外,本披露涵盖其中将来自一个或多个所列权利要求的一个或多个限制、元素、条款和说明性术语引入另一权利要求中的所有变化、组合和排列。例如,可以对附属于另一权利要求的任何权利要求加以修改,以使其包括一个或多个在附属于同一基础权利要求的任何其他权利要求中所见的限制。在元素以列表(例如以马库什组(markush group)形式)呈现的情况下,还披露了元素的每个亚组,并且可以从该组中去除任何元素。
[0186]
应当理解,通常,在本披露或本披露的方面被称作包含特定元素和/或特征的情况下,本披露或本披露的方面的某些实施例由这样的元素和/或特征组成或基本上由其组成。出于简洁目的,这些实施例没有在本文以文字具体地陈述。
[0187]
本说明书中提及的全部专利和出版物通过引用以相同的程度并入本文,如同每份单独的专利和出版物具体地且个别地指出通过引用并入。在本技术的任何部分中的任何参考文献的引用或标识不应被解释为承认这样的参考文献可用作针对本发明的现有技术。
[0188]
表5.实例中使用的序列。
[0189]
[0190]
[0191][0192]
表6.序列
[0193]
[0194]
[0195]
[0196]
[0197]
[0198]
[0199]
[0200]
[0201]
[0202]
[0203]
[0204]
[0205]
[0206]
[0207]
[0208]
[0209]
[0210]
[0211]
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。