1.本发明涉及干细胞技术领域,具体而言,涉及一种增强间充质干细胞免疫调节能力的方法。
背景技术:
2.间充质干细胞是一类具有自我更新、高度增殖、具多向分化潜能的一类细胞,其免疫调节和再生特性在多种疾病的治疗具有良好的应用前景。脐带组织具有采集方便、无伦理学问题等特点,脐带间充质干细胞具有更强的增殖、自我更新和多项分化能力,是再生医学工程领域良好的种子细胞,逐渐成为临床研究和应用的热点。
3.脐带间充质干细胞的免疫调节能力在造血干细胞移植后急性移植物抗宿主病(acute graft-versus-host disease,agvhd)及自身免疫性相关疾病的治疗中显示良好的作用。脐带间充质干细胞可以通过细胞与细胞间的直接接触和旁分泌产生细胞因子等方式,对固有免疫系统和获得性免疫系统的多种免疫细胞进行免疫调节。脐带间充质干细胞的直接作用可作用于自然杀伤细胞、t细胞和b细胞等。脐带间充质干细胞通过旁分泌的方式产生细胞因子、趋化因子和生长因子等大量生物活性物质,调节免疫细胞,如吲哚胺2,3双加氧酶(indoleamine-2,3-dioxygenase,ido)、前列腺素e2(prostaglandin e2,pge2)、白细胞介素(il-6,il-10)、转化生长因子、肝细胞生长因子(hepatocyte growth factor,hgf)、白血病抑制因子(leukemia inhibitory factor,lif)等,形成了一个复杂的网络调控体系。
4.牙髓干细胞是间充质干细胞的一种,于牙齿内部的牙髓组织中分离出的成纤维状细胞,可自我更新及分化为硬骨、脂肪、软骨、肌肉与神经等细胞系类型。牙齿干细胞有很多种,在牙齿所发现的各种干细胞,皆有相当大的潜力,目前在牙齿已陆续发现各种不同的干细胞,包括:乳牙牙髓干细胞、恒牙牙髓干细胞、未完全发育牙根尖干细胞及牙周干细胞等。因此,目前已有乳牙银行的产生,以保留脱落的乳牙,可分离乳牙牙髓干细胞作为将来可能的应用,此外也在恒牙的牙髓中亦可找到干细胞并已证实具有转分化为牙本质母细胞,促进牙本质再生的作用以应用于治疗龋齿。
5.然而,间充质干细胞在使用前需要进行大量的体外扩增,长期传代后降低细胞的增殖和分化能力,影响免疫调节能力的发挥,不同供体来源的间充质干细胞也存在免疫调节能力的差异,因此,在体外扩增中保持或增强脐带间充质干细胞的免疫调节能力,有利于增强间充质干细胞在疾病治疗的效果。
6.目前能够提高脐带间充质干细胞的免疫调节能力的方法主要有以下几种:(1)tnfα、ifnγ、il-1α和il-1β等促炎性因子的预处理。许多研究已经证明了脐带间充质干细胞的启动与促炎细胞因子的作用有关,该策略可以增加其抗炎和免疫调节因子的分泌。(2)低氧预诱导,缺氧预处理下的间充质干细胞显示细胞活力增加,增殖潜能增强,ros产生减少,抗氧化能力增强,促血管生成能力增加。但要在促炎性因子的联合应用下,才能发挥增强免疫调节能力的作用。(3)药物或化学制剂,如组蛋白去乙酰化酶抑制剂丙戊酸(vpa)和生物活
性脂质鞘氨醇-1-磷酸(s1p)能够促进脐带间充质干细胞的增殖、迁移和炎症抑制能力。雷帕霉素的短时暴露能够上调脐带间充质干细胞的cox-2/pge2的表达,使pbmcs和脾细胞增殖减少。
7.尽管促炎性因子的预处理能有效提高脐带间充质干细胞的免疫调节作用,然而促炎性因子会上调脐带间充质干细胞i类和ii类hla分子的表达,使其免疫原性增强,容易被宿主免疫细胞识别,并快速被机体清除,尤其是在异种移植中。而且促炎性因子的预处理也会增加脐带间充质干细胞的使用安全性。缺氧预诱导虽然能提高脐带间充质干细胞的体内定植和功能,但对免疫调节能力的影响较小,需要和炎性因子预处理共同发挥作用。vpa和s1p的联合作用能促进间充质干细胞分泌炎性调节因子的能力,但对免疫细胞功能的调节能力未知。雷帕霉素主要调节间充质干细胞对pge2的分泌,而间充质干细胞的免疫调节能力是多种免疫调节因子的共同作用。
8.鉴于此,特提出本发明。
技术实现要素:
9.本发明的目的在于提供一种增强间充质干细胞免疫调节能力的方法,以克服上述技术问题。
10.本发明是这样实现的:
11.第一方面,本发明提供了一种增强间充质干细胞免疫调节能力的方法,其包括将间充质干细胞接种于含有奥替普拉的基础培养基中培养;
12.上述基础培养基包括完全培养基和无血清培养基。
13.第二方面,本发明提供了由上述方法制备获得的间充质干细胞。
14.第三方面,本发明提供了一种干细胞制剂,其包括上述的间充质干细胞。
15.第四方面,本发明提供了一种用于培养上述间充质干细胞的培养基,其由基础培养基中添加有10-20μm的奥替普拉制得;基础培养基包括完全培养基和无血清培养基。
16.本发明具有以下有益效果:
17.本发明通过将间充质干细胞接种于含有奥替普拉的完全培养基或者无血清培养基中培养,在多种免疫调节因子的分泌上均有良好的优势,也能更好的抑制免疫细胞的增殖。其中所采用的奥替普拉已经被fda批准应用于治疗非酒精性脂肪性肝病的三期临床试验,药物的安全性等方面具有较好的保证。另外,本技术的制备方法为细胞层面技术,无基因工程改造,操作简便易行,全程安全可控,细胞制剂使用风险更低。
附图说明
18.为了更清楚地说明本发明实施例的技术方案,下面将对实施例中所需要使用的附图作简单地介绍,应当理解,以下附图仅示出了本发明的某些实施例,因此不应被看作是对范围的限定,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他相关的附图。
19.图1为实施例1获得的脐带间充质干细胞分泌免疫调节因子的能力的检测结果;
20.图2为实施例2获得的牙髓干细胞分泌免疫调节因子的能力的检测结果;
21.图3为实施例3获得的脐带间充质干细胞分泌免疫调节因子的能力的检测结果;
22.图4为实施例4获得的牙髓干细胞分泌免疫调节因子的能力的检测结果;
23.图5为实施例5获得的脐带间充质干细胞分泌免疫调节因子的能力的检测结果;
24.图6为实施例6获得的牙髓干细胞分泌免疫调节因子的能力的检测结果;
25.图7为实施例1获得的脐带间充质干细胞对外周血单个核细胞增殖影响的检测结果;
26.图8为实施例2获得的牙髓干细胞对外周血单个核细胞增殖影响的检测结果;
27.图9为实施例3获得的脐带间充质干细胞对外周血单个核细胞增殖影响的检测结果;
28.图10为实施例4获得的牙髓干细胞对外周血单个核细胞增殖影响的检测结果;
29.图11为实施例5获得的脐带间充质干细胞对外周血单个核细胞增殖影响的检测结果;
30.图12为实施例6获得的牙髓干细胞对外周血单个核细胞增殖影响的检测结果;
31.图13为实验例3中ido1因子的mrna表达水平的检测结果;
32.图14为实验例3中pdl1因子的mrna表达水平的检测结果;
33.图15为对比例1中ido1和pdl1因子的mrna表达水平的检测结果;
34.图16为对比例2中ido1和pdl1因子的mrna表达水平的检测结果。
具体实施方式
35.为使本发明实施例的目的、技术方案和优点更加清楚,下面将对本发明实施例中的技术方案进行清楚、完整地描述。实施例中未注明具体条件者,按照常规条件或制造商建议的条件进行。所用试剂或仪器未注明生产厂商者,均为可以通过市售购买获得的常规产品。
36.奥替普拉(oltipraz)是一种nrf2激活剂,通过破坏keap1和nrf2之间的相互作用从而促进nrf2入核,激活下游抗氧化基因的表达。最近研究发现奥替普拉能够逆转儿童早衰症来源的间充质干细胞的衰老表型。目前已开展针对奥替普拉在治疗非酒精性脂肪性肝病、低氧性肺病和糖尿病方面的试验性研究,但是奥替普拉在增强间充质干细胞的免疫调节能力方面目前还未有公开。
37.由于现有的能够提高间充质干细胞的免疫调节能力的方法还存在使用安全性、提高程度不高等的缺陷,为了获得更加安全的免疫调节能力增强型间充质干细胞,发明人创造性地将奥替普拉添加到基础培养基中,对间充质干细胞,特别是多次传代后的间充质干细胞进行培养,获得的间充质干细胞在多种免疫调节因子的分泌上均有良好的优势,在也能更好的抑制免疫细胞的增殖。
38.基于此,本发明提供一种增强间充质干细胞免疫调节能力的方法,其包括将间充质干细胞接种于含有奥替普拉的基础培养基中培养。
39.在一些实施例中,间充质干细胞包括牙髓间充质干细胞和脐带间充质干细胞,但并不仅限于牙髓间充质干细胞和脐带间充质干细胞,还可以是骨髓间充质干细胞、脂肪间充质干细胞和滑膜间充质干细胞等。
40.在本发明中,间充质干细胞可以为多次传代后的间充质干细胞,具体为p1代、p2代、p3代、p4代或p5代间充质干细胞。
41.在一些实施例中,间充质干细胞的接种密度为5
×
10
4-6
×
104/cm2。
42.在一些实施例中,奥替普拉在基础培养基中的添加浓度为10-20μm。
43.在一些实施例中,基础培养基包括完全培养基和无血清培养基,但不仅限于完全培养基和无血清培养基,还可以是其他基础培养基,只要能够满足间充质干细胞的正常生长的培养基均可。
44.在一些实施例中,无血清培养基包括therapeak
tm mscgm-cd
tm
人间充质干细胞培养基和gibco间充质干细胞无血清培养基msc sfm,但不仅限于上述无血清培养基,还可以是其他无血清培养基,只要能够满足间充质干细胞的正常生长的培养基均可。
45.在一些实施例中,间充质干细胞在含有奥替普拉的基础培养基中培养的条件为:培养箱中温度为36.5-37.5℃,co2体积浓度为4.5-5.5%;培养时间为7-10天。
46.在一些实施例中,间充质干细胞的培养过程包括更换含有奥替普拉的基础培养基,更换频率为3-4天/次。间充质干细胞在上述培养基中培养3-4天后,细胞达到80-90%融合,此时更换培养基。
47.更换的培养基仍为含有浓度为10-20μm的奥替普拉的基础培养基。
48.以下结合实施例对本发明的特征和性能作进一步的详细描述。
49.本发明的实施例所采用的脐带间充质干细胞均为传至p3代的脐带间充质干细胞,p3代的间充质干细胞的制备方法如下:
50.(1)临床采集的脐带标本,pbs清洗,剪短,去除血管和脐带外围的羊膜组织,将剩余组织剪成直径1-2mm的小块,接种于t25培养瓶中,加入含12.5%胎牛血清的dmem/f12完全培养基,置于5%co2、37℃培养箱内继续培养。
51.(2)3-4天换新鲜培养基,观察细胞80%-90%融合时进行传代。弃培养基,加入5ml pbs清洗2次,加入1ml tryple
tm express重组胰酶替代物消化细胞,待80%的细胞回缩变圆,加入5ml完全培养基终止消化,吹打收集细胞悬液,800rpm离心3分钟,弃上清,按照1:3接种至新培养瓶中,置于5%co2、37℃培养箱内继续培养。
52.(3)传第三代细胞进行冻存。收集细胞,加入10%二甲亚砜的全血清冻存液,液氮保存。
53.本发明的实施例所采用的牙髓干细胞均为传至p3代的间充质干细胞,p3代的间充质干细胞的制备方法如下:
54.(1)新鲜采集的牙髓组织,置于10cm培养皿中,pbs清洗3次,剪成直径1-2mm的小块,接种于t25培养瓶中,加入含12.5%胎牛血清的dmem/f12完全培养基,置于5%co2、37℃培养箱内继续培养。
55.(2)3-4天换新鲜培养基,观察细胞80%-90%融合时进行传代。弃培养基,加入5ml pbs清洗2次,加入1ml tryple
tm express重组胰酶替代物消化细胞,待80%的细胞回缩变圆,加入5ml完全培养基终止消化,吹打收集细胞悬液,800rpm离心3分钟,弃上清,按照1:3接种至新培养瓶中,置于5%co2、37℃培养箱内继续培养。
56.(3)传第三代细胞进行冻存。收集细胞,加入10%二甲亚砜的全血清冻存液,液氮保存。
57.实施例1
58.本实施例提供一种增强脐带间充质干细胞免疫调节能力的方法,其步骤如下:
59.(1)细胞复苏。将p3代脐带间充质干细胞从液氮中取出,37℃水浴中快速解冻,加入含12.5%胎牛血清的dmem/f12完全培养基中,离心,800rpm离心3分钟,弃上清,用完全培养基接种培养,置于5%co2、37℃培养箱内继续培养。
60.(2)48小时后换液,用含有15μm奥替普拉(oltipraz,sm-o9389-5mg)的含12.5%胎牛血清的dmem/f12完全培养基中继续培养。
61.(3)每3天换培养基一次,更换的完全培养基中添加有15μm的奥替普拉。
62.(4)连续培养10天。
63.实施例2
64.本实施例提供一种增强牙髓干细胞免疫调节能力的方法,其步骤如下:
65.(1)细胞复苏。将p3代牙髓干细胞从液氮中取出,37℃水浴中快速解冻,加入含12.5%胎牛血清的dmem/f12完全培养基后再离心,800rpm离心3分钟,弃上清,用完全培养基接种培养,置于5%co2、37℃培养箱内继续培养。
66.(2)48小时后换液,用含有15μm奥替普拉(oltipraz,sm-o9389-5mg)的完全培养基继续培养。
67.(3)每3天换培养基一次,更换的完全培养基中添加有15μm的奥替普拉。
68.(4)连续培养10天。
69.实施例3
70.本实施例提供一种增强脐带间充质干细胞免疫调节能力的方法,其步骤如下:
71.(1)细胞复苏。将p3代脐带间充质干细胞从液氮中取出,37℃水浴中快速解冻,加入含12.5%胎牛血清的dmem/f12完全培养基后离心,800rpm离心3分钟,弃上清,用完全培养基接种培养,置于5%co2、37℃培养箱内继续培养。
72.(2)48小时后换液,用含有15μm奥替普拉(oltipraz,sm-o9389-5mg)的无血清培养基(therapeak
tm mscgm-cd
tm
人间充质干细胞培养基)继续培养。
73.(3)每3天换培养基一次,更换的therapeak
tm mscgm-cd
tm
人间充质干细胞培养基中添加有15μm的奥替普拉。
74.(4)连续培养10天。
75.实施例4
76.本实施例提供一种增强牙髓干细胞免疫调节能力的方法,其步骤如下:
77.(1)细胞复苏。将p3代牙髓干细胞从液氮中取出,37℃水浴中快速解冻,加入含12.5%胎牛血清的dmem/f12完全培养基后再离心,800rpm离心3分钟,弃上清,用完全培养基接种培养,置于5%co2、37℃培养箱内继续培养。
78.(2)48小时后换液,用含有15μm奥替普拉(oltipraz,sm-o9389-5mg)的无血清培养基(therapeak
tm mscgm-cd
tm
人间充质干细胞培养基)继续培养。
79.(3)每3天换培养基一次,更换的therapeak
tm mscgm-cd
tm
人间充质干细胞培养基中添加有15μm的奥替普拉。
80.(4)连续培养10天。
81.实施例5
82.本实施例提供一种增强脐带间充质干细胞免疫调节能力的方法,其步骤如下:
83.(1)细胞复苏。将p3代脐带间充质干细胞从液氮中取出,37℃水浴中快速解冻,加
入含12.5%胎牛血清的dmem/f12完全培养基离心,800rpm离心3分钟,弃上清,用完全培养基接种培养,置于5%co2、37℃培养箱内继续培养。
84.(2)48小时后换液,用含有15μm奥替普拉(oltipraz,sm-o9389-5mg)的gibco间充质干细胞无血清培养基msc sfm继续培养。
85.(3)每3天换培养基一次,更换的gibco间充质干细胞无血清培养基msc sfm中添加有15μm的奥替普拉。
86.(4)连续培养10天。
87.实施例6
88.本实施例提供一种增强牙髓干细胞免疫调节能力的方法,其步骤如下:
89.(1)细胞复苏。将p3代牙髓干细胞从液氮中取出,37℃水浴中快速解冻,加入含12.5%胎牛血清的dmem/f12完全培养基后再离心,800rpm离心3分钟,弃上清,用完全培养基接种培养,置于5%co2、37℃培养箱内继续培养。
90.(2)48小时后换液,用含有15μm奥替普拉(oltipraz,sm-o9389-5mg)的gibco间充质干细胞无血清培养基msc sfm继续培养。
91.(3)每3天换培养基一次,更换的gibco间充质干细胞无血清培养基msc sfm中添加有15μm的奥替普拉。
92.(4)连续培养10天。
93.实验例1
94.将实施例1-6获得的脐带间充质干细胞/牙髓干细胞进行分泌免疫调节因子能力的检测,具体步骤如下:
95.(1)向实施例1-6获得的脐带间充质干细胞/牙髓干细胞中分别加入50ng/ml的ifnγ,处理3天。
96.(2)qrt-pcr检测ido1、pdl1等因子的mrna表达水平,与未加奥替普拉的同批次培养细胞对比。
97.其中,每孔加入1ml trizol直接裂解贴壁细胞,将细胞裂解液转移至离心管中;每管加入氯仿200ul,震荡混匀,室温静置3分钟,12500rpm离心15分钟,收集上清;向上清中加入1倍体积异丙醇,混匀得到的溶液,12500rpm离心15分钟,弃上清,加入75%无水乙醇,混匀后7500rpm离心10分钟,弃掉上清,晾干后所得即为rna;采用cdna合成试剂盒将rna逆转录为cdna总反应体系为10μl,qpcr扩增目的基因和gapdh基因。
98.(3)目的基因mrna相对表达量采用δδct进行计算。
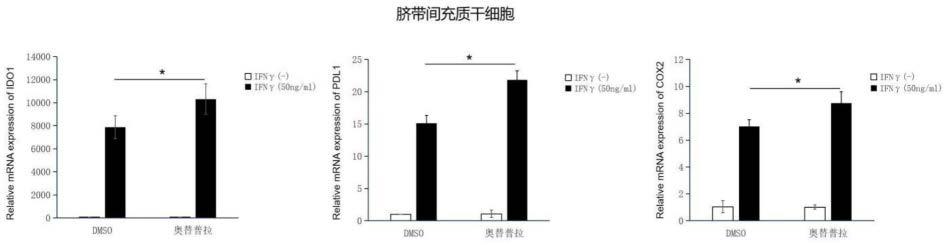
99.实施例1-6获得的脐带间充质干细胞/牙髓干细胞的目的基因mrna相对表达量检测结果依次如图1-6所示。从图1-6中可以发现,与基础培养基(即完全培养基、mscgm-cd
tm
无血清培养基和msc sfm无血清培养基)培养的脐带间充质干细胞/牙髓干细胞相比,奥替普拉预处理10天的脐带间充质干细胞/牙髓干细胞,在ifnγ刺激下,能够表达更多的ido1、pdl1和cox2。证实奥替普拉预处理能够提高脐带间充质干细胞/牙髓干细胞分泌免疫调节因子的能力。
100.实验例2
101.检测实施例1-6获得的脐带间充质干细胞和牙髓干细胞对外周血单个核细胞增殖
的影响,其具体步骤如下:
102.(1)新鲜分离外周血单个核细胞pbmc,用10ml等体积磷酸盐缓冲液(pbs)稀释外周血,将混合物缓慢加入离心管中,以10ml沿管壁梯度加入离心管。600g离心20min后,仔细收集pbmc,用pbs洗涤3次。
103.(2)新鲜分离的pbmcs用2mm羧基荧光素二乙酸琥珀酰亚胺酯(cfse,美国生命技术公司)在pbs中染色。脐带间充质干细胞/牙髓干细胞与cfse标记的pbmc共培养,添加纯化的抗cd3(5ng/ml)和抗cd28(5ng/ml)(添加10%胎牛血清和青霉素/链霉素)。uc-mscs和pbmcs的比例为1:10。72h后收集pbmc,通过荧光活化细胞分选评价细胞的增殖。
104.(3)采用软件进行数据分析。
105.实施例1-6的检测结果依次如图7-12所示。从图7-12中可以发现,与基础培养基(即完全培养基、mscgm-cd
tm
无血清培养基和msc sfm无血清培养基)培养的脐带间充质干细胞/牙髓干细胞相比,奥替普拉预处理10天的脐带间充质干细胞/牙髓干细胞,能够更好的抑制pbmc的增殖能力。证实奥替普拉预处理能够提高脐带间充质干细胞对免疫细胞的调节能力。
106.实验例3
107.本实验例是检测不同奥替普拉的作用时间和浓度下获得的脐带间充质干细胞的ido1、pdl1因子的mrna表达水平,具体步骤如下:
108.(1)细胞复苏。将p3代脐带间充质干细胞从液氮中取出,37℃水浴中快速解冻,加入完全培养基离心,800rpm离心3分钟,弃上清,用完全培养基接种培养,置于5%co2、37℃培养箱内继续培养。
109.(2)48小时后换液,分别用含有10μm、15μm和20μm奥替普拉(oltipraz,sm-o9389-5mg)的含12.5%胎牛血清的dmem/f12完全培养基,置于5%co2、37℃培养箱内继续培养。
110.(3)每3-4天换培养基一次,更换的含12.5%胎牛血清的dmem/f12完全培养基中添加有相应浓度奥替普拉。
111.(4)每个浓度分别连续培养培养7、8、9和10天。
112.(5)加入50ng/ml的ifnγ,处理3天,qrt-pcr检测ido1、pdl1因子的mrna表达水平,并进行比较。
113.检测结果如图13-14所示,10-20μm的奥替普拉作用7-10天均能提高细胞分泌ido1和pdl1的能力,且15μm作用10天效果更明显。
114.对比例1
115.与实施例1的区别在于,本对比例的培养基中含有5μm奥替普拉。
116.如图15所示,与对照组相比,5μm奥替普拉的添加对ido1和pdl1的表达在7-10天都没有明显差异。
117.对比例2
118.与实施例1的区别在于,本对比例的培养基中含有25μm奥替普拉。
119.如图16所示,与对照组相比,25μm奥替普拉的添加对ido1和pdl1的表达在7-10天都没有明显差异。
120.以上所述仅为本发明的优选实施例而已,并不用于限制本发明,对于本领域的技术人员来说,本发明可以有各种更改和变化。凡在本发明的精神和原则之内,所作的任何修
改、等同替换、改进等,均应包含在本发明的保护范围之内。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。