1.本专利申请要求于2019年8月13日向韩国专利局提交的韩国专利第10-2019-0098911号的优先权,该专利申请的全部内容在此引入本技术作为参考。
2.本专利申请要求于2020年8月12日向韩国专利局提交的韩国专利第10-2020-0101087号的优先权,该专利申请的全部内容在此引入本技术作为参考。
3.本专利申请要求于2020年8月12日向韩国专利局提交的韩国专利第10-2020-0101088号的优先权,该专利申请的全部内容在此引入本技术作为参考。
4.本发明涉及糖基化艾塞那肽类似物及其用途。
5.本发明涉及艾塞那肽二聚体类似物及其用途。
背景技术:
6.糖基化(glycosylation)是将糖附着在体内表达的蛋白质上的过程,是发生在作为细胞内小器官的高尔基体中的一种反应,已知由糖基化形成的糖蛋白参与各种生物学现象,例如细胞间结合、组织发育、免疫反应和激素作用等。糖的结构研究始于1880年,至今一直在积极进行糖和糖基化的研究,最近,利用糖基化技术进行药物开发的研究正在进行中。
7.艾塞那肽(exenatide)是一种从在美国西南部栖息的吉拉毒蜥(heloderma suspectum)的唾液腺中分离出来的胰高血糖素样肽-1(glucagon-like peptide-1,glp-1)的功能类似物(analog),被用作2型糖尿病的肽治疗剂。最近,正在积极开发包括艾塞那肽在内的glp-1类似物的体内稳定性得到改善的具有持续性作用的类似物。
8.学名为“exendin-4”的艾塞那肽是一种由39个氨基酸组成的生理活性肽,存在于人体内,但有53%的氨基酸与glp-1相似,对如二肽基肽酶-4(dipetidyl peptidase-4,dpp-4)等分解酶具有稳定性,因此与glp-1相比具有较长的体内半衰期。
9.艾塞那肽每天给药两次,分别为早上和晚餐前。艾塞那肽由肾脏排泄,因此不建议用于严重肾功能不全或终末期肾病患者。
10.艾塞那肽排泄不依赖于肝功能,因此不与肝脏代谢的药物相互作用。相反,由于艾塞那肽影响胃动力(gastric motility),它可能与其他药物在吸收方面发生相互作用。
11.并且,艾塞那肽的合成过程还存在试剂过量和材料成本过高的缺点。而且,由于反应步骤数多,且每一步都需要游离中间体,并且有可能形成异构体,纯化困难。
12.正在积极研究利用glp-1类似物的新型糖尿病的新型治疗剂,但在大多数情况下,重点是开发改善药效持久效果的制剂,而几乎没有开发功效和稳定性得到改善的突破性艾塞那肽类似物和模拟物。
13.另一方面,据报道,艾塞那肽具有由于体内的免疫反应而导致药效降低等副作用。因此,利用体内发生的糖基化过程开发肽药物有望表现出提高的体内稳定性和改善的免疫原性(immunogenicity)。
14.艾塞那肽是胰高血糖素样肽-1受体(glucagon-like peptide-1receptor,glp-1r)的激动剂(agonist),被用作治疗2型糖尿病的肽治疗剂,最近,正在积极开发包括艾塞
那肽在内的glp-1类似物的体内稳定性和低血糖等副作用得到改善的具有持续性作用的类似物。
15.glp-1r和胰高血糖素受体(glucagon receptor,gcgr)分别与体内的glp-1和胰高血糖素结合,通过血糖调节在维持体内稳态中发挥重要作用。众所周知,glp-1r在大脑皮层和肠道中被激活,抑制食欲,同时降低肠道运动,从而在减轻体重中发挥重要作用。并且,已知gcgr通过增加白色脂肪组织中的脂肪分解酶hsl、atgl的活性以及增加棕色脂肪组织中的热能产生来发分解堆积的脂肪,从而有助于减轻体重(参考(reference)),在一项以患有2型糖尿病和肥胖症的患者为对象进行的代谢功能研究中确认到,当同时给药胰高血糖素和glp-1时,通过增加glp-1的胰岛素分泌来防止胰高血糖素的高血糖风险,从而稳定血糖水平,并增加热能产生。
16.上述结果表明,同时靶向gcgr和glp-1r的双靶向激动剂(dual agonist)与现有的glp-1靶向激动剂相比,将具有调节血糖水平和增加减轻体重的效果,双表达激动剂有望成为同时治疗新型2型糖尿病和肥胖症这两种代谢疾病的新型候选药物。
17.糖基化(glycosylation)是将糖附着在体内表达的蛋白质上的过程,是发生在作为细胞内小器官的高尔基体中的一种反应,已知由糖基化形成的糖蛋白参与各种生物学现象,例如细胞间结合、组织发育、免疫反应和激素作用等。糖的结构研究始于1880年,至今一直在积极进行糖和糖基化的研究,最近,利用糖基化技术进行药物开发的研究正在进行中。
18.艾塞那肽(exenatide)是一种从在美国西南部栖息的吉拉毒蜥(heloderma suspectum)的唾液腺中分离出来的胰高血糖素样肽-1(glucagon-like peptide-1,glp-1)的功能类似物(analog),被用作2型糖尿病的肽治疗剂。最近,正在积极开发包括艾塞那肽在内的glp-1类似物的体内稳定性得到改善的具有持续性作用的类似物。
19.学名为“exendin-4”的艾塞那肽是一种由39个氨基酸组成的生理活性肽,存在于人体内,但有53%的氨基酸与glp-1相似,对如二肽基肽酶-4(dipetidyl peptidase-4,dpp-4)等分解酶具有稳定性,因此与glp-1相比具有较长的体内半衰期。
20.艾塞那肽每天给药两次,分别为早上和晚餐前。艾塞那肽由肾脏排泄,因此不建议用于严重肾功能不全或终末期肾病患者。
21.艾塞那肽排泄不依赖于肝功能,因此不与肝脏代谢的药物相互作用。相反,由于艾塞那肽影响胃动力(gastric motility),它可能与其他药物在吸收方面发生相互作用。
22.并且,艾塞那肽的合成过程还存在试剂过量和材料成本过高的缺点。而且,由于反应步骤数多,且每一步都需要游离中间体,并且有可能形成异构体,纯化困难。
23.正在积极研究利用glp-1类似物的新型糖尿病的新型治疗剂,但在大多数情况下,重点是开发改善药效持久效果的制剂,而几乎没有开发功效和稳定性得到改善的突破性艾塞那肽类似物和模拟物。
24.另一方面,据报道,艾塞那肽具有由于体内的免疫反应而导致药效降低等副作用。因此,利用体内发生的糖基化过程开发肽药物有望表现出提高的体内稳定性和改善的免疫原性(immunogenicity)。
技术实现要素:
25.技术问题
26.本发明旨通过结合糖基化技术开发艾塞那肽类似物来开发药物功效及体内稳定性增加的新型糖尿病候选治疗药物。
27.本发明的目的在于,提供糖基化艾塞那肽类似物。
28.本发明的再一目的在于,提供包含糖基化艾塞那肽类似物的用于改善、预防或治疗糖尿病的药物组合物。
29.本发明的另一目的在于,提供包含糖基化艾塞那肽类似物的用于改善、预防或治疗肥胖症的药物组合物。
30.本发明的还有一目的在于,提供包含糖基化艾塞那肽类似物的用于改善或缓解糖尿病的食品组合物。
31.本发明的又一目的在于,提供包含糖基化艾塞那肽类似物的用于改善或缓解肥胖症的食品组合物。
32.本发明的又一目的在于,提供包含糖基化艾塞那肽类似物的用于抑制食欲的食品组合物。
33.本发明的又一目的在于,提供通过向有需要的对象给药糖尿病的改善、预防或治疗有效量的糖基化艾塞那肽类似物来改善、预防或治疗糖尿病的方法。
34.本发明的又一目的在于,提供通过向有需要的对象给药肥胖症的改善、预防或治疗有效量的糖基化艾塞那肽类似物来改善、预防或治疗肥胖症的方法。
35.本发明的又一目的在于,提供糖基化艾塞那肽类似物在改善、预防或治疗糖尿病中的用途。
36.本发明的又一目的在于,提供糖基化艾塞那肽类似物在改善、预防或治疗肥胖症中的用途。
37.本发明的又一目的在于,提供糖基化艾塞那肽类似物在抑制食欲中的用途。
38.本发明人旨应用多抗原肽(multiple antigenic peptide,map)开发基于作为glp-1r激动剂的艾塞那肽开发的具有改善的血糖调节能力及体内稳定性的艾塞那肽二聚体类似物,由此开发新型糖尿病及肥胖症的候选治疗药物。
39.本发明的目的在于,提供艾塞那肽二聚体类似物。
40.本发明的再一目的在于,提供包含艾塞那肽二聚体类似物的用于改善、预防或治疗糖尿病的药物组合物。
41.本发明的另一目的在于,提供包含艾塞那肽二聚体类似物的用于改善、预防或治疗肥胖症的药物组合物。
42.本发明的还有一目的在于,提供包含艾塞那肽二聚体类似物的用于改善或缓解糖尿病的食品组合物。
43.本发明的又一目的在于,提供包含艾塞那肽二聚体类似物的用于改善或缓解肥胖症的食品组合物。
44.本发明的又一目的在于,提供包含艾塞那肽二聚体类似物的用于抑制食欲的食品组合物。
45.本发明的又一目的在于,提供通过向有需要的对象给药糖尿病的改善、预防或治疗有效量的艾塞那肽二聚体类似物来改善、预防或治疗糖尿病的方法。
46.本发明的又一目的在于,提供通过向有需要的对象给药肥胖症的改善、预防或治
疗有效量的艾塞那肽二聚体类似物来改善、预防或治疗肥胖症的方法。
47.本发明的又一目的在于,提供艾塞那肽二聚体类似物在改善、预防或治疗糖尿病中的用途。
48.本发明的又一目的在于,提供艾塞那肽二聚体类似物在改善、预防或治疗肥胖症中的用途。
49.本发明的又一目的在于,提供艾塞那肽二聚体类似物在抑制食欲中的用途。
50.解决问题的方案
51.本发明涉及糖基化艾塞那肽类似物及其用途。
52.以下,更详细地说明本发明。
53.本发明的一例涉及糖基化艾塞那肽类似物。
54.在本发明中,艾塞那肽是一种glp-1受体激动剂,是被二肽基肽酶-iv(dpp-iv)快速降解的模拟glp-1的类似物(glp-1metrics),它是一种不会被dpp-iv快速降解并促进糖依赖性胰岛素分泌、抑制胰高血糖素分泌、胃排空及食欲的药物,并且表现出具有β细胞保护效果的glp-1的效果的药物。
55.在本发明中,艾塞那肽包括包含序列1的氨基酸序列的艾塞那肽或者与序列1的氨基酸序列具有至少80%以上、90%以上、95%以上序列同源性的艾塞那肽类似物。
56.在本发明的一例中,艾塞那肽可以包含序列1的氨基酸序列,例如,可以由序列1的氨基酸序列组成。
57.在本发明中,艾塞那肽类似物中,艾塞那肽的氨基酸序列的部分氨基酸可被缺失并缀合(conjugation)有脂肪酸。
58.在本发明中,缺失可以为艾塞那肽的氨基酸序列的1个至15个、1个至14个、1个至13个、1个至12个、1个至11个、1个至10个、1个至9个、4个至15个、4个至14个、4个至13个、4个至12个、4个至11个、4个至10,4个至9个、7个至15个、7个至14个、7个至13个、7个至12个、7个至11个、7个至10个,例如,7个至9个氨基酸被缺失。
59.在本发明中,缺失可以为艾塞那肽的氨基酸序列的n-末端或c-末端的氨基酸被缺失,例如,可以为艾塞那肽的氨基酸序列的c-末端的氨基酸被缺失。
60.在本发明的一具体例中,缺失可以为艾塞那肽的氨基酸序列的c-末端的氨基酸中的1个至15个、1个至14个、1个至13个、1个至12个、1个至11个、1个至10,1个至9个、4个至15个、4个至14个、4个至13个、4个至12个、4个至11个、4个至10个、4个至9个、7个至15个、7个至14个、7个至13个、7个至12个、7个至11个、7个至10,例如,7个至9个氨基酸被缺失。
61.本发明的艾塞那肽类似物中的脂肪酸可与氨基酸序列的部分氨基酸被缺失的艾塞那肽的不同位置缀合。
62.在本发明中,脂肪酸包括本领域公知的多种饱和脂肪酸及不饱和脂肪酸。
63.在本发明中,脂肪酸可以是碳原子数为c3至c
36
的脂肪酸,例如,该脂肪酸可以为选自由丙酸(propionic acid)、丁酸(butyric acid)、戊酸(valeric acid)、己酸(caproic acid)、庚酸(enanthic acid)、辛酸(caprylic acid)、壬酸(pelargonic acid)、癸酸(capric acid)、十一烷酸(undecylic acid)、月桂酸(lauric acid)、十三烷酸(tridecylic acid)、肉豆蔻酸(myristic acid)、十五烷酸(pentadecylic acid)、棕榈酸(palmitic acid)、十七烷酸(margaric acid)、硬脂酸(stearic acid)、十九烷酸
(nonadecylic acid)、花生酸(arachidic acid)、二十一烷酸(heneicosylic acid)、山萮酸(behenic acid)、二十三烷酸(tricosylic acid)、二十四烷酸(lignoceric acid)、二十五烷酸(pentacosylic acid)、蜡酸(cerotic acid)、二十七烷酸(heptacosylic acid)、褐煤酸(montanic acid)、二十九烷酸(nonacosylic acid)、蜂花酸(melissic acid)、三十一烷酸(henatriacontylic acid)、紫胶蜡酸(lacceroic acid)、叶虱酸(psyllic acid)、格地酸(geddic acid)、三十五烷酸(ceroplastic acid)及三十六烷酸(hexatriacontylic acid)组成的组中的一种以上,但并不限定于此。
64.在本发明的一实例中,脂肪酸可与部分氨基酸被缺失的艾塞那肽的氨基酸序列的c-末端的lys残基、n-末端或c-末端缀合,例如,可与c-末端缀合。
65.在本发明中,氨基酸序列的部分氨基酸被缺失的艾塞那肽与脂肪酸的缀合包括直接结合和/或间接结合。
66.在本发明中,直接结合可以通过使脂肪酸中的如羧基等官能团与氨基酸被缺失的艾塞那肽的官能团(例如,-nh2)反应形成共价键来形成艾塞那肽-脂肪酸缀合。
67.在本发明中,间接结合可以介导本领域中通常用作衔接物的化合物来形成缺失的艾塞那肽-脂肪酸缀合。
68.本发明中利用的衔接物可以是本领域中用作衔接物的任何化合物,可根据缺失的艾塞那肽中的官能团种类选择衔接物,例如,衔接物包括n-琥珀酰亚胺碘乙酸酯(n-succinimidyl iodoacetate)、n-羟基琥珀酰亚胺溴乙酸酯(n-hydroxysuccinimidyl bromoacetate)、间马来酰亚胺基苯甲酰基-n-羟基琥珀酰亚胺酯(m-maleimidobenzoyl-n-hydroxysuccinimide ester),间马来酰亚胺基苯甲酰基-n-羟基磺基琥珀酰亚胺酯(m-maleimidobenzoyl-n-hydroxysulfosuccinimide ester)、n-马来酰亚胺基丁酰氧基琥珀酰胺酯(n-maleimidobutyryloxysuccinamide ester)及lys,但并不限定于此。
69.具体地,氨基酸缺失的艾塞那肽的c-末端还与衔接物结合,上述脂肪酸缀合在与上述c-末端结合的衔接物。例如,氨基酸缺失的艾塞那肽的c-末端与作为衔接物的lys结合,该lys可以与脂肪酸缀合。在这种情况下,可以通过使上述额外的lys的-nh2官能团与脂肪酸的羧基反应形成缀合物。
70.在本发明中,糖基化艾塞那肽类似物中,艾塞那肽类似物的至少一个氨基酸可以与糖类结合,与糖类结合的氨基酸可以被另一个氨基酸取代后与糖类结合。
71.在本发明的一具体例中,上述糖类的结合可在选自由艾塞那肽的第17位、第24位及第28位组成的组中的一个以上位点形成,上述艾塞那肽由序列1的氨基酸序列组成,但并不限定于此。
72.在本发明的一具体例中,上述取代可以为选自如下组中的一种以上:由序列1的氨基酸序列组成的艾塞那肽的第17位氨基酸glu被cys取代;由序列1的氨基酸序列组成的艾塞那肽的第24位氨基酸glu被cys取代;以及由序列1的氨基酸序列组成的艾塞那肽的第28位氨基酸asn被cys取代,但并不限定于此。
73.在本发明中,糖类可以为单糖至十一糖、二糖至十一糖、三糖至十一糖、四糖至十一糖、五糖至十一糖、六糖至十一糖、七糖至十一糖、八糖至十一糖、九糖至十一糖、十糖至十一糖,例如,可以为十一糖,具体地,可以为由下述结构式1表示的溴乙酰聚糖(bromoacetyl glycan)和/或由下述结构式2表示的11nc-asn-fmoc,但并不限定于此。
74.结构式1:
[0075][0076]
结构式2:
[0077][0078]
在本说明书中,术语“agm-212”由艾塞那肽的序列的第1位至第32位序列组成,上述艾塞那肽由序列1组成,上述序列c-末端与在侧链结合癸酸(capric acid)的赖氨酸(lysine)缀合,由ex4(1-32)k-cap的序列所示。
[0079]
在本说明书中,术语“agm-212(e17c-11sugar)”是指ex4(1-32)-cap的序列中的第17位谷氨酸(glutamic acid,glu,e)被cys取代且取代的氨基酸与具有十一糖结构的糖结合的序列。
[0080]
在本说明书中,术语“agm-212(n28c-11sugar)”是指ex4(1-32)-cap的序列中的第28位天冬酰胺(asparagine,asn,n)被cys取代且取代的氨基酸与具有十一糖结构的糖结合的序列。
[0081]
在本说明书中,术语“agm-212(n28-11 sugar)”是指ex4(1-32)-cap的序列中的第28位天冬酰胺与具有十一糖结构的糖结合的序列。
[0082]
在本说明书中,术语“agm-212(e24-11 sugar)”是指ex4(1-32)-cap的序列中的第24位谷氨酸被cys取代且取代的氨基酸与具有十一糖结构的糖结合的序列。
[0083]
在本说明书中,术语“agm-212(e17c-11sugar&e24c-11sugar)”是指通过将ex4(1-32)-cap的序列中的第17位谷氨酸用cys取代并取代第24位谷氨酸来使每个取代的氨基酸与具有十一糖结构的糖结合的序列。
[0084]
在本说明书中,术语“agm-212(e17c-11sugar&n28c-11sugar)”是指通过将ex4(1-32)-cap的序列中的第17位谷氨酸用cys取代并取代第28位天冬酰胺来使每个取代的氨基酸与具有十一糖结构的糖结合的序列。
[0085]
本发明的再一例涉及包含糖基化艾塞那肽类似物的用于改善、预防或治疗糖尿病
的药物组合物。
[0086]
本发明的另一例涉及包含糖基化艾塞那肽类似物的用于改善、预防或治疗肥胖症的药物组合物。
[0087]
本发明的药物组合物中,糖基化艾塞那肽类似物的描述与上述相同,因此将省略其描述。
[0088]
本发明的药物组合物可包含药学上可接受的载体。
[0089]
在本发明中,药学上可接受的载体为在制剂中常用的载体,包括乳糖、葡萄糖、蔗糖、山梨糖醇、甘露醇、淀粉、阿拉伯胶、磷酸钙、海藻酸盐、明胶、硅酸钙、微晶纤维素、聚乙烯吡咯烷酮、纤维素、水、糖浆、甲基纤维素、羟基苯甲酸甲酯、羟基苯甲酸丙酯、滑石粉、硬脂酸镁及矿物油等,但并不限定于此。
[0090]
本发明的药物组合物除上述成分外,还可以包含润滑剂、润湿剂、甜味剂、香味剂、乳化剂、悬浮剂、保存剂等。合适的药学上可接受的载体和制剂详细描述于remington's pharmaceutical sciences(19th ed.,1995)中。
[0091]
本发明的药物组合物可以口服或胃肠外给药,在胃肠外给药的情况下,可以通过静脉内注射、皮下注射、肌肉内注射、腹腔内注射、经皮给药等方式给药。
[0092]
本发明的药物组合物的合适剂量根据制剂方法、给药方式、患者的年龄、体重、性别、病理状态、饮食、给药时间、给药途径、排泄率及反应敏感性等因素而有所不同,普通的熟练医师可以容易地确定和开出对所需治疗或预防有效的剂量。
[0093]
根据本发明的优选实例,本发明的药物组合物的日剂量为0.001~10000
㎎
/
㎏
。
[0094]
本发明的药物组合物可根据本发明所属领域的普通技术人员可以容易地实施的方法利用药学上可接受的载体和/或赋形剂制备成单位剂量或者通过装入多剂量容器中来制备。在这种情况下,剂型可以是在油或水介质中的溶液、悬浮液或乳化液的形式,或者可以是提取物、粉末、颗粒、片剂或胶囊的形式,并且还可以包含分散剂或稳定剂。
[0095]
在本说明书中,术语“包含......作为有效成分”是指包括足以实现以下艾塞那肽类似物的功效或活性的量。本发明的组合物中包含的量的上限可由本领域技术人员在适当的范围内选择。
[0096]
本发明的还有一例涉及包含糖基化艾塞那肽类似物的用于改善或缓解糖尿病的食品组合物。
[0097]
本发明的又一例涉及包含糖基化艾塞那肽类似物的用于改善或缓解肥胖症的食品组合物。
[0098]
本发明的又一例涉及包含糖基化艾塞那肽类似物的用于抑制食欲的食品组合物。
[0099]
本发明的食品组合物,糖基化艾塞那肽类似物的描述与上述相同,因此将省略其描述。
[0100]
当本发明的组合物为食品组合物时,可以制成粉末、颗粒、片剂、胶囊或饮料的形式。例如,糖果类的各种食品类、饮料、口香糖、茶、维生素复合物或保健食品类等。
[0101]
本发明的食品组合物可包含在制备食品时通常添加的成分作为有效成分,例如,包含蛋白质、碳水化合物、脂肪、营养素、调味剂及香味剂。
[0102]
上述碳水化合物的例子包括:单糖,如葡萄糖、果糖等;二糖,如麦芽糖、蔗糖、寡糖等;以及多糖,例如,如糊精、环糊精等常规糖以及如木糖醇、山梨糖醇、赤藓糖醇等糖醇。作
为甜味剂,可以使用天然甜味剂[索马甜、甜叶菊提取物(例如,莱鲍迪苷a、甘草甜素等])和合成甜味剂(糖精、阿斯巴甜等)。例如,当本发明的食品组合物制备成饮剂时,除了本发明的化合物之外,还可以添加柠檬酸、液体果糖、砂糖、葡萄糖、乙酸、苹果酸、果汁、杜仲提取物、枣提取物、甘草提取物等。
[0103]
本发明的又一目的在于,提供通过向有需要的对象给药糖尿病的改善、预防或治疗有效量的艾塞那肽类似物来改善、预防或治疗糖尿病的方法。
[0104]
本发明的又一目的在于,提供通过向有需要的对象给药肥胖症的改善、预防或治疗有效量的艾塞那肽类似物来改善、预防或治疗肥胖症的方法。
[0105]
本发明的又一目的在于,提供艾塞那肽类似物在改善、预防或治疗糖尿病中的用途。
[0106]
本发明的又一目的在于,提供艾塞那肽类似物在改善、预防或治疗肥胖症中的用途。
[0107]
本发明的又一目的在于,提供艾塞那肽类似物在抑制食欲中的用途。
[0108]
本发明涉及艾塞那肽二聚体类似物及其用途。
[0109]
以下,更详细地说明本发明。
[0110]
本发明的一例涉及艾塞那肽二聚体类似物。
[0111]
在本发明中,艾塞那肽二聚体类似物可包含:第一体,由艾塞那肽的氨基酸序列的1个至15个氨基酸被缺失并缀合有脂肪酸的艾塞那肽类似物组成;以及第二体,由艾塞那肽的氨基酸序列的1个至15个氨基酸被缺失并缀合有脂肪酸的艾塞那肽类似物或胰高血糖素组成,由上述第一体与第二体结合形成二聚体类似物。
[0112]
在本发明中,艾塞那肽是一种glp-1受体激动剂,是被二肽基肽酶-iv(dpp-iv)快速降解的模拟glp-1的类似物,它是一种不会被dpp-iv快速降解并促进糖依赖性胰岛素分泌、抑制胰高血糖素分泌、胃排空及食欲的药物,并且表现出具有β细胞保护效果的glp-1的效果的药物。
[0113]
在本发明中,艾塞那肽包括包含序列1的氨基酸序列的艾塞那肽或者与序列1的氨基酸序列具有至少80%以上、90%以上、95%以上序列同源性的艾塞那肽类似物。
[0114]
在本发明的一例中,艾塞那肽可以包含序列1的氨基酸序列,例如,可以由序列1的氨基酸序列组成。
[0115]
在本发明中,胰高血糖素包括包含序列2的氨基酸序列的胰高血糖素或者与序列1的氨基酸序列具有至少80%以上、90%以上、95%以上序列同源性的胰高血糖素类似物。
[0116]
在本发明的一例中,胰高血糖素可以包含序列2的氨基酸序列,例如,可以由序列2的氨基酸序列组成。
[0117]
在本发明中,当上述第二体为艾塞那肽类似物时,上述第一体与第二体可通过二硫键结合,但并不限定于此。
[0118]
在本发明中,当上述第二体为胰高血糖素时,上述第一体与第二体的结合可通过在第一体的c-末端添加lys残基并在其侧链结合由胰高血糖素组成的第二体的方式实现,或者上述第一体与第二体可通过二硫键结合,但并不限定于此。
[0119]
在本发明中,艾塞那肽类似物中,艾塞那肽的氨基酸序列的部分氨基酸可被缺失并缀合有脂肪酸。
[0120]
在本发明中,缺失可以为艾塞那肽的氨基酸序列的1个至15个、1个至14个、1个至13个、1个至12个、1个至11个、1个至10个、1个至9个、4个至15个、4个至14个、4个至13个、4个至12个、4个至11个、4个至10,4个至9个、7个至15个、7个至14个、7个至13个、7个至12个、7个至11个、7个至10个,例如,7个至9个氨基酸被缺失。
[0121]
在本发明中,缺失可以为艾塞那肽的氨基酸序列的n-末端或c-末端的氨基酸被缺失,例如,可以为艾塞那肽的氨基酸序列的c-末端的氨基酸被缺失。
[0122]
在本发明的一具体例中,缺失可以为艾塞那肽的氨基酸序列的c-末端的氨基酸中的1个至15个、1个至14个、1个至13个、1个至12个、1个至11个、1个至10,1个至9个、4个至15个、4个至14个、4个至13个、4个至12个、4个至11个、4个至10个、4个至9个、7个至15个、7个至14个、7个至13个、7个至12个、7个至11个、7个至10,例如,7个至9个氨基酸被缺失。
[0123]
本发明的艾塞那肽类似物中的脂肪酸可与氨基酸序列的部分氨基酸被缺失的艾塞那肽的不同位置缀合。
[0124]
在本发明中,脂肪酸包括本领域公知的多种饱和脂肪酸及不饱和脂肪酸。
[0125]
在本发明中,脂肪酸可以是碳原子数为c3至c
36
的脂肪酸,例如,该脂肪酸可以为选自由丙酸、丁酸、戊酸、己酸、庚酸、辛酸、壬酸、癸酸、十一烷酸、月桂酸、十三烷酸、肉豆蔻酸、十五烷酸、棕榈酸、十七烷酸、硬脂酸、十九烷酸、花生酸、二十一烷酸、山萮酸、二十三烷酸、二十四烷酸、二十五烷酸、蜡酸、二十七烷酸、褐煤酸、二十九烷酸、蜂花酸、三十一烷酸、紫胶蜡酸、叶虱酸、格地酸、三十五烷酸及三十六烷酸组成的组中的一种以上,但并不限定于此。
[0126]
在本发明的一实例中,脂肪酸可与部分氨基酸被缺失的艾塞那肽的氨基酸序列的c-末端的lys残基、n-末端或c-末端缀合,例如,可与c-末端缀合。
[0127]
在本发明中,氨基酸序列的部分氨基酸被缺失的艾塞那肽与脂肪酸的缀合包括直接结合和/或间接结合。
[0128]
在本发明中,直接结合可以通过使脂肪酸中的如羧基等官能团与氨基酸被缺失的艾塞那肽的官能团(例如,-nh2)反应形成共价键来形成艾塞那肽-脂肪酸缀合。
[0129]
在本发明中,间接结合可以介导本领域中通常用作衔接物的化合物来形成缺失的艾塞那肽-脂肪酸缀合。
[0130]
本发明中利用的衔接物可以是本领域中用作衔接物的任何化合物,可根据缺失的艾塞那肽中的官能团种类选择衔接物,例如,衔接物包括n-琥珀酰亚胺碘乙酸酯、n-羟基琥珀酰亚胺溴乙酸酯、间马来酰亚胺基苯甲酰基-n-羟基琥珀酰亚胺酯,间马来酰亚胺基苯甲酰基-n-羟基磺基琥珀酰亚胺酯、n-马来酰亚胺基丁酰氧基琥珀酰胺酯及lys,但并不限定于此。
[0131]
具体地,氨基酸缺失的艾塞那肽的c-末端还与衔接物结合,上述脂肪酸缀合在与上述c-末端结合的衔接物。例如,氨基酸缺失的艾塞那肽的c-末端与作为衔接物的lys结合,该lys可以与脂肪酸缀合。在这种情况下,可以通过使上述额外的lys的-nh2官能团与脂肪酸的羧基反应形成缀合物。
[0132]
在本发明中,艾塞那肽二聚体类似物中,第一体、第二体或它们各自的一个氨基酸可与糖类结合。
[0133]
在本发明中,艾塞那肽二聚体类似物中,第一体、第二体或它们各自的一个氨基酸
可被另一个氨基酸取代,取代的氨基酸可与糖类结合。
[0134]
在本发明的一具体例中,上述糖类的结合可在选自由艾塞那肽的第17位、第24位及第28位组成的组中的一个以上位点形成,上述艾塞那肽由序列1的氨基酸序列组成,但并不限定于此。
[0135]
在本发明的一具体例中,上述取代可以为选自如下组中的一种以上:由序列1的氨基酸序列组成的艾塞那肽的第17位氨基酸glu被cys取代;由序列1的氨基酸序列组成的艾塞那肽的第24位氨基酸glu被cys取代;以及由序列1的氨基酸序列组成的艾塞那肽的第28位氨基酸asn被cys取代,但并不限定于此。
[0136]
在本发明的一具体例中,上述糖类的结合可在选自由胰高血糖素的第16位及第24位组成的组中的一个以上位点形成,上述胰高血糖素由序列2的氨基酸序列组成,但并不限定于此。
[0137]
在本发明的一具体例中,上述取代可以为选自如下组中的一种以上:由序列2的氨基酸序列组成的胰高血糖素的第16位氨基酸ser被cys或asn取代;以及由序列2的氨基酸序列组成的胰高血糖素的第24位氨基酸gln被cys或asn取代,但并不限定于此。
[0138]
在本发明中,糖类可以为单糖至十一糖、二糖至十一糖、三糖至十一糖、四糖至十一糖、五糖至十一糖、六糖至十一糖、七糖至十一糖、八糖至十一糖、九糖至十一糖、十糖至十一糖,例如,可以为十一糖,具体地,可以为由下述结构式1表示的溴乙酰聚糖(bromoacetyl glycan)和/或由下述结构式2表示的11nc-asn-fmoc,但并不限定于此。
[0139]
结构式1:
[0140][0141]
结构式2:
[0142][0143]
在本说明书中,术语“agm-212”由艾塞那肽的序列的第1位至第32位序列组成,上述艾塞那肽由序列1组成,上述序列c-末端与在侧链结合癸酸的赖氨酸缀合,由ex4(1-32)
k-cap的序列所示。
[0144]
在本说明书中,术语“agm-212-1”是指如下的序列,即,agm-212的序列中的第17位谷氨酸(glu,e)被cys取代的两个序列通过二硫键形成二聚体,每个序列的第24位谷氨酸被cys取代,氨基酸与十一糖结合。
[0145]
在本说明书中,术语“agm-212-2”是指如下的序列,即,agm-212的序列中的第17位谷氨酸被cys取代的两个序列通过二硫键形成二聚体,每个序列的第28位天冬酰胺被cys取代并与十一糖结合。
[0146]
在本说明书中,术语“agm-212-3”是指在agm-212的序列的c-末端添加lys并在其侧链结合胰高血糖素(glucagon)的序列。
[0147]
在本说明书中,术语“agm-212-4”是指如下的序列,即,agm-212的序列中的第28位天冬酰胺与十一糖结合,在c-末端添加lys并在其侧链结合胰高血糖素。
[0148]
在本说明书中,术语“agm-212-5”是指如下的序列,即,agm-212的序列中的第28位天冬酰胺与十一糖结合,在c-末端添加lys并在其侧链结合胰高血糖素,胰高血糖素的序列中的第16位丝氨酸(serine,ser,s)被11nc-asn取代并与十一糖结合。
[0149]
在本说明书中,术语“agm-212-6”是指如下的序列,即,agm-212的序列中的第28位天冬酰胺与十一糖结合,在c-末端添加lys并在其侧链结合胰高血糖素,胰高血糖素的序列中的第24位谷氨酰胺(glutamine,gln,q)被11nc-asn取代并与十一糖结合。
[0150]
在本说明书中,术语“agm-212-7”是指由如下两个序列通过二硫键组成二聚体的物质:agm-212的序列中的第17位谷氨酸被cys取代且第24位谷氨酸被cys取代并与十一糖结合的序列;胰高血糖素的序列中的第16位丝氨酸被cys取代并与十一糖结合且第24位谷氨酰胺被cys取代的序列。
[0151]
在本说明书中,术语“agm-212-8”是指由如下两个序列通过二硫键组成二聚体的物质:agm-212的序列中的第17位谷氨酸被cys取代且第24位谷氨酸被cys取代并与十一糖结合的序列;胰高血糖素的构成序列中的第24位谷氨酰胺被cys取代并与十一糖结合且第16位丝氨酸被cys取代的序列。
[0152]
在本说明书中,术语“二硫键”是指两个agm-212的e17被c17取代后每个c17-c17相互形成的二硫键,但并不限定于此。
[0153]
本发明的再一例涉及包含艾塞那肽二聚体类似物的用于改善、预防或治疗糖尿病的药物组合物。
[0154]
本发明的另一例涉及包含艾塞那肽二聚体类似物的用于改善、预防或治疗肥胖症的药物组合物。
[0155]
本发明的药物组合物中,艾塞那肽二聚体类似物的描述与上述相同,因此将省略其描述。
[0156]
本发明的药物组合物可包含药学上可接受的载体。
[0157]
在本发明中,药学上可接受的载体为在制剂中常用的载体,包括乳糖、葡萄糖、蔗糖、山梨糖醇、甘露醇、淀粉、阿拉伯胶、磷酸钙、海藻酸盐、明胶、硅酸钙、微晶纤维素、聚乙烯吡咯烷酮、纤维素、水、糖浆、甲基纤维素、羟基苯甲酸甲酯、羟基苯甲酸丙酯、滑石粉、硬脂酸镁及矿物油等,但并不限定于此。
[0158]
本发明的药物组合物除上述成分外,还可以包含润滑剂、润湿剂、甜味剂、香味剂、
乳化剂、悬浮剂、保存剂等。合适的药学上可接受的载体和制剂详细描述于remington’s pharmaceutical sciences(19th ed.,1995)中。
[0159]
本发明的药物组合物可以口服或胃肠外给药,在胃肠外给药的情况下,可以通过静脉内注射、皮下注射、肌肉内注射、腹腔内注射、经皮给药等方式给药。
[0160]
本发明的药物组合物的合适剂量根据制剂方法、给药方式、患者的年龄、体重、性别、病理状态、饮食、给药时间、给药途径、排泄率及反应敏感性等因素而有所不同,普通的熟练医师可以容易地确定和开出对所需治疗或预防有效的剂量。
[0161]
根据本发明的优选实例,本发明的药物组合物的日剂量为0.001~10000
㎎
/
㎏
。
[0162]
本发明的药物组合物可根据本发明所属领域的普通技术人员可以容易地实施的方法利用药学上可接受的载体和/或赋形剂制备成单位剂量或者通过装入多剂量容器中来制备。在这种情况下,剂型可以是在油或水介质中的溶液、悬浮液或乳化液的形式,或者可以是提取物、粉末、颗粒、片剂或胶囊的形式,并且还可以包含分散剂或稳定剂。
[0163]
在本说明书中,术语“包含......作为有效成分”是指包括足以实现以下艾塞那肽类似物的功效或活性的量。本发明的组合物中包含的量的上限可由本领域技术人员在适当的范围内选择。
[0164]
本发明的还有一例涉及包含艾塞那肽二聚体类似物的用于改善或缓解糖尿病的食品组合物。
[0165]
本发明的又一例涉及包含艾塞那肽二聚体类似物的用于改善或缓解肥胖症的食品组合物。
[0166]
本发明的又一例涉及包含艾塞那肽二聚体类似物的用于抑制食欲的食品组合物。
[0167]
本发明的食品组合物中,艾塞那肽二聚体类似物的描述与上述相同,因此将省略其描述。
[0168]
当本发明的组合物为食品组合物时,可以制成粉末、颗粒、片剂、胶囊或饮料的形式。例如,糖果类的各种食品类、饮料、口香糖、茶、维生素复合物或保健食品类等。
[0169]
本发明的食品组合物可包含在制备食品时通常添加的成分作为有效成分,例如,包含蛋白质、碳水化合物、脂肪、营养素、调味剂及香味剂。
[0170]
上述碳水化合物的例子包括:单糖,如葡萄糖、果糖等;二糖,如麦芽糖、蔗糖、寡糖等;以及多糖,例如,如糊精、环糊精等常规糖以及如木糖醇、山梨糖醇、赤藓糖醇等糖醇。作为甜味剂,可以使用天然甜味剂[索马甜、甜叶菊提取物(例如,莱鲍迪苷a、甘草甜素等])和合成甜味剂(糖精、阿斯巴甜等)。例如,当本发明的食品组合物制备成饮剂时,除了本发明的化合物之外,还可以添加柠檬酸、液体果糖、砂糖、葡萄糖、乙酸、苹果酸、果汁、杜仲提取物、枣提取物、甘草提取物等。
[0171]
本发明的又一目的在于,提供通过向有需要的对象给药糖尿病的改善、预防或治疗有效量的艾塞那肽类似物来改善、预防或治疗糖尿病的方法。
[0172]
本发明的又一目的在于,提供通过向有需要的对象给药肥胖症的改善、预防或治疗有效量的艾塞那肽类似物来改善、预防或治疗肥胖症的方法。
[0173]
本发明的又一目的在于,提供艾塞那肽类似物在改善、预防或治疗糖尿病中的用途。
[0174]
本发明的又一目的在于,提供艾塞那肽类似物在改善、预防或治疗肥胖症中的用
途。
[0175]
本发明的又一目的在于,提供艾塞那肽类似物在抑制食欲中的用途。
[0176]
在本说明书中,术语“糖尿病”是指以相对或绝对缺乏胰岛素导致葡萄糖不耐受(intolerance)为特征的慢性疾病。术语“糖尿病”包括所有类型的糖尿病,例如,包括1型糖尿病、2型糖尿病和遗传性糖尿病。1型糖尿病是胰岛素依赖型糖尿病,主要由β细胞破坏引起。2型糖尿病是非胰岛素依赖型糖尿病,由餐后胰岛素分泌不足或胰岛素抵抗引起。
[0177]
在本说明书中,术语“肥胖症”是指脂肪组织在体内过度堆积到导致健康异常的程度的状态。
[0178]
在本说明书中,术语“食欲抑制”是指抑制摄入食物的欲望。
[0179]
发明的效果
[0180]
本发明涉及糖基化到特定残基的艾塞那肽类似物及其用途,本发明提供与现有的艾塞那肽及其类似物相比表现出体内稳定性得到提高的新型糖尿病治疗物质。
[0181]
本发明涉及艾塞那肽二聚体类似物及其用途,本发明提供与现有的艾塞那肽及其类似物相比表现出体内稳定性得到提高的新型糖尿病治疗物质。
附图说明
[0182]
图1为通过大鼠胰岛素elisa(rat insulin elisa)分析本发明一实施例的糖基化agm-212类似物(实施例1、实施例2及实施例4)在大鼠胰岛(rat islets)中的胰岛素分泌能力的结果。
[0183]
图2为通过大鼠胰岛素elisa分析本发明一实施例的糖基化agm-212类似物(实施例5及实施例6)在大鼠胰岛中的胰岛素分泌能力的结果。
[0184]
图3为皮下给药本发明一实施例的糖基化agm-212类似物后通过血糖仪分析其在2型糖尿病小鼠动物模型中的糖负荷程度的结果。
[0185]
图4为皮下给药本发明一实施例的糖基化agm-212类似物后在野生型小鼠动物模型中通过药代动力学评价试验进行分析的结果。
[0186]
图5为本发明一实施例的糖基化agm-212类似物的免疫原性试验结果。
[0187]
图6为通过大鼠胰岛素elisa分析本发明一实施例的类似物在大鼠胰岛中的胰岛素分泌能力的结果。
[0188]
图7a为皮下给药本发明一实施例的包含agm-212-1及agm-212-2的类似物后通过血糖仪分析其在2型糖尿病小鼠动物模型中的抗糖尿病功效的结果。
[0189]
图7b为皮下给药本发明一实施例的包含agm-212-1及agm-212-2的类似物后通过血糖仪分析其在2型糖尿病小鼠动物模型中的抗糖尿病功效的结果。
[0190]
图8a为皮下给药本发明一实施例的包含agm-212-3、agm-212-4、agm-212-5及agm-212-6的类似物后通过血糖仪分析其在2型糖尿病小鼠动物模型中的抗糖尿病功效的结果。
[0191]
图8b为皮下给药本发明一实施例的包含agm-212-3、agm-212-4、agm-212-5及agm-212-6的类似物后通过血糖仪分析其在2型糖尿病小鼠动物模型中的抗糖尿病功效的结果。
[0192]
图9a为皮下给药本发明一实施例的类似物后在野生型小鼠动物模型中通过药代动力学评价试验进行分析的结果。
[0193]
图9b为皮下给药本发明一实施例的类似物后在野生型小鼠动物模型中通过药代
动力学评价试验进行分析的结果。
[0194]
图10a为本发明一实施例的类似物的饮食调节能力试验结果。
[0195]
图10b为本发明一实施例的类似物的饮食调节能力试验结果。
[0196]
图10c为本发明一实施例的类似物的饮食调节能力试验结果。
[0197]
图11a为本发明一实施例的类似物的葡萄糖耐量改善试验结果。
[0198]
图11b为本发明一实施例的类似物的葡萄糖耐量改善试验结果。
[0199]
图12a为本发明一实施例的类似物的胰岛素抵抗改善试验结果。
[0200]
图12b为本发明一实施例的类似物的胰岛素抵抗改善试验结果。
[0201]
图13a为本发明一实施例的类似物的肝脏中的脂肪堆积量试验结果。
[0202]
图13b为本发明一实施例的类似物的肝脏中的脂肪堆积量试验结果。
[0203]
图14a为本发明一实施例的类似物的热能增加效果试验结果。
[0204]
图14b为本发明一实施例的类似物的热能增加效果试验结果。
[0205]
图15a为本发明一实施例的类似物的热能产生相关因子试验结果。
[0206]
图15b为本发明一实施例的类似物的热能产生相关因子试验结果。
[0207]
图16a为本发明一实施例的类似物的脂肪分解能力试验结果。
[0208]
图16b为本发明一实施例的类似物的脂肪分解能力试验结果。
[0209]
图16c为本发明一实施例的类似物的脂肪分解能力试验结果。
[0210]
图16d为本发明一实施例的类似物的脂肪分解能力试验结果。
[0211]
图16e为本发明一实施例的类似物的脂肪分解能力试验结果。
[0212]
图17a为本发明一实施例的类似物在肌肉细胞中的脂肪分解能力及热能产生效果试验结果。
[0213]
图17b为本发明一实施例的类似物在肌肉细胞中的脂肪分解能力及热能产生效果试验结果。
[0214]
图17c为本发明一实施例的类似物在肌肉细胞中的脂肪分解能力及热能产生效果试验结果。
具体实施方式
[0215]
一种艾塞那肽二聚体类似物,包含:第一体,由艾塞那肽的氨基酸序列的1个至15个氨基酸被缺失并缀合有脂肪酸的糖基化艾塞那肽类似物组成,或者由艾塞那肽的氨基酸序列的1个至15个氨基酸被缺失并缀合有脂肪酸的艾塞那肽类似物组成;以及第二体,由艾塞那肽的氨基酸序列的1个至15个氨基酸被缺失并缀合有脂肪酸的艾塞那肽类似物或胰高血糖素组成,由上述第一体与第二体结合形成二聚体类似物。
[0216]
发明的实施方式
[0217]
以下,通过下述实施例更详细地说明本发明。但是这些实施例仅用于例示本发明,而本发明的范围并不限定于这些实施例。
[0218]
i.糖基化的艾塞那肽类似物
[0219]
实施例1.agm-212(e17c-11sugar)的制备
[0220]
1-1.化学式1
[0221]
为了制备作为agm-212的构成序列的ex4(1-32)k-cap,通过向三苯甲基树脂
(trityl resin)中添加fmoc-lys(dde)-oh及dmf来制备fmoc-lys(dde)三苯甲基树脂。通过向fmoc-lys(dde)三苯甲基树脂中添加包含20%的哌啶(piperidine)的dmf、fmoc-ser(tbu)-oh及1-羟基苯并三唑(hydroxyl-benzo triazole,hobt)来制备fmoc-ser(tbu)-lys(dde)三苯甲基树脂。以与上述制备方法相同的方法通过向fmoc-ser(tbu)-lys(dde)三苯甲基树脂中依次添加fmoc-pro-oh、fmoc-gly-oh、fmoc-gly-oh、fmoc-asn(trt)-oh、fmoc-lys(boc)-oh、fmoc-leu-oh、fmoc-trp(boc)-oh、fmoc-glu(tbu)-oh、fmoc-ile-oh、fmoc-phe-oh、fmoc-leu-oh、fmoc-arg(pbf)-oh、fmoc-val-oh、fmoc-ala-oh、fmoc-glu(tbu)-oh、fmoc-glu(tbu)-oh、fmoc-glu(tbu)-oh、fmoc-met-oh、fmoc-gln(trt)-oh、fmoc-lys(boc)-oh、fmoc-ser(tbu)-oh、fmoc-le)-oh、fmoc-asp(tbu)-oh、fmoc-ser(tbu)-oh、fmoc-thr(tbu)-oh、fmoc-phe-oh、fmoc-thr(tbu)-oh、fmoc-gly-oh、fmoc-glutbu()-oh、fmoc-gly-oh、fmoc-his(trt)-oh来制备下述化学式1。
[0222]
化学式1:
[0223]
fmoc-his(trt)-gly-glu(tbu)-gly-thr(tbu)-phe-thr(tbu)-ser(tbu)-asp(tbu)-leu-ser(tbu)-lyc(boc)-gln(trt)-met-glu(tbu)-glu(tbu)-cys(tbu)-ala-val-arg(pbf)-leu-phe-ile-glu(tbu)-trp(boc)-leu-lys(boc)-asn(trt)-gly-gly-pro-ser(tbu)-lys(dde)-三苯甲基树脂
[0224]
1-2.化学式2
[0225]
通过向化学式1中添加包含2%的nh2nh2·
h2o的dmf并去除dde来制备化学式2。
[0226]
化学式2:
[0227]
fmoc-his(trt)-gly-glu(tbu)-gly-thr(tbu)-phe-thr(tbu)-ser(tbu)-asp(tbu)-leu-ser(tbu)-lyc(boc)-gln(trt)-met-glu(tbu)-glu(tbu)-cys(trt)-ala-val-arg(pbf)-leu-phe-ile-glu(tbu)-trp(boc)-leu-lys(boc)-asn(trt)-gly-gly-pro-ser(tbu)-lys-三苯甲基树脂
[0228]
1-3.化学式3
[0229]
通过向化学式2中添加癸酸以及包含hobt和dic的dmf来制备化学式3。
[0230]
化学式3:
[0231]
fmoc-his(trt)-gly-glu(tbu)-gly-thr(tbu)-phe-thr(tbu)-ser(tbu)-asp(tbu)-leu-ser(tbu)-lyc(boc)-gln(trt)-met-glu(tbu)-glu(tbu)-cys(trt)-ala-val-arg(pbf)-leu-phe-ile-glu(tbu)-trp(boc)-leu-lys(boc)-asn(trt)-gly-gly-pro-ser(tbu)-lys(capric acid)-三苯甲基树脂
[0232]
1-4.化学式4
[0233]
切割化学式3的保护基后,通过纯化来制备化学式4。
[0234]
化学式4:
[0235]
his-gly-glu-gly-thr-phe-thr-ser-asp-leu-ser-lyc-gln-met-glu-glu-cys-ala-val-arg-leu-phe-ile-glu-trp-leu-lys-asn-gly-gly-pro-ser-lys(capric acid)-oh
[0236]
1-5.化学式5
[0237]
通过向化学式4中添加构成十一糖结构的溴乙酰聚糖(11suar)及naoh、磷酸盐缓冲液(phosphate buffer)来制备化学式5。
[0238]
化学式5:
[0239]
his-gly-glu-gly-thr-phe-thr-ser-asp-leu-ser-lyc-gln-met-glu-glu-cys(11sugar)-ala-val-arg-leu-phe-ile-glu-trp-leu-lys-asn-gly-gly-pro-ser-lys(capric acid)-oh
[0240]
实施例2.agm-212(n28c-11sugar)的制备
[0241]
以fmoc-cys(trt)-oh替换作为第28位氨基酸的fmoc-asn(tbu)-oh并通过与实施例1的制备过程中的方法相同的方法制备化学式6。
[0242]
化学式6:
[0243]
his-gly-glu-gly-thr-phe-thr-ser-asp-leu-ser-lyc-gln-met-glu-glu-glu-ala-val-arg-leu-phe-ile-glu-trp-leu-lys-cys(11sugar)-gly-gly-pro-ser-lys(capric acid)-oh
[0244]
实施例3.agm-212(n28-11 sugar)的制备
[0245]
以图2的11nc-asn-fmoc替换作为第28位氨基酸的fmoc-asn(tbu)-oh并通过与实施例1的制备过程中的方法相同的方法制备化学式7。
[0246]
化学式7:
[0247]
his-gly-glu-gly-thr-phe-thr-ser-asp-leu-ser-lyc-gln-met-glu-glu-glu-ala-val-arg-leu-phe-ile-glu-trp-leu-lys-asn(11sugar)-gly-gly-pro-ser-lys(capric acid)-oh
[0248]
表1
[0249][0250]
实施例4.agm-212(e24c-11sugar)的制备
[0251]
以fmoc-cys(trt)-oh替换作为第24位氨基酸的fmoc-glu(tbu)-oh并通过与实施例1的制备过程中的方法相同的方法制备化学式8。
[0252]
化学式8:
[0253]
his-gly-glu-gly-thr-phe-thr-ser-asp-leu-ser-lyc-gln-met-glu-glu-glu-ala-val-arg-leu-phe-ile-cys(11sugar)-trp-leu-lys-asn-gly-gly-pro-ser-lys(capric acid)-oh
[0254]
实施例5.agm-212(e17c-11sugar&e24c-11sugar)的制备
[0255]
5-1.化学式9
[0256]
以fmoc-cys(trt)-oh替换作为第24位氨基酸的fmoc-glu(tbu)-oh并通过与实施例1的制备过程中的方法相同的方法制备化学式9。
[0257]
化学式9:
[0258]
his-gly-glu-gly-thr-phe-thr-ser-asp-leu-ser-lyc-gln-met-glu-glu-cys-ala-val-arg-leu-phe-ile-cys-trp-leu-lys-asn-gly-gly-pro-ser-lys(capric acid)-oh
[0259]
5-2.化学式11
[0260]
通过向化学式9中添加构成十一糖结构的溴乙酰聚糖(11suar)及naoh、磷酸盐缓冲液来制备化学式10。
[0261]
化学式10:
[0262]
his-gly-glu-gly-thr-phe-thr-ser-asp-leu-ser-lyc-gln-met-glu-glu-cys(11sugar)-ala-val-arg-leu-phe-ile-cys(11sugar)-trp-leu-lys-asn-gly-gly-pro-ser-lys(capric acid)-oh
[0263]
实施例6.agm-212(e17c-11sugar&n28c-11sugar)的制备
[0264]
6-1.化学式11
[0265]
以fmoc-cys(trt)-oh替换作为第28位氨基酸的fmoc-asn(tbu)-oh并通过与实施例1的制备过程中的方法相同的方法制备化学式11。
[0266]
化学式11:
[0267]
his-gly-glu-gly-thr-phe-thr-ser-asp-leu-ser-lyc-gln-met-glu-glu-cys-ala-val-arg-leu-phe-ile-glu-trp-leu-lys-cys-gly-gly-pro-ser-lys(capric acid)-oh
[0268]
6-2.化学式12
[0269]
通过向化学式11中添加构成十一糖结构的溴乙酰聚糖(11suar)及naoh、磷酸盐缓冲液来制备化学式12。
[0270]
化学式12:
[0271]
his-gly-glu-gly-thr-phe-thr-ser-asp-leu-ser-lyc-gln-met-glu-glu-cys(11sugar)-ala-val-arg-leu-phe-ile-glu-trp-leu-lys-cys(11sugar)-gly-gly-pro-ser-lys(capric acid)-oh
[0272]
实验例1.类似物与glp-1受体的结合力的确认
[0273]
使用荧光素酶检测系统(luciferase assay system)检测实施例1至实施例6中制备的类似物与glp-1受体的结合力。荧光素酶检测系统是一种通过测定细胞的特定受体与配体的结合力来检测受体的活性程度的方法。
[0274]
具体地,在96孔白色细胞培养板(96well white cell culture plate)中培养成纤维细胞系cv-1(1
×
104个细胞/ml,韩国细胞系银行)24小时后,添加人glp-1r(pcdna3.1_hglp-1r)、camp反应元件(amp response element)(cre,pcdna3.1_hcre)进行转化(transfection)。培养24小时后,将培养基更换为无血清(serum)培养基,培养16小时后,将各类似物处理6小时。使用光度计(luminometer)通过激活的glp-1r对作为报告基因(reporter gene)的荧光素酶(luciferase)的表达水平进行定量,其结果如表2所示。
[0275]
表2
[0276][0277]
可通过表2确认,agm-212对glp-1r的活性与ex4相同,与十一糖(11sugar)结合的agm-212类似物与ex4或agm-212相比具有有所降低的活性。并且可知,虽然各类似物的活性由于糖基化而降低,但仍然具有nm水平的结合力。
[0278]
实验例2.类似物的胰岛素分泌能力确认
[0279]
为了确认实施例1至实施例6中制备的类似物的胰岛素分泌能力,确认了类似物对大鼠胰岛的葡萄糖依赖性胰岛素分泌能力。
[0280]
具体地,取出8周龄的sd大鼠(damul science)的胰腺(pancreas),分离胰岛(islets)。用28mm的葡萄糖(glucose)中的不同浓度(10nm,100nm)的各类似物处理分离的胰岛后,利用大鼠胰岛素elisa试剂盒测定分泌的胰岛素量,其结果如图1至图2及表3至表4所示。
[0281]
表3
[0282][0283]
表4
[0284][0285]
可通过图1至图2及表3至表4确认,与十一糖结合的类似物均以浓度依赖性方式增加胰岛素分泌,并且确认到胰岛素分泌能力比ex4及agm-212增加。
[0286]
实验例3.类似物的糖负荷效果确认
[0287]
为了确认实施例1至实施例4中制备的类似物的糖负荷效果,将作为2型糖尿病小鼠模型的c57bks/j dbdb mice(5~7周龄,中心实验动物)禁食16小时后,皮下给药
10nmole/kg的各类似物,30分钟后,腹腔给药葡萄糖(1.5g/kg)。在120分钟内,在0分钟、15分钟、30分钟、45分钟、60分钟、90分钟、120分钟时从小鼠尾静脉采集血液并利用血糖仪(acu-check,罗氏(roche),德国(germany))测量血糖,其结果如图3a至图3b所示。
[0288]
可通过图3a至图3b确认,所有agm-212类似物表现出与ex4及agm-212相同的糖负荷效果。其结果意味着糖基化的agm-212类似物具有ex4的生物活性。
[0289]
实验例4.类似物的药代动力学试验
[0290]
对实施例2至实施例3中制备的类似物进行药代动力学(pharmacokinetics)试验。向野生型c57bl/6j mice(雄性(male),5~6周龄,n=5)皮下给药50nmole/kg的各类似物后,分别在0小时、0.5小时、1小时、2小时、4小时、8小时、10小时、12小时、14小时、24小时时采集血液。从采集的血液中分离血浆并利用exendin-4eia进行定量分析。将结果利用winnolin程序分析来确定药动学参数(pharmacokinetics parameter),其结果如图4及表5所示。
[0291]
表5
[0292][0293]
可通过图4及表5确认,agm-212(n28-11 sugar)表现出与agm-212相似的半衰期,并观察到agm-212(n28c-11sugar)的半衰期比ex4增加,但确认到与agm-212(n28-11 sugar)相比具有有所降低的水平。通过结果可知,当被糖基化时,不影响体内半衰期。
[0294]
实验例5.类似物的免疫原性试验
[0295]
为了对糖基化agm-212类似物进行免疫原性试验,每周一次向野生型c57bl/6j mice(雄性,6周龄)分别皮下给药1mg/kg的添加有弗氏完全佐剂(freund’s complete adjuvant)(西格玛(sigma))的ex4和agm-212(n28c-11sugar),共三次。采血后,利用抗药物抗体检测试剂盒(antidrug antibody assay kit)对生成的抗体进行定量分析,其结果如图5所示。
[0296]
可通过图5所示,在ex4给药组中,形成了约10pg/ml的针对ex4的igg抗体,而在糖基化agm-212类似物给药组中,并没有检测到形成的抗体。其结果意味着糖基化agm-212类似物由于糖基化而具有改善的免疫原性。
[0297]
实验例6.类似物的溶解度试验
[0298]
糖基化的类似物由于糖结合而可能会具有增加的溶解度(solubility),因此,对糖基化agm-212类似物进行溶解度试验。利用hplc测定agm-212(n28c-11sugar)及agm-212(e17c-11sugar&n28c-11sugar)分别在h2o及磷酸盐缓冲液(phosphate buffered saline,pbs)中的10mg/ml溶解度,其结果如表6所示。
[0299]
表6
[0300][0301]
可通过表6所示,ex4在所有溶剂中的溶解度为10mg/ml,agm-212在h2o中的溶解度有所降低,在pbs中的溶解度为ex4的约0.5倍以上。糖基化类似物在所有溶剂中的溶解度都比agm-212增加,通过比较与一个十一糖结合的类似物和与两个十一糖结合的类似物的溶解度发现,所结合的糖的数量越多,溶解度就越增加。
[0302]
ii.艾塞那肽二聚体类似物
[0303]
实施例1.agm-212-1的制备
[0304]
1-1.化学式1
[0305]
通过向三苯甲基树脂中添加fmoc-lys(dde)-oh及dmf来制备fmoc-lys(dde)三苯甲基树脂。通过向fmoc-lys(dde)三苯甲基树脂中添加包含20%的哌啶的dmf、fmoc-ser(tbu)-oh及hobt来制备fmoc-ser(tbu)-lys(dde)三苯甲基树脂。以与上述制备方法相同的方法通过向fmoc-ser(tbu)-lys(dde)三苯甲基树脂中依次添加fmoc-pro-oh、fmoc-gly-oh、fmoc-gly-oh、fmoc-asn(trt)-oh、fmoc-lys(boc)-oh、fmoc-leu-oh、fmoc-trp(boc)-oh、fmoc-cys(trt)-oh、fmoc-ile-oh、fmoc-phe-oh、fmoc-leu-oh、fmoc-arg(pbf)-oh、fmoc-val-oh、fmoc-ala-oh、fmoc-cys(acm)-oh、fmoc-glu(tbu)-oh、fmoc-glu(tbu)-oh、fmoc-met-oh、fmoc-gln(trt)-oh、fmoc-lys(boc)-oh、fmoc-ser(tbu)-oh、fmoc-le)-oh、fmoc-asp(tbu)-oh、fmoc-ser(tbu)-oh、fmoc-thr(tbu)-oh、fmoc-phe-oh、fmoc-thr(tbu)-oh、fmoc-gly-oh、fmoc-glu(tbu)-oh、fmoc-gly-oh、fmoc-his(trt)-oh来制备下述化学式1。
[0306]
化学式1:
[0307]
fmoc-his(trt)-gly-glu(tbu)-gly-thr(tbu)-phe-thr(tbu)-ser(tbu)-asp(tbu)-leu-ser(tbu)-lyc(boc)-gln(trt)-met-glu(tbu)-glu(tbu)-cys(acm)-ala-val-arg(pbf)-leu-phe-ile-cys(trt)-trp(boc)-leu-lys(boc)-asn(trt)-gly-gly-pro-ser(tbu)-ser(tbu)-gly-ala-pro-pro-pro-ser(tbu)-lys(dde)-三苯甲基树脂
[0308]
1-2.化学式2
[0309]
通过向化学式1中添加包含2%的nh2nh2·
h2o的dmf并去除dde来制备化学式2。
[0310]
化学式2:
[0311]
fmoc-his(trt)-gly-glu(tbu)-gly-thr(tbu)-phe-thr(tbu)-ser(tbu)-asp(tbu)-leu-ser(tbu)-lyc(boc)-gln(trt)-met-glu(tbu)-glu(tbu)-cys(acm)-ala-val-arg(pbf)-leu-phe-ile-cys(trt)-trp(boc)-leu-lys(boc)-asn(trt)-gly-gly-pro-ser(tbu)-ser(tbu)-gly-ala-pro-pro-pro-ser(tbu)-lys-三苯甲基树脂
[0312]
1-3.化学式3
[0313]
通过向化学式2中添加癸酸以及包含hobt和dic的dmf来制备化学式3。
[0314]
化学式3:
[0315]
fmoc-his(trt)-gly-glu(tbu)-gly-thr(tbu)-phe-thr(tbu)-ser(tbu)-asp(tbu)-leu-ser(tbu)-lyc(boc)-gln(trt)-met-glu(tbu)-glu(tbu)-cys(acm)-ala-val-arg(pbf)-leu-phe-ile-cys(trt)-trp(boc)-leu-lys(boc)-asn(trt)-gly-gly-pro-ser(tbu)-ser(tbu)-gly-ala-pro-pro-pro-ser(tbu)-lys(capric acid)-三苯甲基树脂
[0316]
1-4.化学式4
[0317]
切割化学式3的保护基后,通过纯化来制备化学式4。
[0318]
化学式4:
[0319]
his-gly-glu-gly-thr-phe-thr-ser-asp-leu-ser-lyc-gln-met-glu-glu-cys(acm)-ala-val-arg-leu-phe-ile-cys-trp-leu-lys-asn-gly-gly-pro-ser-ser-gly-ala-pro-pro-pro-ser-lys(capric acid)-oh
[0320]
1-5.化学式5
[0321]
通过向化学式4中添加构成十一糖结构的溴乙酰聚糖(11suar)及naoh、磷酸盐缓冲液来制备化学式5。
[0322]
化学式5:
[0323]
his-gly-glu-gly-thr-phe-thr-ser-asp-leu-ser-lyc-gln-met-glu-glu-cys(acm)-ala-val-arg-leu-phe-ile-cys(11sugar)-trp-leu-lys-asn-gly-gly-pro-ser-ser-gly-ala-pro-pro-pro-ser-lys(capric acid)-oh
[0324]
1-6.agm-212-1
[0325]
通过向化学式5中添加乙酸银(silver acetate)、碘(iodine)及50%的乙酸来制备表1的agm-212-1。
[0326]
实施例2.agm-212-2的制备
[0327]
以fmoc-cys(trt)-oh替换作为第28位氨基酸的fmoc-asn(tbu)-oh并通过与实施例1的制备过程中的方法相同的方法制备表1的agm-212-2。
[0328]
实施例3.agm-212-3的制备
[0329]
3-1.化学式6
[0330]
通过向三苯甲基树脂中添加fmoc-lys-oh及dmf来制备fmoc-lys三苯甲基树脂。除了用fmoc-glu(tbu)-oh取代第17位fmoc-cys(acm)-oh之外,通过实施例1的制备过程中的方法相同的方法制备化学式6。
[0331]
化学式6:
[0332]
his-gly-glu-gly-thr-phe-thr-ser-asp-leu-ser-lyc-gln-met-glu-glu-glu-ala-val-arg-leu-phe-ile-asn-trp-leu-lys-asn-gly-gly-pro-ser-ser-gly-ala-pro-pro-pro-ser-lys(capric acid)-lys-oh
[0333]
3-2.化学式7
[0334]
为了制备胰高血糖素,通过向三苯甲基树脂中添加fmoc-thr(tbu)-oh及dmf来制备fmoc-thr(tbu)三苯甲基树脂。通过向fmoc-thr(tbu)三苯甲基树脂中添加包含20%的哌啶的dmf、fmoc-asn(trt)-oh及hobt来制备fmoc-asn(trt)-thr(tbu)三苯甲基树脂。以与上述制备方法相同的方法通过向fmoc-asn(trt)-thr(tbu)三苯甲基树脂中依次添加fmoc-met-oh、fmoc-leu-oh、fmoc-trp(boc)-oh、fmoc-gln(trt)-oh、fmoc-val-oh、fmoc-phe-oh、
fmoc-asp(tbu)-oh、fmoc-gln(trt)-oh、fmoc-ala-oh、fmoc-arg(pbf)-oh、fmoc-arg(pbf)-oh、fmoc-ser(tbu)-oh、fmoc-asp(tbu)-oh、fmoc-leu-oh、fmoc-tyr(tbu)-oh、fmoc-lys(trt)-oh、fmoc-ser(tbu)-oh、fmoc-tyr(tbu)-oh、fmoc-asp(tbu)-oh、fmoc-ser(tbu)-oh、fmor-thr(tbu)-oh、fmoc-phe-oh、fmor-thr(tbu)-oh、fmoc-gly-oh、fmoc-gln(trt)-oh、fmoc-ser(tbu)-oh、fmoc-his(trt)-oh来制备下述化学式7。
[0335]
化学式7:
[0336]
fmoc-his(trt)-ser(tbu)-gln(trt)-gly-thr(tbu)-phe-thr(tbu)-ser(tbu)-asp(tbu)-tyr(tbu)-ser(tbu)-lys(trt)-tyr(tbu)-leu-asp(tbu)-ser(tbu)-arg(pbf)-arg(pbf)-ala-gln(trt)-asp(tbu)-phe-val-gln(trt)-trp(boc)-leu-met-asn(trt)-thr(tbu)-三苯甲基树脂
[0337]
3-3.化学式8
[0338]
切割化学式7的保护基后,通过纯化来制备化学式8。
[0339]
化学式8:
[0340]
his-ser-gln-gly-thr-phe-thr-ser-asp-tyr-ser-lys-tyr-leu-asp-ser-arg-arg-ala-gln-asp-phe-val-gln-trp-leu-met-asn-thr-oh
[0341]
3-4.agm-212-3
[0342]
通过向上述化学式6和化学式8中添加包含20%的哌啶的dmf及hobt来制备由化学式8的第34位lys的侧链与化学式8的第30位thr结合而成的表1的agm-212-3。
[0343]
实施例4.agm-212-4的制备
[0344]
将实施例3中的化学式6的构成序列中的第28位asn用11nc-asn-fmoc取代来制备后,通过向化学式8的物质中添加包含20%的哌啶的dmf及hobt来制备与化学式6的第34位lys的侧链结合的表1的agm-212-4。
[0345]
实施例5.agm-212-5的制备
[0346]
用11nc-asn-fmoc取代化学式6的构成序列中的第16位ser并通过与实施例4的制备过程中的方法相同的方法制备表1的agm-212-5。
[0347]
实施例6.agm-212-6的制备
[0348]
用11nc-asn-fmoc取代化学式6的构成序列中的第24位gln并通过与实施例4的制备过程中的方法相同的方法制备表1的agm-212-6。
[0349]
实施例7.agm-212-7的制备
[0350]
7-1.化学式9
[0351]
在实施例5的制备过程中,通过用cys(acm)取代第16位ser并用cys取代第24位谷氨酰胺来制备化学式10。
[0352]
化学式9:
[0353]
his-ser-gln-gly-thr-phe-thr-ser-asp-tyr-ser-lys-tyr-leu-asp-cys(acm)-arg-arg-ala-gln-asp-phe-val-cys-trp-leu-met-asn-thr-oh
[0354]
7-1.化学式10
[0355]
通过向化学式9中添加构成十一糖结构的溴乙酰聚糖(11suar)及naoh、磷酸盐缓冲液来制备化学式10。
[0356]
化学式10:
[0357]
his-ser-gln-gly-thr-phe-thr-ser-asp-tyr-ser-lys-tyr-leu-asp-cys(acm)-arg-arg-ala-gln-asp-phe-val-cys(11sugar)-trp-leu-met-asn-thr-oh
[0358]
7-2.agm-212-7
[0359]
通过向化学式5和化学式10中添加乙酸银、碘及50%的乙酸来制备表1的agm-212-7。
[0360]
实施例8.agm-212-8的制备
[0361]
8-1.化学式11
[0362]
在实施例5的制备过程中,通过用cys取代第16位ser并用cys(acm)取代第24位gln来制备化学式11。
[0363]
化学式11:
[0364]
his-ser-gln-gly-thr-phe-thr-ser-asp-tyr-ser-lys-tyr-leu-asp-cys-arg-arg-ala-gln-asp-phe-val-cys(acm)-trp-leu-met-asn-thr-oh
[0365]
8-2.化学式12
[0366]
通过向化学式11中添加构成十一糖结构的溴乙酰聚糖(11suar)及naoh、磷酸盐缓冲液来制备化学式12。
[0367]
化学式12:
[0368]
his-ser-gln-gly-thr-phe-thr-ser-asp-tyr-ser-lys-tyr-leu-asp-cys(11sugar)-arg-arg-ala-gln-asp-phe-val-cys(acm)-trp-leu-met-asn-thr-oh
[0369]
8-3.agm-212-8
[0370]
通过向化学式6和化学式12中添加乙酸银、碘及50%的乙酸来制备表7的agm-212-8。
[0371]
表7
[0372][0373]
实验例1.类似物与glp-1受体的结合力的确认
[0374]
使用荧光素酶检测系统(luciferase assay system)检测实施例1至实施例6中制备的类似物与glp-1受体的结合力。荧光素酶检测系统是一种通过测定细胞的特定受体与配体的结合力来检测受体的活性程度的方法。
[0375]
具体地,在96孔白色细胞培养板中培养成纤维细胞系cv-1(1
×
104个细胞/ml,韩
国细胞系银行)24小时后,添加人glp-1r(pcdna3.1_hglp-1r)、camp反应元件(cre,pcdna3.1_hcre)进行转化。培养24小时后,将培养基更换为无血清培养基,培养16小时后,将各类似物处理6小时。使用光度计通过激活的glp-1r对作为报告基因的荧光素酶的表达水平进行定量,其结果如表8所示。
[0376]
表8
[0377]
命名ec
50
(nm)e
max
(基础诱导倍数(fold induction over basal))ex40.8
±
0.1210.6
±
1.5agm-2120.91
±
0.2110.4
±
1.4agm-212-10.13
±
0.410.1
±
1.2agm-212-20.11
±
0.810.2
±
1.3agm-212-38
±
0.710.1
±
1.4agm-212-432
±
1.710.2
±
1.2agm-212-525
±
1.210.4
±
1.1agm-212-634
±
1.57.2
±
1.3agm-212-716
±
1.510.2
±
1.3agm-212-825
±
1.510.3
±
1.5
[0378]
可通过表8确认,agm-212-1及agm-212-2的ec
50
水平比ex4增加约6倍以上。通过结果可知,由二硫键组成的糖基化的艾塞那肽同种类似物对glp-1受体活性高于ex4,甚至高于agm-212。并且观察到agm-212-3的ec
50
水平降低约10倍,观察到agm-212-4、agm-212-5及agm-212-6的活性比agm-212-3降低约4~5倍。通过结果可知,胰高血糖素与艾塞那肽类似物通过二硫键结合,因此对glp-1受体的活性有所降低,它们的异种类似物结构中,胰高血糖素的糖基化可降低glp-1受体的活性。但是,所有类似物对glp-1受体表现出nm水平的高结合力,可见它们具有选择性和特异性激动剂的功能。
[0379]
通过结果确认,agm-212对glp-1r的活性与ex4相同,与十一糖结合的agm-212类似物与ex4或agm-212相比具有有所降低的活性。并且可知,虽然各类似物的活性由于十一糖而降低,但仍然具有nm水平的结合力。
[0380]
实验例2.类似物的胰岛素分泌能力的确认
[0381]
为了确认实施例1至实施例2中制备的类似物的胰岛素分泌能力,确认了类似物对大鼠胰岛的葡萄糖依赖性胰岛素分泌能力。取出8周龄的sd大鼠(damul science)的胰腺,分离胰岛。用28mm的葡萄糖中的不同浓度(10nm,100nm)的各类似物处理分离的胰岛后,利用大鼠胰岛素elisa试剂盒测定分泌的胰岛素量,其结果如图6及表9所示。
[0382]
表9
[0383][0384]
可通过图6及表9确认,糖基化艾塞那肽同种类似物与艾塞那肽及agm-212相比表现出以浓度依赖性方式增加的胰岛素分泌能力。
[0385]
实验例3.类似物的抗糖尿病效果的确认
[0386]
为了确认实施例1至实施例6中制备的类似物的抗糖尿病效果,在作为2型糖尿病小鼠模型的c57bks/j dbdb mice(5~7周龄,中心实验动物)中确认血糖降低效果。
[0387]
具体地,皮下给药20nmole/kg的各类似物,经过0小时、1小时、2小时、4小时、6小时、8小时、12小时、18小时、24小时、44小时、48小时后,从小鼠尾静脉采集血液并测量血糖水平,其结果如图7a至图8b所示。
[0388]
可通过图7a至图7b确认,agm-212-2的血糖降低程度比ex4及agm-212更强。通过与agm-212-1比较活性结果可知,agm-212-1的第24位cys的糖基化表现出降低的抗糖尿病功效。
[0389]
可通过图8a至图8b可知,agm-212-3、agm-212-4、agm-212-5均表现出显著的抗糖尿病功效,但与agm-212相比表现出有所降低的功效。经确认,在抗糖尿病功效方面,在agm-212-4、agm-212-5、agm-212-6的构成序列中胰高血糖素的构成残基上结合糖的结构没有因各残基而显示出显著的活性差异。经确认,agm-212-7、agm-212-8为由互不相同的残基被糖基化的胰高血糖素与agm-212通过二硫键形成的形式,具有与ex4相似的抗糖尿病功效。
[0390]
实验例4.类似物的药代动力学试验
[0391]
对实施例1至实施例8中制备的类似物进行药代动力学试验。向野生型c57bl/6jmice(雄性,5~6周龄,n=5)皮下给药50nmole/kg的各类似物后,分别在0小时、0.5小时、1小时、2小时、4小时、8小时、10小时、12小时、14小时、24小时时采集血液。从采集的血液中分离血浆并利用exendin-4eia进行定量分析。将结果利用winnolin程序分析来确定药动学参数,其结果如图9a至图9b所示。
[0392]
表10
[0393][0394]
可通过图9a至图9b及表10确认,所有类似物表现出比ex4显著增加的半衰期,具体地,agm-212-2、agm-212-3、agm-212-4、agm-212-5、agm-212-6、agm-212-7、agm-212-8与agm-212相比都表现出增加约1~1.5倍以上的半衰期水平。其结果显示,艾塞那肽二聚体类似物通过如二硫键等特定键大幅增加体内稳定性。
[0395]
实验例5.类似物在肥胖症动物模型中的体重及饮食调节能力的确认
[0396]
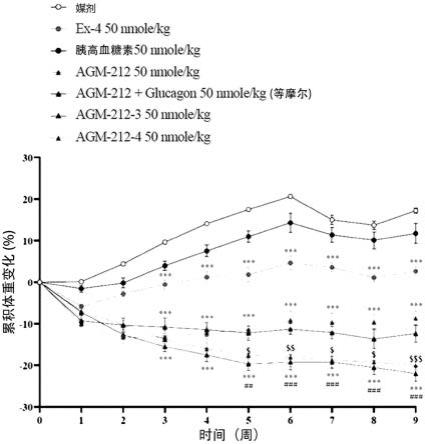
对实施例3中制备的类似物在肥胖症动物模型中的体重减轻及饮食调节能力进行实验及评价。为了使c57bl/6小鼠同时具有肥胖症和高血糖症状,建立了诱导摄入含有60%以上脂肪的高脂肪饮食的肥胖症动物模型。每天一次向16周龄的肥胖症小鼠皮下给药50nmole/kg的agm-212-3及agm-212-4,共9周。其结果如图10a至图10c及表11所示。
[0397]
表11
[0398]
组体重变化量(%)vehicle17.17
±
0.56ex4-2.63
±
1.06agm-21211.71
±
2.40胰高血糖素-8.67
±
1.76agm-212 胰高血糖素-12.36
±
2.11agm-212-3-21.95
±
1.83agm-212-4-20.04
±
2.21
[0399]
可通过图10a至图10c及表11确认,从第3周开始,各类似物给药组的体重显著减轻,从第5周开始,与agm-212给药组或agm-212 胰高血糖素给药组相比具有显著差异。在实验结束的第9周,agm-212-3及agm-212-4给药组的饮食摄入量也显著减少。
[0400]
实验例6.类似物在肥胖症动物模型中的葡萄糖耐量改善效果的确认
[0401]
实施例5的实验过程中确认了7周时间的由agm-212-3产生的葡萄糖耐量改善效果。具体地,在实验的第7周,将肥胖症小鼠禁食16小时后,皮下给药10nmole/kg的各类似物,30分钟后,腹腔给药葡萄糖(1.5g/kg)。在120分钟内,在0分钟、15分钟、30分钟、45分钟、60分钟、90分钟、120分钟时从小鼠尾静脉采集血液并利用血糖仪(acu-check,罗氏,德国)测量血糖,其结果如图11a至图11b及表12所示。
[0402]
表12
[0403]
组血糖(blood glucose)(曲线下面积(area under curve))vehicle43957.5
±
2483.8ex417795.0
±
2137.4agm-21245846.2
±
5538.1胰高血糖素29029.5
±
1784.5agm-212 胰高血糖素23687.5
±
3393.1agm-212-319545
±
623.1agm-212-420936.2
±
837.3
[0404]
可通过图11a至图11b及表12确认,各类似物给药组的小鼠组的血糖降低,与对照组相比,在各血糖测量时间血糖显著降低。上述结果表明,在长期给药类似物后,肥胖症小鼠的葡萄糖耐量得到改善。
[0405]
实验例7.类似物在肥胖症动物模型中的胰岛素抵抗改善效果的确认
[0406]
据报道,肥胖症引起的体内脂肪堆积增加会增加对产生胰岛素的胰岛β细胞的脂毒性,从而减少胰岛素的产生量,并抑制肝脏和肌肉中的胰岛素消耗,这些组织吸收和储存在餐后增加的血糖,从而通过诱导高胰岛素血症和降低胰岛素功能而导致高血糖症状,其
主要原因为胰岛素抵抗增加。
[0407]
使用实验例5的9周龄肥胖症小鼠,在相当于8周的长期给药实验期间进行胰岛素抵抗实验,确认长期给药后的胰岛素敏感性(insulin sensitivity),长期给药实验结束后,采集小鼠血液,通过小鼠胰岛素elisa(mouse insulin elisa)分析血液中的胰岛素浓度,确认是否改善了胰岛素抵抗(insulin resistance)。
[0408]
具体地,将长期给药实验第8周的肥胖症小鼠禁食6小时后,将各类似物以1nmol/kg的浓度皮下给药,30分钟后,腹腔给药胰岛素(1unit/kg)。经过0分钟、15分钟、30分钟、60分钟、90分钟、120分钟后,从小鼠尾部采集血液并利用血糖仪(acc-check,罗氏,德国)测量血糖以分析胰岛素敏感性,其结果如图12a至12b及表13、表14所示。
[0409]
表13
[0410]
组血糖(曲线下面积)vehicle21231.2
±
293.4ex411847.0
±
582.7agm-21223749.5
±
387.6胰高血糖素13102.5
±
638.8agm-212 胰高血糖素15222.0
±
263.6agm-212-313288.5
±
409.1agm-212-413966.2
±
504.1
[0411]
表14
[0412][0413]
可通过图12a至12b及表13确认,给药各类似物的实验组的血糖对腹腔给药的胰岛素表现出高敏感性,血糖迅速下降。
[0414]
并且,可通过表14确认,实验结束后,给药类似物的小鼠组的血液中的胰岛素浓度显著降低。
[0415]
上述结果表明,可通过长期给药agm-212-3及agm-212-4改善胰岛素敏感性、高胰岛素血症,从而诱导肥胖症小鼠的胰岛素功能的恢复。
[0416]
实验例8.类似物在肥胖症动物模型中的肝脏中的脂肪堆积量变化的确认
[0417]
众所周知,由于高脂肪饮食摄入导致的体重过重和肥胖症的发生会增加作为代谢性疾病的非酒精性脂肪性肝病(non-alcoholic fatty liver disease)的发病率,该疾病是在作为代谢组织的肝脏中的脂肪堆积及肝细胞内脂质合成等增加所导致。为了确认长期给药agm-212-3后肥胖症小鼠的体重减轻是否会影响作为相关代谢性疾病的脂肪肝症状的
缓解,通过作为脂质确认染色法的油红o染色(oil red o staining)分析肝组织中的脂质量,并且,通过分解肝组织来确认作为细胞内脂质储存形式的甘油三酯的量。
[0418]
具体地,实验例5的9周长期给药实验结束后,取出小鼠肝脏并按叶(lobe)分离,部分用4%的甲醛(formaldehyde)固定,然后制备石蜡块,切片后放置于制备的载玻片上用作为脂质确认染色试剂的油红o进行染色,然后通过显微镜观察。为了测定肝组织中甘油三酯的量,将分离的肝组织用70μm细胞过滤网(cell strainer)分解后,将以14000rpm离心得到的含有甘油三酯的上清液按一定比例稀释后,并利用甘油三酯elisa分析。其结果图13a至图13b所示。
[0419]
表15
[0420]
组肝脏甘油三酯(hepatic triglyceride)(mg/g)vehicle39.38
±
4.08agm-2127.50
±
1.01agm-212-33.58
±
0.12
[0421]
可通过图13a至图13b及表15确认,给药agm-212-3的小鼠的肝脏中被油红o染色的脂质范围减少,肝组织中的甘油三酯的量也显著减少。
[0422]
上述结果表明,长期给药agm-212-3后的体重减轻具有降低肥胖症小鼠因摄入高脂肪饮食引起的脂肪肝发病风险的效果。
[0423]
实验例9.类似物在肥胖症动物模型中的血液中代谢参与因子量变化的确认
[0424]
当发生2型糖尿病和肥胖症时,由于在组织中对每种激素的抵抗,作为血糖调节激素的胰岛素和作为饮食调节激素的瘦素在血液中的浓度变得高于正常水平,将这些症状分别称为高胰岛素血症和高瘦素血症,用作代谢性疾病诊断的标志。血液中胆固醇和甘油三酯等脂质浓度的升高,即高脂血症是体重过重和肥胖症的代表性症状,是衡量肥胖程度的代表性标志。
[0425]
为了确定实验例5中的长期给药agm-212-3是否诱导了如胰岛素、瘦素抵抗及肥胖程度等代谢异常症状的改善,实验结束后,采集小鼠血液,并通过与需要确认的各因子对应的elisa检测来分析血液中代谢参与因子量,其结果图表13所示。
[0426]
可通过表14确认,给药agm-212-3的小鼠组的血液中的胰岛素、瘦素的浓度显著降低,胆固醇、甘油三酯的脂质浓度也显著降低。
[0427]
上述结果表明,可通过给药agm-212-3诱导肥胖症小鼠因摄入高脂肪饮食引起的对代谢激素的抵抗及高脂血症的改善。
[0428]
实验例10.类似物在肥胖症动物模型中的热能产生增加效果的确认
[0429]
据报道,由胰高血糖素和胰高血糖素受体在棕色脂肪组织中的相互作用诱导的热能产生增加使作为蛋白质的解偶联蛋白-1(uncoupling protein 1,ucp-1)在线粒体中的表达增加,从而在由脂肪酸的氧化产生的乙酰辅酶a(acetyl coa)的氧化、还原过程中产生的氢气被阻止用于氧化磷酸化,即呼吸,使氢气通过ucp1,此时产生的能量以热量的形式释放出来,从而增加体内堆积的脂肪的消耗,对体重减轻起着重要作用。
[0430]
为了确认agm-212-3对增加热能产生的效果,每天一次向16周龄的肥胖症小鼠(diet induced obese c57bl/6)皮下给药5周后,测量热能产生量、运动量、呼吸系数、直肠温度。
[0431]
具体地,将长期给药5周的小鼠在与作为能量代谢分析装置的间接能量测定系统(indirect calorimetry system)相连的代谢笼(metabolic cage)中饲养24小时,每隔1小时测量呼吸消耗的氧气量和排出的二氧化碳量来分析呼吸系数(respiratory quotient),呼吸系数为可确认热能产生量和体内消耗的营养素喜好度的指标。24小时后,将小鼠从代谢笼中取出,通过肝门插入热探针(thermal probe)来测量直肠温度,其结果如图14a至图14b所示。
[0432]
表16
[0433][0434]
可通过图14a至图14b及表16确认,在白天和夜间时间段以12小时间隔测量的给药agm-212-3的小鼠组的热能消耗量和直肠温度显著增加。相反,经确认,与对照组相比,运动模式发生了变化,但总运动量没有显著变化。并且,呼吸系数在白天和夜间时间段均显著下降,接近0.7。
[0435]
上述结果表明,无论肥胖症小鼠的运动量如何,类似物使胰高血糖素活性长期维持从而使消耗脂肪的热能产生增加,在体重减轻中发挥重要作用。
[0436]
实验例11.类似物在肥胖症动物模型中的热能产生参与因子量变化的确认
[0437]
为了验证实验例10中agm-212-3增加热能产生的机制,在5周的长期给药实验后分离小鼠棕色脂肪组织,通过蛋白免疫印迹(western blotting)和实时定量聚合酶链反应(quantitative real time polymerase chain reaction,qrt-pcr)分析热能产生机制的主要因子ucp1、prdm16、cidea的表达量。并且,对固定在4%的多聚甲醛(paraformaldehyde)中的棕色脂肪组织处理对ucp1具有特异性亲和力(affinity)的抗体来观察ucp1在棕色脂肪组织中的表达量,其结果如图15a至图15b。
[0438]
表17
[0439][0440]
表18
[0441][0442]
可通过图15a至图15b及表17、表18确认,与对照组相比,类似物给药组的棕色脂肪组织中ucp1蛋白表达量、ucp-1、prdm16、cidea mrna表达量均显著增加。并且,通过免疫组织化学(immunohistochemistry,ihc)图像确认,与对照组相比,棕色脂肪组织中ucp1量也增加。
[0443]
上述结果表明,agm-212-3通过激活棕色脂肪组织中的胰高血糖素受体来增加用于调节热能产生参与因子表达的信号转导途径的产生。
[0444]
实验例12.类似物的脂肪分解能力的确认
[0445]
为了确认长期给药agm-212-3后脂肪组织的减少及组织中脂质合成/分解机制的主要因子的表达水平的变化,上述实施例11的长期给药实验结束后,分离睾丸和腹股沟的白色脂肪组织和皮下的棕色脂肪组织并测量每个组织的大小后,通过蛋白免疫印迹和qrt-pcr分析每种代谢因子的表达量变化,其结果如图16a至图16e所示。
[0446]
如图16a至图16e所示,通过蛋白免疫印迹确认,实验组小鼠的睾丸的白色组织中作为脂肪分解信号转导重要因子的蛋白激酶a(protein kinase a)和脂解酶hsl的蛋白质表达显著增加。
[0447]
并且,通过qrt-pcr确认,脂解酶atgl、hsl和在脂肪分解作用中作为主要因子的脂围蛋白(perilipin)的mrna表达量显著增加,参与脂质合成及细胞内脂肪酸吸收的cd36、pparr、c/ebpa、fabp4的mrna表达量显著减少。
[0448]
此外,通过蛋白免疫印迹和qrt-pcr确认,实验组小鼠的腹股沟的白色脂肪组织中脂质合成信号转导的主要因子fas的蛋白质表达量和scd、acaca1的mrna表达量减少,相反,脂肪酸的β氧化(beta-oxidation)信号转导的主要因子acsl1的蛋白质表达量、cpt1a、cpt2、cact、pgc-1a蛋白质表达量、mrna表达量显著增加。
[0449]
实验例13.类似物在肌肉细胞中的脂肪分解能力及热能产生效果的确认
[0450]
据报道,骨骼肌作为主要负责基础代谢率的器官,通过与棕色脂肪组织相同的机制增加热能的产生,在体重调节中发挥重要作用。
[0451]
对此,为了验证agm-212-3是否可以增加肌肉中热能产生的功能,通过蛋白免疫印迹和qrt-pcr对成肌细胞系c2c12分析脂质合成、分解、脂肪酸转运信号转导及相关代谢因子的表达量的变化,其结果如图17a至图17c所示。
[0452]
如图17a至图17c所示,通过蛋白免疫印迹确认,当处理作为脂肪酸的棕榈酸(0.75mm)时,与对照组相比,c2c12细胞内热能产生信号转导途径的主要信号转导因子ampk的磷酸化程度降低,但是,当处理不同浓度(10nm、20nm、50nm、100nm)的类似物时,ampk的磷酸化程度以浓度依赖性方式显著增加。
[0453]
并且,通过qrt-pcr确认,c2c12细胞内脂肪酸代谢及线粒体基质中脂肪酸转运参与因子(acsl1、cpt1a、cpt2、cact)和脂肪酸的β氧化信号转导因子(acox1、pgc-1a、foxa2)的mrna表达量以所处理的缀合物的浓度依赖性方式显著增加,相反,脂质合成信号转导因子(fas、srebp-1c)的mrna表达量以缀合物的浓度依赖性方式减少。
[0454]
上述结果表明,像棕色脂肪组织一样,agm-212-3增加骨骼肌中的热能产生,并可以抑制脂质合成,具有有效的体重减轻能力。
[0455]
产业上的可利用性
[0456]
本发明涉及糖基化艾塞那肽类似物及其用途,以及艾塞那肽二聚体类似物及其用途。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。