1.本发明的实施方式涉及一种荧光标识剂、及用于荧光标识剂的荧光色素。
背景技术:
2.生物成像是使生物体内的蛋白质、细胞、及组织等可视化的技术。生物成像例如广泛应用于生物体内的分子及细胞的功能的阐明、以及制药研究等生物学及医学的研究领域。
3.其中,荧光生物成像法是能够进行现象的动态观察、多颜色观察、及高感度观察的成像法。近年来,荧光生物成像法作为一种能够非侵害地诊断的成像法也备受关注,期待在对患者的负担少的图像诊断、及手术中的实时诊断等临床实践中的应用。
4.荧光生物成像法是使用与靶物质特异性地结合的结合型、或者集聚在靶部位的集聚型的荧光色素使靶可视化的方法。在所述方法中,对向所述荧光色素照射紫外区域到近红外区域的光时发出的荧光进行检测。
5.与使用和靶物质特异性结合的结合型荧光生物成像相比,使用向靶部位集聚的集聚型荧光生物成像的标识方法更简单且更迅速。另外,所述集聚型荧光生物成像具有以下优点:由于不需要与靶物质的特异性结合,因此直至荧光强度稳定为止的待机时间长,对靶物质的影响为最小限度。
6.在专利文献1及专利文献2中公开一种以集聚在形成细胞膜的磷脂质中为特征的集聚型荧光色素。
7.磷脂质形成细胞、脂质体、及细胞外囊泡等各种生物体物质的表面。近年来,如用于药物传递系统(drug delivery system,dds)的脂质体成像、及非专利文献1中所记载的外切体(exosome)成像等那样,具有磷脂质的微小物质的成像受到关注。在为了进行此种体外(in vitro)及体内(in vivo)中的成像而使用专利文献1及专利文献2中公开的荧光色素的情况下,存在荧光强度低的问题。
8.现有技术文献
9.专利文献
10.专利文献1:日本专利特开2009-524580号公报
11.专利文献2:日本专利特开2008-209361号公报
12.非技术文献
13.非专利文献1:药物传递系统(drug delivery system)第29卷,第2号,2014年3月25日发行,p.116-124
技术实现要素:
14.发明所要解决的问题
15.鉴于所述情况,本发明的实施方式提供一种荧光色素,所述荧光色素向磷脂质的集聚性优异,显示出高的荧光强度,特别是具有适合用于体外(in vitro)及体内(in vivo)
的成像的荧光标识剂的荧光强度。
16.解决问题的技术手段
17.本发明人们为了解决所述课题而反复努力研究,结果发现了优异的荧光色素,从而完成了本发明。即,本发明的实施方式涉及以下内容。其中,本发明并不限定于以下的实施方式,包含各种实施方式。
18.一实施方式涉及一种荧光标识剂,包含下述通式(1)所表示的荧光色素。
19.通式(1):
20.q-z-r
1-r
2-r321.式中,q表示荧光色素的残基。
22.z表示直接键、经取代或未经取代的亚烷基、或者经取代或未经取代的亚芳基。
23.r1表示直接键、-o-、-op(=o)r
4-、-oc(=o)-、-os(=o)
2-、-osir5r
6-、-c(=o)-、或-c(=o)nh-。
24.r2表示选自由经取代或未经取代的亚烷基、经取代或未经取代的亚芳基、及经取代或未经取代的杂环基所组成的群组中的一种基、或者将这些基组合而成的基。
25.r3表示coom1、nr7r8、n
r9r
10r11
、-om2、或-p(=o)(om3)om4。
26.所述中,r4表示氢原子、羟基、经取代或未经取代的烷基、经取代或未经取代的芳基、经取代或未经取代的烷氧基、经取代或未经取代的芳氧基、或者经取代或未经取代的杂环基。
27.r5及r6分别独立地表示经取代或未经取代的烷基、经取代或未经取代的芳基、或者经取代或未经取代的杂环基。
28.r7~r
11
分别独立地表示氢原子、经取代或未经取代的烷基、或者经取代或未经取代的芳基。
29.m1、m2、m3、及m4分别独立地表示氢原子、或一价阳离子。
30.在一实施方式中,优选为所述荧光标识剂为磷脂质集聚型荧光标识剂。
31.在一实施方式中,优选为所述荧光色素包含下述通式(2)所表示的酞菁色素。
32.[化1]
[0033]
通式(2):
[0034][0035]
式中,x1~x
16
分别独立地表示-z-r
1-r
2-r3、氢原子、经取代或未经取代的烷基、经取代或未经取代的芳基、经取代或未经取代的环烷基、经取代或未经取代的烯基、经取代或未经取代的杂环基、-ab、-so3m5、或者-coom6。
[0036]
所述中,a表示16族元素。b表示氢原子、经取代或未经取代的烷基、经取代或未经取代的芳基、经取代或未经取代的环烷基、或者经取代或未经取代的杂环基。m5及m6分别独立地表示一价阳离子。
[0037]
x1~x
16
中邻接的取代基彼此可相互连结而形成环。
[0038]
x
17
表示-z-r
1-r
2-r3、羟基、卤素元素、经取代或未经取代的烷氧基、经取代或未经取代的芳氧基、-op(=o)x
18
x
19
、-oc(=o)x
20
、-os(=o)2x
21
、或者-osix
22
x
23
x
24
。
[0039]
所述中,x
18
及x
19
分别独立地表示氢原子、羟基、经取代或未经取代的烷基、经取代或未经取代的芳基、经取代或未经取代的烷氧基、经取代或未经取代的芳氧基、或者经取代或未经取代的杂环基。
[0040]
x
20
表示氢原子、经取代或未经取代的烷基、经取代或未经取代的芳基、或者经取代或未经取代的杂环基。
[0041]
x
21
表示羟基、经取代或未经取代的烷基、经取代或未经取代的芳基、或者经取代或未经取代的杂环基。
[0042]
x
22
~x
24
分别独立地表示经取代或未经取代的烷基、经取代或未经取代的芳基、或者经取代或未经取代的杂环基。
[0043]
y表示二价~五价的金属原子,k为整数。y为二价的金属原子时的k为0,y为三价的金属原子时的k为1,y为四价或五价的金属原子时的k为2。
[0044]
其中,所述中,x1~x
17
中的至少一个为-z-r
1-r
2-r3。
[0045]
在一实施方式中,优选为所述荧光标识剂包含所述通式(2)的x
17
为-z-r
1-r
2-r3的荧光色素。
[0046]
一实施方式涉及一种化合物,由下述通式(3)表示。
[0047]
[化2]
[0048]
通式(3):
[0049][0050]
式中,x1~x
16
分别独立地表示-z-r
1-r
2-r3、氢原子、经取代或未经取代的烷基、经取代或未经取代的芳基、经取代或未经取代的环烷基、经取代或未经取代的烯基、经取代或未经取代的杂环基、-ab、-so3m5、或者-coom6。
[0051]
所述中,a表示16族元素。b表示氢原子、经取代或未经取代的烷基、经取代或未经取代的芳基、经取代或未经取代的环烷基、或者经取代或未经取代的杂环基。m5及m6分别独立地表示一价阳离子。
[0052]
x1~x
16
中邻接的取代基彼此可相互连结而形成环。
[0053]
x
17
表示-z-r
1-r
2-r3、羟基、卤素元素、经取代或未经取代的烷氧基、经取代或未经取代的芳氧基、-op(=o)x
18
x
19
、-oc(=o)x
20
、-os(=o)2x
21
、或者-osix
22
x
23
x
24
。
[0054]
所述中,x
18
及x
19
分别独立地表示氢原子、羟基、经取代或未经取代的烷基、经取代或未经取代的芳基、经取代或未经取代的烷氧基、经取代或未经取代的芳氧基、或者经取代或未经取代的杂环基。
[0055]
x
20
表示氢原子、经取代或未经取代的烷基、经取代或未经取代的芳基、或者经取代或未经取代的杂环基。
[0056]
x
21
表示羟基、经取代或未经取代的烷基、经取代或未经取代的芳基、或者经取代或未经取代的杂环基。
[0057]
x
22
~x
24
分别独立地表示经取代或未经取代的烷基、经取代或未经取代的芳基、或者经取代或未经取代的杂环基。
[0058]
y表示二价~五价的金属原子,k为整数。y为二价的金属原子时的k为0,y为三价的金属原子时的k为1,y为四价或五价的金属原子时的k为2。
[0059]
其中,所述中,x1~x
17
中的至少一个为-z-r
1-r
2-r3,如以下那样。
[0060]
z表示直接键、经取代或未经取代的亚烷基、或者经取代或未经取代的亚芳基。
[0061]
r1表示直接键、-o-、-op(=o)r
4-、-oc(=o)-、-os(=o)
2-、-osir5r
6-、-c(=o)-、或-c(=o)nh-。
[0062]
r2表示选自由经取代或未经取代的亚烷基、经取代或未经取代的亚芳基、及经取代或未经取代的杂环基所组成的群组中的一种基、或者将这些基组合而成的基。
[0063]
r3表示coom1、nr7r8、n
r9r
10r11
、-om2、或-p(=o)(om3)om4。
[0064]
所述中,r4表示氢原子、羟基、经取代或未经取代的烷基、经取代或未经取代的芳基、经取代或未经取代的烷氧基、经取代或未经取代的芳氧基、或者经取代或未经取代的杂环基。r5及r6分别独立地表示经取代或未经取代的烷基、经取代或未经取代的芳基、或者经取代或未经取代的杂环基。r7~r
11
分别独立地表示氢原子、经取代或未经取代的烷基、或者经取代或未经取代的芳基。m1、m2、m3、及m4分别独立地表示氢原子、或一价阳离子。
[0065]
本技术的公开与2020年4月2日提出申请的日本专利特愿2020-066924号中记载的主题相关联,其全部的公开内容通过引用而被援引至本技术中。
[0066]
发明的效果
[0067]
根据本发明的实施方式,通过导入向磷脂质的集聚性高的官能基,能够提供一种具有适合用于体外(in vitro)及体内(in vivo)的成像的荧光标识剂的荧光强度的荧光色素。
附图说明
[0068]
图1是表示荧光标识剂1、荧光标识剂15、荧光标识剂19、荧光标识剂24、荧光标识剂25、荧光标识剂68、荧光标识剂75的荧光强度的评价结果的图表。
[0069]
图2是利用荧光标识剂1标识出的细胞的荧光显微镜照片。
[0070]
图3是利用荧光标识剂15标识出的细胞的荧光显微镜照片。
[0071]
图4是利用荧光标识剂19标识出的细胞的荧光显微镜照片。
[0072]
图5是利用荧光标识剂24标识出的细胞的荧光显微镜照片。
[0073]
图6是利用荧光标识剂25标识出的细胞的荧光显微镜照片。
[0074]
图7是利用荧光标识剂68标识出的细胞的荧光显微镜照片。
[0075]
图8是利用荧光标识剂75标识出的细胞的荧光显微镜照片。
[0076]
图9是利用荧光标识剂42标识出的细胞的荧光显微镜照片。
[0077]
图10是利用荧光标识剂53标识出的细胞的荧光显微镜照片。
具体实施方式
[0078]
以下,对本发明的实施方式进行详细说明。其中,本发明的实施方式并不限定于以下的记载,包含各种实施方式。
[0079]
作为本发明的一实施方式的荧光标识剂包含下述通式(1)所表示的化合物。下述通式(1)所表示的化合物为荧光色素。
[0080]
通式(1):
[0081]
q-z-r
1-r
2-r3[0082]
式中,q表示荧光色素的残基。本说明书中荧光色素是指照射紫外区域至近红外区域的光(例如,波长560nm~900nm的光)时发出荧光的色素,可为公知的化合物。作为荧光色素,并无特别限定,但例如可列举:荧光素类、罗丹明类、香豆素类、花青类、酞菁类、二酮吡咯并吡咯类、硼二吡咯亚甲基(boron dipyrromethene,bodipy)类、呫吨类、芘类、部花青类、苝类、吖啶类、二苯乙烯类、吡咯亚甲基类、吖啶类、及伞形花内酯(umbelliferone)类等色素。
[0083]
在一实施方式中,所述通式(1)所表示的化合物(荧光色素)例如可具有所述例示的色素的骨架作为荧光色素的残基q。即,所述通式(1)所表示的化合物可为具有对于所述例示的色素的骨架导入至少一个由-z-r
1-r
2-r3表示的取代基(官能基)的结构的化合物。
[0084]
在一实施方式中,就稳定性、及荧光波长的观点而言,荧光色素优选为酞菁类。在一实施方式中,可将下述通式(2)所表示的化合物(酞菁色素)优选地用作荧光色素。其中,以式中x1~x
17
的至少一个为-z-r
1-r
2-r3所表示的取代基为前提。
[0085]
在构成所述荧光标识剂的荧光色素包含下述通式(2)所表示的化合物的情况下,可容易地获得源自酞菁色素的骨架、且具有优异的耐久性的荧光标识剂。另外,可容易地获得源自酞菁色素的骨架、且适合体外及体内的生物成像的波长(例如,650nm~900nm)下的发光。
[0086]
[化3]
[0087]
通式(2):
[0088]
[0089]
在所述实施方式的荧光色素中,
“‑
z-r
1-r
2-r
3”是具有亲水基的取代基,通过与磷脂质中的亲水基的静电相互作用,可提高荧光色素对磷脂质的集聚性。所述取代基的具体的结构如以下那样。
[0090]
z表示直接键、经取代或未经取代的亚烷基、或者经取代或未经取代的亚芳基。在一实施方式中,z优选为直接键。
[0091]
r1表示直接键、-o-、-op(=o)r
4-、-oc(=o)-、-os(=o)
2-、-osir5r
6-、-c(=o)-、或-c(=o)nh-。在一实施方式中,r1优选为-op(=o)r
4-、-os(=o)
2-、或-osir5r
6-。
[0092]
r2表示选自由经取代或未经取代的亚烷基、经取代或未经取代的亚芳基、及经取代或未经取代的杂环基所组成的群组中的一种基、或者将这些基组合而成的基。在一实施方式中,r2优选为经取代或未经取代的亚烷基、或者经取代或未经取代的亚芳基,或者更优选为经取代或未经取代的亚烷基。在一实施方式中,r2优选为亚烷基。亚烷基的主链的碳数优选为1~10。
[0093]
r3表示-coom1、-nr7r8、或-n
r9r
10r11
。另外,r3表示-om2、或-p(=o)(om3)om4。在一实施方式中,r3优选为-coom1、-nr7r8、-om2、或-p(=o)(om3)om4。
[0094]
所述中,r4表示氢原子、羟基、经取代或未经取代的烷基、经取代或未经取代的芳基、经取代或未经取代的烷氧基、经取代或未经取代的芳氧基、或者经取代或未经取代的杂环基。在一实施方式中,r4优选为氢原子、羟基、经取代或未经取代的烷基、或者未经取代的芳基。
[0095]
r5及r6分别独立地表示经取代或未经取代的烷基、经取代或未经取代的芳基、或者经取代或未经取代的杂环基。在一实施方式中,r5及r6优选为分别独立地为经取代或未经取代的烷基、或者未经取代的芳基。所述烷基更优选为碳数1~5的直链或分支的烷基。
[0096]
r7~r
11
分别独立地表示氢原子、经取代或未经取代的烷基、或者经取代或未经取代的芳基。在一实施方式中,r7~r
11
优选为分别独立地为氢原子、或者经取代或未经取代的烷基。烷基更优选为碳数1~5的直链或分支的烷基。
[0097]
m1、m2、m3、及m4分别独立地表示氢原子、或一价阳离子。作为一价阳离子,例如可列举碱金属、及四级胺等。作为碱金属,可列举:锂、钠、钾、铷、及铯等。在一实施方式中,m1、m2、m3、及m4优选为分别为氢原子。
[0098]
x1~x
16
分别独立地表示氢原子、或者选自由-z-r
1-r
2-r3、经取代或未经取代的烷基、经取代或未经取代的芳基、经取代或未经取代的环烷基、经取代或未经取代的烯基、经取代或未经取代的杂环基、-ab、-so3m5、-coom6所组成的群组中的取代基。
[0099]
所述中,m5及m6分别独立地表示一价阳离子。作为一价阳离子,例如可列举碱金属、及四级胺等。作为碱金属,可列举:锂、钠、钾、铷、及铯等。
[0100]
在一实施方式中,优选为x1~x
16
的至少一个、优选为四个以上为所述取代基。在一实施方式中,相对于色素骨架的所述取代基优选为分别独立地为经取代或未经取代的烷基、经取代或未经取代的芳基、或者-ab。
[0101]
在所述式-ab中,a表示第16族元素。作为第16族元素,可列举:氧、硫、硒、及碲等。在一实施方式中,a优选为氧、硫、或硒。就合成的容易度、及稳定性的方面而言,更优选为氧、或硫。就荧光强度的方面而言,进而优选为氧。b表示氢原子、经取代或未经取代的烷基、经取代或未经取代的芳基、经取代或未经取代的环烷基、或者经取代或未经取代的杂环基,
分别如前面说明那样。在一实施方式中,b优选为氢原子、经取代或未经取代的烷基、或者经取代或未经取代的芳基。因此,在一实施方式中,-ab优选为-or、-oar、-sr、或-sar。此处,r表示烷基,ar表示芳基。
[0102]
y表示二价~五价的金属原子,k为整数。y为二价的金属原子时的k为0,y为三价的金属原子时的k为1,y为四价或五价的金属原子时的k为2。作为二价的金属原子,可列举mg、cu、zn等。作为三价的金属原子,可列举al、ga、in等。作为四价的金属原子,可列举si、mn、sn、cr、zr等。作为五价的金属原子,可列举p等。就荧光强度的观点而言,y优选为al、si、或p,更优选为al。就耐光性的观点而言,y优选为al、或si。
[0103]
在一实施方式中,x1~x
16
中邻接的取代基彼此可相互连结而形成环。所述环的结构可为环烷基、环烯烃、芳基、杂芳基中的任一种,与酞菁骨架中的芳香环形成缩合环。所述环的结构可进一步具有取代基,也可未经取代。形成环的结构的碳数可为2~30,优选为4~6的范围。环优选为5元环或6元环。
[0104]
在一实施方式中,优选为邻接的取代基彼此相互连结而形成亚苯基。所述情况下,与酞菁骨架中的芳香环键结而形成萘结构。在其他实施方式中,邻接的取代基彼此可相互连结而形成包含氮原子的环。所述情况下,与酞菁骨架中的芳香环键结而形成例如咪唑结构。所述萘结构或咪唑结构等环结构也可还具有烷基或芳基等取代基。
[0105]
x
17
表示-z-r
1-r
2-r3、羟基、卤素元素、经取代或未经取代的烷氧基、经取代或未经取代的芳氧基、-op(=o)x
18
x
19
、-oc(=o)x
20
、-os(=o)2x
21
、-osix
22
x
23
x
24
。在一实施方式中,x
17
优选为-z-r
1-r
2-r3、或羟基。z、r1、r2、及r3如前面说明那样。
[0106]
所述中,x
18
及x
19
分别独立地表示氢原子、羟基、经取代或未经取代的烷基、经取代或未经取代的芳基、经取代或未经取代的烷氧基、经取代或未经取代的芳氧基、或者经取代或未经取代的杂环基。
[0107]
x
20
表示氢原子、经取代或未经取代的烷基、经取代或未经取代的芳基、或者经取代或未经取代的杂环基。
[0108]
x
21
表示羟基、经取代或未经取代的烷基、经取代或未经取代的芳基、或者经取代或未经取代的杂环基。
[0109]
x
22
~x
24
分别独立地表示经取代或未经取代的烷基、经取代或未经取代的芳基、或者经取代或未经取代的杂环基。
[0110]
此处,所述r4~r
11
、及x1~x
24
中的烷基可被分别独立地选择。烷基可具有取代基,也可为未经取代。
[0111]
作为烷基,可列举直链状或分支链状的烷基。作为具体例,可列举:甲基、乙基、丙基、丁基、戊基、己基、庚基、辛基、壬基、癸基、十二烷基、十八烷基、异丙基、异丁基、异戊基、2-乙基己基、仲丁基、叔丁基、仲戊基、叔戊基、叔辛基、及新戊基等。烷基的碳数优选为1~30的范围内。所述碳数更优选为1~20的范围,进而优选为1~10的范围。
[0112]
作为所述烷基中的取代基,除了可列举氟、氯、溴等卤素原子、羟基、氨基、硝基、甲酰基、氰基、羧基等以外,也可列举所述的烷基、后述的芳基、环烷基、杂环基。另外,在结构的一部分经酰胺键(-nhco-)、酯键(-coo-)、醚键(-o-)、脲键(-nhconh-)、或氨基甲酸酯键(-nhcoo-)取代的情况下,所述取代部分也视为“取代基”。
[0113]
因此,作为取代烷基,是指经所述取代基取代的烷基。取代烷基可为经一个或两个
以上的取代基取代的烷基。例如,作为经卤素原子取代的烷基的具体例,可列举:三氟甲基、2,2,2-三氟乙基、-(cf2)4cf3、-(cf2)5cf3、-(cf2)6cf3、-(cf2)7cf3、-(cf2)8cf3、三氯甲基、2,2-二溴乙基等。
[0114]
作为经酰胺键取代的烷基的具体例,可列举:-ch
2-ch
2-ch
2-nhco-ch
2-ch3、-ch
2-ch(-ch3)-ch
2-nhco-ch
2-ch3、-ch
2-ch
2-ch
2-nhco-ch
2-ch3、-ch
2-ch
2-ch
2-ch
2-nhco-ch
2-ch(ch
2-ch3)-ch
2-ch
2-ch
2-ch3、-(ch2)
5-nhco-(ch2)
11-ch3、-ch
2-ch
2-ch
2-c(-nhco-ch
2-ch3)3等。经酰胺键取代的烷基的碳数优选为2~30的范围内。所述碳数更优选为2~10的范围,进而优选为2~5的范围。
[0115]
作为经酯键取代的烷基的具体例,可列举:-ch
2-ch
2-ch
2-coo-ch
2-ch3、-ch
2-ch(-ch3)-ch
2-coo-ch
2-ch3、-ch
2-ch
2-ch
2-oco-ch
2-ch3、-ch
2-ch
2-ch
2-ch
2-coo-ch
2-ch(ch
2-ch3)-ch
2-ch
2-ch
2-ch3、-(ch2)
5-coo-(ch2)
11-ch3、-ch
2-ch
2-ch
2-ch-(coo-ch
2-ch3)2等。经酯键取代的烷基的碳数优选为2~30的范围内。所述碳数更优选为2~10的范围,进而优选为2~5的范围。
[0116]
作为经醚键取代的烷基的具体例,可列举:-ch
2-o-ch3、-ch
2-ch
2-o-ch
2-ch3、-ch
2-ch
2-ch
2-o-ch
2-ch3、-(ch
2-ch
2-o)
n-ch3(此处n为1至8的整数)、-(ch
2-ch
2-ch
2-o)
m-ch3(此处m为1至5的整数)、-ch
2-ch(ch3)-o-ch
2-ch
3-、-ch
2-ch-(och3)2等,但并不限定于这些。经醚键取代的烷基的碳数优选为2~30的范围内。所述碳数更优选为2~10的范围,进而优选为2~5的范围。
[0117]
作为经脲键(-nhconh-)取代的烷基的具体例,可列举:-ch
2-nhconh-ch3、-ch
2-ch
2-nhconh-ch
2-ch3、-ch
2-ch
2-ch
2-nhconh-ch
2-ch3、-(ch
2-ch
2-nhconh)
n-ch3(此处n为1至8的整数)、-(ch
2-ch
2-ch
2-nhconh)
m-ch3(此处m为1至5的整数)、-ch
2-ch(ch3)-nhconh-ch
2-ch
3-、-ch
2-ch-(nhconhch3)2等,但并不限定于这些。经醚键取代的烷基的碳数优选为2~30的范围内。所述碳数更优选为2~10的范围,进而优选为2~5的范围。
[0118]
作为经氨基甲酸酯键取代的烷基的具体例,可列举:-ch
2-ch
2-ch
2-nhcoo-ch
2-ch3、-ch
2-ch(-ch3)-ch
2-nhcoo-ch
2-ch3、-ch
2-ch
2-ch
2-nhcoo-ch
2-ch3、-ch
2-ch
2-ch
2-ch
2-nhcoo-ch
2-ch(ch
2-ch3)-ch
2-ch
2-ch
2-ch3、-(ch2)
5-nhcoo-(ch2)
11-ch3、-ch
2-ch
2-ch
2-ch-(nhcoo-ch
2-ch3)2等。经酯键取代的烷基的碳数优选为2~30的范围内。所述碳数更优选为2~10的范围,进而优选为2~5的范围。
[0119]
作为经酰胺键(-nhco-)、酯键(-coo-)、及醚键(-o-)、脲键(-nhconh-)、氨基甲酸酯键(-nhcoo-)中两种以上的取代基取代的烷基的具体例,可列举:-ch
2-ch
2-nhco-ch
2-ch
2-o-ch
2-ch(ch
2-ch3)-ch
2-ch
2-ch
2-ch3、-ch
2-ch
2-coo-ch
2-ch
2-o-ch
2-ch
2-nhcoo-ch
2-ch(ch
2-ch3)-ch
2-ch
2-ch
2-ch3、-ch
2-ch
2-nhco-ch2(oco-ch22)-ch
2-。经酰胺键(-nhco-)、酯键(-coo-)、醚键(-o-)、脲键(-nhconh-)、及氨基甲酸酯键(-nhcoo-)中两种以上的取代基取代的烷基的碳数优选为3~30的范围内。所述碳数更优选为3~10的范围,进而优选为3~5的范围。
[0120]
所述r4~r
11
、及x1~x
24
中的芳基可被分别独立地选择。芳基可具有取代基,也可未经取代。
[0121]
作为芳基,可列举单环、或缩合多环的芳基。例如可列举:苯基、1-萘基、2-萘基、对联苯基、间联苯基、2-蒽基、9-蒽基、2-菲基、3-菲基、9-菲基、2-芴基、3-芴基、9-芴基、1-芘
基、2-芘基、3-苝基、邻甲苯基、间甲苯基、对甲苯基、4-甲基联苯基、三联苯基、4-甲基-1-萘基、4-叔丁基-1-萘基、4-萘基-1-萘基、6-苯基-2-萘基、10-苯基-9-蒽基、螺芴基、2-苯并环丁烯基等。芳基的碳数优选为6~18的范围内。所述碳数更优选为6~10的范围。
[0122]
作为取代芳基的取代基,可与作为所述烷基中的取代基而例示的取代基相同。
[0123]
x1~x
16
中的环烷基可被分别独立地选择。环烷基可具有取代基,也可未经取代。作为环烷基,可列举:环戊基、环己基、2,5-二甲基环戊基、4-叔丁基环己基等。另外,环烷基的碳数优选为3~12的范围内。所述碳数更优选为3~6的范围内。取代环烷基的取代基可与作为所述烷基中的取代基而例示的取代基相同。
[0124]
x1~x
16
中的烯基可被分别独立地选择。烯基可具有取代基,也可未经取代。作为烯基,可列举直链状或分支链状的烯基。烯基一般是指在其结构内具有一个双键的基,在本说明书中,烯基可在其结构内具有多个双键。作为烯基的具体例,可列举:乙烯基、1-丙烯基、烯丙基、2-丁烯基、3-丁烯基、异丙烯基、异丁烯基、1-戊烯基、2-戊烯基、3-戊烯基、4-戊烯基、1-己烯基、2-己烯基、3-己烯基、4-己烯基、1,3-丁二烯基等。烯基的碳数优选为2~18的范围内。所述碳数更优选为2~10,进而优选为2~5。作为取代烯基的取代基,可与作为所述烷基中的取代基而例示的取代基相同。
[0125]
所述r2、r4~r
11
、及x1~x
24
中的杂环基可被分别独立地选择。杂环基可具有取代基,也可未经取代。
[0126]
作为杂环基,可列举脂肪族杂环基或芳香族杂环基。作为具体例,可列举:吡啶基、吡嗪基、哌啶基、吡喃基、吗啉基、吖啶基等。另外,也可列举下述结构式所表示的基。杂环基的碳数(构成环的碳数)优选为4~12。环元数优选为5~13。
[0127]
[化4]
[0128][0129]
作为取代杂环基的取代基,可与作为所述烷基中的取代基而例示的取代基相同。取代杂环基例如可列举:杂环基3-甲基吡啶基、n-甲基哌啶基、n-甲基吡咯基等。
[0130]
所述r4、x
18
、及x
19
中的烷氧基可被分别独立地选择。烷氧基可具有取代基,也可未经取代。
[0131]
作为烷氧基,可列举直链状或分支链状的烷氧基。作为具体例,可列举:甲氧基、乙氧基、丙氧基、异丙氧基、正丁氧基、异丁氧基、叔丁氧基、新戊氧基、2,3-二甲基-3-戊氧基、正己氧基、正辛氧基、硬脂氧基、2-乙基己氧基等。烷氧基的碳数优选为1~6的范围内。
[0132]
作为取代烷氧基的取代基,可与作为所述烷基中的取代基而例示的取代基相同。
[0133]
作为取代烷氧基的取代基,可与作为所述烷基中的取代基而例示的取代基相同。作为取代烷氧基的具体例,可列举:三氯甲氧基、三氟甲氧基、2,2,2-三氟乙氧基、2,2,3,3-四氟丙氧基、2,2-双(三氟甲基)丙氧基、2-乙氧基乙氧基、2-丁氧基乙氧基、2-硝基丙氧基、苄氧基等。
[0134]
所述r4、x
18
、及x
19
中的芳氧基可被分别独立地选择。芳氧基可具有取代基,也可未经取代。
[0135]
作为芳氧基,可列举单环或缩合多环的芳氧基。作为具体例,可列举:苯氧基、对甲基苯氧基、萘氧基、蒽氧基等。芳氧基优选为单环的芳氧基。另外,优选为碳数6~12的芳氧基。
[0136]
作为取代芳氧基的取代基,可与作为所述芳基中的取代基而例示的取代基相同。作为取代芳氧基,例如可列举:对硝基苯氧基、对甲氧基苯氧基、2,4-二氯苯氧基、五氟苯氧基、2-甲基-4-氯苯氧基等。
[0137]
所述z、及r2中的亚烷基可被分别独立地选择。亚烷基可具有取代基,也可未经取代。作为亚烷基,可列举从所述烷基中除去一个氢原子后的二价基。作为经取代或未经取代的亚烷基的具体例,可列举:-ch
2-ch
2-、-ch
2-ch
2-ch
2-nhco-ch
2-ch
2-、-ch
2-ch
2-ch
2-oco-ch
2-ch
2-、-ch
2-ch
2-ch
2-o-ch
2-ch
2-等。
[0138]
所述z、及r2中的亚芳基可分别独立地选择。亚芳基可具有取代基,也可未经取代。作为亚芳基,可列举从芳基中除去一个氢原子后的二价基。亚芳基优选为碳数6~10的范围。在一实施方式中,亚芳基可为亚苯基、或亚萘基。作为经取代或未经取代的亚芳基的具体例,可列举下述结构式所表示的基。
[0139]
[化5]
[0140][0141]
本发明的一实施方式涉及一种包含所述荧光色素的荧光标识剂。所述荧光标识剂在生物化学研究到医疗诊断的广泛领域中,能够应用于生物成像中的荧光标识。例如,在基因诊断领域、免疫诊断领域、医疗开发领域、再生医疗领域、环境试验领域、生物技术领域、及荧光检查等领域中,可用于荧光标识等用途。
[0142]
其中,所述实施方式的荧光标识剂的荧光色素中的-z-r
1-r
2-r3所表示的结构(取代基)承担着与磷脂质相互作用的功能。因此,可优选地用作磷脂质集聚型的荧光标识剂。磷脂质集聚型荧光标识剂在细胞膜的染色、外切体的追踪、及用于药物传递系统(dds)的脂质体成像等中,可优选地用作荧光标识剂。
[0143]
在所述实施方式的荧光标识剂中,荧光色素的浓度并无特别限定。例如,在对细胞进行处理的情况下,若考虑到对细胞的功能障碍、及增殖阻碍等的影响,则荧光色素的浓度优选为低。在一实施方式中,例如所述荧光色素相对于接种在96孔板中的10,000细胞(cells)/孔(well)的细胞的浓度优选为100μm以下。所述浓度更优选为50μm以下,进而优选为10μm以下。根据所述实施方式的荧光标识剂,由于对磷脂质的优异的集聚性,即便是低浓度的荧光色素也可以高荧光强度来成像。因此,例如即便是2μm以下的低浓度,也可进行更
高精度的检测。
[0144]
所述实施方式的荧光标识剂只要含有所述实施方式的荧光色素即可,视需要也可含有其他成分。作为其他成分,可为本技术领域中众所周知的成分。例如可列举溶剂、及两亲媒性物质等。
[0145]
溶剂可为水、或有机溶剂,更优选为水。考虑到荧光色素的溶解性,也可将水与有机溶剂混合而使用。例如,有机溶剂优选为乙醇、或二甲基亚砜(dimethyl sulfoxide,dmso)。
[0146]
两亲媒性物质是指在一个分子内具有亲水基与疏水基的化合物的总称。作为具体例,可列举表面活性剂、或磷脂质等。两亲媒性物质可仅使用一种,或者也可将两种以上混合而使用。在所述实施方式的荧光标识剂中,两亲媒性物质并无特别限定,只要可在水中溶解在近红外区域发出荧光的非水溶性荧光色素,则可为任意化合物。无特别限定,以下列举可使用的两亲媒性物质的具体例。
[0147]
作为表面活性剂,可列举:非离子性表面活性剂、阳离子性表面活性剂、阴离子性表面活性剂、及高分子表面活性剂等。
[0148]
作为非离子性表面活性剂,例如可列举:吐温(tween)(注册商标)20、吐温(tween)(注册商标)40、吐温(tween)(注册商标)60、及吐温(tween)(注册商标)80等聚氧乙烯山梨醇酐系脂肪酸酯、克列莫佛(cremophor)(注册商标)el、及克列莫佛(cremophor)(注册商标)rh60等聚氧乙烯蓖麻油衍生物、索鲁陶璐(solutol)(注册商标)hs 15等12-羟基硬脂酸-聚乙二醇共聚物、以及特力同(triton)(注册商标)x-100、及特力同(triton)(注册商标)x-114等辛基苯酚乙氧基化物、等。
[0149]
作为阳离子性表面活性剂,例如可列举:硬脂基三甲基氯化铵、月桂基三甲基氯化铵等烷基三甲基铵盐、鲸蜡基氯化吡啶鎓等烷基吡啶鎓盐、二硬脂基二甲基氯化铵、二烷基二甲基铵盐、及氯化聚(n,n'-二甲基-3,5-亚甲基哌啶鎓)等烷基四级铵盐、烷基二甲基苄基铵盐、烷基异喹啉鎓盐、二烷基吗啉鎓盐、聚氧乙烯烷基胺、烷基胺盐、聚胺脂肪酸衍生物、戊基醇脂肪酸衍生物、苯扎氯铵、及氯化苯铵松宁、等。
[0150]
作为阴离子性表面活性剂,例如可列举:十二烷基硫酸钠、十二烷基苯磺酸酯、癸基苯磺酸酯、十一烷基苯磺酸酯、十三烷基苯磺酸酯、及壬基苯磺酸酯、以及这些的钠、钾及铵盐等。
[0151]
作为高分子表面活性剂,例如可列举:聚乙烯基醇、聚氧乙烯聚氧丙烯二醇、聚乙二醇-聚烷基、聚乙二醇-聚乳酸、聚乙二醇-聚己内酯、聚乙二醇-聚甘醇酸、聚乙二醇-聚(丙交酯-乙交酯)等嵌段共聚物。
[0152]
在一实施方式中,所述实施方式的荧光标识剂可包含作为两亲媒性物质而所述例示的化合物中的一种或两种以上。但是,所述实施方式的荧光标识剂对磷脂质等靶部位的集聚性优异,因此能够在不需要两亲媒性物质的情况下以高感度进行检测。
[0153]
在所述实施方式的荧光标识剂中,荧光色素优选为包含酞菁色素。酞菁色素的合成方法并无特别限定。例如,首先以邻苯二甲腈衍生物为原料并利用公知的方法合成具有酞菁骨架的色素(酞菁金属络合物)。继而,向所述色素中加入具有取代基(-z-r
1-r
2-r3)的成分,将这些在二甲基亚砜溶媒中加热搅拌并使其反应。通过此种反应,可获得所期望的荧光色素。作为具有所述取代基的成分,例如可使用在后述的实施例中的酸性化合物、或表示
为轴配体的化合物。
[0154]
在作为原料的邻苯二甲腈衍生物为非对称的结构的情况下,可以取代基的位置不同的异构体的混合物的形式获得酞菁。以下,本说明书中仅示出酞菁结构的一例,但不排除取代基的位置不同的异构体。
[0155]
关于作为本发明的一实施方式的荧光色素的具体例,可列举以下。其中,根据本发明的荧光色素并不限定于这些。
[0156]
[表1-1]
[0157][0158]
[表1-2]
[0159][0160]
[表1-3]
[0161][0162]
[表1-4]
[0163][0164]
在所述例示的荧光色素中,荧光色素1~荧光色素37分别是具有酞菁色素的骨架
(色素的残基)的荧光色素。荧光色素38是具有二酮吡咯并吡咯色素的骨架的荧光色素。荧光色素39及40是具有呫吨色素的骨架的荧光色素。
[0165]
荧光色素41是具有含有下述结构的硼二吡咯亚甲基色素的骨架(色素的残基)的荧光色素。例如,荧光色素41中的取代基
“‑
z-r
1-r
2-r
3”中z为-c2h
4-,r1为-c(=o)nh-,r2为-c3h
6-,r3为-n(ch3)2。
[0166]
[化6]
[0167][0168]
[表1-5]
[0169][0170]
[表1-6]
[0171][0172]
[表1-7]
[0173][0174]
[表1-8]
[0175][0176]
在所述例示的荧光色素中,荧光色素42~荧光色素59分别是具有酞菁色素的骨架的荧光色素。荧光色素60是具有二酮吡咯并吡咯色素的骨架的荧光色素。荧光色素61是具有呫吨色素的骨架的荧光色素。荧光色素62是具有花青色素的骨架的荧光色素。荧光色素63是具有硼二吡咯亚甲基色素的骨架的荧光色素。
[0177]
虽无特别限定,但在一实施方式中,就耐久性等稳定性的观点而言,荧光标识剂优选为包含具有酞菁色素的骨架的荧光色素。
[0178]
实施例
[0179]
以下,基于实施例对本发明进行说明,但本发明并不由此限定。此外,实施例中“份”表示“质量份”。
[0180]
(质量分析)
[0181]
通过质量分析装置(tof-ms:布鲁克道尔顿(bruker daltonics)公司制造奥陶福来库斯(autoflex)ii)进行分析。
[0182]
<i>荧光色素
[0183]
[制造例1]
[0184]
<化合物a-1的制造方法>
[0185]
向喹啉50份与无水氯化铝1份的溶液中导入氨气,进而添加5份的3-乙氧基邻苯二甲腈,使这些在180℃下反应7小时。将所述反应液冷却至室温后,加入甲醇200份、及10%盐酸水溶液200份。继而,滤取所析出的固体,并利用水200份进行固体的清洗。将清洗后的固体在80℃下干燥,从而获得4.7份的表2所示的化合物a-1(收率88.4%)。
[0186]
[制造例2~制造例11]
[0187]
<化合物a-2~化合物a-10的制造方法>
[0188]
将化合物a-1的制造方法中使用的3-乙氧基邻苯二甲腈与无水氯化铝变更为表2所示的邻苯二甲腈衍生物与金属源,除此以外与化合物a-1的制造同样地分别制造表2所示的化合物a-2~化合物a-10。此外,邻苯二甲腈衍生物、及金属源以与化合物a-1的制造中的3-乙氧基邻苯二甲腈、及无水氯化铝相同的摩尔量来使用。
[0189]
[表2-1]
[0190][0191]
[表2-2]
[0192][0193]
[制造例11]
[0194]
<化合物b-1的制造方法>
[0195]
相对于使3份的化合物a-1溶解在n-甲基-2-吡咯烷酮(n-methyl-2-pyrrolidone,nmp)10份中而得的溶液,全量添加使氢氧化钾0.45份溶解在水1份中而得的水溶液。使这些在110℃下反应7小时。将所述反应液冷却至室温后,加入水100份。继而,滤取所析出的固体,并利用水100份进行固体的清洗。将清洗后的固体在80℃下干燥,从而获得2.9份的表3所示的化合物b-1(收率99.2%)。
[0196]
[制造例12~制造例15]
[0197]
<化合物b-2~化合物b-5的制造方法>
[0198]
将化合物b-1的制造方法中使用的化合物a-1变更为表3所示的化合物a,除此以外与化合物b-1的制造同样地分别制造表3所示的化合物b-2~化合物b-5。此外,化合物a以与
化合物b-1的制造中的化合物a-1相同的摩尔量来使用。
[0199]
[表3]
[0200][0201][0202]
[制造例16]
[0203]
<化合物c-1的制造方法>
[0204]
向喹啉50份与无水氯化铝1份的溶液中导入氨气,进而添加3.8份的3-乙氧基邻苯二甲腈与1.1份的4-氟邻苯二甲腈。使这些在180℃下反应7小时。将所述反应液冷却至室温
后,加入甲醇200份与10%盐酸水溶液200份。继而,滤取所析出的固体,并利用水200份进行固体的清洗。使用中压分取液相色谱仪(山善制造的智能闪光阿库劳斯(smart flash akros))对清洗后的固体(粗制物)进行精制。将获得的精制物在80℃下干燥,从而获得1.6份的表4所示的化合物c-1(收率30.5%)。
[0205]
[制造例17~制造例19]
[0206]
<化合物c-2~化合物c-4的制造方法>
[0207]
将化合物c-1的制造方法中使用的无水氯化铝变更为表4所示的金属源,除此以外与化合物c-1的制造同样地分别制造表4所示的酞菁c-2~酞菁c-4。此外,金属源以与化合物c-1的制造中的无水氯化铝相同的摩尔量来使用。
[0208]
[表4]
[0209][0210][0211]
[实施例1]
[0212]
<荧光色素1的制造方法>
[0213]
使1份的化合物b-1与3-氨基丙基二甲基乙氧基硅烷0.6份溶解在吡啶中,将所述
溶液在115℃下回流3小时而获得反应液。使用蒸发器从反应液中去除吡啶后,加入乙醇10份与水50份的混合溶液。继而,滤取所析出的固体,并利用水50份进行固体的清洗。将清洗后的固体在80℃下干燥,从而获得0.39份的表1所示的荧光色素1(收率33.7%)。质量分析的结果是,在m/z=848.64(理论值847.99)处检测到分子离子峰,鉴定为具有表1所示的荧光色素1的结构。
[0214]
[实施例2~实施例5]
[0215]
<荧光色素2~荧光色素5的制造方法>
[0216]
将荧光色素1的制造方法中使用的化合物b-1变更为表5所示的化合物b,除此以外与荧光色素1的制造同样地分别制造表1所示的荧光色素2~荧光色素5。此外,化合物b以与荧光色素1的制造中的化合物b-1相同的摩尔量来使用。通过质量分析对所获得的荧光色素2~荧光色素5的结构进行鉴定,确认到具有表1所示的结构。表11表示质谱的分析结果。
[0217]
[表5]
[0218] 荧光色素化合物b实施例1荧光色素1b-1实施例2荧光色素2b-2实施例3荧光色素3b-3实施例4荧光色素4b-4实施例5荧光色素5b-5
[0219]
[实施例6]
[0220]
<荧光色素6的制造方法>
[0221]
使0.7份的化合物a-1与4-(3-氨基丙基)苯磺酸0.4份溶解在二甲基亚砜50份中,进而添加1,8-二氮杂二环[5.4.0]-7-十一碳烯0.3份,使这些在90℃下反应5小时。将所述反应液冷却至室温后,加入水100份与食盐10份。继而,滤取所析出的固体,并利用水50份进行固体的清洗。将清洗后的固体在80℃下干燥,从而获得0.36份的表1所示的荧光色素6(收率41.6%)。质量分析的结果是,在m/z=916.57(理论值915.96)处检测到分子离子峰,鉴定为具有表1所示的荧光色素6的结构。
[0222]
[实施例7~实施例14]
[0223]
<荧光色素7~荧光色素14的制造方法>
[0224]
将荧光色素6的制造方法中使用的化合物a-1与4-(3-氨基丙基)苯磺酸变更为表6所示的化合物a与酸性化合物,除此以外与荧光色素6的制造同样地分别制造表1所示的荧光色素7~荧光色素14。此外,化合物a及酸性化合物以与荧光色素6的制造中的化合物a-1及4-(3-氨基丙基)苯磺酸相同的摩尔量来使用。通过质量分析对所获得的荧光色素7~荧光色素14的结构进行鉴定,确认到具有表1所示的结构。表11表示质谱的分析结果。
[0225]
[表6]
[0226][0227]
[实施例15]
[0228]
<荧光色素15的制造方法>
[0229]
使0.5份的化合物a-1与(2-羧基乙基)苯基次膦酸0.29份溶解在二甲基亚砜20份中,使所述溶液在80℃下反应8小时。将所述反应液冷却至室温后,加入水50份与食盐10份。继而,滤取所析出的固体,并利用水50份进行固体的清洗。将清洗后的固体在80℃下干燥,从而获得0.46份的表1所示的荧光色素15(收率74.4%)。质量分析的结果是,在m/z=929.46(理论值928.88)处检测到分子离子峰,鉴定为具有表1所示的荧光色素15的结构。
[0230]
[实施例16~实施例18]
[0231]
<荧光色素16~荧光色素18的制造方法>
[0232]
将荧光色素15的制造方法中使用的化合物a-1与(2-羧基乙基)苯基次膦酸变更为表7所示的化合物a与酸性化合物,除此以外与荧光色素15的制造同样地分别制造表1所示的荧光色素16~荧光色素18。此外,化合物a及酸性化合物以与荧光色素15的制造中的化合物a-1及(2-羧基乙基)苯基次膦酸相同的摩尔量来使用。通过质量分析对所获得的荧光色素16~荧光色素18的结构进行鉴定,确认到具有表1所示的结构。表11表示质谱的分析结果。
[0233]
[表7]
[0234][0235]
[实施例19]
[0236]
<荧光色素19的制造方法>
[0237]
使0.5份的荧光色素1、0.8份的碘化甲烷、以及碳酸钾0.8份溶解在四氢呋喃50份中,使所述溶液在25℃下反应5小时。使用蒸发器从反应液中去除四氢呋喃后,加入四氢呋喃20份与水60份。继而,滤取所析出物的固体,并利用水60份进行固体的清洗。将清洗后的固体在80℃下干燥,从而获得0.21份的表1所示的荧光色素19(收率33.3%)。质量分析的结果是,在m/z(正(positive))=892.25(理论值891.08)处检测到分子离子峰,鉴定为具有表1所示的荧光色素19的结构。
[0238]
[实施例20~实施例23]
[0239]
<荧光色素20~荧光色素23的制造方法>
[0240]
将荧光色素19的制造方法中使用的碘化甲烷与荧光色素1变更为表8所示的碘化化合物与胺类,除此以外与荧光色素19的制造同样地分别制造表1所示的荧光色素20~荧光色素23。此外,碘化化合物及胺类以与荧光色素19的制造中的碘化甲烷及荧光色素1相同的摩尔量来使用。通过质量分析对所获得的荧光色素20~荧光色素23的结构进行鉴定,确认到具有表1所示的结构。表11表示质谱的分析结果。
[0241]
[表8]
[0242][0243]
[实施例24]
[0244]
<荧光色素24的制造方法>
[0245]
使0.06份的荧光色素1与琥珀酸酐0.007份溶解在n-甲基-2-吡咯烷酮(nmp)5份中,使所述溶液在90℃下反应4小时。使用离心蒸发器从反应液中去除nmp后,加入水5份。继而,滤取所析出的固体,并利用水5份进行固体的清洗。将清洗后的固体在80℃下干燥,从而获得0.041份的表1所示的荧光色素24(收率61.1%)。质量分析的结果是,在在/z=949.07(理论值948.06)处检测到分子离子峰,鉴定为具有表1所示的荧光色素24的结构。
[0246]
[实施例25~实施例30]
[0247]
<荧光色素25~荧光色素30的制造方法>
[0248]
将荧光色素24的制造方法中使用的琥珀酸酐与荧光色素1变更为表9所示的琥珀酸酐衍生物与胺类,除此以外与荧光色素24的制造同样地分别制造表1所示的荧光色素25~荧光色素30。此外,琥珀酸酐衍生物及胺类以与荧光色素24的制造中的琥珀酸酐及荧光色素1相同的摩尔量来使用。通过质量分析对所获得的荧光色素25~荧光色素30的结构进行鉴定,确认到具有表1所示的结构。表11表示质谱的分析结果。
[0249]
[表9]
[0250]
[0251][0252]
[实施例31]
[0253]
<荧光色素31的制造方法>
[0254]
使1.0份的化合物c-1与(2-羧基乙基)苯基次膦酸0.6份溶解在二甲基亚砜50份中,进而添加1,8-二氮杂二环[5.4.0]-7-十一碳烯0.4份后,使所述溶液在90℃下反应8小时。将所述反应液冷却至室温后,加入水100份。继而,滤取所析出的固体,并利用水50份进行固体的清洗。使用中压分取液相色谱仪(山善制造的智能闪光阿库劳斯(smart flash akros))对所获得的固体(粗制物)进行精制。将所获得的精制物在80℃下干燥,从而获得0.72份的表1所示的荧光色素31(收率60.1%)。质量分析的结果是,在m/z=901.46(理论值900.82)处检测到分子离子峰,鉴定为具有表1所示的荧光色素31的结构。
[0255]
[实施例32~实施例37]
[0256]
<荧光色素32~荧光色素37的制造方法>
[0257]
将荧光色素31的制造方法中使用的化合物c-1与(2-羧基乙基)苯基次膦酸变更为表10所示的化合物c与酸性化合物,除此以外与荧光色素31的制造同样地分别制造表1所示的荧光色素32~荧光色素37。此外,化合物c及酸性化合物以与荧光色素31的制造中的化合物c-1及(2-羧基乙基)苯基次膦酸相同的摩尔量来使用。通过质量分析对所获得的荧光色素32~荧光色素37的结构进行鉴定,确认到具有表1所示的结构。表11表示质谱的分析结果。
[0258]
[表10]
[0259]
[0260][0261]
[实施例38]
[0262]
<荧光色素38的制造方法>
[0263]
使1.0份的二酮吡咯并吡咯系色素即颜料红(pigment red)255(东京化成制造)、4-溴丁酸0.6份、以及氢化钠(60%)0.1份溶解在n,n-二甲基甲酰胺50份中,使所述溶液在90℃下反应4小时。将所述反应液冷却至室温后,加入水100份。继而,滤取所析出的固体,并利用水50份进行固体的清洗。使用中压分取液相色谱仪(山善制造的智能闪光阿库劳斯(smart flash akros))对清洗后的固体(粗制物)进行精制。将所获得的精制物在80℃下干燥,从而获得0.70份的表1所示的荧光色素38(收率53.9%)。质量分析的结果是,在m/z=375.28(理论值374.40)处检测到分子离子峰,鉴定为具有表1所示的荧光色素38的结构。
[0264]
[实施例39]
[0265]
<荧光色素39的制造方法>
[0266]
使1.0份的5-羧基荧光素(东京化成制造)、n,n-二甲基-1,3-丙二胺0.3份、以及对甲苯磺酸0.1份溶解在二甲苯50份中,使所述溶液在140℃下反应24小时。将所述反应液冷却至室温后,使用蒸发器从反应液中去除二甲苯,加入50份的石油醚。继而,通过抽吸过滤来去除不溶物后,使用蒸发器去除石油醚,从而获得固体。将所述固体在80℃下干燥,从而获得0.57份的表1所示的荧光色素39(收率46.6%)。质量分析的结果是,在m/z=461.37(理论值460.49)处检测到分子离子峰,鉴定为具有表1所示的荧光色素39的结构。
[0267]
[实施例40]
[0268]
<荧光色素40的制造方法>
[0269]
使1.0份的罗丹明(rhodamin)b(东京化成制造)、n,n-二甲基-1,3-丙二胺0.2份、以及对甲苯磺酸0.1份溶解在二甲苯50份中,使所述溶液在140℃下反应24小时。将所述反应液冷却至室温后,使用蒸发器从反应液中去除二甲苯,加入50份的石油醚。继而,通过抽吸过滤来去除不溶物后,使用蒸发器去除石油醚,从而获得固体。将所述固体在80℃下干燥,从而获得0.46份的表1所示的荧光色素40(收率39.1%)。质量分析的结果是,在m/z=564.02(理论值563.18)处检测到分子离子峰,鉴定为具有表1所示的荧光色素40的结构。
[0270]
[实施例41]
[0271]
<荧光色素41的制造方法>
[0272]
使1.0份的bodipy系色素即bdp fl(东京化成制造)与n,n-二甲基-1,3-丙二胺0.3份溶解在二甲苯50份中,使所述溶液在140℃下反应24小时。将所述反应液冷却至室温后,使用蒸发器从反应液中去除二甲苯,加入50份的石油醚。继而,通过抽吸过滤来去除不溶物后,使用蒸发器去除石油醚,从而获得固体。将所述固体在80℃下干燥,从而获得0.38份的表1所示的荧光色素41(收率29.3%)。质量分析的结果是,在m/z=379.11(理论值378.27)处检测到分子离子峰,鉴定为具有表1所示的荧光色素41的结构。
[0273]
[表11]
[0274][0275]
[制造例20]
[0276]
<化合物a-11的制造方法>
[0277]
向喹啉50份与无水氯化铝1份的溶液中导入氨气,进而添加5份的3、6-双(苯硫基)邻苯二甲腈,使这些在180℃下反应7小时。将所述反应液冷却至室温后,加入甲醇200份与10%盐酸水溶液200份。继而,滤取所析出的固体,并利用水200份进行固体的清洗。将清洗后的固体在80℃下干燥,从而获得表12所示的化合物a-11(收率72.8%)。
[0278]
[制造例21、制造例22]
[0279]
<化合物a-12、化合物a-13的制造方法>
[0280]
将化合物a-11的制造方法中使用的3、6-双(苯硫基)邻苯二甲腈变更为表12所示的邻苯二甲腈衍生物,除此以外与化合物a-11的制造同样地分别制造表12所示的化合物a-12及化合物a-13。此外,邻苯二甲腈衍生物以与化合物a-11的制造中的3、6-双(苯硫基)邻苯二甲腈相同的摩尔量来使用。
[0281]
[表12]
[0282][0283]
[实施例42]
[0284]
<荧光色素42的制造方法>
[0285]
使0.7份的化合物a-1与1,2-亚乙基二膦酸0.4份溶解在二甲基亚砜50份中,进而添加1,8-二氮杂二环[5.4.0]-7-十一碳烯0.3份后,将所述溶液在90℃下反应5小时。将所述反应液冷却至室温后,加入水100份与食盐10份。继而,滤取所析出的固体,并利用水50份进行固体的清洗。将清洗后的固体在80℃下干燥,从而获得0.42份的表1所示的荧光色素1(收率50.6%)。质量分析的结果是,在m/z=905.35(理论值905.21)处检测到分子离子峰,鉴定为具有表1所示的荧光色素1的结构。
[0286]
[实施例43-实施例55]
[0287]
<荧光色素43-荧光色素55的制造方法>
[0288]
将荧光色素1的制造方法中使用的化合物a-1与1,2-亚乙基二膦酸变更为表13所示的化合物a与轴配体,除此以外与荧光色素6的制造同样地分别制造表1所示的荧光色素2~荧光色素14。此外,化合物a及轴配体以与荧光色素1的制造中的化合物a-1及1,2-亚乙基二膦酸相同的摩尔量来使用。通过使用质量分析装置的分析对所获得的荧光色素2~荧光色素14的结构进行鉴定,确认到具有表1所示的结构。表3表示质谱的分析结果。
[0289]
[表13-1]
[0290][0291]
[表13-2]
[0292][0293]
[表13-3]
[0294]
[0295][0296]
[制造例23]
[0297]
<化合物d-1的制造>
[0298]
向环丁砜200份、及1,8-二氮杂二环[5,4,0]-7-十一碳烯(1,8-diazabicyclo[5,4,0]-7-undecene,dbu)15.7份中加入4-丁硫基-1,3-二亚氨基异吲哚啉5份、及四氯化硅8.8份,在160℃~170℃下历时8小时对这些进行加热搅拌。继而,将反应液冷却至室温(25℃),加入甲醇200份。继而,对所析出的沉淀物(固体)进行过滤分离,并利用甲醇:水(质量比4:1)的混合溶液将固体清洗后并加以干燥,从而获得2.6份的表14所示的化合物d-1(收率63.6%)。质量分析的结果是,在m/z=751.65(理论值751.24)处检测到分子离子峰,确认到具有表14所示的化合物d-1的结构。
[0299]
[表14]
[0300][0301]
[实施例56]
[0302]
<荧光色素56的制造方法>
[0303]
使1.0份的化合物b-5与1,2-亚乙基二膦酸0.5份溶解在二甲基亚砜50份中,进而添加1,8-二氮杂二环[5.4.0]-7-十一碳烯0.3份,使这些在90℃下反应5小时。将所述反应液冷却至室温后,加入水100份与食盐10份。继而,滤取所析出的固体,并利用水50份进行固体的清洗。将清洗后的固体在80℃下干燥,从而获得0.52份的表1所示的荧光色素1(收率42.3%)。质量分析的结果是,在m/z=923.47(理论值923.21)处检测到分子离子峰,鉴定为具有表1所示的荧光色素56的结构。
[0304]
[制造例57]
[0305]
<荧光色素57的制造方法>
[0306]
将荧光色素1的制造方法中使用的化合物b-5变更为d-1,除此以外与荧光色素56的制造同样地制造表1所示的荧光色素57。此外,化合物d-1以与荧光色素56的制造中的化合物b-5相同的摩尔量来使用。通过使用质量分析装置的分析对所获得的荧光色素57的结
构进行鉴定,确认到具有表1所示的结构。表15表示质谱的分析结果。
[0307]
[表15]
[0308][0309]
[实施例58]
[0310]
<荧光色素58的制造方法>
[0311]
使0.7份的化合物c-3与1,2-亚己基二膦酸0.7份溶解在二甲基亚砜50份中,在所述溶液中进而添加1,8-二氮杂二环[5.4.0]-7-十一碳烯0.3份,使这些在90℃下反应5小时。将所述反应液冷却至室温后,加入水100份与食盐10份。继而,滤取所析出的固体,并利用水50份进行固体的清洗。将清洗后的固体在80℃下干燥,从而获得0.39份的表1所示的荧光色素1(收率42.3%)。质量分析的结果是,在m/z=913.66(理论值913.24)处检测到分子离子峰,鉴定为具有表1所示的荧光色素58的结构。
[0312]
[实施例59]
[0313]
<荧光色素59的制造方法>
[0314]
将荧光色素58的制造方法中使用的化合物c-3及1,2-亚己基二膦酸变更为表16所示的化合物c-4及环取代基,除此以外与荧光色素58的制造同样地制造表1所示的荧光色素59。此外,化合物c-4以与荧光色素17的制造中的化合物c-3相同的摩尔量来使用。通过使用质量分析装置的分析对所获得的荧光色素59的结构进行鉴定,确认到具有表1所示的结构。表16表示质谱的分析结果。
[0315]
[表16]
[0316][0317]
[实施例60]
[0318]
<荧光色素60的制造方法>
[0319]
使1.0份的二酮吡咯并吡咯系色素即颜料红(pigment red)255(东京化成)、3-氨基丙基膦酸0.6份、以及氢化钠(60%dispersion)0.1份溶解在n,n-二甲基甲酰胺50份中,使所述溶液在90℃下反应4小时。将所述反应液冷却至室温后,加入水100份。继而,滤取所析出的固体,并利用水50份进行固体的清洗。使用中压分取液相色谱仪(山善制造的智能闪
光阿库劳斯(smart flash akros))对清洗后的固体(粗制物)进行精制。将所获得的精制物在80℃下干燥,从而获得0.65份的表1所示的荧光色素60(收率45.5%)。质量分析的结果是,在m/z=411.52(理论值411.10)处检测到分子离子峰,鉴定为具有表1所示的荧光色素60的结构。
[0320]
[实施例61]
[0321]
<荧光色素61的制造方法>
[0322]
使1.0份的5-羧基荧光素(东京化成)、3-氨基丙基膦酸0.7份、以及对甲苯磺酸0.1份溶解在二甲苯50份中,使所述溶液在140℃下反应24小时。将所述反应液冷却至室温后,使用蒸发器从反应液中去除二甲苯,加入50份的石油醚。继而,通过抽吸过滤来去除不溶物后,使用蒸发器去除石油醚,从而获得固体。将所述固体在80℃下干燥,从而获得0.75份的表1所示的荧光色素61(收率51.2%)。质量分析的结果是,在m/z=551.02(理论值551.18)处检测到分子离子峰,鉴定为具有表1所示的荧光色素61的结构。
[0323]
[实施例62]
[0324]
<荧光色素62的制造方法>
[0325]
将cy5-nhs酯(ester)(船越(funakoshi))1.0份、3-氨基丙醇0.5份、以及三乙胺0.5份溶解在dmf 50份中,使所述溶液在室温下反应12小时。向所述反应液中加入水50份,并对所析出的沉淀物(固体)进行过滤,进而利用水清洗固体。将清洗后的固体在80℃下干燥,从而获得0.70份的表1所示的荧光色素62(收率86.4%)。质量分析的结果是,在m/z=541.18(理论值541.36)处检测到分子离子峰,鉴定为具有表1所示的荧光色素62的结构。
[0326]
[实施例63]
[0327]
<荧光色素63的制造方法>
[0328]
使1.0份的bodipy系色素即bdp fl(东京化成制造)与3-氨基丙醇0.3份溶解在二甲苯50份中,使所述溶液在140℃下反应24小时。将所述反应液冷却至室温后,使用蒸发器从反应液中去除二甲苯,加入50份的石油醚。继而,通过抽吸过滤来去除析出的不溶物后,使用蒸发器从反应液中去除石油醚,从而获得固体。将所述固体在80℃下干燥,从而获得0.64份的表1所示的荧光色素63(收率70.6%)。质量分析的结果是,在m/z=350.01(理论值350.18)处检测到分子离子峰,鉴定为具有表1所示的荧光色素63的结构。
[0329]
[比较例1]
[0330]
作为比较化合物1,使用化合物a-1。
[0331]
[比较例2]
[0332]
作为比较化合物2,使用化合物a-9。
[0333]
在后述的比较例3~比较例11中,制造表17所示的比较化合物3~比较化合物11。
[0334]
[表17]
[0335][0336]
[比较例3]
[0337]
<比较化合物3的制造方法>
[0338]
使氯化铝7.0份、尿素39份、钼酸铵0.2份、以及偏苯三甲酸酐25份溶解在n-甲基-2-吡咯烷酮(nmp)40份中,将所述溶液在139℃下搅拌9小时。将所述反应液冷却至室温后,加入水100份。继而,滤取所析出的固体,并利用水50份进行固体的清洗。将清洗后的固体在80℃下干燥,从而获得14.5份的表17所示的比较化合物3(收率59.3%)。质量分析的结果是,在m/z=751.84(理论值751.00)处检测到分子离子峰,鉴定为具有表17所示的比较化合物3的结构。
[0339]
[比较例4]
[0340]
<比较化合物4的制造方法>
[0341]
向喹啉30份与无水氯化铝0.7份的溶液中导入氨气,进而添加1.5份的3-乙氧基邻苯二甲腈与2.1份的4-十八烷基氧基邻苯二甲腈,使所述溶液在180℃下反应7小时。将所述反应液冷却至室温后,加入甲醇200份与10%盐酸水溶液200份。继而,滤取所析出的固体,并利用水200份进行固体的清洗。使用中压分取液相色谱仪(山善制造的智能闪光阿库劳斯(smart flash akros))对清洗后的固体(粗制物)进行精制。将所获得的精制物在80℃下干燥,从而获得0.36份的表17所示的比较化合物4(收率12.6%)。质量分析的结果是,在m/z=976.44(理论值975.61)处检测到分子离子峰,鉴定为具有表17所示的比较化合物4的结构。
[0342]
[比较例5]
[0343]
<比较化合物5的制造方法>
[0344]
使1.0份的化合物a-9与三苯基硅烷醇0.35份溶解在二甲基亚砜20份中,使所述溶液在80℃下反应8小时。将所述反应液冷却至室温后,加入水50份与食盐10份。继而,滤取所
析出的固体,并利用水50份进行固体的清洗。将清洗后的固体在80℃下干燥,从而获得1.00份的表17所示的比较化合物5(收率80.5%)。质量分析的结果是,在m/z=1282.53(理论值1271.67)处检测到分子离子峰,鉴定为具有表17所示的比较化合物5的结构。
[0345]
[比较例6~比较例9]
[0346]
<比较化合物6~比较化合物9的制造方法>
[0347]
将比较化合物5的制造方法中使用的化合物a-9与三苯基硅烷醇变更为表18所示的卤素类与酸性化合物,除此以外与比较化合物5的制造同样地分别制造表17所示的比较化合物6~比较化合物9。此外,卤素类及酸性化合物以与比较化合物5的制造中的化合物a-9及三苯基硅烷醇相同的摩尔量来使用。通过质量分析对所获得的比较化合物6~比较化合物9的结构进行鉴定,确认到具有表17所示的结构。表19表示质谱的分析结果。
[0348]
[表18]
[0349][0350]
[比较例10]
[0351]
<比较化合物10的制造方法>
[0352]
使2.0份的化合物a-9与对甲苯磺酸1.0份溶解在二甲基亚砜50份中,进而向所述溶液中添加1,8-二氮杂二环[5.4.0]-7-十一碳烯0.3份,使这些在90℃下反应5小时。将所述反应液冷却至室温后,加入水100份。继而,滤取所析出的固体,并利用水50份进行固体的清洗。将清洗后的固体在80℃下干燥,从而获得1.35份的表17所示的比较化合物10(收率60.0%)。质量分析的结果是,在m/z=933.67(理论值932.74)处检测到分子离子峰,鉴定为具有表17所示的比较化合物10的结构。
[0353]
[比较例11]
[0354]
<比较化合物11的制造方法>
[0355]
向浓硫酸9.2份与25%发烟硫酸5.5份的混合溶液中加入1份的化合物a-1,在50℃下对所述溶液加热搅拌4小时。将所述反应液冷却后,添加到80份的冰中,并对所析出的沉淀物(固体)进行过滤分离。进而,使过滤分离后的固体悬浮在四氢呋喃50份中,再次对沉淀进行过滤分离。利用四氢呋喃50份将过滤分离后的固体清洗,并将清洗后的固体加以干燥,从而获得0.5份的粗制物。使用中压分取液相色谱仪(山善制造的智能闪光阿库劳斯(smart flash akros))对粗制物进行精制,从而获得0.2份的比较化合物11(收率16.0%)。质量分析的结果是,在m/z=939.65(理论值940.75)处检测到分子离子峰,鉴定为具有表17所示的比较化合物11的结构。
[0356]
示出比较例3~比较例11中制造的比较化合物3~比较化合物11的质谱的分析结果。
[0357]
[表19]
[0358] 理论值测定值比较化合物3751.00751.84比较化合物4975.61976.44比较化合物51271.671282.53比较化合物61127.541128.49比较化合物71169.621170.82比较化合物81231.451232.37比较化合物9932.74933.67比较化合物101167.461168.37比较化合物11940.75939.65
[0359]
[比较例12]
[0360]
作为比较化合物12,使用花青系色素即荧光染料(xenolight dir)(住商医药(summitpharma)制造)。所述化合物相当于具有长链亚烷基的现有的荧光标识剂,经由疏水相互作用而集聚在磷脂质上。
[0361]
[化7]
[0362][0363]
[比较例13]
[0364]
作为比较化合物13,使用罗丹明b(东京化成制造)。
[0365]
<ii>色素溶液
[0366]
[实施例64]
[0367]
<色素溶液1的制备>
[0368]
在二甲基亚砜10ml中溶解1.696mg的荧光色素1。使用孔径0.2μm的尼龙制膜滤器对所述溶液进行过滤后,利用二甲基亚砜稀释100倍,由此制备荧光色素1的色素溶液1。
[0369]
[实施例65~实施例126]
[0370]
<色素溶液2~色素溶液63的制备>
[0371]
将色素溶液1的制备中使用的荧光色素1与二甲基亚砜变更为表20所示的荧光色素与溶剂,除此以外与色素溶液1的制备同样地分别制备色素溶液2~色素溶液63。其中,各荧光色素以与荧光色素1相同的摩尔量来使用,溶剂以与二甲基亚砜相同的体积量来使用。
[0372]
[比较例12~比较例24]
[0373]
<色素溶液64~色素溶液76的制备>
[0374]
将色素溶液1的制备中使用的荧光色素1与二甲基亚砜变更为表20所示的荧光色素与溶剂,除此以外与色素溶液1的制备同样地分别制备色素溶液64~色素溶液76。其中,各荧光色素以与荧光色素1相同的摩尔量来使用,溶剂以与二甲基亚砜相同的体积量来使用。
[0375]
[表20-1]
[0376] 色素溶液荧光色素溶剂实施例64色素溶液1荧光色素1dmso实施例65色素溶液2荧光色素2dmso实施例66色素溶液3荧光色素3dmso实施例67色素溶液4荧光色素4dmso实施例68色素溶液5荧光色素5dmso实施例69色素溶液6荧光色素6dmso实施例70色素溶液7荧光色素7dmso实施例71色素溶液8荧光色素8dmso实施例72色素溶液9荧光色素9dmso实施例73色素溶液10荧光色素10dmso实施例74色素溶液11荧光色素11dmso实施例75色素溶液12荧光色素12dmso实施例76色素溶液13荧光色素13dmso实施例77色素溶液14荧光色素14dmso实施例78色素溶液15荧光色素15dmso实施例79色素溶液16荧光色素16dmso实施例80色素溶液17荧光色素17dmso实施例81色素溶液18荧光色素18dmso实施例82色素溶液19荧光色素19dmso实施例83色素溶液20荧光色素20dmso实施例84色素溶液21荧光色素21dmso实施例85色素溶液22荧光色素22dmso实施例86色素溶液23荧光色素23dmso实施例87色素溶液24荧光色素24dmso实施例88色素溶液25荧光色素25dmso实施例89色素溶液26荧光色素26dmso
实施例90色素溶液27荧光色素27dmso实施例91色素溶液28荧光色素28dmso实施例92色素溶液29荧光色素29dmso实施例93色素溶液30荧光色素30dmso实施例94色素溶液31荧光色素31dmso实施例95色素溶液32荧光色素32dmso
[0377]
[表20-2]
[0378] 荧光标识剂荧光色素溶剂实施例96色素溶液33荧光色素33dmso实施例97色素溶液34荧光色素34dmso实施例98色素溶液35荧光色素35dmso实施例99色素溶液36荧光色素36dmso实施例100色素溶液37荧光色素37dmso实施例101色素溶液38荧光色素38dmso实施例102色素溶液39荧光色素39dmso实施例103色素溶液40荧光色素40dmso实施例104色素溶液41荧光色素41dmso实施例105色素溶液42荧光色素42dmso实施例106色素溶液43荧光色素43dmso实施例107色素溶液44荧光色素44dmso实施例108色素溶液45荧光色素45dmso实施例109色素溶液46荧光色素46dmso实施例110色素溶液47荧光色素47dmso实施例111色素溶液48荧光色素48dmso实施例112色素溶液49荧光色素49dmso实施例113色素溶液50荧光色素50dmso实施例114色素溶液51荧光色素51dmso实施例115色素溶液52荧光色素52dmso实施例116色素溶液53荧光色素53dmso实施例117色素溶液54荧光色素54dmso实施例118色素溶液55荧光色素55dmso实施例119色素溶液56荧光色素56dmso实施例120色素溶液57荧光色素57dmso实施例121色素溶液58荧光色素58dmso实施例122色素溶液59荧光色素59dmso实施例123色素溶液60荧光色素60dmso实施例124色素溶液61荧光色素61dmso实施例125色素溶液62荧光色素62dmso实施例126色素溶液63荧光色素63dmso
[0379]
[表20-3]
[0380] 荧光标识剂荧光色素溶剂比较例12色素溶液64比较化合物1dmso比较例13色素溶液65比较化合物2dmso比较例14色素溶液66比较化合物3dmso比较例15色素溶液67比较化合物4dmso比较例16色素溶液68比较化合物5dmso比较例17色素溶液69比较化合物6dmso比较例18色素溶液70比较化合物7dmso比较例19色素溶液71比较化合物8dmso比较例20色素溶液72比较化合物9dmso比较例21色素溶液73比较化合物10dmso比较例22色素溶液74比较化合物11dmso比较例23色素溶液75比较化合物12dmso比较例24色素溶液76比较化合物13水
[0381]
<色素溶液的荧光强度评价>
[0382]
对于各种色素溶液,使用荧光光度计(日本分光股份有限公司制造,fp-6500)测定荧光光谱。进而,通过将所获得的测定值与表22所示的荧光波长的范围内的荧光强度相加来求出荧光强度。另外,此时的激发光使用了相当于色素的最长波长侧的吸收最大波长的波长。
[0383]
<iii>荧光标识剂
[0384]
[实施例127]
[0385]
<荧光标识剂1的制备>
[0386]
在二甲基亚砜10ml中溶解1.696mg的荧光色素1。利用孔径0.2μm的尼龙制膜滤器进行过滤后,利用洛斯维帕克纪念研究所(roswell park memorial institute,rpmi)1640培养基稀释100倍,由此制备荧光色素1的荧光标识剂1。
[0387]
[实施例128~实施例189]
[0388]
<荧光标识剂2~荧光标识剂63的制备>
[0389]
将荧光标识剂1的制备中使用的荧光色素1与二甲基亚砜变更为表21所示的荧光色素与溶剂,除此以外与荧光标识剂1的制备同样地分别制备荧光标识剂2~荧光标识剂63。其中,各荧光色素以与荧光色素1相同的摩尔量来使用,溶剂以与二甲基亚砜相同的体积量来使用。
[0390]
[比较例25~比较例37]
[0391]
<荧光标识剂64~荧光标识剂76的制备>
[0392]
将荧光标识剂1的制备中使用的荧光色素1与二甲基亚砜变更为表21所示的荧光色素与溶剂,除此以外与荧光标识剂1的制备同样地分别制备荧光标识剂64~荧光标识剂76。其中,各荧光色素以与荧光色素1相同的摩尔量来使用,溶剂以与二甲基亚砜相同的体积量来使用。
[0393]
[表21-1]
[0394] 荧光标识剂荧光色素溶剂实施例127荧光标识剂1荧光色素1dmso实施例128荧光标识剂2荧光色素2dmso实施例129荧光标识剂3荧光色素3dmso实施例130荧光标识剂4荧光色素4dmso实施例131荧光标识剂5荧光色素5dmso实施例132荧光标识剂6荧光色素6dmso实施例133荧光标识剂7荧光色素7dmso实施例134荧光标识剂8荧光色素8dmso实施例135荧光标识剂9荧光色素9dmso实施例136荧光标识剂10荧光色素10dmso实施例137荧光标识剂11荧光色素11dmso实施例138荧光标识剂12荧光色素12dmso实施例139荧光标识剂13荧光色素13dmso实施例140荧光标识剂14荧光色素14dmso实施例141荧光标识剂15荧光色素15dmso实施例142荧光标识剂16荧光色素16dmso实施例143荧光标识剂17荧光色素17dmso实施例144荧光标识剂18荧光色素18dmso实施例145荧光标识剂19荧光色素19dmso实施例146荧光标识剂20荧光色素20dmso实施例147荧光标识剂21荧光色素21dmso实施例148荧光标识剂22荧光色素22dmso实施例149荧光标识剂23荧光色素23dmso实施例150荧光标识剂24荧光色素24dmso实施例151荧光标识剂25荧光色素25dmso实施例152荧光标识剂26荧光色素26dmso实施例153荧光标识剂27荧光色素27dmso实施例154荧光标识剂28荧光色素28dmso实施例155荧光标识剂29荧光色素29dmso实施例156荧光标识剂30荧光色素30dmso实施例157荧光标识剂31荧光色素31dmso实施例158荧光标识剂32荧光色素32dmso
[0395]
[表21-2]
[0396] 荧光标识剂荧光色素溶剂实施例159荧光标识剂33荧光色素33dmso实施例160荧光标识剂34荧光色素34dmso实施例161荧光标识剂35荧光色素35dmso实施例162荧光标识剂36荧光色素36dmso
实施例163荧光标识剂37荧光色素37dmso实施例164荧光标识剂38荧光色素38dmso实施例165荧光标识剂39荧光色素39dmso实施例166荧光标识剂40荧光色素40dmso实施例167荧光标识剂41荧光色素41dmso实施例168荧光标识剂42荧光色素42dmso实施例169荧光标识剂43荧光色素43dmso实施例170荧光标识剂44荧光色素44dmso实施例171荧光标识剂45荧光色素45dmso实施例172荧光标识剂46荧光色素46dmso实施例173荧光标识剂47荧光色素47dmso实施例174荧光标识剂48荧光色素48dmso实施例175荧光标识剂49荧光色素49dmso实施例176荧光标识剂50荧光色素50dmso实施例177荧光标识剂51荧光色素51dmso实施例178荧光标识剂52荧光色素52dmso实施例179荧光标识剂53荧光色素53dmso实施例180荧光标识剂54荧光色素54dmso实施例181荧光标识剂55荧光色素55dmso实施例182荧光标识剂56荧光色素56dmso实施例183荧光标识剂57荧光色素57dmso实施例184荧光标识剂58荧光色素58dmso实施例185荧光标识剂59荧光色素59dmso实施例186荧光标识剂60荧光色素60dmso实施例187荧光标识剂61荧光色素61dmso实施例188荧光标识剂62荧光色素62dmso实施例189荧光标识剂63荧光色素63dmso
[0397]
[表21-3]
[0398] 荧光标识剂荧光色素溶剂比较例25色素溶液64比较化合物1dmso比较例26色素溶液65比较化合物2dmso比较例27色素溶液66比较化合物3dmso比较例28色素溶液67比较化合物4dmso比较例29色素溶液68比较化合物5dmso比较例30色素溶液69比较化合物6dmso比较例31色素溶液70比较化合物7dmso比较例32色素溶液71比较化合物8dmso比较例33色素溶液72比较化合物9dmso比较例34色素溶液73比较化合物10dmso
比较例35色素溶液74比较化合物11dmso比较例36色素溶液75比较化合物12dmso比较例37色素溶液76比较化合物13rpmi1640培养基
[0399]
<荧光标识剂的细胞毒性评价>
[0400]
将人类上皮癌细胞a431接种到96孔板上(1
×
104细胞/孔)。继而,使用包含10%胎牛血清(fetal bovine serum,fbs)及1%青霉素-链霉素(penicillin-streptomycin)的rpmi1640培养基,在培养箱(37℃,含5%co2的空气(air),加湿环境)内,将所述a431培养24小时。在rpmi1640培养基中使用西格玛奥德里奇制造的rpml-164-介质(medium)。
[0401]
在所述培养后,除去培养基,并添加实施例83~实施例123、及比较例25~比较例37中制备的荧光标识剂与包含1%二甲基亚砜的rpmi1640培养基(dmso培养基溶液)。将这些在培养箱内静置1小时后,利用rpmi1640培养基进行清洗。向各孔中各添加10μl的细胞计数试剂盒(cell counting kit)-8(同仁化学制造),在培养箱(37℃,含5%co2的空气(air),加湿环境)内静置1小时。继而,使用盘判读器(帝肯(tecan)公司制造,斯帕库(spark))测定450nm处的吸光度。
[0402]
计算出将添加了dmso培养基溶液的孔的吸光度设为1时的各个荧光标识剂的吸光度的相对值,并基于下述基准进行评价。可以说若评价为“p”,则不会显示细胞毒性。此外,在计算出荧光标识剂的吸光度的相对值时,使用从所测定的吸光度中减去细胞计数试剂盒-8(同仁化学制造)添加前的吸光度而得的值。将评价结果示于表22。
[0403]
(评价基准)
[0404]
p(合格):0.8以上
[0405]
f(不合格):未满0.8
[0406]
<荧光标识剂的荧光强度评价>
[0407]
将人类上皮癌细胞a431接种到96孔板上(1
×
104细胞/孔)。继而,使用包含10%胎牛血清(fbs)及1%青霉素-链霉素的rpmi1640培养基,在培养箱(37℃,含5%co2的空气,加湿环境)内,将所述a431培养24小时。
[0408]
在所述培养后,除去培养基,并添加实施例127~实施例167、及比较例25~比较例37中制备的荧光标识剂,在培养箱内静置1小时。继而,利用rpmi1640培养基进行清洗。使用盘判读器(帝肯(tecan)公司制造,斯帕库(spark)),在表22所示的荧光波长的范围内进行荧光强度评价。
[0409]
图1表示荧光标识剂1、荧光标识剂15、荧光标识剂19、荧光标识剂24、荧光标识剂25、荧光标识剂68、及荧光标识剂75的荧光强度评价结果。可确认到,与使用比较化合物而制备的荧光标识剂68及荧光标识剂75(比较例)相比,作为本发明的实施方式的荧光标识剂1、荧光标识剂15、荧光标识剂19、荧光标识剂24、及荧光标识剂25(实施例)显示出高的荧光强度。
[0410]
<荧光色素的磷脂质集聚性评价>
[0411]
根据表22所示的由色素溶液的荧光光谱求出的荧光强度积分值与由荧光标识剂的荧光强度获得的荧光强度,使用式(1)计算出各色素的磷脂质集聚性。计算出将比较化合物12的磷脂质集聚性设为1时的各个荧光标识剂的磷脂质集聚性的相对值,并基于下述基准进行评价。在评价为3以上的情况下,可以说各荧光色素的磷脂质集聚性良好。
[0412]
(评价基准)
[0413]
4:磷脂质集聚性为4以上
[0414]
3:磷脂质集聚性为2以上且未满4
[0415]
2:磷脂质集聚性为1以上且未满2
[0416]
1:磷脂质集聚性未满1
[0417]
[数式1]
[0418][0419]
将磷脂质集聚性的评价结果示于表22。
[0420]
可确认到,与使用比较化合物而制备的荧光标识剂(比较例)相比,作为本发明的实施方式的荧光标识剂(实施例)显示出高的磷脂质集聚性。
[0421]
<细胞的视认性评价>
[0422]
将人类上皮癌细胞a431接种到96孔板上(1
×
104细胞/孔)。使用包含10%胎牛血清(fbs)及1%青霉素-链霉素的rpmi1640培养基,在培养箱(37℃,含5%co2的空气(air),加湿环境)内,将所述a431培养24小时。
[0423]
在所述培养后,除去培养基,并添加实施例127~实施例189、及比较例25~比较例37中制备的荧光标识剂,在培养箱内静置1小时。继而,利用rpmi1640培养基进行清洗。
[0424]
使用设置了适当波长的激发滤光片及荧光滤光片的荧光显微镜(基恩士(keyence)公司制造,bz-x800),对细胞的暗视场像与荧光像进行观察,并基于下述基准进行评价。将评价结果示于表22。
[0425]
(评价基准)
[0426]
p(合格):清晰
[0427]
f(不合格):不清晰
[0428]
[表22-1]
[0429][0430]
[表22-2]
[0431][0432]
[表22-3]
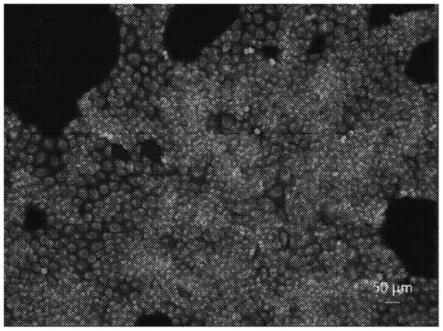
[0433][0434]
将利用荧光标识剂1、荧光标识剂15、荧光标识剂19、荧光标识剂24、荧光标识剂25、荧光标识剂68、及荧光标识剂75标识出的细胞的视认性评价结果依次示于图2~图8(倍
率:10倍,荧光摄取时间:1秒)。
[0435]
将利用荧光标识剂42、及荧光标识剂53标识出的细胞的视认性评价结果依次示于图9及图10(倍率:40倍,荧光摄取时间:1秒)。
[0436]
由与比较例对应的图7及图8和与实施例对应的图2~图6、图9及图10的对比所明确的那样,根据本发明的实施方式的荧光标识剂,观察到源自特定的取代基,显示出更高的荧光强度。如此,可知与比较化合物相比,本发明的实施方式的荧光标识剂(实施例)的细胞集聚性优异,由此可获得更优异的视认性。根据以上内容,明确本发明的实施方式的荧光标识剂作为荧光标识剂具有优异的特性。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。