1.本发明涉及生物医学材料领域,具体涉及一种肾清除性稀土配合物探针的制备及其在活体疾病诊断方面的应用。
背景技术:
2.药物引起的脏器损伤是当前临床疾病治疗和药物使用中面临的一个重要问题。例如,急性肾损伤(aki)和药物性肝损伤(dili)具有高发病率和死亡率。目前aki和dili的临床诊断方法主要依赖于血清学指标,如血清肌酐和血尿素氮的测量用于诊断aki,谷丙转氨酶、谷丙转氨酶等水平用于诊断dili。然而这种血清学方法通常不灵敏,无法实现脏器损伤的早期准确诊断和疾病发展监控。由于肾小球滤过率(gfr)可直接反应出肾小球受损的情况及整体肾功能的受损程度,近年来发展了菊粉和
99m
tc-dtpa等标记物用于评估gfr和肾损伤诊断。然而,该方法具有评估过程相对繁琐、敏感性低、费用贵、且具有放射性等缺点。尽管当前有些研究利用活体荧光成像实现了小鼠肝损伤的早期诊断,活体光学成像仍然面临穿透深度有限、干扰大等问题。因此,开发活体脏器损伤的早期高灵敏特异性诊断新方法具有重要的现实意义。
3.稀土离子(ln
3
)由于其独特的电子构型,具有优异的发光性能,如窄发射峰、高量子产率、大的stokes位移和长荧光寿命等。尤其是eu
3
,tb
3
,sm
3
,dy
3
,其螯合物的荧光寿命可从几十纳秒到几毫秒,远超过其它非特异性荧光背景(纳秒级荧光寿命),且稀土离子配合物能够有效地被肾脏清除。当前,基于稀土配合物的时间分辨荧光免疫分析(trfia)技术相比于其他免疫分析方法,包括放射免疫分析(ria)、酶联免疫吸附分析(elisa),它克服了放射性污染、酶底物不稳定、灵敏度低等缺点。尤其是溶解增强稀土化合物荧光免疫分析法(delfia),被公认为是最灵敏的商业生物测定方法之一。利用时间分辨(tr)技术,delfia可以完全消除散射光和其他短寿命生物自体荧光的背景噪声,从而提供比常规稳态荧光免疫分析更高的灵敏度。因此,构建肾可清除的时间分辨荧光稀土探针,通过体外尿液分析实现脏器损伤等体内重大疾病的高灵敏早期诊断和发展监控,在临床疾病诊断和精准医学研究等领域具有广阔的应用前景。
技术实现要素:
4.本发明的目的在于提供一种制备简单,水溶性好,生物安全性高,肾清除效率高,可用于体外光学尿液分析的时间分辨荧光稀土探针的制备方法及其在活体疾病诊断方面的应用。
5.为实现上述目的,采用以下技术方案:
6.本发明的第一个目的是提供肾可清除的时间分辨荧光稀土探针的制备方法,包括具有长寿命荧光寿命特性的稀土离子与配位体形成的稀土配合物探针以及以该稀土配合物探针为基础制备的稀土配合物生物标记的可激活型智能纳米探针。
7.(1)稀土配合物探针的制备方法包括以下步骤:
8.s1、将配位体加入去离子水中加热搅拌;
9.s2、将稀土盐化合物于去离子水中溶解,按一定比例将稀土盐水溶液缓慢加入步骤s1所得的悬浊液中,继续加热搅拌至混合液澄清透明,用naoh溶液调ph,得到所述稀土配合物探针。
10.步骤s1中,所用配位体可以是二乙基三胺五乙酸(dtpa)、1,4,7,10-四氮杂环十二烷-1,4,7,10-四乙酸(dota)、1,4,7-三氮杂环环壬烷-n,n',n
”‑
三乙酸(nota)中的一种或多种,优选为dtpa;步骤s1中,为使配体混合充分,更有利于后续反应,50℃水浴加热并保温20分钟。
11.步骤s2中,所述稀土盐为具有长寿命荧光寿命特性的稀土离子eu
3
、tb
3
、sm
3
和dy
3
中的一种或多种的醋酸盐、盐酸盐、硫酸盐或硝酸盐,优选为硝酸盐,如eu(no3)3,tb(no3)3,sm(no3)3,dy(no3)3中的一种或多种;所用配位体与稀土离子的摩尔比为1:(1~1.2),优选为1:1。
12.步骤s2中,50℃水浴加热搅拌直至溶液澄清透明,以使反应完全;所用naoh溶液浓度为0.4m,所调ph范围为6.8~7.2,以使产物稳定。
13.(2)稀土配合物生物标记的可激活型智能纳米探针的制备方法包括以下步骤:
14.s1、将所述稀土配合物探针加入乙醇和浓氨水的混合液中搅拌使其沉淀;
15.s2、将正硅酸乙酯(teos)与双-[3-(三乙氧基硅)丙基]-四硫化物btepds(cas号40372-72-3)按比例混合均匀,再将其缓慢滴加入s1所得的悬浊液中,室温下搅拌12~24h,离心洗涤,得到白色沉淀;
[0016]
s3、将步骤s2所得的白色沉淀重新分散在去离子水中,再加入到二硬脂酰基磷脂酰乙醇胺-聚乙二醇2000(dspe-peg2000)溶液中搅拌过夜,离心洗涤,得到稀土配合物生物标记的可激活型智能纳米探针。
[0017]
步骤s1中,所用稀土配合物探针优选为eu-dtpa,将500μl 40mm eu-dtpa加入由600μl 30wt%氨水和12ml无水乙醇组成的混合液中,搅拌20min使其充分沉淀;
[0018]
步骤s2中,所用teos和btepds体积分别为360μl和240μl,将其混合均匀后,按30μl/min的速度缓慢滴加入步骤s1所得的悬浊液中,室温下搅拌反应12~24h,离心得到沉淀,所得沉淀用乙醇洗涤1次,再用水洗涤3次,得到白色沉淀。
[0019]
步骤s3中,将步骤s2所得的白色沉淀重新分散在去离子水中,再加入到浓度为10mg/ml的dspe-peg2000溶液中搅拌过夜,离心洗涤,得到稀土配合物生物标记的可激活型智能纳米探针,记为eu-dtpa@sio2/dspe-peg2000。
[0020]
所得的稀土配合物探针水溶性好,安全性高,能被肾脏有效清除并随尿液排出;在天线配体的作用下,能够发射荧光,其荧光强度与尿液中稀土探针含量具有相关性;并且,该探针可包埋于可降解硅球中构建可激活型智能纳米探针,其在活性氧特异性激活下释放肾清除性稀土配合物,从而实现活体肝损伤的高灵敏尿液诊断。
[0021]
本发明的第二个目的是提供肾可清除的时间分辨荧光稀土探针在诊断药物性急性肾损伤和肝损伤方面的应用。在某个特定的实施例中,所述药物性急性肾损伤为顺铂诱导的急性肾损伤,肝损伤为对乙酰氨基酚诱导的药源性肝损伤。
[0022]
本发明的优点在于:
[0023]
(1)荧光探针制备步骤环保简单,水溶性好,生物安全性高,肾清除效率高;
[0024]
(2)所制备的荧光探针可通过肾清除随尿液排出,并且能够与稀土溶解荧光增强液作用,使得荧光信号放大百万倍,通过时间分辨荧光分析技术定量探针清除率,以实现活体器脏疾病的早期诊断和发展监控。
附图说明
[0025]
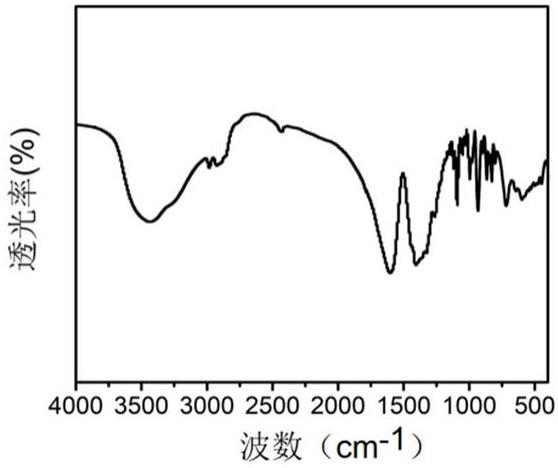
图1是本发明实施例1中制备的肾清除性稀土配合物荧光探针eu-dtpa的红外光谱图。
[0026]
图2是本发明实施例1中肾清除性稀土配合物荧光探针eu-dtpa的激发光谱和荧光发射光谱。
[0027]
图3是本发明实例3中收集的不同时间点的尿液在365nm紫外灯激发下的荧光图。
[0028]
图4是尿液中探针eu-dtpa的稳态与时间分辨荧光光谱图。
[0029]
图5是尿液中eu-dtpa时间分辨荧光强度随浓度变化的关系曲线。
[0030]
图6是本发明实例7中收集的对照组健康小鼠和实验组肾损伤小鼠不同时间点的尿液在365nm紫外灯激发下的荧光图。
[0031]
图7是本发明实例7中不同时间点收集的对照组健康小鼠和实验组肾损伤小鼠的尿液中eu-dtpa时间分辨荧光强度柱状图。
[0032]
图8是本发明实例8所制得的eu-dtpa@sio2/dspe-peg2000的形貌图(右上角)和x射线能谱分析。
[0033]
图9是本发明实例9中,eu-dtpa@sio2/dspe-peg2000对onoo-的响应性分析。
[0034]
图10是本发明实例10中探针注射后6h所收集的尿液中eu-dtpa时间分辨荧光强度柱状图。
具体实施方式
[0035]
以下结合附图和实施例对本发明作进一步的详细说明。但本领域技术人员了解,本发明的保护范围不仅限于以下实施例。根据本发明公开的内容,本领域技术人员将认识到在不脱离本发明技术方案所给出的技术特征和范围的情况下,对以上所述实施例做出许多变化和修改都属于本发明的保护范围。
[0036]
实施例1:肾清除性稀土配合物荧光探针eu-dtpa的制备。具体步骤如下:
[0037]
称取二乙基三胺五乙酸(dtpa),放入单口圆底烧瓶中,分散在5ml去离子水中,50℃水浴加热搅拌20min;然后称取稀土硝酸化合物,稀土硝酸化合物选自eu(no3)3·
6h2o,用500μl去离子水溶解,将稀土离子水溶液逐渐缓慢滴加到dtpa混合液中(dtpa和eu的摩尔比为1:1),继续50℃加热搅拌,直到混合溶液澄清透明停止加热搅拌;用0.4m naoh溶液调节ph,使其在6.8~7.2之间,再将溶液进行冻干,得到对应的白色固体粉末。其红外光谱图如图1所示(参见图1)。
[0038]
实施例2:对实施例1制备得到的eu-dtpa进行光学性质测试。具体步骤如下:
[0039]
取实施例1制备得到的eu-dtpa粉末溶于水溶液中,使其终浓度为1mm。取一定体积的eu-dtpa溶液加入一定体积的荧光增强液(15μmβ-nta,50μm topo,1%冰醋酸,0.1%triton-x100)中,eu-dtpa水溶液与荧光增强液的体积比为1:19。测量其光学性质,稀土配合物荧光探针eu-dtpa在荧光增强液中,在340~360nm范围有较强的吸收,进一步用340nm
的激发光激发,能够观察到在614
±
5nm处的荧光吸收峰(参见图2)。
[0040]
实施例3:对实施例1制备得到的eu-dtpa进行肾清除性分析。具体步骤如下:
[0041]
取实施例1制备得到的eu-dtpa粉末溶于水溶液中,使其终浓度为1mm。取200μleu-dtpa溶液尾静脉注射进小鼠体内,按不同时间点收集尿液,并记录尿液体积。取一定体积的不同时间点收集到的尿液和一定体积的荧光增强液(15μmβ-nta,50μm topo,1%冰醋酸,0.1%triton-x100),尿液与荧光增强液的体积比为1:19,一同加入96孔板中,室温下孵育30min。用365nm紫外灯照射,能够观察到各个时间点尿液中的eu-dtpa的荧光。稀土配合物荧光探针eu-dtpa在静脉注射后1~2h能够观察到明显荧光,4h以后几乎观察不到荧光(参见图3)。该现象证明本发明提供的稀土配合物荧光探针eu-dtpa能够在短时间内有效被肾脏清除,并且能够通过肉眼便捷直观地观察探针清除状况。
[0042]
实施例4:对实施例3收集到的尿液进行稳态和时间分辨荧光测试。具体步骤如下:
[0043]
取10μl实施例3收集到的1h内尿液,再取190μl荧光增强液(15μmβ-nta,50μmtopo,1%冰醋酸,0.1%triton-x100),一同加入96孔板中,室温下孵育30min。将孔板放置在酶标仪上,设置激发波长340nm,延迟时间0μs,扫描450~725nm范围内荧光信号;进一步,设置激发波长340nm,延迟时间100μs,扫描450~725nm范围内荧光信号,得到尿液中的稀土配合物荧光探针eu-dtpa的稳态和时间分辨荧光光谱(参见图4)。该现象可以证明本发明提供的检测方法能够有效屏蔽尿液的背景荧光,从而提高检测灵敏度。
[0044]
实施例5:时间分辨荧光免疫分析法定量尿液中的eu-dtpa荧光探针。具体步骤如下:
[0045]
配置一系列不同浓度的eu-dtpa水溶液,按eu-dtpa水溶液/空白尿液=1/9的体积比混合,得到尿液中的一系列不同浓度的eu-dtpa溶液,以此模拟体内排出的含eu-dtpa的尿液样品。按样品/增强液=1/9的体积比,将样品与增强液在96孔板中孵育30min,得到一系列的标准样品(其中,eu-dtpa的含量依次为:0.005,0.01,0.02,0.04,0.08,0.2,0.4,0.8,4,8,20μm)。将含有标准样品的酶标板放置在酶标仪上,设置激发波长340nm,延迟时间100μs,测量发射波长在614nm的荧光强度,得到尿液中eu-dtpa浓度-荧光强度图(参见图5)。依据浓度-荧光标准曲线可以对尿液中所含的eu-dtpa荧光探针进行定量分析。
[0046]
实施例6:小鼠药物性急性肾损伤模型建立。具体步骤如下:
[0047]
选用balb/c裸鼠,将小鼠随机分为两组:
[0048]
(1)空白组(n=3):连续灌胃0.9%生理盐水(0.1ml/10g)两周,在第15天单次腹腔注射生理盐水(0.1ml/10g)。
[0049]
(2)实验组(n=3):连续灌胃0.9%生理盐水(0.1ml/10g)两周,在第15天单次腹腔注射顺铂(20mg/kg)。
[0050]
实施例7:体外尿液分析评估药物性急性肾损伤。具体步骤如下:
[0051]
取实施例1制备得到的eu-dtpa粉末溶于水溶液中,使其终浓度为1mm。分别取200μleu-dtpa水溶液尾静脉注射进实施例6的两组小鼠中,按不同时间点收集空白组健康小鼠和实验组急性肾损伤小鼠的尿液,并记录尿液体积。取一定体积的不同时间点收集到的尿液和一定体积的荧光增强液(15μmβ-nta,50μm topo,1%冰醋酸,0.1%triton-x100),尿液与荧光增强液的体积比为1:19,一同加入96孔板中,室温下孵育30min。用365nm紫外灯照射,能够观察到各个时间点尿液中的eu-dtpa探针的荧光及其变化趋势(参照图6)。可以看
出空白组健康小鼠体内的eu-dtpa探针在1~2h时间段大量排出,4h以后几乎排尽;而实验组肾损伤小鼠持续到24h仍然可以观察到较强荧光,说明体内依然残余eu-dtpa探针,说明其肾功能受到损伤。进一步地,将含有两组小鼠尿液样本的酶标板放置在酶标仪上,设置激发波长340nm,延迟时间100μs,测量发射波长在614nm的荧光强度,得到两组小鼠不同时间点的尿液荧光强度随时间的变化(参照图7),结合实施例5的浓度-荧光标准曲线,可以估算出不同时间尿液中eu-dtpa荧光探针的含量,进而评估小鼠的肾清除能力。
[0052]
实施例8:eu-dtpa@sio2/dspe-peg2000的制备。具体步骤如下:
[0053]
取500μl 40mm的eu-dtpa加入于12ml乙醇和600μl的30wt%氨水混合液中,室温下搅拌20min,使其充分沉淀;将360μlteos和240μl btepds混合均匀后,按30μl/min的速度缓慢滴加入上述混合液中,室温下搅拌反应24h,离心得到白色沉淀,用乙醇洗涤1次,再用水洗涤3次,将所得沉淀重新分散在10ml去离子水中,再将其加入到10ml10 mg/ml的dspe-peg2000溶液中搅拌过夜,离心洗涤2次,得到eu-dtpa@sio2/dspe-peg2000,其形貌及x射线能谱分析(eds)如图8(参照图8),由tem插图可知,其粒径约为180nm,eds分析定量eu负载率为0.18%(w/w)。
[0054]
实施例9:eu-dtpa@sio2/dspe-peg2000对活性氧的响应性验证。具体步骤如下:
[0055]
取1ml实例8所制备的eu-dtpa@sio2/dspe-peg2000分别与0μm和20μm的onoo-在37℃条件下孵育4h后,离心取上清。取一定体积上清液和一定体积的荧光增强液(15μmβ-nta,50μm topo,1%冰醋酸,0.1%triton-x100),上清液与荧光增强液的体积比为1:19,一同加入96孔板中,室温下孵育30min。将含有两组样本的酶标板放置在酶标仪上,设置激发波长340nm,延迟时间100μs,测量发射波长在614nm的荧光强度(参照图9),由此可以看出,稀土配合物生物标记的可激活型智能纳米探针eu-dtpa@sio2/dspe-peg2000对活性氧具有较好的响应性能。
[0056]
实施例10:体外尿液分析评估药物性肝损伤。具体步骤如下:
[0057]
s1,肝损伤模型构建
[0058]
选用balb/c裸鼠,将小鼠随机分为两组:
[0059]
(1)空白组(n=3):断粮12h后,腹腔注射生理盐水(0.1ml/10g);
[0060]
(2)实验组(n=3):断粮12h后,腹腔注射对乙酰氨基酚(500mg/kg)。
[0061]
s2,体外尿液分析评估药物性肝损伤
[0062]
取200μl实施例8所制备的eu-dtpa@sio2/dspe-peg2000尾静脉注射进以上两组小鼠体内,6h后收集空白组健康小鼠和实验组肝损伤小鼠的尿液,并记录尿液体积。取一定体积收集到的尿液和一定体积的荧光增强液(15μmβ-nta,50μm topo,1%冰醋酸,0.1%triton-x100),尿液与荧光增强液的体积比为1:19,一同加入96孔板中,室温下孵育30min。将含有两组小鼠尿液样本的酶标板放置在酶标仪上,设置激发波长340nm,延迟时间100μs,测量发射波长在614nm的荧光强度,得到两组小鼠尿液的时间分辨荧光强度(参照图10)。可以看出,肝损伤组尿液的荧光强度明显高于健康对照组,由此,可以通过比较尿液荧光强度间接评估肝脏中活性氧的水平,进而实现诊断肝损伤的目的。
[0063]
以上所述仅为本发明的较佳实施例,凡依本发明申请专利范围所做的均等变化与修饰,皆应属本发明的涵盖范围。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。