1.本发明属于基因检测技术领域,具体涉及一种用于中国人群乳腺癌精准诊疗的多基因检测方法。
背景技术:
2.乳腺癌发病位于中国女性癌症发病首位,临床分型复杂,且部分分型的乳腺癌的预后较差,严重威胁女性生命安全。目前已有越来越多的证据显示驱动基因的变异会导致乳腺癌的发生,其他肿瘤相关重要信号通路中的基因变异,也对乳腺癌的发展、转移有关键作用;同时,越来越多的靶向药物被证实对于乳腺癌的治疗有显著效果,如针对pik3ca的错义突变的靶向药阿培利司(alpelisib)、依维莫司(everolimus)等,针对erbb2的拷贝数变异的靶向药物曲妥珠单抗(trastuzumab)、帕妥珠单抗(pertuzumab)以及erbb2激活性突变的靶向药吡咯替尼(pyrotinib)、来那替尼(neratinib)等,针对brca1/2有害突变的奥拉帕利(olaparib)、鲁卡帕利(rucatinib)等parp抑制剂。基于上述基因变异对于乳腺癌诊断和治疗的重要性,基因变异信息对于制定肿瘤的治疗方案和预后评估具有重要的参考意义。
3.目前相关检测最主流的方法仍为以单个基因或单个变异位点为主的纯实验方法,如免疫组化(ihc)、免疫荧光原位杂交(fish)等。此类方法由于每次实验只能检测单个基因或位点,效率低,且无法对与被检测基因关联的其他关键基因进行有效检测,存在很大的局限性。应用靶向多基因二代测序(next-generation sequencing,ngs)检测基因变异作为临床诊断和治疗的辅助手段,可以提高检测效率,目前已有该类检测在乳腺癌中应用。如2016年发表于《journal of clinical oncology》的研究利用了182基因的靶向二代测序项目对bolero-2临床试验中的乳腺癌患者进行靶向测序(hortobagyi,g.n.et al.correlative analysis of genetic alterations and everolimus benefit in hormone receptor-positive,human epidermal growth factor receptor 2-negative advanced breast cancer:results from bolero-2.journal of clinical oncology:official journal of the american society of clinical oncology 34,419-426,doi:10.1200/jco.2014.60.1971(2016));2016年发表于《nature communication》的一项研究利用173基因的靶向测序探究2433例乳腺癌患者的基因组特征(pereira,b.et al.the somatic mutation profiles of 2,433 breast cancers refines their genomic and transcriptomic landscapes.nature communications 7,11479,doi:10.1038/ncomms11479(2016))。纪念斯隆-凯特琳癌症研究中心(memorial sloan kettering cancer center,msk)的肿瘤多基因检测技术msk-impact(integrated mutational profiling of actionable cancer targets),包含486个检测基因,于2017年获得fda(美国食品药品管理局)的上市许可,是第一个获得此类批准的肿瘤检测基因集产品。2017年发表在《nature medicine》的研究,利用了msk-impact对超过10000名晚期癌症患者进行了靶向基因测序,其中1200多例是乳腺癌患者(zehir,a.et al.mutational landscape of metastatic cancer revealed from prospective clinical sequencing of 10,
000patients.nat med 23,703-713,doi:10.1038/nm.4333(2017).);2018年发表在《nature cancer》的研究通过msk-impact产品对39例乳腺癌患者进行了靶向测序,探究了乳腺癌的耐药性成因。
4.为了造福更多患者,更合理地利用测序数据,目前的多基因靶向测序除了满足辅助临床诊断的需求,还肩负着从基因水平探索乳腺癌生物学机制的重要使命。然而,目前国内多基因检测产品检测的基因只集中在诊断和靶向治疗关注的基因,功能单一,缺少乳腺癌重点通路相关的上下游基因和其他起重要调控作用的基因,无法进行遗传性发病的预防指导和生物学机制的进一步研究,这也导致产生的大量测序数据无法进一步用于乳腺癌分子水平机制的研究,造成资源的浪费;另一方面,现有的多基因检测技术缺少针对中国乳腺癌人群特点的设计,如kmt2d在中国人群中的突变频率显著高于mskcc数据库的欧美人群的突变频率,而大部分现有的多基因检测产品未重视该类基因,存在漏检中国人群重要变异的风险。
5.综上,提供一种针对中国乳腺癌人群设计的基因集检测产品,且检测信息更全面的乳腺癌检测基因集具有重要临床意义和研究意义。
技术实现要素:
6.为解决上述技术问题,本发明提供了用于中国人群乳腺癌精准诊疗的检测基因集及相应检测方法,所述基因集全面覆盖了中国乳腺癌人群的高频突变基因、遗传易感性基因、靶向用药指导相关的基因与耐药相关的基因,不仅为临床靶向治疗提供了所需的基因变异信息,还与复旦大学附属肿瘤医院精准肿瘤中心的数据矩阵结合,为中国人群的基因检测标准化提供详尽的数据,为乳腺癌的新机制、新靶点的探索提供数据基础。
7.具体地,本发明第一方面提供了一种用于乳腺癌检测的基因集,所述基因集包括突变基因拷贝数变异基因,基因总数为539个,所述突变基因见下表1,所述拷贝数变异基因见下表2。
8.表1 乳腺癌检测突变基因
9.10.[0011][0012]
其中,akt1、akt3、brca1、brca2、cdk4、cdk6、egfr、esr1为关键基因中的核心基因。
[0013]
表2 乳腺癌检测拷贝数变异基因
[0014]
akt3ccnd1cdk4cdk6egfrerbb2erlin2fgfr1fgfr2fgfr3grb7jak2mdm2mdm4metmien1mycnsd3plpp5ptenrb1runx1tp53trps1
ꢀꢀꢀꢀꢀꢀ
[0015]
其中,akt3、ccnd1、erbb2、fgfr1、fgfr2、jak2、myc、pten、rb1、tp53为重点关注的拷贝数变异基因。本发明第二方面提供了一种乳腺癌多基因检测试剂盒,所述试剂盒包括用于本发明第一方面所述基因集的检测试剂。
[0016]
在某些实施方式中,所述检测试剂包括用于所述基因集基因捕获的dna探针。
[0017]
在某些实施方式中,所述dna探针的靶向序列见选自表3。
[0018]
本发明第三方面提供了用于乳腺癌多基因检测的探针,所述dna探针的靶向序列选自表3。
[0019]
本发明第四方面提供了用于乳腺癌多基因检测的液态基因芯片,所述基因芯片包括本发明第二方面所述的试剂盒或本发明第三方面所述的探针。
[0020]
本发明第五方面提供了本发明第一方面所述的基因集或本发明第二方面所述的试剂盒或本发明第三方面所述的探针或本发明第四方面所述的液态基因芯片在制备乳腺癌检测装置中的应用。
[0021]
本发明第六方面提供了一种乳腺癌的检测装置,包括:测序模块和分析模块。
[0022]
进一步地,所述测序模块可用于对待测乳腺癌样本(包括新鲜组织和ffpe样本)和血液样本的dna进行提取,基因捕获,并进行高通量测序,获得测序结果。
[0023]
进一步地,所述分析模块,用于对测序结果进行分析,获得基因集的变异信息,并注释用药信息。
[0024]
本发明的有益效果是:
[0025]
1)检测的基因集符合中国乳腺癌人群特点:本发明结合本中心(复旦大学附属肿瘤医院)的数据矩阵和以往的研究结果,并对tcga、mskcc、metabric和cosmic数据库中的乳腺癌高发基因进行筛选,筛选出与中国乳腺癌人群基因特征有密切关联的539个基因,其中539个基因均涉及突变,539个基因中的24个基因还涉及拷贝数变异。相较现有的基因检测项目,本发明具有检测更全面、更符合中国乳腺癌人群基因特征的优点,解决了目前已有技术存在中国特异的乳腺癌关键基因变异漏检的情况。
[0026]
2)检测结果指导作用全面:本发明提供的基因集覆盖了中国人群乳腺癌的高频突变基因、遗传易感基因、靶向用药指导相关的基因与耐药相关基因,满足了患者的精准诊疗需求,还对有家族遗传的患者家庭有预防指导作用。
[0027]
3)乳腺癌精准检测已写入《中国抗癌协会乳腺癌诊治指南与规范》,已有大规模人群因此受益。
[0028]
4)本发明作为构建精准中心数据矩阵的重要一环,经过多轮的技术迭代,覆盖更全面,技术更完善,更能服务于中国乳腺癌人群的精准诊疗。
[0029]
5)检测方法效率高:本发明采用的是dna探针。相较于rna探针,dna探针更稳定,降解速率更低,结合效率更高,对于提高基因检测的稳定性和准确性具有明显的提升。
附图说明
[0030]
为了更清楚地说明本发明具体实施方式或现有技术中的技术方案,下面将对具体实施方式或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图是本发明的一些实施方式,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
[0031]
图1显示复旦大学附属肿瘤医院精准肿瘤中心的数据矩阵结构。
[0032]
图2显示实施例3中发生brca2胚系致病突变的乳腺癌病例的样本质控信息。
[0033]
图3显示实施例3的乳腺癌病例的胚系突变信息。
[0034]
图4显示实施例3的乳腺癌病例的体细胞突变信息。
[0035]
图5显示实施例3中乳腺癌病例的拷贝数变异信息。
[0036]
图6显示实施例3中乳腺癌病例的检测结果小结,总结了根据上述检测结果,该样本可用的靶向药信息。
[0037]
图7显示实施例4中发生pik3ca体细胞突变的乳腺癌病例的样本质控信息。
[0038]
图8显示实施例4中乳腺癌病例的胚系突变检测结果。
[0039]
图9显示实施例4中乳腺癌病例的组织多基因突变检测结果。
[0040]
图10显示实施例4中乳腺癌病例的组织多基因拷贝数变异检测结果。
[0041]
图11显示实施例4中乳腺癌病例的检测结果小结,总结了根据上述检测结果,该样本可用的靶向药信息。
[0042]
图12显示实施例5中发生erbb2基因扩增的乳腺癌病例的样本质控信息。
[0043]
图13显示实施例5中乳腺癌病例的胚系突变检测结果。
[0044]
图14显示实施例5中乳腺癌病例的体细胞突变检测结果。
[0045]
图15显示实施例5中乳腺癌病例的拷贝数变异检测结果。
[0046]
图16显示实施例5中乳腺癌病例检测结果小结,综合上述胚系、体细胞和拷贝数检测,提供该样本可用的靶向药信息。
[0047]
图17显示本发明的多基因检测方案在中国乳腺癌千人基因组检测计划的应用,以及检测结果和临床结合关系的示意图。
[0048]
图18显示由本发明提供的多基因检测方案获得的中国人群乳腺癌基因突变图谱。
[0049]
图19显示由本发明提供的多基因检测方案获得的中国人群乳腺癌热点基因突变位点及其突变频率。
[0050]
图20显示由本发明提供的多基因检测方案获得的中国乳腺癌人群的变异情况和mskcc的欧美乳腺癌人群基因变异情况的频率对比。
[0051]
图21显示中国乳腺癌人群中的精准治疗靶点分布情况。
[0052]
图22显示中国人群乳腺癌中基因组促癌变异和精准治疗靶点比例。
[0053]
图23显示通过本发明提供的检测方案,一例携带erbb2 l755s突变的晚期乳腺癌患者,通过砒洛替尼的靶向治疗后病情缓解。
[0054]
图24显示一例her2受体阴性的多线治疗失败的乳腺癌患者,经过本发明的检测方案,发现新的可用于治疗的靶点(akt1 e17k突变)后制定新的治疗方案(白蛋白紫杉醇联合依维莫司),病情得到缓解。
[0055]
图25显示基于本发明获得的检测结果在乳腺癌胚系-体细胞交互模式应用的示意图。
[0056]
图26显示乳腺癌胚系-体细胞交互模式在不同临床分组中的趋向性,证明了基于本发明的胚系-体细胞交互模式具有临床应用的潜在价值。
[0057]
图27显示基于本发明的检测结果获得future(fuscc-tnbc-umbrella)临床试验(nct03805399)的患者分组情况。
[0058]
图28显示基于本发明的精准治疗策略不同程度缓解了future临床试验各分组三阴性乳腺癌患者的病情。
[0059]
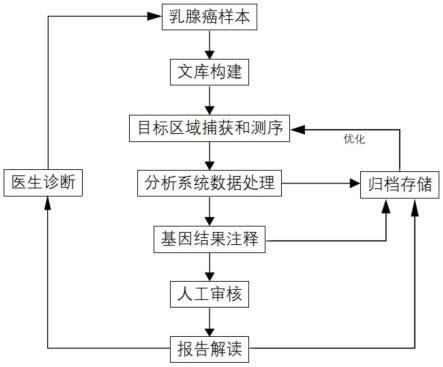
图29显示本发明乳腺癌精准诊疗检测方法示意图。
具体实施方式
[0060]
下面进一步描述本发明,本描述中介绍的实施案例仅是范例性的,并不对本发明的范围构成限制。本专业技术人员应该理解的是,在不偏离本发明原理和方法的情况下,对本发明技术方案的细节和形式进行部分修改或替换,但基于此修改或替换均属于本发明的保护范围内。
[0061]
实施例1用于乳腺癌检测的基因集的确定及其在数据矩阵中的应用
[0062]
本发明用于乳腺癌检测的基因集的确定主要依赖本中心的数据矩阵中的数据集,具体步骤如下:首先参考公开的数据库metabric、tcga、msk-impact、cosmic,并关注乳腺癌重点信号通路:pi3k-akt pathway,mapk pathway,ras pathway,erbb pathway,er pathway,筛选中国乳腺癌人群高频突变位点,确定基础基因集,共397个基因;其次,参考复旦大学附属肿瘤医院三阴性乳腺癌数据集(jiang,y.z.et al.genomic and transcriptomic landscape of triple-negative breast cancers:subtypes and treatment strategies.cancer cell 35,428-440.e425(2019))、千人基因组检测计划数
据集(lang gt,et al.characterization of the genomic landscape and actionable mutations in chinese breast cancers by clinical sequencing.nat commun.2020 nov 10;11(1):5679.doi:10.1038/s41467-020-19342-3)和药物靶向知识库premedkb,通过三个数据集统计中国乳腺癌人群的基因突变情况,筛选高频突变的位点,除去基础基因集中重合的基因,确定符合中国人群的特定基因,共142个基因。通过上述方法,最终挑选出中国乳腺癌人群高度相关且具有意义的539个突变基因(表1),24个拷贝数变异基因(表2)。
[0063]
本发明确定的乳腺癌相关突变和拷贝数变异基因不仅包含了辅助临床诊断(例如esr1,erbb2等)、指导靶向治疗(例如brca1,brca2,pik3ca等)的基因,还包括与一些遗传相关基因(例如tp53,brca1,brca2等),对于家族遗传型的乳腺癌可以起到预警作用。除此之外,所述基因集还覆盖了乳腺癌的重要信号通路的相关基因(例如ccnd1,akt1,pten,cdk4,cdk6,myc等),与转移和耐药等生物学机制有关,对于乳腺癌新靶点的探索、开展临床试验具有极高的价值。
[0064]
本发明确定的基因集及其检测方法是大学附属肿瘤医院精准肿瘤中心数据矩阵中重要的一环。该检测方案通过检测基因集中基因的变异情况,描绘符合中国人群的基因变异数据,汇总于fudan dataportal,将多维数据结合形成共同体,从而提供更精准的临床诊断,同时为未来精准医学数字化和大数据探索提供数据支撑。
[0065]
具体地,精准肿瘤中心的数据矩阵以临床需求为基础,医生在医生工作站申请检测后,信息流进入本中心信息管理系统,样本经过实验端的dna抽提和测序后,交由分析系统进行数据分析,分析结果经过人工审核和临床解读后,回传至医生工作站,完成整个信息流和样本流的循环,同时由本发明提供的基因集检测产生的原始数据和基因变异分析结果在fudan dataportal归档(图1)。其中,用于数据存储的数据库fudan dataportal和用于自动化临床用药信息注释的知识库premedkb是数据矩阵的核心:(1)fudan dataportal数据库:中国癌症人群基因变异情况数据库,为优化更具有中国人群特点的乳腺癌基因集提供数据支撑;并辅助临床试验快速、准确地锚定获益人群,节约患者募集的时间;(2)premedkb知识库:用于基因变异的自动化用药注释,实现精准测序数据和靶点预测的对接。注释信息的来源除公开的数据库如oncokb,还整合了复旦信息团队和肿瘤医院临床专家团队用药经验,最大程度做到提供贴合实际、符合中国人群特征的自动化用药注释。
[0066]
实施例2受试者样本基因集变异信息获取
[0067]
2.1样本dna提取
[0068]
对患者的组织样本和血样分别提取dna,采用组织/血液基因组dna提取试剂盒。
[0069]
2.2样本dna打断
[0070]
取dna 500ng,无核酸酶的水(nuclease-free water,nfw)稀释至50μl,转移至96孔打断板内,充分混匀,短暂离心后使用全自动超声波破碎仪对dna随机打断。然后进行文库制备。
[0071]
2.3文库制备、杂交捕获及测序
[0072]
末端修复和接头添加:提前取出end repair&a-tailing buffer和end repair&a-tailing enzyme置于冰上融化,待融化后按照以下比例配置end repair&a-tailing mix反应体系(冰盒上操作),震荡混匀,封口膜后放置pcr仪上。反应体系如下表4所示。设置pcr程序:孵育20℃30分钟;65℃30分钟;保温4℃。待pcr仪反应结束,取出96孔板。
[0073]
表4 末端修复和a尾添加体系
[0074]
组分用量dna50μlend repair&a-tailing buffer7μlend repair&a-tailing enzyme3μl
[0075]
配制ligation反应体系(在冰盒上操作),进行连接反应。连接反应体系如表5所示。震荡混匀并进行pcr反应。pcr仪设置:孵育20℃15分钟;保温4℃。
[0076]
表5 连接反应体系
[0077][0078][0079]
磁珠纯化:提前半小时将纯化磁珠平衡至室温,震荡平衡至室温的纯化磁珠完全混匀;预先配好80%的乙醇。
[0080]
取88μl磁珠至新的圆底pp板中,将上一步的dna反应样品和磁珠混匀,室温孵育5分钟。圆底pp板置于磁力架上,5分钟磁珠吸附管壁后,用移液器取上清遗弃,加入200μl新鲜的80%乙醇至圆底pp板,静置30秒,弃上清。重复清洗2遍。圆底pp板干燥5分钟,加入31μl te至上一步的pp板中,封口膜封口,震荡均匀后离心,室温孵育5分钟。圆底pp板置于磁力架,室温静置至溶液完全澄清。转移30μl上清至新的96孔板中。
[0081]
杂交前pcr扩增:提前将pcr试剂从-20℃冰箱取出,在冰上融化后轻微涡旋混匀后按照以下比例配置pre-pcr reaction mix,振荡混匀,简短离心后放入pcr仪内进行反应。反应体系如表6所示。
[0082]
表6 杂交前pcr反应体系
[0083]
组分用量nuclease-free water3.5μlindex primer5μl100mm dntp0.5μl5
×
herculase ii reaction buffer10μlherculase ii fusion dna polymerase1μl上一步制备产物1μl
[0084]
磁珠纯化:如上磁珠纯化步骤,纯化磁珠体积为50μl。
[0085]
杂交体系制备:提前取出探针(表3)融化。将dna按照如下体系用量配制(表7)。
[0086]
表7 杂交体系
[0087]
组分用量
探针4μluniversal blockers8μlblocking solution5μl
[0088]
将以上混合好的预杂交试剂在真空浓缩仪(30℃)中烘干。取出fast hybridization mix,65℃孵育至沉淀溶解,涡旋加入20μl至上一步冻干样本中,避免产生气泡。离心去气泡,加入30μl hybridization enhancer至以上试剂表面,放置预热好的pcr仪上。
[0089]
洗脱:提前取出binding beads室温平衡。取出fast binding buffer,fast wash buffer1,wash buffer 2。震荡预平衡的binding beads至完全混匀,加入100μl磁珠至1.5ml离心管中。加入200μl fast binding buffer并用枪头吹打混匀。离心管置于磁力架上1min,弃上清,重复以上步骤3次。清洗后,加入200μl fast binding buffer,充分混匀。杂交结束后,打开pcr仪迅速将杂交液转移至平衡好的磁珠中。将加入fast binding buffer的磁珠在shaker上室温混匀。在磁力架上静置,去上清。加入200μl预热的fast wash buffer1,混匀,66℃孵育5分钟,然后离心管置于磁力架1分钟后去上清。重复步骤两次。之后再加入200μl预热的fast wash buffer2,混匀,48℃孵育5分钟,然后离心管置于磁力架1分钟后去上清。重复步骤三次。最后一次用10μl枪头吸干净洗涤液,加入45μlnfw,冰上孵育。
[0090]
杂交捕获后pcr扩增:提前将扩增buffer和扩增引物在冰上融化,轻微涡旋混匀后按照以下比例(表8)配置post-capture pcr reaction mix,震荡混匀。设置pcr程序,等pcr反应结束后,取出pcr管并离心。
[0091]
表8 pcr扩增体系
[0092]
扩增buffer25μl扩增引物2.5μl包括磁珠的样本22.5μl
[0093]
扩增产物磁珠纯化:如上磁珠纯化步骤,纯化磁珠体积为50μl。
[0094]
文库质检:取1ul文库,使用酶标仪检测文库浓度,浓度大于1ng/ul,总量不低于10ng。
[0095]
测序结果分析:测序下机的原始fastq文件进行基因组匹配后,分别分析胚系突变、体细胞突变、拷贝数变异,并分析肿瘤突变负荷(tmb)和二次打击。利用公共数据库,进行突变位点的基因信息注释。最后参考公开数据库、nccn指南和本中心的premedkb知识库,对样本的检测结果注释相关的用药信息和其他临床信息。本发明提供的多基因检测方案下机后的分析流程《ptak 1.0》已申请软著(登记号2021sr2138067)。实施例3、4和5展示了本发明的检测结果和临床解读,作为本发明具有代表性的结果(需要指出的是,实施例3-5仅为本发明检测方法的代表性示例,除本发明具体列出的代表性示例外,该方法在已经广泛应用于本中心临床,实现了中国人群乳腺癌的精准诊疗)。临床中其他样本的检测结果与实施例3、4和5类似。实施例6-10展示了基于本发明的多基因测序数据在其他项目上的探索性应用和临床试验应用。
[0096]
图29显示了本发明多基因检测和分析的示意图。
[0097]
实施例3胚系突变样本临床报告展示
[0098]
本实施例样本来源于一例乳腺癌患者的乳房肿瘤新鲜组织和配对的血液提取的人基因组dna,按照实施例2的步骤完成样本dna提取、目标序列杂交捕获、洗脱富集纯化、文库质检、上机测序和数据分析,获得组织样本280ng,血液样本800ng。具体检测结果如下:
[0099]
图2显示该样本的检测质量,包括dna质量和测序数据质量。
[0100]
图3是该样本的胚系突变检测结果,检测发现该样本的胚系突变存在brca2基因8号外显子发生657_658del的移码缺失,评估为致病。
[0101]
图4是该样本体细胞突变的检测结果,检测发现8个基因的突变,但不存在靶向用药指导相关基因的突变。
[0102]
图5展示了拷贝数变异基因的检测结果,该样本未发生拷贝数变异。
[0103]
根据该样本的胚系突变、体细胞突变和拷贝数变异的检测,用药注释1类药物:olaparib和talazoparib;2b类药物:niraparib和rucaparib(图6)。
[0104]
brca2基因与brca1基因是与乳腺癌直接有关的抑癌基因,在调解人体细胞的复制、遗传物质dna损伤修复、细胞的正常生长方面有重要作用。拥有brca基因突变的家族倾向于具有高乳腺癌发生率,通常发生在较年轻的阶段。
[0105]
实施例4体细胞突变样本临床报告展示
[0106]
本实施例样本来源于一例乳腺癌患者的乳房肿瘤新鲜组织和血液提取的人基因组dna。按照实施例2的步骤完成样本dna提取、目标序列杂交捕获、洗脱富集纯化、文库质检、上机测序和数据处理分析,所获组织dna浓度为40ng/μl,血液dna浓度为42.5ng/μl。结果如下:
[0107]
检测数据质量如图7,主要包括dna样本的抽提质量评估和测序,质量评估,是整个实验最基础的部分,数据质量的不合格将会影响后续结果的准确性及可信度。
[0108]
图8为胚系基因突变(germline mutation)的检测结果,展示该样本遗传易感性基因的突变情况,本发明的分析结果会标注是否致病的信息,该样本显示无遗传的性致病突变。
[0109]
图9展示该样本的体细胞突变(somatic mutation)检测结果,通过样本的测序序列与配对的正常基因组dna比较,确定了5个突变位点,突变类型包括剪切区域突变和错义突变,突变丰度均在10%以上。其中,该样本存在可以作为用药靶点的错义突变,pik3ca基因的21号外显子发生h1047r(1047位组氨酸变为精氨酸)的氨基酸改变,突变丰度21.2%。
[0110]
图10展示该样本的拷贝数变异情况,该样本无拷贝数变异。
[0111]
汇总上述基因变异情况,根据本中心的药物注释知识库为该样本注释的用药信息为针对pik3ca氨基酸h1047r改变的药物:1类靶向药物alpelisib;3a类:taselisib、buparlisib和everolimus;3b类:copanlisib;4类:pictrelisib和mk-2206(图11)。
[0112]
实施例5拷贝数变异样本临床报告展示
[0113]
本实施例样本来源于一例乳腺癌患者的乳房肿瘤新鲜组织和血液提取的人基因组dna,经过dna抽提、目标序列杂交捕获、洗脱富集纯化、文库质检、上机测序和数据处理分析后,检测结果如下:
[0114]
图12展示该样本检测的dna量和测序质量信息,是保证数据稳定可靠的基础。
[0115]
图13是该样本血白细胞基因突变检测结果,是胚系突变的检测来源,该样本没有致病的胚系突变。
[0116]
图14是该样本的体细胞基因突变检测结果,表格中本发明展示了突变基因、突变类型、突变位点和突变丰度。该样本没有靶向用药相关基因的体细胞突变。
[0117]
图15可见该样本发生了erbb2和myc基因的扩增。
[0118]
根据该样本的基因变异检测结果,由于该样本发生了erbb2和myc的拷贝扩增,用药注释用于erbb2拷贝数扩增的1类靶向药:trastuzumab、pertuzumab、lapatinib、neratinib、pyrotinib和ado-trastuzumab-emtansine;用于myc拷贝数扩增的4类靶向药:jq1、thz1r和azd1208(图16)。
[0119]
实施例6中国乳腺癌千人基因组检测计划
[0120]
本实施例的患者来源于复旦大学附属肿瘤医院的乳腺癌手术患者、化疗和内分泌治疗患者,根据实施例2的步骤完成样本dna提取、目标序列杂交捕获、洗脱富集纯化、文库之间、上机测序和数据处理分析,一共获得1134例患者的基因变异信息。
[0121]
图17是千人基因组计划的示意图。通过本发明提供的基因集检测后,1134例中国乳腺癌患者的多维数据整合,整合的数据包括基因组变异信息、fudan dataportal、个人基因组解读、临床报告和临床试验的结果。
[0122]
图18为中国乳腺癌人群基因突变的结果,其中,tp53(53%)和pik3ca(32%)是突变频率最高的两个基因。
[0123]
图19为中国乳腺癌人群的热点突变(hotspot)位点和突变频率。
[0124]
图20展示了中国乳腺癌人群和mskcc的国外人群乳腺癌的基因变异差异。左图为早期乳腺癌中外患者对比,右图为中晚期乳腺癌中外患者对比,其中横轴为中国乳腺癌人群的高频突变基因情况,纵轴为外国乳腺癌人群的高频突变基因情况,越接近图中虚线,表示中国人群和外国人群的基因突变频率越相似。从左图可以看出,nf1、nf2、kmt2c、kmt2d在欧美人群中的突变频率接近于0,是中国早期乳腺癌患者特有的发生突变的基因;右图可以看出,kmt2c和kmt2d在欧美人群中的突变频率接近于0,属于中国中晚期乳腺癌患者特异的突变基因。综上可知,kmt2c和kmt2d是中国乳腺癌人群的特异突变基因。其在中国人群中的突变频率显著高于mskcc数据库的欧美人群的突变频率,突出了中国乳腺癌人群独有的基因变异特征,体现了本发明提供的基因集的创新性。其中,中国人的数据来自复旦大学附属肿瘤医院,外国人群的数据来自mskcc数据库。
[0125]
图21是中国乳腺癌人群中治疗证据分级信息和精准治疗靶点分布情况。通过对本研究中接受乳腺癌多基因测序的1134例中国乳腺癌患者中的精准治疗靶点进行统计,从高到低进一步按照1、2a、2b、3a、3b、4、r1进行治疗证据分级。精准药物数据库注释后的各个亚型潜在的治疗靶点比,三阴性乳腺癌亚群拥有最高比例的潜在治疗靶点及药物。在癌症中有临床试验数据的靶点及药物(1,2a,2b)在中国乳腺癌人群中可以占到27%。
[0126]
图22表明67%以上的乳腺癌患者存在促癌突变,35%以上的乳腺癌患者具有2个以上的促癌突变。54%以上的乳腺癌存在敏感治疗靶点,约22%以上具有2个以上靶点。
[0127]
综上,根据本发明提供的基因集和检测方案,发现的潜在治疗靶点,为未来乳腺癌患者的诊疗提供更多的选择。
[0128]
实施例7临床效果展示1
[0129]
图23展示了一例晚期乳腺癌患者,经过本发明提供的多基因检测方案发现携带erbb2 l755s突变,建议使用吡咯替尼(pyrotinib)联合卡培他滨(capecitabine)治疗,2疗
程后影像学评估为pr(部分缓解)。
[0130]
实施例8临床效果展示2
[0131]
图24是一例her2受体阴性的多线治疗失败的乳腺癌患者,经过本发明提供的多基因检测方案发现携带akt1 e17k突变,白蛋白紫杉醇(nab-paclitaxel)联合依维莫司(everolimus)治疗2疗程后,影像学疗效评估为pr(部分缓解)。
[0132]
实施例9中国乳腺癌胚系-体细胞交互模式图谱
[0133]
通过本发明提供的多基因检测方案获得测序数据,经过和标准基因组文件(grc37/hg19)匹配后获得的bam文件,将其作为推断二次打击的原始文件,通过对目标位点的肿瘤组织样本和白细胞样本(正常对照)的read数量进行单边fisher检验,p值小于0.05作为结果显著的筛选条件筛选出发生了二次打击的突变位点;另一方面,若致病的胚系突变位点的等位基因存在体细胞错义突变或截断突变,则认为该位点发生了二次打击。
[0134]
图25是利用本发明提供的基因集的测序结果,建立了以二次打击为主(two-hit)的中国乳腺癌胚系和体细胞变异交互(germline and somatic interactions,gsi),在dna修复、tp53信号通路和细胞周期调控等重要通路中有富集,提供了乳腺癌预测和诊断的新模式。
[0135]
图26可见gsi在不同的乳腺癌分组中具有临床趋向性(年龄、肿瘤突变负荷tmb和ki67),证明gsi具有应用于临床诊断的潜在价值。
[0136]
实施例10临床试验展示
[0137]
future(fuscc-tnbc-umbrella,nct03805399)临床研究是在国内开展的首个针对乳腺癌的“伞形”精准治疗临床试验(jiang,y.z.et al.molecular subtyping and genomic profiling expand precision medicine in refractory metastatic triple-negative breast cancer:the future trial.cell res.2021 feb;31(2):178-186.doi:10.1038/s41422-020-0375-9),通过本发明提供的多基因检测方案将三阴性乳腺癌分为四个亚型,每个亚型对应不同的治疗靶点,最终进入七个不同的治疗组,展开分类而治的精准治疗。目前的研究成果显示,通过精准治疗策略,将多线治疗失败后的难治性三阴性乳腺癌总体客观缓解率提高到29.0%,其中免疫治疗臂的orr更是高达52.6%,突破既往免疫治疗有效率低的瓶颈。future临床试验将原来几乎无药可用的三阴性乳腺癌治疗有效率提高了三倍,成功验证了基于本发明提供的多基因检测方案对三阴性乳腺癌精准治疗的有效性。
[0138]
图27展示了难治性三阴性乳腺癌纳入研究的患者分组。通过本发明提供的多基因检测方案和乳腺癌基因组生物标志物进行分层,并将其分为以下七个治疗臂:her2阳性的lar型(a臂):吡咯替尼 卡培他滨治疗;her2阴性的lar型(b臂):雄激素受体拮抗剂 cdk4/6抑制剂治疗;im型(c臂):pd-1单抗 白蛋白紫杉醇治疗;brca1/2胚系突变阳性的blis型(d臂):parp抑制剂联合治疗;brca1/2胚系突变阴性的blis型(e臂):抗vegfr靶向药联合治疗;pi3k/akt通路突变阳性的mes型(f臂):抗vegfr靶向药联合治疗;pi3k/akt通路突变阴性的mes型(g臂):依维莫司 白蛋白紫杉醇。
[0139]
图28展示了future试验成功验证了基于本发明提供的多基因检测方案的精准治疗策略的有效性,将多线治疗失败后的难治性三阴性乳腺癌总体客观缓解率提升到29.0%,其中免疫治疗臂的客观缓解率更是高达52.6%。
[0140]
[0141]
[0142]
[0143]
[0144]
[0145]
[0146]
[0147]
[0148]
[0149]
[0150]
[0151]
[0152]
[0153]
[0154]
[0155]
[0156]
[0157]
[0158]
[0159]
[0160]
[0161]
[0162]
[0163]
[0164]
[0165]
[0166]
[0167]
[0168]
[0169]
[0170]
[0171]
[0172]
[0173]
[0174]
[0175]
[0176]
[0177]
[0178]
[0179]
[0180]
[0181]
[0182]
[0183]
[0184]
[0185]
[0186]
[0187]
[0188]
[0189]
[0190]
[0191]
[0192]
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。