κ
阿片受体激动剂的寡糖配制品
技术领域
1.本发明涉及用于口服递送治疗剂的配制品。该配制品包括活性药物成分(api)形式的治疗剂和稳定剂,例如寡糖。合适的活性药物成分包括κ阿片受体激动剂,例如d-氨基酸肽酰胺。
2.本发明还提供了一种制备用于口服递送κ阿片受体激动剂的配制品的方法,该方法包括将κ阿片受体激动剂或κ阿片受体激动剂和寡糖如海藻糖的混合物包衣在固体表面如固体珠的表面上,以在珠的固体表面上产生可释放地结合的κ阿片受体激动剂。珠可以进一步用一种或多种药学上可接受的吸收增强剂、粘合剂、稀释剂或赋形剂包衣,并且还可以包括肠溶包衣以提供在酸性条件下对配制品的保护和在肠道生理条件下配制品的溶解。
3.可替代地,用于口服递送κ阿片受体激动剂的配制品可由喷雾干燥的颗粒产生,这些颗粒由寡糖如海藻糖与κ阿片受体激动剂的混合物形成。在一个实施例中,κ阿片受体激动剂包埋在寡糖颗粒中。该颗粒还可以包括或包衣有一种或多种药学上可接受的吸收增强剂、粘合剂、稀释剂或赋形剂,并且还可以包括肠溶包衣。
4.本发明进一步涉及预防、抑制或治疗人类患者或其他哺乳动物中κ阿片受体相关疾病和病症的方法,该方法包括向该患者或该哺乳动物施用本发明的口服配制品。
背景技术:
5.κ阿片受体激动剂是一类新型的治疗剂,其具有独特的理化性质,这使得需要新的配制品,用于有效递送和针对与κ阿片受体相关的疾病和病症的预防、抑制或治疗功效的足够生物利用度。这类新型κ阿片受体激动剂包括美国专利号7,402,564、7,713,937、7,842,662和10,550,150中披露的合成肽酰胺。其他κ阿片受体激动剂包括阿西马朵林(asimadoline)(n-[(1s)-2-[(3s)-3-羟基吡咯烷-1-基]-1-苯基乙基]-n-甲基-2,2-二苯基乙酰胺)以及纳呋拉啡(nalfurafine)((2e)-n-[(5α,6β)-17-(环丙基甲基)-3,14-二羟基-4,5-环氧吗啡喃-6-基]-3-(3-呋喃基)-n-甲基丙烯酰胺)。
[0006]
可以针对不同的递送途径,例如静脉内或肌内注射、局部施用、吸入或口服施用,调整药物配制品。这些配制品中的每一种都必须满足特定的稳定性要求,这些要求允许在制备后和对患者施用之前储存一段时间。在某些情况下,配制品的不同组分可能会随着时间而相互作用,从而导致长期稳定性降低。使特定的κ阿片受体激动剂的生物利用度最大化的合适配制品和添加剂是不可预测的。
技术实现要素:
[0007]
本发明提供了一种用于口服递送治疗剂的配制品,该配制品包含作为活性药物成分(api)的κ阿片受体激动剂和稳定剂如寡糖。在一个实施例中,稳定剂使得配制品中的api在延长的时间段内稳定储存,例如在环境温度下一年内;可替代地,稳定剂使配制品中的κ阿片受体激动剂在升高的温度如40℃下稳定储存数月。在另一个实施例中,本发明的配制品包含κ阿片受体激动剂和稳定剂如寡糖,以及吸收增强剂。
[0008]
本发明进一步提供了一种配制品,该配制品是生物活性组合物,其包括包埋在寡糖中的生物活性肽,形成包括稳定的生物活性肽的颗粒。可替代地,包括生物活性肽的生物活性组合物可以与寡糖混合并包衣在固体颗粒或珠上。包衣颗粒或珠可以是肠溶包衣的。
[0009]
生物活性肽可以是任何合适的生物活性肽,例如包括一种或多种d-氨基酸的生物活性肽。在一个实施例中,包括一种或多种d-氨基酸的生物活性肽是κ阿片受体激动剂。包括一种或多种d-氨基酸的生物活性肽κ阿片受体激动剂可以是任何合适的、包括一种或多种d-氨基酸的生物活性肽κ阿片受体激动剂,例如但不限于,在美国专利号7,402,564中披露的肽κ阿片受体激动剂中的任一种。在一个实施例中,包括一种或多种d-氨基酸的生物活性肽κ阿片受体激动剂是d-phe-d-phe-d-leu-d-lys-[ω(4-氨基哌啶-4甲酸)]-oh,也称为cr845,如在美国专利号7,402,564中披露并标识为化合物2。
[0010]
在一个实施例中,本发明提供用于口服递送κ阿片受体激动剂的配制品,其中该配制品包含含有κ阿片受体激动剂和寡糖的颗粒。κ阿片受体激动剂可以为
[0011]
(i)cr845,其具有式:
[0012][0013]
d-phe-d-phe-d-leu-d-lys-[ω(4-氨基哌啶-4-甲酸)]-oh
[0014]
或cr845的水合物、盐、酸式盐或酸式盐水合物;
[0015]
(ii)阿西马朵林(n-[(1s)-2-[(3s)-3-羟基-吡咯烷-1-基]-1-苯基乙基]-n-甲基-2,2-二苯基乙酰胺),
[0016]
或
[0017]
(iii)纳呋拉啡((2e)-n-[(5α,6β)-17-(环丙基甲基)-3,14-二羟基-4,5-环氧吗啡喃-6-基]-3-(3-呋喃基)-n-甲基丙烯酰胺)。
[0018]
寡糖可以是任何合适的寡糖,例如海藻糖、蔗糖、麦芽糖、甘露糖、乳糖和菊糖。
[0019]
在本发明的另一个实施例中,用于口服递送治疗剂的配制品(在本文中可互换地称为本发明的口服配制品)包含含有一种或多种d-氨基酸的肽酰胺κ阿片受体激动剂和稳定剂如寡糖以及一种或多种吸收增强剂。含有一种或多种d-氨基酸的肽酰胺κ阿片受体激动剂可以是含有至少一种d-氨基酸的任何合适的肽酰胺,例如但不限于授予schteingart等人的美国专利号7,402,564、7,713,937和7,842,662(其全部披露内容通过引用并入本文)中披露的合成肽酰胺中的任一种。
[0020]
在另一个实施例中,生物活性组合物包含包埋在寡糖中的生物活性肽,形成包含稳定的生物活性肽的颗粒,其中寡糖包括二糖。二糖可以是任何合适的二糖,例如包括一个或多个葡萄糖单体的二糖。在一个实施例中,二糖包括海藻糖,即1,1-α-糖苷连接的葡萄糖二聚体。在特定的实施例中,二糖可以完全由海藻糖组成。
[0021]
在一个实施例中,生物活性组合物包含包埋在寡糖中的生物活性肽,形成包含稳定的生物活性肽的颗粒,其中该寡糖在25℃下至少一年内增强生物活性肽的稳定性。
[0022]
在本发明的口服配制品的另一个实施例中,口服配制品包含肽酰胺κ阿片受体激
动剂、寡糖和一种或多种吸收增强剂,其中肽酰胺κ阿片受体激动剂具有下式的结构:
[0023]
xaa
1-xaa
2-xaa
3-xaa
4-(g)
ꢀꢀꢀ
式i
[0024]
其中g为酰胺基团,如美国专利号7,402,564、7,713,937和7,842,662中任一个中所述。
[0025]
在另一个实施例中,本发明的口服配制品包含肽酰胺κ阿片受体激动剂和一种或多种吸收增强剂,其中肽酰胺κ阿片受体激动剂是具有下式结构的cr845:
[0026][0027]
式ii
[0028]
d-phe-d-phe-d-leu-d-lys-[ω(4-氨基哌啶-4-甲酸)]-oh
[0029]
或其水合物、盐或酸式盐水合物。
[0030]
在又另一个实施例中,本发明的口服配制品可进一步包含一种或多种吸收增强剂、粘合剂、表面活性剂、螯合剂和药学上可接受的赋形剂或稀释剂。
[0031]
在一个实施例中,本发明提供一种制备用于口服递送κ阿片受体激动剂的配制品的方法,该方法包括将κ阿片受体激动剂和寡糖的混合物喷雾干燥以形成由包埋在寡糖中的κ阿片受体激动剂形成的颗粒。颗粒可以配制成片剂、囊片、胶囊、粉末、浆液、液体悬浮剂或凝胶。
[0032]
本发明还提供了一种制备用于口服递送κ阿片受体激动剂的配制品的方法,该方法包括将κ阿片受体激动剂或κ阿片受体激动剂和寡糖如海藻糖的混合物包衣到固体表面如固体珠或微珠的表面上,以在珠或微珠的固体表面上产生可释放地结合的κ阿片受体激动剂。
[0033]
用根据本发明的κ阿片受体激动剂包衣的珠或微珠可以由任何药学上合适的材料形成,例如但不限于:微晶纤维素;蔗糖颗粒组合物(例如宾夕法尼亚州查尔丰特卡乐康公司(colorcon,chalfont,pa),其为由蔗糖和淀粉制成的均匀药物分层小丸,用于立即、延迟、持续或延长释放剂型,具有低脆性、一致的球形度、紧密的粒度控制和高批次间均匀性;pharm-a-spheres
tm
,德国托尔内施(tornesch,germany):糖球,其特征在于用于进一步加工的突出的机械稳定性,为持续释放型配制品提供合适的载体)。用于用κ阿片受体激动剂组合物包衣的其他合适的颗粒包括甘露醇小丸和酒石酸小丸(瑞士basel-allschwil的pharmatrans sanaq ag公司(pharmatrans sanaq ag,basel-allschwil,switzerland))。
[0034]
一种或多种寡糖包埋的κ阿片受体激动剂包衣的珠或微珠还可以用一种或多种药学上可接受的吸收增强剂、粘合剂、螯合剂、稀释剂或赋形剂包衣,并且还可以包括肠溶包衣以在酸性条件下提供对配制品的保护和在肠道生理条件(例如ph 5.5-6.0)下配制品的溶解。可替代地,一种或多种寡糖包埋的κ阿片受体激动剂包衣的珠或微珠可以包封在肠溶包衣胶囊中用于口服递送。
[0035]
本发明进一步提供了用于口服递送包含κ阿片受体激动剂的治疗剂和吸收增强剂
的配制品的使用方法,用于预防、抑制或治疗人类患者或其他哺乳动物中的κ阿片受体相关的疾病和病症,该方法包括向患者或哺乳动物施用本发明的配制品。在一个实施例中,本发明的配制品包含寡糖,例如海藻糖。所施用的配制品可进一步包含一种或多种粘合剂、表面活性剂、螯合剂和药学上可接受的赋形剂或稀释剂以及一种或多种适于优化κ阿片受体激动剂从胃肠系统吸收并由此增强其生物活性的吸收增强剂。所施用的配制品可进一步包含一种或多种粘合剂、表面活性剂、螯合剂和药学上可接受的赋形剂或稀释剂以及一种或多种适于优化κ阿片受体激动剂从胃肠系统吸收并由此增强其生物活性的吸收增强剂。
[0036]
本发明还提供一种预防、抑制或治疗κ阿片受体激动剂相关疾病或病症的方法,该方法包括向患有κ阿片受体激动剂相关疾病或病症的患者或其他哺乳动物施用包含κ阿片受体激动剂和稳定剂如寡糖的口服配制品。在另一个实施例中,该方法包括施用口服配制品,该口服配制品包含κ阿片受体激动剂和稳定剂如寡糖以及吸收增强剂。所施用的口服配制品可进一步包含一种或多种粘合剂、表面活性剂、螯合剂和药学上可接受的赋形剂或稀释剂以及一种或多种适于优化κ阿片受体激动剂从胃肠系统吸收并由此增强其生物活性的吸收增强剂。
附图说明
[0037]
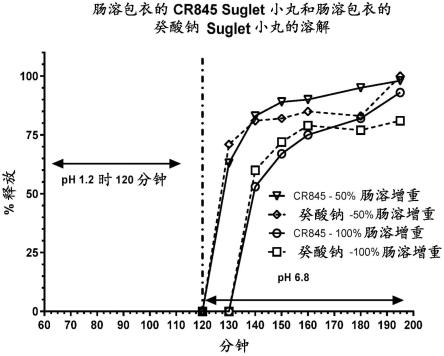
图1显示了肠溶包衣的cr845 suglet小丸和肠溶包衣的癸酸钠suglet小丸随时间的溶解曲线。
[0038]
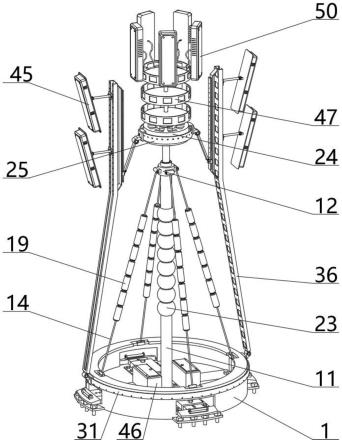
图2-6分别显示了来自实例3的包衣在复合颗粒a-e上的海藻糖包埋的cr845在针对每种复合物施用于八只犬科受试者后的生物活性曲线。
具体实施方式
[0039]
在一个实施例中,本发明的口服配制品包含含有κ阿片受体激动剂肽的治疗剂和寡糖稳定剂。寡糖稳定剂可以是任何合适的寡糖稳定剂,例如但不限于麦芽糖、蔗糖、乳糖和海藻糖。在一个实施例中,κ阿片受体激动剂可任选地包埋在寡糖的颗粒基质中,例如1,1α-葡萄糖二聚体、海藻糖(α-d-吡喃葡萄糖基-(1
→
1)-α-d-吡喃葡萄糖苷)。在一个实施例中,κ阿片受体激动剂可任选地与寡糖混合或包埋在由寡糖形成的颗粒基质中或可形成配制品层(包衣固体基质如珠或微珠)。κ阿片激动剂和寡糖的包衣可以通过将含有在挥发性溶剂中的κ阿片激动剂和寡糖的溶液喷雾干燥以形成固体颗粒来实现,或者可以将溶液喷雾到任何所需的固体上,以在固体表面形成κ阿片激动剂和寡糖的包衣。在一个实例中,固体表面可以是任何合适的固体表面,例如珠或微珠的表面,并且寡糖是海藻糖。
[0040]
在一个实施例中,本发明提供一种包含κ阿片受体激动剂cr845和二糖海藻糖的配制品。配制品可进一步包含ph调节剂(例如羧酸或羧酸的盐)、吸收增强剂、粘合剂、螯合剂和药学上可接受的载体或赋形剂中的一种或多种。
[0041]
在另一个实施例中,配制品包含cr845和海藻糖,进一步包含柠檬酸或柠檬酸钠、螯合剂如edta和吸收增强剂如月桂酰l-肉碱或癸酸钠。在一个实施例中,柠檬酸可以是包衣的柠檬酸,例如粉末dcf 20包衣的柠檬酸。
[0042]
本发明的配制品可以呈药学上可接受的片剂、囊片、胶囊、粉末、浆液或液体悬浮剂的形式,并且可以被调味或包含在例如苹果酱或果汁中供儿科使用。
[0043]
在另一个实施例中,本发明提供一种制备用于口服递送κ阿片受体激动剂的配制品的方法,该方法包括:将κ阿片受体激动剂和寡糖的雾化混合物喷雾干燥或喷雾包衣到一种或多种固体颗粒上以形成κ阿片受体激动剂/海藻糖包衣的固体颗粒;以及在κ阿片受体激动剂/海藻糖包衣的固体颗粒上形成肠溶包衣,以产生包含一种或多种具有肠溶包衣的κ阿片受体激动剂/海藻糖包衣的固体颗粒的配制品。
[0044]
在另一个实施例中,本发明提供用于口服递送治疗剂的配制品的剂型,其中该配制品在胶囊、囊片、片剂、粉末或凝胶中包含κ阿片受体激动剂、寡糖和一种或多种吸收增强剂。肠溶包衣的胶囊可以是具有肠溶包衣的胶囊或具有固有肠溶性质的组合物的胶囊。具有固有肠溶性质的组合物的实例是聚合物羟丙基甲基纤维素(hpmc)。
[0045]
在另一个实施例中,本发明的口服配制品包含κ阿片受体激动剂肽、寡糖稳定剂和至少一种吸收增强剂。吸收增强剂可以是任何合适的吸收增强剂。可以加入的合适的吸收增强剂的实例包括亲水性表面活性剂,例如80(聚氧乙烯20山梨醇单油酸酯)、60(聚氧乙烯20山梨醇单硬脂酸酯)、alf(peg-8-辛酸/癸酸甘油酯)、el(peg-35甘油蓖麻醇酸酯)、hs 15(peh-15羟基硬脂酸酯)和44/14(月桂酰peg-32单/二/三甘油酯)。可以加入的合适的吸收增强剂的其他实例包括疏水性吸收增强剂,例如capmul mcm、captex 100、captex 200和capryol pgmc以及色氨酸;和两亲性吸收增强剂,例如脂肪酸二醇和壳聚糖的季铵盐,例如季铵棕榈酰二醇壳聚糖。
[0046]
在一个实施例中,本发明的配制品包含含有一种或多种d-氨基酸的κ阿片受体激动剂、寡糖稳定剂和至少一种吸收增强剂,该配制品可以呈凝胶、胶囊或片剂的形式,其中该配制品进一步包含药学上可接受的稀释剂、赋形剂或载体。在一个实施例中,胶囊是肠溶包衣的胶囊或具有固有肠溶性质的胶囊。
[0047]
在一个实施例中,本发明的配制品包括κ阿片受体激动剂(例如但不限于阿西马朵林(n-[(1s)-2-[(3s)-3-羟基-吡咯烷-1-基]-1-苯基乙基]-n-甲基-2,2-二苯基乙酰胺)或纳呋拉啡((2e)-n-[(5α,6β)-17-(环丙基甲基)-3,14-二羟基-4,5-环氧吗啡喃-6-基]-3-(3-呋喃基)-n-甲基丙烯酰胺),或美国专利号10,550,150中披露的任何四肽酰胺κ阿片受体激动剂),和任选地一种或多种吸收增强剂。任选的吸收增强剂可以是许多合适的吸收增强剂中的一种或多种,例如上述亲水性表面活性剂、疏水性吸收增强剂和两亲性吸收增强剂中的任一种或多种。
[0048]
在本发明的一个实施例中,包含κ阿片受体激动剂和一种或多种吸收增强剂的配制品还包含寡糖,例如海藻糖。寡糖可以是包衣或与κ阿片受体激动剂混合,并且在一些实施例中,寡糖可以以足够的量提供,使得κ阿片受体激动剂包埋或基本上包埋在寡糖中。在一个实施例中,约1%-50%(w/w)的κ阿片受体激动剂包埋在50%-99%(w/w)的海藻糖中。可替代地,约2%-25%(w/w)的κ阿片受体激动剂包埋在75%-98%(w/w)的海藻糖中。在另一个实施例中,约5%-15%(w/w)的κ阿片受体激动剂包埋在85%-95%(w/w)的海藻糖中。在又另一个实施例中,约10%(w/w)的κ阿片受体激动剂包埋在90%(w/w)的海藻糖中。
[0049]
在本发明的另一个实施例中,包含κ阿片受体激动剂和一种或多种吸收增强剂的配制品还包含中链脂肪酸或中链脂肪酸的盐以及中链脂肪酸甘油酯。
[0050]
在另一个实施例中,本发明的口服配制品包含:含有肽的治疗剂和至少一种吸收
增强剂,吸收增强剂包括中链脂肪酸或中链脂肪酸的盐以及中链脂肪酸甘油酯,其中中链脂肪酸或中链脂肪酸的盐包含癸酸或癸酸的盐,其中配制品不包括稳定剂,例如聚乙烯吡咯烷酮(pvp)。出人意料地,发现本发明的配制品在不使用pvp或其他此类稳定剂的情况下是有效的。
[0051]
本发明还提供了治疗或预防哺乳动物的κ阿片受体相关疾病或病症的方法。该方法包括向哺乳动物施用包含有效量的上述本发明配制品的组合物。
[0052]
用于定义本发明配制品的肽和d-氨基酸肽的命名法在schroder和lubke,the peptides[肽],academic press[学术出版社],1965中进行了说明,其中根据传统表示法,n末端出现在左侧,而c末端出现在右侧。其中氨基酸残基具有异构形式,意图是同时涵盖氨基酸的l-异构体形式和d-异构体形式,除非另有说明。本文中通常通过标准的3字母代码来标识氨基酸。氨基酸的d异构体由前缀“d
‑”
标明,例如表示d-苯丙氨酸(即苯丙氨酸的d-异构体)的“d-phe”。类似地,l-异构体由前缀“l
‑”
标明,如“l-phe”一样。
[0053]
如本文所用,κ阿片受体相关疾病、病症或障碍是可通过激活κ阿片受体预防或治疗的任何疾病、病症或障碍。在一些实施例中,临床医生可以选择包含κ阿片受体激动剂肽酰胺的本发明的配制品的特定口服剂量以完全预防或治愈疾病、病症或障碍。在其他实施例中,临床医生选择的包含κ阿片受体激动剂肽酰胺的本发明的配制品的特定口服剂量改善或减轻疾病、病症或障碍的一种或多种症状。
[0054]
如本文所用,包含在本发明的配制品中的包含κ阿片受体激动剂肽酰胺的本发明配制品的“有效量”或“足够量”是指本文所述的配制品的量,其在治疗上可以有效地抑制、预防或治疗特定疾病、障碍、病症或副作用的症状。
[0055]
如本文所用,“药学上可接受的”是指在可靠的医学判断的范围内、适于与人类和动物的组织接触而没有严重的毒性、刺激、过敏反应,或其他并发症、与对于所治疗的医学病症而言合理的益处/风险比相符的化合物、材料、组合物、和/或剂型。
[0056]
如本文所用,“剂量单位”是指用于待治疗的特定个体或病症的适合作为单位剂量的物理上分离的单位。每个单位可包含预定量的本发明配制品,其包含经计算可产生期望的一种或多种治疗效果的活性κ阿片受体激动剂肽酰胺,任选地与药物载体缔合。剂量单位形式的规范可由以下来指定:(a)活性κ阿片受体激动剂肽酰胺的独特特性,以及要实现的特定治疗效果,和(b)复合这种活性κ阿片受体激动剂肽酰胺的领域中固有的局限性。剂量单位通常表示为化合物重量/单位体重,例如,以化合物毫克数/千克受试者或患者的体重(mg/kg)表示。可替代地,在特定的剂量方案中,剂量可以被表示为化合物量/单位体重/单位时间(mg/kg/天)。在又一种替代方案中,剂量可以被表示为化合物量/单位体表面积(mg/m2)或化合物量/单位体表面积/单位时间(mg/m2/天)。
[0057]
如本文所用,“药学上可接受的盐”是指化合物的衍生物,其中母体化合物通过制备其酸或碱式盐而被修饰。药学上可接受的盐的实例包括但不限于碱性残基例如胺的无机或有机酸盐;酸性残基例如羧酸等的碱金属或有机盐。药学上可接受的盐包括例如由无毒的无机或有机酸形成的母体化合物的常规无毒盐或季铵盐。例如,这种常规的无毒盐包括衍生自无机酸(如盐酸、氢溴酸、硫酸、氨基磺酸、磷酸,硝酸等)的那些;以及从以下有机酸制备的盐,如乙酸、丙酸、琥珀酸、乙醇酸(glycolic)、硬脂酸、乳酸、苹果酸、酒石酸、柠檬酸、抗坏血酸、帕莫酸(pamoic)、马来酸、羟基马来酸、苯乙酸、谷氨酸、苯甲酸、水杨酸、对氨
基苯磺酸、2-乙酰氧基苯甲酸、富马酸、甲苯磺酸、甲烷磺酸、乙烷二磺酸、草酸、异硫羰酸(isothionic acid)等。这些生理上可接受的盐通过本领域已知的方法制备,例如通过将游离胺碱与过量的酸溶解在含水醇中,或用碱金属碱(例如氢氧化物)或胺中和游离羧酸。因此,合成的肽酰胺的药学上可接受的盐可以由任何具有酸性、碱性或两种官能团的肽酰胺形成。例如,在药学上适合的碱的存在下,具有羧酸基团的肽酰胺可以形成与如钠或钾阳离子等阳离子配对的羧酸根阴离子。类似地,在药学上适合的酸例如hcl的存在下,具有胺官能团的肽酰胺可以形成盐。
[0058]
κ阿片受体激动剂肽酰胺的药学上可接受的溶剂化物的实例是肽酰胺与溶剂分子的组合,其产生这种溶剂分子与肽酰胺缔合的一种络合物。药物和丙二醇(1,2-丙二醇)的组合已用于形成药物溶剂化物。参见例如美国专利号3,970,651。其他合适的溶剂化物是药物化合物的水合物。此类水合物包括具有相当活性的水合物或施用后可被转变回活性化合物的水合物。合成的肽酰胺的药学上可接受的n-氧化物是这样的化合物,其包含胺基,其中胺的氮键合至氧原子。
[0059]
可用于本发明的配制品中的κ阿片受体激动剂肽酰胺的药学上可接受的结晶、同构结晶或无定形形式可以是根据本发明的κ阿片受体激动剂肽酰胺的药学上可接受的酸式盐、碱式盐、两性离子盐、水合物或任何其他适当稳定、生理相容的形式的任何结晶或非结晶形式。
[0060]
可将本发明配制品中的κ阿片受体激动剂肽酰胺掺入药物组合物中。该组合物可以包含处于药学上可接受的稀释剂、赋形剂或载体中的有效量的κ阿片受体激动剂肽酰胺。药物组合物中所用的常规赋形剂、载体和/或稀释剂通常是惰性的并构成制剂的主要部分。药物赋形剂或载体可以是适合作为用于递送本发明的合成肽酰胺的媒剂的任何相容的、无毒性物质。适合的赋形剂或载体包括但不限于,无菌水(优选无热原)、盐水、磷酸盐缓冲的盐水(pbs)、水/乙醇、水/甘油、水/山梨糖醇、水/聚乙二醇、丙二醇、鲸蜡硬脂醇、羧甲基纤维素、玉米淀粉、乳糖、葡萄糖、微晶纤维素、硬脂酸镁、聚乙烯吡咯烷酮(pvp)、柠檬酸、酒石酸、油、脂肪性物质、蜡或任何上述物质的合适混合物。
[0061]
可以将根据本发明的药物组合物配制为液体、半固体或固体剂型。例如药物制剂可以呈下述形式:溶液、滴剂、糖浆剂、喷雾、悬浮剂、凝胶剂、乳剂或处于微粒形式,例如小丸或颗粒,任选地可压制为片剂或锭剂,封装于胶囊剂中或者悬浮在液体中。片剂可以含有粘合剂、润滑剂、稀释剂、着色剂、调味剂、湿润剂并且可以具有肠溶包衣从而能够耐受胃的酸性环境而在肠腔的更偏碱性的条件中溶解。可替代地,片剂可以有糖衣或以水溶性膜包被的膜衣。还可以向药物组合物中掺入药学上可接受的佐剂、缓冲剂、分散剂等。
[0062]
粘合剂包括例如淀粉、胶浆剂、明胶和蔗糖。润滑剂包括滑石、石松子、硬脂酸镁和硬脂酸钙/硬脂酸。稀释剂包括乳糖、蔗糖、甘露醇、盐、淀粉和高岭土。湿润剂包括丙二醇和山梨醇单硬脂酸酯。
[0063]
对于口服施用,可以以固体剂型例如胶囊剂、片剂和粉末,或液体剂型例如酏剂、糖浆剂和悬浮剂来施用活性成分。可将一种或多种活性组分与非活性成分和粉状载体(如葡萄糖、乳糖、蔗糖、甘露醇、淀粉、纤维素或者纤维素衍生物、硬脂酸镁、硬脂酸、糖精钠、滑石和碳酸镁等)一起包封入明胶胶囊中。可以加入从而提供所需的颜色、味道、稳定性、缓冲能力、分散作用或者其他已知的期望特征的另外非活性成分的实例是红氧化铁、硅胶、十二
烷基硫酸钠、二氧化钛和食用白墨等。可以使用类似的稀释剂来制造压制片剂。片剂和胶囊均可制作成缓释产品从而使药物在数小时的时段内连续释放。压制片剂可以有糖衣或膜衣,以掩蔽任何令人不愉快的味道,并保护片剂免受大气的影响,或者可以有肠溶包衣,以在胃肠道中选择性地崩解。口服施用的液体剂型可含有着色剂和调味剂,以提高患者的接受程度。为了有利于药物稳定性和吸收性,本发明的肽可以在通过胃的严酷的蛋白水解性环境后从胶囊中释放出来。
[0064]
活性成分可一次全部施用,或者可以分为许多更小剂量以一定的时间间隔进行施用,或者作为控释配制品施用。术语“控释配制品”涵盖允许本发明的合成肽酰胺在一段时间内,例如几天至几周内连续递送至受试者的配制品。此类配制品可以皮下施用或肌内施用,并随着时间的推移在受试者中以连续稳定状态释放预定量的化合物。κ阿片受体激动剂肽酰胺的控释配制品可以是例如含有聚合物微囊的药物配制品,例如在美国专利号4,677,191和4,728,721(通过引用并入本文)中所述的那些。药物活性化合物的浓度经调节使得其施用可提供产生期望效果的有效量。本领域中已知的是,确切剂量取决于患者或动物的年龄、重量和状况。对于任何特定的受试者,可以根据个体需要以及管理或监督配制品施用的人员的专业判断而随着时间调整具体的剂量方案。因此,本文所述的浓度范围仅是示例性的,而并非旨在限制要求保护的本发明的范围或实施。
[0065]
可施用组合物以预防或治疗患有疾病或障碍或者处于患上疾病或障碍风险中的个体。预防被定义为旨在维护个体健康的措施。对于治疗性应用,药物组合物通常以足以抑制、预防或者改善疾病或障碍的量施用于患有该疾病或障碍的受试者。将足以实现这些的量定义为“治疗有效剂量”。
[0066]
为了预防或治疗目的,可以将本发明的药物配制品施用于哺乳动物。哺乳动物可以是任何哺乳动物,例如驯养的或未驯化的哺乳动物,或者甚至是野生哺乳动物。哺乳动物可以是任何灵长类、有蹄类、犬科或猫科动物。例如但不限于,哺乳动物可以是宠物或伴侣动物,例如狗或猫;高价值的哺乳动物,例如纯种马或表演动物;农场动物,例如牛、山羊、绵羊或猪;或灵长类动物,例如猿、大猩猩、猩猩、狐猴、猴或黑猩猩。适合于使用本发明的药物配制品来预防或治疗的哺乳动物是人。
[0067]
可以对患有可通过活化κ阿片受体来治疗的疾病或病症的哺乳动物施用本发明的药物配制品。可替代地,可以将药物组合物作为预防用药施用于有风险感染或发展下述疾病或病症的哺乳动物,该疾病或病症可通过活化κ阿片受体来预防。可通过施用本发明的药物组合物来治疗或预防的疾病或病症包括但不限于,可通过活化κ阿片受体来减轻的任何病症,包括诸如疼痛、炎症、瘙痒、低钠血症、低钾血症、充血性心力衰竭、肝硬化、肾病综合征、高血压、水肿、肠梗阻、咳嗽和青光眼等病症。
[0068]
本发明进一步提供了治疗或预防哺乳动物的κ阿片受体相关疾病或病症的方法,其中该方法包括向该哺乳动物施用含有有效量的本发明的配制品中的κ阿片受体激动剂肽酰胺的组合物。哺乳动物可以是任何哺乳动物,例如驯养的或未驯化的哺乳动物,或者甚至是野生哺乳动物。可替代地,哺乳动物可以是任何灵长类、有蹄类、犬科或猫科动物。例如但不限于,哺乳动物可以是宠物或伴侣动物,例如高价值哺乳动物,例如纯种动物或表演动物;农场动物,例如牛、山羊、绵羊或猪;或灵长类动物,例如猿或猴。在一个特定方面,哺乳动物是人。
[0069]
可用本发明的配制品中的κ阿片受体激动剂肽酰胺预防或治疗的κ阿片受体相关疾病、障碍或病症可以是任何κ阿片受体相关病症,包括但不限于急性或慢性疼痛、炎症、瘙痒、低钠血症、水肿、肠梗阻、咳嗽和青光眼。例如,κ阿片受体相关疼痛可以是神经性疼痛、躯体痛、内脏痛或皮肤痛。一些疾病、障碍或病症与多于一种的疼痛形式有关,例如,手术后痛可以具有神经性疼痛、躯体痛、内脏痛或皮肤痛因素中的任一种或全部,这取决于所采用的外科手术的类型和程度。
[0070]
κ阿片受体相关炎症可以是任何炎性疾病或病症,包括但不限于窦炎、类风湿性关节炎腱鞘炎、滑囊炎、腱炎、肱骨外上髁炎、粘性囊炎、骨髓炎、骨关节炎性炎症、炎性肠病(ibd)、肠易激综合征(ibs)、眼部炎症、耳炎性炎症或自体免疫性炎症。
[0071]
κ阿片受体相关瘙痒可以是任何瘙痒疾病或病症,例如眼部瘙痒(与术语瘙痒可互换使用)(例如结膜炎相关的眼部瘙痒),耳炎性瘙痒,与以下有关的瘙痒:末期肾病(也称为尿毒症瘙痒)(其中许多患者接受肾透析),和其他形式的胆汁淤积,包括原发胆汁性肝硬化、妊娠肝内胆汁淤积症、慢性胆固醇肝病、尿毒症、恶性胆汁淤积、黄疸,以及皮肤病症,例如湿疹(皮炎),包括特应性皮炎或接触性皮炎、牛皮癣、红细胞增多症、扁平苔藓、慢性单纯性苔藓、虱病(虱)、甲状腺毒症、足癣、荨麻疹、疥疮、阴道炎、痔疮相关的肛门瘙痒,以及毒虫螫伤瘙痒、化疗引起的瘙痒和药物引起的瘙痒,例如μ阿片引起的瘙痒。
[0072]
κ阿片受体相关瘙痒可以是任何神经性瘙痒,例如但不限于感觉异常性背痛、接触性皮炎和特应性皮炎。
[0073]
κ阿片受体相关水肿可以是任何水肿性疾病或病症,例如充血性心脏病引起的水肿或抗利尿激素(adh)分泌不当综合征引起的水肿。κ阿片受体相关肠梗阻可以是任何肠梗阻疾病或病症,包括但不限于术后肠梗阻和阿片引起的肠功能障碍。κ阿片受体相关神经性疼痛可以是任何神经性疼痛,例如,三叉神经痛、糖尿病性疼痛、病毒性疼痛例如带状疱疹相关的疼痛、化疗引起的疼痛、侵袭神经的转移癌症疼痛、外伤和外科手术相关的神经性疼痛、以及各种被认为具有神经病理因素的头痛变体例如偏头痛。
[0074]
κ阿片相关疼痛还包括眼部疼痛,例如,屈光性角膜切削术(prk)、眼撕裂、眼底骨折、化学烧伤、角膜上皮擦伤或刺激之后的眼部疼痛,或与结膜炎、角膜溃疡、巩膜炎、巩膜外层炎、巩膜角膜炎、眼部带状疱疹、间质性角膜炎、急性虹膜炎、干燥性角膜结膜炎、眼眶蜂窝织炎、眼眶假瘤、天疱疮、沙眼或葡萄膜炎相关的疼痛。
[0075]
κ阿片相关疼痛还包括喉咙痛,尤其是与炎性病症,例如过敏性鼻炎、急性支气管炎、普通感冒、接触性溃疡、单纯疱疹病毒损伤、感染性单核细胞增多症、流行性感冒、喉癌、急性喉炎、急性坏死性溃疡齿龈炎、扁桃腺脓肿、咽部烧灼、咽炎、反流性咽喉炎、急性窦炎和扁桃腺炎相关的喉咙痛。
[0076]
本发明提供了一种在哺乳动物例如人中治疗或预防κ阿片受体相关疾病或病症的方法,其中该方法包括向该哺乳动物施用本发明配制品,其包含有效量的κ阿片受体激动剂肽酰胺和本发明的吸收增强剂。在另一个实施例中,κ阿片受体相关病症是疼痛。
[0077]
在另一个实施例中,可用本发明的配制品治疗的κ阿片受体相关病症是炎症,例如类风湿性关节炎性炎症、骨关节炎性炎症、ibd炎症、ibs炎症、眼部炎症、耳炎性炎症、自体免疫性炎症或由病毒感染引起的炎症,例如由人流感病毒或人畜共患流感病毒(例如引起猪流感的h1n1病毒)引起的炎症。可以用本发明的κ阿片受体激动剂配制品治疗的引起炎症
的其他病毒感染包括由以下冠状病毒感染引起的炎症:sars相关冠状病毒(严重急性呼吸综合征相关病毒,sars cov)和新型冠状病毒ncov2引起的炎症,ncov2是冠状病毒covid19大流行的原因。
[0078]
在又另一个实施例中,可用本发明的配制品治疗的κ阿片受体相关病症是瘙痒(例如特应性皮炎、肾透析相关的瘙痒、眼部瘙痒、耳炎性瘙痒、毒虫螫伤瘙痒或阿片引发的瘙痒)、水肿、肠梗阻、咳嗽或青光眼。
[0079]
在一方面,疼痛是神经性疼痛(例如三叉神经痛、偏头痛、糖尿病性疼痛、病毒性疼痛、化疗引起的疼痛或转移癌症疼痛)、躯体痛、内脏痛或皮肤痛。在另一方面,疼痛是关节炎疼痛、肾结石疼痛、子宫痉挛、痛经、子宫内膜异位症、消化不良、外科手术后疼痛、医疗程序后疼痛、眼部疼痛、耳炎疼痛、爆发性癌症疼痛或与gi障碍(例如ibd或ibs)相关的疼痛。在另一方面,疼痛是与外科手术相关的疼痛,其中外科手术是骨盆腹腔镜检查、输卵管结扎、子宫切除术和胆囊切除术。可替代地,疼痛可以是与医疗程序(例如,结肠镜检查、膀胱镜检查、宫腔镜检查或子宫内膜活组织检查)相关的疼痛。在一个具体方面,特应性皮炎可以是牛皮癣、湿疹或接触性皮炎。在另一个具体方面,肠梗阻是术后肠梗阻或阿片引起的肠功能障碍。
[0080]
可用本发明的合成肽酰胺治疗或预防的另一种形式的κ阿片受体相关疼痛是痛觉过敏。在一个实施例中,该方法包括对患有或有风险发展为痛觉过敏的哺乳动物施用有效量的本发明的合成肽酰胺从而预防、改善或彻底减轻痛觉过敏。
[0081]
κ阿片受体相关疼痛包括痛觉过敏,该痛觉过敏据信是由局部组织损伤之后发生的外周感觉末梢的环境改变引起的。组织损伤(例如擦伤,烧伤)和炎症会导致多峰伤害感受器(c纤维)和高阈值机械感受器的兴奋性显著提高。这种被提高的兴奋性和感觉传入被放大的反应据信是痛觉过敏的基础,其中疼痛反应是对刺激的反应被放大的结果。痛觉过敏状态在损伤后疼痛状态中的重要性已被反复证明并似乎是大部分损伤后/炎性疼痛状态的原因。
[0082]
在另一个实施例中,与κ阿片受体相关的病症是疼痛、炎症(例如类风湿性关节炎性炎症、骨关节炎性炎症、ibd炎症、ibs炎症、眼部炎症、耳炎性炎症或自体免疫性炎症)、瘙痒(例如特应性皮炎、肾透析相关的瘙痒、眼部瘙痒、耳炎性瘙痒、毒虫螫伤瘙痒或阿片引发的瘙痒)、水肿、肠梗阻、咳嗽或青光眼。在一方面,疼痛是神经性疼痛(例如三叉神经痛、偏头痛、糖尿病性疼痛、病毒性疼痛、化疗引起的疼痛或转移癌症疼痛)、躯体痛、内脏痛或皮肤痛。在另一方面,疼痛是关节炎疼痛、肾结石疼痛、子宫痉挛、痛经、子宫内膜异位症、消化不良、外科手术后疼痛、医疗程序后疼痛、眼部疼痛、耳炎疼痛、爆发性癌症疼痛或与gi障碍(例如ibd或ibs)相关的疼痛。在另一方面,疼痛是与外科手术相关的疼痛,其中外科手术是骨盆腹腔镜检查、输卵管结扎、子宫切除术和胆囊切除术。可替代地,疼痛可以是与医疗程序(例如,结肠镜检查、膀胱镜检查、宫腔镜检查或子宫内膜活组织检查)相关的疼痛。在一个具体方面,特应性皮炎可以是牛皮癣、湿疹或接触性皮炎。在另一个具体方面,肠梗阻是术后肠梗阻或阿片引起的肠功能障碍。
[0083]
在另一个实施例中,κ阿片受体相关病症是可通过保钠利尿和保钾利尿(也被称为促水排泄(aquaresis))预防或治疗的κ阿片受体相关病症。可通过施用本发明的配制品中的κ阿片受体激动剂肽酰胺来预防或治疗的κ阿片受体相关病症的实例包括水肿。水肿可以
是各种疾病或病症(例如充血性心脏病或adh分泌不当综合征)中的任意一种引起的。
[0084]
在另一个实施例中,κ阿片受体相关病症是低钠血症或其他水肿性疾病。κ阿片受体相关低钠血症或水肿可以是任何低钠血性或水肿性疾病或病症,例如,充血性心力衰竭相关的或抗利尿激素(adh)分泌不当综合征相关的低钠血症以及水肿,或者与以噻嗪类和/或袢利尿剂过度利尿疗法相关的低钠血症。本发明的合成肽酰胺显示了显著的保钠和保钾促水排泄效果,这有利于治疗与低钠血症和/或低钾血症相关的形成水肿的病理状况。相应地,本发明的合成肽酰胺还可以用于治疗或预防低钠血症相关病症的方法中,下文中提供了其实例。可以根据容量状况(如血容量过高、血容量正常或血容量过低)来对低钠血症相关病症分类。
[0085]
κ阿片受体相关低钠血症可以是存在低钠血症(低钠病症)的任何疾病或病症,例如,在人中,当血浆中钠浓度低于135mmol/l时,异常可能单独发生,或者更多见地是作为其他医学病症的并发症或作为使用可引起钠缺乏的药物的结果而发生。
[0086]
除了这些病症,许多其他病症与低钠血症相关,包括但不限于:过度adh分泌的肿瘤原因,包括肺癌、十二指肠癌、胰腺癌、卵巢癌、膀胱癌和输尿管癌、胸腺瘤、间皮瘤、支气管腺瘤、类癌、神经节细胞瘤和尤因肉瘤;感染,例如:肺炎(细菌性或病毒性)、脓肿(肺或脑)、空腔形成(曲霉病)、结核病(肺或脑)、脑膜炎(细菌性或病毒性)、脑炎和aids;血管性原因,例如:脑血管闭塞或出血和海绵窦血栓形成;神经原因,例如:格-巴综合征、多发性硬化、震颤性谵妄、肌萎缩性侧索硬化、脑积水、精神病、周围神经病变、头部创伤(闭合性和穿透性)、cns肿瘤或感染和影响下丘脑渗透感受器的cns损伤;先天性畸形,包括:胼胝体发育不全、唇裂/腭裂和其他中线缺陷;代谢原因,例如:急性间歇性卟啉症、哮喘、气胸和正压呼吸;药物,例如:噻嗪类利尿剂、对乙酰氨基酚、巴比妥类药物、胆碱能药物、雌激素、口服降糖药、血管加压素或去氨加压素、高剂量催产素、氯磺丙脲、长春新碱、卡马西平、烟碱、吩噻嗪、环磷酰胺、三环类抗抑郁药、单胺氧化酶抑制剂和血清素再摄取抑制剂;例如在住院、手术期间,或在运动事件(即,运动相关的低钠血症)期间或之后施用过量的低渗流体,以及在老年个体中使用低钠营养补充剂。
[0087]
其他与低钠血症相关的病症包括肾衰、肾病综合征(膜性肾病和微小病变疾病)、恶病质、营养不良、横纹肌溶解、外科手术、选择性心导管插入、失血、以及血钙过多、低钾血症,和结果是可导致渗透性利尿的糖尿的高血糖症。
[0088]
本发明还提供了一种生物活性组合物,其包含包埋在寡糖中的生物活性肽,形成包含稳定的生物活性肽的颗粒。在一个实施例中,包含包埋在寡糖中的生物活性肽(形成包含稳定的生物活性肽的颗粒)的生物活性组合物还包含以下中的一种或多种:羧酸的盐、吸收增强剂、粘合剂、螯合剂和药学上可接受的载体或赋形剂。羧酸的盐可以是羧酸的任何合适的盐,例如但不限于柠檬酸钠。吸收增强剂可以是任何合适的吸收增强剂,例如癸酸钠或月桂酰l-肉碱。粘合剂可以是提高粘结性的任何合适的粘合剂,例如纤维素、甲基纤维素或乙基纤维素、淀粉、明胶、pvp、peg、聚乙烯醇和聚甲基丙烯酸酯。螯合剂可以是任何合适的螯合剂,例如但不限于琥珀酸或edta。常用的药学上可接受的载体或赋形剂包括钙盐,例如氯化钙、磷酸钙和硫酸钙;金属氧化物、糖、糖醇和甜味剂,仅列举本领域中众所周知的那些。
[0089]
生物活性肽可以是任何合适的生物活性肽,例如但不限于κ阿片受体激动剂肽。在
一个实施例中,κ阿片受体激动剂肽可以是d-氨基酸四肽酰胺,如美国专利号7,402,564、7,713,937和7,842,662中所述。
[0090]
在一个实施例中,d-氨基酸四肽酰胺是κ阿片受体激动剂化合物:d-phe-d-phe-d-leu-d-lys-[ω(4-氨基哌啶-4-甲酸)]-oh,在文献中也称为cr845(地克法林)。
[0091]
对生物活性肽进行包衣或其中包埋生物活性肽的寡糖可以是任何合适的寡糖,例如寡糖,例如二糖。在一个实施例中,二糖可包括葡萄糖单体,例如右旋糖。在另一个实施例中,二糖可以是葡萄糖二聚体,例如海藻糖。
[0092]
在一个实施例中,生物活性肽是四肽酰胺κ阿片受体激动剂,其包埋在包含海藻糖的组合物中以形成包含稳定的生物活性肽的颗粒,其中颗粒的平均直径是约2微米至约1000微米。在另一个实施例中,颗粒的平均直径是约5微米至约750微米。
[0093]
在另一个实施例中,本发明提供了一种生物活性组合物,该生物活性组合物包含生物活性肽,例如κ阿片受体激动剂cr845,其包埋在寡糖中形成包含稳定的生物活性肽的颗粒,其中寡糖包括二糖,例如海藻糖(1,1-α-糖苷连接的葡萄糖二聚体)。此类海藻糖/cr845颗粒可用作药用干粉,掺入药用干粉的共混物中或与许多其他众所周知的吸收增强剂中的固体吸收增强剂(如月桂酰l-肉碱和/或柠檬酸)压制成片剂,而没有使用中链脂肪酸、中链脂肪酸的盐或中链脂肪酸甘油酯。
[0094]
本发明进一步提供了一种生物活性组合物,其包含包埋在寡糖颗粒中以形成稳定的生物活性肽颗粒的生物活性肽,其中该寡糖在25℃下至少一年内增强生物活性肽的稳定性。在一个实施例中,生物活性肽是包含一种或多种d-氨基酸的κ阿片受体激动剂,并且寡聚二糖包含葡萄糖。包含一种或多种d-氨基酸的κ阿片受体激动剂可以是任何合适的κ阿片受体激动剂,例如四肽酰胺κ阿片受体激动剂,例如cr845,并且寡糖可以是包含葡萄糖的二糖,例如但不限于1-1,α-连接的吡喃葡萄糖苷二聚体、海藻糖。
[0095]
包含包埋在寡糖颗粒中的生物活性肽的本发明的生物活性组合物可以包含在药学上可接受的片剂、囊片、胶囊、粉末或液体悬浮剂中,作为药物施用。药学上可接受的片剂、囊片、胶囊、粉末、浆液或液体悬浮剂可以进一步包含羧酸的盐、吸收增强剂、粘合剂和药学上可接受的载体或赋形剂中的一种或多种。在一个实施例中,药学上可接受的片剂、囊片、胶囊、粉末、浆液或液体悬浮剂可包含柠檬酸钠作为羧酸。在另一个实施例中,药学上可接受的片剂、囊片、胶囊、粉末、浆液或液体悬浮剂可包含月桂酰l-肉碱作为吸收增强剂。
[0096]
在另一个实施例中,药学上可接受的片剂、囊片、胶囊、粉末、浆液或液体悬浮剂可包括cr845作为κ阿片受体激动剂生物活性肽,其包埋在直径约5至约10微米或约5至约50微米的呈稳定化颗粒形式的寡糖中。在一些实施例中,寡糖是含葡萄糖的寡糖,例如海藻糖。
[0097]
可以通过本发明所披露的方法施用本发明的配制品(其包括κ阿片受体激动剂肽酰胺和吸收增强剂),以治疗或预防任何痛觉过敏病症,例如但不限于:与过敏性皮炎、接触性皮炎、皮肤溃疡、炎症、皮疹、真菌刺激相关的痛觉过敏病症,和与感染原、烧伤、擦伤、挫创、挫伤、冻疮、皮疹、痤疮、毒虫螫伤/叮、皮肤溃疡、粘膜炎、龈炎、支气管炎、喉炎、咽喉痛、带状疱疹、真菌刺激、热病性疱疹、疖、足底疣、外科处理或阴道病损相关的痛觉过敏病症。
[0098]
此外,可以以本文所披露的方法来施用本发明的配制品(其包含κ阿片受体激动剂肽酰胺和吸收增强剂),以治疗或预防任何与烧伤、擦伤、挫创、擦伤(例如角膜上皮擦伤)、挫伤、冻疮、皮疹、痤疮、毒虫螫伤/叮、皮肤溃疡(例如,糖尿病性溃疡或褥疮溃疡)、粘膜炎、
炎症、龈炎、支气管炎、喉炎、咽喉痛、带状疱疹、真菌刺激(例如脚气或股癣)、热病性疱疹、疖、足底疣或阴道病损(例如与霉菌病或性传播疾病相关的阴道病损)相关的痛觉过敏病症。
[0099]
还可以通过施用本发明的配制品(其包含κ阿片受体激动剂肽酰胺和吸收增强剂)来解决与手术后恢复相关的痛觉过敏病症。与手术后恢复相关的痛觉过敏病症可以是任何与手术后恢复相关的痛觉过敏病症,例如,放射状角膜切开术、拔牙、乳房肿瘤切除术、外阴切开术、腹腔镜检查和关节镜检查。还可以通过施用本发明的配制品(其包含κ阿片受体激动剂肽酰胺和吸收增强剂)来解决与炎症相关的痛觉过敏病症。
[0100]
实施例
[0101]
实施例1:犬科的给药配制品的口服施用
[0102]
测试配制品在胶囊中以单剂量口服递送。施用前立即用反渗透纯化水润滑胶囊。给药后沿颈部轻轻抚摸动物以刺激吞咽反射。给药后立即向动物施用5-10ml的纯化水。水冲洗后检查口腔,以确保已吞服胶囊。
[0103]
如本文所示使用的cr845的生物利用度计算如下:
[0104]
%f=(auc口服/口服剂量)x 100
[0105]
(auc iv/剂量iv)
[0106]
实施例2:海藻糖包埋的cr845盐原型配制品的生物活性
[0107]
将cr845乙酸盐/海藻糖/柠檬酸(9.8/88.2/2.2%w/w)和cr845.hcl/海藻糖(23/77%w/w)的喷雾干燥颗粒填充入固有肠溶(耐酸)hpmc胶囊(平均粒径约5μm;粒度分布d(v0.1)=1.5μm,d(v0.9)=12.1μm)中并施用给八只犬科群组。将柠檬酸加入到乙酸盐中以平衡ph。如上所述测定每种配制品的平均生物利用度(%f)和平均值的标准误差(sem)并示于下表1中:
[0108]
表1
[0109]
配制品%fsemcr845乙酸盐/海藻糖/柠檬酸43.23cr845.hcl/海藻糖106.75
[0110]
在下文中,在所述配制品中使用的所有cr845是指盐酸盐cr845.hcl。
[0111]
实施例3:通过喷雾干燥将cr845包埋在海藻糖颗粒中
[0112]
通过制备含有适量组分的水溶液以提供下表2中所示的百分比来产生cr845/海藻糖复合颗粒。将含有5%固体的溶液以35kg/hr的干燥气体容量以8克/分钟泵入实验室规模的喷雾干燥器中。将溶液在10psig下雾化成入口温度为123℃至131℃的干燥气体。使用旋风分离器从干燥气流中分离颗粒。
[0113]
表2
[0114]
[0115]
复合cr845/海藻糖颗粒的每个配制品批次具有一致的粒度分布,hplc纯度和通过卡尔费休(karl fisher)分析的水含量,如下表3所示。
[0116]
表3
[0117][0118]
将配制品填充到3号肠溶胶囊(每个配制品22粒胶囊)中,目标填充重量为每剂5mg cr845。使用羟丙基甲基纤维素乙酸酯琥珀酸酯的乙醇溶液,穿过主体和头部接合处将胶囊密封。
[0119]
表4
[0120][0121]
实施例4:将cr845/hpmc喷雾包衣到微晶纤维素颗粒上
[0122]
为了制备口服固体剂量配制品,向均匀的球形微晶纤维素核(500,500-710μm)喷雾包衣一层api(cr845)和羟丙基甲基纤维素(hpmc)的混合物,随后添加肠溶包衣层用于调节释放。
[0123]
例如,使用具有6”wurster插入物的glatt gpcg-1.1流化床制备批次2。将40立方英尺/分钟的工艺气流在入口处设定为50℃。向系统中装入756克cellet 500颗粒。药物包衣溶液在800克纯化水中含有4克cr845和40克hpmc。使用具有1.5mm孔的喷嘴将药物包衣溶液作为雾化液滴喷雾到流化的cellet颗粒上。在将全部量的药物包衣溶液进行喷雾后,将入口气体温度设定为25℃,并且一旦冷却就收集包衣颗粒。
[0124]
配制品提供增加的载药量和改善的活性药物成分(api)回收率。参见下表5。
[0125]
表5
[0126][0127]
*rsd:回收率的相对标准偏差
[0128]
产率(%)基于在完成包衣过程后回收的cr845包衣的颗粒计算。调和(%)包括在
清洁设备后回收的容器壁等上的材料损失。
[0129]
实例5:cr845/海藻糖在微晶纤维素或三氯蔗糖小丸上的肠溶包衣
[0130]
向第一混合容器中加入1923克l30 d55聚合物分散液。使用均化混合器搅拌悬浮液。
[0131]
向也设置有均化混合器的第二混合容器中加入2146.3克纯化水。在混合的同时缓慢加入57.7克柠檬酸三乙酯和288.5克滑石。通过持续混合最少10分钟制备均匀分散液。
[0132]
通过将来自第二混合容器的柠檬酸三乙酯/滑石分散液缓慢加入到第一混合容器中的eudragit悬浮液中来合并混合容器的内容物,同时持续混合。然后用100克纯化水冲洗第二容器和混合器,并将冲洗的材料加入到第一容器中的混合物中。分散液的混合持续不少于60分钟,然后使分散液通过美国标准#35网筛(0.5mm筛)进入第三容器。然后使100克纯化水通过网筛进入第三容器,并使用推进式混合器以低速混合eudragit/柠檬酸三乙酯/滑石分散液。
[0133][0134]
然后将cr845载药小丸装载到具有6”wurster插入物的流化床干燥器gpcg-1.1(参见表6)。在35℃至40℃下,使气体以35-65m3/h的速率通过载药小丸。将雾化的eudragit/柠
檬酸三乙酯/滑石分散液以8至15g/min的喷雾速率施加到小丸上。
[0135]
实施例6:肠溶包衣小丸的溶解
[0136]
用cr845包衣或用癸酸钠包衣的小丸是肠溶包衣的,并监测ph 6.8下随时间的溶解百分比,如图1所示。50%或100%的肠溶增重是由于肠溶包衣导致的颗粒重量的增加。这两种肠溶包衣用于评估靶向肠道吸收部位的溶解曲线。
[0137]
实例7:向犬科施用
[0138]
将包埋在海藻糖中并包衣在来自实例3的复合颗粒a-e上的cr845在标准测试环境中施用于犬科,并如上所述测定cr845的生物利用度。将配制品a-e各自施用给八只动物后的结果分别示于图2-6的dmpk图中。
[0139]
将本说明书所提及的每项美国专利和公布的专利申请的说明书以及本说明书中所引用的参考文献的文本通过引用全部并入本文。对于这些引用内容的一个或多个中所见的任何定义或描述与本文中相应的定义或描述矛盾的情况,则以本文中披露的定义或描述为准。
[0140]
本文所提供的实例仅用于阐释目的而不是用来限制本发明的范围,本发明的全部范围将容易被本领域的技术人员所认识。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。