1.本发明涉及中药提取、分离领域,尤其涉及从马齿苋药材中提取、分离和鉴别出的新化合物及其提取分离方法。
背景技术:
2.马齿苋(portulaca oleracea l.),又名长命菜、马苋菜,为马齿苋科植物。马齿苋耐旱耐涝,且耐光耐阴,分布广泛、资源丰富,作为药食两用的野生植物备受关注。2020版《中华人民共和国药典》中收载马齿苋的干燥地上部分入药,具有清热解毒、凉血止血、止痢等功效,用于热毒血痢、痈肿疔疮、湿疹、丹毒、蛇虫咬伤、便血、痔血、崩漏下血等。
3.马齿苋现代药理学研究表明,其具有抗炎止痛、抗菌、抗病毒、降血压、降血脂、抗氧化、抗癌、松弛骨骼肌和平滑肌、调节免疫功能等作用。研究表明马齿苋众多化学成分为其多样的药理作用提供了物质基础,马齿苋主要化学成分包括黄酮类、香豆素类、萜类、甾类、有机酸类、挥发油、生物碱类、氨基酸类、各种色素类和矿物质类等。其中生物碱是马齿苋中一类主要的化学成分,目前已报道的生物碱类成分有去甲肾上腺素、多巴胺、少量多巴、腺苷、尿嘧啶、腺嘌呤、n,n-二环己基脲、尿囊素、n-反式-阿魏酰基酪胺;还有环二肽生物碱和酰胺类生物碱:马齿苋酰胺a-s。
4.目前从马齿苋中分离出的化学成分大多数是已知的,且结构新颖性较低,因此,对马齿苋中新化合物的开发和分离是亟待需要的。
技术实现要素:
5.针对上述问题,本发明提供一种新型异喹啉类生物碱及其提取分离方法,具体为从马齿苋中提取一种新型异喹啉类生物碱,经研究发现本发明的新化合物具有抗炎、抗癌的作用,同时提供一种针对本发明新化合物的简便、快速、环保、纯度高的提取分离方法。为实现本发明的上述目的,本发明提供新化合物,分子式为c
16h16
n2o3,命名为oleraisoquinoline,化学结构式为:。
6.为实现本发明的上述目的,本发明还提供一种马齿苋中新化合物的提取分离方法,具体步骤为:
步骤1:取马齿苋干燥药材,采用乙醇回流提取两次,醇提液过滤,合并滤液直接加热浓缩,放凉至室温,得药液备用;步骤2:将步骤1中的药液蒸干后上硅胶柱,用乙酸乙酯洗脱,减压回收乙酸乙酯至浸膏,得到乙酸乙酯提取物;步骤3:将步骤2中所得物再经si正相硅胶中压柱进行层析分离,用乙酸乙酯、乙酸乙酯:甲醇、甲醇进行洗脱,得到若干洗脱部位,经薄层色谱进行检测、显色,将各显色的洗脱部位分别减压浓缩至干,得到浓缩物备用;步骤4:将步骤3中所得物再经预处理的si正相硅胶中压柱进行层析分离,用环己烷:乙酸乙酯,乙酸乙酯,乙酸乙酯:甲醇梯度洗脱,得到若干洗脱部位,经薄层色谱进行检测及显色,将各显色的洗脱部位分别减压浓缩至干,得到浓缩物备用;步骤5:将步骤4中所得物再经预处理的葡聚糖凝胶柱层析分离,用甲醇洗脱,得到若干洗脱部位,经薄层色谱进行检测,显色,合并显色的洗脱部位,将合并后的洗脱部位经减压浓缩至干,备用;步骤6:将步骤5中所得物再经预处理的si正相硅胶中压柱进行层析分离,用环己烷:乙酸乙酯,乙酸乙酯,乙酸乙酯:甲醇梯度洗脱,得到若干洗脱部位,经薄层色谱进行检测及显色,将各显色的洗脱部位分别减压浓缩至干,得到浓缩物备用;步骤7:将步骤6中的浓缩物通过hplc分离制备,以甲醇∶0.1%甲酸水为流动相进行等度洗脱,最终得到本发明所述的新化合物。
7.进一步地,所述步骤1中50%乙醇回流提取两次,每次2小时,50%乙醇用量为药材的10倍。
8.进一步地,所述步骤2中所用流动相洗脱程序为等度洗脱。
9.进一步地,步骤3中的si正相硅胶层析分离用乙酸乙酯、乙酸乙酯:甲醇(5:1、1:1)、甲醇进行梯度洗脱。加压,使流速为1ml/min,温度为室温,其中填料粒度为40μm。
10.进一步地,步骤4中的si正相硅胶层析分离用环己烷:乙酸乙酯(5:1、1:1)、乙酸乙酯、乙酸乙酯:甲醇(5:1)、甲醇进行梯度洗脱。加压,使流速为1ml/min,温度为室温,其中填料粒度为40μm。
11.进一步地,所述步骤5中的sephadex lh-20凝胶的预处理过程为甲醇浸泡过24小时,上柱,以初始流动相平衡,所用流动相洗脱程序为等度洗脱。
12.进一步地,所用步骤6中的si正相硅胶层析分离用环己烷:乙酸乙酯(5:1、1:1)、乙酸乙酯、乙酸乙酯:甲醇(5:1、1:1)、甲醇进行梯度洗脱。加压,使流速为1ml/min,温度为室温,其中填料粒度为40μm。
13.进一步地,所述步骤7中所用甲醇∶0.1%甲酸等度洗脱中甲醇和水的体积比为70∶30。
14.与现有技术相比本发明的有益效果。
15.本发明中所述马齿苋新化合物的分离和药理活性研究未被现有论文期刊所报道。本发明提供来源于马齿苋的新化合物及一种针对本发明新化合物的提取分离方法,依次采用乙醇回流提取、硅胶柱层析、si正相硅胶柱层析、sephadex lh-20及hplc进行分离纯化与制备,成功提取分离出oleraisoquinoline。该方法操作步骤仅为七步,操作方法简便及快速,提取分离过程主要采用乙醇回流提取及乙酸乙酯洗脱,工艺方法环保,且经该方法分离
得到的化合物纯度较高且大于90%。此外经研究表明该新化合物具有抗炎作用,因此本发明新化合物及其盐和衍生物可以作为其他化合物合成先导物,以及新药开发和药理活性研究的原料,亦可用于制备抗炎药物。
附图说明
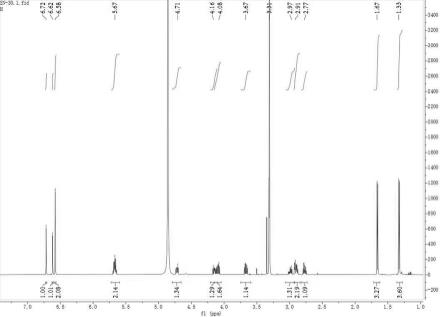
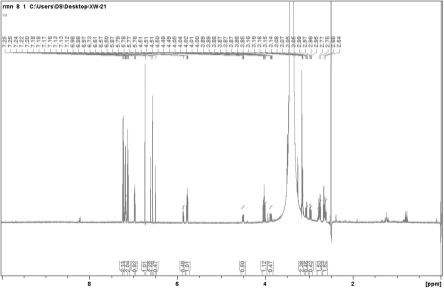
16.图1为本发明新化合物oleraisoquinoline的1h-nmr光谱图。
17.图2为本发明新化合物oleraisoquinoline的1h-nmr光谱图局部放大图。
18.图3为本发明新化合物oleraisoquinoline的1h-nmr光谱图局部放大图。
19.图4为本发明新化合物oleraisoquinoline的
13
c-nmr光谱图。
20.图5为本发明新化合物oleraisoquinoline的dept 135光谱图。
21.图6为本发明新化合物oleraisoquinoline的1h-1
h cosy光谱图。
22.图7为本发明新化合物oleraisoquinoline的hsqc光谱图。
23.图8为本发明新化合物oleraisoquinoline的hmbc光谱图。
24.图9为本发明新化合物oleraisoquinoline的roesy光谱图。
25.图10为本发明新化合物oleraisoquinoline的高分辨质谱图。
具体实施方式
26.下面结合具体实施例对本发明做详细的说明。
27.实施例1。
28.本发明提供一种新化合物,分子式分别为c
16h16
n2o3,命名为oleraisoquinoline,化学结构式分别为:。
29.所述新化合物根据结构分别命名为1-benzyl-2-nitroso-1,2,3,4-tetrahydroisoquinoline-6,7-diol,表1为该新化合物的核磁数据:1h-nmr与
13
c-nmr在dmso-d
6.
中。
30.表1:本发明新化合物oleraisoquinoline的核磁数据
。
31.本发明一种新化合物oleraisoquinoline的结构鉴定及推导。
32.oleraisoquinoline:黄色油状物,在薄层板板上用碘化铋钾试剂喷洒时呈现橙色。该化合物1以纯形式分离,由于围绕亚硝胺的n-n部分双键的缓慢旋转,在nmr中显示为2:1的异构体混合物。分子式为c
16h16
n2o3,从m/z283.1084 [m-h]-处的uhplc-esi-qtof/ms去质子化分子离子推导出来(c
16h15
n2o
3-的计算值,283.1088),对应于具有10个不饱和度的化合物。在e异构体中,可以指出存在δ
h 6.57至7.24和δ
c 114.0至129.5的九种芳族次甲基,以及δ
h 5.78和δ
c 62.6处的一种次甲基、三个亚甲基和五个非质子化碳。1h、
13
c、dept和hsqc光谱。基于h-3之间的cosy相关性,将δ 7.13 (h-3'/7')、7.24 (h-4'/6')和7.19 (h-5') 处的五个芳族质子分配给单取代苯环'/7'和h4'/6'以及h-3'/7'与c-3'/7'和c-5'以及h4'/6'与c-1'和c4的hmbc相关性'/6'。基于 h3'/7'与c-1'和h-1'与c-2'和c-3'/7'的相关性揭示了位置1'的芳基亚甲基。基于h-1'和h-1之间的耦合,c-1'与c-1相关联。
[0033]
由于h-1与c-4a、c-8和c-8a的相关性以及h-8与c-1的相关性,位置1位于第二个芳环旁边。h-5和c-4a之间的相关性表明h-5相对于c-4a是间位的,即对位8。碳6和7在δ 144.7和144.0处的化学位移,基于相关性确定h-8/c-6和h-5/c-7,得出这些碳都带有羟基的结论。最后,亚甲基质子h-3和h-4之间的cozy相关性,以及h-5/c-4和h-1/c-3相关性使得定位c-3-c-4乙烯成为可能亚基并证明c-1和c-3碳通过杂原子连接。根据化合物1的原始分子式和c-1和c-3碳分别在δ 62.6和38.2处的化学位移,可以说化合物1为1-benzyl-2-nitroso-1,2,3,4-tetrahydroisoquinoline-6,7-diol,命名为oleraisoquinoline。
[0034]
混合物中的次要化合物与这个非常相似。化学位移很接近,并且相关性,特别是在hmbc中,几乎相同。总体而言,相同的分析使我们能够确定该化合物中质子和碳的化学位移,并得出结论,它是前者的异构体。在亚硝胺中,n-n部分双键已被证明旋转非常缓慢,并且非对称亚硝胺在nmr中通常以旋转异构体的混合物形式出现。空间位阻原则上应该有利于e异构体而不是z。文献中已经确定,当顺式(e异构体)比反式(z异构体)向亚硝基时,亚硝胺α-亚甲基质子信号向高场移动。相反,当顺式到亚硝基氧(z异构体)时,次甲基质子应该在较低的场共振。这些数据与nmr中的主要旋转异构体e-亚硝胺一致。
[0035]
本发明还提供上述新化合物的提取分离方法,具体步骤为。
[0036]
步骤1:称取马齿苋干燥药材250kg,采用50%乙醇回流提取,水用量为药材的10倍,乙醇回流提取两次,每次2h,直接加热浓缩,放凉至室温,得药液备用。
[0037]
步骤2:将步骤1中所得药液部分蒸干后经硅胶柱层析分离,用乙酸乙酯等度洗脱,其中硅胶为100-200目,40℃以下减压回收乙酸乙酯至浸膏,得到乙酸乙酯提取物。
[0038]
步骤3:将步骤2中乙酸乙酯提取物经si正相硅胶中压柱分离,用乙酸乙酯、乙酸乙酯∶甲醇、甲醇进行洗脱,加压,使流速为1ml/min,温度为室温,其中si正相硅胶粒度为40μm。得到10个部位(即梯度洗脱得10个瓶,每瓶500ml),经薄层色谱进行检测、显色,留下显色的第1部位,50℃以下减压浓缩至干,备用。
[0039]
步骤4:将步骤3中所得的第1部位再经预处理的si正相硅胶中压柱层析分离,用环己烷∶乙酸乙酯(5∶1、1∶1)、乙酸乙酯、乙酸乙酯∶甲醇(5∶1)、甲醇进行梯度洗脱。加压,使流速为1ml/min,温度为室温,其中填料粒度为40μm,得到11个部位(即梯度洗脱得11个瓶,每瓶200ml),经薄层色谱进行检测、显色,留下显色的第3部位,50℃以下减压浓缩至干,备用。
[0040]
步骤5:将步骤4中所得的第3部位再经预处理的葡聚糖凝胶柱层析分离,用甲醇洗脱,得到12个洗脱部位(即共得到12个瓶,每瓶120ml),经薄层色谱进行检测,显色,将显色的第7部位在50℃以下减压浓缩至干,备用。
[0041]
步骤6:将步骤5中所得的第7部位再经预处理的si正相硅胶中压柱层析分离,用环己烷∶乙酸乙酯(5∶1、1∶1)、乙酸乙酯、乙酸乙酯∶甲醇(5∶1、1∶1)、甲醇进行梯度洗脱。加压,使流速为1ml/min,温度为室温,其中填料粒度为40μm,得到11个部位(即梯度洗脱得6个瓶,每瓶50ml),经薄层色谱进行检测、显色,留下显色的第1部位,50℃以下减压浓缩至干,备用。
[0042]
步骤7:将步骤6中所得的显色部位经hplc分离制备,以甲醇∶0.1%甲酸水(70∶30,v/v)作为流动相,检测波长为210nm和254nm,分离制备得到本发明新化合物,归一法测定纯度为98%。
[0043]
所述葡聚糖凝胶的预处理过程为甲醇浸泡过24h,上柱,以初始流动相平衡。
[0044]
实施例2 本发明新化合物的抗炎作用。
[0045]
1 主要材料。
[0046]
1.1 药品和试剂:实验所用新化合物由上述方法制备,纯度为98%,精密称取,用dmso稀释至下述各剂量组所需溶液。dmem高糖培养基、胎牛血清(美国hyclone公司);青霉素、链霉素(杭州四季青公司);lps(美国sigma公司);il-1β和tnf-α的elisa试剂盒(美国cayman公司);细胞裂解液(碧云天生物技术有限公司)。
[0047]
1.2 细胞株:raw264.7巨噬细胞(美国atcc细胞库)。
[0048]
1.3 分组:分为对照组、lps组和实验组,各一组。
[0049]
2 实验方法。
[0050]
2.1 细胞培养:dmem高糖培养基,加入l0%的胎牛血清,l%抗菌素(100u/ml青霉素和100μg/ml链霉素),置于37℃,5%co2培养箱中培养。
[0051]
2.2 mtt比色法测定细胞活力:raw 264.7细胞系在含有10%热灭活胎牛血清(fbs)和抗生素(100u/ml青霉素和100μg/ml链霉素)的dmem中在37℃和5%co2的湿化培养箱中培养。通过3-(4,5-dimethylthiazol-2-yl)-2,5-diphenyltetrazolium bromide(mtt)测定法评估细胞活力。然后将raw264.7细胞以1
×
104个细胞/孔的密度接种在96孔板中,随后在有或没有各种浓度(5、10、25、50和100μm)的新化合物的情况下在培养箱中预孵育1小时,然后加入1μg/ml lps孵育24小时。处理后除去培养基并与5mg/ml mtt溶液在37℃下孵育4小时。弃去上清液,将甲臜溶解在150μl dmso中。使用bio-tek酶标仪在570nm处检测吸光度值,而未处理组的吸光度为100%。
[0052]
2.3 elisa法测定炎症因子il-1β和tnf-α:将对数生长期raw264.7巨噬细胞接种于96孔培养板中,细胞密度为1
×
105个/ml,每孔1ml,温度37℃,5%co2条件下培养过夜,实验组加入本发明的新化合物oleraisoquinoline(0.1μm~10μm),培育1h后,在每孔加入lps(终浓度为1μg/ml),共孵育24h,每组处理重复3孔。elisa法测定该马齿苋来源新化合物处理后的raw264.7巨噬细胞分泌的il-1β和tnf-α的含量。
[0053]
3 实验结果。
[0054]
实验结果表明本发明的新化合物小剂量时对lps诱导的巨噬细胞raw264.7的增殖无影响,安全无毒;并可有效抑制lps诱导的巨噬细胞raw264.7所产生过量炎症细胞因子il-1β和tnf-α,且呈浓度依赖。
[0055]
细胞相对存活率实验结果如表2所示。
[0056]
表2:本发明对raw264.7巨噬细胞相对存活率的影响。
[0057]
elisa法测定炎症因子il-1β和tnf-α结果如表3所示。
[0058]
表3:本发明对lps诱导的raw264.7细胞分泌的il-1β和tnf-α含量的影响
。
[0059]
综上所述,本发明提供马齿苋中oleraisoquinoline及其提取分离方法,依次采用乙醇回流提取、硅胶柱层析、si正相硅胶中压柱层析、sephadex lh-20及hplc进行分离纯化与制备,成功的分离得到该新化合物。该方法简便、快速、环保,且经该方法分离得到的化合物纯度较高。由于所得化合物化学结构独特,从常用中药马齿苋中提取出来,其具有抗炎作用,因此本发明的新化合物oleraisoquinoline可以作为天然产物开发中药新药,具有广阔的前景。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。