抗sars-cov-2的s抗原的igm抗体及covid-19重症化风险的辅助判定
【技术领域】
1.本发明涉及covid-19(coronavirus disease 2019)的重症化风险相关信息的取得方法。本发明涉及抗sars-cov-2(重症acute respiratory syndrome coronavirus 2)的s抗原的igm抗体的测定值的监测方法。本发明涉及辅助covid-19的重症化风险的判定的方法。本发明涉及在这些方法中使用的试剂盒。本发明涉及covid-19的重症化风险相关信息的取得装置。本发明涉及用于取得covid-19的重症化风险相关信息的计算机程序。
背景技术:
2.covid-19患者在多数情况是轻症而无住院的必要,但一部分的患者重症化,有受住院治疗的必要。在covid-19最重症化时,有对于所述患者优先进行人工呼吸管理等的高度的治疗的必要。因此,预测covid-19的重症化的手段的需求高。在非专利文献1中记载了,将covid-19患者分类为轻症、中等症及重症,在对各患者的血清中的各种细胞因子进行测定时,重症患者组的il-6(白细胞介素-6)及il-10(白细胞介素-10)的测定值与轻症及中等症的患者组相比显著地高。结果,在非专利文献1中记载了il-6及il-10可成为covid-19的重症化的预测标志物。
3.【现有技术文献】
4.【非专利文献】
5.【非专利文献1】han h.等,profiling serum cytokines in covid-19patients reveals il-6and il-10are disease severity predictors,emerg microbes infect.,2020,vol.9,pp.1123-1130
6.【发明的概要】
7.【发明要解决的课题】
8.在非专利文献1中,作为与covid-19的重症化关联的生物标志物,关注于由sars-cov-2感染在患者发生的炎症性细胞因子。一方面知晓,也含sars-cov-2,一般在感染病毒时,在患者的体内发生抗所述病毒的蛋白质(抗原)的抗体。作为生物标志物,本发明人关注于由sars-cov-2感染在患者发生的抗sars-cov-2抗原的抗体。本发明旨在提供用于以受试体中的抗sars-cov-2抗原的抗体的测定值作为指标,取得covid-19的重症化风险相关信息的新的手段。即,本发明的课题提供covid-19的重症化风险相关信息的取得方法、抗sars-cov-2的s抗原的igm抗体的监测方法、辅助covid-19的重症化风险的判定的方法、试剂盒、covid-19的重症化风险相关信息的取得装置及用于取得covid-19的重症化风险相关信息的计算机程序。
9.【用于解决课题的手段】
10.本发明提供covid-19的重症化风险相关信息的取得方法,包括对从感染sars-cov-2的受试者或疑似罹患covid-19的受试者采集的受试体中所含的抗sars-cov-2的s抗原的igm抗体进行测定,由该igm抗体的测定得到的值成为受试者的covid-19的重症化风险
的指标。
11.本发明提供抗sars-cov-2的s抗原的igm抗体的监测方法,包括使用从感染sars-cov-2的受试者或疑似罹患covid-19的受试者在多个时间点采集的受试体,对各受试体中所含的抗sars-cov-2的s抗原的igm抗体进行测定,由该igm抗体的测定得到的值成为受试者的covid-19的重症化风险的指标。
12.本发明提供辅助covid-19的重症化风险的判定的方法,包括对从感染sars-cov-2的受试者或疑似罹患covid-19的受试者采集的受试体中所含的抗sars-cov-2的s抗原的igm抗体进行测定的工序,基于由该igm抗体的测定得到的值而判定受试者的covid-19的重症化风险的工序。
13.本发明提供在上述的方法中使用的试剂盒,其含有含能与抗sars-cov-2的s抗原的igm抗体特异性地结合的物质的试剂。
14.本发明提供covid-19的重症化风险相关信息的取得装置,具备含处理器及处于处理器控制下的存储器的计算机,在存储器中记录用于使计算机执行取得由从感染sars-cov-2的受试者或疑似罹患covid-19的受试者采集的受试体中所含的抗sars-cov-2的s抗原的igm抗体的测定得到的值的步骤和输出此值的步骤的计算机程序,上述的值成为受试者的covid-19的重症化风险的指标。
15.本发明提供用于取得covid-19的重症化风险相关信息的计算机程序,其为记录在计算机能读取的介质的计算机程序,计算机程序用于使计算机执行取得由从感染sars-cov-2的受试者或疑似罹患covid-19的受试者采集的受试体中所含的抗sars-cov-2的s抗原的igm抗体的测定得到的值的步骤和输出此值的步骤,上述的测定值成为受试者的covid-19的重症化风险的指标。
16.【发明的效果】
17.根据本发明,可判定受试者的covid-19的重症化风险。
18.【附图的简单的说明】
19.【图1a】是显示本实施方式的试剂盒的一例的概略图。
20.【图1b】是显示本实施方式的试剂盒的一例的概略图。
21.【图1c】是显示本实施方式的试剂盒的一例的概略图。
22.【图2】是显示本实施方式的取得装置的一例的概略图。
23.【图3】是显示本实施方式的取得装置的硬件构成的框图。
24.【图4a】是显示利用本实施方式的取得装置的处理程序的流程图。
25.【图4b】是显示利用本实施方式的取得装置的处理程序的流程图。
26.【图4c】是显示利用本实施方式的取得装置的处理程序的流程图。
【具体实施方式】
27.在本实施方式的covid-19的重症化风险相关信息的取得方法(以下,也称为“取得方法”)中,对从感染sars-cov-2的受试者或疑似罹患covid-19的受试者采集的受试体中所含的抗sars-cov-2的s抗原的igm抗体(以下,也称为“s-igm”)进行测定。在本实施方式中,sars-cov-2不仅是最初知晓基因组序列的病毒(重症acute respiratory syndrome coronavirus 2isolate wuhan-hu-1,genbank的登录编号:mn908947.3),还包含其亚种。
28.作为本实施方式中的受试者,可举出感染sars-cov-2的受试者及疑似罹患covid-19的受试者。感染sars-cov-2的受试者是指通过用pcr检查、抗原检查等的公知的检查检测sars-cov-2确认感染的者。感染sars-cov-2的受试者含患covid-19的者(covid-19患者)及无症状的者。在受试者是covid-19患者时,其重症度优选为轻症、无呼吸衰竭的中等症、或者有呼吸衰竭的中等症。轻症是指例如氧饱和度(spo2)是96%以上,无呼吸器官症状,仅咳而无气促的状态。无呼吸衰竭的中等症是指例如spo2高于93%并且不足96%,有气促,见到肺炎的状态。呼吸衰竭的有的中等症是指例如spo2是93%以下,需要氧施用的状态。
29.疑似罹患covid-19的受试者含出现在covid-19见到的症状、但未受sars-cov-2的检查的者、sars-cov-2感染者或与covid-19患者接触的者及疑似接触的者。疑似罹患covid-19的受试者还可称为疑似感染sars-cov-2的者。作为covid-19中见到的症状,可举出例如发热、咳、鼻水、咽头痛等的感冒症状及/或呼吸困难,劳作时的气促,味觉及嗅觉的异常等。与感染者或患者的接触是指例如,与感染者或患者在1m以内的距离进行会话,滞留在感染者或患者存在的密闭空间内,被感染者或患者的唾液、咳嗽等的飞沫笼罩等的行为。
30.受试体只要是可从受试者采集并且含s-igm抗体的试样,就不特别限定。作为这样的试样,可举出例如血液试样、淋巴液、脑脊髓液、唾液、鼻咽头拭液、咳痰、支气管肺泡清洗液、尿、大便等。作为血液试样,可举出例如,从受试者采集的血液(全血)、及从该血液调制的血浆或血清。在本实施方式中,优选全血、血浆及血清,特别优选血浆及血清。
31.在受试体中含细胞等的不溶性的混杂物时,也可由例如离心分离、过滤等的公知的手段从受试体除去混杂物。另外,受试体也可根据需要用适合的水性介质稀释。这样的水性介质只要是不妨碍后述的生物标志物的测定,就不特别限定,可举出例如水、生理盐水、缓冲液等。缓冲液只要是在中性附近的ph(例如6以上8以下的ph)具有缓冲作用,就不特别限定。这样的缓冲液可举出例如hepes、mes、pipes等的good缓冲液、磷酸缓冲生理盐水(pbs)、tris盐酸缓冲液、tris缓冲生理盐水(tbs)等。
32.在本实施方式的取得方法中,作为生物标志物,测定s-igm。s-igm是通过感染sars-cov-2而在受试者的体内发生的抗sars-cov-2的刺突蛋白质的igm抗体。sars-cov-2的刺突蛋白质也称为s抗原。sars-cov-2的s抗原本身是公知的,其氨基酸序列可例如从ncbi(national center for biotechnology information)等的公知的数据库取得。
33.在本说明书中,“对抗sars-cov-2的s抗原的igm抗体进行测定”含取得反映s-igm的量或浓度的值及确定s-igm的量或浓度的值。“反映s-igm的量或浓度的值”是依据后述的标记物质的种类的值,可由对应于标记物质的种类的测定装置取得。作为这样的值,可举出例如,发光强度的测定值、荧光强度的测定值、放射线强度的测定值、光学密度的测定值等。“s-igm的量或浓度的值”可基于反映s-igm的量或浓度的值和校准物的测定结果而确定。校准物是指作为对照试样的一种,以已知浓度含受试物质或与其相对应的标准物质的受试物质的定量用试样。在本实施方式中,可例如,以市售的sars-cov-2igm阳性受试体(血浆或血清)作为校准物使用。
34.在本实施方式中,由s-igm的测定得到的值(以下,也称为“s-igm的测定值”)可为反映受试体中的s-igm的量或浓度的值。另外,s-igm的测定值可为基于校准物的测定结果而确定的受试体中的s-igm的量或浓度的值。
35.对s-igm进行测定的手段不特别限定,可从公知的测定方法适宜选择。在本实施方
式中,优选包括使用能与s-igm特异性地结合的物质,捕获s-igm的方法。通过将由这样的物质捕获的s-igm用公知的方法检测,可对受试体中所含的s-igm进行测定。
36.作为能与s-igm特异性地结合的物质,可举出例如sars-cov-2的s抗原(以下,也简称为“s抗原”)、抗体、适体等。在它们之中,也优选s抗原,特别优选s抗原的s1亚基。s抗原可为天然存在的蛋白质,也可为重组型蛋白质。天然的s抗原可例如,从sars-cov-2阳性受试体由常规方法单离。重组型s抗原可由dna重组技术及其他分子生物学技术等的公知的方法得到。首先,通过将编码s抗原的多核苷酸整合到公知的蛋白质表达用载体,得到s抗原表达载体。通过向适当的宿主细胞转化或转染得到的s抗原表达载体,可得到重组型s抗原。编码s抗原的多核苷酸的碱基序列本身是公知的,可从ncbi等的公知的数据库取得。蛋白质表达用载体的种类不特别限定,可为哺乳动物细胞用载体,也可为大肠杆菌用载体。
37.使用s抗原对s-igm进行测定的方法不特别限定,可从酶联免疫吸附法(elisa法)、酶联免疫测定法、免疫透射比浊法、免疫散射比浊法、乳胶凝集法等的公知的免疫学测定法适宜选择。在本实施方式中,优选elisa法。elisa法的种类可为夹心法、竞争结合法、直接法、间接法等之任一者,特别优选夹心法。作为一例,接下来说明由夹心elisa法测定受试体中的s-igm的情况。
38.由使用s抗原的夹心elisa法的s-igm的测定包括s抗原和s-igm的复合体的形成工序和该复合体的检测工序。在复合体的形成工序中,在固相上形成含s-igm、s抗原和用于检测s-igm的抗体(以下,也称为“s-igm检测用抗体”)的复合体。在此夹心elisa法中,s抗原作为用于捕获s-igm的物质发挥功能。在受试体含s-igm时,通过将所述受试体、s抗原和s-igm检测用抗体混合,可形成含s-igm、s抗原和s-igm检测用抗体的复合体。进而,通过使含复合体的溶液和可固定s抗原的固相接触,可在固相上形成上述的复合体。或者,也可使用预先固定了s抗原的固相。即,通过使受试体、固定s抗原的固相和s-igm检测用抗体接触,可在固相上形成上述的复合体。在别的实施方式中,在复合体的形成工序中,在固相上形成含s-igm、用于检测s-igm的s抗原和用于捕获s-igm的抗体(以下,也称为“s-igm捕获用抗体”)的复合体。
39.s-igm检测用抗体及s-igm捕获用抗体只要是可与s-igm或人igm特异性地结合的抗体,就不特别限定。在本说明书中,“抗体”的用语包含全长的抗体及其片段。作为抗体的片段,可举出例如还原型igg(rigg)、fab、fab'、f(ab')2、fv、单链抗体(scfv)、双抗体、三体抗体等。抗体也可为单克隆抗体及多克隆抗体之任一者。可与s-igm特异性地结合的抗体也可由例如,kohler g.及milstein c.,nature,vol.256,pp.495-497,1975中记载的方法制作并取得产生所述抗体的杂交瘤。可与人igm特异性地结合的抗体本身是公知的,市售。
40.固相只要是能固定s抗原或s-igm捕获用抗体的不溶性的载体即可。向固相固定s抗原或s-igm捕获用抗体的实施方式不特别限定。例如,可使s抗原或s-igm捕获用抗体和固相直接键,也可将s抗原或s-igm捕获用抗体和固相经别的物质间接结合。作为直接的结合,可举出例如,物理的吸附、由交联剂的共价键等。作为间接的结合,也可使用例如,介于s抗原或s-igm捕获用抗体和固相之间的物质的组合,将s抗原或s-igm捕获用抗体固定在固相上。作为这样的物质的组合,可举出生物素类和亲和素类、半抗原和抗半抗原抗体等的组合。生物素类含生物素、以及脱硫生物素及氧基生物素等的生物素类似物。亲和素类含亲和素、以及链霉亲和素及tamavidin(注册商标)等的亲和素类似物。作为半抗原和抗半抗原抗
体的组合,可举出具有2,4-二硝基苯基(dnp)基团的化合物和抗dnp抗体的组合。例如,可通过使用预先经生物素类(或具有dnp基团的化合物)修饰的s抗原或s-igm捕获用抗体和预先结合亲和素类(或者抗dnp抗体)的固相,经生物素类和亲和素类的结合(或者dnp基团和抗dnp抗体的结合)而将s抗原或s-igm捕获用抗体固定在固相上。
41.固相的原料不特别限定,可从例如有机高分子化合物、无机化合物、生物体高分子等选择。作为有机高分子化合物,可举出乳胶、聚苯乙烯、聚丙烯等。作为无机化合物,可举出磁性体(氧化铁、氧化铬及铁素体等)、氧化硅、氧化铝、玻璃等。作为生物体高分子,可举出不溶性琼脂糖、不溶性葡聚糖、明胶、纤维素等。也可将这些中的2种以上组合使用。固相的形状不特别限定,可举出例如粒子、膜、微平板、微管、试管等。在它们之中,也优选粒子,特别优选磁性粒子。
42.在本实施方式中,也可在复合体的形成工序和复合体的检测工序之间,进行除去未形成复合体的未反应的游离成分的b/f(bound/free)分离。未反应的游离成分是指不构成复合体的成分。例如,可举出不与s-igm结合的s抗原及检测用抗体等。b/f分离的手段不特别限定,当固相是粒子时,可通过由离心分离仅回收捕获复合体的固相来进行b/f分离。当固相是微平板或微管等的容器时,可通过除去含未反应的游离成分的液来进行b/f分离。另外,在固相是磁性粒子时,可通过在用磁铁磁约束磁性粒子的状态下,由管嘴吸除含未反应的游离成分的液来进行b/f分离,在自动化的观点优选。也可在除去未反应的游离成分之后,将捕获复合体的固相用pbs等的适合的水性介质清洗。
43.在复合体的检测工序中,通过将在固相上形成的复合体用现有技术中公知的方法检测,可取得s-igm的测定值。例如,作为s-igm检测用抗体,在使用被标记物质标记的抗体时,通过检测由该标记物质发生的信号,可取得s-igm的测定值。或者,在使用抗s-igm检测用抗体的标记第二抗体时,也可同样取得s-igm的测定值。
44.在本说明书中,“检测信号”含定性检测信号的有无,对信号强度进行定量,及半定量检测信号的强度。半定量的检测是指将信号的强度如“未发生信号”、“弱”、“中”、“强”等一样阶段性地表示。在本实施方式中,优选定量或半定量检测信号的强度,特别优选定量检测。
45.标记物质不特别限定,例如,可为其本身发生信号的物质(以下,也称为“信号发生物质”),也可为催化其他物质的反应而发生信号的物质。作为信号发生物质,可举出例如荧光物质、放射性同位素等。作为催化其他物质的反应而发生能检测的信号的物质,可举出例如酶。作为酶,可举出碱性磷酸酶(alp)、过氧化物酶、β-半乳糖苷酶、荧光素酶等。作为荧光物质,可举出异硫氰酸荧光素(fitc)、若丹明、alexa fluor(注册商标)等的荧光染料、gfp等的荧光蛋白质等。作为放射性同位素,可举出
125
i、
14
c、
32
p等。作为标记物质,优选酶,特别优选alp。
46.检测信号的方法本身是在现有技术中公知的。在本实施方式中,适宜选择对应于来源于上述的标记物质的信号的种类的测定方法即可。例如,在标记物质是酶时,可通过使用分光光度计等的公知的装置测定通过使对于该酶的底物反应而发生的光、色等的信号进行。
47.酶的底物可对应于该酶的种类而从公知的底物适宜选择。例如,在作为酶,使用碱性磷酸酶时,作为底物,可举出cdp-star(注册商标)(4-氯-3-(甲氧基螺[1,2-二氧杂环丁
烷-3,2'-(5'-氯)三环[3.3.1.13,7]癸烷]-4-基)苯基磷酸2钠)、cspd(注册商标)(3-(4-甲氧基螺[1,2-二氧杂环丁烷-3,2-(5'-氯)三环[3.3.1.13,7]癸烷]-4-基)苯基磷酸2钠)等的化学发光底物、5-溴-4-氯-3-吲哚基磷酸(bcip)、5-溴-6-氯-吲哚基磷酸2钠、p-硝基苯基磷酸等的显色底物。另外,在作为酶,使用过氧化物酶时,作为底物,可举出luminor及其衍生物等的化学发光底物、2,2'-连氮基双(3-乙基苯并噻唑啉-6-磺酸铵)(abts)、1,2-亚苯基二胺(opd)、3,3',5,5'-四甲基联苯胺(tmb)等的显色底物。
[0048]
在标记物质是放射性同位素时,可使用闪烁计数器等的公知的装置测定作为信号的放射线。另外,在标记物质是荧光物质时,可使用荧光酶标仪等的公知的装置测定作为信号的荧光。再者,激发波长及荧光波长可对应于使用的荧光物质的种类而适宜确定。
[0049]
信号的检测结果可作为s-igm的测定结果使用。例如,在定量检测信号的强度时,可以信号强度的测定值本身或从该测定值取得的值作为s-igm的测定值使用。作为从信号强度的测定值取得的值,可举出例如,从该测定值减去阴性对照试样的测定值或背景的值的值等。阴性对照试样可适宜选择,可举出例如,不含s-igm的缓冲液、从未感染sars-cov-2的健康人得到的受试体等。
[0050]
在本实施方式中,优选由使用固定于磁性粒子的s抗原和酶标记的检测用抗体的夹心elisa法测定受试体中所含的s-igm。测定也可使用hiscl(注册商标)系列(sysmex株式会社制)等的市售的测定装置进行。
[0051]
如后述的实施例所示,covid-19重症化的患者组的血清中s-igm浓度与covid-19未重症化的患者组相比显著地高。这样,s-igm的测定结果可作为受试者的covid-19的重症化风险的指标利用。在本实施方式中,受试者的covid-19的重症化风险是指从受试者采集受试体之日起经过指定的期间(例如1天~1个月)后,该受试者的covid-19重症化的可能性。在一实施方式中,covid-19的重症化是指有含人工呼吸管理的集中治疗管理必要的状态、或者体外式膜型人工肺(ecmo:extracorporeal membrane oxygenation)的导入变得必要的状态。
[0052]
在本实施方式中,也可通过对s-igm的测定值和指定的阈值进行比较,以s-igm的测定值作为受试者的covid-19的重症化风险的指标利用。在一实施方式中,在s-igm的测定值在指定的阈值以上时,提示受试者的covid-19的重症化风险高。在进一步的的实施方式中,在s-igm的测定值不足指定的阈值时,提示受试者的covid-19的重症化风险低。
[0053]
在进一步的的实施方式中,也可将s-igm和其他生物标志物组合。作为其他生物标志物,可举出例如il-4。il-4是th2细胞因子之一,知晓与从igm向igg的类切换相关。il-4的氨基酸序列可从例如ncbi等的公知的数据库取得。一实施方式是包括对从感染sars-cov-2的受试者采集的受试体中所含的生物标志物进行测定,由上述生物标志物的测定得到的值成为上述受试者的covid-19的重症化风险的指标,上述生物标志物含抗sars-cov-2的s抗原的igm抗体及il-4的covid-19的重症化风险相关信息的取得方法。
[0054]
在别的实施方式中,也可代替s-igm而测定il-4。此时,il-4的测定值成为受试者的covid-19的重症化风险的指标。一实施方式是包括对从感染sars-cov-2的受试者或疑似罹患covid-19的受试者采集的受试体中所含的il-4进行测定,由上述il-4的测定得到的值成为上述受试者的covid-19的重症化风险的指标的,covid-19的重症化风险相关信息的取得方法。
[0055]
在本说明书中,“对il-4进行测定”含取得反映il-4的量或浓度的值,及确定il-4的量或浓度的值。“反映il-4的量或浓度的值”是指依据上述的标记物质的种类的值,可由对应于标记物质的种类的测定装置取得。“il-4的量或浓度的值”可基于反映il-4的量或浓度的值和校准物的测定结果而确定。在本实施方式中,可以例如il-4的重组型蛋白质作为校准物使用。
[0056]
在本实施方式中,可为由il-4的测定得到的值(以下,也称为“il-4的测定值”)、反映受试体中的il-4的量或浓度的值。另外,il-4的测定值可为基于校准物的测定结果而确定的受试体中的il-4的量或浓度的值。
[0057]
对il-4进行测定的手段不特别限定,可从公知的测定方法适宜选择。在本实施方式中,优选包括使用能与il-4特异性地结合的物质,捕获il-4的方法。通过将由这样的物质捕获的il-4用公知的方法检测,可对受试体中所含的il-4进行测定。作为能与il-4特异性地结合的物质,可举出例如抗体、适体等。在它们之中,也特别优选抗体。与il-4特异性地结合的抗体本身是公知的,市售。使用抗体对il-4进行测定的方法不特别限定,可从公知的免疫学测定法适宜选择。在本实施方式中,优选elisa法。
[0058]
作为一例,接下来说明由夹心elisa法的il-4的测定。此测定包括抗体和il-4的复合体的形成工序和该复合体的检测工序。在复合体的形成工序中,在固相上形成含il-4、用于捕获il-4的抗体(以下,也称为“捕获用抗体”)和用于检测il-4的抗体(以下,也称为“il-4检测用抗体”)的复合体。固相的详细如上述。在受试体含il-4时,通过将所述受试体、捕获用抗体和il-4检测用抗体混合,可形成含il-4、捕获用抗体和il-4检测用抗体的复合体。进而,通过使含复合体的溶液和可固定捕获用抗体的固相接触,可在固相上形成上述的复合体。或者,也可使用预先固定了捕获用抗体的固相。即,通过使固定了捕获用抗体的固相、受试体和il-4检测用抗体接触,可在固相上形成上述的复合体。再者,在捕获用抗体及il-4检测用抗体均为单克隆抗体时,优选表位互相不同。
[0059]
含il-4、捕获用抗体和il-4检测用抗体的复合体的检测工序的详细内容与对s-igm的测定所述的同样。在优选的实施方式中,通过使用被标记物质标记的il-4检测用抗体,检测由该标记物质发生的信号,取得il-4的测定值。或者,在使用抗il-4检测用抗体的标记第二抗体时,也可同样取得il-4的测定值。信号的检测结果可作为il-4的测定结果使用。例如,在定量检测信号的强度时,可以信号强度的测定值本身或从该测定值取得的值作为il-4的测定值使用。
[0060]
在本实施方式中,优选由使用固定于磁性粒子的捕获用抗体和酶标记的检测用抗体的夹心elisa法测定受试体中所含的il-4。
[0061]
与s-igm同样地,covid-19重症化的患者组的血清中il-4浓度与covid-19未重症化的患者组相比显著地高。从而,il-4的测定结果可作为受试者的covid-19的重症化风险的指标利用。
[0062]
在进一步的的实施方式中,也可通过对s-igm及il-4的测定值和与各自相对应的指定的阈值进行比较,以s-igm及il-4的测定值作为受试者的covid-19的重症化风险的指标利用。以下,将与s-igm相对应的指定的阈值称为“第1阈值”,将与il-4相对应的指定的阈值称为“第2阈值”。在一实施方式中,在s-igm的测定值是第1阈值以上,或者il-4的测定值是第2阈值以上时,提示受试者的covid-19的重症化风险高。在一实施方式中,在s-igm的测
定值不足第1阈值,并且il-4的测定值不足第2阈值时,提示受试者的covid-19的重症化风险低。
[0063]
在进一步的的实施方式中,取得方法包括对从受试者采集的受试体中所含的s-igm及il-4进行测定,由s-igm及il-4的测定值,将受试者的covid-19的重症化风险分类为3阶段。具体而言,如下所述:
[0064]
·
在s-igm的测定值是第1阈值以上,并且il-4的测定值是第2阈值以上时,提示受试者的covid-19的重症化风险高;
[0065]
·
在s-igm的测定值是第1阈值以上,或者il-4的测定值是第2阈值以上时,提示受试者的covid-19的重症化风险是中度;
[0066]
·
在s-igm的测定值不足第1阈值,并且il-4的测定值不足第2阈值时,提示受试者的covid-19的重症化风险低。
[0067]
在别的实施方式中,也可通过对il-4的测定值和第2阈值进行比较,以il-4的测定值作为受试者的covid-19的重症化风险的指标利用。在一实施方式中,在il-4的测定值是第2阈值以上时,提示受试者的covid-19的重症化风险高。在一实施方式中,在il-4的测定值不足第2阈值时,提示受试者的covid-19的重症化风险低。
[0068]
与s-igm及il-4的各自相对应的阈值不特别限定,可适宜设定。例如,从多个sars-cov-2感染者或covid-19患者采集受试体,对受试体中的s-igm及il-4进行测定。受试体采集之日起经过指定的期间(例如2周)后,确认covid-19重症化与否。将s-igm及il-4的测定值的数据分类为重症化的患者组的数据和未重症化的患者组的数据。进而,对于s-igm及il-4的各自而求出能最高精度地区别重症化的患者组和未重症化的患者组的值,将该值设定为阈值。在阈值的设定中,可考虑灵敏度、特异性、阳性的中率、阴性的中率等。
[0069]
在一实施方式中,与s-igm相对应的指定的阈值从例如35au/ml以上42au/ml以下,优选37au/ml以上41au/ml以下,更优选38au/ml以上41au/ml以下的范围设定。对于il-4,由于在被认为重症化风险低的受试者中几乎检测不到,与il-4相对应的指定的阈值可作为例如测定试剂盒的检测界限。具体而言,与il-4相对应的指定的阈值从0.1pg/ml以上2pg/ml以下,优选0.5pg/ml以上1.5pg/ml以下,更优选0.8pg/ml以上1.2pg/ml以下的范围设定。
[0070]
医师等的医疗从事者也可将由s-igm及/或il-4的测定值的提示和其他信息组合,判定受试者的covid-19重症化的风险。其中,“其他信息”含肺的x射线图像或ct图像的见解、此外的医学见解。
[0071]
在本实施方式中,也可取得s-igm及/或il-4的测定值的经时变化。此时,s-igm及/或il-4的测定值的经时变化成为受试者的covid-19的重症化风险的指标。测定值的经时变化只要是表示从相同的受试者定期或不定期多次采集的受试体中的s-igm及/或il-4的测定值的推移的信息,就不特别限定。作为这样的经时变化,可举出例如,从多个测定值算出的值(例如,在任意的2个时间点从受试者采集的2个受试体的测定值的差异、比等)、测定值的记录(例如,测定值的表或对测定值进行标绘的坐标图等)等。
[0072]
在本实施方式中,在由s-igm及/或il-4的测定值,提示为受试者的covid-19的重症化风险高时,在该受试者中可进行对于重症covid-19的医学介入。医学介入的例含药剂的施用、外科手术、免疫疗法、基因治疗、氧供给处置、使用人工心肺装置的处置等。药剂可从对于covid-19的公知的治疗药或成为其候选的医药适宜选择。例如,可举出有抗病毒作
用的药剂、减轻炎症的药剂、ace抑制药等。具体而言,可举出favipiravir、lopinavir、ritonavir、nafamostat、camostat、remdesivir、ribavirin、ivermectin、ciclesonide、chloroquine、hydroxychloroquine、干扰素、tocilizumab、sarilumab、tofacitinib、baricitinib、鲁索替尼、acalabrutinib、ravulizumab、eritoran、ibudilast、hlcm051、ly3127804等。另外,在别的实施方式中,药剂是疫苗。作为疫苗的例,可举出病毒载体疫苗、mrna疫苗、dna疫苗、重组蛋白质疫苗、vlp疫苗、灭活疫苗等。
[0073]
一实施方式是辅助受试者的covid-19的重症化风险的判定的方法(以下,也称为“判定方法”)。在此方法中,与本实施方式的取得方法同样地,对从受试者采集的受试体中所含的s-igm进行测定。进而,基于由s-igm的测定得到的值而判定受试者的covid-19的重症化风险。例如,也可对s-igm的测定值和指定的阈值进行比较,基于其比较结果而判定受试者的covid-19的重症化风险高或低。与s-igm相对应的指定的阈值的详细内容如上述。
[0074]
在一实施方式中,在s-igm的测定值在指定的阈值以上时,可判定为受试者的covid-19的重症化风险高。在进一步的的实施方式中,在s-igm的测定值不足指定的阈值时,可判定为受试者的covid-19的重症化风险低。
[0075]
在进一步的的实施方式中,判定方法也可包括对从受试者采集的受试体中所含的s-igm及il-4进行测定,通过对s-igm及il-4的测定值和与各自相对应的指定的阈值进行比较,判定受试者的covid-19的重症化风险。在一实施方式中,在s-igm的测定值是第1阈值以上,或者il-4的测定值是第2阈值以上时,可判定为受试者的covid-19的重症化风险高。在一实施方式中,在s-igm的测定值不足第1阈值,并且il-4的测定值不足第2阈值时,可判定为受试者的covid-19的重症化风险低。
[0076]
在一实施方式中,判定方法也可包括对从受试者采集的受试体中所含的s-igm及il-4进行测定,由s-igm及il-4的测定值如下所述判定受试者的covid-19的重症化风险:
[0077]
·
在s-igm的测定值是第1阈值以上,并且il-4的测定值是第2阈值以上时,判定为受试者的covid-19的重症化风险高;
[0078]
·
在s-igm的测定值是第1阈值以上,或者il-4的测定值是第2阈值以上时,判定为受试者的covid-19的重症化风险是中度;
[0079]
·
在s-igm的测定值不足第1阈值,并且il-4的测定值不足第2阈值时,判定为受试者的covid-19的重症化风险低。
[0080]
在别的实施方式中,也可通过对il-4的测定值和第2阈值进行比较,判定受试者的covid-19的重症化风险。在一实施方式中,在il-4的测定值是第2阈值以上时,可判定为受试者的covid-19的重症化风险高。在一实施方式中,在il-4的测定值不足第2阈值时,可判定为受试者的covid-19的重症化风险低。
[0081]
在本实施方式中,可在判定为covid-19的重症化风险高的受试者进行对于急性肾障碍或肺的纤维化的医学介入。一实施方式涉及重症化风险高的covid-19患者的治疗方法(以下,也称为“治疗方法”)。本实施方式的治疗方法包括对从感染sars-cov-2的受试者或疑似罹患covid-19的受试者采集的受试体中所含的s-igm进行测定的工序,基于由上述s-igm的测定得到的值而判定上述受试者的covid-19的重症化风险的工序,对判定为上述风险高的受试者进行对于重症covid-19的医学介入的工序。受试者、受试体、s-igm及其测定、医学介入等的详细与对本实施方式的取得方法所述的相同。
[0082]
在进一步的的实施方式中,治疗方法也可包括对从受试者采集的受试体中所含的s-igm及il-4进行测定,通过对s-igm及il-4的测定值和与各自相对应的指定的阈值进行比较,判定受试者的covid-19的重症化风险。il-4和其测定、及判定的详细与对本实施方式的取得方法及判定方法所述的相同。
[0083]
一实施方式是抗sars-cov-2的s抗原的igm抗体的监测方法(以下,也称为“监测方法”)。在本实施方式的监测方法中,使用从受试者在多个时间点采集的受试体,对各受试体中所含的s-igm进行测定。其中,受试者、受试体、s-igm及其测定的详细与对本实施方式的取得方法所述的相同。
[0084]
在本实施方式中,多个时间点只要是2以上的互相不同的时间点即可。例如,多个时间点含第1时间点和与该第1时间点不同的第2时间点。第1时间点不特别限定,是任意的时间点。例如,第1时间点也可为确证受试者感染sars-cov-2的时间点、在受试者中呈现covid-19的症状的时间点、受试者住院的时间点等。第2时间点只要是与第1时间点不同,就不特别限定。第2时间点优选是从第1时间点起经过1个月以内的期间的时间点。例如,第2时间点是从第1时间点起经过0.5小时、1小时、2小时、3小时、4小时、5小时、6小时、7小时、8小时、9小时、10小时、12小时、15小时、18小时、1天、2日、3天、4日、5天、6日、7天、8日、9天、10日、12天、2周、3周、4周或1个月的时间点。
[0085]
在本实施方式中,“从受试者在多个时间点采集的受试体”是在多个时间点的各自从相同的受试者采集的受试体。例如,从受试者在多个时间点采集的受试体含在第1时间点从受试者采集的第1受试体和在与该第1时间点不同的第2时间点从该受试者采集的第2受试体。在本实施方式的监测方法中,可在采集受试体时对s-igm进行测定,也可保存采集的各受试体而将它们综合测定。
[0086]
在本实施方式的监测方法中,监测相同的受试者中的s-igm的测定值,成为covid-19的重症化风险的指标。也可通过对各受试体的s-igm的测定值和指定的阈值进行比较,以s-igm的测定值作为受试者的covid-19的重症化风险的指标利用。指定的阈值的详细内容与对本实施方式的取得方法所述的同样。
[0087]
在一实施方式中,在多个时间点之中至少1个时间点,在s-igm的测定值在指定的阈值以上时,提示受试者的covid-19的重症化风险高。在进一步的的实施方式中,在多个时间点之中全部时间点,在s-igm的测定值不足指定的阈值时,提示受试者的covid-19的重症化风险低。
[0088]
在进一步的的实施方式中,判定方法也可包括对从受试者在多个时间点采集的各受试体中所含的s-igm及il-4进行测定,通过对s-igm及il-4的测定值和与各自相对应的指定的阈值进行比较,判定受试者的covid-19的重症化风险。在一实施方式中,在多个时间点之中至少1个时间点,在s-igm的测定值是第1阈值以上,或者il-4的测定值是第2阈值以上时,提示受试者的covid-19的重症化风险高。在一实施方式中,在多个时间点之中全部时间点,在s-igm的测定值不足第1阈值,并且il-4的测定值不足第2阈值时,提示受试者的covid-19的重症化风险低。
[0089]
在一实施方式中,监测方法含对从受试者采集的受试体中所含的s-igm及il-4进行测定,由s-igm及il-4的测定值,将受试者的covid-19的重症化风险分类为3阶段。具体而言,如下所述:
[0090]
·
在多个时间点之中至少1个时间点,在s-igm的测定值是第1阈值以上,并且il-4的测定值是第2阈值以上时,提示受试者的covid-19的重症化风险高;
[0091]
·
在多个时间点之中至少1个时间点,在s-igm的测定值是第1阈值以上,或者il-4的测定值是第2阈值以上时,提示受试者的covid-19的重症化风险是中度;
[0092]
·
在多个时间点之中全部时间点,在s-igm的测定值不足第1阈值,并且il-4的测定值不足第2阈值时,提示受试者的covid-19的重症化风险低。
[0093]
在别的实施方式中,也可通过对在多个时间点采集的各受试体的il-4的测定值和第2阈值进行比较,以il-4的测定值作为受试者的covid-19的重症化风险的指标利用。在一实施方式中,在多个时间点之中至少1个时间点,在il-4的测定值是第2阈值以上时,提示受试者的covid-19的重症化风险高。在一实施方式中,在多个时间点之中全部时间点,在il-4的测定值不足第2阈值时,提示受试者的covid-19的重症化风险低。
[0094]
结束本实施方式的监测方法的条件不特别限定,也可由医师等的医疗从事者适宜确定。例如,也可在由从受试者在多个时间点采集的受试体的s-igm及/或il-4的测定值,提示为受试者的covid-19的重症化风险高时,结束本实施方式的监测方法。此时,在该受试者中,优选进行对于重症covid-19的医学介入。医学介入的详细内容如上述。或者,也可在由从受试者在多个时间点采集的受试体的s-igm及/或il-4的测定值,提示为受试者的covid-19的重症化风险低,并且,在该受试者确认不到covid-19的症状时,结束本实施方式的监测方法。
[0095]
在上述的各实施方式中,也可在s-igm及il-4的测定值与和各自相对应的阈值相同时,提示或判定为受试者的covid-19的重症化风险高,或提示或判定为所述风险低。
[0096]
一实施方式是用于在上述的本实施方式的取得方法、判定方法、监测方法或治疗方法中使用的试剂盒。本实施方式的试剂盒含有含能与s-igm特异性地结合的物质的试剂。在进一步的的实施方式中,试剂盒也可含能与il-4特异性地结合的物质的试剂还含。在别的实施方式中,试剂盒也可代替含能与s-igm特异性地结合的物质的试剂而还含有含能与il-4特异性地结合的物质的试剂。能与s-igm及il-4的各自特异性地结合的物质如上所述。
[0097]
在本实施方式中,试剂盒也可收容各试剂的容器捆包在箱中而提供于使用者。在箱中,也可同装附带文书。在附带文书中也可记载试剂盒的构成、各试剂的组成、使用方法等。本实施方式的试剂盒的一例示于图1a。在图1a中,11表示试剂盒,12表示收容含能与s-igm特异性地结合的物质的试剂的容器,13表示捆包箱,14表示附带文书。
[0098]
在进一步的的实施方式中,试剂盒也可还含有含能与il-4特异性地结合的物质的试剂。此时,在附带文书中,对于含能与s-igm特异性地结合的物质的试剂和含能与il-4特异性地结合的物质的试剂,记载了试剂组成、使用方法等。在别的实施方式中,也可代替含能与s-igm特异性地结合的物质的试剂而含含能与il-4特异性地结合的物质的试剂。此时,在附带文书中,对于含能与il-4特异性地结合的物质的试剂,记载了试剂组成、使用方法等。
[0099]
在优选的实施方式中,本实施方式的试剂盒含用于捕获s-igm的s抗原及s-igm检测用抗体。s抗原也可固定于固相、优选磁性粒子。此实施方式的试剂盒的一例示于图1b。在图1b中,21表示试剂盒,22表示收容含用于捕获s-igm的s抗原的试剂的第1容器,23表示收容含s-igm检测用标记抗体的试剂的第2容器,24表示捆包箱,25表示附带文书。
[0100]
在进一步的的实施方式中,试剂盒也可还含有含il-4的捕获用抗体及检测用标记抗体的各自的试剂。在别的实施方式中,也可代替含s抗原的试剂及含s-igm检测用标记抗体的试剂而含含il-4的捕获用抗体及检测用标记抗体的各自的试剂。
[0101]
在上述之任一者的试剂盒中优选含校准物。作为校准物,可举出例如用于s-igm的定量的校准物(s-igm用校准物)及用于il-4的定量的校准物(il-4用校准物)。s-igm用校准物也可具备例如,不含s-igm的缓冲液(阴性对照)和sars-cov-2igm阳性受试体(血浆或血清)。il-4用校准物也可具备例如,不含il-4的缓冲液(阴性对照)和以已知浓度含il-4的缓冲液。
[0102]
含校准物的试剂盒的一例示于图1c。在图1c中,31表示试剂盒,32表示收容含s抗原的试剂的第1容器,33表示收容含s-igm检测用标记抗体的试剂的第2容器,34表示收容不含s-igm的缓冲液的第3容器,35表示收容sars-cov-2igm阳性受试体的第4容器,36表示捆包箱,37表示附带文书。不含s-igm的缓冲液及sars-cov-2igm阳性受试体可作为s-igm用校准物使用。
[0103]
在进一步的的实施方式中,试剂盒也可还含有含il-4的捕获用抗体及检测用标记抗体的各自的试剂和il-4用校准物。在别的实施方式中,也可代替含s抗原的试剂、含s-igm检测用标记抗体的试剂及s-igm用校准物而含含il-4的捕获用抗体及检测用标记抗体的各自的试剂和il-4用校准物。
[0104]
在本实施方式中,也含有含能与s-igm特异性地结合的物质的试剂用于制造上述的试剂盒的用途。一实施方式是试剂用于制造用于取得covid-19的重症化风险相关信息的试剂盒的用途,上述试剂是含能与s-igm特异性地结合的物质的试剂。进一步的的实施方式是试剂用于制造用于辅助covid-19的重症化风险的判定的试剂盒的用途,上述试剂是含能与s-igm特异性地结合的物质的试剂。进一步的的实施方式是试剂用于制造用于监测s-igm的试剂盒的用途,上述试剂是含能与s-igm特异性地结合的物质的试剂。在这些实施方式中,试剂也可还含有含能与il-4特异性地结合的物质的试剂。或者,试剂也可代替含能与s-igm特异性地结合的物质的试剂而含能与il-4特异性地结合的物质。
[0105]
一实施方式是covid-19的重症化风险相关信息的取得装置。另外,别的实施方式是用于取得covid-19的重症化风险相关信息的计算机程序。
[0106]
参照附图说明本实施方式的取得装置的一例。但是,本实施方式不仅限定于此例所示的形态。图2中所示的取得装置10含免疫测定装置20和计算机系统30。
[0107]
免疫测定装置的种类不特别限定,可对应于s-igm及il-4的测定方法而适宜选择。在将s-igm及il-4由elisa法测定时,免疫测定装置只要是能基于使用的标记物质检测信号,就不特别限定。在图2中所示的例中,免疫测定装置20是能检测由使用固定s抗原或抗il-4抗体的磁性粒子、及酶标记的s-igm或il-4检测用抗体的夹心elisa法发生的化学发光信号的市售的自动免疫测定装置。
[0108]
免疫测定装置20含检测部201。在将受试体、含上述的磁性粒子的试剂及含检测用抗体的试剂设置在免疫测定装置20时,免疫测定装置20使用各试剂执行抗原抗体反应,将基于与s-igm或il-4特异性地结合的酶标记抗体的化学发光信号由检测部201检测,将检测的化学发光信号变换为表示其强度的数字信号,将得到的数字信号(以下,称为“光学信息”)发送到计算机系统30。
[0109]
计算机系统30含计算机本体301和显示输入部302。计算机系统30从免疫测定装置20接收光学信息。进而,计算机系统30的处理器执行用于基于光学信息而取得安装到固态硬盘(以下,称为“ssd”)313上的covid-19的重症化风险相关信息的计算机程序。显示输入部302可为在显示部的表面配置输入部的触控面板,兼为显示部和输入部。作为触控面板,可举出例如静电容量方式等的公知的方式的触控面板。再者,图2中所示的取得装置10也可为免疫测定装置20和计算机系统30一体构成,但免疫测定装置20和计算机系统30是分别的机器。
[0110]
参照图3,计算机本体301具备cpu(central processing unit)310、rom(read only memory)311、ram(random access memory)312、ssd313、读取装置314、通信接口315、图像输出接口316和输入接口317。cpu310、rom311、ram312、ssd313、读取装置314、通信接口315、图像输出接口316及输入接口317由总线318能数据通信地连接。另外,免疫测定装置20能由通信接口315与计算机系统30通信地连接。
[0111]
cpu310能执行存储到rom311或ssd313的程序及加载到ram312上的程序。cpu310算出s-igm的测定值,显示于显示输入部302。
[0112]
rom311可由掩模型rom、prom、eprom或eeprom构成。在rom311中存储bios(basic input output system)。
[0113]
ram312可由sram或dram构成。ram312在记录在rom311及ssd313的程序的读取中使用。ram312在进一步执行这些程序之时,作为cpu310的作业区域利用。
[0114]
ssd313安装用于被cpu310执行的操作系统、应用程序等的计算机程序及在所述计算机程序的执行中使用的数据。再者,也可代替ssd而使用硬盘驱动器。在应用程序中,含用于取得covid-19的重症化风险相关信息的计算机程序。在计算机程序的执行中使用的数据中含用于判定covid-19的重症化风险的阈值。
[0115]
读取装置314是可读取记录在可移动型记录介质40的程序或数据的装置。读取装置314可由例如软盘驱动器、cd-rom驱动器、dvd-rom驱动器、usb端口、sd卡读取器、cf卡读取器、或者存储棒读取器构成。
[0116]
通信接口315是根据ethernet(注册商标)接口等的规格的有线接口等。计算机本体301也能由通信接口315向打印机等发送印刷数据。
[0117]
图像输出接口316是根据指定的规格的接口。指定的规格可是指d-sub、dvi-i、dvi-d、hdmi(注册商标)、或者displayport。图像输出接口316经与其规格相对应的线缆连接到显示输入部302。由此,显示输入部302可输出对应于cpu310给的图像数据的影像信号。显示输入部302根据输入的影像信号而显示图像(画面)。cpu310显示于显示输入部302的画面含操作按钮等的操作涉及的要素。
[0118]
输入接口317是可使cpu310识别显示输入部302检测的使用者的操作的接口电路。显示输入部302检测对于显示的操作按钮等的要素的使用者的操作,将检测信号输出到输入接口317。输入接口317驱动显示输入部302,cpu310可将自显示输入部302的检测信号识别为例如触摸的有无、触摸的位置等。使用者能由显示输入部302向计算机本体301输入各种指令。
[0119]
参照附图说明由本实施方式的取得装置10执行的处理程序。参照图4a,对取得s-igm的测定值而输出时的处理程序进行说明。在此例中,从由使用固定s抗原的磁性粒子及
酶标记的s-igm检测用抗体的夹心elisa法发生的化学发光信号取得s-igm的测定值,输出。在别的实施方式中,也可代替s-igm的测定值而取得il-4的测定值。
[0120]
在步骤s101中,cpu310从免疫测定装置20接收光学信息。在步骤s102中,cpu310从接收的光学信息取得s-igm的测定值。具体而言,cpu310对含有已知浓度的s-igm的校准物进行测定,向预先制成的校准曲线适用步骤s101中取得的光学信息,将所述光学信息变换为s-igm的浓度,以所述浓度作为测定值取得。cpu310将所述测定值存储到ssd313。在步骤s103中,cpu310输出s-igm的测定值。例如,cpu310向显示输入部302显示s-igm的测定值,或用打印机印刷,或发送到移动装置。在输出s-igm的测定值时,也可作为参照信息还输出与s-igm相对应的指定的阈值。这样,本实施方式的取得装置可作为covid-19的重症化风险相关信息,将s-igm的测定值提供于医师等。如上所述,s-igm的测定值成为covid-19的重症化风险的指标。
[0121]
在进一步的的实施方式中,取得s-igm及il-4的测定值而输出。例如,cpu310从免疫测定装置20取得光学信息(化学发光信号),从取得的光学信息算出s-igm及il-4的测定值存储到ssd313。cpu310输出s-igm及il-4的测定值。例如,cpu310向显示输入部302显示s-igm及il-4的测定值,或用打印机印刷,或发送到移动装置。在输出s-igm及il-4的测定值时,也可作为参照信息还输出第1阈值及第2阈值。
[0122]
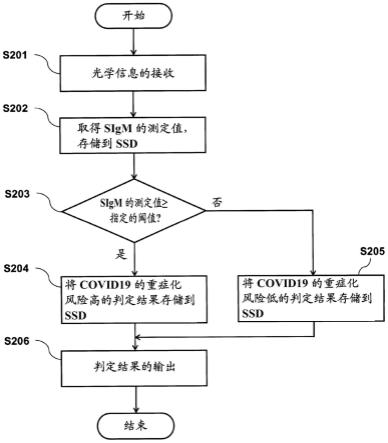
参照图4b,对于基于s-igm的测定值而判定covid-19的重症化风险时的流程进行说明。在步骤s201中,cpu310从免疫测定装置20接收光学信息。在步骤s202中,cpu310从接收的光学信息由与步骤s102同样的方法取得s-igm的测定值。cpu310将所述测定值存储到ssd313。在步骤s203中,cpu310对取得的s-igm的测定值和存储到ssd313的指定的阈值进行比较。s-igm的测定值在指定的阈值以上之时,处理进程到步骤s204。在步骤s204中,cpu310将covid-19的重症化风险高的判定结果存储到ssd313。在步骤s203中,在s-igm的测定值比阈值低时,处理进程到步骤s205。在步骤s205中,cpu310将covid-19的重症化风险低的判定结果存储到ssd313。在步骤s206中,cpu310输出判定结果。例如,cpu310向显示输入部302显示判定结果,或用打印机印刷,或发送到移动装置。在此例中,也可代替s-igm的测定值而取得il-4的测定值。这样,本实施方式的取得装置可将covid-19的重症化风险的判定结果提供于医师等。
[0123]
参照图4c,对于基于s-igm及il-4的测定值而判定covid-19的重症化风险时的流程进行说明。在步骤s301中,cpu310从免疫测定装置20接收光学信息。在步骤s302中,cpu310从接收的光学信息由与步骤s102同样的方法取得s-igm及il-4的测定值。cpu310将所述测定值存储到ssd313。在步骤s303中,cpu310对取得的s-igm的测定值和存储到ssd313的第1阈值进行比较。在s-igm的测定值比第1阈值低时,处理进程到步骤s304。在步骤s304中,对取得的il-4的测定值和存储到ssd313的第2阈值进行比较。在il-4的测定值比第2阈值低时,处理进程到步骤s305。在步骤s305中,cpu310将covid-19的重症化风险低的判定结果存储到ssd313。
[0124]
在步骤s303中,s-igm的测定值是第1阈值以上之时,处理进程到步骤s306。在步骤s304中,il-4的测定值是第2阈值以上之时,处理进行到步骤s306。在步骤s306中,cpu310将covid-19的重症化风险高的判定结果存储到ssd313。在步骤s307中,cpu310输出判定结果。例如,cpu310向显示输入部302显示判定结果,或用打印机印刷,或发送到移动装置。在此例
中,步骤s303及步骤s304的处理可改换顺序。
[0125]
在别的实施方式中,取得装置也可在s-igm的测定值是第1阈值以上,并且il-4的测定值在第2阈值以上时,判定为covid-19的重症化风险高。对于此时的流程进行说明。cpu310从免疫测定装置20接收光学信息,从接收的光学信息由与步骤s102同样的方法取得s-igm及il-4的测定值而存储到ssd313。cpu310对s-igm的测定值和第1阈值进行比较。s-igm的测定值是第1阈值以上之时,cpu310对il-4的测定值和第2阈值进行比较。il-4的测定值是第2阈值以上之时,cpu310将covid-19的重症化风险高的判定结果存储到ssd313。在s-igm的测定值比第1阈值低时,或者在il-4的测定值比第2阈值低时,cpu310将covid-19的重症化风险低的判定结果存储到ssd313。cpu310输出判定结果。例如,cpu310向显示输入部302显示判定结果,或用打印机印刷,或发送到移动装置。
[0126]
接下来,将本发明由实施例详细地说明,但本发明不限定于这些实施例。以下,“hiscl”是sysmex株式会社的注册商标。
[0127]
【实施例】
[0128]
【实施例1】
[0129]
(1)受试体
[0130]
以从由pcr检查确认sars-cov-2的感染的24名患者得到的血清作为受试体使用。血清由各患者住院之日采集的血液调制。对于患者住院后的最终的病状,在24名患者之中,5名成为“危重”,19名成为“重症”。“危重”是指有必要含人工呼吸管理的集中治疗管理或有探讨ecmo的导入的重症肺炎的病例,“重症”是指有氧施用必要的肺炎(spo2≤93%)的中等症的病例。
[0131]
(2)受试体中的生物标志物的测定
[0132]
(2.1)抗sars-cov-2抗原的抗体的测定
[0133]
作为抗sars-cov-2抗原的抗体,测定抗sars-cov-2的核衣壳蛋白质(n抗原)的igg抗体及igm抗体(以下,各自称为“n-igg”及“n-igm”)和抗刺突蛋白质(s抗原)的igg抗体及igm抗体(以下,各自称为“s-igg”及“s-igm”)的血清中的浓度。测定由全自动免疫测定装置hiscl-5000(sysmex株式会社)进行。在测定中,使用下述的试剂等。
[0134]
·
含固定了sars-cov-2抗原的磁性粒子的试剂(第1试剂)
[0135]
基于sars-cov2的基因组rna序列(ncbi的登录编号:yp_009724397及yp_009724390)而如以下一样调制sars-cov-2的n抗原及s抗原(s1亚基)的各自。在各序列附加his标签序列,克隆到pcdna3.4载体(thermo fisher scientific公司)中,向expi293细胞(thermo fisher scientific公司)转染得到的表达载体。6天后,回收培养上清。使用histrap hp柱(cytiva公司)及hiload 26/600superde
×
200pg柱(cytiva公司)纯化培养上清中的重组型抗原。使用1-乙基l-3-(3-二甲基氨基丙基)碳二亚胺(dojindo molecular technologies inc.)及n-羟基琥珀酰亚胺(sigma-aldrich公司)纯化的重组型n抗原及s抗原的各自,固定于磁性粒子的表面。将固定各抗原的磁性粒子用10mm hepes缓冲液(ph 7.5)清洗3次。向10mm hepes(ph 7.5)添加清洗后的磁性粒子至磁性粒子的浓度成0.48~0.52mg/ml,得到含固定了重组型n抗原的磁性粒子的试剂和含固定重组型s抗原的磁性粒子的试剂。
[0136]
·
含抗人igg或人igm的alp标记抗体的试剂(第2试剂)
[0137]
将与人igg特异性地结合的抗体由惯用的方法用alp标记而溶解于含有1%bsa及0.5%酪蛋白的缓冲液。对于与人igm特异性地结合的抗体也同样。
[0138]
·
测定用缓冲液及alp基质溶液
[0139]
作为测定用缓冲液,使用hiscl r4试剂(sysmex株式会社)。作为alp的化学发光底物的溶液,使用含cdp-star(注册商标)(applied biosystems公司)的hiscl r5试剂(sysmex株式会社)。
[0140]
由hiscl-5000的测定程序如下。将血清(20μl)和第1试剂(50μl)混合。对得到的混合液中的磁性粒子进行集磁而除上清,加hiscl清洗液(300μl)而清洗磁性粒子。除上清,向磁性粒子添加第2试剂(100μl)而混合。对得到的混合液中的磁性粒子进行集磁而除上清,加hiscl清洗液(300μl)而清洗磁性粒子。除上清,向磁性粒子添加测定用缓冲液(50μl)及alp底物溶液(100μl)而对化学发光强度进行测定。作为校准物,将sars-cov-2阳性受试体(cantor bioconnect公司及trina bioreactives公司)用磷酸缓冲液阶段稀释而使用。对校准物进行3次测定,由逻辑回归分析制成校准曲线。将在各血清的测定中得到的化学发光强度适用于校准曲线,确定抗体的浓度。
[0141]
(2.2)il-4的测定
[0142]
使用human il-4simplestep elisa试剂盒(ab215089,abcam公司),对血清中的il-4浓度进行测定。将稀释的标准样品(50μl)及各患者的血清(50μl)添加到板的各孔。接下来,向各孔加抗体混合物(50μl)。在密封板,设定为400rpm的板摇床上于室温温育1小时。将板用1
×
wash buffer pt清洗3次。在各清洗步骤中,添加wash buffer pt,静置30秒钟。接下来,向各孔加tmb development solution(100μl),在板摇床上在暗处温育10分钟。其后,向各孔加stop solution(100μl),在板摇床混合1分钟。将450nm处的od用vmax microplate reader(molecular devices公司)测定。基于从标准样品的测定值制成的标准曲线而算出各患者的血清中的il-4浓度。
[0143]
(3)测定结果
[0144]
抗体的测定结果示于表1。表中,抗体浓度的值是中位值,括弧内的值表示分布范围,“n.s.”表示无显著差异(not significant)。il-4的测定结果示于表2。表中,il-4浓度的值是中位值,括弧内的值表示分布范围。
[0145]
【表1:住院时的血清中的抗体浓度(au/ml)】
[0146]
抗体重症危重p值n-igg6.6(1.6~78.8)51.5(2.1~156.4)n.s.s-igg0.5(0.3~2.3)6.3(1.1~104.5)n.s.n-igm7.6(3.5~59.5)15.2(9.4~28.4)n.s.s-igm9.4(3.5~37.5)125.8(41.7~304.5)p<0.05
[0147]
【表2:住院时的血清中的il-4浓度(pg/ml)】
[0148] 重症危重p值il-40(0~10.84)1.34(0~5.01)p<0.05
[0149]
如表1所示,抗sars-cov-2抗原的4种抗体的浓度均与重症组相比,在危重组中处于高的倾向。但是,在危重组和重症组之间确认到显著差异的抗体仅为s-igm。结果提示,s-igm可作为用于判定covid-19的重症化风险的生物标志物利用。如表2所示,il-4浓度与重
症组相比,在危重组中显著地高。il-4被认为对于从igm向igg的类切换重要,在危重组中的il-4的测定结果被认为与同组中的s-igm的测定结果某些关联。均提示,il-4也可作为用于判定covid-19的重症化风险的生物标志物利用。
[0150]
【符号的说明】
[0151]
11、21、31:试剂盒
[0152]
12、22、32:第1容器
[0153]
23、33:第2容器
[0154]
34:第3容器
[0155]
35:第4容器
[0156]
13、24、36:捆包箱
[0157]
14、25、37:附带文书
[0158]
10:取得装置
[0159]
20:免疫测定装置
[0160]
30:计算机系统
[0161]
40:记录介质
[0162]
201:检测部
[0163]
301:计算机本体
[0164]
302:显示输入部
[0165]
310:cpu
[0166]
311:rom
[0167]
312:ram
[0168]
313:ssd
[0169]
314:读取装置
[0170]
315:通信接口
[0171]
316:图像输出接口
[0172]
317:输入接口
[0173]
318:总线
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。