1.本发明涉及光刻技术领域,特别涉及一种二胺化合物,由该二胺化合物制备的树脂、感光性树脂组合物及它们的用途。
背景技术:
2.随着技术的进步,半导体、显示面板等器件向小型化、薄型化、柔性化发展,这对产品的封装技术及工艺提出了越来越高的要求。通常而言,聚酰亚胺、聚苯并噁唑等树脂,由于良好的耐热性、高强度等特性,广泛应用于半导体等电子器件的封装领域,具体而言,如ic器件中rdl(ridistribution layer)、solder bump,器件的抗辐射保护、绝缘层,oled器件中的像素限定层(pdl)、平坦化层(pln)等。但是,由于聚酰亚胺、聚苯并恶唑等材料本体加工性不佳,通常而言,此类材料常经由其前驱体,如聚酰胺酸(或其酯化物)、羟基聚酰胺,或其齐聚物加工成型后,再经由高温环化、交联获得所需材料。为了获得良好的性能,降低未环化位点导致的性能缺陷(如未闭环的位点易发生降解导致分子键断裂而导致材料稳定性变差、拉伸强度变差等),较高的闭环率(接近100%)必不可少,而为了提高闭环率,通常需要将材料在高温下进行固化(》300℃),这不利于进一步改进器件的制程工艺,同时也导致较高的能耗。
3.为了降低聚酰亚胺、聚苯并噁唑等树脂的固化温度,可行的办法是在结构中引入柔性基团,如脂肪烃基团、烷氧基团、硅烷基团等。此类基团的引入,亦可能导致材料性能的劣化,如耐药性不佳等。
4.另外,随着可弯曲显示、半导体器件的技术发展,对封装、隔离材料的机械强度、延展性也提出了更高的要求,柔性基团的引入虽然可以提高材料的延展性,但同时亦带来强度降低、耐重复弯折性能不佳等问题。
技术实现要素:
5.发明要解决的问题
6.由此可见,提高封装材料的耐热性、耐化学药品、高断裂伸长率等性能,是当前产业界的长期课题。
7.解决问题的手段
8.针对上述问题,本发明的发明人通过大量试验发现,在二胺化合物中引入柔性链基团,同时引入可交联基团,可以在降低材料的固化温度、缩短固化时间的同时,获得具有良好耐药性、延展性(高断裂伸长率)等性能的固化膜。
9.具体而言,本发明的感光性树脂组合物的特征在于,包含碱溶性树脂和光产酸剂,其中,所述碱溶性树脂由二胺化合物与二羧酸酐、二羧酸、羧酸酯、二酰卤化合物中的一种或两种经缩聚得到。
10.本发明的发明人通过大量试验发现,在二胺化合物中引入交联位点,可以在固化过程中使组合物薄膜形成体型网络结构,从而降低材料的热膨胀系数、提高材料的强度、耐
热性、耐化学药品腐蚀等性能,以提高封装材料的可靠性,获得高可靠性的器件。
11.上述二胺化合物优选具有式(1)所示的结构:
[0012][0013]
式(1)中,f具有式(1-1)所示的结构,s具有式(1-2)所示的结构,t1、t2具有式(1-3)所示的结构,t1和t2可以相同或不同,
[0014][0015]
式(1-1)~(1-3)中,a选自二价的脂肪族基团、脂环式基团、芳香族基团、通过单键连接两个以上上述基团而得的二价基团中的一种,r1和r2各自独立的为氢、卤素、羟基、硝基、氰基、脂肪族基团、芳香族基团、羧基、酰胺基中的一种,q为1至3的整数,k为1至3的整数,m为1至3的整数;r3为二价的柔性链基团,n为1至4的整数,r4具有式(2)所示的结构,
[0016][0017]
式(2)中,r5选自氢、卤素、羟基、硝基、氰基、脂肪族基团、芳香族基团、羧基、酯基、酰胺基中的一种,p为0至4的整数,i为0至8的整数。
[0018]
通过在二胺化合物中引入交联位点,并将特定的基团连接至分子内的特定位置,能够解决本发明要解决的技术问题,实现本发明的上述有益的效果。值得注意的是,如果i大于8,会导致闭环反应所需温度过高,不利于后续制程的工艺改善及对降低能耗的要求。
[0019]
在上述方案中,p优选为1至4,即二胺化合物包含式(2)中的-ch2oc
ih2i 1
基团。通过包含式(2)中的-ch2oc
ih2i 1
基团,可以有效地防止所得的感光性树脂组合物的固化膜的热膨胀系数变高,能够更好地实现本发明的上述有益的效果。二价柔性链基团通常是指二价脂肪族基团,脂肪族基团是指不含环状结构的链状有机基团(包括直链和支链)。作为二价柔性链基团,可以列举例如亚烷基、亚烷基氧基、或亚硅烷基氧基等。
[0020]
需要说明的是,在本说明书中,结构式中的取代键指向芳香环中央的表达方式,表示取代位置可以在芳香环中的任意可能位置。
[0021]
在本说明书中,ca~cb的表达方式代表该基团具有的碳原子数为a~b,除非特殊说明,一般而言该碳原子数不包括取代基的碳原子数。本发明中,对于化学元素的表述,若无特别说明,通常包含化学性质相同的同位素的概念,例如“氢”的表述,也包括化学性质相同
的“氘”、“氚”的概念。
[0022]
在本发明书中,所述的“取代或未取代”的基团,可以取代有一个取代基,也可以取代有多个取代基,当取代基为多个时,可以选自不同的取代基,也可以全部或部分相同。
[0023]
在本说明书中,若无特别说明,芳基和杂芳基均包括单环和稠环的情况。
[0024]
在本说明书中,有机基团是指有机化合物中常见的基团,包括芳香族基团、脂环式基团和上述脂肪族基团。芳香族基团是指包含芳香环的有机基团,例如苯基、亚苯基、萘基、联苯基等;脂环式基团是指包含非芳香性的环的有机基团,例如环己基、环氧丙氧基、亚环戊烯基等。同时包含芳香环和非芳香环的基团在本发明中设为芳香族基团。
[0025]
具体而言,本发明的二价脂肪族基团优选为c1~c10的亚烷基、c1~c10的氟代亚烷基、c1~c20的氧亚烷基、c1~c20的亚聚氧乙烯基等,二价脂环式基团优选为c4~c18的亚环烷基,二价芳香族基团优选为c6~c20的取代或未取代的亚芳基,其中,取代的亚芳基优选被例如羟基、氟原子、羧基、-ch2oc
ih2i 1
等基团取代。另外,本发明的一价脂肪族基团优选为c1~c10的烷基、c1~c10的氟代烷基、c1~c20的烷氧基、-ch2oc
ih2i 1
、c1~c20的聚氧乙烯基等,一价芳香族基团优选为c6~c20的取代或未取代的芳基,其中,取代的芳基优选被例如羟基、氟原子、羧基、-ch2oc
ih2i 1
等基团取代。
[0026]
本发明的感光性树脂组合物中,二胺化合物优选f与s相连的位点和a与苯环相连的位点为间位关系;优选式(1-1)中,a与各苯环相连的位点的对位为羟基;优选式(1-3)中,r4与r3相连的位点和r4与氨基相连的位点为间位或对位关系。
[0027]
本发明的感光性树脂组合物中,二胺化合物优选a为-o-、-s-、-c(ch3)
2-、-c(ch3)(c2h5)-、-s(=o)
2-、-c(cf3)
2-或-c(c6h4oh)-。发明人发现,通过将a设为上述基团,能够降低闭环反应所需温度,有利于后续制程的工艺改善及对降低能耗的要求。
[0028]
本发明的感光性树脂组合物中,二胺化合物优选式(1-3)中,r4与r3相连的位点和r4与氨基相连的位点为对位关系;优选r1为氢;优选r2为氢;优选r3为亚烷基、亚烷基氧基、或亚硅烷基氧基;优选r5为氢;优选q为1;优选p为1或2;优选i为0或1;优选n为1。
[0029]
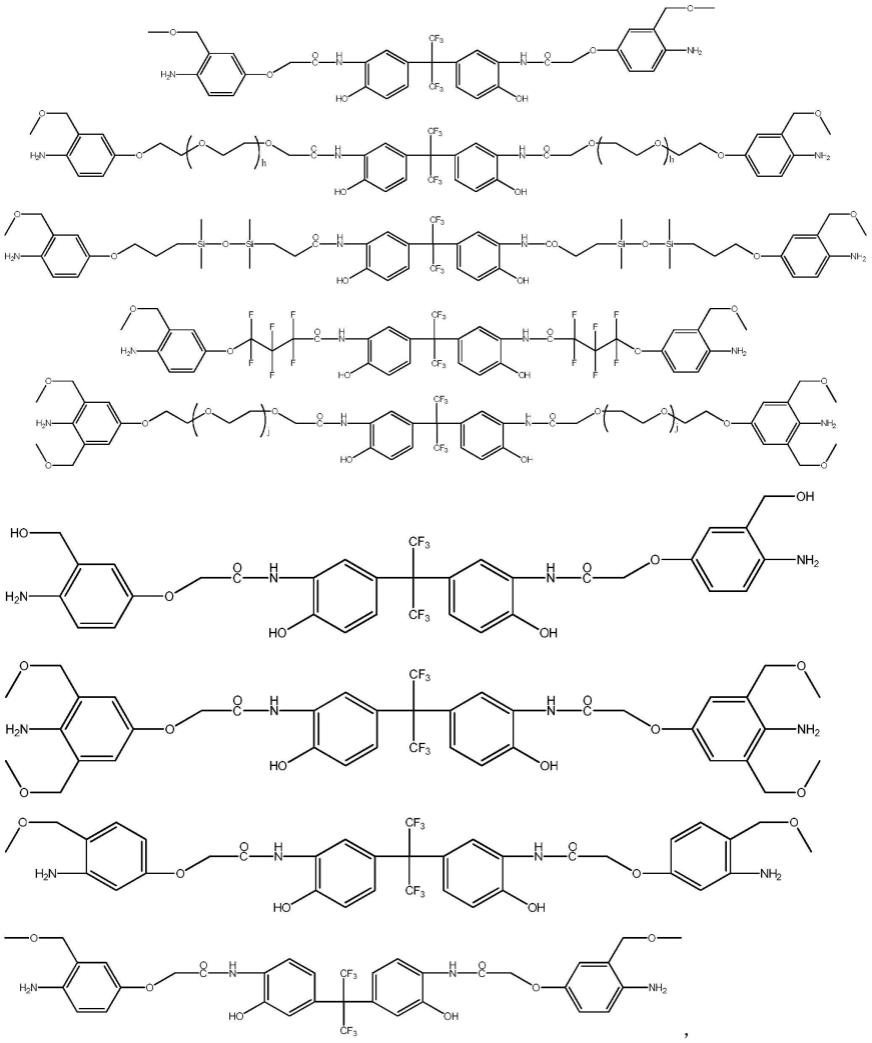
本发明的感光性树脂组合物中,二胺化合物优选具有以下结构中的一种:
[0030][0031][0032]
其中,h和j各自独立地表示0~50的整数,更优选各自独立地表示2~20的整数。
[0033]
本发明的树脂可以为聚酰亚胺或其前驱体(如聚酰胺酸、聚酰胺酸酯)聚苯并恶唑或其前驱体(如羟基聚酰胺等)、亦可以为上述所提结构的共聚物。上述所述树脂,可以通过本领域公知的方式将二胺化合物与二羧酸酐、二羧酸、二酰卤等化合物经缩聚制备而得,例如,将二胺化合物直接与二酸酐聚合得聚酰胺酸,再经酯化反应生成聚酰胺酸酯;将二胺化合物与二酰氯聚合得羟基聚酰胺;将二酸酐与醇反应生成二羧酸二酯,再经由与氯化亚砜反应生成二酰氯二酯,之后与二胺化合物聚合得羟基聚酰胺酸酯;将二酸酐与醇反映生成二羧酸二酯,再在环己基碳二亚胺等脱水剂存在下与二胺化合物反应聚合得羟基聚酰胺酸酯;将二胺化合物在环己基碳二亚胺等脱水剂存在下与二羧酸化合物反应得羟基聚酰胺。
[0034]
上述所述树脂中包含的本发明所制备的二胺化合物,可以是单一二胺化合物均
聚,亦可以是多种二胺进行共聚制备;此外,为调节树脂固化膜的性能,亦可以在结构中引入本领域公知的二胺单体进行共聚,具体可以如,二氨基二苯醚、2,2-双(3-氨基-4-羟基苯基)六氟丙烷、2,2-双(4-羟基-3-氨基苯基)丙烷、4,4'-二氨基二苯砜、4,4-环己烷二胺、1,3-双(4'-氨基苯氧基)苯等。
[0035][0036]
上述树脂中,二羧酸酐、二羧酸、羧酸酯、二酰卤化合物可以是市售的通用试剂,亦可以定制合成,可以是单一种类,亦可以将多种单体进行共聚。
[0037]
作为二羧酸酐,可以举出如二苯醚二酐、4,4'-(六氟异丙烯)二酞酸酐、双酚a二醚二酐、二苯甲醇二酐、2,3,3',4'-二苯醚四甲酸二酐、氢化均苯四甲酸二酐、二苯甲酮四羧酸二酐、环丁烷四甲酸二酐等。
[0038][0039]
作为羧酸酯,可举出例如二酸酐化合物经由醇或醇水混合物开环反应所产生的化合物。
[0040]
作为二酸化合物,可举出例如对苯二甲酸、二苯基醚二甲酸、双(羧基苯基)六氟丙烷、二苯甲酮二甲酸、联苯二甲酸等。
[0041]
为了获得较佳的分辨率及工艺性能,本发明的上述树脂的分子量优选为2000~100000,更优选为5000~50000;
[0042]
本发明所制备的树脂可以利用具有活性基团的单胺、酸酐、酰氯、单羧酸、活性酯
等封端剂对树脂末端进行封端,且为了进一步提高性能,封端剂可以引入烯基、炔基、苄醚、苄醇、硅烷等特有的功能基团,在后续的固化过程中进一步提高交联密度。
[0043]
本发明所制备的树脂,与感光剂、溶剂、产碱剂、流平剂、交联剂、偶联剂等组分混合可制备出具有良好解像性能的感光性树脂组合物。
[0044]
在一个典型实施方案中,本发明的感光性组合物可选择如下组成之添加剂:含硅氧烷基团的偶联剂,含氟表面活性剂,含聚乙二醇结构的表面活性剂等,这些助剂有助于起到提高薄膜的平坦化程度、感光性树脂组合物与基板之间附着力及降低显影后的残膜等效果。
[0045]
本发明的感光性树脂组合物中,树脂在组合物中占4重量%至30重量%,优选为5重量%至20重量%,感光剂占0.4重量%至8重量%,其它助剂占0.01重量%至0.5重量%,溶剂占55重量%至95重量%。本发明的感光性树脂组合物的固体成分含量为5重量%至45重量%,优选为8重量%至30重量%。过低的固含量不利于形成具有一定厚度的连续薄膜,而过高的固含量可能导致粘度过高进而导致在涂膜过程产生气泡、平整度变差等问题。
[0046]
本发明所述溶剂为本领域内通用的溶剂,包括但不限于γ-丁内酯,丙二醇单甲醚,丙二醇单乙醚,丙二醇单甲醚甲酸酯,丙二醇单乙醚甲酸酯,乳酸乙酯,氮甲基吡咯烷酮,n,n-二甲基甲酰胺,n,n-二甲基乙酰胺等。
[0047]
本发明的感光性树脂组合物中可以进一步含有热产碱和/或光产碱剂。从提高器件可靠性的角度考虑,一定范围内的碱性化合物可以作为在器件制程、使用过程中的酸性气体吸收剂,从而降低/避免酸性气体对器件中金属成分的腐蚀、引起化合物反应而导致像素收缩、亮度降低、功能失效等现象,提高器件的长期可靠性。此外,热产碱和/或光产碱剂可促进树脂主体结构在热固化过程中的闭环反应及与交联剂活性基团间的交联反应,降低光阻膜层的固化温度、提高反应的转化率,因此,能够进一步提高固化膜的机械性能、耐化学药品性、耐热性等指标,从而提高器件的长期可靠性。
[0048]
上述热产碱剂/光产碱剂,其用量占组合物中按树脂质量计的0.005%到10%,优选为0.02%到3%,更优选为0.1%到1%。
[0049]
从环境友好、改善器件制程工艺的角度考虑,为了降低器件的制程温度,热产碱剂应有较低的热起始分解温度;此外,出于储存稳定性、低挥发性的要求,感光性树脂组合物中的溶剂其标准大气压下沸点通常高于90℃,光刻制程中的除溶剂的烘烤温度通常介于90~140℃之间,因此,本发明的热产碱剂,优选热分解温度为90℃~250℃,更优选为100~200℃。
[0050]
从提高光量子效率的角度考虑,本发明所述的光产碱剂,优选其光吸收波段为200~450nm,更优选为250~435nm。
[0051]
本发明中使用的热产碱和/或光产碱剂产生的碱为有机含氮化合物,具体可以为脂肪伯胺、脂肪叔胺、芳香伯胺、芳香叔胺、季铵碱、咪唑、脒、喹啉、吡啶、哌啶等,从提高器件稳定性的角度考虑,优选不含卤素的化合物,具体可以举出例如对甲苯磺酰基乙酸胍,苯磺酰基乙酸胍、苯基丙炔酸胍、9-蒽甲酯哌啶-1-甲酸叔丁酯、9-蒽甲酯n,n-二乙基氨基甲酸酯、(e)-n-环己基-3-(2-羟基苯基)丙烯酰胺、(e)-1-哌啶子基-3-(2-羟基苯基)-2-丙烯-1-酮、9-蒽甲酯n-环己基氨基甲酸甲酯、胍基2-(3-苯甲酰基苯基)丙酸、1-(蒽醌-2-基)乙基咪唑-1-羧酸、(2-硝苯基)甲基-4-羟基哌啶-1-甲酸叔丁酯、(2-硝苯基)甲基-4-(甲基
丙烯酰氧基)、1-(蒽醌-2-基)乙基-n,n-二环己基氨基甲酸酯、二环己基-2-(3-苯甲酰基苯基)丙酸、环己-2-(3-苯甲酰基苯基)丙酸、9-蒽甲酯n,n-二环己基氨基甲酸酯、1-(蒽醌-2-基)乙基n-环己基氨基甲酸等。
[0052]
将本发明的感光性树脂组合物,经涂膜、前烘、光刻、显影、固化后可形成固化膜,永久留存于半导体芯片、面板等器件中,该固化膜具有优良的耐药性、耐高温、低热膨胀系数、高强度、高绝缘性等特点,可用于半导体芯片、平板显示等领域的封装工艺。
[0053]
发明的效果
[0054]
本发明的二胺化合物在结构中引入了特定的柔性链基团及多个交联位点,因此在感光性树脂薄膜固化过程中,通过树脂之间、树脂与交联剂之间、树脂与pac分子之间的交联反应,可以在降低固化温度的同时,进一步降低感光性树脂薄膜的热膨胀系数,提高薄膜的耐热性、耐化学药品性、力学性能等指标,从而提高半导体器件的稳定性。
[0055]
本发明所制备的树脂,与pac、溶剂、流平剂、交联剂、偶联剂等组分混合可制备出具有良好解像性能的感光性树脂组合物。
[0056]
本发明的感光性树脂组合物用于平板显示、半导体等电子器件制造中的层间绝缘、应力缓冲、平坦化层(pln)及oled化合物经沉积形成的像素分割(pdl层)等。
具体实施方式
[0057]
中间体的合成:
[0058]
5-氯-2-硝基苯甲醇乙酯的合成:
[0059]
氮气气氛下,将1eq 5-氯-2-硝基苯甲醇溶于二氯甲烷中,加入1.5eq乙酸酐,室温搅拌过夜后,用氢氧化钠溶液调节体系ph值至中性,收集有机相,将有机相用去离子水洗涤三遍,加入无水硫酸镁干燥过夜,去除残余水分,旋蒸除掉二氯甲烷,得5-氯-2-硝基苯甲醇乙酯。
[0060][0061]
(5-氯-2-硝基-1,3-亚苯基)二甲醇的合成:
[0062]
氮气气氛下,将1eq 5-氯-2硝基异酞醛溶于四氢呋喃中,保持室温搅拌。将2eq nabh4溶于水中,逐滴滴加nabh4水溶液至反应容器中,室温搅拌6h。滴加盐酸至反应体系中,使体系呈中性,旋蒸除掉四氢呋喃。用二氯甲烷萃取并收集有机相,有机相用去离子水洗三遍后,加入无水硫酸镁干燥过夜,去除残余水分,旋蒸除掉二氯甲烷,得(5-氯-2-硝基-1,3-亚苯基)二甲醇。
[0063][0064]
(5-氯-2-硝基-1,3-亚苯基)二(亚甲基)二乙酸酯的合成:
[0065]
与5-氯-2-硝基苯甲醇乙酯的合成方法类似,不同的是,将5-氯-2-硝基苯甲醇乙酯替换等物质的量的(5-氯-2-硝基-1,3-亚苯基)二甲醇,乙酸酐加入量调整为3eq,得(5-氯-2-硝基-1,3-亚苯基)二(亚甲基)二乙酸酯。
[0066][0067]
5-氯-1,3-二甲氧基甲基-2-硝基苯的合成:
[0068]
氮气保护、冰水浴冷却下,将2.5eq nah溶解于无水四氢呋喃中。保持冰水浴下搅拌,逐滴滴加1eq(5-氯-2-硝基-1,3-亚苯基)二甲醇的无水四氢呋喃溶液于反应瓶中,搅拌1h。保持冰水浴冷却,逐滴滴加2eq碘甲烷于反应瓶中,低温继续反应6h。加入甲醇猝灭过量的nah,向反应体系中加入水,用盐酸调节体系ph值为中性,旋蒸除掉四氢呋喃,甲醇。用二氯甲烷/水萃取产物,收集有机相,有机相用去离子水洗涤三遍,用无水硫酸镁干燥后,旋蒸除掉二氯甲烷,得5-氯-1,3-二甲氧基甲基-2-硝基苯。
[0069][0070]
4-氯-1-甲氧基甲基-2-硝基苯的合成:
[0071]
与合成5-氯-1,3-二甲氧基甲基-2-硝基苯类似,将(5-氯-2-硝基-1,3-亚苯基)二甲醇替换为4-氯-2-硝基苯甲醇,nah、碘甲烷用量分别更换为1.3eq、1eq,得4-氯-1-甲氧基甲基-2-硝基苯。
[0072][0073]
合成例1
[0074]
合成二胺化合物1
[0075]
氮气气氛下,将100.80g 4-氯-2(甲氧基甲基)-1-硝基苯与150ml四氢呋喃混合,冷水浴下加入30g氢氧化钠及0.5g四丁基氯化铵,升温至60℃,向体系中缓慢滴加45.6g羟基乙酸四氢呋喃溶液,保持60℃反应5h。将反应体系降至室温,在冰水浴冷却下缓慢滴加1mol/l盐酸至体系ph值为5,过滤收集沉淀,将沉淀溶于二氯甲烷后用去离子水洗涤,收集有机相,旋蒸除去大部分溶剂后,40℃下真空干燥,得中间体2-(3-(甲氧基甲基)-4-硝基苯氧基)乙酸。
[0076]
将36.6g 2,2-双(3-氨基-4-羟基苯基)六氟丙烷、41.2g环己基碳二亚胺(dcc)溶于四氢呋喃中,降温到0℃;保持0℃,将2-(3-(甲氧基甲基)-4-硝基苯氧基)乙酸(48.2g)的四氢呋喃溶液缓慢滴加到反应体系中,持续搅拌反应3h,过滤,除掉生成的环己基脲(dcu),旋蒸除掉大部分溶剂后将产物在40℃下真空干燥得二硝基化合物粗产物。将二硝基化合物粗产物用柱层析法纯化后用乙醇重结晶得二硝基化合物。
[0077]
将上述二硝基化合物溶于四氢呋喃/乙醇/吡啶中,加入1g 5%c-pd催化剂,剧烈搅拌下,通入氢气室温下还原,反应2h后停止反应,过滤除去c-pd催化剂,旋蒸除去大部分溶剂后,在40℃下真空干燥8h,得二胺化合物1。
[0078][0079]
质谱:zab-hs型质谱仪(英国micromass公司制造)m/z值(m 1):753。
[0080]
合成例2
[0081]
合成二胺化合物2
[0082]
与合成2-(3-(甲氧基甲基)-4-硝基苯氧基)乙酸类似,将4-氯-2(甲氧基甲基)-1-硝基苯替换为等物质的量的5-氯-2-硝基苯甲醇乙酯,得2-(3-(乙酰氧基甲基)-4-硝基苯氧基)乙酸。
[0083]
氮气气氛下,将36.6g 2,2-双(3-氨基-4-羟基苯基)六氟丙烷、41.2g环己基碳二亚胺(dcc)溶于四氢呋喃中,降温到0℃;保持0℃,将2-(3-(乙酰氧基甲基)-4-硝基苯氧基)乙酸(53.8g)的四氢呋喃溶液缓慢滴加到反应体系中,持续搅拌反应3h,过滤,除掉生成的环己基脲(dcu)。向反应溶液中加入0.1g四丁基溴化铵,并缓慢滴加40%naoh水溶液,调节并维持ph值为10,室温下反应5h后,将反应体系加入大量去离子水中,过滤收集沉淀。将沉淀溶于二氯甲烷,用去离子水洗涤至中性后,将有机相旋蒸除掉大部分溶剂,40℃下真空干
燥,得二硝基化合物粗产物。将粗产物用柱层析法纯化后用乙醇重结晶,得二硝基化合物。
[0084]
将上述二硝基化合物溶于四氢呋喃/乙醇中,加入1g 5%c-pd催化剂,剧烈搅拌下,通入氢气室温下还原,反应2h后停止反应,过滤除去c-pd催化剂,旋蒸除去大部分溶剂后,在40℃下真空干燥8h,得二胺化合物2。
[0085][0086]
质谱:zab-hs型质谱仪(英国micromass公司制造)m/z值(m 1):725。
[0087]
合成例3
[0088]
合成二胺化合物3
[0089]
与合成2-(3-(甲氧基甲基)-4-硝基苯氧基)乙酸类似,将4-氯-2(甲氧基甲基)-1-硝基苯替换为等物质的量的5-氯-1,3-二甲氧基甲基-2-硝基苯,得2-(3,5-二(甲氧基甲基)-4-硝基苯氧基)乙酸。
[0090]
以下与合成二胺化合物1类似,将2-(3-(甲氧基甲基)-4-硝基苯氧基)乙酸替换为等物质的量的2-(3,5-二(甲氧基甲基)-4-硝基苯氧基)乙酸,得二胺化合物3。
[0091][0092]
质谱:zab-hs型质谱仪(英国micromass公司制造)m/z值(m 1):841。
[0093]
合成例4
[0094]
合成二胺化合物4
[0095]
与合成2-(3-(甲氧基甲基)-4-硝基苯氧基)乙酸类似,将羟基乙酸替换为等物质的量的ho-(ch2ch2o)
n-ch2cooh(分子量约200),得如下结构中间体4a,并将产物溶于dmf后用碳酸氢钠水溶液滴定法测出准确单位质量羧基含量。
[0096][0097]
与二胺化合物1相比,将2-(3-(甲氧基甲基)-4-硝基苯氧基)乙酸更换为等物质的量(以羧基物质的量计)的中间体4a,得二胺化合物4,并将产物溶于dmf后用盐酸调节ph值为酸性,用氢氧化钠滴定法测出单位质量氨基含量。
[0098][0099]
合成例5
[0100]
合成二胺化合物5
[0101]
与合成2-(3-(甲氧基甲基)-4-硝基苯氧基)乙酸类似,将羟基乙酸更换为等物质的量的全氟4-羟基丁酸,得如下结构中间体5a。
[0102][0103]
与二胺化合物1相比,将2-(3-(甲氧基甲基)-4-硝基苯氧基)乙酸更换为等物质的量的中间体5a,得二胺化合物5。
[0104][0105]
质谱:zab-hs型质谱仪(英国micromass公司制造)m/z值(m 1):1025。
[0106]
合成例6
[0107]
合成二胺化合物6
[0108]
与合成2-(3-(甲氧基甲基)-4-硝基苯氧基)乙酸类似,将羟基乙酸更换为等物质的量的3-[3-(3-羟丙基)-1,1,3,3-四甲基-1-二硅氧烷基]丙酸,得如下结构中间体6a。
[0109][0110]
与二胺化合物1相比,将2-(3-(甲氧基甲基)-4-硝基苯氧基)乙酸更换为等物质的量的中间体6a,得二胺化合物6。
[0111][0112]
质谱:zab-hs型质谱仪(英国micromass公司制造)m/z值(m 1):1129。
[0113]
合成例7
[0114]
合成二胺化合物7
[0115]
与2-(3-(甲氧基甲基)-4-硝基苯氧基)乙酸的合成类似,将4-氯-2(甲氧基甲基)-1-硝基苯,替换为等物质的量的4-氯-1-甲氧基甲基-2-硝基苯,得2-(4-(甲氧基甲基)-3-硝基苯氧基)乙酸。
[0116]
与二胺化合物1相比,将2-(3-(甲氧基甲基)-4-硝基苯氧基)乙酸更换为等物质的量的2-(4-(甲氧基甲基)-3-硝基苯氧基)乙酸,得二胺化合物7。
[0117][0118]
质谱:zab-hs型质谱仪(英国micromass公司制造)m/z值(m 1):753。
[0119]
合成例8
[0120]
合成二胺化合物8
[0121]
与二胺化合物1相比,将2,2-双(3-氨基-4-羟基苯基)六氟丙烷替换为等物质的量
的2,2-双(4-氨基-3-羟基苯基)六氟丙烷,得二胺化合物8。
[0122][0123]
质谱:zab-hs型质谱仪(英国micromass公司制造)m/z值(m 1):753。
[0124]
合成例9
[0125]
合成二胺化合物9
[0126]
与二胺化合物1相比,不同的是,将4-氯-2(甲氧基甲基)-1-硝基苯替换为等物质的量的对硝基氯苯,合成中间体2-(4-硝基苯氧基)乙酸,将2-(3-(甲氧基甲基)-4-硝基苯氧基)乙酸替换为等物质的量的2-(4-硝基苯氧基)乙酸,得二胺化合物9。
[0127][0128]
质谱:zab-hs型质谱仪(英国micromass公司制造)m/z值(m 1):665。
[0129]
制备例1
[0130]
制备聚酰亚胺前驱体1:
[0131]
在氮气保护下,将7.53g二胺化合物1溶于20ml n-甲基吡咯烷酮(nmp)中,降温到0℃,将3.87g 3,3,4,4-二苯醚四酸酐与12g无水n-甲基吡咯烷酮的混合物快速加入反应体系中,保持0℃反应5h。升温至60℃,将2.68g n,n-二甲基甲酰胺二甲基缩醛缓慢滴加入反应体系中,保持60℃反应2h,降温到室温,将反应溶液倒入300ml去离子水中,过滤收集沉淀,将沉淀在50℃下真空干燥24h,得聚酰亚胺前驱体1(pi-1),分子量8000(马尔文公司viscotek凝胶渗透色谱仪,d6000m色谱柱)。
[0132]
制备例2
[0133]
制备聚酰亚胺前驱体2
[0134]
与制备例1相比,不同的是将二胺化合物1替换为等物质的量的二胺化合物2,得聚酰亚胺前驱体2(pi-2),分子量8000(马尔文公司viscotek凝胶渗透色谱仪,d6000m色谱柱)。
[0135]
制备例3
[0136]
制备聚酰亚胺前驱体3
[0137]
与制备例1相比,不同的是将二胺化合物1替换为等物质的量的二胺化合物3,得聚酰亚胺前驱体3(pi-3),分子量8200(马尔文公司viscotek凝胶渗透色谱仪,d6000m色谱柱)。
[0138]
制备例4
[0139]
制备聚酰亚胺前驱体4
[0140]
与制备例1相比,不同的是将二胺化合物1替换为等物质的量的二胺化合物4(以氨基含量计),得聚酰亚胺前驱体4(pi-4),分子量9000(马尔文公司viscotek凝胶渗透色谱仪,d6000m色谱柱)。
[0141]
制备例5
[0142]
制备聚酰亚胺前驱体5
[0143]
与制备例1相比,不同的是将二胺化合物1替换为等物质的量的二胺化合物5,得聚酰亚胺前驱体5(pi-5),分子量8800(马尔文公司viscotek凝胶渗透色谱仪,d6000m色谱柱)。
[0144]
制备例6
[0145]
制备聚酰亚胺前驱体6
[0146]
与制备例1相比,不同的是将二胺化合物1替换为等物质的量的二胺化合物6,得聚酰亚胺前驱体6(pi-6),分子量9000(马尔文公司viscotek凝胶渗透色谱仪,d6000m色谱柱)。
[0147]
制备例7
[0148]
制备聚酰亚胺前驱体7
[0149]
与制备例1相比,不同的是将二胺化合物1替换为等物质的量的二胺化合物7,得聚酰亚胺前驱体7(pi-7),分子量8200(马尔文公司viscotek凝胶渗透色谱仪,d6000m色谱柱)。
[0150]
制备例8
[0151]
制备聚酰亚胺前驱体8
[0152]
与制备例1相比,不同的是将二胺化合物1替换为等物质的量的二胺化合物8,得聚酰亚胺前驱体8(pi-8),分子量8100(马尔文公司viscotek凝胶渗透色谱仪,d6000m色谱柱)。
[0153]
制备例9
[0154]
制备聚酰亚胺前驱体9
[0155]
与制备例1相比,不同的是将二胺化合物1替换为等物质的量的二胺化合物9,得聚酰亚胺前驱体9(pi-9),分子量8200。
[0156]
制备例10(比较例)
[0157]
制备聚酰亚胺前驱体a
[0158]
与制备例1相比,不同的是将二胺化合物1替换为等物质的量的二胺化合物a,得聚酰亚胺前驱体a(pi-a),分子量8000。
[0159][0160]
实施例和比较例
[0161]
实施例1
[0162]
将制备例1的树脂(10g)、下述结构的感光剂(2g)及交联剂(2g)、0.1%的含氟表面活性剂、0.1%的硅烷偶联剂,γ-丁内酯(85g)混合并充分溶解,得到感光性树脂组合物c1。
[0163][0164]
实施例2-9
[0165]
与实施例1的方法相同,不同的是将制备例1的树脂分别替换为等质量制备例2~8所合成的树脂,得到感光性树脂组合物c2-c9。
[0166]
比较例1
[0167]
与实施例1的方法相同,不同的是将制备例1的树脂替换为制备例10所合成的树脂,得感光性树脂组合物b1。
[0168]
性能测试:
[0169]
耐化学药品性能测试:
[0170]
将上述所制备的感光性树脂组合物,采用旋转涂膜(250rpm)的方法涂敷于4英寸的方形玻璃基板上,在120℃下预烘烤180s以去除大部分溶剂,测量膜厚t,之后将覆膜玻璃基板置于180℃洁净烘箱中氮气保护下(氧气浓度《20ppm)固化60min,用椭偏仪测试膜厚(t1)。将覆膜玻璃基板浸泡于40℃剥离液中刻蚀130s或室温下,浸泡于n-甲基吡咯烷酮(nmp)中15min,取出后迅速用去离子水冲洗,然后在100℃洁净烘箱中氮气保护下(氧气浓度《20ppm)烘干20min,用椭偏仪测试膜厚t2,计算刻蚀前及刻蚀后的膜厚变化δt=∣(t2-t1)/t1∣*100%,膜厚损失低于5%,判定为良好。
[0171]
上述性能测试结果如表1所示。
[0172]
表1
[0173][0174]
拉伸测试:
[0175]
采用旋转涂膜法,将上述感光性树脂组合物c1-c8,b1涂敷于4英寸方形玻璃基板上,烘烤形成约13μm厚的薄膜,在紫外曝光机下曝光后显影形成10mm宽标准样条图形。
[0176]
将覆膜玻璃基板置于洁净烘箱中,在氮气保护下(氧气浓度《20ppm),按照5℃/min的升温速率,100℃(保温30min)—140℃(保温10min)—180℃(保温60min)-自然冷却到室温的温度程序进行固化。
[0177]
在100℃(氮气保护下)烘干,得测试标准样条,膜厚10μm,用万能材料试验机测试薄膜拉伸性能(拉伸速率2mm/min,环境温度23℃,湿度50
±
5%。),断裂伸长率高于50%,判定为良好。
[0178]
上述性能测试结果如表2所示。
[0179]
表2
[0180] 感光性树脂组合物断裂伸长率(%)实施例1c190实施例2c290实施例3c3100实施例4c4130实施例5c5100实施例6c6120实施例7c785实施例8c885实施例9c935对比例1b115
[0181]
本发明通过上述实施例来说明本发明的新型二胺化合物、感光性树脂组合物及其应用。从以上数据可知,本发明所制备的二胺化合物,相较于当前技术而言,本发明所制备的二胺化合物在相对较低的温度下、短时间内即可完成充分的固化,其相同固化条件下成膜后的药品耐受性明显优于现有产品,可显著降低此类光刻胶的加工温度;同时,由于柔性基团及交联基团的同时引入,材料的断裂伸长率亦显著由于未引入此类基团的产品。
[0182]
另外,实施例9的感光性树脂使用了n为1但p为0的二胺化合物9,即,二胺化合物虽然包含柔性基团但不含式(2)中的-ch2oc
ih2i 1
基团,因此其性能虽然明显优于比较例,但与实施例1~6相比明显不足。
[0183]
但本发明并不局限于上述实施例,即不意味着本发明必须依赖上述实施例才能实施。所属技术领域的技术人员应该明了,对本发明的任何改进,对本发明产品各原料的等效替换及辅助成分的添加、具体方式的选择等,均落在本发明的保护范围和公开范围之内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。
