1.本发明涉及一种用于锂二次电池的正极活性物质及制造其的方法,并且更具体地,涉及一种可以包含锂金属氧化物的用于锂二次电池的正极活性物质和制造该正极活性物质的方法。
背景技术:
2.二次电池是可重复充电和放电的电池,并已广泛应用于如移动电话、笔记本电脑等的便携式电子设备而作为其电源。
3.二次电池的实例可以包括锂二次电池、镍镉电池、镍氢电池等。其中,锂二次电池的工作电压和每单位重量的能量密度高,并且在充电速度和重量轻方面是有利的。就此而言,锂二次电池已经被积极开发并应用为电源。
4.锂二次电池的正极包括能够使锂离子可逆地嵌入和脱嵌的正极活性物质。例如,可以使用锂复合氧化物作为正极活性物质。
5.锂复合氧化物可以包括例如金属元素,如镍、钴、锰、铝等。
6.随着锂二次电池的应用领域扩大到例如混合动力汽车等的大型设备,已经积极进行研究和开发具有增加的镍含量以确保锂二次电池的高容量的高镍锂复合氧化物。
7.例如,韩国专利登记公布第10-0821523号公开了一种制造包括高镍基锂复合氧化物的正极活性物质的方法。
8.[现有技术文献]
[0009]
[专利文献]
[0010]
韩国专利登记公布第10-0821523号
技术实现要素:
[0011]
本发明的一个目的是提供一种具有改善的寿命特性和高温储存性能的锂二次电池。
[0012]
本发明的另一个目的是提供一种可以实现改善的寿命特性和高温储存性能的正极活性物质,及制造其的方法。
[0013]
为了实现上述目的,根据本发明的一个方面,提供了一种用于二次电池的正极活性物质,其包含:具有其中多个一次颗粒聚集的二次颗粒形式的锂金属氧化物颗粒,其中一次颗粒包含具有最小内角为45
°
以上,并且最大高度(maximum height)为0.5μm以上的尺寸的三角形形状(triangular shape)的颗粒。
[0014]
在一个实施方案中,锂金属氧化物颗粒可以含有占除锂和氧之外的所有元素的80摩尔%以上的镍。
[0015]
在一个实施方案中,锂金属氧化物颗粒可以由下面的式1表示:
[0016]
[式1]
[0017]
li
x
niacobmcoz[0018]
(在式1中,m为mg、sr、ba、b、al、si、mn、ti、zr和w中的至少一种,并且x、a、b、c和z分别在0.9《x《1.2,0.8≤a≤0.98,0≤c/(a b)≤0.25,0≤c≤0.2和1.9≤z≤2.1的范围内)。
[0019]
在一个实施方案中,三角形(triangular shape)的最小内角的大小可以为45
°
至60
°
。
[0020]
在一个实施方案中,三角形的最大高度可以为1μm至4μm。
[0021]
在一个实施方案中,锂金属氧化物颗粒可以具有3μm至20μm的粒度(d
50
)。
[0022]
此外,根据本发明的另一方面,提供了一种制造用于二次电池的正极活性物质的方法,该方法包括:在包含金属盐、螯合剂和共沉淀剂(co-precipitating agent)的反应溶液中进行共沉淀反应;及获得通过共沉淀反应形成的金属氢氧化物颗粒。
[0023]
进行共沉淀反应的步骤可以包括:在保持反应溶液的ph值和反应溶液中螯合剂的浓度的同时进行第一共沉淀反应;在降低反应溶液的ph值并增加反应溶液中的螯合剂的浓度的同时进行第二共沉淀反应;和在保持反应溶液的ph值和反应溶液中的螯合剂的浓度的同时进行第三共沉淀反应,并且依次进行第一共沉淀反应至第三共沉淀反应。
[0024]
在一个实施方案中,可以通过混合含有金属盐的水溶液和含有螯合剂和共沉淀剂的水溶液来制备反应溶液。
[0025]
在一个实施方案中,当共沉淀反应的总反应时间为1t时,第二共沉淀反应的反应时间可以为0.001t至0.02t。
[0026]
在一个实施方案中,在第二共沉淀反应中,反应溶液的ph值可以由第一共沉淀反应中的ph值降低0.7至2.5,并且,基于第一共沉淀反应中的螯合剂的浓度,可以将反应溶液中螯合剂的浓度增加至1.2倍至2.5倍的数值。
[0027]
在一个实施方案中,金属氢氧化物颗粒可以具有其中多个一次颗粒聚集的二次颗粒形式,并且一次颗粒可以包含具有三角形形状的颗粒,以及当共沉淀反应的总反应时间为1t时,从共沉淀反应开始经过0.6t的时间之前可以形成具有三角形形状的颗粒。
[0028]
在一个实施方案中,三角形形状的最大高度可以为0.5μm以上。
[0029]
在一个实施方案中,金属盐可以含有镍。
[0030]
在一个实施方案中,金属盐可以进一步含有co、mg、sr、ba、b、al、si、mn、ti、zr和w中的至少一种。
[0031]
在一个实施方案中,金属盐所含有的全部金属中的镍的摩尔比可以为0.8以上。
[0032]
在一个实施方案中,在进行共沉淀反应的步骤中,可以将反应溶液中的ni
2
的浓度保持在50ppm至100ppm。
[0033]
在一个实施方案中,在第三共沉淀反应期间,可以将反应溶液中的固形物浓度(solid content concentration)控制在30重量%至55重量%。
[0034]
在一个实施方案中,制造用于二次电池的正极活性物质的方法可以进一步包括:将金属氢氧化物颗粒与锂源混合;和煅烧金属氢氧化物颗粒和锂源的混合物以制备锂金属氧化物颗粒。
[0035]
锂金属氧化物颗粒可以具有其中多个一次颗粒聚集的二次颗粒形式,其中该一次颗粒可以包含具有最小内角为45
°
以上,并且最大高度为0.5μm以上的尺寸的三角形形状的颗粒。
[0036]
在一个实施方案中,可以在670℃至785℃的温度范围内进行煅烧。
[0037]
此外,根据本发明的另一方面,提供了一种锂二次电池,其包括:包含根据示例性实施方案的正极活性物质的正极;和设置为与正极相对的负极。
[0038]
根据示例性实施方案的用于二次电池的正极活性物质可以包括锂金属氧化物颗粒,该锂金属氧化物颗粒包括具有预定大小以上的最小内角和预定最大高度以上的三角形形状的一次颗粒,从而该用于二次电池的正极活性物质具有改善的寿命特性和高温储存性能。
[0039]
根据示例性实施方案的锂二次电池可以包括正极活性物质,从而具有改善的寿命特性和高温储存性能。
附图说明
[0040]
根据以下结合附图的详细说明,将更清楚地理解本发明的上述和其他目的、特征和其他优点,其中:
[0041]
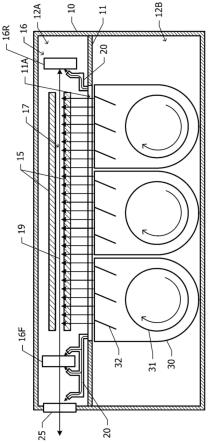
图1为示出根据本发明的一个实施方案的锂二次电池的示意性横截面图;
[0042]
图2为示意性地示出根据本发明的示例性实施方案的制造用于锂二次电池的正极活性物质的方法的流程图;
[0043]
图3a至图3d分别为在实施例1和比较例1-比较例3的金属氢氧化物颗粒表面上拍摄的扫描电子显微镜(sem)图像;
[0044]
图4a至图4d分别为在实施例1-实施例3和比较例3的锂金属氧化物颗粒表面上拍摄的扫描电子显微镜(sem)图像;
[0045]
图5a和图5b分别为在比较例1和比较例2的锂金属氧化物颗粒的表面上拍摄的扫描电子显微镜(sem)图像;
[0046]
图6a和图6b分别为在实施例1和比较例3的金属氢氧化物颗粒的表面上拍摄的扫描电子显微镜(sem)图像,这些图像是在从共沉淀反应开始经过0.55t(共沉淀反应的总反应时间:1t)的时间时拍摄的。
具体实施方式
[0047]
如本文所用,术语“锂金属氧化物(lithium metal oxide)”可以指作为能够使锂离子嵌入和脱嵌的氧化物的化合物,并且包括锂和金属元素。
[0048]
如本文所用,术语“一次颗粒(primary particle)”可以指单独存在而不形成聚集体(aggregate)的单个颗粒(整体(monolith))。
[0049]
如本文所用,术语“二次颗粒(secondary particle)”可以指具有其中一次颗粒聚集的形式的颗粒。
[0050]
根据本发明,提供了一种锂金属氧化物颗粒,其具有其中多个一次颗粒聚集的二次颗粒形式,其中一次颗粒包括具有三角形形状的颗粒。可以将锂金属氧化物颗粒提供为用于锂二次电池的正极活性物质。此外,根据本发明,提供了一种制造锂金属氧化物颗粒的方法。
[0051]
用于锂二次电池的正极活性物质
[0052]
根据示例性实施方案的用于二次电池的正极活性物质可以包括具有其中多个一次颗粒聚集的二次颗粒形式的锂金属氧化物颗粒。一次颗粒可以包括具有三角形形状的颗
粒。三角形的最小内角的大小可以为45
°
以上,并且三角形的最大高度可以为0.5μm以上。
[0053]
根据示例性实施方案的锂二次电池可以包括作为正极活性物质的锂金属氧化物颗粒,从而具有改善的寿命特性(例如,在25℃下的容量保持率)和高温储存性能(例如,在45℃下的容量保持率)。
[0054]
在一个实施方案中,一次颗粒可以进一步包括具有最小内角的大小为小于45
°
的三角形形状的颗粒、无定形颗粒、针状颗粒等。
[0055]
具有三角形形状的颗粒可以指,当从顶部观察锂金属氧化物颗粒的表面时,待观察的表面(即,与观察者相对的表面)具有三角形形状的一次颗粒。例如,在使用扫描电子显微镜(sem)测量锂金属氧化物颗粒的表面时,如果在sem图像(即二维图像)中测得的一次颗粒的表面形状为三角形,则可以将该一次颗粒定义为具有三角形形状的颗粒。
[0056]
在一些实施方案中,三角形形状可以具有顶点(顶角)弯曲(curved)的形状。例如,其中由三个边在大约20%(基于各边的100%长度)范围内延伸形成的假想延伸边形成三个顶点的情况也可以包括在三角形形状中。
[0057]
例如,三角形的边可以是直线或具有微小曲率(slight curvature)的曲线,只要能够保持三角形形状即可。
[0058]
三角形的最小内角(minimum internal angle)可以指三角形的最小值内角(smallest internal angle)。但是,当所有三个角度都相同时,最小内角可能为60
°
。
[0059]
在一个实施方案中,三角形的最小内角的大小可以为45
°
以上且小于60
°
。
[0060]
在一个实施方案中,三角形的最小内角的大小可以是45
°
至60
°
。例如,可以包括三角形的一个内角为60
°
以具有等边三角形形状的情况。
[0061]
三角形的最大高度可以指三角形的最长高度(longest height)。例如,三角形的高度可以意指当从一个顶点向相对侧向下绘制垂线时该垂线的长度,并且三角形中可能存在三条垂线。其中,最长垂线的长度可以指最大高度。
[0062]
在一个实施方案中,三角形的最大高度可以为0.5μm以上、1μm以上或2μm以上。在上述范围内,可以进一步改善二次电池的寿命特性和高温储存性能。
[0063]
在一个实施方案中,三角形的最大高度可以为6μm以下、5μm以下或4μm以下。
[0064]
在一些实施方案中,三角形的最大高度可以为0.5μm至6μm、0.5μm至5μm、1μm至4μm、2μm至4μm或3μm至4μm。
[0065]
在一个实施方案中,锂金属氧化物颗粒(即二次颗粒)可以具有3μm至20μm的粒度(d
50
)。
[0066]
例如,粒度d
50
可以限定为基于体积的累积分布(volume-based cumulative distribution)的50%的点处的粒度。例如,粒度d
50
可以通过使用激光衍射粒度测量装置(例如,麦奇克(microtrac),mt 3000)的激光衍射方法来测量。
[0067]
在一些实施方案中,三角形的最大高度与锂金属氧化物颗粒的粒度(d
50
)的长度比可以为0.025至1、0.05至0.4或0.1至0.25。
[0068]
在一个实施方案中,锂金属氧化物颗粒可以含有镍(ni)。
[0069]
在一些实施方案中,锂金属氧化物颗粒中镍的含量可以为除锂和氧之外的所有元素的80摩尔%以上、83摩尔%以上、88摩尔%以上或93摩尔%以上。在上述范围内,可以实现具有高容量的二次电池。在这点上,随着锂金属氧化物颗粒中镍的含量的增加,锂金属氧
化物颗粒的化学稳定性可能劣化。然而,根据本发明的锂金属氧化物颗粒可以通过包含具有上述三角形形状的一次颗粒而具有改善的化学稳定性。
[0070]
在一个实施方案中,锂金属氧化物颗粒可以由下式1表示。[式1]
[0071]
li
x
niacobmcoz[0072]
在式1中,m可以为mg、sr、ba、b、al、si、mn、ti、zr和w中的至少一种,并且x、a、b、c和z可以分别在0.9《x《1.2,0.8≤a≤0.98,0≤c/(a b)≤0.25,0≤c≤0.2和1.9≤z≤2.1的范围内。
[0073]
在一些实施方案中,a可以在0.83≤a≤0.98、0.85≤a≤0.98、0.88≤a≤0.98或0.9≤a≤0.98的范围内。
[0074]
在一些实施方案中,锂金属氧化物颗粒可以进一步包括掺杂元素(doping element)。例如,掺杂元素可以包括al、ti、ba、zr、si、b、mg、sr、w、la等。可以通过掺杂元素改善锂金属氧化物颗粒的结构稳定性。
[0075]
在一个实施方案中,正极活性物质可以进一步包括在锂金属氧化物颗粒表面上的涂层。例如,涂层可以包括al、ti、ba、zr、si、b、mg、sr、w、la等。在这种情况下,可以进一步改善二次电池的寿命特性、高温稳定性等。
[0076]
制造用于锂二次电池的正极活性物质的方法
[0077]
图2为示意性地示出根据示例性实施方案的制造用于锂二次电池的正极活性物质的方法的流程图。
[0078]
制备金属氢氧化物颗粒的步骤
[0079]
根据示例性实施方案的制造用于二次电池的正极活性物质的方法可以包括制备金属氢氧化物颗粒的步骤。
[0080]
制备根据示例性实施方案的金属氢氧化物颗粒的步骤可以包括在包含金属盐、螯合剂和共沉淀剂的反应溶液中进行共沉淀反应的步骤(例如,s10);以及获得通过该共沉淀反应形成的金属氢氧化物颗粒的步骤(例如,s20)。
[0081]
在一个实施方案中,可以通过在含有螯合剂和共沉淀剂的水溶液中加入(inputting)金属盐的水溶液并混合来制备反应溶液。
[0082]
例如,步骤s10可以包括制备含有螯合剂和共沉淀剂的水溶液;将金属盐的水溶液加入到该水溶液中。例如,水溶液的ph值可以为11.7至12.3。例如,可以使用naoh水溶液来控制ph值。
[0083]
在一个实施方案中,步骤s10可以包括在保持反应溶液的ph值和该反应溶液中的螯合剂的浓度的同时进行第一共沉淀反应(例如,s12);在降低该反应溶液的ph值和增加该反应溶液中的螯合剂的浓度的同时进行第二共沉淀反应(例如,s14);和在保持该反应溶液的ph值和该反应溶液中的螯合剂的浓度的同时进行第三共沉淀反应(例如,s16)。例如,可以连续且依次地进行第一共沉淀反应至第三共沉淀反应。
[0084]
在一个实施方案中,共沉淀反应可以由第一共沉淀反应至第三共沉淀反应(例如,s12、s14和s16)组成。例如,共沉淀反应可以从第一共沉淀反应开始并以第三共沉淀反应结束。
[0085]
例如,保持反应溶液的ph值可以是指基于反应段(reaction section)中的平均ph值,将在反应期间的ph值偏差保持在5%以下,优选地2.5%以下。
[0086]
例如,保持反应溶液中的螯合剂的浓度可以指基于反应段中的螯合剂的平均浓度,将在反应期间的螯合剂的浓度的偏差保持在10%以下,优选地7.5%以下。
[0087]
在一个实施方案中,当将共沉淀反应的总反应时间限定为1t时,第二共沉淀反应(例如,s14)的反应时间可以为0.001t至0.02t。优选地,基于共沉淀反应的总反应时间1t,第二共沉淀反应的反应时间为0.01t至0.02t。在上述范围内,可以稳定地形成包含三角形形状的一次颗粒的金属氢氧化物颗粒。
[0088]
例如,共沉淀反应的总反应时间(1t)可以是指第一共沉淀反应至第三共沉淀反应的反应时间的总和(例如,s12、s14和s16的总反应时间)。例如,共沉淀反应的总反应时间(1t)可以是指从第一共沉淀反应(例如,s12)开始到第三共沉淀反应(例如,s16)结束时所需要的总时间。
[0089]
例如,第一共沉淀反应开始的时间可以定义为当开始加入金属盐的水溶液时的时间,并且第三共沉淀反应结束的时间可以定义为当金属盐的水溶液的加入结束时的时间。
[0090]
例如,初始颗粒(initial particle)可以通过第一共沉淀反应(例如,s12)形成,并且初始颗粒可以通过第二共沉淀反应(例如,s14)和第三共沉淀反应(例如,s16)生长。例如,初始颗粒可以具有1μm至2μm的直径。
[0091]
在一个实施方案中,在步骤s14中,反应溶液的ph值可以由步骤s12中的ph值降低0.7至2.5。例如,如果步骤s12中的反应溶液的ph值为a,则步骤s14中的反应溶液的ph值可以降低至a-0.7至a-2.5的值。优选地,在步骤s14中,反应溶液的ph可以由步骤s12中的ph值降低1至2。
[0092]
在一个实施方案中,在步骤s14中,基于步骤s12中的螯合剂的浓度,反应溶液中的螯合剂的浓度可以增加至1.2倍至2.5倍的数值。例如,如果步骤s12中的反应溶液中的螯合剂的浓度为b,则可以将步骤s14中的反应溶液中的螯合剂的浓度增加至1.2b至2.5b的值。优选地,在步骤s14中,基于步骤s12中的螯合剂的浓度,可以将反应溶液中的螯合剂的浓度增加至1.5倍至1.75倍的值。
[0093]
例如,在步骤s12中,可以在将反应溶液的ph值保持为11.5至12.5,并且将反应溶液中的螯合剂的浓度保持为3g/l至5g/l的同时进行共沉淀反应。可选地,例如可以将反应溶液的ph值保持为11.7至12.3,并且可以将反应溶液中的螯合剂的浓度的保持为3.5g/l至4.5g/l。
[0094]
例如,在步骤s14中,可以在将反应溶液的ph值降低至10.2至11.0,并且将反应溶液中的螯合剂的浓度增加至6g/l至7g/l的同时,进行共沉淀反应。可选地,例如可以将反应溶液的ph值降低至10.4至10.8。
[0095]
例如,在步骤s16中,可以在将反应溶液的ph值保持为10.2至11.0(即,在步骤s14中降低至的最终数值),并且将反应溶液中的螯合剂的浓度保持为6g/l至7g/l(即,在步骤s14中增加至的最终数值)的同时,进行共沉淀反应。可选地,例如,可以将反应溶液的ph值保持为10.4至10.8。
[0096]
在一个实施方案中,金属氢氧化物颗粒可以具有其中多个一次颗粒聚集的二次颗粒的形式,并且一次颗粒可以包括具有三角形形状的颗粒。
[0097]
在一些实施方案中,基于共沉淀反应的总反应时间(1t),具有三角形形状的颗粒可以在从共沉淀反应开始经过0.6t的时间之前形成。
[0098]
在一个实施方案中,金属氢氧化物颗粒的一次颗粒可以包括具有最大高度为0.5μm以上的三角形形状的颗粒。例如,基于共沉淀反应的总反应时间1t,从共沉淀反应开始的时间(例如,从第一共沉淀反应开始的时间)起经过0.6t的时间之前,从三角形形状的颗粒的形成开始起,共沉淀反应结束时(例如,第三共沉淀反应结束时)的三角形的最大高度可以为0.5μm以上。
[0099]
在一些实施方案中,所获得的金属氢氧化物颗粒的一次颗粒可以包括具有最大高度为1μm以上或2μm以上的三角形形状的颗粒。
[0100]
例如,如果从第一共沉淀反应开始经过0.6t的时间之后开始形成具有三角形形状的颗粒,则在所有共沉淀反应结束之后,三角形难以具有满足上述范围的最大高度。例如,当共沉淀反应结束后的三角形形状的颗粒不具有满足上述范围的最大高度时,三角形可能在金属氢氧化物颗粒的煅烧期间坍塌(collapsed)而成为无定形。
[0101]
在一个实施方案中,金属氢氧化物颗粒的一次颗粒可以包括具有最小内角为45
°
以上大小的三角形形状的颗粒。
[0102]
在一个实施方案中,共沉淀剂可以包括碱性化合物,例如氢氧化钠、碳酸钠等。
[0103]
在一个实施方案中,螯合剂可以包括氨水(例如,nh3h2o)、碳酸铵等。
[0104]
在一个实施方案中,在步骤s16中,可以将反应溶液中的固形物(solid content)的浓度控制在30重量%至55重量%。
[0105]
在一个实施方案中,金属盐可以包括金属硫酸盐、金属硝酸盐、金属乙酸盐、金属氢氧化物、金属碳酸盐及它们的水合物中的至少一种。
[0106]
在一个实施方案中,金属盐可以包括镍(ni)。
[0107]
在一些实施方案中,金属盐可以进一步包括co、mg、sr、ba、b、al、si、mn、ti、zr和w中的至少一种。
[0108]
在一些实施方案中,金属盐中包括的所有金属中的镍的摩尔比可以为0.8以上。
[0109]
在一个实施方案中,在进行共沉淀反应期间(例如,在进行步骤s12、s14和s16期间),可以将反应溶液中的ni
2
的浓度保持在50ppm至100ppm。
[0110]
在共沉淀反应结束后(例如,步骤s16结束后),可以将沉淀物干燥以获得金属氢氧化物颗粒。例如,干燥可以在100℃至150℃的温度范围内进行。
[0111]
在一个实施方案中,金属氢氧化物颗粒可以具有3μm至20μm的粒度(d
50
)。
[0112]
制备锂金属氧化物颗粒的步骤
[0113]
在一个实施方案中,制造正极活性物质的方法可以包括由金属氢氧化物颗粒制备锂金属氧化物颗粒的步骤。
[0114]
在一些实施方案中,制备锂金属氧化物颗粒的步骤可以包括将金属氢氧化物颗粒与锂源混合(例如,s30);和煅烧金属氢氧化物颗粒和锂源的混合物以制备锂金属氧化物颗粒(例如,s40)。
[0115]
在一个实施方案中,该锂金属氧化物颗粒具有其中多个一次颗粒聚集的二次颗粒形式,并且一次颗粒可以包含具有最小内角为45
°
以上,并且最大高度为0.5μm以上的尺寸的三角形形状的颗粒。
[0116]
在一个实施方案中,锂源可以是锂盐。在一些实施方案中,锂盐可以包括碳酸锂、硝酸锂、乙酸锂、氧化锂、氢氧化锂等。
[0117]
在一个实施方案中,在步骤s40中,煅烧可以在670℃至785℃的温度范围内进行。在这种情况下,可以防止三角形形状的一次颗粒坍塌为无定形。
[0118]
例如,在步骤s40中,可以将煅烧产物冷却至室温,然后进行研磨和分级(classification),以得到锂金属氧化物颗粒。
[0119]
在一个实施方案中,锂金属氧化物颗粒可以具有3μm至20μm的粒度(d
50
)。
[0120]
上述关于锂金属氧化物颗粒的内容可以直接应用于该步骤,因此将不再详细描述。
[0121]
在一个实施方案中,在步骤s40之后,该方法可以进一步包括在锂金属氧化物颗粒中掺杂金属元素和/或类金属元素(metalloid element)。
[0122]
在一个实施方案中,在步骤s40之后,该方法可以进一步包括用金属元素和/或类金属元素涂覆锂金属氧化物颗粒的表面。
[0123]
例如,金属元素(或类金属元素)可以包括al、ti、ba、zr、si、b、mg、sr、w、la等。
[0124]
可以通过本领域已知的方法进行掺杂和涂覆,因此本文将不再进行详细描述。
[0125]
锂二次电池
[0126]
图1为示意性地示出根据示例性实施方案的锂二次电池的横截面图。
[0127]
参照图1,锂二次电池可以包括正极100、负极130和介于正极100和负极130之间的隔膜140。
[0128]
正极100可以包括正极集流体105和正极集流体105上的正极活性物质层110。
[0129]
正极活性物质层110可以包括正极活性物质,并且如必要,还可以包括正极粘合剂和导电材料。
[0130]
例如,可以通过在分散介质中将正极活性物质、正极粘合剂和导电材料等混合并搅拌来制备正极浆料,然后用该正极浆料涂覆正极集流体105,随后对其进行干燥并辊压来制备正极100。
[0131]
正极集流体105可以包括例如不锈钢、镍、铝、钛、铜或它们的合金,并且优选地包括铝或铝合金。
[0132]
正极活性物质可以包括本发明的上述正极活性物质。
[0133]
正极粘合剂可以包括例如有机粘合剂,例如聚偏二氟乙烯(pvdf)、聚偏二氟乙烯-六氟丙烯共聚物(pvdf-co-hfp)、聚丙烯腈、聚甲基丙烯酸甲酯等,或者水性粘合剂如丁苯橡胶(sbr)。此外,正极粘合剂可以与增稠剂如羧甲基纤维素(cmc)一起使用。
[0134]
导电材料可以包括例如碳基导电材料,例如石墨、炭黑、石墨烯或碳纳米管,和/或例如锡的金属基导电材料、氧化锡、氧化钛,或例如lasrcoo3和lasrmno3的钙钛矿材料。
[0135]
负极130可以包括负极集流体125和负极集流体125上的负极活性物质层120。
[0136]
负极活性物质层120可以包括负极活性物质,并且如必要,还可以包括负极粘合剂和导电材料。
[0137]
例如,可以通过在溶剂中将负极活性物质、负极粘合剂和导电材料等混合并搅拌来制备负极浆料,然后用该负极浆料涂覆负极集流体125,随后对其进行干燥和辊压来制备负极130。
[0138]
负极集流体125可以包括例如金、不锈钢、镍、铝、钛、铜或它们的合金,并且优选地包括铜或铜合金。
[0139]
负极活性物质可以是能够使锂离子嵌入和脱嵌的物质。负极活性物质可以包括例如碳基物质,例如结晶碳、无定形碳、碳复合物质或碳纤维等;硅基物质;锂合金等。
[0140]
无定形碳可以是例如硬碳、焦炭、在1500℃以下煅烧过的中间相炭微球(mcmb)、中间相沥青基碳纤维(mpcf)等。结晶碳可以是例如天然石墨、石墨焦炭、石墨化mcmb、石墨化mpcf等。
[0141]
硅基物质可以包括例如si、sio
x
(0《x《2)、si/c、sio/c、si-金属等。
[0142]
锂合金可以包括例如金属元素,例如铝、锌、铋、镉、锑、硅、铅、锡、镓、铟等。
[0143]
负极粘合剂和导电材料可以与上述正极粘合剂和导电材料基本相同或相似。负极粘合剂可以是例如水性粘合剂如丁苯橡胶(sbr)以与碳基活性物质相容(consistency),并且可以与增稠剂如羧甲基纤维素(cmc)一起使用。
[0144]
隔膜140可以介于正极100和负极130之间。在一些实施方案中,负极130的面积(例如,与隔膜140的接触面积)可以大于正极100的面积。因此,从正极100产生的锂离子可以顺利地(smoothly)移动到负极130,而不会在中间沉淀。
[0145]
隔膜140可以包括由聚烯烃聚合物如乙烯均聚物、丙烯均聚物、乙烯/丁烯共聚物、乙烯/己烯共聚物、乙烯/甲基丙烯酸酯共聚物等制成的多孔聚合物膜。
[0146]
隔膜140可以包括由具有高熔点的玻璃纤维、聚对苯二甲酸乙二醇酯纤维等制成的非织造织物。
[0147]
可以通过包括正极100、负极130和隔膜140来形成电极单元。此外,可以将多个电极单元层叠以形成电极组件150。例如,电极组件150可以通过隔膜140的卷绕(winding)、层叠(lamination)、z-折叠(z-folding)等来形成。
[0148]
电极组件可以与电解液一起容纳在外壳160中,以形成锂二次电池。
[0149]
电解液可以包括例如锂盐,并且锂盐可以与有机溶剂一起以非水电解液的状态容纳在外壳中。
[0150]
锂盐可以由例如li
x-表示。
[0151]
锂盐的阴离子(x-)可以是例如,选自f-、cl-、br-、i-、no
3-、n(cn)
2-、bf
4-、clo
4-、pf
6-、(cf3)2pf
4-、(cf3)3pf
3-、(cf3)4pf
2-、(cf3)5pf-、(cf3)6p-、cf3so
3-、cf3cf2so
3-、(cf3so2)2n-、(fso2)2n-、cf3cf2(cf3)2co-、(cf3so2)2ch-、(sf5)3c-、(cf3so2)3c-、cf3(cf2)7so
3-、cf3co
2-、ch3co
2-、scn-和(cf3cf2so2)2n-等中的任何一种。在一些实施方案中,锂盐可以包括libf4和lipf6中的至少一种。
[0152]
有机溶剂可以包括,例如,选自碳酸乙烯酯(ec)、碳酸丙烯酯(pc)、碳酸二甲酯(dmc)、碳酸二乙酯(dec)、碳酸甲乙酯(emc)、碳酸甲丙酯、碳酸二丙酯、二甲基亚砜、乙腈、二甲氧基乙烷、二乙氧基乙烷、碳酸亚乙烯酯、环丁砜、γ-丁内酯、亚硫酸丙烯酯、四氢呋喃等中的任意一种或多种。
[0153]
可以将锂二次电池制造成例如圆柱形、方形、软包形或硬币形。
[0154]
在下文中,将描述本发明的优选实施例和比较例。然而,以下实施例仅是本发明的优选实施例,并且本发明不限于此。
[0155]
[实施例1]
[0156]
(1)金属氢氧化物颗粒的制备
[0157]
在将内部温度保持在60℃的同时,将1.8m3的水加入配备有搅拌器和浓缩器
(concentrator)并且具有2m3容积的间歇式反应器(batch reactor)中,通过用氮气鼓泡4小时以上的时间来除去内部溶解氧。
[0158]
将25重量%的naoh水溶液和28重量%的氨水加入反应器中以制备ph为12.0且nh3浓度为4g/l的水溶液。
[0159]
在以300rpm的速度搅拌反应器中的水溶液的同时,将2.0m金属硫酸盐水溶液(ni:co:mn的摩尔比=88:9:3)、25重量%naoh水溶液和28重量%的氨水加入反应器中,同时用n2鼓泡以制备反应溶液。
[0160]
在将反应溶液的ph值保持在11.9至12.1,并将nh3的浓度保持在4g/l的同时,进行第一共沉淀反应2小时,形成初始颗粒。
[0161]
此后,将反应溶液的搅拌速度降低至240rpm,然后在控制naoh水溶液和nh3的加入量的同时进行第二共沉淀反应。
[0162]
更具体地,将反应溶液的ph值降低至10.4至10.8,并且将反应溶液中的nh3浓度增加至6g/l至7g/l,然后进行第二共沉淀反应以使初始颗粒生长。当共沉淀反应的总反应时间(320小时)为1t时,进行第二共沉淀反应的时间为约0.019t(6小时)。
[0163]
接下来,将反应溶液的ph(10.4至10.8)和反应溶液中的nh3浓度(6g/l至7g/l)保持到共沉淀反应结束,进行第三共沉淀反应。
[0164]
在共沉淀反应期间,将金属盐的水溶液连续加入反应器,通过反应器中配备的浓缩器将滤液连续排放至反应器外,并且将形成的固形物(solid content)保留在反应器中的同时将反应进行320小时。
[0165]
搅拌速度逐渐降低至120rpm,直到共沉淀反应结束,并且将反应溶液的ph值和反应溶液中的nh3的浓度保持在上述范围内。此外,将反应溶液中的ni
2
的浓度保持在50ppm至100ppm。
[0166]
在共沉淀反应期间,为了将反应溶液中的固形物的浓度保持在30重量%至55重量%,从共沉淀反应开始经过240小时的时间时,使反应溶液分流一次(branched once)。
[0167]
共沉淀反应结束后,确认反应器中的固形物的浓度为53重量%。将共沉淀结束的反应溶液依次用12.5重量%的naoh水溶液和纯水洗涤,然后对洗涤后的反应溶液进行过滤。
[0168]
将滤液在130℃下干燥12小时,获得粒径(d
50
)为约11.0μm的金属氢氧化物颗粒ni
0.88
co
0.09
mn
0.03
(oh)2。
[0169]
当将共沉淀反应的总反应时间(320小时)限定为1t时,确认在经过相当于0.53t的170小时的时间形成了三角形形状的一次颗粒。
[0170]
图6a为从共沉淀反应开始经过0.55t的时间时,在金属氢氧化物颗粒的表面拍摄的扫描电子显微镜(sem)图像。参照图6a,可以确认在金属氢氧化物颗粒的表面上观察到了三角形形状的一次颗粒。
[0171]
(2)锂金属氧化物颗粒的制备
[0172]
将10kg的金属氢氧化物颗粒和氢氧化锂(lioh
·
h2o)以1.01的li/m摩尔比加入高速混合器中,然后混合。
[0173]
将制得的混合物加入陶瓷坩埚中,并且放入煅烧炉(则武(noritake),rhk模拟器(simulator)),然后以2.5℃/分钟的加热速率将混合物加热至730℃,并在730℃保持10小
时。在加热和保持温度期间,使氧气以40ml/分钟的流速连续通过。
[0174]
煅烧结束后,将煅烧产物自然冷却至室温,随后进行研磨和分级以获得粒径(d
50
)为约11.0μm的锂金属氧化物颗粒lini
0.88
co
0.09
mn
0.03
o2。
[0175]
[实施例2]
[0176]
除了在制备锂金属氧化物颗粒时将煅烧温度改变为740℃,通过进行与实施例1中所述相同的步骤获得粒径(d
50
)为约11.1μm的锂金属氧化物颗粒lini
0.88
co
0.09
mn
0.03
o2。
[0177]
[实施例3]
[0178]
除了在制备锂金属氧化物颗粒时将煅烧温度改变为750℃,通过进行与实施例1中所述相同的步骤获得粒径(d
50
)为约11.3μm的锂金属氧化物颗粒lini
0.88
co
0.09
mn
0.03
o2。
[0179]
[比较例1]
[0180]
(1)金属氢氧化物颗粒的制备
[0181]
在将内部温度保持在55℃的同时,将1.8m3的水加入配备有搅拌器和浓缩器并且具有2m3容积的间歇式反应器中,通过用氮气鼓泡4小时以上的时间除去内部溶解氧。
[0182]
将25重量%的naoh的水溶液和28重量%的氨水加入反应器中以制备ph值为12.1且nh3浓度为27g/l的水溶液。
[0183]
在以300rpm的速度搅拌反应器中的水溶液的同时,将2.0m金属硫酸盐水溶液(ni:co:mn的摩尔比=88:9:3)、25重量%naoh水溶液和28重量%的氨水加入反应器中,同时用n2鼓泡以制备反应溶液。
[0184]
在将反应溶液的ph值保持在11.9至12.1,并且将nh3的浓度保持在24g/l的同时,进行用于形成初始颗粒的反应2小时。
[0185]
此后,将反应溶液的搅拌速度降低至240rpm,然后进行共沉淀反应。将反应溶液的搅拌速度逐渐降低至200rpm,直到共沉淀反应结束。另外,将反应溶液的ph值逐渐降低并保持为11.4。此外,将反应溶液中的ni
2
的浓度保持在50ppm至100ppm,并且将nh3的浓度保持在24g/l至27g/l。
[0186]
在反应期间,通过反应器中配备的浓缩器将滤液连续排放至反应器外,并且将形成的固形物保留在反应器中的同时将反应继续进行65小时。
[0187]
共沉淀反应结束后,确认反应器中的固形物的浓度为27重量%。将共沉淀结束的反应溶液依次用12.5重量%的naoh水溶液和纯水洗涤,过滤,并且在130℃下干燥12小时以获得粒径(d
50
)为约17μm的金属氢氧化物颗粒ni
0.88
co
0.09
mn
0.03
(oh)2。
[0188]
(2)锂金属氧化物颗粒的制备
[0189]
将10kg的金属氢氧化物颗粒和氢氧化锂(lioh
·
h2o)以1.01的li/m摩尔比加入高速混合器中,然后混合。
[0190]
将制得的混合物加入陶瓷坩埚中,并且放入煅烧炉(则武(noritake),rhk模拟器),然后以2.5℃/分钟的加热速率将混合物加热至730℃,并在730℃保持10小时。在加热和保持温度期间,使氧气以40ml/分钟的流速连续通过。
[0191]
煅烧结束后,将煅烧产物自然冷却至室温,随后进行研磨和分级以获得粒径(d
50
)为约17μm的锂金属氧化物颗粒lini
0.88
co
0.09
mn
0.03
o2。
[0192]
[比较例2]
[0193]
(1)金属氢氧化物颗粒的制备
[0194]
在金属盐的水溶液中,niso4、coso4和mnso4分别以88:9:3的摩尔比混合,并使用通过用氮气(n2)鼓泡24小时去除溶解氧的蒸馏水。
[0195]
将金属盐的水溶液加入到50℃、容积为2m3的连续搅拌釜反应器(continuous stirred-tank reactor,cstr)中,并且使用naoh作为沉淀剂和nh3h2o作为螯合剂连续进行共沉淀反应。
[0196]
从共沉淀反应开始经过50小时后,在接收器中接收从反应器连续溢出的反应溶液10小时。
[0197]
将所获得的反应溶液依次用12.5重量%naoh水溶液和纯水洗涤、过滤,并且在130℃下干燥12小时以获得粒径(d
50
)为约11μm的金属氢氧化物颗粒ni
0.88
co
0.09
mn
0.03
(oh)2。
[0198]
(2)锂金属氧化物的制备
[0199]
将10kg的金属氢氧化物颗粒和氢氧化锂(lioh
·
h2o)以1.01的li/m摩尔比加入高速混合器中,然后混合。
[0200]
将制得的混合物投入煅烧炉(则武(noritake),rhk模拟器),然后以2℃/分钟的加热速率将混合物加热至730℃,并在730℃保持10小时。在加热和保持温度期间,使氧气以10ml/分钟的流速连续通过。
[0201]
煅烧结束后,将煅烧产物自然冷却至室温,随后进行研磨和分级,获得粒径(d
50
)为约11.0μm的锂金属氧化物颗粒(lini
0.8
co
0.1
mn
0.1
o2)。
[0202]
[比较例3]
[0203]
(1)金属氢氧化物颗粒的制备
[0204]
将1.8m3的水加入配备有搅拌器和浓缩器并且具有2m3容积的间歇式反应器中,并且在将内部温度保持在60℃的同时,通过用氮气鼓泡4小时以上的时间来除去内部溶解氧。
[0205]
将25重量%的naoh水溶液和28重量%的氨水加入反应器中以制备ph值为12.0且nh3的浓度为4g/l的水溶液。
[0206]
在以300rpm的速度搅拌反应器中的水溶液的同时,将2.0m金属硫酸盐的水溶液(ni:co:mn的摩尔比=88:9:3)、25重量%的naoh水溶液和28重量%的氨水加入反应器中,同时用n2鼓泡以制备反应溶液。
[0207]
在将反应溶液的ph值保持在11.9至12.1,并且将nh3的浓度保持在4g/l的同时,进行2小时的第一共沉淀反应以形成初始颗粒。
[0208]
然后,将反应溶液的搅拌速度降低至240rpm,然后控制naoh水溶液和nh3的加入量。
[0209]
更具体地,将反应溶液的ph值逐渐地降低至10.8,并且将反应溶液中的nh3的浓度逐渐增加至6g/l直到共沉淀反应结束,并且进行第二共沉淀反应以使初始颗粒生长。
[0210]
另外,将反应溶液的搅拌速度逐渐降低至120rpm,直到共沉淀反应的结束,并且将反应溶液中ni
2
的浓度保持在50ppm至100ppm。
[0211]
在共沉淀反应期间,将金属盐的水溶液连续加入反应器,通过反应器中配备的浓缩器将滤液连续排放至反应器外,并且将形成的固形物保留在反应器中的同时将反应进行320小时。
[0212]
在共沉淀反应期间,为了将反应溶液中的固形物的浓度保持在30重量%至55重量%,从共沉淀反应开始经过250小时的时间时,使反应溶液分流一次(branched once)。
[0213]
共沉淀反应结束后,确认反应器中的固形物的浓度为51重量%。将共沉淀结束的反应溶液依次用12.5重量%naoh水溶液和纯水洗涤、过滤,并且在130℃下干燥12小时,获得粒径(d
50
)为约11.0μm的金属氢氧化物颗粒ni
0.88
co
0.09
mn
0.03
(oh)2。
[0214]
当将共沉淀反应的总反应时间(300小时)限定为1t时,确认在经过相当于0.7t的210小时的时间形成了三角形形状的一次颗粒。
[0215]
图6b为从共沉淀反应开始经过0.55t的时间时,在金属氢氧化物颗粒的表面拍摄的扫描电子显微镜(sem)图像。参照图6b,可见在金属氢氧化物颗粒的表面上没有观察到三角形形状的一次颗粒。
[0216]
(2)锂金属氧化物的制备
[0217]
将10kg的金属氢氧化物颗粒和氢氧化锂(lioh
·
h2o)以1.01的li/m摩尔比加入高速混合器中,然后混合。
[0218]
将制得的混合物加入陶瓷坩埚中,并且放入煅烧炉(则武(noritake),rhk模拟器),然后以2.5℃/分钟的加热速率将混合物加热至730℃,并在730℃保持10小时。在加热和保持温度期间,使氧气以40ml/分钟的流速连续通过。
[0219]
煅烧结束后,将煅烧产物自然冷却至室温,随后进行研磨和分级,获得粒径(d
50
)为约11μm的锂金属氧化物颗粒lini
0.88
co
0.09
mn
0.03
o2。
[0220]
实验例1:表面结构分析
[0221]
(1)金属氢氧化物颗粒和锂金属氧化物颗粒中的一次颗粒形状的观察
[0222]
使用扫描电子显微镜(sem)获得实施例1和比较例1-比较例3的金属氢氧化物颗粒的表面sem图像;和实施例1-实施例3和比较例1-比较例3的锂金属氧化物颗粒表面sem图像。
[0223]
图3a至图3d分别为实施例1和比较例1-比较例3的金属氢氧化物颗粒表面上拍摄的扫描电子显微镜(sem)图像;图4a至图4d分别为实施例1-实施例3和比较例3的锂金属氧化物颗粒表面上拍摄的扫描电子显微镜(sem)图像;图5a和图5b分别为比较例1和比较例2的锂金属氧化物颗粒的表面上拍摄的扫描电子显微镜(sem)图像。
[0224]
参照图3a和图3d,可见在实施例1和比较例3的金属氢氧化物颗粒的表面上观察到了三角形形状的一次颗粒。另一方面,参照图3b和图3c,可见在比较例1和比较例2的金属氢氧化物颗粒的表面上观察到了针状的一次颗粒。
[0225]
参照图4a至图4c,可见在实施例的锂金属氧化物颗粒的表面上观察到了三角形形状的一次颗粒。即,在实施例的锂金属氧化物颗粒中,在金属氧化物颗粒中观察到的三角形形状的一次颗粒,即使在煅烧后也可以保持良好。另一方面,参照图4d可以确认,在比较例3的锂金属氧化物颗粒中的三角形形状坍塌为无定形。
[0226]
(2)锂金属氧化物颗粒的三角形形状的一次颗粒的评价
[0227]
用扫描电子显微镜(sem)测量实施例和比较例的锂金属氧化物颗粒。使用获得的sem图像测量三角形的最大高度和最小内角。
[0228]
1)最大高度
[0229]
当从一个顶点向相对侧向下绘制垂线时将该垂线的长度定义为高度。垂线的长度是相对于每个顶点和相对侧而测量的,并且将垂线的测得长度的最长长度定义为最大高度。测得的最大高度描述于下表1中。
[0230]
2)最小内角
[0231]
测量了三角形的最小内角,并描述于下表1中。
[0232]
实验例2:硬币电池的制造与评价
[0233]
通过将实施例和比较例的锂金属氧化物、作为导电材料的炭黑和作为粘合剂的聚偏二氟乙烯(pvdf)以92:5:3的重量比混合来制备浆料。
[0234]
将制得的浆料涂覆在厚度为15μm的铝薄膜上,并在130℃下真空干燥以制备正极。然后,使用正极、作为对电极(counter electrode)的锂箔和作为隔膜的厚度为21μm的多孔聚乙烯膜形成电极组件。
[0235]
使用电极组件和1.0m的lipf6电解液(其中碳酸乙烯酯和碳酸甲乙酯以3:7的体积比混合的溶剂),根据通常已知的制造方法,制造具有硬币半电池形状(coin half-cell shape)的二次电池。
[0236]
(1)初始充电容量和初始放电容量的测量
[0237]
对于实施例和比较例的二次电池,进行一次cc/cv充电(0.1c 4.3v 0.05c截止)和cc放电(0.1c 3.0v截止)以测量初始充电容量和初始放电容量,并且其结果描述于下表2中。
[0238]
(2)初始效率的测量
[0239]
通过将根据上述(1)测得的初始放电量除以初始充电量而获得的百分比值来测量初始效率。
[0240]
初始效率=(初始放电容量/初始充电容量)
×
100(%)
[0241]
(3)室温寿命特性(室温容量保持率)的测量
[0242]
对于实施例和比较例的二次电池,在室温(25℃)下重复进行300次cc/cv充电(0.5c 4.3v 0.05c截止)和cc放电(1.0c 3.0v截止)。
[0243]
通过将第300次测得的放电容量除以上述(1)中测得的初始放电容量获得的百分比值来计算室温容量保持率。
[0244]
室温容量保持率=(第300次的放电容量/初始放电容量)
×
100(%)
[0245]
计算得出的室温容量保持率描述于下表2中。
[0246]
(4)高温储存性能(高温容量保持率)的评价
[0247]
对于实施例和比较例的二次电池,在高温(45℃)下重复进行100次cc/cv充电(0.33c 4.3v 0.05c截止)和cc放电(0.33c 3.0v截止)。
[0248]
通过将第100次测得的放电容量除以上述(1)中测得的初始放电容量获得的百分比值来计算高温容量保持率。
[0249]
高温容量保持率=(第100次的放电容量/初始放电容量)
×
100(%)
[0250]
计算得出的高温容量保持率描述于下表2中。
[0251]
[表1]
[0252][0253]
在表1中,
○
表示存在三角形形状的一次颗粒;
×
表示不存在三角形形状的一次颗粒。
[0254]
[表2]
[0255][0256][0257]
参照上面的表1和表2,可见实施例的二次电池表现出改善的室温容量保持率和高温容量保持率。
[0258]
比较例1和比较例2的二次电池不包含三角形形状的一次颗粒,而是使用了包含针状一次颗粒的锂金属氧化物颗粒作为正极活性物质。与实施例相比,比较例1和比较例2的二次电池在室温容量保持率方面表现出约10%的劣化值(inferior value),并且在高温容量保持率方面表现出约20%的劣化值。
[0259]
比较例3的二次电池使用了包含其中在煅烧期间三角形形状坍塌的无定形一次颗粒的锂金属氧化物颗粒作为正极活性物质。与实施例相比,比较例3的二次电池表现出较差的室温容量保持率和高温容量保持率。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。