1.本发明涉及两亲性分子膜领域,具体涉及一种两亲性分子层的制备方法及装置。
背景技术:
2.纳米孔蛋白需要在一个磷脂或是高分子形成的薄膜,如两亲性分子层(也即两亲性分子膜)上实现稳定得嵌入才可以使待检测的dna序列通过,以达到检测dna序列的目的。然而,目前的一些用于制备两亲性分子层的制备装置与相应的方法在应用上仍存在一些问题。
3.现有的成膜方法主要有折叠双层形成法(montal&mueller的方法),浸尖法,涂布法,膜片钳法和油包水微滴界面法等等。以上方法如折叠双层法、浸尖法、涂布双层法等,往往初次所形成的膜较厚,需要进行薄化处理,例如通过有机溶剂挥发,或通过物理涂抹铺展,或通过空气气压挤压等。薄化处理对于膜厚的控制十分重要,但是操作过程复杂,且薄化步骤难以控制(例如,难以保证物理涂抹过程中能够均匀铺展)。而微滴界面法则往往需要逐个形成微滴,并且需要对微滴的体积、位置等进行控制,操作具有一定难度,且当需要形成多个两亲性分子层时,需要首先形成多个微滴,操作繁琐。同时,现有的成膜方法通常都涉及到对制备装置的预处理,如氟等离子体处理,硅烷化处理等等,这些预处理操作都需要用的高危化学品,并需要在建设成本高昂,维护费用高昂的实验室内进行。对操作人员的生命安全和周围环境存在潜在威胁。此外,预处理还需要对所使用到的涂料用量进行精确计算,涂料过多过少都会影响试验效果。而两亲性分子膜的制备装置通常都是小型芯片,其内部结构(如微孔等)尺寸微小,因此所选的涂料用量也非常少,在微小的结构上涂抹极少量的涂料在操作上并不简单,因此,在涂抹过程中也难以避免出现涂抹过多、过少的问题。
4.例如,如申请号为201480056839.5的中国发明专利,该发明公开了一种用于生物芯片,且该发明还公开了该生物芯片的成膜方法,成膜方法包括步骤:将包含脂质分子(也即两亲性分子)的液体加入芯片表面,然后通过气泡隔开所述液体,使得脂质分子分布在芯片表面上,并且通过气泡使得脂质变薄。但是气泡生成往往需要手动操作控制(如通过移液枪制备出气泡),这个过程难以进行自动化控制,而手动操作难以控制气泡的大小,且难以保证气泡的形态稳定,因此该方法的重复性也较差。并且也该方法也需要进行预处理。
5.再例如,申请号为cn200880126160.3的中国发明,该发明公开了一种形成分隔两个体积的水溶液的层的方法,该方法通过使包含两亲性分子的水溶液流过主体以覆盖凹槽(也即微孔),使得水溶液可以跨越凹槽形成两亲性分子,虽然使得水溶液流过凹槽以形成两亲性分子这一技术容易实现,但是所制备的膜较厚,需要后续进行薄化处理,且该方法也涉及到预处理步骤。
6.此外,市面上现有的制备装置也存在一些问题,例如,现有的一些制备装置为了实现量产,并保证槽体(即用于添加溶液样品的流道)的一致性(即减少生产误差),往往选用铸造工艺(即通过模具)来制作槽体,因此,为了能够满足更多的实验需求,通常将槽体内部结构设置得较大,由此,当一些实验仅需要少量溶液样品时,将会对样品造成不必要的浪
费。而如果要避免样品的浪费,则需要针对不同实验需求(不同的测序试验需要不同体积大小的槽体)制备不同尺寸的样品槽,由此需要针对不同尺寸的样品槽制备出相应的模具(也即每次生产都需要开模),这在工业生产过程中成本较高。
技术实现要素:
7.为了部分地解决或部分缓解上述技术问题,本发明提供了一种两亲性分子层的制备方法,包括:
8.s1提供用于制备两亲性分子层的制备装置,所述制备装置内设有用于为所述两亲性分子层提供成长平台的至少一个微孔,以及能够使得溶液流经所述微孔的第一通道和第二通道,且所述微孔的第一端和第二端分别与所述第一通道和所述第二通道连通,其中,所述第一通道的横截面呈方形或类方形设置;
9.s2向所述第二通道内加入第一极性溶液,使得所述第一极性溶液进入至少一个所述微孔内;
10.s3依次向所述第一通道内加入膜溶液和第二极性溶液,使得所述膜溶液在所述第一通道内形成弯月面;
11.s4基于预设速度向所述第一通道内加入第二极性溶液,使得所述第二极性溶液推动所述膜溶液移动并流经所述微孔,所述膜溶液在所述微孔处形成两亲性分子层;
12.其中,所述第一通道内表面的接触角为大约65
°‑
大约120
°
。
13.在一些实施例中,所述膜溶液包括:非极性溶液,以及两亲性分子。
14.在一些实施例中,所述两亲性分子可选地包括:磷脂,或高分子,或磷脂和高分子的混合物。
15.在一些实施例中,所述第一极性溶液包括:电解质,和/或聚电解质。
16.在一些实施例中,所述第一极性溶液包括:氧化还原对,和/或可以被部分氧化或还原以提供氧化还原对的氧化还原对的组合。
17.在一些实施例中,所述第一极性溶液包括:交联的琼脂糖凝胶,和/或交联的海藻酸钠凝胶。
18.在一些实施例中,所述第一极性溶液包括:用于调节ph的缓冲剂。
19.在一些实施例中,所述第二极性溶液包括:电解质,和/或聚电解质。
20.在一些实施例中,所述第二极性溶液包括:氧化还原对,和/或可以被部分氧化或还原以提供氧化还原对的氧化还原对的组合。
21.在一些实施例中,所述第二极性溶液包括:交联的琼脂糖凝胶,和/或交联的海藻酸钠凝胶。
22.在一些实施例中,所述第二极性溶液包括:用于调节ph的缓冲剂。
23.在一些实施例中,在s3中,所述第二极性溶液的注入速度为大约5μl/min到大约10μl/min;
24.在一些实施例中,,在s4中,所述第二极性溶液的所述预设速度为大约10μl/min到大约20μl/min。
25.在一些实施例中,该方法还包括步骤:
26.分别向所述第一通道和所述第二通道插入第一电极和第二电极,并向第一通道
和/或第二通道内加入蛋白溶液,所述蛋白溶液包括:纳米孔蛋白;
27.通过第一、第二电极施加电压向所述两亲性分子层插入纳米孔蛋白。
28.本发明还提供了一种两亲性分子层的制备装置,包括:用于为所述两亲性分子层提供成长平台的微孔,以及能够使得溶液流经所述微孔的第一通道和第二通道,且所述微孔的第一端和第二端分别与所述第一通道和所述第二通道连通;
29.其中,所述第一通道的横截面呈方形或类方形设置,且所述第一通道的内表面材料可选地为:聚甲醛、聚四氟乙烯、聚甲基丙烯酸甲酯、环氧树脂、聚碳酸酯。
30.在一些实施例中,所述第一通道包括:第一流道,所述制备装置包括:
31.第一结构层,所述第一流道设置在所述第一结构层的第一表面,且所述第一流道的两端分别设有第一开口和第二开口,其中,所述第一开口用于加样,所述第二开口用于出样;
32.第二结构层,所述第二通道设置在所述第二结构层的第一表面上,且所述第二通道上设有第三开口,所述第三开口用于加样;
33.第三结构层,至少一个所述微孔设置所述第三结构层上;
34.其中,第一、三、二结构层依次紧密连接,使得所述第一流道与所述第二结构层的第一表面相配合形成供溶液流动的第一通道,所述微孔的第一端和第二端分别与所述第一通道和所述第二通道连通。
35.在一些实施例中,所述第三结构层的第一表面上还设有凹槽,所述微孔设置在所述凹槽上,当第一、三结构层紧密连接时,所述凹槽与所述第一流道相配合共同构成可供溶液流动的第一通道。
36.在一些实施例中,所述微孔的内径在100微米到200微米之间。
37.在一些实施例中,所述第一开口和/或所述第二开口呈上大下小的设置。有益技术效果:
38.本发明提供了一种用于制备两亲性分子层(或两亲性分子膜,也简称“膜”)的制备方法(即成膜方法)及制备装置。具体地,本发明提出了一种新的成膜方法,即使得膜溶液在第一通道内形成弯月面,并通过极性溶液(如第二极性溶液)推动弯月面,从而使得弯月面能够在第一通道内移动并经过微孔,然后在相应的微孔上形成两亲性分子层(膜)。
39.具体地,本发明提出的制备装置选用了具有一定疏水性的材料,即该制备装置内的第一通道内表面的材料的接触角为大约65
°‑
120
°
,使得加入到第一通道内的膜溶液能够在第一通道内表面、极性溶液(第二极性溶液)以及第一通道内的空气的共同作用下,形成弯月面。其中,第一通道的横截面优选地呈方形或类方形的设置,此时,第一通道对膜溶液(或者说膜溶液所形成的弯月面)的移动会产生一定的阻力,使得膜溶液在第一通道内的移动速度不会过快,且膜溶液上各个位置的移动速度相对均匀(或者说,各个位置的流动速度的差别对弯月面的稳定性影响不大),使得弯月面能够在移动过程中能够保持稳定的形态。
40.通过极性溶液推动弯月面(即膜溶液)在微孔处成膜的成膜方式,可以对膜溶液的移动速率进行较为精准的控制(例如,通过移液枪或注射泵等对极性溶液的注入速度进行控制,从而对膜溶液的移动速度进行控制),从而使得膜溶液在微孔处的停留时间可控,避免膜溶液在微孔区域停留过久而形成厚的膜,或者在微孔区域移动过快而没有成功形成膜。因此,本发明能够通过对膜溶液的移动速度进行较为精准的控制,从而直接制成膜厚符
合使用要求的两亲性分子层,而无需在成膜后对膜进行薄化处理(如高压击穿,多次成膜)。换句话说,本发明的成膜方法可控性较好(如相较于现有技术的气泡挤压的方式),可以一次成膜。
41.因此,在实际应用场景中,当膜溶液的浓度、移动速度等参数选定后(如通过预实验,或通过工作人员的操作经验确定),可以基于相同的实验条件和参数进行多次实验,且多次实验所得结果(如成膜情况)差别很小,也即是本方法的重复性较好。换句话说,本发明所提供的方法可以避免或减少工作人员的手动操作对实验操作的影响,以避免或减少操作过程中的不可控因素(即本方法可控性更好),从而具有较好的可重复性。
42.并且,由于制备装置的第一通道内表面以及微孔内表面选用了具有一定疏水性的材料(如聚甲醛),本发明提出的成膜方法无需进行预处理,成膜方法更加简单,且操作过程中对工作人员的安全性更有保障(不涉及到危险物品的操作与使用)。
43.进一步地,对极性溶液的注入速度的控制可以通过注射泵(或其他能够控制溶液注入速度的装置)来实现,且注射泵可以通过电子设备(如计算机等)进行自动化控制(即本发明所提出的成膜方法可以实现自动化控制),从而可以进一步地减少工作人员的手动操作步骤,相应地也避免了工作人员手动操作可能造成的误差,以进一步地保证了成膜的稳定性与均一性。
44.本发明所提供成膜方法以及装置能够应用于实验室中的多种检测需求(如适用于科研单位、商业检测公司等不同的应用场景),进一步地,本发明所提出的成膜方法以及装置优选地适用于数据量少的应用场景(例如,一次性只需要形成少量甚至一个两亲性分子层的试验研发阶段)。
45.可以理解的是,本发明所提供的方法及装置可以与现有的自动化控制相配合,以实现流程的自动化,从而进一步地对操作流程进行精准控制,以提高实验结果的准确性和可靠性。但是,当对数据量需求较少时(如仅需要一个或少个两亲性分子层时),自动化操作的使用成本相对较高。此时,综合考虑时间与成本,手动操作更加适用于实际需求。而本发明所提供的方法流程简单,可以通过控制膜溶液的移动速度一次成膜(具有较好的可控性),且无需对装置进行预处理,也无需对膜进行薄化处理,既降低了操作难度,也减少了成膜耗时。因此,即使通过工作人员手动操作全程,也能制备到厚度适宜的薄膜,并且能够达到与自动化控制相同或相近的技术效果。
46.进一步地,与现有技术不同的是,本发明的制备装置在微孔的两端均设有用于通入溶液的通道(也即第一通道和第二通道)。因此,本发明的制备装置可以在微孔的两侧灵活的插入电极,而无需在微孔处预设电极(现有技术中,需要在小型的芯片上加工设置电极,生产工艺较为复杂),制备装置的生产工艺更简单,生产成本更低。同时,在微孔的两端分别设有第一通道和第二通道,更利于对装置内部(如微孔)以及电极进行清洁,例如,分别向第一通道、第二通道通入清洁液即能实现对微孔的第一端与第二端的清洁,从而实现对装置内部的清洁维护,提高装置的使用寿命(同时避免清洁不全面影响后续实验)。
附图说明
47.为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作一简单地介绍。在所有附图中,类似的元件或部分一般
由类似的附图标记标识。附图中,各元件或部分并不一定按照实际的比例绘制。显而易见地,下面描述中的附图是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动性的前提下,还可以根据这些附图获得其它的附图。
48.图1是本发明一示例性实施例中的制备装置的俯视图;
49.图2示出了本发明一示例性实施例中的第一、二、三结构层的横截面结构示意图;
50.图3是本发明又一示例性实施例中的制备装置的截面结构示意图;
51.图4是本发明又一示例性实施例中第一通道和第三通道的截面结构示意图;
52.图5a示出了接触角与固、液、气之间的关系;
53.图5b示出了液体润湿毛细管的过程;
54.图5c是弯月面在流道内的第一结构示意图;
55.图6为两亲性分子的结构示意图;
56.图7a为两亲性分子膜的形成过程示意图;
57.图7b为两亲性分子膜的结构示意图;
58.图8为本发明另一示例性实施例中的制备装置的第一透视图;
59.图9为本发明另一示例性实施例中的制备装置的结构示意图;
60.图10为本发明另一示例性实施例中的制备装置的第二透视图;
61.图11为本发明另一示例性实施例中的制备装置的第三透视图;
62.图12示出了微孔处形成的不同厚度的膜的结构示意图。
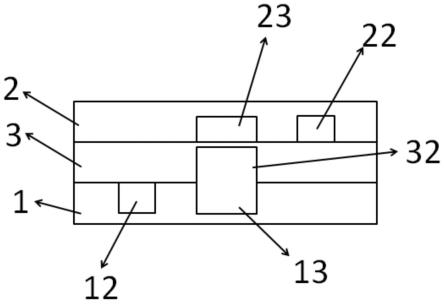
63.1为第一结构层,11为第一通道,11a为第一段,11b为第二段,12为第一开口,13为第二开口,14为第一流道,2为第二结构层,21为第二通道,22为第三开口,23为第四开口,3为第三结构层,31为微孔,32为凹槽,4为两亲性分子,41为疏水端,42为亲水端,5为膜溶液(弯月面),6为极性溶液,7为空气。
具体实施方式
64.为使本发明实施例的目的、技术方案和优点更加清楚,下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述。显然,所描述的实施例是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
65.本文中,使用用于表示元件的诸如“模块”、“部件”或“单元”的后缀仅为了有利于本发明的说明,其本身没有特定的意义。因此,“模块”、“部件”或“单元”可以混合地使用。
66.本文中,术语“上”、“下”、“内”、“外”“前端”、“后端”、“两端”、“一端”、“另一端”等指示的方位或位置关系为基于附图所示的方位或位置关系,仅是为了便于描述本发明和简化描述,而不是指示或暗示所指的装置或元件必须具有特定的方位、以特定的方位构造和操作,因此不能理解为对本发明的限制。此外,术语“第一”、“第二”仅用于描述目的,而不能理解为指示或暗示相对重要性。
67.本文中,除非另有明确的规定和限定,术语“安装”、“设置有”、“连接”、“相连”等,应做广义理解,例如“相连”,可以是固定连接,也可以是可拆卸连接,或一体地连接;可以是机械连接,也可以是电连接;可以是无线连接,也可以是无线通信连接;可以是直接相连,也可以通过中间媒介间接相连,可以是两个元件内部的连通。对于本领域的普通技术人员而
言,可以具体情况理解上述术语在本发明中的具体含义。
68.如本文所使用,“两亲性”分子是指同时具有亲水性和亲脂性这两种性质的化合物,其具有亲水的头部和疏水的尾部。亲水的头部(即亲水端)一般由极性基团组成,例如胆碱、铵盐;疏水的尾部(即疏水端)一般由长的脂肪链组成。在本文,“两亲”和“两亲性”被同义地使用。两亲性分子可以是脂质分子。典型的两亲性分子层(或两亲性分子膜,也可简称为“膜”)可以是脂质双层,其为两个相对的脂质单层形成的双层,两个脂质单层经过自组装排布,使得疏水的尾部相互面对以形成疏水性内部,而亲水的头部分别朝向外部(每一侧都为极性亲水环境)。形成脂质双层的脂质可以包括任何合适的脂质,例如1,2-二植烷酰-sn-甘油-3-磷脂胆碱、二植酰磷脂酰胆碱(dphpc)。两亲性分子可以被化学修饰或功能化以促进多核苷酸的偶联。两亲性分子还可以是通过物理化学方法合成的高分子材料,例如aba三嵌段共聚物(pmoxa-pdms-pmoxa二甲基恶唑啉-聚二甲基硅氧烷-二甲基恶唑啉)。两亲性分子可以是混合物。
69.如本文所使用,“非极性溶剂”或“非极性溶液”是指不与水混溶的化合物或化合物混合物。非极性溶剂可以是油,更具体地,可以是纯链烷烃,例如正十六烷、正癸烷、正戊烷、正己烷、正庚烷、正辛烷、四氯化碳。其他类型的油也是可能的,例如,硅油。更具体地,油可以是甲基苯基硅油ar20、羟基封端聚二甲基硅氧烷pdms-oh。
70.如本文所使用,“极性水溶液”或“极性溶液”是指容易与水和其他极性溶剂混溶的含有水的水溶液。极性水溶液可以包括一种或多种溶质。例如,可以包括能够调节极性水溶液的ph的缓冲剂。缓冲剂可以包括任何合适的缓冲剂,例如磷酸盐缓冲剂(pbs)、4-双-2-乙烷磺酸缓冲剂pipes、n-2-羟乙基哌嗪-n
’‑
乙烷磺酸缓冲剂(hepes)。极性水溶液还可以是电解质或聚电解质,以有效提升离子交换寿命。极性水溶液还可以包含氧化还原对或可以被部分氧化或还原以提供氧化还原对的氧化还原对的组合,例如铁/压铁氰化物。极性水溶液也可以是交联的琼脂糖凝胶和海藻酸钠凝胶。
71.如本文所使用,“自组装”是指分子在合适的环境中自发组装或组织,以形成高度有序的结构如两亲性分子膜的能力。
72.本文中,“方形”包括邻边夹角呈大约90
°
或接近90
°
的多边形,例如,方形为四边形,如正方形,或矩形等。当然,本文中的“方形”并不一定需要设置为标准的正方形或矩形或其他多边形,例如,方形中的“四边形”的对边可以呈平行设置,也可以设置为不平行,相应地,“四边形”的邻边可以呈相互垂直的设置,也可以设置为不垂直。“类方形”包括在邻边夹角处作了倒角处理的方形,或者邻边通过圆弧连接的方形,例如,类四边形,如类矩形(矩形的顶角替换为圆弧结构)、类正方形(如将正方形的顶角替换为圆弧结构)等。例如,本文中,“流道的横截面呈方形或类方形”指的是流道的横截面可以设置为矩形,或正方形,或类矩形,或类正方形等。为了避免流道内表面在加工过程中出现毛刺等缺陷,优选地,将流道的横截面设置为类方形,如类矩形,或类正方形等。
73.本文中,术语“约”、“大约”,典型地表示为所述值的 /-5%,更典型的是所述值的 /-4%,更典型的是所述值的 /-3%,更典型的是所述值的 /-2%,甚至更典型的是所述值的 /-1%,甚至更典型的是所述值的 /-0.5%,或者表示的是本领域技术人员理解的包括了本领域惯常的误差范围的取值。
74.本文中,某些实施方式可能以一种处于某个范围的格式公开。应该理解,这种“处
于某个范围”的描述仅仅是为了方便和简洁,且不应该被解释为对所公开范围的僵化限制。因此,范围的描述应该被认为是已经具体地公开了所有可能的子范围以及在此范围内的独立数字值,例如接触角在“大约65度到大约120度”可以理解为已经公开了如下范围:接触角在大约65-95度、95-105度、105-120度等等,还公开了在此范围内的独立数字值,如65度、69度、75度、80度、90度、100度、110度、120度。实施例一
75.本发明第一方面在于,提供了一种两亲性制备装置,包括:用于为所述两亲性分子层提供成长平台的微孔,以及能够使得溶液流经所述微孔的第一通道和第二通道,且所述微孔的第一端和第二端分别与所述第一通道和所述第二通道连通;
76.其中,所述第一通道的横截面呈方形或类方形设置,且所述第一通道的内表面材料可选地为:聚甲醛、特氟龙(聚四氟乙烯)、聚甲基丙烯酸甲酯、环氧树脂、聚碳酸酯等。
77.本实施例中,通过设置第一通道、第二通道可以灵活地向微孔的两端插入第一电极和第二电极,由此无需在制备装置内部(如微孔附近)预先设置电极层,从而使得制备装置的结构更加简单,进而大大的降低了生产成本。同时,由于微孔的两侧均设有供溶液流动的通道,对装置内部结构的清洗也更加方便,例如,可以通过向第一、二通道通入清洗液(如蒸馏水等)对微孔的第一端和第二端进行较为全面的清洁。
78.可以理解的是,第一电极、第二电极的极性相反。
79.进一步地,参见图1-图3,本发明提供了一种可以快速形成两亲性分子层(即两亲性分子膜)的两亲性分子层制备装置(即制备装置),包括:
80.第一结构层1,所述第一结构层1上设有第一通道11,且所述第一通道11的两端分别设有第一开口12和第二开口13,其中所述第一开口用于加样(即添加溶液),所述第二开口用于出样(即用于多余液体的排出)以及用于观察溶液高度;
81.第二结构层2,所述第二结构层2上设有第二通道21,且所述第二通道21上设有用于加样的第三开口;
82.其中,第一、二结构层依次紧密连接,且第一通道11和第二通道21通过至少一个微孔相连通。
83.具体地,在一些实施例中,微孔由设置在第一通道11上的微孔与设置在第二通道上的微孔相连通形成(此时,第一、二通道分别设置在第一、二结构层的内部)。
84.进一步地,在一些实施例中为了降低加工难度,该制备装置还包括:第三结构层3,且所述微孔31设置在所述第三结构层上,所述微孔贯穿所述第三结构层的第一表面(即与第一结构层相连接的一侧)和第二表面(即与第二结构层相连接的一侧),相应地,第一通道设置在第一结构层的第一表面上,第二通道设置在第二结构层的第一表面(即与第三结构层相连接的一侧)上;其中,所述第三结构层设置在所述第一结构层和所述第二结构层之间(即第一、三、二结构层依次紧密连接),且第一通道和第二通道通过所述微孔相连通。
85.具体地,在一些实施例中,参见图2所示,所述第一通道包括:第一流道14,所述制备装置包括:
86.第一结构层1,所述第一流道14设置在所述第一结构层的第一表面,且所述第一流道的两端分别设有第一开口和第二开口,其中,所述第一开口用于加样,所述第二开口用于出样;
87.第二结构层2,所述第二通道21设置在所述第二结构层的第一表面上,且所述第二通道上设有第三开口,所述第三开口用于加样;
88.第三结构层,至少一个所述微孔设置所述第三结构层上;
89.其中,第一、三、二结构层依次紧密连接,使得所述第一流道与所述第二结构层的第一表面相配合形成供溶液流动的第一通道,所述微孔的第一端和第二端分别与所述第一通道和所述第二通道连通。
90.进一步地,在一些实施例中,所述第三结构层的第一表面上还设有凹槽32,所述微孔31设置在所述凹槽32上,当第一、三结构层紧密连接时,所述凹槽与所述第一流道相配合共同构成可供溶液流动的第一通道。
91.在一些实施例中,所述微孔的内径在100微米到200微米之间,例如,微孔的第一端(与第一通道连通的一端)的内径大小在100微米到200微米之间。
92.进一步地,在一些实施例中,所述微孔的内径在150微米到200微米之间,例如,微孔的第一端的内径大小在150微米到200微米之间。
93.对于本领域技术人员来说,通过预实验选取适合的原材料是能够实现的。具体地,可以通过接触角测试方法(如外形图像分析方法,或称重法)测试得到不同材料的接触角,以选用出适合的制备材料。具体地,当材料的接触角处于大约65
°‑
120
°
时(当然,只要选出的材料所制备出的流道能够形成弯月面即可),则认为该材料制备得到的流道具备形成弯月面的能力。
94.本实施例中,通过设置第三结构层减小了制备装置的加工难度。由于制备装置的整体体积相对较小,因此第一、二结构层的厚度也较小。此时若要在第一、二结构层内部设置第一通道和的第二通道,并还要在第一、二通道上开设相应微孔,加工难度很大。而通过增设第三结构层,并将微孔开设在第三结构层上,一方面使得第一、二通道可以直接设置在第一、二结构层的表面,大大降低了加工难度;另一方面在第三结构层上直接开设微孔相较于在第一通道或第二通道上开设微孔也更加简单。具体的,当第一、三、二结构层依次紧密连接后,第一流道、第二通道分别与第三结构层的第一表面和第二表面相配合,形成位于制备装置内部的两个通道,也即使得第一、二通道实现了设置在第一、结构层内部的效果,相当于第三结构层对第一、二通道起到了封闭的作用。
95.在实际应用过程中,不同的实验需要使用到的样品量(即膜溶液的体积)并不相同。为避免对样品造成浪费,需要针对不同样品使用量的实验场景,对第一通道的大小进行相应的设置,从而适用于不同样品量的实验。本实施例中,由于制备装置可以由第一、三、二结构层组合而成,因此可以直接通过改变第三结构层以及凹槽的厚度,对第一通道的横截面大小进行灵活调整,从而制备出不同尺寸的制备装置。例如,在实际生产过程中,第一、二结构层的尺寸不需要作出调整,可以统一加工以提高生产效率。此时仅对第三结构层进行尺寸调整,即通过加工出不同厚度的第三结构层(相应的,凹槽的厚度也不相同),将第一、二结构层分别与不同厚度的第三结构层相配合,从而制备出不同尺寸(第一通道尺寸不同)的制备装置。本实施例中的制备装置在生产过程中,可以简单的通过调整第三结构层的厚度进而制备出不同的装置,且第一、二、三结构层的加工简单,生产成本低,工艺上更易于实现。
96.当然,在另一些实施例中,在装置生产过程中,也可以通过对第一结构层上的第一
流道尺寸进行调整,以改变装置的第一通道的尺寸。
97.进一步地,在一些实施例中,第二通道上还设有用于出样的第四开口。
98.进一步地,在一些实施例中,参见图3,第一通道包括:相连通的第一段11a和第二段11b,其中,第一段11a为第一通道中靠近第一开口处的部分,第二段11b为第一流道与凹槽共同构成的部分。
99.进一步地,在一些实施例中,第一段的横截面为边长为大约5mm到大约20mm的方形或类方形,如矩形;第二段的横截面为边长大约5mm到大约20mm的方形或类方形,如矩形。
100.进一步地,在一些实施例中,第一段的深度(也即第一段的长度)为大约5mm到大约10mm。
101.同样地,在一些实施例中,第二段的深度(也即第一段的长度)为大约5mm到大约10mm。
102.在一些实施例中,第二段的内径大于第一段的内径,也即第二段的横截面面积大于第一段的横截面面积。
103.本实施例中,由于第一段的内径小于第二段的内径,当膜溶液通过第一开口加入第一通道内部时,膜溶液先进入内径较小的第一段,此时第一通道(即第一通道的第一段处)的内部空间较窄,膜溶液所形成的弯月面较厚,形态也相对稳定。因此,膜溶液在前期的移动速度可以设置得较快。当膜溶液逐渐移动到第二段时,膜溶液所形成的弯月面逐渐变薄,此时,当第二段与第一段的内径差距较大时,可以适当减小膜溶液的移动速度,以保证弯月面在移动过程中的稳定性。
104.在一些实施例中,若是第二段的内径仅略大于第一段的内径(即第一、二段的内径差距相对较小),此时弯月面的变化程度也较小(或者说,弯月面的变薄过程相应地也较为缓慢),因此,弯月面的移动速度可以不作调整。
105.进一步地,第一段到第二段的变化趋势可以设置得较缓,如第一段与第二段相连接处的内径逐渐由小变大(具体地,沿第一段向第二段的方向),使得膜溶液能够首先形成较厚且较稳定的弯月面,并在第一通道内移动过程中逐渐变薄,且由于第一段到第二段的内径变化较为缓慢,弯月面能够在变薄过程中继续保持形态的稳定,由此使得弯月面在其形成与移动过程中能够保持相对稳定的状态。
106.当然,在另一些实施例中,第一通道也可以呈等径设置,即第一段和第二段的内径相同或相近。
107.优选地,在一些实施例中,第一通道11可以呈弯曲设置,如设置为u型槽结构。
108.优选地,在一些实施例中,第二通道12可以呈弯曲设置,如设置为u型槽结构。
109.本实施例中,参见图3所示,第一、二通道均呈u型槽设置,其中,第一通道呈u型槽设置,便于工作人员在实验操作时通过控制向第一开口的极性溶液添加量和添加速率来控制膜溶液的高度以及移动速率(具体地,通过第二开口观察膜溶液的高度),从而可以控制极性溶液的加入量,并有助于工作人员判断两亲性分子层是否生成。
110.在一些实施例中,微孔可以设置一个或两个或多个。在一些实施例中,当制备装置处于使用状态(也即工作状态)时,上述第一、二、三、四开口均位于朝上设置。且该微孔呈竖直状态设置或接近竖直状态设置(即微孔上所形成的膜与水平面呈90
°
或接近90
°
的夹角),具体地,微孔的轴向与水平面方向相互平行或接近相互平行。
111.为了更清楚地说明本实施例所提供的技术方案,结合操作方法对该制备装置的结构进行进一步地说明;
112.通过第三开口22向第二通道内加入适量极性溶液(如30微升的极性溶液),使得极性溶液的液面高度没过至少一个微孔;
113.通过第一开口12向第一通道内加入适量的膜溶液(如浓度为25mg/ml)的1微升非极性溶液,或适量非极性溶液与浓度为25mg/ml)的1微升非极性溶液的混合液);
114.继续通过第一开口12向第一通道内加入适量的极性溶液(如5微升的极性溶液),使得膜溶液形成弯月面(具体地,膜溶液在极性溶液、空气所提供的表面张力作用下(极性溶液的表面张力,液体和空气界面作用下)形成弯月面),并在极性溶液的推动下沿着第一通道的内部路径移动,并没过至少一个微孔;
115.当膜溶液所形成的弯月面在极性溶液的推动下没过微孔时,膜溶液中的两亲性分子在微孔处形成两亲性分子膜。
116.其中,两亲性分子的成膜原理如下:
117.如图6所示,两亲性分子4包括亲水端42和疏水端41。
118.如图7a所示,当膜溶液5(溶解有两亲性分子的非极性溶液)加入到第一通道时,膜溶液5的两侧液面形成弯月面,当膜溶液流经(或没过)微孔(具体地,流经微孔的一端),且此时微孔的另一端已设有极性溶液,膜溶液5中的两亲性分子4的亲水端42将会指向并接触极性溶液,疏水端41会和另外一层两亲性分子4的疏水端41组合,从而在微孔处形成两亲性分子膜(如图7a所示)。通过控制膜溶液的流速,使得两亲性分子4不会堆积越来越厚造成无法嵌孔。
119.当制备装置中的微孔处形成了两亲性分子膜之后,可以分别向第一通道的其中一个开口(第一开口或第二开口)和第二通道中的其中一个开口(第三开口或第四开口)插入第一电极和第二电极,从而向两亲性分子膜上插入纳米孔蛋白(具体地,可以向第一通道或第二通道内加入包括纳米孔蛋白的蛋白溶液,然后利用第一、二电极向溶液施加电压),以便进行后续的dna测序。也即是说本实施可以在制备装置两端灵活地插入电极,从而使得制备装置内部无需预设用于导电的电极层,由此简化了两亲性分子膜制备装置的结构以及加工工艺,降低了制备装置的生产成本。
120.可以理解的是,添加入制备装置中的膜溶液的浓度(即膜溶液中的两亲性分子的浓度)与第一通道的尺寸(即第一通道的横截面大小)有关,当膜溶液浓度过大时,形成的两亲性分子膜偏厚,难以在后续进一步插入蛋白(即打不通通道),而浓度过低,可能无法形成两亲性分子膜。
121.在一些实施例中,膜溶液为含有两亲性分子的非极性溶液。
122.进一步地,在一些实施例中,两亲性分子可以是磷脂,可以是高分子,例如,两亲性分子可以是通过物理化学方法合成的高分子材料,aba三嵌段共聚物(pmoxa-pdms-pmoxa二甲基恶唑啉-聚二甲基硅氧烷-二甲基恶唑啉),或是磷脂和高分子的混合物。
123.进一步地,在一些实施例中,非极性溶液是烷烃类有机溶剂,包含癸烷,十六烷,戊烷,或是以上两种或多种有机溶剂的混合液,该非极性溶液用来溶解磷脂或是高分子三嵌段共聚物制成膜溶液。
124.在一些实施例中,极性溶液为基因测序过程中的电解液,包含电解质或聚电解质
用来有效提升离子交换寿命,也可以包含氧化还原对或可以被部分氧化或还原以提供氧化还原对的氧化还原对的组合,例如铁/压铁氰化物;也可以是交联的琼脂糖凝胶和海藻酸钠凝胶;也可以包含有缓冲剂用来调节水溶液介质的ph,适当的缓冲剂包括但不限于磷酸缓冲液pbs;4-双-2-乙烷磺酸缓冲剂pipes,n-2-羟乙基哌嗪-n
’‑
乙烷磺酸缓冲剂(hepes)等。
125.具体地,在一些实施例中,微孔的第一端(即上端,也即与第一通道相连通的一端)的内径大于微孔的第二端(即微孔的另一端,与第二通道相连)的内径大小。本实施例中,微孔呈上小下大的设计,从而能够在不影响微孔第一端的大小(微孔的第一端的内径大小与两亲性分子层的形成密切相关,因此,微孔的第一端的内径尺寸通常固定设置在大约100微米-200微米之间)的情况下,使得微孔内部有足够的空间来容纳极性溶液(如容纳首先加入微孔内的第一极性溶液)。具体地,当弯月面流经微孔时,弯月面中的两亲性分子层形成于微孔最窄处,即两亲性分子在微孔的第一端处自组装形成两亲性分子层。
126.在另一些实施例中,微孔也可呈圆柱状设置(即上下端等大),或呈上大下小设置。当然,微孔也可以设置为其他形状,只要微孔的形状设置能够成功形成两亲性分子层,则均属于本发明的保护范围内。
127.可以理解的是,在第一通道的横截面形状一定(第一横截面的形状、尺寸一定)的情况下,针对相应形状的第一通道,要使得膜溶液在第一通道内形成弯月面,则需要加入的膜溶液的量满足一定的要求,优选地,在一些实施例中,当第一通道的横截面呈边长大约5mm-大约20mm的矩形设置时,加入1微升到5微升的膜溶液可以形成一个比较理想的弯月面;当第一通道内有不同数量的微孔,且需要制备两亲性分子膜的数量不同时,则对膜溶液中含有的两亲性分子的浓度要求也不相同的。为了试验操作简便,通常选用不同量的两亲性分子和非极性溶液的混合液,即制备得到不同浓度的膜溶液。
128.优选地,在一些实施例中,制备装置的制备材料选用具有一定疏水性和亲脂性的材料,例如,选用接触角在大约75
°
到大约120
°
的材料,如特氟龙、德尔林(聚甲醛)、pmma(有机玻璃,也即聚甲基丙烯酸甲酯)、环氧树脂、pc(聚碳酸酯)和pdms(聚二甲基硅氧烷)等。本实施例中,可以选取具有一定疏水性和亲脂性的原材料(如聚甲醛)加工成制备装置,满足试验操作过程中对第一通道及微孔处疏水性和亲脂性的要求,从而无需对制备装置进行预处理操作,对操作流程进行了简化。
129.在一些实施例中,制备装置可采用的加工方式有:机械加工、铸造加工、激光加工、电穿孔、微注塑加工、3d打印加工等。
130.进一步地,在一些实施例中,微孔的加工方式包括:激光加工、机械加工、电穿孔等。
131.优选地,为了保证微孔的截面呈圆形,且内壁光滑,在一些实施例中,微孔选用激光加工。
132.在一些实施例中,参见图4,该制备装置内部设有第一通道11和第二通道21,第一通道设置为u型槽流道,第一通道内体积设置在大约40微升到大约80微升之间,可根据实际用户需要采用不同厚度的板材制造不同体积的第一通道。
133.优选地,在一些实施例中,第二开口13(即第一流道的出样口)设置为上大下小的喇叭状。
134.若第二开口的内径偏小,当溶液从第二开口流出时不会直接流出,而是先形成一
个小液滴,随着小液体逐渐变大最终破裂,在小液滴的破裂过程中,对第一通道内部的液体产生了较强的剪切应力,将会影响到成膜的效果。而本实施例中通过扩大第二开口位于制备装置表面一端的内径大小,使得溶液能够从第二开口快速顺利地排出,避免了液滴的形成与破碎过程,相应地避免了对成膜效果造成的不利影响。
135.在另一些实施例中,第一开口也可呈上大下小设置。
136.进一步地,在一些实施例中,第三、四开口也可呈上大下小的设置。
137.优选地,在一些实施例中,制备装置中的第一通道内径l1设置在大约0.5mm-2.0mm之间,且第一通道与第三通道共同形成的流道部分l2的内径在大约1.0mm-5.0mm之间,第一开口l3的第一端内径大小在大约1.0mm-4.0mm之间(第二、三、四开口的内径大小可参见第一开口),第三通道的长度l4(也即第一通道和第三通道相配合的一部分)在大约5.0mm到10.0mm之间,制备装置的整体高度l5在大约15mm到25mm之间,制备装置的宽度l6在大约23mm-32mm之间。
138.优选地,在一些实施例中,微孔的位置可以根据不同第一通道的结构进行相适应的设计,如微孔设置在距离第一通道底端约1/3到2/3l的位置,其中l为第一通道开口距底端的长度。优选地,第一结构层以及第二结构层的厚度一共为大约2mm。实施例二
139.参见图8-图11,本发明还提供了一种可以快速形成两亲性分子膜的装置,与上述实施例一相同的是,该制备装置包括:
140.第一结构层1,所述第一结构层1上设有第一通道11,且所述一通道11的两端分别设有第一开口12和第二开口13,其中所述第一开口用于加样(即添加溶液),所述第二开口用于出样(即用于多余液体的排出)以及用于观察溶液高度;
141.第二结构层2,所述第二结构层2上设有第二通道21,且所述第二通道21上设有用于加样的第三开口;
142.其中,第一、二结构层依次连接,且第一通道11和第二通道21通过至少一个微孔相连通。
143.具体地,在一些实施例中,当该制备装置处于使用状态(即工作状态)时,微孔呈水平设置或接近水平设置,也即微孔上形成的两亲性分子膜与水平面平行或接近平行(如膜所在的平面与水平面的夹角为0度或接近为0度),且第一通道位于第二通道上方。
144.具体地,在一些实施例中,第二通道分别设有用于加样的第三开口和用于出样的第四开口。
145.进一步地,在一些实施例中,第一结构层和第二结构层由上到下依次设置,使得第一通道位于第二通道上方,且第一通道的第一、二开口和第二通道上的第三、四开口均朝上设置,便于工作人员操作加样,以及便于插入电极。
146.进一步地,在一些实施例中,第二开口呈上大下小的设置。
147.若以上开口的内径偏小,当溶液相应的开口流出时不会直接流出,而是先形成一个小液滴,随着小液体逐渐变大小液滴最终破裂,在小液滴的破裂过程中,对第一通道内部的液体产生了较强的剪切应力,将会影响到成膜的效果。而本实施例中通过扩大开口位于制备装置表面一端的内径大小,使得溶液能够从开口快速顺利地排出,避免了液滴的形成与破碎过程,相应地避免了对成膜效果造成的不利影响。
148.进一步地,在一些实施例中,第三、四开口呈上大下小的设置,其中,第二通道的第一、二开口处内径较大,可便于加样。
149.本实施例中,制备装置可以选用分层加工的方式分别加工出第一结构层和第二结构层,再将第一结构层和第二结构层组装成制备装置。当然该制备装置还可以选用一体成型的方式,直接在一块板材上加工出第一通道和第二通道以及相关结构。因此,无论是一体成型(如一体注塑成型),还是分层加工方式制备的制备装置均应涵盖在本技术的保护范围内。
150.在一些实施例中,第二通道(由于当装置处于工作状态时,第二通道位于第一通道的下方,也称下流道)用于添加极性溶液,第一通道(也称上流道)用于添加膜溶液。为了进一步地说明本实施例所采用的技术方案,下面对本实施例中的制备装置的使用方法及两亲性分子膜的成膜过程进行说明:
151.首先分别向第一通道(上流道)的第一开口加入适量的膜溶液、向第二通道(下流道)的第三开口适量的极性溶液;
152.继续通过第一开口向第一通道加入适量的膜溶液(如浓度为25mg/ml的1微升非极性溶液,或适量非极性溶液与浓度为25mg/ml的1微升非极性溶液的混合液),再继续通过第一开口向第一通道内加入适量的极性溶液(如5微升的极性溶液),使得膜溶液在第一通道内部形成弯月面;
153.膜溶液所形成的弯月面在极性溶液的推动下沿着第一通道的内部路径移动,并穿过至少一个微孔处(即在极性溶液的推动下逐渐靠近并到达微孔处,然后在极性溶液的推动下继续向前移动并逐渐远离微孔),且在膜溶液移动到微孔处时,膜溶液中的两亲性分子在微孔处形成两亲性分子膜。其中,所形成的两亲性分子膜与水平面方向相互平行或接近相互平行。
154.本实施例中,选用的膜溶液、极性溶液以及非极性溶液参见上述实施例。
155.在一些实施例中,基于不同试验需求,第一通道和第二通道之间可以设置有一个微孔,两个微孔或者多个微孔,以便于一次性制备一个两亲性分子膜,两个两亲性分子膜或多个两亲性分子膜。
156.同样地,由于制备装置的整体体积较小,其内部通道与微孔的尺寸设置也相对较小,因此对加工精度要求相对较高。为了进一步简化制备工艺,在第一结构层和第二结构层之间还设有第三结构层,且至少一个微孔设置在第三结构层上,第一、三、二结构层依次紧密连接,使得第一通道和第二通道通过设置于第三结构层上的微孔相连通。
157.优选地,在一些实施例中,基于固定的流道(如横截面大小固定的流道),膜溶液选用的量也相同或近似相同,以保证弯月面能够顺利形成并保持状态稳定。
158.优选地,在一些实施例中,制备装置的长度m1为大约26mm-36mm之间,制备装置的宽度m2为大约18mm-28mm之间,第一结构层的长度m3为大约14.5mm-24.5mm之间,第一结构层的宽度m4在大约8mm-18mm之间,第一开口的内径m5在大约1.0-4.0mm之间,第三开口和第四开口的第一端的内径m6在大约2.0-4.0mm之间,第三、四开口的第二端的内径m7在大约0.5-2.0mm之间。实施例三
159.基于上述实施例所提供的装置,本发明还提供了一种两亲性分子膜的制备方法,
包括以下步骤:
160.s1提供用于制备两亲性分子层的制备装置,制备装置内设有用于为两亲性分子层提供成长平台的至少一个微孔,以及能够使得溶液流经微孔的第一通道和第二通道,且微孔的第一端和第二端分别与第一通道和第二通道连通,其中,第一通道的横截面呈方形或类方形设置;
161.s2向第二通道内加入第一极性溶液,使得第一极性溶液进入至少一个微孔内;
162.s3依次向第一通道内加入膜溶液和第二极性溶液,使得膜溶液在第一通道内形成弯月面;
163.s4基于预设速度向第一通道内加入第二极性溶液,使得第二极性溶液推动膜溶液移动并流经微孔,膜溶液在微孔处形成两亲性分子层;
164.其中,第一通道内表面所选的接触角为大约65
°‑
大约120
°
。
165.可以理解的是,在一些实施例中,上述步骤s3和s4可以连续进行(或者说,在实际操作过程中,步骤s3和步骤s4可以为一个步骤),当然,在另一些实施例,步骤s3和步骤s4也可以分步进行。
166.在一些实施例中,在s3中,所述第二极性溶液的注入速度为大约5μl/min到大约10μl/min;
167.在一些实施例中,在s4中,所述第二极性溶液的所述预设速度为大约10μl/min到大约20μl/min。
168.在一些实施例中,第二极性溶液前期的注入速度小于后期的注入速度,由于前期属于弯月面形成期间,因此膜溶液的移动速度较小相对较为稳定,更利于弯月面的形成。
169.本实施例中,制备装置优先选用了具有一定疏水性的材料,且该制备装置内的第一通道的内表面的材料接触角(即内表面材料与纯水之间的接触角)为大约65
°‑
120
°
,使得加入到第一通道内的膜溶液能够在流道内表面、极性溶液以及流道内的空气的共同作用下,形成弯月面。其中,第一通道的横截面优选地呈方形或类方形的设置,此时,第一通道对膜溶液(或者说膜溶液所形成的弯月面)的移动会产生一定的阻力,使得膜溶液在第一通道内的移动速度不会过快,且膜溶液上各个位置的移动速度相对均匀(或者说,各个位置的流动速度的差别对弯月面的稳定性影响不大),使得弯月面能够在移动过程中能够保持稳定的形态。
170.具体地,第一通道内表面以及微孔的表面(即微孔侧壁)均选用接触角在大约65
°‑
120
°
之间的材料制成(优选地,由聚甲醛制成),使得膜溶液移动到对应的微孔处时,能够在微孔处(具体地,在微孔的第一端)上顺利形成两亲性分子膜,而无需提前对装置(如设置在流道处的微孔)进行预处理。
171.其中,在膜溶液形成弯月面与弯月面移动过程中,膜溶液的加入量(体积)、膜溶液所形成弯月面的移动速度对弯月面的形成与移动过程也非常重要,并且对于本领域的技术人员来说,通过预实验选取适合的膜溶液加入量、移动速度是可以实现的。
172.例如,在膜溶液的加入量的选择或预测步骤中,主要考虑的参数有:雷诺数(reynolds number,即re),雷诺数是一种可用来表征流体流动情况的无量纲数。雷诺数的计算方法为:re=ρvd/μ,其中v、ρ、μ分别为流体的流速(相当于膜溶液的移动速度)、密度与黏性系数,d为特征长度(相当于第一通道的长度)。其中,膜溶液的密度和粘度系数均可以
通过实验测量得到,保持弯月面的稳定需要使得流体的雷诺系数偏小(雷诺数越小,流体流动越小),即为层流状态。
173.因此,本发明优选地使得流体的re《2300,由此,通过雷诺数可以对第一通道的长度与膜溶液的移动速度的关系作出了初步限制(因此,当膜溶液选定,且装置的第一通道长度已确定时,膜溶液的移动速度可以基于雷诺数作出初步限制,也即膜溶液的移动速度受到了膜溶液与第一通道长度的约束)。也即是说,对于本领域技术人员而言,当膜溶液选定后,在此基础上选用制备装置进行预实验,能够筛选出选取较为合适的膜溶液的移动速度。基于预实验筛选出的移动速度对极性溶液(如第二极性溶液)的注入速度进行对应的设计,可以得到第二极性溶液的预设的注入速度。当然,第二极性溶液的注入速度也可以提供工作人员的操作经验作出初步预估,然后进行预实验,从而获取到适宜的注入速度。
174.进一步地,在一些实施例中,第一通道的内表面所选材料的接触角为大约75
°‑
大约95
°
。具体地,在一些实施例中,多个微孔设置在第一通道内表面,也即第一通道内表面以及微孔表面所选材料的接触角为大约75
°‑
大约95
°
。
175.为了更清楚地说明本发明所采用的技术方案,下面对接触角、弯月面的形成进行简单说明:
176.参见图5a,接触角(contact angle)是指在固体s、液体l、气体g三相交界处,自固-液界面经过液体内部到气-液界面之间的夹角。若θ《90
°
,即液体较易润湿固体,其角越小,表示润湿性越好;若θ》90
°
,即液体不容易润湿固体,容易在表面上移动。具体地,当θ=0,完全润湿;当θ《90
°
,部分润湿或润湿;当θ=90
°
,是润湿与否的分界线;当θ》90
°
,不润湿;当θ=180
°
,完全不润湿。
177.参见图5b,沿图中的毛细管壁升高的液体压强为其中,δp为沿毛细管壁上升的液体的压强,σ为表面张力,r为液体表面的曲率半径,ρ为液体密度,g为重力加速度,h为液面升高的高度。基于接触角的定义可知:例如,当接触角θ小于90
°
时,溶液可以在毛细管内形成弯月面,且此时所形成的弯月面为凹状。同时可知所形成弯月面的曲率半径和毛细管的半径r有关,当接触角θ大于90
°
时,溶液可以在毛细管内形成凸状的弯月面。
178.具体地,加入第一通道内部的极性溶液(如第二极性溶液)的表面张力使得膜溶液在极性溶液的液体表面(即与膜溶液相接触的一端)扩散开来。由于第一通道内表面选用的是具有一定疏水性的材料,因此,第一通道内表面对膜溶液有一定的吸附作用。此时,参见图5c,膜溶液一边是极性溶液(第二极性溶液)6,另一边是空气7。其中,液体表面有收缩力,膜溶液与空气接触的界面层分子受到一指向液体内部的拉力,从而使得膜溶液在第一通道内部逐渐形成弯月面5。
179.参见图7a,膜溶液里溶解有两亲性分子4,由于两亲性分子5有亲水端42和疏水端41(参见图6)。由于两亲性分子具有自组装能力,当膜溶液流过微孔时,里面的两亲性分子的亲水端42会指向并接触第一极性溶液,而疏水端41会和另外一层两亲性分子的疏水端41相组合,从而形成两亲性分子层,如图7a和图7b所示。本实施例中,通过控制膜溶液的移动速度,可以避免两亲性分子在微孔处堆积越来越厚(如图12中的(a)所示)造成无法嵌孔。
180.本实施例中,通过第二极性溶液推动膜溶液发生移动,从而使得膜溶液经过至少一个微孔,并在至少一个微孔处形成两亲性分子膜。且第二极性溶液的流速(或者说第二极性溶液的加样速度)相对可控,由此可以通过控制后续加入第二极性溶液的加样速度控制膜溶液在第一通道中的移动速度(也即流动速度),从而控制两亲性分子膜的形成过程,避免膜溶液流动过快而没有成功形成两亲性分子膜,或者膜溶液流动过慢而形成过厚的两亲性分子膜。
181.通过极性溶液推动弯月面(膜溶液)在微孔处成膜的成膜方式,可以对膜溶液的移动速度进行较为精准的控制(例如,通过移液枪或注射泵等对极性溶液的注入速度进行控制,从而对膜溶液的移动速度进行控制),从而使得膜溶液在不同的微孔处停留时间相同或相近,避免膜溶液在部分微孔区域停留过久而形成厚的膜,或者在部分微孔区域移动过快而没有成功形成膜。因此,本发明能够通过对膜溶液的移动速度进行较为精准的控制,从而直接制成膜厚符合使用要求的两亲性分子层,而无需在成膜后对膜进行薄化处理(如通过薄化处理使得膜由厚变薄,如图12中的(a)-(d)所示)。换句话说,本发明的成膜方法可以一次成膜,成膜效果较好,如通过控制极性溶液的注入速度进而控制膜溶液的移动速度,可以直接形成厚度适宜的膜(如直接制成图12中(d)所示的膜)。
182.例如,在一些实施例中,通过注射泵控制第二极性溶液的注入速度,以控制膜溶液的移动速度。本实施例中,所提供的方法更可控(例如,相较于现有技术的气泡挤压成膜)。当然,还可以采用其他注入方式以控制溶液的注入速度,且任何能够控制溶液注入速度的方式均属于本发明的保护范围内。
183.进一步地,在一些实施例中,提供往复式注射泵加入(注入)第二极性溶液。例如,选用的注射泵型号为harvard apparatus 4400。
184.在一些实施例中,该方法所使用的到的膜溶液、非极性溶液参见上述实施例,第一、二极性溶液同样参见上述实施例。
185.例如,在一些实施例中,所述膜溶液包括:非极性溶液,以及两亲性分子,其中,所述两亲性分子可选地包括:所述两亲性分子包括:磷脂,或高分子,或磷脂和高分子的混合物。
186.进一步地,为了实现后续的dna测序,在一些实施例中,还包括步骤:
187.分别向所述第一通道和所述第二通道插入第一电极和第二电极,通过第一、二电极向所述两亲性分子层插入纳米孔蛋白。
188.具体的,分别向第一极性溶液、第二极性溶液中插入第一电极(正电极或负电极)、第二电极(正电极或负电极),使得第一极性溶液和/或第二极性溶液中的纳米孔蛋白插入到所述两亲性分子膜上。
189.进一步地,在一些实施例中,纳米孔蛋白可以预先添加在极性溶液(如第一极性溶液或第二极性溶液种)。
190.当然,在另一些实施例中,也可以在两亲性分子层形成后,向第一通道内加入纳米孔蛋白(如包括纳米孔蛋白的溶液)。
191.在一些实施例中,可以在制备两亲性分子膜的之前基于制备装置进行预实验,即分别选用不同量的膜溶液进行不同试验,以确定稳定形成弯月面的膜溶液的量。
192.基于不同的试验需求,可以在制备装置上设置一个或多个微孔。例如,在一具体实
施例中,第一通道和第二通道之间仅通过一个微孔相连通,先在第二通道(下流道)加入30微升极性溶液充满第二通道,在第一通道(上流道)加入1到5微升膜溶液即可以形成合适的弯月面,其中,膜溶液的浓度是10mg/ml。然后向第一通道(上流道)加入5微升的极性溶液使得膜溶液在第一通道内形成弯月面,然后再加入30微升的极性溶液推动弯月面流过微孔以在微孔处形成两亲性分子层。若进一步地在第一通道和第二通道设置两个微孔,此时第一通道的截面形成和尺寸不变,因此,稳定形成的弯月面所需的膜溶液的体积一定,但是形成两亲性分子膜需要的两亲性分子(如磷脂或是高分子三嵌段共聚物)的量增加了,也即是需要增加膜溶液中两亲性分子的浓度,例如12.5mg/ml,即保持膜溶液含量不变的情况下,通过增加浓度的方法使得膜溶液里含有更多的两亲性分子。
193.进一步地,在一些实施例中,检测电极(即第一、二电极)采用的是ag或是ag/cl,即银或是氯化银丝做电极。具体地,将检测电极分别插入第一开口和第三开口,通过使用商用axon 1550b仪器检测电信号或是输出三角波测量两亲性分子膜两端的电容判断是否形成两亲性分子膜。
194.在一些实施例中,该方法中的制备装置可以选用实施例一或实施例二中所示出的制备装置。
195.需要说明的是,在本文中,术语“包括”、“包含”或者其任何其他变体意在涵盖非排他性的包含,从而使得包括一系列要素的过程、方法、物品或者装置不仅包括那些要素,而且还包括没有明确列出的其他要素,或者是还包括为这种过程、方法、物品或者装置所固有的要素。在没有更多限制的情况下,由语句“包括一个
……”
限定的要素,并不排除在包括该要素的过程、方法、物品或者装置中还存在另外的相同要素。
196.以上各实施例仅用以说明本发明的技术方案,而非对其限制;尽管参照前述各实施例对本发明进行了详细的说明,本领域的普通技术人员应当理解:其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分或者全部技术特征进行等同替换;而这些修改或者替换,并不使相应技术方案的本质脱离本发明各实施例技术方案的范围,其均应涵盖在本发明的权利要求和说明书的范围当中。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。
