1.本发明涉及萃取技术领域,具体涉及一种含有机氧化膦类萃取剂的镍钴协萃体系以及镍钴萃取方法。
背景技术:
2.镍、钴是重要的有色金属,被广泛应用于航空、石油化工、陶瓷、电子、电池和医学等领域。湿法浸出是处理低品位难冶含镍钴资源的重要方法。由于溶剂萃取法具有能耗低、流程短、净化效果好和易自动化控制等优点,已被广泛应用于酸浸液中镍钴分离提纯。
3.溶剂萃取法主要有酸性膦类萃取法、胺类萃取法、协同萃取法等,其中协同萃取法是两种或两种以上的萃取剂混合后,在同样的萃取条件下萃取金属,具有协同增效效果的协同萃取剂分配比显著大于单独的萃取剂萃取金属的分配比之和,可以避免对酸性膦类萃取剂的皂化,因此不会出现氨氮废水,对环境无危害。对于镍钴协同萃取剂,如“二(2,4,4-三甲基戊基)二硫代磷酸 (2,4,4-三甲基戊基)次膦酸”、“烷基羟基肟 versatic10 acid”,“吡啶羧酸酯 versatic10 acid”,“烷基羟基肟 versatic10 acid 磷酸三丁酯”等协萃体系,其中部分协萃体系分相差,分离系数差,有些对镍的反萃速率慢等缺点。其中“烷基羟基肟 versatic10 acid 磷酸三丁酯”协萃体系,其优点有较好的分离系数,但存在仍需加热来实现镍的反萃,在实际应用中不仅工艺复杂,而且增加能耗,使其受到限制。
技术实现要素:
4.本发明意在提供一种含有机氧化膦类萃取剂的镍钴协萃体系,以解决现有技术中的镍钴共萃工艺中镍反萃效率低的技术问题。
5.为达到上述目的,本发明采用如下技术方案:
6.一种含有机氧化膦类萃取剂的镍钴协萃体系,包括如式(1)所示的烷基羟基肟、如式(2)所示的羧酸萃取剂和如式(3)所示的有机氧化膦类萃取剂;
[0007][0008]
其中,r1和r2分别为碳原子数为4-12的取代或未取代的烷基中的任意一种;r3为氢,或者为取代或未取代的烷基中的任意一种;r4为碳原子数为4-12的取代或未取代的直链烷基、取代或未取代的环烷基以及取代或未取代的支链烷基中的任意一种;r5、r6、r7为碳原子数为4-12的取代或未取代的烷基中的任意一种。
[0009]
本方案还提供了一种含有机氧化膦类萃取剂的镍钴协萃体系的镍钴共萃的方法,
、co
2
的离子浓度范围均为0.01-10g/l;zn
2
、mn
2
、mg
2
和ca
2
的离子浓度范围均为0.01-20g/l;金属离子溶液的ph值为4.0-6.0,初始有机相与金属离子溶液的体积比为6:1-1:1,萃取混合时间为1-5min;环境温度为-10-45℃;平衡ph为5-5.5。采用上述的参数条件,可以将镍和钴以较高的萃取率从金属离子溶液中萃取,实现这两种离子与其他金属离子的分离。
[0027]
进一步,在s2中,所述反萃剂为浓度在20-200g/l的硫酸溶液;在s2中,负载有机相与反萃剂的体积比为5:1-1:5,反萃混合时间为3-10min;环境温度为-10-45℃。采用上述的参数条件,可以将镍和钴以较高的饭萃率从负载有机相中萃出,实现对这两种金属离子的回收和富集。
[0028]
进一步,在ss2中,洗涤液为含0.01-10g/l ni
2
的酸性溶液,负载有机相与洗涤液的体积比为0.8:1-50:1,洗涤混合时间为1-5min;环境温度为-10-45℃;平衡ph为1.0-5.5。采用上述洗脱参数条件,可以实现对锌和钴的高校洗脱,实现镍与锌钴的分离。
[0029]
进一步,在ss3中,所述反萃剂为浓度在20-200g/l的硫酸溶液;洗涤后负载有机相与反萃剂的体积比为5:1-1:5,反萃混合时间为3-10min;环境温度为-10-45℃。采用上述的参数条件,可以将镍以较高的饭萃率从负载有机相中萃出,实现对这镍的回收和富集。
附图说明
[0030]
图1为本发明实施例1中金属离子萃取ph平衡等温线。
[0031]
图2为本发明实施例2中金属离子萃取动力学。
[0032]
图3为本发明实施例5中金属离子反萃酸浓度平衡等温线。
[0033]
图4为本发明实施例6中金属离子洗涤ph平衡等温线。
具体实施方式
[0034]
下面结合实施方式对本发明做进一步详细的说明,但本发明的实施方式不限于此。若未特别指明,下述实施所用的技术手段为本领域技术人员所熟知的常规手段:所用的材料、试剂等,均可从商业途径得到。
[0035]
一种含有机氧化膦类萃取剂的镍钴协萃体系的镍钴共萃的方法,包括以下依次进行的步骤:
[0036]
s1萃取:使用所述初始有机相萃取金属离子溶液,获得负载有机相和萃余液。
[0037]
金属离子溶液中含有zn
2
、ni
2
、co
2
、mn
2
、mg
2
和ca
2
。ni
2
、co
2
的离子浓度范围均为0.01-10g/l;zn
2
、mn
2
、mg
2
和ca
2
的离子浓度范围均为0.01-20g/l。金属离子溶液的ph值为4.0-6.0。
[0038]
初始有机相与金属离子溶液的体积比为5:1-1:5(优选为6:1-1:1),萃取混合时间为1-5min;环境温度为-10-45℃(可在室温下进行,0-30℃);平衡ph为5-5.5。
[0039]
初始有机相由镍钴协萃体系和稀释剂组成。稀释剂为磺化煤油和/或航空煤油。镍钴协萃体系在初始有机相中的体积浓度为0.1-60%。含有机氧化膦类萃取剂的镍钴协萃体系,其特征在于,包括如式(1)所示的烷基羟基肟、如式(2)所示的羧酸萃取剂和如式(3)所示的有机氧化膦类萃取剂;
[0040][0041]
其中,r1和r2分别为碳原子数为4-12的取代或未取代的烷基中的任意一种;r3为氢,或者为取代或未取代的烷基中的任意一种;r4为碳原子数为4-12的取代或未取代的直链烷基、取代或未取代的环烷基以及取代或未取代的支链烷基中的任意一种;r5、r6、r7为碳原子数为4-12的取代或未取代的烷基中的任意一种。烷基羟基肟、羧酸萃取剂和有机氧化膦类萃取剂的摩尔比为0.1-2.0:0.1-5.0:0.1-6.0,优选为0.1-2.0;0.1-5.0;0.1-2.0。经过实验研究,发现上述摩尔比以及浓度范围的三种萃取剂的组合物,可以实现镍、钴的高效萃取,并且在酸作为反萃剂的情况下,可实现镍、钴的高效反萃;还可以在萃取后洗涤过程中,实现镍与钴锌的有效分离。
[0042]
s2反萃:使用反萃剂反萃所述负载有机相,获得空载有机相和反萃液。
[0043]
反萃剂为浓度在0.02-2mol/l的硫酸溶液(优选20-200g/l)。负载有机相与反萃剂的体积比为5:1-1:5,反萃混合时间为3-10min;环境温度为-10-45℃。
[0044]
本方案的含有机氧化膦类萃取剂的镍钴协萃体系除了用于镍钴共萃,还可以通过洗涤实现镍钴的分离,具体流程如下:
[0045]
ss1萃取:使用所述初始有机相萃取金属离子溶液,获得负载有机相和萃余液。该步骤同上文描述的s1萃取。
[0046]
ss2洗涤:使用洗涤液洗涤所述负载有机相,获得洗涤后负载有机相。更具体地,在ss2中,洗涤液为含0.01-10g/l ni
2
的酸性溶液,负载有机相与洗涤液的体积比为0.8:1-50:1,洗涤混合时间为1-5min;环境温度为-10-45℃;平衡ph为1.0-5.5。
[0047]
ss3反萃:使用反萃剂反萃所述洗涤后负载有机相,获得空载有机相和反萃液。更具体地,在ss3中,所述反萃剂为浓度在20-200g/l的硫酸溶液;洗涤后负载有机相与反萃剂的体积比为5:1-1:5,反萃混合时间为3-10min;环境温度为-10-45℃。
[0048]
以上为镍钴共萃工艺的工艺流程描述,具体的实施例详见下文:
[0049]
实施例1:萃取金属顺序实验
[0050]
水相料液(金属离子溶液):模拟料液(硫酸盐体系),料液含cu
2
0.057g/l,ni
2
3.48g/l,co
2
0.79g/l,zn
2
0.34g/l,ca
2
0.98g/l,mg
2
10.78g/l,mn
2
2.97g/l,ph为5.21。
[0051]
初始有机相:以磺化煤油为稀释剂,异丁酸浓度为0.5mol/l,3-羟基-5-乙基-壬烷-4-肟浓度为0.35mol/l,三丁基氧化膦浓度为0.5mol/l。
[0052]
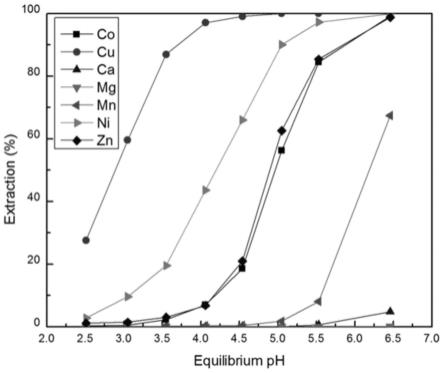
萃取:上述初始有机相与水相料液相比为(o/a)1:1,混合时间5min,振荡频率300r/min,温度25℃,使用碳酸钠调节萃取平衡ph分别为2.5、3.0、3.5、4.0、4.5、5.0、5.5、6.5进行萃取。
[0053]
由图1可以看出,金属萃取顺序为:cu》ni》zn≈co》mn》ca》mg。由图中曲线可得,在ph=5-5.5时,可以将镍和钴与钙、镁、锰有效的分离开来。
[0054]
实施例2:萃取的动力学实验
[0055]
水相料液(金属离子溶液):为模拟料液(硫酸盐体系),料液含cu
2
0.052g/l,ni
2
3.64g/l,co
2
0.87g/l,zn
2
0.28g/l,ca
2
0.78g/l,mg
2
12.54g/l,mn
2
2.57g/l,ph为5.01;
[0056]
初始有机相:以磺化煤油为稀释剂,异丁酸浓度为0.5mol/l,3-羟基-5-乙基-壬烷-4-肟浓度为0.35mol/l,三丁基氧化膦浓度为0.5mol/l;
[0057]
萃取:上述有机相与料液相比为(o/a)1:1,混合时间分别为1、2、3、5、8、10、15min,振荡频率300r/min,温度25℃,使用碳酸钠调节萃取平衡ph为5.5进行萃取。实验结果如图2所示。
[0058]
由图2可以看出,该萃取反应速度很快,当反应时间为5min时,镍的萃取率接近100%。随着时间的延长,钴、钙、镁、锰的萃取率呈下降趋势,这可能是由于随着萃取平衡ph趋于稳定,金属的萃取达到饱和,使得钴、钙、镁、锰的萃取率先升高后降低,同时,添加有机氧化膦类萃取剂未影响到镍的萃取速率以及萃取率。
[0059]
实施例3:不同相比对萃取的影响
[0060]
水相料液(金属离子溶液):为模拟料液(硫酸盐体系),料液含ni
2
3.87g/l,co
2
0.35g/l,ca
2
0.58g/l,mg
2
13.47g/l,mn
2
2.25g/l,ph为5.14;
[0061]
初始有机相:以磺化煤油为稀释剂,异丁酸浓度为0.5mol/l,3-羟基-5-乙基-壬烷-4-肟浓度为0.35mol/l,三丁基氧化膦浓度为0.5mol/l;
[0062]
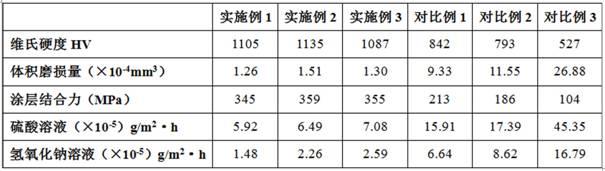
萃取:上述有机相与料液相比分别设定为(o/a)6:1、4:1、2:1、1:1、1:2、1:4、1:6,混合时间分别为5min,振荡频率300r/min,温度25℃,使用碳酸钠调节萃取平衡ph为5.5进行萃取。实验结果如表1所示。
[0063]
表1:不同相比对萃取率的影响(表中实验数据为至少三次平行试验的平均值)
[0064]
相比(o/a)6:14:12:11:11:21:41:6镍萃取率(%)99.7899.7898.4598.7878.4530.7418.04钴萃取率(%)99.7899.4599.1284.4517.1200钙萃取率(%)3.551.520.990.670.2200镁萃取率(%)0.110.10.080.080.0400锰萃取率(%)9.459.455.451.455.430.110
[0065]
由表1可以看出,随着相比o/a的降低,各个金属的萃取率迅速下降,在相同条件下,镍的萃取率明显高于钴、钙、镁、锰,综合考虑,当相比o/a=2:1时,该协萃体系对各个金属的萃取效果最好,镍的萃取率在98.45%,钴的萃取率为99.12%,而钙、镁、锰的萃取率均保持在较低水平,从而达到理想的分离效果。
[0066]
实施例4:酸度对反萃性能的影响
[0067]
负载有机相的获取方法如下:使用上述实施例3中初始有机相对本实施例的水相料液进行萃取。更具体地,按相比o/a=1:1,混合时间分别为5min,振荡频率300r/min,温度25℃,使用碳酸钠调节萃取平衡ph分别为5.5进行萃取。其中,水相料液(金属离子溶液)为模拟料液,料液金属浓度为:ni
2
3.59g/l,co
2
0.33g/l;经过萃取获得负载有机相,其中含有ni
2
3.58g/l,co
2
0.28g/l。
[0068]
反萃剂:硫酸溶液,浓度分别设置为3g/l、5g/l、10g/l、20g/l、30g/l、40g/l、50g/l、80g/l、100g/l、200g/l。
[0069]
反萃取:使用负载有机相与不同浓度硫酸相比为(o/a)1:1,混合时间5min,振荡频率300r/min,温度25℃,进行反萃取,实验结果如表2所示。
[0070]
表2:温度25℃时不同硫酸浓度对反萃率的影响(表中实验数据为至少三次平行试验的平均值)
[0071]
浓度(g/l)35102030405080100200镍反萃率(%)20.5440.5485.197.9598.8999.4999.4999.5499.5899.67钴反萃率(%)78.9890.4298.1198.9999.1199.2499.3799.4599.4699.66
[0072]
根据表2中反萃剂浓度条件实验结果,随着硫酸浓度增加越有利于镍和钴的反萃,当硫酸浓度为20g/l时,镍和钴的反萃值趋于平衡。
[0073]
实施例5:反萃动力学
[0074]
水相料液(金属离子溶液):为模拟料液(硫酸盐体系),料液含ni
2
3.54g/l,co
2
0.35g/l,zn
2
0.18g/l,ca
2
0.5g/l,mg
2
9.54g/l,mn
2
2.25g/l,ph为5.57。
[0075]
初始有机相:以磺化煤油为稀释剂,异丁酸浓度为0.5mol/l,3-羟基-5-乙基-壬烷-4-肟浓度为0.35mol/l,三丁基氧化膦浓度为0.5mol/l。
[0076]
负载有机相:上述初始有机相与料液相比为(o/a)1:1,混合时间为5min,振荡频率300r/min,温度25℃,使用碳酸钠调节萃取平衡ph为5.5进行萃取。
[0077]
反萃取:使用负载有机相与20g/l硫酸相比为(o/a)1:1,混合时间分别为1、2、3、5、8、10、15min,振荡频率300r/min,温度25℃,进行反萃取,实验结果如图3所示。
[0078]
由图3可以看出,该反萃取反应速度很快,当反应时间为5min时,镍和钴的反萃取率接近100%。同时锌、钙、镁、锰同样很好反萃。在常温条件下,通过添加有机氧化膦类萃取剂,能够提高镍的反萃速率以及反萃率。
[0079]
实施例6
[0080]
水相料液(金属离子溶液):为模拟料液(硫酸盐体系),料液含ni
2
3.54g/l,co
2
0.35g/l,zn
2
0.18g/l,ca
2
0.5g/l,mg
2
9.54g/l,mn
2
2.25g/l,ph为5.57。
[0081]
洗水:为模拟洗涤液(硫酸盐体系),含ni
2
0.5g/l,ph为2.0。
[0082]
初始有机相:以磺化煤油为稀释剂,异丁酸浓度为0.5mol/l,3-羟基-5-乙基-壬烷-4-肟浓度为0.35mol/l,三丁基氧化膦浓度为0.5mol/l。
[0083]
萃取:上述初始有机相与料液相比为(o/a)1:1,混合时间为5min,振荡频率300r/min,温度25℃,使用碳酸钠调节萃取平衡ph为5.5进行萃取。
[0084]
洗涤:将负载有机相与洗涤液相比为(o/a)10:1,混合时间3min,振荡频率300r/min,温度25℃,使用碳酸钠调节洗涤平衡ph分别为3.0、4.0、4.5、5.0、5.5、6.0进行洗涤。实验结果如图4所示。
[0085]
由图4可以看出,当洗涤平衡ph在4.5-5.5之间时,钴和锌的洗脱率很高,而镍的洗脱率较低,能够实现镍与钴锌的分离。
[0086]
在先专利使用烷基羟基肟、羧酸萃取剂和有机胺组成协萃体系(cn114317961a一种用于镍钴共萃的协萃体系及其共萃方法)。在先专利的协萃体系和本技术方案的协萃体系在不同方面各有优势,在功效上两者形成良好补充。例如,使用烷基羟基肟、羧酸萃取剂和有机胺组成协萃体系的一大优势在于:协萃体系中含有对锌萃取能力强的有机碱,使得该协萃体系能在较低的ph值(ph=2.0)条件下萃取锌而基本不萃取镍钴,从而实现锌与镍
钴的良好分离,因为萃取镍钴的理想ph值范围为4.5-6.0。无需再将镍钴与锌进行分离,大大简化了分离流程,既有利于节能减排,又大幅降低了运行成本。
[0087]
而在本技术方案中,使用有机氧化膦类萃取剂代替有机胺,在萃取和反萃过程中,分相速度加快。添加有机氧化膦类萃取剂,能够将烷基羟基肟与镍形成的螯合物,变成镍的配合物。从而在很短的时间以及室温条件(无需加热)下并使用酸为反萃剂,可以轻易地使镍反萃下来,解决了反萃镍困难的问题,同时它的添加不会影响萃取速率以及萃取率,实现镍和钴的共萃。并且,如果想直接实现镍钴的分离(而不是镍钴的共反萃)的时候,我们可以通过洗涤实现镍与钴锌的分离,然后再通过反萃获取镍。而在使用烷基羟基肟、羧酸萃取剂和有机胺组成协萃体系时,并不能通过洗涤实现镍与钴锌的分离,并且使用该工艺耗碱量比较大,成本稍高。发明人尝试过按照本实施例的工艺条件,将三丁基氧化膦等量替换为甲基三丁基溴化胺,金属离子洗涤ph平衡等温线未出现图4中的规律,即无法找到钴和锌的洗脱率很高且镍的洗脱率较低的洗涤平衡ph。发明人还尝试过按照本实施例的工艺条件,不使用三丁基氧化膦(即初始有机相只含有异丁酸和3-羟基-5-乙基-壬烷-4-肟),无法找到钴和锌的洗脱率很高且镍的洗脱率较低的洗涤平衡ph。在分相速度方面,在本实施例中,萃取、反萃和洗涤均分相的速度均加快,尤其是洗涤分相的速度。更具体地,萃取分相只需要30s,洗涤分相只需要50s,反萃分相只需要40s。按照本实施例的工艺条件,将三丁基氧化膦等量替换为甲基三丁基溴化胺,萃取分相需要50s,反萃分相需要60s。
[0088]
实施例7
[0089]
水相料液(金属离子溶液):为模拟料液(硫酸盐体系),料液含ni
2
3.54g/l,co
2
0.35g/l,zn
2
0.18g/l,ca
2
0.5g/l,mg
2
9.54g/l,mn
2
2.25g/l,ph为5.57。
[0090]
洗水:为模拟洗涤液(硫酸盐体系),含ni
2
0.5g/l,ph为2.0。
[0091]
反萃取液:为模拟反萃取液(硫酸盐体系),含ni
2
6g/l,h2so
4 20g/l。
[0092]
初始有机相:以磺化煤油为稀释剂,异丁酸浓度为0.5mol/l,3-羟基-5-乙基-壬烷-4-肟浓度为0.35mol/l,三丁基氧化膦浓度为0.5mol/l。
[0093]
工艺条件:“两萃两洗两反”工艺。
[0094]
萃取:上述初始有机相与料液相比为(o/a)2:1,混合时间为5min,振荡频率300r/min,温度25℃,使用碳酸钠调节萃取平衡ph,第一级萃取平衡ph=5.3,第二级萃取平衡ph=5.6。
[0095]
洗涤:萃取后有机相与洗涤液相比为(o/a)10:1,混合时间为5min,振荡频率300r/min,温度25℃,使用碳酸钠调节萃取平衡ph,第一级洗涤平衡ph=4.5,第二级洗涤平衡ph=4.5。
[0096]
反萃取:使用负载有机相与20g/l硫酸相比为(o/a)1:1,混合时间为5min,振荡频率300r/min,温度25℃,进行两级反萃取。实验结果如表3所示。
[0097]
由表中数据可得,通过洗涤阶段,可以将钴、锌、钙、镁、锰有效的与镍分离,同时镍的损失率在4%以下。
[0098]
表3:“两萃两洗两反”工艺条件下萃取、反萃和洗脱效率
[0099]
金属元素钴镍锰镁钙锌两级萃取率(%)99.6899.9710.891.281.0599.57两级反萃率(%)99.9899.98\\\99.95
两级洗脱率(%)96.783.2199.9999.9899.9797.35
[0100]
实施例8:
[0101]
本实施例基本同实施例7,不同点在于有机氧化膦类萃取剂,r5、r6、r7均为碳原子数为12的正烷烃基。实验数据参见表4。
[0102]
表4:“两萃两洗两反”工艺条件下萃取、反萃和洗脱效率
[0103][0104][0105]
对比例1:
[0106]
水相料液(金属离子溶液):为模拟料液(硫酸盐体系),料液含ni
2
3.48g/l,co
2
0.79g/l,ca
2
0.98g/l,mg
2
10.78g/l,mn
2
2.97g/l,ph为5.21。
[0107]
初始有机相:以磺化煤油为稀释剂,异丁酸浓度为0.5mol/l,3-羟基-5-乙基-壬烷-4-肟浓度为0.35mol/l。
[0108]
萃取和反萃取:上述初始有机相与金属离子溶液相比为(o/a)1:1,混合时间5min,振荡频率300r/min,温度25℃,使用碳酸钠调节萃取平衡ph为5.5进行萃取。分相得到负载有机相和萃余液,使用负载有机相与50g/l硫酸相比为(o/a)1:1,混合时间5min,振荡频率300r/min,室温温度25℃,进行反萃取,获得空载有机相和反萃液。检测萃取后负载有机相和萃余液中的、反萃后的空载有机相和反萃液中的各金属离子的浓度,计算各种金属离子的萃取率(%)和反萃率(%)。萃取率的计算公式为:e=c1/c0,其中,c1为萃取到有机相中的目标金属浓度,c0为萃取之前金属离子溶液中目标金属到浓度。反萃率的计算公式为:s=c2/c1,c1为萃取到有机相中的目标金属浓度,c2为反萃到水相中的目标金属的浓度。经过检测和计算,得到如表5所示的结果。
[0109]
表5:协萃体系“异丁酸 3-羟基-5-乙基-壬烷-4-肟”的萃取反萃效果(表中实验数据为至少三次平行试验的平均值)
[0110]
金属元素钴镍锰镁钙萃取率(%)99.1297.515.410.220.11反萃率(%)98.7840.4599.1199.9899.97
[0111]
由表5可知,协萃体系“异丁酸 3-羟基-5-乙基-壬烷-4-肟”进行萃取时(没有使用有机氧化膦类萃取剂),虽然钴、镍的萃取均较好,萃取率分别为99.13%,97.51%,但是镍的反萃效果较差,反萃率仅为40.45%。因此该协萃体系不能有效的反萃取镍。
[0112]
作为对比,在初始有机相中加入0.5mol/l的三丁基氧化膦,其他条件不变,钴、镍的萃取率可保持在80%%和98%以上,并且钴、镍的反萃率可保持在99%和98%以上。说明了三丁基氧化膦的加入,在保持钴、镍的萃取率的基础上,保证了钴、镍的反萃率。
[0113]
对比例2
[0114]
本对比例基本同对比例1,不同点在于初始有机相:以磺化煤油为稀释剂,异丁酸浓度为0.5mol/l,3-羟基-5-乙基-壬烷-4-肟浓度为0.35mol/l,磷酸三丁酯浓度为0.5mol/
l。实验结果如表6所示。
[0115]
表6:协萃体系“异丁酸 3-羟基-5-乙基-壬烷-4-肟 磷酸三丁酯”的萃取反萃效果
[0116]
金属元素钴镍锰镁钙萃取率(%)96.8998.753.410.280.18反萃率(%)99.2555.7899.5599.9199.93
[0117]
由表6可知,协萃体系“异丁酸 3-羟基-5-乙基-壬烷-4-肟 磷酸三丁酯”进行萃取时,虽然钴、镍的萃取均较好,但是,在25℃的条件下镍的反萃效果较差。因此该协萃体系在室温条件下不能有效的反萃取镍。如果想要使用本对比例的协萃体系实现镍的反萃效果的提升,必须对反萃体积进行加热(至少40℃),会带来一定的能源浪费,以及设备成本的增加。
[0118]
对比例3
[0119]
本对比例基本同对比例1,不同点在于初始有机相:以磺化煤油为稀释剂,异丁酸浓度为0.5mol/l,3-羟基-5-乙基-壬烷-4-肟浓度为0.35mol/l,(2,4,4-三甲基戊基)次膦酸浓度为0.5mol/l。实验结果如表7所示。
[0120]
表7:协萃体系“异丁酸 3-羟基-5-乙基-壬烷-4-肟 (2,4,4-三甲基戊基)次膦酸”的萃取反萃效果
[0121]
金属元素钴镍锰镁钙萃取率(%)94.3596.056.740.580.99反萃率(%)99.8845.3899.8899.3499.75
[0122]
由表7可知,协萃体系“异丁酸 3-羟基-5-乙基-壬烷-4-肟 (2,4,4-三甲基戊基)次膦酸”进行萃取时,虽然钴、镍的萃取均较好,但是,在25℃的条件下镍的反萃效果较差。
[0123]
对比例4
[0124]
本对比例基本同实施例7,不同点在于,三丁基氧化膦浓度为2.05mol/l,浓度较理想范围高,导致萃取率降低。钴两级萃取率为60.78%,镍两级萃取率为70.83%。
[0125]
对比例5
[0126]
本对比例基本同实施例7,不同点在于,三丁基氧化膦浓度为0.05mol/l,浓度较理想范围低,导致反萃率降低。镍两级反萃率为51.24%。
[0127]
综合对比例4和对比例5的结果,三丁基氧化膦浓度过高或者过低,都不利于获得理想的工艺效果。相对于对比例4和对比例5,实施例7使用0.5mol/l的三丁基氧化膦浓度,萃取率和反萃都比较理想。并且将三丁基氧化膦在初始有机相中的浓度控制在0.1-2.0mol/l之间,可以实现镍、钴的高效萃取,并且在酸作为反萃剂的情况下,可实现镍、钴的高效反萃;还可以在萃取后洗涤过程中,实现镍与钴锌的有效分离。
[0128]
以上所述的仅是本发明的实施例,方案中公知的具体技术方案和/或特性等常识在此未作过多描述。应当指出,对于本领域的技术人员来说,在不脱离本发明技术方案的前提下,还可以作出若干变形和改进,这些也应该视为本发明的保护范围,这些都不会影响本发明实施的效果和专利的实用性。本技术要求的保护范围应当以其权利要求的内容为准,说明书中的具体实施方式等记载可以用于解释权利要求的内容。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。