一种天然产物( )-machaeriols b的合成方法
技术领域
1.本发明属于有机合成领域,特别涉及一种天然产物( )-machaeriols b合成方法。
背景技术:
2.( )-machaeriols b是一种从何首乌云杉的树皮中分离出来的、含有苯并呋喃结构的天然产物。据报道,它对金黄色酿脓葡萄球菌具有体外抗菌活性,此外它还显示出了强大的体外抗恶性疟原虫活性。这些重要的活性被人们注意到,促使合成这种天然产物的方法有了长足的发展。
[0003][0004]
该天然产物的主架结构包含2-芳基苯并呋喃,合成2-芳基苯并呋喃的方法已经有不少报道,具体如下:
[0005]
(1)钯金属催化临溴苯酚和末端炔完成sonogashira偶联-环化反应的过程,合成2-芳基苯并呋喃反应。 (villemin d,goussu d.palladium in homogeneous and supported catalysis:synthesis of functionalacetylenics and cyclization to heterocycles[j].heterocycles,1989,29(7):1255-61)。
[0006]
(2)铜催化临溴苯酚和末端炔完成sonogashira偶联-环化反应的过程,合成2-芳基苯并呋喃反应 (thomas a m,asha s,menon r,et al.one-pot synthesis of benzofurans via cu-catalyzed tandemsonogashira coupling-cyclization reactions[j].chemistryselect,2019,4(19):5544-7.)。
[0007]
(3)sc(otf)3作为催化剂,甲酸三乙酯作为添加剂,1,4-苯醌和芳基甲基酮进行1,4加成和环化反应合成苯并呋喃衍生物(wu f,bai r,gu y.synthesis of benzofurans from ketones and 1,4-benzoquinones[j]. adv synth catal,2016,358(14):2307-16.)。
[0008]
(4)
t
buok介导的烷基自由基对醛类化合物的分子间加成反应,经过分子内环化合成苯并呋喃 (zheng h-x,shan x-h,qu j-p,et al.strategy for overcoming full reversibility of intermolecular radicaladdition to aldehydes:tandem c-h and c-o bonds cleaving cyclization of(phenoxymethyl)arenes withcarbonyls to benzofurans[j].org lett,2018,20(11):3310-3.)。
[0009]
使用这些方法合成2-芳基苯并呋喃仍然有不少问题,例如使用昂贵的过渡金属催化剂,合成最终产物需要设计多步反应。使用更加高效简单的方法合成2-芳基苯并呋喃,对合成此类天然产物有着重大意义。
技术实现要素:
[0010]
本发明提供了一种合成天然产物( )-machaeriols b的新路线,而且本发明合成方法简单、路线短、成本低、起始原料简单易于合成,不需要制备复杂的前体。本发明介绍的天然产物( )-machaeriols b的合成路线参见式2。
[0011][0012]
本发明天然产物( )-machaeriols b的具体合成方法包括如下步骤:
[0013]
(1)2-(3,5-二甲氧基苯基)苯并呋喃的合成
[0014]
氩气保护下,将双(三甲基硅烷基)氨基铯加入四氢呋喃中,加入邻氟甲苯,搅拌均匀,加入n,3,5
‑ꢀ
三甲氧基-n-甲基苯甲酰胺。在180℃下回流12小时,冷却至室温,加水淬灭反应,减压去除溶剂,粗产品柱层析分离,得到产品2-(3,5-二甲氧基苯基)苯并呋喃。
[0015]
(2)5-(苯并呋喃-2-基)苯-1,3-二醇的合成
[0016]
氩气保护下,将2-(3,5-二甲氧基苯基)苯并呋喃加入二氯甲烷中,将反应体系降至-78℃,将三溴化硼缓慢滴加至反应体系中,搅拌反应,缓慢将体系温度升至室温,搅拌24小时。加水淬灭反应,减压去除溶剂,粗产品柱层析分离,得到产品5-(苯并呋喃-2-基)苯-1,3-二醇。
[0017]
(3)( )-machaeriols b的合成
[0018]
氩气保护下,将5-(苯并呋喃-2-基)苯-1,3-二醇加入间二甲苯中,加入香茅醛5,加入乙二胺-n,n
′‑
二乙酸(edda),加入三乙胺,160℃下回流24小时。加水淬灭反应减压去除溶剂,粗产品柱层析分离,得到产品( )-machaeriols b。
[0019]
说明书附图
[0020]
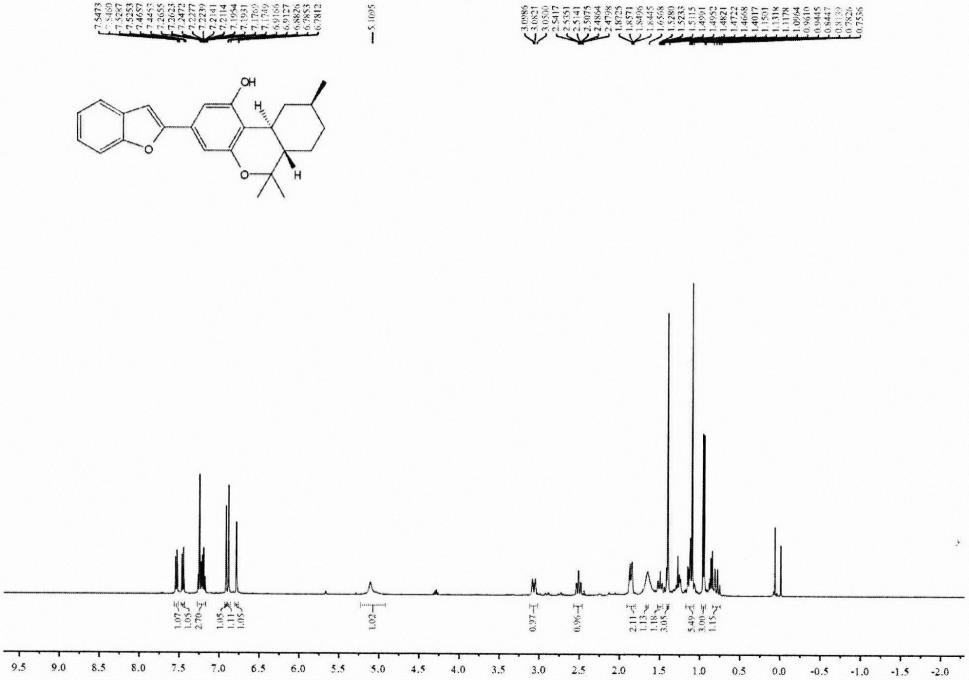
附图为实施例3产物的氢谱及碳谱核磁共振谱图,图1a为氢谱核磁共振谱图,图1b为碳谱核磁共振谱图,实施例3所得产物的氢谱图和碳谱图分别为图1a和图1b。
具体实施例
[0021]
实施例1
[0022]
氩气环境下,将双(三甲基硅烷基)氨基铯(175.8mg,0.6mmol)加入微波管中,之后加入1ml 2
‑ꢀ
氟甲苯,加入1ml四氢呋喃,搅拌均匀,加入n,3,5-三甲氧基-n-甲基苯甲酰胺(67.5mg,0.3mmol),在180℃下回流12小时,冷却至室温,加水淬灭反应,减压去除溶剂,粗
产品柱层析分离(石油醚),即可得2-(3,5-二甲氧基苯基)苯并呋喃(35.8mg,47%产率),为白色固体。
[0023]
实施例2
[0024]
氩气环境下,将2-(3,5-二甲氧基苯基)苯并呋喃(33.0mg,0.13mmol)加入二氯甲烷(5ml)中,将反应体系降至-78℃,将三溴化硼(79mg,0.31mmol)缓慢滴至反应体系中,搅拌反应,缓慢将体系温度升至室温,搅拌24小时。加入冰水淬灭反应,减压去除溶剂,粗产品柱层析分离(石油醚∶乙酸乙酯=3∶1),得到产品5-(苯并呋喃-2-基)苯-1,3-二醇(28.2mg,96%),为红棕色固体。
[0025]
实施例3
[0026]
氩气环境下,将5-(苯并呋喃-2-基)苯-1,3-二醇(27.1mg,0.12mmol)加入间二甲苯(0.2ml)中,加入香茅醛5(40.8mg,0.27mmol),加入乙二胺-n,n
′‑
二乙酸(edda)(4.19mg,0.024mmol),加入三乙胺 (0.2ml),160℃下回流24小时。加水淬灭反应减压去除溶剂,粗产品柱层析分离(石油醚∶乙酸乙酯=5∶1),得到产品( )-machaeriols b(28.2mg,65%),为棕色固体。产物的氢谱和碳谱核磁共振谱图分别为图1a和图1b,谱图数据为:1h nmr(400mhz,chloroform-d)δ:7.54(d,j=6.9hz,1h),7.46(d,j=8.1hz, 1h),7.27-7.17(m,2h),6.91(d,j=1.6hz,1h),6.88(s,1h),6.78(d,j=1.6hz,1h),5.11(s,1h),3.07(d,j= 12.8hz,1h),2.51(td,j=11.1,2.6hz,1h),1.86(dd,j=7.1,4.1hz,2h),1.66(s,1h),1.54-1.46(m,1h), 1.40(s,3h),1.18-1.07(m,5h),0.95(d,j=6.6hz,3h),0.84-0.74(m,1h)ppm.
13
c{1h}nmr(101mhz, chloroform-d)δ:155.66,155.61,155.41,154.78,129.64,129.29,124.20,122.93,120.95,114.04,111.17,107.11,104.00,101.23,49.09,38.82,35.76,35.54,32.99,28.12,27.80,22.70,19.16ppm。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。
