1.本发明属于感染实验模型构建领域,具体涉及一种急性脓毒症非人灵长类动物模型及其构建方法。
背景技术:
2.脓毒症(sepsis)是由细菌等病原微生物侵入机体引宿主全身炎症反应或免疫紊乱的过程。脓毒症可导致机体凝血系统激活和免疫反应失调,主要表现为血浆蛋白浓度降低、外周血小板计数减少、中性粒细胞技术增多等,最显著的变化为血清c-反应蛋白(c-reactive protein,crp)及降钙素原(procalcitonin,pct)水平升高。除血液指标显著变化为,严重的脓毒症病症会引起机体多个器官功能改变,其病情凶险、治疗成本高昂。
3.近年来,尽管针对脓毒症的实验与临床研究日趋增多,但脓毒症的具体发生机制仍缺乏深入认知,这对脓毒症的相关临床防治研究及药物研发及其不利,因此,了解脓毒症病程的发生发展尤为重要。已有研究报道,抗促炎因子对小鼠脓毒症治疗具有一定作用,然而在临床研究中此方法并无成效,尽管引起结论相悖的原因非常复杂,但采用的动物模型不合临床病理是显而易见的。因此,脓毒症动物模型作为为研究相关病症发病机制及临床防治所必须的实验平台,同时也是研究脓毒症的难点之一。
4.目前,脓毒症动物模型的构建方法主要包括1)通过盲肠结扎穿孔术(clp),2)升结肠支架置入腹膜炎(casp)制作腹腔感染的脓毒症模型,3)通过注射细菌内毒素(lps)构建脓毒血症模型。clp模型可模拟肠道细菌移位引起脓毒性休克,但漏入腹腔的粪便物质在实验组与对照组间很难控制,且由于动物的个体差异使得结扎后的坏死区域大小不均一,从而引起感染程度的不同。casp模型与clp模型类似,也是通过破坏宿主屏障造成细菌移位,进一步引起炎症,但两种方法引起的机体反应不尽相同。以lps作为感染源构建的脓毒症模型通过注射lps式诱导脓毒血症的发生,此法虽易重复,但并非所有细菌菌壁都含有脂多糖,如厚壁菌门所包含的芽孢杆菌、李斯特菌、葡萄球菌等细菌菌壁为肽聚糖。此外,国外研究报道了balb/c小鼠通过小剂量临床分离的绿脓杆菌联合30%烧伤构建的脓毒症模型,但由于临床分离菌群批次不同,毒性机理不同,从而影响模型稳定性。更重要的一点是,现有的脓毒症模型主要以啮齿类动物作为模式动物,但啮齿类动物与人类不仅在生理学方面不尽相同,在对脓毒性损伤的反应方面也存在的显著差异,如脓毒症期间产生的主要急性期蛋白在人类中是crp,而在小鼠中是sap。
5.综上可知,啮齿类动物与人类遗传背景的差异不能很好的模拟人类脓毒症的发生发展,且在模型的应用上,啮齿类动物在常规采血方法开展药物动力学研究耗损的动物数量较大,不利于动物保护福利。基于此,建立与人类病变相似、疾病谱完整、稳定可靠,同时能更好地模拟人类脓毒症时机体免疫系统紊乱的动物模型成为亟待解决的问题。非人灵长类动物由于其几乎相同的心肺解剖和生理学以及宿主对感染的反应,是一种较好的模拟人类脓毒症的模式动物。ravi shankar kesharia报道了利用大肠杆菌诱导的狒狒脓毒症模型研究补体对器官衰竭影响的研究,因其研究目的所以并未对于模型的构建方法进行详细
描述(keshari rs,silasi r,popescu ni,et al.inhibition of complement c5 protects against organ failure and reduces mortality in a baboon model of escherichia coli sepsis.proc natl acad sci u s a.2017;114(31):e6390-e6399.doi:10.1073/pnas.1706818114)。
技术实现要素:
6.为了克服现有技术存在的问题,本发明的目的是提供一种急性脓毒症非人灵长类动物模型及其构建方法。与啮齿类动物作为模式动物构建的模型相比,本发明提供的急性脓毒症非人灵长类动物模型具有更好的模拟人类脓毒症生理过程的优点,对开展相关领域的营养素及药物研发具有重要意义。
7.本发明的目的至少通过如下技术方案之一实现。
8.本发明的目的是为了解决现有脓毒症模型与人类试剂脓毒症生理过程差异较大的问题,提供一种急性脓毒症非人灵长类动物模型的构建方法。
9.本发明提供了一种急性脓毒症非人灵长类动物模型的构建方法,所述构建方法对非人灵长类动物注射细菌,使该动物患上急性脓毒症,所述细菌的类型是大肠杆菌,大肠杆菌的单次注射剂量是1.0
×
10^3个/kg~8.0
×
10^8个/kg。
10.进一步地,所述构建方法中,所述非人灵长类动物为食蟹猴。
11.进一步地,所述构建方法中,所述食蟹猴的年龄范围是5-25岁。
12.进一步地,所述构建方法中,所述食蟹猴的饲养方式为单笼饲养。
13.进一步地,所述构建方法中,所述大肠杆菌的菌液浓度是6.3
×
10^3个/ml~6.3
×
10^8个/ml。
14.进一步地,所述构建方法中,所述注射的方式是动物四肢静脉注射。
15.进一步地,所述构建方法中,所述大肠杆菌的注射方法是:0.5~3.0ml/kg。
16.进一步地,所述构建方法中,所述大肠杆菌的注射方法是:0.5~2.0ml/kg。
17.进一步地,所述构建方法中,所述大肠杆菌的注射方法是:1ml/kg,注射1次。
18.本发明还提供所述一种急性脓毒症非人灵长类动物模型的构建方法构建得到的急性脓毒症非人灵长类动物模型,模型动物在注射大肠杆菌120h内血液多项指标发生显著变化:反映机体炎症及全身性感染相关指标的c-反应蛋白以及降钙素原水平显著升高;反映机体发生急性免疫反应的白细胞数量及中性粒细胞百分比占比显著升高;谷丙转氨酶、谷草转氨酶升高以及白蛋白水平降低反映了肝功能受损,活化部分凝血活酶时间延长以及凝血酶原活动度降低反映了凝血功能紊乱。
19.进一步地,动物在注射大肠杆菌120h内血液中的指标发生显著变化:c-反应蛋白以及降钙素原作为机体脓毒症状态的生物标志物的水平显著升高。
20.本发明构建的急性脓毒症非人灵长类动物模型,与现有技术相比,本发明具有如下优点和有益效果:
21.(1)本发明构建的急性脓毒症非人灵长类动物模型,相比啮齿类动物作为模式动物构建的模型,其生理、病理、解剖结构等与人类更接近,更适用于人类脓毒症相关治疗方法、药物以及营养素的开发。
22.(2)本发明构建模型的方法简单,构建的模型结果稳定,填补急性脓毒症食蟹猴模
型的空白,能够很好的推广应用到脓毒症领域的研究。
附图说明
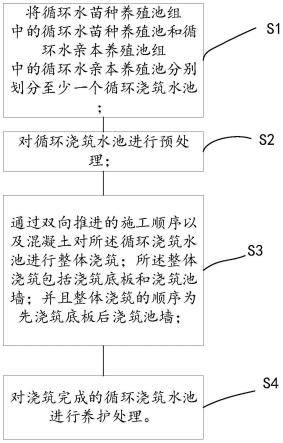
23.图1为本发明急性脓毒症非人灵长类动物模型的构建流程图。
24.图2为大肠杆菌注射剂量为0.5ml/kg,1.0ml/kg,1.5m l/kg,3.0ml/kg构建所得的急性脓毒症非人灵长类动物模型120h内的降钙素原的变化图。
25.图3为大肠杆菌注射剂量为0.5ml/kg,1.0ml/kg,1.5m l/kg,3.0ml/kg构建所得的急性脓毒症非人灵长类动物模型120h内的c-反应蛋白的变化图。
26.图4是大肠杆菌剂量为6.3
×
10^3个/kg时构建所得的急性脓毒症模型120h内体温、c-反应蛋白以及降钙素原的变化图。
27.图5是大肠杆菌剂量为6.3
×
10^3个/kg时构建所得的急性脓毒症模型120h内的血清生化水平(谷丙转氨酶,谷草转氨酶,白蛋白以及球蛋白)变化结果图。
28.图6是大肠杆菌剂量为6.3
×
10^3个/kg时构建所得的急性脓毒症模型120h内的全血细胞(白细胞数量,中性粒细胞百分比占比,血小板数量,淋巴细胞占比,红细胞数量,血红蛋白浓度)计数结果图。
29.图7是大肠杆菌剂量为6.3
×
10^3个/kg时构建所得的急性脓毒症模型120h内的凝血指标(活化部分凝血活酶时间,血浆凝血酶原时间,凝血酶时间,凝血酶原活动度,纤维蛋白原,样本pt与正常对照pt之比的isi次方)结果图。
30.图8是大肠杆菌剂量为6.3
×
10^5个/kg时构建所得的急性脓毒症模型120h内体温、c-反应蛋白以及降钙素原的变化图。
31.图9是大肠杆菌剂量为6.3
×
10^5个/kg时构建所得的急性脓毒症模型120h内的血清生化水平(谷丙转氨酶,谷草转氨酶,白蛋白以及球蛋白)变化结果图。
32.图10是大肠杆菌剂量为6.3
×
10^5个/kg时构建所得的急性脓毒症模型120h内的全血细胞(白细胞数量,中性粒细胞百分比占比,血小板数量,淋巴细胞占比,红细胞数量,血红蛋白浓度)计数结果图。
33.图11是大肠杆菌剂量为6.3
×
10^5个/kg时构建所得的急性脓毒症模型120h内的凝血指标(活化部分凝血活酶时间,血浆凝血酶原时间,凝血酶时间,凝血酶原活动度,纤维蛋白原,样本pt与正常对照pt之比的isi次方)结果图。
34.图12是大肠杆菌剂量为6.3
×
10^8个/kg时构建所得的急性脓毒症模型120h内体温、c-反应蛋白以及降钙素原的变化图。
35.图13是大肠杆菌剂量为6.3
×
10^8个/kg时构建所得的急性脓毒症模型120h内的血清生化水平(谷丙转氨酶,谷草转氨酶,白蛋白以及球蛋白)变化结果图。
36.图14是大肠杆菌剂量为6.3
×
10^8个/kg时构建所得的急性脓毒症模型120h内的全血细胞(白细胞数量,中性粒细胞百分比占比,血小板数量,淋巴细胞占比,红细胞数量,血红蛋白浓度)计数结果图。
37.图15是大肠杆菌剂量为6.3
×
10^8个/kg时构建所得的急性脓毒症模型120h内的凝血指标(活化部分凝血活酶时间,血浆凝血酶原时间,凝血酶时间,凝血酶原活动度,纤维蛋白原,样本pt与正常对照pt之比的isi次方)结果图。
具体实施方式
38.以下结合附图和实例对本发明的具体实施作进一步说明,但本发明的实施和保护不限于此。需指出的是,以下若有未特别详细说明之过程,均是本领域技术人员可参照现有技术实现或理解的。所用试剂或仪器未注明生产厂商者,视为可以通过市售购买得到的常规产品。
39.图1为本发明急性脓毒症非人灵长类动物模型的构建流程图。
40.实施例1
41.本实验选用18只8-16岁成年食蟹猴分为a,b,c,d,四组,分别给与正常饲料单笼饲养,适应喂养7天。食蟹猴适应性喂养期间,将大肠杆菌atcc25922标准菌株以营养琼脂培养基37℃下有氧培养18小时,得到菌液稀释至5
×
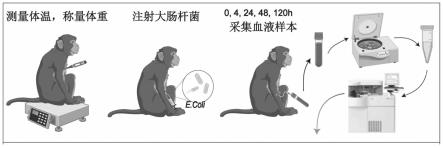
10^5个/ml。对食蟹猴进行夜间禁食,于次日早晨7:30-8:00称量体重。将食蟹猴称重后保定,左手臂内侧暴露向上,使用动物剃毛器将毛发去除,酒精棉球擦拭,使静脉充盈。将分为a,b,c,d四组的食蟹猴分别以0.5ml/kg,1.0ml/kg,1.5ml/kg,3.0ml/kg进行大肠杆菌静脉注射,平行进针,推注菌液后用干棉球按压止血,a,b,c,d四组的食蟹猴此大肠杆菌atcc25922剂量为2.5
×
10^5个/kg,5
×
10^5个/kg,7.5
×
10^5个/kg,1.5
×
10^6个/kg。测定0h、4h、24h、48h以及120h时食蟹猴体温,同时通过四肢静脉对食蟹猴进行血液样本采集。利用分离胶促凝管采集全血2ml,3000r/min,4℃,离心15min,收集血清测定降钙素原及c-反应蛋白。
42.实验结果
43.图2-3为大肠杆菌注射剂量0.5ml/kg,1.0ml/kg,1.5ml/kg,3.0ml/kg时构建所得的急性脓毒症非人灵长类动物模型120h内pct及crp含量变化图。由图2及图3可知,相同浓度大肠杆菌的四种注射体积均可引起食蟹猴机体降钙素原及crp水平的显著升高,降钙素原及c-反应蛋白对细菌感染诊断具有较高的敏感性和特异性,是诊断脓毒症常用的生物标志物,由此可知,急性脓毒症非人灵长类动物模型构建成功。
44.实施例2
45.一种急性脓毒症非人灵长类动物模型的构建方法,包括如下步骤:
46.本实验选用6只12-18岁成年食蟹猴,给与正常饲料单笼饲养,适应喂养7天。食蟹猴适应性喂养期间,将大肠杆菌atcc25922标准菌株以营养琼脂培养基37℃下有氧培养18小时,得到菌液稀释至6.3
×
10^3个/ml。对食蟹猴进行夜间禁食,于次日早晨7:30-8:00称量体重。将食蟹猴称重后保定,左手臂内侧暴露向上,使用动物剃毛器将毛发去除,酒精棉球擦拭,使静脉充盈。将大肠杆菌以1ml/kg进行静脉注射,平行进针,推注菌液后用干棉球按压止血,此大肠杆菌atcc25922剂量为6.3
×
10^3个/kg。测定0h、4h、24h、48h以及120h时食蟹猴体温,同时通过四肢静脉对食蟹猴进行血液样本采集。利用edta抗凝管采集全血1.5ml,2小时内利用血常规分析仪测定全血细胞计数;枸椽酸钠抗凝管采集全血2.0ml,测定凝血指标;分离胶促凝管采集全血3ml,3000r/min,4℃,离心15min,收集血清测定炎症及生化指标。
47.实验结果:
48.图4-7为低剂量大肠杆菌剂量为6.3
×
10^3个/kg时构建所得的急性脓毒症非人灵长类动物模型的研究结果。研究结果表明,低剂量大肠杆菌注射24h时可引起食蟹猴机体crp显著升高。此外,白细胞数量以及中性粒细胞数量也显著升高,其中中性粒细胞是一种
多形核白细胞,具有吞噬、氧化破裂、中性粒细胞胞外陷阱(nets)以执行微生物杀灭等功能,同时也是急性炎症的主要作用细胞之一,通常是第一个被招募到炎症部位的白细胞,由结果可知,食蟹猴经静脉注射大肠杆菌后机体中性粒细胞在迅速升高,进一步表明急性脓毒症非人灵长类动物模型构建成功。
49.实施例3
50.一种急性脓毒症非人灵长类动物模型的构建方法,包括如下步骤:
51.本实验选用6只15-20岁成年食蟹猴,给与正常饲料单笼饲养,适应喂养7天。食蟹猴适应性喂养期间,将大肠杆菌atcc25922标准菌株以营养琼脂培养基37℃下有氧培养18小时,得到菌液稀释至6.3
×
10^5个/ml。对食蟹猴进行夜间禁食,于次日早晨7:30-8:00称量体重。将食蟹猴称重后保定,左手臂内侧暴露向上,使用动物剃毛器将毛发去除,酒精棉球擦拭,使静脉充盈。将大肠杆菌以1ml/kg进行静脉注射,平行进针,推注菌液后用干棉球按压止血,此大肠杆菌atcc25922剂量为6.3
×
10^5个/kg。测定0h、4h、24h、48h以及120h时食蟹猴体温,同时通过四肢静脉对食蟹猴进行血液样本采集。利用edta抗凝管采集全血1.5ml,2小时内利用血常规分析仪测定全血细胞计数;枸椽酸钠抗凝管采集全血2ml,测定凝血指标;分离胶促凝管采集全血3ml,3000r/min,4℃,离心15min,收集血清测定炎症及生化指标。
52.实验结果:
53.图8-11为中剂量大肠杆菌剂量为6.3
×
10^5个/kg时构建所得的急性脓毒症非人灵长类动物模型的研究结果。研究结果表明,此剂量大肠杆菌构建所得的急性脓毒症食蟹猴模型,其机体crp水平、白细胞数量及中性粒细胞占比均高于低剂量大肠杆菌构建所得脓毒症模型,表明此剂量下的模型急性脓毒症严重程度相对较高。
54.实施例4
55.一种急性脓毒症非人灵长类动物模型的构建方法,包括如下步骤:
56.本实验选用6只15岁成年食蟹猴,给与正常饲料单笼饲养,适应喂养7天。食蟹猴适应性喂养期间,将大肠杆菌atcc25922标准菌株以营养琼脂培养基37℃下有氧培养18小时,得到菌液稀释至6.3
×
10^8个/ml。对食蟹猴进行夜间禁食,于次日早晨7:30-8:00称量体重。将食蟹猴称重后保定,左手臂内侧暴露向上,使用动物剃毛器将毛发去除,酒精棉球擦拭,使静脉充盈。将大肠杆菌以1ml/kg进行静脉注射,平行进针,推注菌液后用干棉球按压止血,此大肠杆菌atcc25922剂量为6.3
×
10^8个/kg测定0h、4h、24h、48h以及120h时食蟹猴体温,同时通过四肢静脉对食蟹猴进行血液样本采集。利用edta抗凝管采集全血1.5ml,2小时内利用血常规分析仪测定全血细胞计数;枸椽酸钠抗凝管采集全血2ml,测定凝血指标;分离胶促凝管采集全血3ml,3000r/min,4℃,离心15min,收集血清测定炎症及生化指标。
57.实验结果:
58.图12-15高剂量大肠杆菌剂量为6.3
×
10^8个/kg时构建所得的急性脓毒症非人灵长类动物模型的研究结果。研究结果表明,此剂量大肠杆菌构建所得的急性脓毒症食蟹猴模型,其机体crp水平在注射大肠杆菌120h后仍较高;此外,降钙素原(pct)是用于表征全身性感染及脓毒症的指标之一,炎性细胞因子特别是细菌内毒素可在几乎任何器官中刺激pct的产生,导致大量的降钙素原释放到血液,由结果可以看出,此剂量下pct水平48h内也显著升高。与低、中剂量大肠杆菌相比,高剂量大肠杆菌会引起血液谷丙转氨酶(alt)、谷草
转氨酶(ast)升高以及白蛋白(alb)水平显著降低。alt及ast升高是肝细胞损伤的敏感指标,同时alb是主要在肝脏中合成,alb水平的降低进一步表明肝脏功能的损伤。因此,由结果可知高剂量大肠杆菌引起了食蟹猴肝脏的损伤。凝血因子大部分均在肝细胞内合成,在肝脏功能正常时凝血因子的含量和活动度在正常范围,当肝脏实质受到损伤,凝血酶原活动度呈现一定程度的减低,进一步表现出凝血功能紊乱,包括凝血时间延长、活化部分凝血活酶时间延长、血小板轻度下降以及血栓形成风险增高等。由结果可知,高剂量大肠杆菌可引起食蟹猴机体血小板降低,活化部分凝血活酶时间延长以及凝血酶原活动度的降低,与临床表现一致,表明高剂量的大肠杆菌可较好模拟人类急性脓毒症的生理变化。
59.本发明构建的急性脓毒症非人灵长类动物模型,相比啮齿类模型,其生理、病理、解剖结构等与人类更接近,更适用于人类脓毒症相关治疗方法、药物以及营养素的开发。造模方法简单,结果稳定,填补了脓毒症领域非人灵长类脓毒症食蟹猴模型的空白,能够很好的推广应用到脓毒症领域的研究。
60.上述实施例为本发明较佳的实施方式,但本发明的实施方式并不受上述实施例的限制,其它的任何未背离本发明的精神实质与原理下所作的改变、修饰、替代、组合、简化,均应为等效的置换方式,都包含在本发明的保护范围之内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。