用于介入手术规划的计算模拟平台
1.相关申请的交叉引用
2.本技术要求2020年10月21日提交的并且名称为“computational simulation platform for planning of interventional pr ocedures”的美国非临时申请序列号17/076,213的优先权,其根据美国法典第35篇第119条(e)款要求2019年12月5日提交的并且名称为“comput ational simulation platform for planning of intervent ional procedures”的美国临时申请序列号62/944,054的优先权,所述申请以引用的方式整体并入本文。
技术领域
3.本发明总体上涉及用于模拟和规划介入手术的系统和方法。
背景技术:
4.冠状动脉疾病是西方社会的主要死亡原因。在美国每年进行的130万例经皮冠状动脉介入治疗中70%-90%植入了支架,其中20%涉及分叉。冠状动脉分叉仍然是介入心脏病学中最具挑战性的病变亚群之一,其手术成功率较低并且不良心脏事件发生率增加,介入后6个月至1年为15%-20%。代替复杂冠状动脉介入治疗(包括分叉)的频率不断增加,与分叉相关的不良后果的发生率预计将进一步增加。尽管药物洗脱支架减弱新生内膜形成,但药物洗脱支架的再狭窄仍然显著,特别是在分叉病变中与无分支区段相比,这表明支架置入技术和相关联的生物力学环境在这种解剖亚群的再狭窄倾向中起主导作用。事实上,药物洗脱支架并未解决与支架相关联的基本流体和固体力学问题,这些问题似乎显著地促成支架再狭窄,尤其是在分叉处。尽管人们对冠状动脉分叉有极大兴趣并且提出了多种技术策略,但分叉的经皮介入仍然具有挑战性,并且理想的治疗策略仍然难以实现。
5.由于没有两个分叉是相同的,因此不存在可应用于每个分叉的单一治疗策略。分叉介入中最重要的问题是选择针对特定分叉定制的最适当的技术。计算模拟有可能评估支架置入前和支架置入后分叉处的局部血流动力学微环境,从而提供对局部生物力学应力对新生内膜增生和支架血栓形成的作用的重要见解。介入后血流动力学与解剖支架再狭窄的定量关联可有助于优化支架置入技术和支架设计,从而最终改善临床结果。在现今的稳健计算时代,使用患者特定解剖和高分辨率冠状动脉内成像模态(例如光学相干断层扫描、血管内超声)以及实际边界条件和材料(动脉壁、球囊和支架)进行分叉支架模拟似乎是可行且准确的。在这些模拟中可考虑不同的支架和球囊设计和材料特性以及斑块材料特性(例如纤维、纤维脂肪、钙化)。根据患者的特定几何形状和生物力学环境定制分叉支架置入可有助于改善临床结果。
技术实现要素:
6.公开了一种用于介入手术规划的计算模拟平台。在实施方案中,所述计算模拟平台包括计算机实现的方法,所述计算机实现的方法包括:基于侵入性或非侵入性成像,生成
血管管腔和所述血管管腔的表面(例如,管腔壁和/或积聚在管腔壁上的任何斑块)的三维(3d)重建;生成经3d重建的血管管腔和所述血管管腔的表面的网格;向经3d重建的所述血管管腔的表面分配材料特性;导入支架和球囊的设计和材料特性;生成支架和球囊的网格;将网格化的支架和球囊定位在经3d重建的血管管腔和所述血管管腔的表面的所述网格内;利用经3d重建的血管管腔和所述血管管腔的表面的所述网格执行球囊扩张前、支架置入和球囊扩张后计算模拟;以及基于所述计算模拟,评估支架和血管形态测量学和生物力学指标。
7.在所述计算模拟平台的一些实施方案中,经3d重建的血管管腔和所述血管管腔的表面没有网格化。就此而言,3d重建本身可用于执行球囊扩张前、支架置入和球囊扩张后计算模拟。
8.在所述计算模拟平台的一些实施方案中,所述侵入性或非侵入性成像包括以下中的至少一者:冠状动脉造影、血管内超声、光学相干断层扫描或计算机断层扫描血管造影。
9.在所述计算模拟平台的一些实施方案中,所述支架和球囊的所述设计和材料特性是基于侵入性或非侵入性成像导入的。
10.在所述计算模拟平台的一些实施方案中,所述支架和球囊的所述设计和材料特性是从包括制造商提供的数据的一个或多个数据库导入的。
11.在所述计算模拟平台的一些实施方案中,处于其卷曲状态的网格化的支架和球囊通过计算定位在经3d重建的血管管腔和所述血管管腔的表面的所述网格中并弯曲。
12.在所述计算模拟平台的一些实施方案中,所述球囊扩张前、支架置入和球囊扩张后计算是使用有限元分析通过计算模拟的。
13.在所述计算模拟平台的一些实施方案中,所述材料特性是基于侵入性或非侵入性成像向经3d重建的所述血管管腔的表面分配的。
14.在所述计算模拟平台的一些实施方案中,所述基于侵入性或非侵入性成像向经3d重建的所述血管管腔的表面分配所述材料特性包括:基于侵入性或非侵入性成像,确定壁或斑块厚度、管腔面积、斑块偏心率和斑块成分。
15.在所述计算模拟平台的一些实施方案中,所述基于侵入性或非侵入性成像向经3d重建的斑块分配所述材料特性还包括:将所述血管管腔划分成斑块材料的连续区;以及分配范围为从纯钙斑块材料到纯脂质斑块材料的四分之一数。
16.在所述计算模拟平台的一些实施方案中,所述计算机实现的方法还包括:基于向经3d重建的斑块分配的所述材料特性,分配斑块塑性。
17.还公开了一种用于模拟和规划介入手术的系统。在实施方案中,所述系统包括:一个或多个医学成像设备;以及一个或多个计算机系统,所述一个或多个计算机系统通信地耦接到所述一个或多个医学成像设备。所述一个或多个计算机系统可被配置为:基于从所述一个或多个医学成像设备接收的侵入性或非侵入性成像数据,生成血管管腔和所述血管管腔的表面(例如,管腔壁和/或积聚在管腔壁上的任何斑块)的三维(3d)重建;生成经3d重建的血管管腔和所述血管管腔的表面的网格;向经3d重建的所述血管管腔的表面分配材料特性;导入支架和球囊的设计和材料特性;生成支架和球囊的网格;将网格化的支架和球囊定位在经3d重建的血管管腔和所述血管管腔的表面的所述网格内;利用经3d重建的血管管腔和所述血管管腔的表面的所述网格执行球囊扩张前、支架置入和球囊扩张后计算模拟;
并且基于所述计算模拟,评估支架和血管形态测量学和生物力学指标。
18.在所述系统的一些实施方案中,所述侵入性或非侵入性成像数据包括冠状动脉造影数据、血管内超声数据、光学相干断层扫描数据和/或计算机断层扫描血管造影数据。
19.在所述系统的一些实施方案中,所述支架和球囊的所述设计和材料特性是基于从所述一个或多个医学成像设备接收的侵入性或非侵入性成像数据导入的。
20.在所述系统的一些实施方案中,所述支架和球囊的所述设计和材料特性是从包括制造商提供的数据的一个或多个数据库导入的。
21.在所述系统的一些实施方案中,处于其卷曲状态的网格化的支架和球囊通过计算定位在经3d重建的血管管腔和所述血管管腔的表面的所述网格中并弯曲。
22.在所述系统的一些实施方案中,所述球囊扩张前、支架置入和球囊扩张后计算是使用有限元分析通过计算模拟的。
23.在所述系统的一些实施方案中,所述材料特性是基于从所述一个或多个医学成像设备接收的侵入性或非侵入性成像数据向经3d重建的所述血管管腔的表面分配的。
24.在所述系统的一些实施方案中,所述基于侵入性或非侵入性成像数据向经3d重建的所述血管管腔的表面分配所述材料特性包括:基于侵入性或非侵入性成像数据,确定壁或斑块厚度、管腔面积、斑块偏心率和斑块成分。
25.在所述系统的一些实施方案中,所述基于侵入性或非侵入性成像数据向经3d重建的所述血管管腔的表面分配所述材料特性还包括:将所述血管管腔划分成斑块材料的连续区;以及分配范围为从纯钙斑块材料到纯脂质斑块材料的四分之一数。
26.在所述系统的一些实施方案中,所述一个或多个计算机系统进一步被配置为:基于向经3d重建的斑块分配的所述材料特性,分配斑块塑性。
27.本发明内容仅仅作为对在具体实施方式和附图中充分描述的主题的介绍而提供。发明内容不应被视为描述必要特征,也不应用于确定权利要求的范围。此外,应当理解,前述发明内容和以下具体实施方式两者仅是示例性和解释性的,并且不一定限制所要求保护的主题。
附图说明
28.参考附图来描述详细描述。在描述和附图中的不同实例中使用相同的附图标记可指示类似或相同的项。以下详细描述和附图中公开了本公开的各种实施方案或示例(“示例”)。附图不一定是按比例绘制的。通常,除非权利要求中另有规定,否则可以任意顺序执行所公开过程的操作。
29.图1是示出根据本公开的一个或多个实施方案的用于介入手术的模拟和规划的系统的框图。
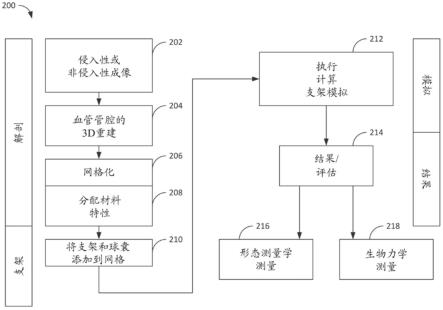
30.图2是示出根据本公开的一个或多个实施方案的用于介入手术规划的计算模拟平台的流程图。
31.图3是示出根据本公开的一个或多个实施方案的临床分叉支架置入模拟的工作流程的流程图。
32.图4示出根据本公开的一个或多个实施方案的用于在患者特定分叉处进行计算模拟工作台支架置入的过程。
33.图5示出根据本公开的一个或多个实施方案的支架置入模拟结果与微计算机断层扫描(μct)重建模型的比较的结果。
34.图6示出根据本公开的一个或多个实施方案的工作台分叉模型的计算支架置入模拟的定性比较的结果。
35.图7示出根据本公开的一个或多个实施方案的支架置入后的管腔的形态测量比较的结果。
36.图8示出根据本公开的一个或多个实施方案的计算支架置入与临床病例中的实际情况的形态测量比较的结果。
37.图9示出根据本公开的一个或多个实施方案的用于计算模拟临床支架置入的过程。
38.图10示出根据本公开的一个或多个实施方案的支架置入后的管腔的形态测量比较的结果。
39.图11示出根据本公开的一个或多个实施方案的计算支架置入与临床病例中的实际情况的形态测量比较的结果。
40.图12示出根据本公开的一个或多个实施方案的在支架置入之前和之后的单个模拟剖面与光学相干断层扫描(oct)的形态测量比较的结果。
41.图13示出根据本公开的一个或多个实施方案的计算流体动力学研究的结果。
42.图14示出根据本公开的一个或多个实施方案的患者特定硅胶分叉模型和生物反应器流动回路。
43.图15示出根据本公开的一个或多个实施方案的用于3d分叉重建步骤和血管造影处理的过程。
44.图16示出根据本公开的一个或多个实施方案的用于根据oct对分叉管腔进行3d重建的过程。
具体实施方式
45.本公开涉及用于介入手术规划的计算模拟平台。特别地,参考图1至图16公开计算支架置入平台。计算模拟可在导管插入术(catheterization)实验室中为冠状动脉疾病的解剖和功能评估产生增量信息,从而指导经皮介入。计算支架置入模型可在3d环境中并且以具有成本和时间效益的方式重现有争议的“假设(what if)”场景,以阐明支架置入手术期间发生的事件。计算支架置入可表征支架置入前和支架置入后的局部生物力学微环境,从而提供用于分叉支架置入优化的框架并且生成可临床测试的新假设。
46.迄今为止,已经报道了关于支架模拟的若干计算研究,其中绝大多数都集中在理想化的无分叉几何形状上。已经报道了关于分叉支架置入的有限计算研究。这些研究仅在有限数量(《2)的病例中使用简化斑块材料特性通过计算模拟1支架技术,并且未进行模拟与参考血管的定量比较。本公开提出用于完全计算的患者特定支架置入的新型平台。
47.图1示出根据本公开的一个或多个实施方案的用于介入手术的模拟和规划的系统100。系统100包括一个或多个计算机系统102(例如,计算机、执行不同步骤/过程的多个计算机和/或顺序地或并行地一起工作的计算机系统的本地或云计算集群)。系统100还包括一个或多个侵入性或非侵入性医学成像设备110,它们通信地耦接到一个或多个计算机系
统102。例如,一个或多个医学成像设备110可物理地连接(例如,有线连接)到一个或多个计算机系统102,无线地连接(例如,通过wifi、wlan、蓝牙等)和/或通过被配置为存储由一个或多个医学成像设备110收集的数据的至少一个便携式存储设备(例如,usb驱动器、便携式硬盘驱动器等)通信地耦接,使得数据可传输到一个或多个计算机系统102。
48.侵入性或非侵入性医学成像设备110的示例包括但不限于ct扫描仪、x射线扫描仪、荧光镜、超声扫描仪。在实施方案中,一个或多个侵入性或非侵入性医学成像设备110可包括任何数量或组合的前述设备。
49.一个或多个计算机系统102可被配置为通过执行本文讨论的各种功能、步骤和/或操作来实现计算模拟平台。在实施方案中,计算机系统102(或集群的每个计算机系统102)包括至少一个处理器104、存储器106和通信接口108。
50.处理器104为至少计算机系统102提供处理功能并且可包括任何数量的处理器、微处理器、微控制器、电路、现场可编程门阵列(fpga)或其他处理系统以及用于存储由计算机系统102访问或生成的数据、可执行代码和其他信息的常驻或外部存储器。处理器104可执行体现在非暂时性计算机可读介质(例如,存储器106)中的实现本文描述的技术/操作的一个或多个软件程序。处理器104不受形成其的材料或其中采用的处理机制的限制,并且因此可通过半导体和/或晶体管(例如,使用电子集成电路(ic)部件)等等来实现。
51.存储器106可以是有形计算机可读存储介质的示例,所述有形计算机可读存储介质提供存储功能以存储与计算机系统102/处理器104的操作相关联的各种数据和/或程序代码,诸如指示处理器104以及可能的计算机系统102的其他部件执行本文描述的功能的软件程序和/或代码段或其他数据。因此,存储器106可存储数据,诸如用于操作计算机系统102(包括其部件(例如,处理器104、通信接口108等))的指令程序等等。应当注意,虽然描述了单个存储器106,但是可采用广泛多种的存储器类型和组合(例如,有形的、非暂时性的存储器)。存储器106可与处理器104成为整体,可包括独立存储器,或者可以是两者的组合。存储器106的一些示例可包括可移动和不可移动存储器部件,诸如随机存取存储器(ram)、只读存储器(rom)、闪存存储器(例如,安全数字(sd)存储卡、迷你sd存储卡和/或微型sd存储卡)、固态驱动器(ssd)存储器、磁存储器、光学存储器、通用串行总线(usb)存储设备、硬盘存储器、外部存储器等等。
52.通信接口108可操作地被配置为与计算机系统102的部件通信。例如,通信接口108可被配置为从处理器104或其他设备(例如,医学成像设备110、其他计算机系统102、本地/远程服务器等)检索数据,传输数据以供存储在存储器106中,从存储器106中的存储装置检索数据等等。通信接口108还可与处理器104通信地耦接以促进计算机系统102的部件与处理器104之间的数据传输。应当注意,虽然通信接口108被描述为计算机系统102的部件,但通信接口108的一个或多个部件可实现为通过有线和/或无线连接通信地耦接到计算机系统102的外部部件。计算机系统102还可包括和/或连接到一个或多个输入/输出(i/o)设备(例如,通过通信接口108),诸如输入设备(例如,鼠标、轨迹球、触控板、操纵杆、触摸板、触摸屏、键盘、小键盘、麦克风(例如,用于语音命令)等)和/或输出设备(例如,显示器、扬声器、触觉反馈设备等)。在实施方案中,通信接口108还可包括发射器、接收器、收发器、物理连接接口或它们的任何组合或者可与它们耦接。
53.应当理解,本文描述的任何功能、步骤或操作不一定全部由一个计算机系统102执
行。在一些实施方案中,各种功能、步骤或操作可由一个或多个计算机系统102执行。例如,一个或多个操作和/或子操作可由第一计算机系统执行,另外的操作和/或子操作可由第二计算机系统执行等等。此外,操作和/或子操作中的一些可并行执行,并且不一定按本文中公开它们的顺序执行。
54.图2是示出用于介入手术规划的计算模拟平台200的流程图。在实施方案中,计算模拟平台200由包括以下框(例如,功能、步骤和/或操作)的计算机实现的方法来体现。
55.在框202处,收集一个或多个血管(例如,冠状动脉分叉或任何其他脉管系统或其部分)的侵入性或非侵入性成像数据。例如,通过一个或多个成像设备110,一个或多个计算机系统102可被配置为收集与一个或多个血管相关联的侵入性成像数据(例如,通过冠状动脉造影、血管内超声和/或光学相干断层扫描)和/或非侵入性成像数据(例如通过计算机断层扫描血管造影)。另外,通过一个或多个成像设备110,一个或多个计算机系统102可被配置为使用在下面讨论的示例性实施方案(例如,实施例1-3)中描述的工具和/或技术中的任一种来收集与一个或多个血管相关联的侵入性成像数据和/或非侵入性成像数据。
56.在框204处,基于由一个或多个成像设备110收集的侵入性或非侵入性成像数据,生成至少一个血管管腔(例如,冠状动脉分叉或任何其他脉管系统或其部分)和血管管腔表面(例如,管腔壁和/或积聚在管腔壁上的任何斑块)的3d重建。例如,一个或多个计算机系统102可被配置为基于侵入性(例如血管造影、光学相干断层扫描或血管内超声)或非侵入性(计算机断层扫描血管造影)成像模态或这些模态的任何组合,生成分叉管腔和壁/斑块的3d重建。特别强调重建动脉壁和斑块的真实尺寸(厚度、偏心率)。此外,经3d重建的分叉是患者特定的。另外,一个或多个计算机系统102可被配置为基于由一个或多个成像设备110收集的侵入性或非侵入性成像数据,使用在下面讨论的示例性实施方案(例如,实施例1-3)中描述的工具和/或技术中的任一种来生成至少一个血管管腔(例如,冠状动脉分叉或任何其他脉管系统或其部分)和血管管腔表面(例如,管腔壁和/或积聚在管腔壁上的任何斑块)的3d重建。
57.可选地,在框206处,生成经3d重建的血管管腔和血管管腔表面的网格。例如,一个或多个计算机系统102可被配置为使用在下面讨论的示例性实施方案(例如,实施例1-3)中描述的工具和/或技术中的任一种来生成经3d重建的血管管腔和血管管腔表面的网格。在所述计算模拟平台的一些实施方案中,经3d重建的血管管腔和所述血管管腔的表面没有网格化。就此而言,3d重建本身可用于执行球囊扩张前、支架置入和球囊扩张后计算模拟。
58.在框208处,向经3d重建的血管管腔表面分配材料特性。例如,一个或多个计算机系统102可被配置为基于由一个或多个成像设备110收集的侵入性或非侵入性成像数据,向经3d重建的血管管腔表面分配材料特性。基于从一个或多个医学成像设备110接收的成像数据,可向动脉壁和斑块分配实际材料特性。这可包括从脂质到纤维和钙化的材料的广泛覆盖,包括这些材料之间的广泛范围的组合。在一些实施方案中,一个或多个计算机系统102被配置为通过基于侵入性或非侵入性成像确定壁或斑块厚度、管腔面积、斑块偏心率和斑块成分,向经3d重建的血管管腔表面分配材料特性。在一些实施方案中,一个或多个计算机系统102进一步被配置为通过将血管管腔划分成斑块材料的连续区并且分配范围为从纯钙斑块材料到纯脂质斑块材料的四分之一数,向经3d重建的血管管腔表面分配材料特性。在一些实施方案中,一个或多个计算机系统102被配置为基于向经3d重建的斑块分配的材
料特性,分配斑块塑性。另外,一个或多个计算机系统102可被配置为基于由一个或多个成像设备110收集的侵入性或非侵入性成像数据,使用在下面讨论的示例性实施方案(例如,实施例1-3)中描述的工具和/或技术中的任一种来向经3d重建的血管管腔表面分配材料特性。
59.在框210处,导入支架和球囊的设计和材料特性并使用所述设计和材料特性来生成支架和球囊的网格。真实的支架设计和材料以及具有顺应性、半顺应性和非顺应性特性的实际扩张前和扩张后球囊几何形状都并入在计算平台200中。例如,一个或多个计算机系统102可被配置为基于从一个或多个医学成像设备110接收的侵入性或非侵入性成像数据,导入支架和球囊的设计和材料特性。替代地或另外地,一个或多个计算机系统102可被配置为从包括制造商提供的数据的一个或多个数据库导入支架和球囊的设计和材料特性。一个或多个计算机系统102可被配置为使用在下面讨论的示例性实施方案(例如,实施例1-3)中描述的工具和/或技术中的任一种来生成支架和球囊的网格,优选地结构化网格。处于其卷曲状态的网格化支架和球囊可通过计算定位在3d重建的血管管腔和血管管腔的表面的网格中并弯曲。在一些实施方案中,支架和球囊沿循动脉的真实3d路线弯曲并定位在管腔网格中。另外,一个或多个计算机系统102可被配置为使用在下面讨论的示例性实施方案(例如,实施例1-3)中描述的工具和/或技术中的任一种来导入支架和球囊的设计和材料特性,生成支架和球囊的网格和/或将支架和球囊的网格定位在经3d重建的血管管腔和血管管腔表面的网格内或相对于所述网格定位支架和球囊的网格。
60.在框212处,执行计算支架模拟。例如,一个或多个计算机系统102可被配置为利用经3d重建的血管管腔和血管管腔表面的网格来执行球囊扩张前、支架置入和球囊扩张后计算模拟。在一些实施方案中,球囊扩张前、支架置入和球囊扩张后计算是使用有限元分析通过计算模拟的。优选地,使用实际充胀压力。每个步骤的预加载可能是下一步骤的基线,从而致使管腔和壁扩张遵循实际模式。另外,一个或多个计算机系统102可被配置为使用在下面讨论的示例性实施方案(例如,实施例1-3)中描述的工具和/或技术中的任一种利用网格化结构来执行球囊扩张前、支架置入和球囊扩张后计算模拟。
61.在框214至218处,基于计算模拟,评估支架和血管形态测量学和生物力学指标。例如,一个或多个计算机系统102可被配置为评估形态测量学指标,包括但不限于支架扩张和贴壁。一个或多个计算机系统102可进一步被配置为使用计算流体动力学和有限元分析来评估生物力学指标(例如,血液动力学指标),包括但不限于动脉管腔、壁和支架中的流体和固体应力。另外,一个或多个计算机系统102可被配置为基于计算模拟,使用在下面讨论的示例性实施方案(例如,实施例1-3)中描述的工具和/或技术中的任一种来评估支架和血管形态测量学和生物力学指标。
62.所提出的计算支架置入平台200可在cath lab中为冠状动脉疾病的解剖和功能评估产生增量信息,从而指导经皮介入。患者特定计算支架置入模型可在3d环境中并且以具有成本和时间效益的方式重现有争议的“假设(what if)”场景,以阐明支架置入手术期间发生的事件。这些模型可表征支架置入前和支架置入后的局部生物力学微环境,从而提供用于支架置入优化的框架并且生成随后可临床测试的新假设。在强大的计算机时代,分叉支架置入的预测患者特定计算模拟是可行且可靠的。
63.分叉支架置入的计算模拟可有助于行业开发新一代支架,从而最终改善临床结
果。支架置入模拟有可能(接近)实时地用于指导分叉pci(自动舵pci),这可能对非专家介入医师特别有用。患者特定计算支架置入方法将分叉解剖、疾病复杂性和生物力学整合在综合方案中。这允许生成患者分叉和应用于整个现实世界分叉几何形状范围的各种支架置入技术的模拟的综合图谱集。这种患者分叉图谱集可有助于为特定的分叉解剖组确定有利的支架置入技术,并且为使用机器和深度学习策略在cath lab中进行实时决策奠定基础。此外,所提出的计算平台可演变为有用的教育和培训工具,并且最终可应用于其他血管床(即颈动脉分叉或主动脉分叉或结构性心脏病介入)。
64.在下面讨论的示例和实施方案(例如,实施例1-3)中讨论计算模拟平台200的具体实现方式。除非权利要求中另有说明,否则以下示例和实施方案不应被诠释为对本公开的限制。在其他实现方式中,在不脱离本公开的范围的情况下,可采用等效的系统、工具、材料、软件和/或过程。此外,在不脱离本公开的范围的情况下,关于特定实施方案描述的某些方面或配置可与另一个实施方案的任何方面或配置组合实现。
65.实施例1
–
患者特定工作台支架置入
66.硅胶分叉模型:使用内部技术创建患者特定冠状动脉分叉的四个工作台模型。具体地,根据人类冠状动脉造影对初始分叉几何形状进行3d重建。针对每个模型,设计阴模并利用丙烯腈丁二烯苯乙烯(abs)材料进行3d打印。在使用丙酮蒸汽使模具的内表面平滑之后,将聚二甲基硅氧烷(pdms)注入模具中,并且然后放入烘箱中以固化pdms。然后将物理模型浸入丙酮烧杯中以溶解abs并生成用于工作台测试的硅胶分叉模型。
67.对比增强微计算机断层扫描(μct)成像:为了获取高分辨率管腔几何形状,利用对比剂填充所有硅胶分叉模型,并且然后利用μct(例如,skyscan1172版本1.5,skyscan,antwerpen,belgium)使用以下参数进行扫描:图像像素大小(26.9μm)、电压(100kv)和电流(100μa)。将支架置入前的基于μct的重建3d模型用作计算支架模拟的解剖输入。
68.硅胶分叉模型的工作台支架置入:将硅胶分叉模型放置在定制的流动室中。将计算机控制的生物反应器回路连接到分叉的入口和出口,从而允许1l的去离子水以100ml/min的稳定流量循环。
69.立体扫描:利用立体显微镜(例如,olympus szx16,tokyo,japan)对部署在硅胶分叉模型中的所有支架进行成像。使用显微图像来测量支架边缘距固定点(例如,隆突)的距离并且指导支架在计算模型中的正确定位。
70.计算网格:使用hypermesh(altair engineering,troy,mi,usa)利用四节点四边形壳单元对通过μct进行的3d重建的管腔进行网格化。用于工作台支架置入手术的支架的计算机辅助设计模型由制造商(boston scientific,maple groove,mn,usa和medtronic vascular,santa rosa,ca,usa)按它们的标称尺寸提供。球囊在grasshopper(rhinoceros 6.0的插件,robert mcneel and associates,seattle,wa,usa)中以它们的卷曲状态通过计算创建。支架使用梁单元(resolute integrity和onyx.medtronic)或六面体单元(synergy,boston scientific)在hypermesh中进行网格化,而球囊则利用四边形有限膜应变单元进行网格化。
71.材料特性:将固化的硅胶样品切成矩形样本并使其经受单轴压缩测试。将获得的力位移曲线转换为应变应力曲线。使用neo-hookean超弹性模型来拟合非线性应变应力曲线。向每个分叉的壳单元分配特定厚度以表示硅胶模型的真实厚度。分别将顺应性、半顺应
性和非顺应性球囊的弹性模量定义为300mpa、900mpa和1,500mpa。
72.支架和球囊卷曲、定位和弯曲:通过置入支架的硅胶模型的血管造影、μct和立体图像来确定在计算分叉模型中的正确支架和球囊定位。首先通过使用由径向位移驱动的表面单元来使支架从其标称状态卷曲。将卷曲的支架和球囊沿动脉中心线定位并弯曲。
73.工作台支架置入手术的计算模拟:使用中心差分法(abaqus/explicit求解器)通过多步准静态有限元分析来模拟工作台支架置入手术。固定分叉管腔的边缘以避免刚体运动。约束球囊边缘以消除它们在所有方向上的运动。为了对不同单元(球囊-支架、支架-管腔、球囊-管腔、球囊-球囊)之间的相互作用建模,在摩擦系数为0.2的情况下使用稳健通用接触算法。向对应球囊的内表面上施加每个程序步骤中使用的实际充胀压力。将每个步骤之后的管腔和支架的受应力配置用作下一步骤的初始条件。考虑到计算模型中的大量单元和复杂接触,使用计算机集群(452intel xeon e5-2670 2.60ghz 2cpu/16内核和每个节点64gb ram,university of nebraska)来执行高速计算模拟。
74.计算工作台支架置入的训练:将支架置入后通过μct进行的3d重建的分叉和支架几何形状用作计算支架置入训练的基准数据(ground truth)。使用分叉隆突作为固定点对模拟分叉和μct分叉进行共同配准。使用平均管腔直径(mld)来进行比较研究。
75.结果:成功模拟所有工作台支架置入手术,其中大部分是多步二支架技术。图4示出利用两个支架的t型和突出(tap)技术的代表性示例。从视觉上看,通过计算模拟的支架在大小和形状上与实际的经μct重建支架几乎相同(图5(a))。沿模拟支架和经μct重建支架的轴向方向绘制mld(图5(b)),并且使用bland altman分析在方法之间对mld进行定量比较,产生0.02(-0.12至0.17)mm的最小平均差。
76.对比增强μct和立体图像进一步揭示所公开的计算支架置入平台能够以高精度复制工作台支架置入手术的细微细节,包括贴壁不良的支柱、侧分支孔口大小和形状以及隆突解剖敏感部位周围的支柱间隙(图6)。
77.实施例2
–
临床支架置入
78.患者数据:从propot(冠状动脉分叉病变近端优化技术随机试验,irb批准号15-159-2)选择七个患者病例进行患者特定计算模拟,propot是一项多中心、前瞻性、开放标签研究,在使用佐他莫斯洗脱支架(resolute integrity或onyx,medtronic)的冠状动脉分叉临时支架置入中比较近端优化技术与对吻球囊充胀。在经皮冠状动脉介入治疗(pci)前、支架置入后和手术结束时使所有患者经受多个血管造影平面下的冠状动脉造影和利用oct对主血管(mv)和侧分支(sb)的冠状动脉内成像。使用pci前解剖成像数据对患者特定冠状动脉分叉解剖进行3d重建,将所述患者特定冠状动脉分叉解剖用作计算支架置入模拟的解剖输入。图3中示出用于临床分叉支架置入的计算模拟的工作流程。
79.训练组:七例中使用五例来进行计算支架置入平台的训练,其中没有一个操作员不知情。在计算环境中复制这组病例中执行的所有pci步骤。将pci后oct数据用作用于与计算模拟进行比较的基准数据。
80.测试组:选择两个病例进行计算支架置入平台的测试。负责血管造影和oct成像分析、血管3d重建、计算支架置入模拟和比较研究的操作员彼此不知情。将支架置入模拟结果与pci后oct成像进行比较。
81.分叉几何形状的3d重建:根据血管造影和oct的融合对pci前分叉几何形状进行3d
重建,如先前所描述。简言之,分叉中心线从两个血管造影平面(pie medical imaging bv,maastricht,netherlands)生成,并且用作重建的主干。使用隆突作为参考点使分割的oct图像(echoplaque 4.0,indec,los altos,ca,usa)沿中心线对齐。之后进行逐步方法以描绘oct图像中的外边界,如先前所描述。所公开的方法在》95%的图像中成功进行并且涉及以下步骤:(i)在外壁边界不明确的情况下,将外壁限制在信号完全丢失的边缘;(ii)如果在《180度的血管圆周中无法标识信号完全丢失的边缘,则内插可见的外壁边界;以及(iii)如果在》180度的血管圆周中无法标识信号完全丢失的边缘,则丢弃该特定oct帧并按照相同的步骤(i-ii)分割相邻的帧。对经对齐的管腔和壁轮廓进行放样以构建mv和sb内表面和外表面,并且最终将mv和sb表面合并以创建pci前和pci后分叉管腔和壁。
82.计算网格:利用六面体单元(icem cfd 17.2,ansys,inc.,canonsburg,pa,usa)对经3d重建的分叉模型进行网格化。支架设计模型由制造商(medtronic vascular,santa rosa,ca,usa)以它们的标称尺寸提供。球囊在grasshopper中以它们的卷曲状态创建。支架和球囊分别使用完全六面体和四边形有限膜应变元进行网格化。
83.材料特性:在计算模拟中,通过oct确定壁厚、管腔面积、斑块偏心率和斑块材料。基于六阶多项式系数的应力/应变图所表示的实验数据,建立新型斑块评分系统。由成像专家(ysc)在mv和sb拉回的每个oct帧中评估脂质、纤维和钙化材料的面积、周长和厚度。值得注意的是,成像专家对测试组的模拟结果不知情。然后,将mv和sb划分成均质斑块材料的连续区。向每个区分配从 2(仅钙)至-2(仅脂质)的四分之一数(例如-0.25、0、 0.25等)。向以脂质为主的纤维脂质斑块分配-0.75或-0.5的分数,具有坏死核心的纤维脂质斑块-0.25,纤维斑块0,以纤维为主的纤维脂质斑块 0.25,具有中度钙的纤维钙化斑块 0.5,具有重度钙的纤维钙化斑块 0.75或 1。通过oct评估正常的壁厚和锥度。使用六阶简化多项式本构方程对正常壁材料进行建模,以表征各向同性超弹性力学行为,如先前所描述。通过将方程拟合到实验数据来获得动脉介质层的系数。基于材料特性,分配19%-25%的壁塑性。resolute integrity和onyx的钴合金mp35n使用von mises-hill塑性模型以各向同性硬化进行建模,而resolute onyx的pt-ir合金核心则以完美塑性建模。球囊建模为纯线性弹性材料,其材料特性与工作台组的模拟中的相同。
84.支架和球囊卷曲、定位和弯曲:首先使用由径向位移驱动的表面单元来使所有支架从其标称状态卷曲。将卷曲的支架和球囊沿中心线定位并弯曲(图3)。通过参考血管造影和oct上的基准标记(例如,支架/球囊的不透射线标记、隆突以及导丝的交点),将支架和球囊精确定位在分叉处。
85.计算模拟:使用中心差分法(abaqus/explicit求解器)通过多步、大变形、准静态有限元分析计算复制pci手术的所有步骤。边界条件和模拟参数如上所述。使用上面的计算机集群来执行计算模拟。
86.根据oct的3d支架重建:使用定制构建的grasshopper python代码根据oct和血管造影图像对支架进行3d重建。首先,将支架支柱分割为单独的点并展平为2d表面。使用2d支架设计模式作为参考,通过代表支架支柱和连杆的中心线的线连接支架点。将2d支架中心线包裹并映射回3d管腔中心线,并且然后添加支架支柱的体积。
87.计算流体动力学(cfd)研究:使用计算pci后分叉几何形状来离散流体域以进行cfd分析(图3)。使用icem cfd(ansys inc.,canonsburg,pa,usa)利用四面体单元对流体域
进行网格化。借助于fluent(ansys inc.)执行瞬态cfd模拟。在每条动脉的入口处施加脉动流。使用huo-kassab(hk)定律来推导两个子分支的直径比与通过分支的流量比之间的关系。管腔和支架表面近似为刚体,其中应用了无滑移边界条件。血液密度被认为是恒定的,值为1,060kg/m3。采用carreau模型来考虑血液的非牛顿性质。对于每个参数,使用以下值:μ
∞
=0.0035pa
·
s,μ0=0.25pa
·
s,λ=25s以及n=0.25。模拟了划分成100个时间步数的一个完整心动周期,其中步长时间为0.009s。
88.比较度量:将计算支架置入模拟之后的最终管腔和支架几何形状与在pci后oct上分割的管腔和支架剖面进行比较。使用来自pci后oct的剖面作为参考。使用隆突作为固定标记对oct剖面的模拟分叉和帧数进行共同配准。使用沿置入支架的mv的mld和平均支架直径(msd)作为比较度量。
89.统计方法:利用统计软件包graphpad prism 8.0(graphpad inc.,san diego,ca,usa)来执行统计分析。将连续变量表示为平均值
±
平均值的标准误差。使用bland-altman分析进行比较,认为p值《0.05具有统计学意义。
90.训练组结果:在训练组中,利用计算平台成功模拟临床支架置入手术,所有临床支架置入手术均利用一支架技术来执行。从视觉上看,通过计算置入支架的分叉管腔产生与支架置入后的血管造影管腔的高度定性一致性(图7)。bland altman分析揭示mld差异接近于零[平均偏差0.07mm(-0.31至0.45)mm]。类似地,通过计算模拟的支架表现出与通过融合oct和血管造影3d重建的实际支架的形状和大小的高相似性(图8(a)和(b))。将16个通过计算模拟的支架的msd与oct支架区段进行定量比较,产生非常高的一致性[平均偏差0.14mm(-0.22至0.49)mm]。值得注意的是,在患者#1中,计算模拟复制了继发于局部僵硬斑块材料的隆突周围支架扩张不足。在患者#5中,计算支架置入再现了支架支柱之间的大的间隙以及在近端支架后扩张之后随之而来的近端mv处过度扩张的管腔。
[0091]
测试组结果:在测试组中,使用术前解剖信息(血管造影和oct)来评估所公开的计算平台复制临床支架置入的能力(图9)。计算模拟操作员对术后oct不知情。如图10和图11所示,计算支架置入产生与术后oct的非常高的一致性,这表明平台的稳健性。bland-altman的定量比较显示mld和msd的差异小[平均偏差分别为0.09mm(-0.29至0.46)和0.13mm(-0.24至0.49)mm。图12提供术前oct的盲法使用的示例,用于将管腔面积、斑块厚度和偏心率的解剖信息并入到计算平台中并且还分配患者特定材料特性,以便实现产生与术后oct类似的管腔和支架扩张的实际计算模拟。
[0092]
cfd研究:为了显示cfd在所公开的模拟手术中的可行性,比较计算支架置入之前和之后的沿mv和sb的轴向方向的时间平均壁剪应力(tawss)(图13)。如定量和定性所示,支架置入使mv中的tawss归一化。
[0093]
所提出的用于患者特定分叉支架置入模拟的计算平台(即,计算模拟平台200)为临床研究、临床决策制定、支架制造和支架置入技术教育提供可靠的资源。更具体地,计算支架置入可用于使用患者特定解剖和生理学数据以及高度预测临床终点的替代终点(即扩张不足、贴壁不良、流体动力学)的虚拟(计算机模拟(in-silico))临床试验。这些虚拟临床试验可充分利用大量患者数据来研究不同支架置入技术或支架平台的性能,从而指导实际临床试验。当前正在进行的流动isr就是这种虚拟临床试验的示例。研究在患者特定冠状动脉分叉处比较不同的1支架技术和2支架技术。在心导管插入术实验室中,计算支架置入模
拟可用于术前规划和决策制定。确保最有利的支架扩张和贴壁的最佳支架置入和后扩张技术的计算标识同血流动力学微环境一起可向介入医师提供宝贵的指导,并且可能增加手术成功率和长期临床结果(精准医学)。对于支架制造商而言,使用患者特定解剖的具有成本和时间效益的计算支架置入策略有可能最小化对用于支架测试的工作台和动物研究的需要。计算模拟可有助于优化支架设计(例如冠部和连杆的数量、支柱大小)和力学(径向和纵向强度、扩张能力、血管支架效应)。计算方法可有效地估计实际血管环境中的不同支架设计,无需制造和实验测试支架原型,从而显著减少开发时间和制造成本。计算支架置入的另一个重要考虑因素是,它可用作培训工作人员和医生分叉支架置入技术的教育工具。混合现实技术可进一步帮助朝向这个方向发展。最后,计算分叉支架置入可转化为其他血管床(例如颈动脉、肾或主动脉分叉)。
[0094]
冠状动脉分叉代表心外膜冠状动脉树中具有增加的对冠状动脉疾病的易感性的独特解剖位置。分叉的特定解剖特征(包括主血管(mv)和侧分支(sb)的角度和直径)对局部血流动力学环境和随后的动脉粥样硬化倾向具有显著影响。分叉解剖和疾病范围是分叉支架置入策略和临床结果的实质性决定因素。分叉解剖和疾病负担的三维(3d)表示可有助于更好地了解分叉疾病的解剖复杂性并优化所公开的支架置入策略。
[0095]
可利用3d定量冠状动脉造影(3d qca)或冠状动脉计算机断层扫描血管造影(cta)执行冠状动脉分叉的专用单模态3d重建。然而,这两种模态具有以下主要限制:由于与使用两个2d血管造影平面相关的固有假设,3dqca无法提供分叉管腔的正确几何信息。尽管如此,3d qca提供关于分叉中心线的3d路线的准确细节。冠状动脉cta受到心肺运动伪影和冠状动脉钙化的限制,从而导致患者的下降(descent)部分的排除。已经描述了基于mv的血管内超声(ivus)或光学相干断层扫描(oct)仅与冠状动脉cta或侵入性血管造影术的融合对分叉的混合多模态3d重建。这些方法具有主要与sb重建的准确性有关的限制。值得注意的是,对mv和sb重建使用不同的成像模态导致几何上敏感和临床上重要的分叉隆突和sb的重建的不准确。此外,使用侵入性成像(ivus)进行mv重建以及使用非侵入性成像(cta)进行sb重建在临床环境中不易应用。
[0096]
本公开建立在当前最先进技术的基础上,并且提出用于基于侵入性冠状动脉造影(提供分叉中心线)与mv和sb两者的oct的融合进行冠状动脉分叉的3d重建的新型策略。执行本文描述的研究以:(i)描述冠状动脉分叉的3d重建的方法;并且(ii)系统地测试方法在患者特定硅胶分叉模型中的以及在患有不同程度疾病的患者冠状动脉分叉中的准确性、可行性和再现性。
[0097]
实施例3
–
冠状动脉分叉的3d重建
[0098]
硅胶模型:使用所公开的算法对五个患者特定冠状动脉分叉硅胶模型进行3d重建。使用可商购获得的软件(3d caas workstation 8.2,pie medical imaging,maastricht,the netherlands)根据心动周期的舒张阶段期间的人类冠状动脉造影对分叉几何形状进行3d重建。所述过程的流程图在图14(a)中示出。为了在成像过程期间定界感兴趣的区域并稳定硅胶模型,使用计算机辅助设计软件(rhinoceros 6,robert mcneel&associates,seattle,usa)在经重建的分叉的入口和出口处添加管状延伸和固定标记。针对每个模型,设计阴模并将其转换为立体光刻(stl)文件。使用stratasys dimension elite 3d打印机(stratasys,rehovot,israel)以178μm的分辨率利用丙烯腈丁二烯苯乙烯
材料对stl文件进行3d打印。使用丙酮蒸汽来产生平滑的内表面。将模具在室温下存放8-12小时,并且用蒸馏水清洁并干燥。将聚二甲基硅氧烷与其固化剂混合,并且然后放置于真空中达总共1小时30分钟以去除气泡。随后,将聚二甲基硅氧烷倒入干燥清洁的模具中,将所述模具放置于真空中以去除任何残留的气泡,并且然后放入烘箱中以使聚二甲基硅氧烷在65℃的温度下固化48小时。固化之后,将硅胶模型放入丙酮烧杯中,将所述丙酮烧杯放置于超声波清洁器(branson 1800,cleanosonic,virginia,usa)中达8-10小时以溶解所有丙烯腈丁二烯苯乙烯材料。
[0099]
对比增强微计算机断层扫描(μct)成像:利用μct(skyscanner 1172版本1.5)使用以下参数对所有分叉模型进行成像:图像像素大小26.94μm,电压100kv,电流100μa,以及切片厚度27μm。为了有效地可视化管腔边界,将碘化对比剂(37%)注入管腔中。使用3d医学成像软件(materialise mimics22.0,materialise,leuven,belgium)根据μct图像对分叉进行3d重建,并使用meshmixer(autodesk research,new york,ny)对所述分叉进行平滑化。
[0100]
用于侵入性成像程序的生物反应器回路:将基于硅胶的分叉模型放置于定制的流动室中。将聚氯乙烯管道连接在硅胶模型的入口端和出口端处。将生物反应器回路连接到流动室的入口和出口,从而允许1,000ml的去离子水在室温下以100ml/min的稳定流量循环(图14(b))。利用mv和sb两者的血管造影和oct成像对所有分叉模型进行成像。
[0101]
用于分叉中心线的3d重建的3d qca:用于分叉模型的3d重建的流程图示出在图15(a)中并且详细步骤示出在图15(b)和(c)以及图16中。在具有至少30
°
视角差异的两个投影处执行分叉模型的血管造影(图16(b))。在每个投影中,手动检测感兴趣区段的管腔,并将分叉隆突设置为公共参考位置(例如,隆突参考)。在caas中创建分叉模型的3d复制品并将其导出到vmtk(orobix,bergamo,italy)以用于提取mv和sb中心线。在每条中心线上,可根据投影到中心线的隆突参考找到隆突点(图16(c))。
[0102]
oct的采集和分割:使用optis integrated system(abbott,chicago,il,usa;图16(a))获得mv和sb的oct成像。将oct导管(dragonfly,optis imaging catheter)推进通过6f引导导管并以36mm/s(5帧/mm)的速度拉回(无对比剂的生理盐水自动触发)75mm,从而覆盖从远端到近端固定标记的整个mv和sb长度(图14(a))。使用echoplaque 4.0(indec medical systems,los altos,ca,usa;图16(b))半自动地执行oct帧的管腔分割。
[0103]
分叉管腔重建的oct处理:分叉管腔重建的详细步骤示出在图16中。简言之,将所分割的oct帧导入grasshopper 3d(在rhinoceros 3d内运行的可视化编程语言和环境)中并以沿导管中心的直线打包(图16(c))。利用内部脚本校正oct帧错位(misalignment)(图16(d)和(e))。将正确对齐的oct帧垂直定位在相应的分叉中心线上,使得中心线穿过每个帧的质心(图16(f))。特别地,隆突处的oct帧定位在隆突点(图16(f)中的点a)处,并且其余帧根据它们之间的已知距离定位在沿中心线的特定位置。然后将帧旋转成与隆突参考(图16(g)中的点c)对齐。创建mv和sb的主表面并将其用作使用t样条方法创建最终均匀、平滑且连续的分叉表面的参考(图16(h))。
[0104]
另外的细节在wu,w.等人的scientific reports(2020)的“3dreconstruction of coronary artery bifurcations from coronary angiography and optical coherence tomography:feasibility,validation,and reproducibility”中加以讨论,其以引用方式整体并入本文。
[0105]
所公开的方法具有若干临床上重要的应用。经3d重建的分叉可将关于精确的分叉解剖以及冠状动脉疾病的范围和严重程度告知程序师。更好地了解疾病负担可产生更好的手术规划和结果。此外,经3d重建的分叉管腔本身可用于计算和实验(工作台)流体动力学研究,以探索流动在原生冠状动脉疾病发展和进展以及支架内再狭窄和血栓形成中的作用。所公开的方法提供实际计算流体动力学研究所需的准确几何输入。所公开的技术可为有限元分析和患者特定计算分叉支架置入模拟创建基础。
[0106]
此外,使用患者特定分叉解剖和斑块特性以及实际支架几何形状进行计算支架置入模拟可提供支架置入技术的个性化规划。患者特定分叉解剖还与行业测试和开发新一代支架特别相关。最后,所公开的方法的基本原理可转化为其他侵入性成像模态(例如,ivus)或甚至非侵入性成像(例如,冠状动脉cta)。只要存在可用于提取管腔中心线和管腔/血管壁边界的成像数据,所公开的方法就有可能执行良好。
[0107]
尽管已经参考附图中所示的实施方案描述了技术,但是在不脱离如权利要求中所叙述的技术范围的情况下,可在本文中采用等效物并进行替换。本文示出和描述的部件是可用于实现本发明的实施方案的设备和部件的示例,并且可在不脱离本发明的范围的情况下用其他设备和部件替换。此外,除非权利要求中另有说明,否则本文提供的任何尺寸、度数和/或数值范围应理解为非限制性示例。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。