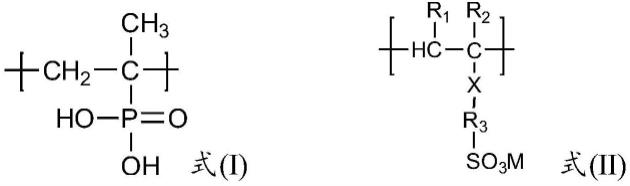
1.本发明涉及一种奥氮平衍生物、免疫原、抗奥氮平特异性抗体及其制备方法与应用,属于生物医学检测技术领域。
背景技术:
2.奥氮平(olanzapine)是一种新型非典型神经安定药,能与多巴胺受体、5-羟色胺(5-ht)受体和胆碱能受体结合,并发挥拮抗作用。奥氮平在临床上主要用于治疗精神分裂症和其他有严重阳性症状/或阴性症状的精神病的急性期和维持治疗;在缓解精神分裂症及相关疾病常见的继发性情感症状中也能发挥一定的作用。奥氮平的化学名称为化学名为2-甲基-4
‑ꢀ
(4-甲基-1-哌嗪基)
ꢀ‑
10h-噻吩并[2, 3-b][1,5]苯二氮杂卓,以硫、丙醛以及丙二腈为原料关环,再与邻硝基氟苯反应得到2-(2-硝基苯胺基)-3-氰基-5-甲基噻吩,经还原并与n-甲基哌嗪作用一步得到奥氮平产品,具有步骤短,收率较高,易于实现工业化的特点。奥氮平的临床应用有:
①
治疗精神分裂症及其它精神病性障碍。奥氮平能显著降低阳性症状,还能减轻阴性症状。精神分裂症 85%的阴性症状改善是奥氮平的直接治疗效应;
②
治疗情感障碍。奥氮平能有效治疗双向情感障碍,包括一些对锂盐、抗惊厥剂及典型抗精神病药反应不佳的病人;
③
治疗老年痴呆伴发的精神障碍;
④
治疗强迫症;
⑤
治疗躯体形式障碍;
⑥
治疗神经性厌食症。但其受到各种因素的影响,如年龄、给药方式、吸烟、喝咖啡等,与其他药物联合使用,容易产生具有临床意义的药物相互作用,导致药理作用和毒副反应的改变。及时监测血清中氯氮平水平和及时调整治疗剂量是至关重要的。此外,患者用药依从性难以判断、治疗剂量下无效以及可能存在药代动力学药物间相互作用等情况下,测定氯氮平血药浓度是非常有用的。因此,对给药患者血液中氯氮平的浓度进行监测可以制定和调整个体化给药方案,提高疗效,保障用药安全。
[0003]
奥氮平的血药浓度检测方法有多种,包括液相色谱结合串联质谱法(lc-ms/ms)、高效液相色谱法(hplc)、反向高效液相色谱法(rp-hplc)、高效液相色谱-紫外检测法(hplc-uv)、高效液相色谱-电化学法(hplc-ecd)、气相色谱-质谱法(gc-ms)、全自动二维液相色谱法(2d-lc/uv)等。高效液相色谱法具有准确、灵敏、廉价的特点;但测定时间较长,且检测浓度有限;该法流动相使用缓冲液,使其操作比较繁琐;难以实现自动化监测,制约了其在临床检测上的大规模使用。液相色谱-串联质谱法可大大简化样品纯化过程,且结果不受奥氮平代谢产物的干扰,且线性范围广、定量下限低,但对试验的要求和成本较高,其前处理较为复杂,条件不易控制。
[0004]
因此,目前市面上缺乏线性范围宽、灵敏度高、准确度高、精密度高,检测时间短,样品处理简单,仪器自动化程度高,可多样本连续检测的奥氮平检测产品。
技术实现要素:
[0005]
为了克服现有技术的不足,本发明的第一个目的在于提供一种奥氮平衍生物,该
衍生物为新合成的化合物,自然界中不存在。
[0006]
本发明的第一个目的采用以下技术方案实现:一种奥氮平衍生物,其结构式如式ⅰ所示:式ⅰ。
[0007]
本发明的第二个目的在于提供一种如上所述的奥氮平衍生物的合成方法,该合成方法不同于常规合成方法,具有良好的合成效果,显著提高了奥氮平衍生物的合成效率。
[0008]
本发明的第二个目的采用以下技术方案实现:一种如上述结构式ⅰ所示的奥氮平衍生物的合成方法,反应过程如下式所示:;具体的,反应过程包括以下步骤:(a1)化合物2的合成:将化合物1 (6 g,26 mmol)、哌嗪(18 g,0.19 mol) 在室温下加入丁醇(100 ml)中制成反应混合物,将此反应混合物在125℃加热条件下搅拌18小时。反应结束后将上述反应混合物在真空中浓缩。将浓缩所得残留物通过快速色谱分析仪(甲醇:二氯甲烷0-10%)进行纯化,得到化合物2。
[0009]
(a2)化合物3的合成:
将化合物2 (6 g,20 mmol)、5-溴戊酸叔丁基酯(5.7 g,24 mmol)、k2co3(4.2 g,28 mmol)、ki(0.3 g,2 mmol)在室温下加入乙腈(100 ml)中制成反应混合物。将此反应混合物在室温下搅拌18小时。反应结束后将上述反应混合物在真空中浓缩。将浓缩所得残留物通过快速色谱分析仪(甲醇:二氯甲烷0
‑ꢀ
5%)进行纯化,得到化合物3。
[0010]
(a3)奥氮平衍生物的合成:将化合物3 (5 g,11 mmol)、三氟乙酸(5 ml)共同溶解于dcm(45 ml)中制成反应混合物,将此反应混合物在室温下搅拌2小时。反应结束后将上述反应混合物在真空中浓缩。将浓缩所得残留物通过快速色谱分析仪(甲醇:二氯甲烷0
‑ꢀ
5%)进行纯化,得到奥氮平衍生物。
[0011]
本发明的第三个目的在于提供一种奥氮平免疫原。
[0012]
本发明的第三个目的采用以下技术方案实现:一种奥氮平免疫原,所述奥氮平免疫原由上述结构式ⅰ所示的奥氮平衍生物与载体蛋白连接而成,其结构式如式ⅱ所示:式ⅱ;其中,载体蛋白为重组绵羊血清白蛋白,进一步地,所述重组绵羊血清白蛋白的氨基酸序列如序列表seq id no:1所示。
[0013]
重组绵羊血清白蛋白的氨基酸序列(seq id no:1)具体如下:mkwvtfislllkfssaysrgvfrrdthkseiahrfndlgeenfqglvliafsqylkqcpfdehvklvkeltefaktcvadeshagkdkslhtlfgdelckvatlretygdmadkcekqepernecflnhkdkspdlpklkpepdtlcaefkadekkfwgkylyevarkhpyfyapellyyankyngvfqeckqaedkgacllpkidamrekvlassarqrlkcasiqkfgeralkawsvarlsqkfpkadftdvtkivtdltkvhkecchgdklecaddradlakyicdhqdalksklkeckdkpvlekshciaevdkdavpenlppltadfaedkevcknyqeakdvflgsflyeyskrhpeyavsvklrlakeyeatledccakedphacyktvfdklkhlvdepqnlikkncelfekhgeygfqnalivkytrkapqvstptlveisrslgkvgtkckakpesermpctedylslilnrlcvlhektpvsekvtkkcteslvnrrpcfsdltldetyvpkpfdekfktfhadictlpdtekqikkqtalvelkkhkpkatdeqlktvmenfvafvdkccaadkkegcfvlegpklvastqaala
本发明的第四个目的在于提供一种如上所述的奥氮平免疫原的制备方法。
[0014]
本发明的第四个目的采用以下技术方案实现:一种如上所述的奥氮平免疫原的制备方法,包括以下步骤:(b1)载体蛋白溶液的制备:将上述的重组绵羊血清白蛋白溶解于磷酸盐缓冲液中,得到载体蛋白溶液;(b2)奥氮平衍生物溶液的制备:将上述结构式ⅰ所示的奥氮平衍生物与二甲基甲酰胺、乙醇、磷酸钾缓冲液、1-乙基-3-(-3-二甲氨丙基)碳二亚胺和n-羟基硫代琥珀酰亚胺混合,搅拌溶解,得到奥氮平衍生物溶液;(b3)奥氮平免疫原的合成:将步骤(b2)得到的奥氮平衍生物溶液加入到步骤(b1)得到的载体蛋白溶液中,搅拌反应,经透析纯化,得到奥氮平免疫原。
[0015]
具体的,所述奥氮平免疫原的制备方法,包括以下步骤:(b1)载体蛋白溶液的制备:将重组绵羊血清白蛋白溶解于0.35mol/l的磷酸钾缓冲液(ph=8.5)中,重组绵羊血清白蛋白的终浓度为5.0mg/ml,得到载体蛋白溶液;(b2)奥氮平衍生物溶液的制备:将250.0mg上述的奥氮平衍生物、7.5ml二甲基甲酰胺、7.5ml乙醇、15.0ml的磷酸钾缓冲液(10.0mmol/l,ph=8.0)、150.0mg 1-乙基-3-(-3-二甲氨丙基)碳二亚胺、90.0mg n-羟基硫代琥珀酰亚胺混合,搅拌溶解反应3小时,得到奥氮平衍生物溶液;(b3)奥氮平免疫原的合成:将步骤(b2)得到的奥氮平衍生物溶液逐滴加入到步骤(b1)得到的载体蛋白溶液中,并在-4℃下搅拌过夜,经透析纯化,得到奥氮平免疫原。
[0016]
本发明的第五个目的在于提供一种抗奥氮平特异性抗体。
[0017]
本发明的第五个目的采用以下技术方案实现:一种抗奥氮平特异性抗体,所述抗奥氮平特异性抗体为使用上述的奥氮平免疫原对实验动物进行注射后所得到的特异性抗体,所述的实验动物为兔子、山羊、绵羊、小鼠、大鼠、豚鼠或马中的一种。
[0018]
本发明的第六个目的在于提供一种如上所述的抗奥氮平特异性抗体的制备方法。
[0019]
本发明的第六个目的采用以下技术方案实现:一种如上所述的抗奥氮平特异性抗体的制备方法,包含以下步骤:(c1)将上述的奥氮平免疫原用磷酸盐缓冲液稀释,得到奥氮平人工抗原溶液,然后将奥氮平人工抗原溶液与等量弗氏完全佐剂混合,对上述的实验动物进行多点注射;(c2)3-6周后,再用相同的奥氮平人工抗原溶液与等量弗氏不完全佐剂混合,对上述实验动物进行多点注射,之后每隔3-6周注射一次,共计注射3-10次;(c3)对步骤(c2)中完成注射的实验动物取血,分离纯化,得到抗奥氮平特异性抗体。
[0020]
具体的,所述抗奥氮平特异性抗体的制备方法,包含以下步骤:(c1)将上述的奥氮平免疫原用0.15mol/l磷酸钠缓冲液(ph=7.0)稀释至终浓度为3.5mg/ml,得到人工抗原溶液,然后将3.0ml人工抗原溶液与等量弗氏完全佐剂混合,对实验动物兔子进行多点注射;(c2)4周后,再用3.0ml相同的人工抗原溶液与等量弗氏不完全佐剂对上述实验动物兔子进行多点注射,之后每隔5周注射一次,共计注射6次;(c3)对步骤(c2)完成注射的实验动物兔子取血,分离纯化,得到抗奥氮平特异性
抗体。
[0021]
本发明的第七个目的在于提供一种如上所述的抗奥氮平特异性抗体的应用。
[0022]
本发明的第七个目的采用以下技术方案实现:一种如上所述的抗奥氮平特异性抗体的应用,将所述抗奥氮平特异性抗体用于制备奥氮平检测试剂,所述奥氮平检测试剂包括奥氮平均相酶免疫检测试剂与奥氮平胶乳增强免疫比浊检测试剂。
[0023]
优选地,上述的抗奥氮平特异性抗体的应用,所述奥氮平均相酶免疫检测试剂,由r1试剂与r2试剂组成,所述r1试剂包含上述的抗奥氮平特异性抗体与r1缓冲液,所述r2试剂包含奥氮平葡萄糖-6-磷酸脱氢酶标记偶联物与r2缓冲液;所述的r1缓冲液含有酶底物、辅酶、牛血清白蛋白及tris缓冲液,所述的酶底物为葡萄糖-6-磷酸,所述的辅酶为氧化型烟酰胺腺嘌呤二核苷酸;所述的奥氮平葡萄糖-6-磷酸脱氢酶标记偶联物由上述结构式ⅰ所示的奥氮平衍生物与葡萄糖-6-磷酸脱氢酶偶联而成;其结构式如式ⅲ所示:式ⅲ;所述的r2缓冲液为含有牛血清白蛋白的tris缓冲液。
[0024]
具体的,所述奥氮平均相酶免疫检测试剂的制备方法,包含以下步骤:(d1)将250.0mg牛血清白蛋白、250.0mg葡萄糖-6-磷酸及50.0mg氧化型烟酰胺腺嘌呤二核苷酸依次加入250ml tris缓冲液(50mmol/l,ph=8.5)中搅拌溶解制成r1缓冲液,再将抗奥氮平特异性抗体以1∶1000的体积比加入到上述r1缓冲液中混匀,再用1.0 mol/l的盐酸调节ph至7.6,制成r1试剂;(d2)将250.0mg牛血清白蛋白加入250ml tris缓冲液(100mmol/l,ph=8.7)中搅拌溶解制成r2缓冲液,再将奥氮平葡萄糖-6-磷酸脱氢酶标记偶联物以1∶1000的体积比加入到上述r2缓冲液中混匀,再用1.0 mol/l的盐酸调节ph至8.0,制成r2试剂。
[0025]
所述的奥氮平葡萄糖-6-磷酸脱氢酶标记偶联物的制备方法,包含以下步骤:(e1)称取20.0 mg活力单位为200ku的葡萄糖-6-磷酸脱氢酶,在室温条件下溶解于50.0ml磷酸钠(100mmol/l,ph=8.0)缓冲液中,然后加入150.0 mg还原态的烟酰胺腺嘌呤二核苷酸、75.0 mg葡萄糖-6-磷酸以及0.75 ml卡必醇,再逐滴加入2.5 ml二甲基亚砜,搅拌溶解,得到葡萄糖-6-磷酸脱氢酶溶液;(e2)在无水状态下称取15.0 mg上述结构式ⅰ所示的奥氮平衍生物,溶解于500.0
ꢀµ
l二甲基甲酰胺中,将上述溶液温度降到0℃后加入4.5
ꢀµ
l三丁胺、2.5
ꢀµ
l氯甲酸异丁酯、3.5
ꢀµ
l n,n
′‑
二环己基碳二亚胺,0℃下搅拌45分钟,得到奥氮平衍生物激活液;(e3)将奥氮平衍生物激活液逐滴加入到葡萄糖-6-磷酸脱氢酶溶液中,-4℃搅拌反应12小时,反应结束后经g-25凝胶层析柱纯化得到奥氮平葡萄糖-6-磷酸脱氢酶标记偶联物。
[0026]
优选地,上述的抗奥氮平特异性抗体的应用,所述奥氮平胶乳增强免疫比浊检测试剂,由l1试剂与l2试剂组成;
所述l1试剂由上述的抗奥氮平特异性抗体、ph=8.0的缓冲液、牛血清白蛋白、氯化钠、吐温-20、丙三醇、乙二胺四乙酸、促凝剂以及防腐剂组成;所述l2试剂由奥氮平-牛血清白蛋白复合体包被的聚苯乙烯胶乳颗粒、ph=8.0的缓冲液、牛血清白蛋白、氯化钠、吐温-20、丙三醇、乙二胺四乙酸以及防腐剂组成;所述的奥氮平-牛血清白蛋白复合体由上述结构式ⅰ所示的奥氮平衍生物与牛血清白蛋白偶联而成,其结构式如式ⅳ所示:式ⅳ;所述的聚苯乙烯胶乳颗粒直径范围为50-250nm;所述的缓冲液为磷酸盐缓冲液、甘氨酸缓冲液、mes缓冲液、硼酸盐缓冲液、tris-hcl缓冲液或巴比妥缓冲液中的一种;所述促凝剂为peg-4000、peg-6000、peg-8000或硫酸葡聚糖钠中的一种;所述防腐剂为叠氮钠、硫柳汞、苯酚或乙基汞硫代硫酸钠中的一种。
[0027]
具体的,所述奥氮平胶乳增强免疫比浊检测试剂的制备方法,包含以下步骤:(f1)将5.0ml的抗奥氮平特异性抗体溶解于250.0ml磷酸钾缓冲液(50.0 mmol/l ph=8.0)中,然后添加100.0mg牛血清白蛋白、25.0mg氯化钠、250.0μl吐温-20、250.0μl丙三醇、100.0μl的乙二胺四乙酸、150.0μl的peg-4000以及5.0mg叠氮钠,搅拌均匀,调节ph=7.3,制成l1试剂;(f2)将1.5mg表面带有羧基的直径为125nm的聚苯乙烯胶乳颗粒加入15.0ml的mes缓冲液(50.0mmol/l,ph=7.0)中,然后加入5.0mg碳二亚胺,在25℃下反应3小时,制成胶乳颗粒溶液,再将1.2mg奥氮平-牛血清白蛋白复合体用7.5ml的硼酸盐缓冲液(50.0mmol/l,ph=9.2)稀释后,立即加入到上述胶乳颗粒溶液中,在41℃下反应18小时,然后加入3.0ml的甘氨酸缓冲液(100.0mmol/l,ph=8.0)搅拌3小时,反应终止后离心去除上清液,再将沉淀物用20.0ml的tris-hcl缓冲液(50.0mmol/l,ph=8.0)洗涤3次,再用50.0ml的甘氨酸缓冲液(50.0mmol/l,ph=8.6)稀释成胶乳悬浊液,最后加入质量分数为100.0mg牛血清白蛋白、25.0mg氯化钠、250.0μl吐温-20、250.0μl丙三醇、100.0μl的乙二胺四乙酸以及5.0mg叠氮钠,搅拌均匀,制成l2试剂。
[0028]
所述的奥氮平-牛血清白蛋白复合体的制备方法,包含以下步骤:将10.0mg牛血清白蛋白用7.5ml的磷酸钠缓冲液(100.0mmol/l,ph=7.5)稀释,然后加入100.0mg上述结构式ⅰ所示的奥氮平衍生物,再加入50.0mg的1-乙基-3-(3-二甲基氨基丙基)碳二亚胺,在0℃下反应10 小时,再用100.0ml磷酸盐缓冲液(100.0mmol/l,ph=7.5)在-4℃下透析12小时,得到奥氮平-牛血清白蛋白复合体。
[0029]
相比现有技术,本发明的有益效果在于:1、本发明设计的奥氮平衍生物及其合成方法均为针对性的新设计与研究,在现有技术中并不存在;2、本发明使用经过基因工程改造得到的重组绵羊血清白蛋白与奥氮平衍生物偶
联得到奥氮平免疫原,偶联效率高,显著提高奥氮平免疫原的免疫原性。使用本发明的奥氮平免疫原制备得到的抗奥氮平特异性抗体的特异性强、灵敏度高,并且与100种常见药物无任何交叉反应,因此能够用于制备具有较高的准确性、精密度、灵敏度和特异性的奥氮平检测试剂。
[0030]
3、本发明的两种奥氮平检测试剂可以实现在全自动生化分析仪上对奥氮平高通量、快速化的检测,能同时测定多个样品,具有操作简便、灵敏度高、特异性强、结果准确等优点,还能有效降低奥氮平检测成本,有利于临床推广使用。
附图说明
[0031]
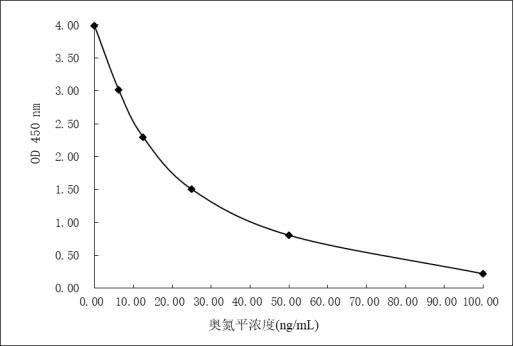
图1为实施例4 奥氮平的elisa检测标准曲线;图2为实施例8奥氮平均相酶免疫检测试剂校准曲线;图3为实施例10奥氮平胶乳增强免疫比浊检测试剂校准曲线。
具体实施方式
[0032]
下面结合附图以及具体实施方式,对本发明做进一步描述,这些附图均为简化的示意图,仅以示意方式说明本发明的基本结构,因此其仅显示与本发明有关的构成。除非特别指明,以下实施例中所用的试剂、仪器、设备、耗材均可从正规渠道商购买获得。
[0033]
实施例1:奥氮平衍生物的合成通过以下合成路线合成奥氮平衍生物:;具体的合成步骤如下:(1)化合物2的合成:
将化合物1 (6 g,26 mmol)、哌嗪(18 g,0.19 mol) 在室温下加入丁醇(100 ml)中制成反应混合物,将此反应混合物在125℃加热条件下搅拌18小时。反应结束后将上述反应混合物在真空中浓缩。将浓缩所得残留物通过快速色谱分析仪(甲醇:二氯甲烷0-10%)进行纯化,得到6 g化合物2为黄色固体。
[0034]
(2)化合物3的合成:将化合物2 (6 g,20 mmol)、5-溴戊酸叔丁基酯(5.7 g,24 mmol)、k2co3(4.2 g,28 mmol)、ki(0.3 g,2 mmol)在室温下加入乙腈(100 ml)中制成反应混合物。将此反应混合物在室温下搅拌18小时。反应结束后将上述反应混合物在真空中浓缩。将浓缩所得残留物通过快速色谱分析仪(甲醇:二氯甲烷0
‑ꢀ
5%)进行纯化,得到5 g化合物3为黄色固体。
[0035]
(3)奥氮平衍生物的合成:将化合物3 (5 g,11 mmol)、三氟乙酸(5 ml)共同溶解于dcm(45 ml)中制成反应混合物,将此反应混合物在室温下搅拌2小时。反应结束后将上述反应混合物在真空中浓缩。将浓缩所得残留物通过快速色谱分析仪(甲醇:二氯甲烷0
‑ꢀ
5%)进行纯化,得到2.5 g奥氮平衍生物。
[0036]
实施例2:奥氮平免疫原的制备奥氮平免疫原的制备方法具体步骤如下:(1)载体蛋白溶液的制备:将重组绵羊血清白蛋白溶解于0.35mol/l的磷酸钾缓冲液(ph=8.5)中,重组绵羊血清白蛋白的终浓度为5.0mg/ml,得到载体蛋白溶液;(2)奥氮平衍生物溶液的制备:将250.0mg上述的奥氮平衍生物、7.5ml二甲基甲酰胺、7.5ml乙醇、15.0ml的磷酸钾缓冲液(10.0mmol/l,ph=8.0)、150.0mg 1-乙基-3-(-3-二甲氨丙基)碳二亚胺、90.0mg n-羟基硫代琥珀酰亚胺混合,搅拌溶解反应3小时,得到奥氮平衍生物溶液;
(3)奥氮平免疫原的合成:将步骤(2)得到的奥氮平衍生物溶液逐滴加入到步骤(1)得到的载体蛋白溶液中,并在-4℃下搅拌过夜,经透析纯化,得到奥氮平免疫原。
[0037]
实施例3:抗奥氮平特异性抗体的制备抗奥氮平特异性抗体的制备方法具体步骤如下:(1)将上述的奥氮平免疫原用0.15mol/l磷酸钠缓冲液(ph=7.0)稀释至终浓度为3.5mg/ml,得到人工抗原溶液,然后将3.0ml人工抗原溶液与等量弗氏完全佐剂混合,对实验动物兔子进行多点注射;(2)4周后,再用3.0ml相同的人工抗原溶液与等量弗氏不完全佐剂对上述实验动物兔子进行多点注射,之后每隔5周注射一次,共计注射6次;(3)对步骤(2)完成注射的实验动物兔子取血,分离纯化,得到抗奥氮平特异性抗体。
[0038]
实施例4:elisa法检验抗奥氮平特异性抗体的性能1.奥氮平的elisa检测标准曲线的建立:(1)标准品的制备:将奥氮平纯品粉末(购于sigma公司) 溶解于甲醇溶液,制备成1mg/ml的储存液。用elisa缓冲液将储存液依次稀释为100.00ng/ml、50.00ng/ml、25.00ng/ml、12.50ng/ml、6.25ng/ml、0.00ng/ml的标准溶液。其中,elisa缓冲液由50.0mmol/l的tris缓冲液,质量分数为1.5%的nacl以及体积分数为0.25%的bsa配制而成。
[0039]
(2)利用奥氮平的elisa检验方法制备标准曲线:用磷酸钾缓冲液(50.0mmol/l,ph=8.0)将实施例3中所制备的抗奥氮平特异性抗体稀释成1 : 10000的终浓度溶液,100μl/孔包被在96孔酶联板上,4℃放置18小时;用磷酸钾缓冲液将包被有抗奥氮平特异性抗体的96孔酶联板洗涤3次后,加入200μl/孔的体积分数0.5%的bsa溶液,4℃下放置12小时。然后用磷酸钾缓冲液洗涤3次,加入20μl/孔的标准溶液。再加入100μl/孔工作浓度的hrp-奥氮平偶联物;室温下孵育30min后磷酸钾缓冲液洗板5次;然后每孔加入100μl的tmb 底物,室温孵育30min。再每孔加入100μl的终止液(2.0mol/l的硫酸)。使用酶标仪测定450nm的吸光值。根据各标准溶液所对应的450nm的吸光值定标,制作标准曲线,结果如图1所示。
[0040]
2.待测样品中奥氮平含量的检测:(1)制作待测样品:制备方法:将奥氮平纯品粉末(购于sigma公司) 溶解于甲醇溶液制成1.0mg/ml的储存液,并将此储存液稀释于空白血浆中,至终浓度分别为0.00ng/ml、12.50ng/ml、25.00ng/ml、50.00ng/ml,分别形成空白、低、中、高浓度的血浆样本。所述空白血浆为不含奥氮平的健康人血浆。
[0041]
(2)测试方法:利用上述奥氮平的elisa检验方法,将上述空白、低、中、高浓度的血浆样本代替标准溶液,测试上述空白、低、中、高浓度的血浆样本在450nm的吸光值。
[0042]
(3)测试结果:对照图1中所示的奥氮平的elisa检验的标准曲线,计算每个样本中奥氮平含量,并对每个样本进行3个复孔测定,根据上述样本中奥氮平的实际含量计算回收率,结果如表
1所示。
[0043]
表1 奥氮平的elisa检测结果血浆样本空白低值中值高值样本浓度(ng/ml)0.0012.5025.0050.00测定10.0012.7325.1750.40测定20.0012.5124.8749.88测定30.0012.3625.0351.00平均值(ng/ml)0.0012.5325.0250.43回收率(%)-100.27100.09100.85由表1中结果可知:使用本发明奥氮平特异性抗体的elisa检测方法测定不同浓度样本中的奥氮平回收率都较高,均在97%-103%之间,说明本发明所述的抗奥氮平特异性抗体可以用于样本中奥氮平的检测,并且灵敏度高,检测结果准确度高。
[0044]
实施例5:100种常见药物干扰试验选取100种常见药物作为干扰物进行干扰试验,将100种常见药物纯品粉末配制成浓度为100.0μg/ml的溶液作为待测干扰物样本,采用实施例4的elisa检验方法对相应干扰物的浓度进行检测,100种常见药物名称以及检测结果详见表2。
[0045]
表2 常见药物干扰试验检测结果
序号化合物名称实际检测值(ng/ml)序号化合物名称实际检测值(ng/ml)1阿司匹林0.002苯丙醇胺0.003β-苯基乙胺0.004普鲁卡因酰胺0.005安非他命0.006普鲁卡因0.007氨苄青霉素0.008奎尼丁0.009甲氨二氮卓0.0010佐美酸0.0011氯丙嗪0.0012苯肾上腺素0.0013氯拉卓酸0.0014桂皮酰艾克宁0.0015二甲苯氧庚酸0.0016芽子碱0.0017非诺洛芬0.0018地西洋0.0019甲基苯丙胺0.0020可替宁0.0021龙胆酸0.0022阿替洛尔0.0023吉非贝齐0.0024心得安0.0025氢可酮0.0026苯乙哌啶酮0.0027布洛芬0.0028苯基丁氮酮0.0029丙咪嗪0.0030麦角酸二乙基酰胺0.0031二氨基二苯砜0.0032大麻酚0.0033萘普生0.0034洛哌丁胺0.0035氢氯噻嗪0.0036异克舒令0.0037哌替啶0.0038苯基丙氨酸0.0039烯丙羟吗啡酮0.0040盐酸氟西汀0.0041麻黄素0.0042柳丁氨醇0.0043烟酰胺0.0044青霉素0.0045甲胺呋硫0.0046甲基二乙醇胺0.0047异戊巴比妥0.0048二亚甲基双氧苯丙胺0.00
49甲撑二氧苯丙胺0.0050琥珀酸多西拉敏0.0051四氢大麻酚0.0052纳布啡0.0053制霉菌素0.0054去甲吗啡0.0055乙酰吗啡0.0056羟考酮0.0057苄非他明0.0058克他命0.0059异丙嗪0.0060苯海拉明0.0061阿司帕坦0.0062苯丁胺0.0063阿立哌唑0.0064氟康唑0.0065氯氮平0.0066呋塞米0.0067艾司西酞普兰0.0068加巴喷丁0.0069伊马替尼0.0070华法林0.0071拉莫三嗪0.0072瑞舒伐他汀0.0073利奈唑胺0.0074对乙酰氨基酚0.0075利培酮0.0076舒必利0.0077舍曲林0.0078氟伏沙明0.0079托吡酯0.0080氟西汀0.0081文拉法辛0.0082齐拉西酮0.0083伏立康唑0.0084氟哌啶醇0.0085左乙拉西坦0.0086亚胺培南0.0087奥卡西平0.0088阿昔替尼0.0089唑尼沙胺0.0090培唑帕尼0.0091阿米替林0.0092瑞戈非尼0.0093氯丙嗪0.0094异烟肼0.0095多虑平0.0096利福平0.0097帕罗西汀0.0098左氧氟沙星0.0099氯霉素0.00100莫西沙星0.00
测定结果显示:采用实施例4的elisa检验方法对相应干扰物的浓度进行检测,上述100种常见药物实际检测值均为0.00ng/ml。由此可见,本发明的抗奥氮平特异性抗体具有较强的抗原识别特异性,与100种常见药物无任何交叉反应。
[0046]
实施例6:奥氮平均相酶免疫检测试剂的制备奥氮平均相酶免疫检测试剂的制备方法,具体步骤如下:(1)将250.0mg牛血清白蛋白、250.0mg葡萄糖-6-磷酸及50.0mg氧化型烟酰胺腺嘌呤二核苷酸依次加入250ml tris缓冲液(50mmol/l,ph=8.5)中搅拌溶解制成r1缓冲液,再将抗奥氮平特异性抗体以1∶1000的体积比加入到上述r1缓冲液中混匀,再用1.0 mol/l的盐酸调节ph至7.6,制成r1试剂;(2)将250.0mg牛血清白蛋白加入250ml tris缓冲液(100mmol/l,ph=8.7)中搅拌溶解制成r2缓冲液,再将奥氮平葡萄糖-6-磷酸脱氢酶标记偶联物以1∶1000的体积比加入到上述r2缓冲液中混匀,再用1.0 mol/l的盐酸调节ph至8.0,制成r2试剂。
[0047]
所述的奥氮平葡萄糖-6-磷酸脱氢酶标记偶联物的制备方法,包含以下步骤:(1)称取20.0 mg活力单位为200ku的葡萄糖-6-磷酸脱氢酶,在室温条件下溶解于50.0ml磷酸钠(100mmol/l,ph=8.0)缓冲液中,然后加入150.0 mg还原态的烟酰胺腺嘌呤二核苷酸、75.0 mg葡萄糖-6-磷酸以及0.75 ml卡必醇,再逐滴加入2.5 ml二甲基亚砜,搅拌
溶解,得到葡萄糖-6-磷酸脱氢酶溶液;(2)在无水状态下称取15.0 mg实施例1合成的奥氮平衍生物,溶解于500.0
ꢀµ
l二甲基甲酰胺中,将上述溶液温度降到0℃后加入4.5
ꢀµ
l三丁胺、2.5
ꢀµ
l氯甲酸异丁酯、3.5
ꢀµ
l n,n
′‑
二环己基碳二亚胺,0℃下搅拌45分钟,得到奥氮平衍生物激活液;(3)将奥氮平衍生物激活液逐滴加入到葡萄糖-6-磷酸脱氢酶溶液中,-4℃搅拌反应12小时,反应结束后经g-25凝胶层析柱纯化得到奥氮平葡萄糖-6-磷酸脱氢酶标记偶联物。
[0048]
实施例7:奥氮平校准品、质控品的制备(1)校准品的制备:将奥氮平纯品粉末分别加入6份浓度为50.0mmol/l ph=7.2的tris-hcl缓冲液中,搅拌溶解,至终浓度分别为0.00ng/ml、6.25ng/ml、12.50ng/ml、25.00ng/ml、50.00ng/ml、100.00ng/ml,然后在每份溶液中分别加入质量分数为0.5%的氯化钠、1.0%的牛血清白蛋白、0.75%的乙二胺四乙酸、0.05%的叠氮钠,搅拌均匀,即为奥氮平校准品(6个浓度)。
[0049]
(2)质控品的制备:将奥氮平纯品粉末分别加入4份浓度为50.0mmol/l ph=7.2的tris-hcl缓冲液中,搅拌溶解,至终浓度分别为0.00ng/ml、12.50ng/ml、25.00ng/ml、50.00ng/ml,然后在每份溶液中分别加入质量分数为0.5%的氯化钠、1.0%的牛血清白蛋白、0.75%的乙二胺四乙酸、0.05%的叠氮钠,搅拌均匀,即为奥氮平质控品(4个浓度)。
[0050]
实施例8:奥氮平均相酶免疫检测试剂校准曲线制作及质控实验1. 制作奥氮平均相酶免疫检测校准曲线:在迈瑞 bs480全自动生化分析仪中放入r1试剂、r2试剂及校准品,然后对生化分析仪进行反应参数设置,具体参数详见表3;实际操作过程中需不断调整r1试剂和r2试剂的体积比例,同时调整测光点,最后由生化分析仪自动得出均相酶免疫检测校准曲线,如图2所示。
[0051]
表3 迈瑞 bs480全自动生化分析仪反应参数设置
项目名称奥氮平r1试剂160.0
µ
lr2试剂40.0
µ
l样本量10.0
µ
l定标方法两点终点法主波长340nm次波长405nm反应时间10分钟温育时间8分钟反应方向上升结果ng/ml结果精度0.01拟合方法linegraph校准品浓度0.00ng/ml、6.25ng/ml、12.50ng/ml、25.00ng/ml、50.00ng/ml、100.00ng/ml
2. 质控品检测实验:利用上述的奥氮平均相酶免疫检测方法,对质控品进行测定,并根据步骤1中制作
的均相酶免疫检测校准曲线,计算每个质控品中奥氮平的含量,每个质控品重复测定10次,检测结果及数据分析详见表4。
[0052]
表4 奥氮平均相酶免疫检验试剂检测结果及数据分析质控品空白低值中值高值浓度(ng/ml)0.0012.5025.0050.00测试10.0012.5225.8750.50测试20.0012.4626.0450.45测试30.0012.6725.0351.00测试40.0012.6025.1549.74测试50.0012.4025.2648.95测试60.0012.5024.7549.98测试70.0012.5924.9250.01测试80.0012.7024.5550.10测试90.0012.7125.4150.24测试100.0012.3924.7749.79平均值(ng/ml)0.0012.5525.1850.08标准差(sd)/0.120.480.55精密度(cv%)/0.941.931.09回收率(%)/100.43100.70100.15实验结果表明:测定不同浓度质控品中奥氮平含量的cv值均低于5%,回收率均在95%-105%之间,说明本发明的奥氮平均相酶免疫检测试剂测定生物样本中奥氮平含量的精密度较高,结果准确。
[0053]
实施例9:奥氮平胶乳增强免疫比浊检测试剂的制备奥氮平胶乳增强免疫比浊检测试剂的制备方法,包含以下步骤:(f1)将5.0ml的抗奥氮平特异性抗体溶解于250.0ml磷酸钾缓冲液(50.0 mmol/l ph=8.0)中,然后添加100.0mg牛血清白蛋白、25.0mg氯化钠、250.0μl吐温-20、250.0μl丙三醇、100.0μl的乙二胺四乙酸、150.0μl的peg-4000以及5.0mg叠氮钠,搅拌均匀,调节ph=7.3,制成l1试剂;(f2)将1.5mg表面带有羧基的直径为125nm的聚苯乙烯胶乳颗粒加入15.0ml的mes缓冲液(50.0mmol/l,ph=7.0)中,然后加入5.0mg碳二亚胺,在25℃下反应3小时,制成胶乳颗粒溶液,再将1.2mg奥氮平-牛血清白蛋白复合体用7.5ml的硼酸盐缓冲液(50.0mmol/l,ph=9.2)稀释后,立即加入到上述胶乳颗粒溶液中,在41℃下反应18小时,然后加入3.0ml的甘氨酸缓冲液(100.0mmol/l,ph=8.0)搅拌3小时,反应终止后离心去除上清液,再将沉淀物用20.0ml的tris-hcl缓冲液(50.0mmol/l,ph=8.0)洗涤3次,再用50.0ml的甘氨酸缓冲液(50.0mmol/l,ph=8.6)稀释成胶乳悬浊液,最后加入质量分数为100.0mg牛血清白蛋白、25.0mg氯化钠、250.0μl吐温-20、250.0μl丙三醇、100.0μl的乙二胺四乙酸以及5.0mg叠氮钠,搅拌均匀,制成l2试剂。
[0054]
所述的奥氮平-牛血清白蛋白复合体的制备方法,包含以下步骤:将10.0mg牛血清白蛋白用7.5ml的磷酸钠缓冲液(100.0mmol/l,ph=7.5)稀释,然
后加入100.0mg实施例1合成的奥氮平衍生物,再加入50.0mg的1-乙基-3-(3-二甲基氨基丙基)碳二亚胺,在0℃下反应10 小时,再用100.0ml磷酸盐缓冲液(100.0mmol/l,ph=7.5)在-4℃下透析12小时,得到奥氮平-牛血清白蛋白复合体。
[0055]
实施例10:奥氮平胶乳增强免疫比浊检测试剂校准曲线制作及质控实验1. 制作奥氮平胶乳增强免疫比浊检测试剂校准曲线:在奥林巴斯au480全自动生化分析仪中放入l1试剂、l2试剂及校准品,然后对生化分析仪进行反应参数设置,具体参数详见表5;实际操作过程中需不断调整l1试剂和l2试剂的体积比例,同时调整测光点,最后由生化分析仪自动得出胶乳增强免疫比浊检测校准曲线,如图3所示。
[0056]
表5 奥林巴斯au480全自动生化分析仪反应参数
项目名称奥氮平l1试剂160.0
µ
ll2试剂40.0
µ
l样本量10.0
µ
l定标方法两点终点法主波长570nm次波长412nm反应时间10分钟温育时间5分钟反应方向下降结果ng/ml结果精度0.01拟合方法logit-log4p校准品浓度0.00ng/ml、6.25ng/ml、12.50ng/ml、25.00ng/ml、50.00ng/ml、100.00ng/ml
2. 质控品检测实验:利用上述的胶乳增强免疫比浊检测方法,对质控品进行测定,并根据步骤1中制作的胶乳增强免疫比浊检测校准曲线,计算每个质控品中奥氮平的含量,每个质控品重复测定10次,检测结果及数据分析详见表6。
[0057]
表6 奥氮平胶乳增强免疫比浊试剂检测结果及数据分析质控品空白低值中值高值浓度(ng/ml)0.0012.5025.0050.00测试10.0012.5525.1149.59测试20.0012.5724.9850.45测试30.0012.7024.7352.10测试40.0012.5025.8749.43测试50.0012.5426.0050.81测试60.0012.3225.0349.49测试70.0012.4625.0450.52测试80.0012.3824.5949.70测试90.0012.6224.8651.03
测试100.0012.6624.9050.20平均值(ng/ml)0.0012.5325.1150.33标准差(sd)/0.120.460.84精密度(cv%)/0.951.841.67回收率(%)/100.24100.44100.66实验结果表明:测定不同浓度质控品中奥氮平含量的cv值均低于5%,回收率均在95%-105%之间,说明本发明的奥氮平胶乳增强免疫比浊检测试剂测定生物样本中奥氮平含量的精密度较高,结果准确。
[0058]
对于本领域的技术人员来说,可根据以上描述的技术方案以及构思做出其它各种相应的变更以及修改,而所有的这些变更以及修改都应该属于本发明权利要求的保护范围之内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。