抑制hif2
α
基因表达的组合物及方法
背景技术:
1.epas1为hif(低氧诱导性因子)基因家族的成员。还称为 hif2α(hif2alpha/hif2α)的epas1编码与通过氧调节的基因诱导有关且在氧含量降低时(称为低氧的条件)诱导的转录因子的一半。
2.此基因的某些变化形式会保护生活于高海拔的人。然而,在低海拔下,野生型(wt)epas1的过度表达与高血压及中风增加且与类似于高山病的症状相关。此基因的突变与4型家族红细胞增多症及肺高血压有关。epas1可过量产生红血球,从而导致抑制生殖能力或甚至死亡。
3.epas1已展示为与各种疾病(包含肿瘤进展)有关的多种基因的表达或表达增加所需要。举例而言,epas1可通过促进自分泌环vegf-pvegfr2/kdr且通过增强ldha的表达在葡萄膜黑色素瘤进展中起作用,因此提供生长优势。
4.epas1还已展示与其他因子有关或上调其他因子的表达,所述因子包含: cmyc(其有利于细胞增殖、转化、瘤形成及肿瘤形成,且其在大部分癌症中高度表达);介白素8(促炎性介体,例如在齿龈炎及牛皮癣中);sp-1(与il-8调节有关的转录因子及cmyc的共活化剂);ldh5(其与肿瘤坏死有关且增加肿瘤尺寸);及 lana(时延相关的细胞核抗原,其与卡波西氏肉瘤相关的疱疹病毒(kaposi'ssarcoma-associated herpesvirus)相关)。另外,hif(低氧诱导因子)活性可在癌症肿瘤生长所需的血管生成中起作用。epas 1还可与若干其他疾病有关,包含炎症、慢性炎症、新生血管性疾病、类风湿性关节炎、肾癌、透明细胞肾细胞癌(及此及其他癌症的癌转移)、黑素瘤、葡萄膜黑素瘤、软骨肉瘤及多发性骨髓瘤。
5.epas1基因的突变已与例如副神经节瘤、生长抑制素瘤和/或嗜铬细胞瘤的神经内分泌肿瘤的早期发作相关。突变一般为位于hif-2α的第一羟基化位点中的体细胞错义突变。据信这些突变会破坏蛋白羟基化/降解机制且会导致蛋白稳定及假低氧性信号传导。另外,神经内分泌肿瘤将红血球生成素(epo)释放至循环血液中且导致多血症。
技术实现要素:
6.本文所述为能够选择性且有效地降低hif2α表达的hif2α(还称为epas或 hif2α(hif2alpha))基因特异性rna干扰(rnai)触发剂分子(还称为rnai剂、rnai 触发剂或触发剂)。各rnai触发剂至少包括正义链及反义链。正义链与反义链可彼此间部分地、实质上或完全互补。本文所述的rnai触发剂正义链及反义链的长度各可为长度16至30个核苷酸。在一些实施方式中,正义链及反义链独立地为长度17至26个核苷酸。正义链及反义链的长度可相同或其长度不同。本文所述的 rnai触发剂在递送至表达hif2α基因的细胞时,体外或体内抑制该hif2α基因的表达。表1-2及5中提供可用于hif2αrnai触发剂中的hif2αrnai触发剂正义链及反义链的示例。
7.hif2αrnai触发剂的正义链含有与hif2αmrna中的序列在至少16个连续核苷酸的核心片段上至少90%一致的核苷酸序列。在一些实施方式中,与hif2α mrna中的序列至少90%一致的核苷酸序列为长度16、17、18、19、20、21、22 或23个核苷酸。hif2αrnai触发剂的
反义链含有与hif2αmrna及对应正义链中的序列在至少16个连续核苷酸的核心片段上至少90%互补的核苷酸序列。在一些实施方式中,与hif2αmrna或对应正义链中的序列至少90%互补的核苷酸序列为长度16、17、18、19、20、21、22或23个核苷酸。
8.在一些实施方式中,一种或多种hif2αrnai触发剂使用本领域中已知的任何寡核苷酸递送技术递送至靶细胞或组织中。核酸递送方法包括(但不限于)通过包封于脂质粒中、通过离子导入或通过并入至其他载剂中,例如水凝胶、环糊精、生物可降解纳米胶囊及生物黏附微球体、蛋白质载体或dynamic polyconjugates
tm
(dpc)。在一些实施方式中,使hif2αrnai触发剂偶联至靶向基团,例如整合素结合化合物。在一些实施方式中,hif2αrnai触发剂偶联至递送聚合物或载剂。递送聚合物可为经可逆修饰的膜活性多胺。递送聚合物还可为靶向整合素的经可逆修饰的膜活性多胺。
9.靶向整合素的经可逆修饰的膜活性多胺包括经由可逆的生理学不稳定共价键偶联至一种或多种整合素结合化合物的膜活性多胺。在一些实施方式中,靶向整合素的经可逆修饰的膜活性多胺进一步包含经由可逆的生理学不稳定共价键偶联至一种或多种空间稳定剂的膜活性多胺。整合素结合化合物可为(但不限于)rgd肽及 rgd模拟物。可逆的生理学不稳定共价键包括(但不限于)二肽氨基苯甲基氨基甲酸酯键、四肽键及双取代的马来酰氨酸酯键。
10.hif2αrnai触发剂任选与一种或多种额外(即第二、第三等)治疗剂组合。第二治疗性可为另一hif2αrnai触发剂(例如靶向hif2α靶标内的不同序列的hif2αrnai触发剂)。额外治疗性还可为小分子药物、抗体、抗体片段和/或疫苗。hif2α rnai触发剂可在有或无一种或多种额外治疗剂下与一种或多种赋形剂组合以形成医药组合物。
11.本发明还涵盖治疗有至少部分通过hif2α表达介导的病理性病况的人类对象的方法,该方法包含向对象给予治疗有效量的hif2αrnai触发剂或含hif2αrnai 触发剂的组合物步骤。用hif2αrnai触发剂或含hif2αrnai触发剂的组合物治疗对象的方法可任选与一个或多个给予一种或多种额外(即第二)治疗剂(therapeutic) 或治疗(treatment)的步骤组合。hif2αrnai触发剂及额外治疗剂可以单一组合物给予或将其分别给予。额外治疗剂的非限制性示例包括(但不限于)vegfr抑制剂(例如示例包括(但不限于)vegfr抑制剂(例如)、细胞激素(例如il-2、ifn-α)、mtor抑制剂(例如)、抗pd1药物(例如及)、抗ctla4(例如)、靶向癌细胞中的信号转导路径组分的药物(例如vegf、pi-3-激酶、mek、jak、akt、myc、met、src家族激酶、 abl、axl、mer)、抗pd-l1、抗pd-l2、抗tim3、抗lag3、抗cd28、抗ox40、抗ox-40l、抗cd39、抗cd40、抗cd80、抗cd86、抗cd137、抗41bbl、抗 tigit、抗gitr、抗girtl、抗cd155、抗fas、抗fasl、抗trail/trail-l、 ido-1抑制剂及tdo-2抑制剂。
12.医药组合物可根据所需局部或全身治疗及待治疗的区域而以多种方式给予。给药可为局部(例如通过经皮贴片)、经肺(例如通过吸入或吹入粉末或气溶胶,包括通过喷雾器、气管内、鼻内)、表皮、经皮、经口或非经肠。非经肠给予包括(但不限于)静脉内、动脉内、皮下、腹膜内或肌肉内注射或输注;皮下(例如经由植入装置)、颅内、脑实质内、鞘内及室内
给予。
13.所述hif2αrnai触发剂和/或组合物可用于治疗性治疗疾病的方法中,所述疾病包括(但不限于):癌症、肾癌、透明细胞肾细胞癌、非小细胞肺癌、星形细胞瘤 (脑癌)、膀胱癌、乳癌、软骨肉瘤、结肠直肠癌、胃癌、神经胶母细胞瘤、头颈鳞状细胞癌、肝细胞癌、肺腺癌、神经母细胞瘤、黑素瘤、多发性骨髓瘤、卵巢癌、直肠癌、癌转移、齿龈炎、牛皮癣、卡波西氏肉瘤相关的疱疹病毒、子痫前症、炎症、慢性炎症、新生血管性疾病及类风湿性关节炎。此类方法包括向例如人类或动物对象的对象给予如本文所述的hif2αrnai触发剂。
14.除非另外定义,否则本文中所用的所有技术及科学术语均具有与本发明所属领域中的普通技术人员通常所理解相同的含义。尽管类似或等效于本文所述的那些方法及材料的方法及材料可用于实践或测试本发明,但下文描述适合方法及材料。本文中所提及的所有公开案、专利申请、专利及其他参考均以全文引用的方式并入本文中。在有矛盾的情况下,将以本说明书(包括定义)为准。另外,材料、方法及实施方式仅为说明性且不意欲限制。
15.本发明的其他特征及优势将自以下详细说明及权利要求而显而易见。
16.附图简单说明
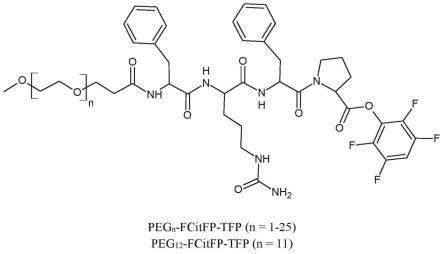
17.图1.表示peg
n-fcitfp-tfp修饰剂的化学结构。
18.图2.表示rgd-peg
n-fcitfp-tfp修饰剂的化学结构。
19.图3.表示rgd-peg
n-acit-pabc-pnp修饰剂的化学结构。
20.图4.表示醛-peg
n-fcit-pabc-pnp修饰剂的化学结构。
21.图5.表示醛-peg
n-acit-pabc-pnp修饰剂的化学结构。
22.图6.表示spdp-peg
n-fcit-pabc-pnp修饰剂的化学结构。
23.图7.表示peg
n-acit-pabc-pnp及peg
n-fcit-pabc-pnp修饰剂的化学结构。
24.图8.说明小鼠中治疗期间的血清seap含量的图。相对于(-1)天给药前含量,血清seap含量的倍数变化。对于g1及g2,n=4。对于g3,n=3。
25.图9.小鼠中3次每周治疗后的肿瘤总体形态。g1,载剂;g2400μghif2α-itg-dpc;g3 280μg hif2α-itg-dpc。展示来自各动物的两个肾。将肿瘤植入右侧所示的肾脏中。来自治疗组的肿瘤均显着较小且展示与对照物相比时有一些变色。
26.图10.肿瘤福尔马林固定的石蜡部分的h&e染色。细箭头表明凋亡的细胞。粗箭头表明巨噬细胞浸润。a图,g1载剂处理。在罕见凋亡细胞下为典型管型rcc 形态(细箭头)b图,g2 400μg hif2α-itg-dpc处理。在许多凋亡细胞下在周围区域中有巨大坏死中心及肿瘤结构的整体丧失。c图,g3 280μg hif2α-itg-dpc处理。在巨噬细胞浸润及许多凋亡细胞下有典型管肿瘤结构的破坏。
具体实施方式
27.本文描述用于抑制hif2α基因表达的rnai触发剂(在本文中称为hif2αrnai 触发剂)。各hif2αrnai触发剂包含正义链及反义链。正义链及反义链彼此间部分地、实质上或完全互补。在一些实施方式中,本文所述rnai触发剂正义链及反义链的长度独立地为长度16至30个核苷酸。在一些实施方式中,本文所述rnai 触发剂正义链及反义链的长度独立地为长度17至26个核苷酸。在一些实施方式中,本文所述rnai触发剂正义链及反义链独立地为长度17、18、19、20、21、22、 23、24、25或26个核苷酸。正义链及反义链可为相同长度或其可
为不同长度。在一些实施方式中,正义链为长度约19个核苷酸,而反义链为长度约21个核苷酸。在一些实施方式中,正义链为长度约21个核苷酸,而反义链为长度约23个核苷酸。在其他实施方式中,正义链及反义链独立地为长度17至21个核苷酸。在一些实施方式中,正义链与反义链各自为长度21至26个核苷酸。用于形成hif2αrnai触发剂分子的核苷酸序列的示例提供于表1至2及5中。
28.rnai触发剂包括(但不限于):短干扰rna(sirna)、双链rna(dsrna)、微 rna(mirna)、短发夹rna(shrna)及内切酶底物(美国专利第8,084,599号、第 8,349,809号及第8,513,207号)。本文所述的rnai触发剂在递送至表达hif2α基因的细胞时,经由rna干扰(rnai)的生物过程而体外或体内抑制或减少hif2α基因表达。
29.hif2αrnai触发剂包含正义链及反义链,其各自含有长度16至23个核碱基的核心序列。反义链核心序列为与hif2αmrna中存在的核苷酸序列(有时称为例如靶标序列)100%(完全)互补或至少90%(实质上)互补。正义链核心序列与反义链中的序列100%(完全)互补或至少90%(实质上)互补,且因此正义链核心序列与 hif2αmrna中存在的核苷酸序列(靶标序列)完全一致或至少90%一致。正义链核心序列可为与对应反义核心序列长度相同或其可为长度不同。在一些实施方式中,反义链核心序列为长度16、17、18、19、20、21、22或23个核苷酸。在一些实施方式中,正义链核心序列为长度16、17、18、19、20、21、22或23个核苷酸。
30.hif2αrnai触发剂有义及反义链通常退火以形成双链。在互补双链区内,正义链核心序列与反义核心序列至少90%互补或100%互补。在一些实施方式中,正义链核心序列含有至少16、至少17、至少18、至少19、至少20或至少21个核苷酸的序列,该序列与反义链核心序列的对应16、17、18、19、20或21个核苷酸序列至少90%或100%互补(即hif2αrnai触发剂的正义链及反义核心序列具有至少 16、至少17、至少18、至少19、至少20或至少21个核苷酸的区域,即至少90%碱基配对或100%碱基配对)。
31.如本文所用,术语“序列”或“核苷酸序列”指核碱基、核苷酸和/或核苷的顺序或次序,其使用标准核苷酸命名法及本文所述的经修饰核苷酸的索引、使用一连串字母来描述。
32.如本文所用,除非另外指明,否则术语“互补”在用于描述第一核苷酸序列(例如rnai触发剂正义链或hif2αmrna)与第二核苷酸序列(例如rnai触发剂反义链)的关系时,指包含第一核苷酸序列的寡核苷酸或聚核苷酸能够与包含第二核苷酸序列的寡核苷酸或聚核苷酸在某些条件下杂交(形成碱基对氢键)及形成双链或双螺旋结构。互补序列包括沃森-克里克碱基对(watson-crick base pairs)或非沃森
‑ꢀ
克里克碱基对且包括天然或经修饰的核苷酸或核苷酸模拟物,只要满足其能够杂交的上述要求即可。“全部互补”或“完全互补”表示第一聚核苷酸的邻接序列中的所有(100%)碱基将与第二聚核苷酸的邻接序列中的相同数目的碱基杂交。邻接序列可包含第一或第二核苷酸序列的全部或一部分。如本文所用,“部分互补”表示在杂交的核碱基序列对中,第一聚核苷酸的邻接序列中的至少70%碱基将与第二聚核苷酸的邻接序列中的相同数目的碱基杂交。如本文所用,“实质性互补”表示在杂交的核碱基序列对中,第一聚核苷酸的邻接序列中的至少85%碱基将与第二聚核苷酸的邻接序列中的相同数目的碱基杂交。如本文所用,术语“互补”、“完全互补”及“实质上互补”可结合rnai触发剂的正义链与反义链之间或rnai触发剂的反义链与hif2αmrna的序列之间的碱基匹配使用。序列一致性或互补性与修饰无关。出于测定一致性或互
补性的目的,例如a及af与u(或t)互补且与a一致。
33.正义链和/或反义链可任选且独立地在核心序列的3'端、5'端或3'端与5'端含有额外1、2、3、4、5或6个核苷酸(延伸部分)。反义链中的额外核苷酸若存在,则可与或可不与hif2αmrna中的对应序列互补。正义链中的额外核苷酸若存在,则可与或可不与hif2αmrna中的对应序列一致。反义链中的额外核苷酸若存在,则可与或可不与对应正义链中的额外核苷酸(若存在)互补。
34.如本文所用,延伸部分在正义链核心序列和/或反义链核心序列的5'端和/或3' 端包含1、2、3、4、5或6个核苷酸。正义链上的延伸核苷酸可与或可不与对应反义链中的核苷酸(核心序列核苷酸或延伸核苷酸)互补。相反,反义链中的延伸核苷酸可与或可不与对应正义链中的核苷酸(核心序列核苷酸或延伸核苷酸)互补。在一些实施方式中,rnai触发剂的正义链与反义链含有3'及5'延伸部分。在一些实施方式中,一个链的一个或多个3'延伸核苷酸与另一链的一个或多个5'延伸核苷酸碱基配对。在其他实施方式中,一个链的一个或多个3'延伸核苷酸与另一链的一个或多个5'延伸核苷酸并非碱基配对。在一些实施方式中,hif2αrnai触发剂具有含有3'延伸部分的反义链及含有5'延伸部分的正义链。
35.在一些实施方式中,hif2αrnai触发剂分子包含具有长度1、2、3、4、5或 6个核苷酸的3'延伸部分的反义链。在其他实施方式中,hif2αrnai触发剂分子包含具有长度1、2或3个核苷酸的3'延伸部分的反义链。在一些实施方式中,一个或多个反义链延伸核苷酸包含尿嘧啶或胸苷核苷酸或与对应hif2αmrna序列互补的核苷酸。在一些实施方式中,反义链延伸部分可为(但不限于):uau、ugu、 udtsdt、usdtsdt、ufau、aua、afsusa、uau、uafu、uau、udau、uscu、usgu、 uscsu、cau、aua、aua、u(invda)u、cag、agu、gcg、caa、usasu、uamtm或ustmsam(各以5'至3'列出,表2中的记法相同)。
36.在一些实施方式中,hif2αrnai触发剂分子包含具有长度1、2、3、4或5 个核苷酸的5'延伸部分的反义链。在其他实施方式中,hif2αrnai触发剂分子包含具有长度1或2个核苷酸的5'延伸部分的反义链。在一些实施方式中,一个或多个反义链延伸核苷酸包含尿嘧啶或胸苷核苷酸或与对应hif2αmrna序列互补的核苷酸。在一些实施方式中,反义链延伸部分包括或由da、dt、pdt、vpdt或u 组成,其中da及dt分别表示脱氧腺苷及脱氧胸苷核苷酸,pdt表示具有5'磷酸酯的脱氧胸苷核苷酸,vpdt表示乙烯基膦酸酯脱氧胸苷核苷酸,且u表示经2'-ome 修饰的尿嘧啶核苷酸。反义链可具有任一个上述3'延伸部分与任一个所述5'反义链延伸部分(若存在)的组合。
37.在一些实施方式中,hif2αrnai触发剂分子包含3'延伸部分长度为1、2、3、 4或5个核苷酸的正义链。在一些实施方式中,一个或多个正义链延伸核苷酸包含腺苷、尿嘧啶或胸苷核苷酸、at二核苷酸,或与hif2αmrna序列中的核苷酸对应的核苷酸。在一些实施方式中,3'正义链延伸部分包括或由组成af、invda、invdt、 a(invdt)、af(invdt)、u(invdt)、uf(invdt)、afabuau、dtdt或dtsdt,其中af 及uf分别表示2'-氟腺苷及尿嘧啶核苷酸,invda及invdt分别表示3'-3'连接(反向) 脱氧腺苷及脱氧胸苷核苷酸,ab表示无碱基核糖,u表示经2'-ome修饰的尿嘧啶核苷酸,dt表示脱氧胸苷核苷酸,sdt表示具有5'硫代磷酸的脱氧胸苷核苷酸,且 u及a表示尿嘧啶及腺苷核糖核苷酸。
38.在一些实施方式中,hif2αrnai触发剂分子包含5'延伸部分长度为1、2、3、 4、5或6个核苷酸的正义链。在一些实施方式中,一个或多个正义链延伸核苷酸包含尿嘧啶或腺苷
核苷酸或与hif2αmrna序列中的核苷酸对应的核苷酸。在一些实施方式中,正义链5'延伸部分可为(但不限于):uauaus、uauau、uauuagfs、 ufaufaa、uauaa、auauu、afuafuu、auauu、uaufau、uaua(uuna)、uauau、 udaudau、uuaga、uuauu、uugau、uuaga、uauga、auagas、uauaus、uauaas、 udauau、adtaga、auaga、u(invda)uau、gacau、ugaau、gcgau、uauga、uugga、auaga(各以5'至3'列出,表2中的记法相同)。正义链可具有3'延伸部分和/或5'延伸部分。
39.表1及表5中提供未经修饰的hif2αrnai触发剂正义链及反义链序列。形成 hif2αrnai触发剂时,表1及5中所列举的各序列中的各核苷酸可为经修饰的核苷酸。
40.表1.未修饰的hif2αrnai触发剂反义链和正义链序列
41.[0042][0043]
本文所述的hif2αrnai触发剂由反义链与正义链退火而形成。在一些实施方式中,hif2αrnai触发剂反义链包含表1及5中的任一种序列的核苷酸序列。在一些实施方式中,hif2αrnai触发剂反义链包含表1及5中的任一种序列的核苷酸1-17、2-17、1-18、2-18、1-19、2-19、1-20、2-20、1-21、2-21、1-22、2-22、 1-23、2-23、1-24、2-24、1-25、2-25、1-26或2-26的序列。在一些实施方式中, hif2αrnai触发剂正义链包含表1及5中的任一种序列的核苷酸序列。在一些实施方式中,hif2αrnai触发剂正义链包含表1及5中的任一种序列的核苷酸1-17、2-17、1-18、2-18、1-19、2-19、1-20、2-20、1-21、2-21、1-22、2-22、1-23、2-23、 1-24、2-24、1-25、2-25、1-26或2-26的序列。
[0044]
在一些实施方式中,本文所述的rnai触发剂的正义链及反义链含有相同数目的核苷酸。在一些实施方式中,本文所述的rnai触发剂的正义链及反义链含有不同数目的核苷酸。在一些实施方式中,rnai触发剂的正义链5'端及反义链3'端形成钝端。在一些实施方式中,rnai触发剂的正义链3'端及反义链5'端形成钝端。在一些实施方式中,rnai触发剂的两个末端形成钝端。在一些实施方式中,rnai 触发剂的末端皆非钝端。如本文所用,钝端指双链触发剂分子的末端,其中所退火的两个链的末端核苷酸为互补的(形成互补碱基对)。在
一些实施方式中,rnai触发剂的正义链5'端及反义链3'端形成磨损端。在一些实施方式中,rnai触发剂的正义链3'端及反义链5'端形成磨损端。在一些实施方式中,rnai触发剂的两个末端形成磨损端。在一些实施方式中,rnai触发剂的末端皆非磨损端。如本文所用,磨损端指双链触发剂分子的末端,其中所退火的两个链的末端核苷酸形成对(即不形成突出端),但不互补(即形成非互补对)。如本文所用,突出端为位于双链rnai 触发剂分子的一个链的末端的一个或多个不成对核苷酸的片段。不成对核苷酸可位于正义链或反义链上,从而产生3'或5'突出端。在一些实施方式中,rnai触发剂分子含有:一个钝端及一个磨损端、一个钝端及一个5'突出端、一个钝端及一个 3'突出端、一个磨损端及一个5'突出端、一个磨损端及一个3'突出端、两个5'突出端、两个3'突出端、一个5'突出端及一个3'突出端、两个磨损端或两个钝端。
[0045]
核苷酸碱基(或核碱基)为杂环嘧啶或嘌呤化合物,其为所有核酸的成分且包括腺嘌呤(a)、鸟嘌呤(g)、胞嘧啶(c)、胸腺嘧啶(t)及尿嘧啶(u)。如本文所用,“g”、“g”、“c”、“c”、“a”、“a”、“u”、“u”及“t”各自通常表示含有鸟嘌呤、胞嘧啶、腺嘌呤、尿嘧啶及胸苷作为碱基的核碱基、核苷、核苷酸或核苷酸模拟物。还如本文所用,术语“核苷酸”可包括经修饰的核苷酸或核苷酸模拟物、无碱基位点或替代置换部分。
[0046]
如本文所用,“经修饰的核苷酸”是不为核糖核苷酸(2'-羟基核苷酸)的核苷酸。在一些实施方式中,hif2αrnai触发剂含有一个或多个经修饰的核苷酸。在一些实施方式中,至少50%、至少60%、至少70%、至少80%、至少90%、至少95%或100%的核苷酸经修饰。经修饰的核苷酸包括(但不限于)脱氧核苷酸、核苷酸模拟物、无碱基核苷酸(本文中表示为x或ab)、经2'-修饰的核苷酸、3'-3'键连(反向) 核苷酸(在本文中表示为invdn、invn、invn、invx)、包含非天然碱基核苷酸、桥接核苷酸、肽核酸、2',3'-断核苷酸模拟物(未锁定核碱基类似物,在本文中表示为 n
una
或n
una
)、锁定核苷酸(在本文中表示为nlna或nlna)、3'-o-甲氧基(2'核苷酸间连接的)核苷酸(在本文中表示为3'-omen)、2'-f-阿拉伯糖核苷酸(在本文中表示为nfana或nfana)、吗啉基核苷酸、乙烯基膦酸酯脱氧核糖核苷酸(在本文中表示为vpdn)及乙烯基膦酸核苷酸。经2'-修饰的核苷酸(即五员糖环的2'位的基团不为羟基的核苷酸)包括(但不限于)2'-o甲基核苷酸(在本文中表示为核苷酸序列中的小写字母
‘
n’)、2'-脱氧-2'-氟核苷酸(在本文中表示为nf,在本文中还表示为 2'-氟核苷酸)、2'-脱氧核苷酸(在本文中表示为dn)、2'-甲氧基乙基(2'-o-2-甲氧基乙基)核苷酸(在本文中表示为nm或2'-moe)、2'-氨基核苷酸、2'-烷基核苷酸。指示化合物中的所有位置不需要均一修饰。相反,可在单一hif2αrnai触发剂中或甚至在其单一核苷酸中并入超过一个修饰。hif2αrnai触发剂正义链及反义链可通过本领域中已知的方法合成和/或修饰。一个核苷酸的修饰独立于另一核苷酸的修饰。
[0047]
经修饰的核苷酸还包括具有经修饰的核碱基的核苷酸。经修饰的核碱基包括(但不限于)合成及天然核碱基、经5-取代的嘧啶、6-氮杂嘧啶及n-2、n-6及o-6 取代的嘌呤,包括2-氨基丙基腺嘌呤、5-丙炔基尿嘧啶及5-丙炔基胞嘧啶、5-甲基胞嘧啶(5-me-c)、5-羟甲基胞嘧啶、黄嘌呤、次黄嘌呤、2-氨基腺嘌呤、腺嘌呤及鸟嘌呤的6-甲基及其他烷基衍生物、腺嘌呤及鸟嘌呤的2-丙基及其他烷基衍生物、 2-硫基尿嘧啶、2-硫基胸腺嘧啶及2-硫基胞嘧啶、5-卤基尿嘧啶及胞嘧啶、5-丙炔基尿嘧啶及胞嘧啶、6-偶氮尿嘧啶、胞嘧啶及胸腺嘧啶、5-尿嘧啶(假尿嘧啶)、4
‑ꢀ
尿嘧啶;8-卤基、8-氨基、8-硫醇、8-硫烷基、8-羟基及其他经
8-取代的腺嘌呤及鸟嘌呤;5-卤基(尤其5-溴、5-三氟甲基)及其他经5-取代的尿嘧啶及胞嘧啶;7-甲基鸟嘌呤及7-甲基腺嘌呤、8-氮鸟嘌呤及8-氮腺嘌呤、7-去氮鸟嘌呤及7-去氮腺嘌呤及3-去氮鸟嘌呤及3-去氮腺嘌呤。
[0048]
在一些实施方式中,20%或小于20%的经修饰的核苷酸为经2'-氟修饰的核苷酸。在一些实施方式中,hif2αrnai触发剂正义链在从3’端计的位置11含有2'-f 核苷酸。在一些实施方式中,hif2αrnai触发剂正义链在从3’端计的位置12含有 2'-f核苷酸。在一些实施方式中,hif2αrnai触发剂正义链在从3’端计的位置13 含有2'-f核苷酸。在一些实施方式中,hif2αrnai触发剂正义链在从3’端计的位置11、12及13含有至少两个2'-f核苷酸。在一些实施方式中,hif2αrnai触发剂正义链在从3’端计的位置11及12、位置11及13或位置12及13含有2'-f核苷酸。在一些实施方式中,hif2αrnai触发剂正义链在从3’端计的位置11、12及 13含有2'-f核苷酸。
[0049]
在一些实施方式中,hif2αrnai触发剂反义链在从5’端计的位置2含有2'-f 核苷酸。在一些实施方式中,hif2αrnai触发剂反义链在从5’端计的位置14含有 2'-f核苷酸。在一些实施方式中,hif2αrnai触发剂反义链在从5’端计的位置2 及14含有2'-f核苷酸。在一些实施方式中,hif2αrnai触发剂在相对于正义链的 3'端的位置11、12及13及在相对于反义链的5'端的位置2及14含有至少两个2'-f 核苷酸。
[0050]
在一些实施方式中,hif2αrnai触发剂反义链在从5’端计的位置4含有2'-f 核苷酸。在一些实施方式中,hif2αrnai触发剂反义链在从5’端计的位置6含有 2'-f核苷酸。在一些实施方式中,hif2αrnai触发剂反义链在从5’端计的位置8 含有2'-f核苷酸。在一些实施方式中,hif2αrnai触发剂反义链在从5’端计的位置10含有2'-f核苷酸。在一些实施方式中,hif2αrnai触发剂反义链在从5’端计的位置12含有2'-f核苷酸。在一些实施方式中,hif2αrnai触发剂正义链在从5’端计的位置4、6、8、10及12含有至少两个2'-f核苷酸。在一些实施方式中,hif2α rnai触发剂反义链在从5’端计的位置4及6、位置4及8、位置4及10、位置4 及12、位置6及8、位置6及10、位置6及12、位置8及10、位置8及12或位置10及12含有2'-f核苷酸。在一些实施方式中,hif2αrnai触发剂反义链在从 5’端计的位置4、6、8、10及12含有三个2'-f核苷酸。在一些实施方式中,hif2α rnai触发剂反义链在从5’端计的位置4、6、8、10及12含有至少四个2'-f核苷酸。在一些实施方式中,hif2αrnai触发剂反义链在从5’端计的位置4、6、8及 10、位置4、6、8及12、位置4、6、10及12、位置4、8、10及12或位置6、8、 10及12含有2'-f核苷酸。
[0051]
在一些实施方式中,hif2αrnai触发剂反义链在从5’端计的位置2和/或位置 14含有2'-f核苷酸且在从5’端计的位置11、12及13含有一、两或三个2'-f核苷酸。在一些实施方式中,hif2αrnai触发剂在相对于反义链的5'端的位置2和/或位置14含有2'-f核苷酸且在相对于反义链的5'端的位置11、12及13含有一、两或三个2'-f核苷酸,且在相对于正义链的3'端的位置11、12及13含有至少两个2'-f核苷酸。
[0052]
在一些实施方式中,hif2αrnai触发剂的一个或多个核苷酸通过非标准键或主链(即经修饰的核苷间连接或经修饰的主链)连接。在一些实施方式中,经修饰的核苷间连接为不含磷酸酯基的共价核苷间连接。经修饰的核苷间键或主链包括(但不限于)硫代磷酸酯基、5'-硫代磷酸酯基、(在本文中表示为核苷酸前的小写字母
‘
s’,如在sn、sn、snf或sdn中)、手性硫代磷酸酯基、硫代磷酸酯基、二硫代磷酸酯基、磷酸三酯基、氨基烷基-磷酸三酯
基、甲基及其他烷基膦酸酯基(包含3'-烷撑膦酸酯及手性膦酸酯)、亚膦酸酯基、氨基磷酸酯(包含3'-氨基氨基磷酸酯)及氨基烷基氨基磷酸酯基、硫逐氨基磷酸酯基、硫逐烷基-磷酸酯基、硫逐烷基磷酸三酯基、吗啉基键及具有正常3'-5'键的硼烷磷酸酯基、这些基团的2'-5'连接的类似物及具有反向极性的那些基团,其中相邻对核苷单元3'-5'至5'-3'或2'-5'至5'-2'连接。在其他实施方式中,经修饰的核苷间键或主链不具有磷原子。缺乏磷原子的经修饰的核苷间键包括(但不限于)短链烷基或环烷基糖间键、混合杂原子及烷基或环烷基食糖键、或一个或多个短链杂原子或杂环糖间键。在一些实施方式中,经修饰的核苷间主链包括(但不限于)硅氧烷主链、硫基、亚砜及砜主链;甲酰基及硫甲酰基主链、亚甲基甲酰基及硫甲酰基主链、含烯烃的主链、氨基磺酸酯基主链、亚甲基亚氨基及亚甲基肼基主链、磺酸酯基及磺酰胺主链、酰胺主链;及具有n、o、s及ch2组分部分的其他主链。
[0053]
在一些实施方式中,hif2αrnai触发剂含有一个或多个经修饰的核苷酸及一个或多个经修饰的核苷间键。在一些实施方式中,经2'-修饰的核苷酸与经修饰的核苷间键组合。举例而言,在一些实施方式中,hif2αrnai触发剂的正义链可含有1、2、3、4个硫代磷酸酯键,hif2αrnai触发剂的反义链可含有1、2、3或4 个硫代磷酸酯键,或正义链与反义链独立地可含有1、2、3或4个硫代磷酸酯键。
[0054]
在一些实施方式中,hif2αrnai触发剂正义链含有两个硫代磷酸酯核苷间键。在一些实施方式中,两个硫代磷酸酯核苷间键位于相对于正义链的3'端的位置1-3 的核苷酸之间。在一些实施方式中,两个硫代磷酸酯核苷间键位于相对于正义链的 5'端的位置1-3、2-4、3-5、4-6、4-5或6-8的核苷酸之间。在一些实施方式中,hif2α rnai触发剂反义链含有四个硫代磷酸酯核苷间键。在一些实施方式中,四个硫代磷酸酯核苷间键位于相对于正义链的5'端的位置1-3的核苷酸之间及从5’端计的位置19-21、20-22、21-23、22-24、23-25或24-26的核苷酸之间。在一些实施方式中,hif2αrnai触发剂含有正义链中的两个硫代磷酸酯核苷间键及反义链中的四个硫代磷酸酯核苷酸间连接(internucleotide linkage)。
[0055]
在一些实施方式中,hif2αrnai触发剂以盐、混合盐或无酸的形式制备或提供。
[0056]
表2a及表5b中提供含有经修饰的核苷酸的反义链的示例。表2b及表5b 中提供含有经修饰的核苷酸的正义链的示例。在表2a、2b及5b中,使用以下标记指示经修饰的核苷酸:
[0057]
n=2'-oh(未经修饰)核糖核苷酸(未指示f或d的大写字母)
[0058]
n=经2'-ome修饰的核苷酸
[0059]
nf=经2'-氟修饰的核苷酸
[0060]
dn=2'-脱氧核苷酸
[0061]nuna
=2',3'-断核苷酸模拟物(未锁定核碱基类似物)
[0062]
nm=2'-甲氧基乙基核苷酸
[0063]
(invdn)=反向脱氧核糖核苷酸(3'-3'连接型核苷酸)
[0064]
(invab)=反向无碱基核苷酸
[0065]
s=硫代磷酸酯连接型核苷酸
[0066]
p=磷酸酯
[0067]
vpdn=乙烯基膦酸酯脱氧核糖核苷酸
[0068]
表2a.具有经修饰的核苷酸的hif2αrnai触发剂反义链
[0069]
[0070]
[0071][0072]
表2b.具有经修饰的核苷酸的hif2αrnai触发剂正义链
[0073]
[0074]
[0075]
[0076][0077]
表3.双id编号的hif2αrnai触发剂双链体
[0078]
[0079]
[0080]
[0081]
[0082][0083]
含有表2b中所列举的序列的正义链可与含有表2a中所列举的序列的任何反义链杂交,限制条件为两个序列具有在邻接16、17、18、19、20或21核苷酸序列上至少90%互补的区域。代表性hif2αrna触发剂由表3中所示的双链id号表示。在一些实施方式中,hif2αrnai触发剂由本文中呈现的双链id号中的任一种组成。在一些实施方式中,hif2αrnai触发剂包含本文中所呈现的任一双链id号。在一些实施方式中,hif2αrnai触发剂包含本文中所呈现的任一双链id号的正义链及反义链核苷酸序列。在一些实施方式中,hif2αrnai触发剂包含本文中所呈现的任一双链id号的正义链及反义链核苷酸序列及靶向基团和/或连接基团,其中靶向基团和/或连接基团共价连接至正义链或反义链。在一些实施方式中,hif2αrnai 触发剂包含本文中所呈现的任一双链id号的正义链及反义链经修饰的核苷酸序列。在一些实施方式中,hif2αrnai触发剂包含本文中所呈现的任一双链id号的正义链及反义链经修饰的核苷酸及靶向基团和/或连接基团,其中靶向基团和/或连接基团共价连接至正义链或反义链。
[0084]
在一些实施方式中,hif2αrnai触发剂包含有包含seq id no.4的核苷酸 2-21的核苷酸碱基序列的反义链。在一些实施方式中,hif2αrnai触发剂包含有包含seq id no.4的核苷酸2-21的核苷酸碱基序列的反义链及包含seq id no.53 的核苷酸碱基序列的正义链。
[0085]
在一些实施方式中,hif2αrnai触发剂包含有包含seq id no.88、seq idno.157、seq id no.159或seq id no.163的核苷酸碱基序列的反义链。在一些实施方式中,hif2αrnai触发剂包含有包含seq id no.88的核苷酸碱基序列的反义链及包含seq id no.179的核苷酸碱基序列的正义链。在一些实施方式中, hif2αrnai触发剂包含有包含seq id no.88的核苷酸碱基序列的反义链及包含seq id no.177的核苷酸碱基序列的正义链。在一些实施方式中,hif2αrnai触发剂包含有包含seq id no.157的核苷酸碱基序列的反义链及包含seq idno.175的核苷酸碱基序列的正义链。在一些实施方式中,hif2αrnai触发剂包含有包含seq id no.159的核苷酸碱基序列的反义链及包含seq id no.185的核苷酸碱基序列的正义链。在一些实施方式中,hif2αrnai触发剂包含有包含seq idno.163的核苷酸碱基序列的反义链及包含seq id no.185的核苷酸碱基序列的正义链。
[0086]
在一些实施方式中,hif2αrnai触发剂包含有包含seq id no.88、seq idno.157、seq id no.159或seq id no.163的反义链。在一些实施方式中,hif2α rnai触发剂包含有包含seq id no.88的反义链及包含seq id no.179的正义链。在一些实施方式中,hif2αrnai触发剂包含有包含seq id no.88的反义链及包含 seq id no.177的正义链。在一些实施方式中,hif2αrnai触发剂包含有包含seqid no.157的反义链及包含seq id no.175的正义链。在一些实施方式中,hif2α rnai触发剂包含有包含seq id no.159的反义链及包含
seq id no.185的正义链。在一些实施方式中,hif2αrnai触发剂包含有包含seq id no.163的反义链及包含seq id no.185的正义链。
[0087]
在一些实施方式中,hif2αrnai触发剂包含反义链,其包含seq id no.38 的核苷酸2-21的核苷酸碱基序列。在一些实施方式中,hif2αrnai触发剂包含有包含seq id no.38的核苷酸2-21的核苷酸碱基序列的反义链及包含seq idno.56的核苷酸1-19的核苷酸碱基序列的正义链。
[0088]
在一些实施方式中,hif2αrnai触发剂包含有包含seq id no.86、seq idno.155、seq id no.156的核苷酸碱基序列的反义链。在一些实施方式中,hif2α rnai触发剂包含有包含seq id no.156的核苷酸碱基序列的反义链及包含seqid no.195的核苷酸碱基序列的正义链。在一些实施方式中,hif2αrnai触发剂包含有包含seq id no.86的核苷酸碱基序列的反义链及包含seq id no.197的核苷酸碱基序列的正义链。在一些实施方式中,hif2αrnai触发剂包含有包含seq idno.155的核苷酸碱基序列的反义链及包含seq id no.209的核苷酸碱基序列的正义链。
[0089]
在一些实施方式中,hif2αrnai触发剂包含有包含seq id no.86、seq idno.155、seq id no.156的反义链。在一些实施方式中,hif2αrnai触发剂包含有包含seq id no.156的反义链及包含seq id no.195的正义链。在一些实施方式中,hif2αrnai触发剂包含有包含seq id no.86的反义链及包含seq idno.197的正义链。在一些实施方式中,hif2αrnai触发剂包含有包含seq idno.155的反义链及包含seq id no.209的正义链。
[0090]
在一些实施方式中,hif2αrnai触发剂含有或偶联至靶向基团、连接基团、递送聚合物、递送载剂和/或其他非核苷酸基团。靶向基团、连接基团、递送聚合物、递送载剂和/或其他非核苷酸基团可共价连接至任一正义链和/或反义链的3'和/ 或5'端。在一些实施方式中,hif2αrnai触发剂可含有连接至正义链的3'和/或5' 端的靶向基团、连接基团、递送聚合物、递送载剂或其他非核苷酸基团。在一些实施方式中,靶向基团、连接基团、递送聚合物、递送载剂或其他非核苷酸基团连接至hif2αrnai触发剂正义链的5'端。在一些实施方式中,靶向基团、连接基团、递送聚合物、递送载剂和/或其他非核苷酸基团经由接头每连接基团直接或间接连接至触发剂。在一些实施方式中,靶向基团、连接基团、递送聚合物、递送载剂和 /或其他非核苷酸基团经由不稳定、可裂解或可逆键或接头连接至触发剂。
[0091]
靶向基团可增强rnai触发剂或与其连接的偶联物的药物动力学或生物分布特性,以改良偶联物的细胞特异性或组织特异性分布及细胞特异性吸收。在一些情况下,靶向基团偶联至细胞或细胞受体可起始内吞作用。靶向基团可为单价、二价、三价、四价或具有较高价数。代表性靶向基团包括(但不限于)对细胞表面分子具有亲和力的化合物、对细胞表面分子具有亲和力的细胞受体配体、半抗原、抗体、单抗、抗体片段及抗体模拟物。
[0092]
可合成在5'端具有例如氨基的反应性基团的本文所述的rnai触发剂分子。反应性基团可用于随后使用本领域中典型的方法连接靶向部分。
[0093]
在一些实施方式中,hif2αrnai触发剂包括与触发剂结合的连接基团。连接基团有助于触发剂共价键至靶向基团或递送聚合物或递送载剂。连接基团可连接至 rnai触发剂正义链或反义链的3'或5'端。在一些实施方式中,连接基团连接至 rnai触发剂正义链。在一些实施方式中,连接基团偶联至rnai触发剂正义链的 5'或3'端。在一些实施方式中,连接基团偶联至rnai触发剂正义链的5'端。连接基团的示例包括(但不限于):alk-smpt-c6、
alk-ss-c6、dbco-teg、me-alk-ss-c6 及c6-ss-alk-me、反应性基团(例如伯胺及炔烃)、烷基、无碱基核糖、核糖醇和/ 或peg基团。
[0094]
接头或连接基团为两个原子之间的连接,其使所关注的一个化学基团(例如 rnai触发剂)或区段经由一个或多个共价键接至所关注的另一个化学基团(例如靶向基团或递送聚合物)或区段。不稳定键(labile linkage)含有不稳定键合(labilebond)。键可任选包括使两个所连接原子之间的距离增加的间隔子。间隔子可进一步增加键连的柔性和/或长度。间隔子可包括(但不限于)烷基、烯基、炔基、芳基、芳烷基、芳烯基及芳炔基;其中的每一种可含有一个或多个杂原子、杂环、氨基酸、核苷酸及醣类。间隔基团在本领域中已熟知且前述列表不意欲限制本发明的范围。
[0095]
靶向基团及连接基团包括(但不限于)(alk-c6)、(alk-c6-c6)、 (alk-c6-smpt-c6)、(alk-peg5-c6)、(alk-peg5-c6)(alk-peg5-ser)、 (alk-smpt-c6)、(alk-ss-c6)、(c6-ss-alk-me)、(chol-teg)、(dbco-teg)、 (me-alk-ss-c6)、(nag13)、(nh2-c6)。在一些实施方式中,表2b中所列举的含有3'或5'靶向基团或连接基团的任一hif2αrnai触发剂正义链线可替代地不含有 3'或5'靶向基团或连接基团,或可含有不同的3'或5'靶向基团或连接基团,包括(但不限于)表4中描绘的那些。
[0096]
在一些表4中所示的靶向基团及连接基团结构中,rnai触发剂通过触发剂、 rna、r、或r1或r2所展示并指示(即触发剂、rna或r1或r2各包含rnai 触发剂)。举例而言,关于(alk-c6-ser)、(alk-peg5-ser)及(alk-peg13-ser),r1及 r2之一包含rnai触发剂且其它可为氢。
[0097]
表4.代表靶向基团和连接基团的结构
[0098]
[0099]
[0100]
[0101]
[0102]
[0103][0104]
在一些实施方式中,递送载剂可用于将rnai触发剂递送至细胞或组织中。递送载剂为使rnai触发剂递送至细胞或组织改良的化合物。递送载剂可包括(但不限于)以下或由其组成:聚合物,例如两性聚合物、膜活性聚合物、肽、蜂毒素肽、蜂毒素样肽、脂质、经可逆修饰的聚合物或肽或经可逆修饰的膜活性多胺。
[0105]
在一些实施方式中,rnai触发剂可与脂质、纳米颗粒、聚合物、脂质粒、微胞、dpc或本领域中可利用的其他递送系统组合。rnai触发剂还可以化学方式偶联至靶向基团、脂质(包括(但不限于)胆固醇及胆固醇基衍生物)、纳米粒子、聚合物、脂质粒、微胞、dpc(参见例如wo 2000/053722、wo 2008/0022309、wo2011/104169及wo 2012/083185、wo 2013/032829、wo 2013/158141,其各以引用的方式并入本文中)或本领域中可利用的其他递送系统。
[0106]
在一些实施方式中,描述将hif2αrnai触发剂体内递送至肿瘤细胞的医药组合物。此类医药组合物可包括(但不限于)偶联至递送聚合物以形成rnai触发剂
‑ꢀ
递送聚合物偶联物的hif2αrnai触发剂。在一些实施方式中,递送聚合物为膜活性多胺。在一些实施方式中,递送聚合物为经可逆修饰的膜活性多胺。
[0107]
hif2αrnai触发剂-递送聚合物偶联物
[0108]
在一些实施方式中,描述由下式表示的组合:
[0109][0110]
其中rnai触发剂为如本文所述的hif2αrnai触发剂,p为膜活性多胺,m1包含经由可逆生理学不稳定键l1连接至p的靶向基团,且m2包含经由可逆生理学不稳定键l2连接至p的空间位阻稳定剂,x为大于1,y为大于或等于0。 (m
2-l2)
y-p-(l
1-m1)
x
不具膜活性。如本文所用,(m
2-l2)
y-p-(l
1-m1)
x
指递送聚合物。 (l
1-m1)及(m
2-l2)的裂解使p恢复至膜活性状态。在一些实施方式中,x y的值为p 的伯胺的数量的大于80%、大于90%或大于95%。在一些实施方式中,x y的值为p群的伯胺数量的大于80%、大于90%或大于95%。n的值可为0.25
至5(每4 个聚合物一(1)个rnai触发剂至每聚合物5个rnai触发剂)。在一些实施方式中, n值为0.5至5。在一些实施方式中,n为0.5至2。在一些实施方式中,n为0.8 至1.6。在一些实施方式中,x为1-20、2-20、3-20、4-20、5-20、6-20、7-20、8-20、 9-20、10-20、11-20、12-20、13-20、14-20或15-20。
[0111]
在一些实施方式中,m1包含整合素结合化合物。在一些实施方式中,整合素结合化合物包含αvβ3结合化合物。在一些实施方式中,整合素结合化合物包含rgd 配体。在一些实施方式中,αvβ3结合化合物包含rgd配体。在一些实施方式中, rgd配体包含rgd模拟物。在一个实施方式中,空间位阻稳定剂包含聚乙二醇 (peg)。在一些实施方式中,l1和/或l2的裂解使p上的未经修饰的胺恢复。在一些实施方式中,(l
1-m1)及(l
2-m2)独立地为四肽修饰剂和/或二肽修饰剂。在一些实施方式中,l1及l2独立地为四肽键或二肽-pabc(对氨基苯甲基-氨基甲酸酯)键。在一些实施方式中,l1及l2为四肽键。在其他实施方式中,l1及l2为二肽-pabc 键。在一些实施方式中,l1为二肽-pabc键且l2为四肽键。在其他实施方式中, l1为四肽键且l2为二肽-pabc键。在一些实施方式中,四肽键为fcitfp(苯丙氨酸-瓜氨酸-苯丙氨酸-脯氨酸)四肽键。在一些实施方式中,二肽-pabc键为 acit-pabc键。对于x=2或大于2,l1可为所有四肽键、所有二肽-pabc键或组合四肽键及二肽-pabc键。对于y=2或大于2,l2可为所有四肽键、所有二肽-pabc 键或组合四肽键及二肽-pabc键。
[0112]
在一些实施方式中,所述hif2αrnai触发剂偶联至经可逆修饰的膜活性多胺以形成rnai触发剂-递送聚合物偶联物。在一些实施方式中,rnai触发剂-递送聚合物偶联物包含由以下表示的式:
[0113]
(rnai触发剂)
n-聚(a
a-共-(b
b-接枝-(cc;dd)))(式2)
[0114]
其中
[0115]
a为含疏水性基团的单体单元,
[0116]
b为含伯胺的单体单元,
[0117]
c包含经由可逆生理学不稳定键连接(即接枝)至含伯胺的单体单元的整合素结合配体,
[0118]
d包含经由可逆生理学不稳定键连接(即接枝)至含伯胺的单体单元的空间位阻稳定剂,
[0119]
a为大于零的整数,
[0120]
b为大于或等于2的整数,
[0121]
c为大于或等于1的整数,
[0122]
d为大于或等于1的整数,
[0123]
c d的值为b值的大于80%、大于85%、大于90%或大于95%,
[0124]
聚(a
a-共-bb)为具有a及b单体单元的膜活性多胺共聚物
[0125]
rnai触发剂包含本文所述的hif2αrnai触发剂,及
[0126]
n具有0.25(即偶联至每四种递送聚合物中的仅一种)至5.0的值。
[0127]
聚(a
a-共-(b
b-接枝-(cc;dd)))不具膜活性。在一些实施方式中,整合素结合化合物包含αvβ3结合化合物。在一些实施方式中,整合素结合化合物包含rgd配体,例如rgd模拟物。在一些实施方式中,αvβ3结合化合物包含rgd配体,例如rgd 模拟物。在一个实施方式中,空间位阻稳定剂包含聚乙二醇(peg)。在一些实施方式中,peg含有2至25个乙二醇单元。在
一些实施方式中,c为1-75、1-50、5-50、 5-40、5-30、5-25、5-20、5-15、10-35、10-30、10-25、10-20或15-20的任何整数。在一些实施方式中,n具有0.5至2的值。在一些实施方式中,比率a:b(即a: b)为30:70至60:40。在一些实施方式中,比率a:b为60:40至40:60。在一些实施方式中,比率a:b为约45
±
5:55
±
5。在一些实施方式中,比率a:b 为约44:56。在一些实施方式中,比率a:b为约46:54。在一些实施方式中,聚合物的分子量(mw)为30kda至70kda。在其他实施方式中,聚合物的mw为 40kda至60kda。在其他实施方式中,聚合物的mw为40kda至50kda。在其他实施方式中,聚合物的mw约43kda至约48kda。在一些实施方式中,聚合物的多分散指数(pdi)小于1.4、小于1.3、1.25、小于1.2、小于1.15或小于1.1。在一些实施方式中,聚合物含有连接rnai触发剂的末端叠氮基团。在一些实施方式中, n为0.8至1.6。在一些实施方式中,n为1
±
0.5。在一些实施方式中,c为1-20、2-20、3-20、4-20、5-20、6-20、7-20、8-20、9-20、10-20、11-20、12-20、13-20、 14-20或15-20。在一些实施方式中,c d的值为b值大于80%、大于90%或大于 95%。在一些实施方式中,c为rgd-pegx-fcitfpro且d为peg
y-acit-pabc,其中x为1-50,y为4-30。在一些实施方式中,x大于y。
[0128]
在一些实施方式中,多胺聚(a
a-共-bb)为聚(丙烯酸酯)无规共聚物,其中a为含疏水性基团的丙烯酸酯单体且b为含伯胺的丙烯酸酯单体。在一些实施方式中, a为丙烯酸丙酯单体且b为乙氧基-乙胺丙烯酸酯单体。
[0129]
膜活性多胺具有膜活性且因此能够使电浆膜或溶酶体/内吞膜破裂。如本文所用,膜活性多胺为表面活性、两性聚合物,其能够诱导针对生物膜的以下效应中的一种或多种:膜变化或破裂,从而允许不可透过膜的分子进入细胞或穿越膜;膜中形成孔隙;膜分裂;或膜破裂或溶解。如本文所用,膜或细胞膜包含脂质双层。膜变化或破裂在功能上可通过至少一种以下分析中的肽活性定义:红血球溶胞(溶血)、脂质粒泄漏、脂质粒融合、细胞融合、细胞溶解及核内体释放。优选导致内体或溶酶体优先于电浆膜发生破裂的肽或经修饰的肽视为核内体裂解。经可逆修饰的膜活性多胺为核内体裂解肽的示例。膜活性聚合物对细胞膜的影响可为短暂的。膜活性聚合物对膜具有亲和力且引起双层结构发生变性或变形。rnai触发剂递送至细胞系通过膜活性多胺介导,其使质膜或内部微脂粒膜(例如核内体或溶酶体)破裂或不稳定,包括在膜中形成孔隙,或使核内体或溶酶体微脂粒破裂,由此允许微脂粒内含物释放至细胞质中。优选聚合物为两性聚(丙烯酸酯)无规共聚物。
[0130]
整合素结合化合物
[0131]
整合素结合化合物对细胞表面上表达的一种或多种整合素具有亲和力。整合素的非限制性示例包括αvβ3整合素。整合素结合化合物的示例包括(但不限于):αvβ3结合化合物、rgd配体。rgd配体包括含rgd肽的化合物及含rgd模拟物的化合物。如本文所用,rgd肽包含精氨酸-甘氨酸-天冬氨酸三肽。rgd肽可构型上受限。rgd肽可具有连接至rgd氨基酸序列的非肽组分。
[0132]
如本文所用,rgd配体包含《1500kda的rgd肽或rgd模拟物,其偶联至例如αv/β3(αvβ3或αvβ3)整合素的整合素(对其具有亲和力)。
[0133]
如本文所用,rgd模拟物为不为rdg肽的非肽合成分子,其从生物上模拟 rgd肽、整合素结合蛋白的整合素结合rgd部分或αvβ3整合素结合rgd基元的活性决定子。rgd模拟物可含有经由酰胺键连接的一个或两个天然存在的氨基酸。rgd模拟物可为经修饰的肽,含有非标准氨基酸或非标准氨基酸侧链。
[0134]
在一个实施方式中,rgd配体包含经由酰胺键连接至甘氨酸-天冬氨酸二肽的胍基团。本发明的胍基团具有由以下表示的结构:
[0135][0136]
其中r9及r
10
独立地为氢或烷基且可通过连接形成环,且r
11
为使胍基团连接至甘氨酸-天冬氨酸二肽的接头。胍基团包括上述所表示的结构与其共振结构。优选接头为:-(crr')-(crr')-(crr')-或-(crr')-(crr')-(crr')-(crr')-,其中:a)各 r独立地为任选存在且若存在则独立地为氢、烷基或芳基,b)r'独立地为氢、烷基、芳基或nh2,且c)各碳(c)可通过一个或多个单键及双键或芳族键连接。
[0137]
在一些实施方式中,rgd模拟物含有连接至天冬氨酸氨基酸的苯氧基。在一些实施方式中,rgd模拟物包含胍-甘氨酸-天冬氨酸-4-氨基苯氧基化合物。在一些实施方式中,胍-甘氨酸-天冬氨酸-4-氨基苯氧基化合物包含由表示的结构:
[0138][0139]
其中r
13
为:
[0140][0141]
在一些实施方式中,胍为
[0142]
及其共振结构。
[0143]
在一些实施方式中,rgd模拟物包含由以下表示的结构:
[0144][0145]
其中:
[0146]r14
是
[0147]
并且
[0148]
a包含接头。接头使rgd模拟物连接至另一分子,例如二肽氨基苯甲基-碳酸酯或四肽,使得溶解度增加或提供与另一分子共价键连的方式。
[0149]
空间位阻稳定剂
[0150]
如本文所用,空间位阻稳定剂为非离子型亲水性聚合物(天然、合成或非天然),相对于不含空间位阻稳定剂的聚合物,其防止或抑制与其所连接的分子发生分子内或分子间相互作用。空间稳定剂阻碍与其连接的聚合物参与静电相互作用。静电相互作用为两种或两种以上物质由于正电荷与负电荷之间的吸引力而发生的非共价结合。空间稳定剂可抑制与血液组分发生相互作用且因此抑制网状内皮系统的调理素作用、吞噬及吸收。空间稳定剂从而可使与其连接的分子的循环时间延长。空间稳定剂还可抑制分子聚集。在一些实施方式中,空间位阻稳定剂为聚乙二醇(peg)或peg衍生物。在一些实施方式中,peg可具有约1-500个乙烯单体或单元。在一些实施方式中,peg含有2至25个乙烯单元。在一些实施方式中,peg含有4至30个乙烯单元。在一些实施方式中,peg含有5至24个乙烯单元。在一些实施方式中,peg的平均分子量为约85至20,000道尔顿(da)。在一些实施方式中,peg的分子量为约85至1000da。如本文所用,相对于水溶液中不含有空间位阻稳定剂的聚合物,空间稳定剂防止或抑制其所连接的聚合物的分子内或分子间相互作用。
[0151]
可逆生理学不稳定键/修饰剂
[0152]
膜活性多胺可经可逆修饰。可逆修饰可经由修饰剂与膜活性多胺的伯胺可逆结合来实现。
[0153]
在一些实施方式中,可逆生理学不稳定键包含四肽键。在一些实施方式中,p-(l
1-m1)
x
和/或p-(l
2-m2)y(式1)包含:
[0154]r5-a
4-a
3-a
2-a
1-r6[0155]
其中r5包含靶向基团(m1)或空间位阻稳定剂(m2),
[0156]
a4为天然、非天然异构或合成疏水性l氨基酸,其中当其关于氨基酸侧链(r-基团)的组合时,针对甘氨酸校正的ph7下的疏水性指数(monera等人,j.proteinsci.1995,1,319)为41或大于41,
[0157]
a3为不带电亲水性l氨基酸,其中当其关于氨基酸侧链(r-基团)的组合时,针对甘氨酸校正的ph7下的疏水性指数(monera等人,j.proteinsci.1995,1,319)为-28或小于-28,
[0158]
a2为天然、非天然异构或合成疏水性公升氨基酸,其中当其关于氨基酸侧链(r-基团)的组合时,针对甘氨酸校正的ph7下的疏水性指数(monera等人,j.proteinsci.1995,1,319)为41或大于41,
[0159]
a1为l-脯氨酸、l-亮氨酸或l-n-甲基丙氨酸,且
[0160]
r6为p,其中p为式1膜活性多胺。
[0161]
在一些实施方式中,a1为脯氨酸,a2及a4独立地为丙氨酸、缬氨酸、亮氨酸、异亮氨酸或苯丙氨酸(分别为-ch3、-ch(ch3)2、-ch2ch(ch3)2、-ch(ch3)ch2ch3或-ch2c6h6的侧链),且
a3为瓜氨酸或天冬酰胺(分别为-(ch2)3nhconh2或
ꢀ‑
ch2conh2的侧链)。
[0162]
在一些实施方式中,a1为脯氨酸,a2及a4为苯丙氨酸,且a3为瓜氨酸 (fcitfpro)。在一些实施方式中,a1为脯氨酸,a2为苯丙氨酸,且a3为瓜氨酸,且a4为丙氨酸(acitfpro)。
[0163]
在一些实施方式中,四肽修饰剂具有以下表示的结构:
[0164][0165]
其中,
[0166]
r5包含靶向基团(m1)或空间位阻稳定剂(m2),
[0167]
r4为天然、非天然异构或合成疏水性氨基酸的侧链,
[0168]
r3为不带电亲水性氨基酸,优选瓜氨酸的侧链,
[0169]
r2为天然、非天然异构或合成疏水性氨基酸,优选苯丙氨酸的侧链,
[0170]
x及y为:a)分别(ch2)2(ch3)2及h(四肽a1为亮氨酸),b)分别ch
3-及ch
3-(四肽a1为n-甲基丙氨酸),或c)分别ch
2-及ch
2-ch
2-(四肽a1为脯氨酸);及r'为
[0171]
四肽修饰剂与多胺反应产生p-(l-m)。
[0172]
在一些实施方式中,r4为苯丙氨酸或丙氨酸的侧链。在一些实施方式中,r3为瓜氨酸的侧链。在一些实施方式中,r2为苯丙氨酸的侧链。
[0173]
在一些实施方式中,膜活性多胺经具有以下通式的二肽修饰剂(二肽
ꢀ‑
pabc-pnp修饰剂)修饰:
[0174]
r-a1a
2-氨基苯甲基-碳酸酯。
[0175]
其中r包含空间位阻稳定剂或靶向基团,a1为疏水性氨基酸,且a2为亲水性不带电氨基酸。修饰剂碳酸酯与聚合物胺反应产生氨基甲酸酯键。在一些实施方式中,氨基苯甲基(amidobenzyl)为对氨基苯甲基。在一些实施方式中,碳酸酯为活化的胺反应性碳酸酯。在一些实施方式中,二肽-pabc可裂解接头具有以下通式结构:
[0176][0177]
其中r4包含靶向基团或空间位阻稳定剂,r3包含胺反应性碳酸酯部分,例如对硝基苯基,r1为疏水性氨基酸的侧链,例如苯丙氨酸或丙氨酸,且r2为亲水性不带电氨基酸,例如瓜氨酸(cit)的侧链。在一些实施方式中,r1为苯丙氨酸或丙氨酸的侧链。在一些实施方式中,r2为瓜氨酸(cit)的侧链。
[0178]
在一些实施方式中,rgd修饰剂包含由以下表示的结构:
[0179][0180]
其中r
14
为如上述所定义的含胍基团,a'包含含peg的接头,r1为苯丙氨酸或丙氨酸的侧链,r2为瓜氨酸的侧链,且r3为胺反应性碳酸酯。
[0181]
递送聚合物可包括通过聚合物上的伯胺与双取代的烷基顺丁烯二酸酐的反应可逆修饰的多胺:
[0182]
其中r1包含靶向基团或空间位阻稳定剂。
[0183]
在一些实施方式中,双取代的烷基顺丁烯二酸酐具有由以下表示的结构:
[0184][0185]
其中r1包含靶向基团或空间位阻稳定剂。
[0186]
在一些实施方式中,靶向基团(例如rgd配体)经由例如peg接头的接头连接至修饰剂。peg接头可具有1-50个乙烯单元。
[0187]
rgd及peg修饰剂示于图1至7中。
[0188]
在一些实施方式中,描述由下式表示的组合:
[0189][0190]
其中:rnai触发剂为hif2αrnai触发剂,n为0.5-5,p为膜活性多胺,l
1-m1包含rgd-pega-fcitfpro-,a为1-50,x为1-20,l
2-m2包含pegb-acit-pabc-, b为4-30且y大于或等于0,且(m
2-l2)
y-p-(l
1-m1)
x
不具膜活性。在一些实施方式中,x y的值为p的伯胺的数量的大于80%、大于90%或大于95%。在一些实施方式中,n为0.5-2。在一些实施方式中,n为0.8-1.6。在一些实施方式中,x为2-20、 3-20、4-20、5-20、6-20、7-20、8-20、9-20、10-20、11-20、12-20、13-20、14-20 或15-20。在一些实施方式中,a的值大于b的值。
[0191]
医药组合物
[0192]
在一些实施方式中,使用所述hif2αrnai触发剂中的至少一种制备用于治疗会因
hif2α表达的降低或抑制而受益的对象的医药组合物(即药物)。这些医药组合物适用于抑制细胞、组织或生物体中的hif2α基因表达。在一些实施方式中,所述医药组合物用于治疗患有会因hif2α表达的降低或抑制而受益的疾病或病症的对象。
[0193]
如本文所用,医药组合物或药剂包含药理学上有效量的所述hif2αrnai触发剂或含hif2αrnai触发剂的偶联物中的至少一种及一种或多种医药学上可接受的赋形剂。医药学上可接受的赋形剂(赋形剂)为不为活性医药成分(api,治疗性产物,例如rnai触发剂)的物质,其已接受适当的安全评估且特意包括于药物递送系统中。赋形剂在预定剂量下不发挥或不意欲发挥治疗作用。赋形剂可用于a)在制造期间有助于药物递送系统的处理;b)保护、支持或增强api的稳定性、生物可用性或患者可接受性;c)有助于产物鉴别;和/或d)在储存或使用期间增强api递送的总体安全性、有效性的任何其他属性。医药学上可接受的赋形剂可为或可不为惰性物质。
[0194]
赋形剂包括(但不限于):吸收增强剂、抗黏剂、消泡剂、抗氧化剂、黏合剂、缓冲剂、载剂、涂布剂、颜料、递送增强剂、葡聚糖、右旋糖、稀释剂、崩解剂、乳化剂、增量剂、填充剂、调味剂、滑动剂、保湿剂、润滑剂、油状物、聚合物、防腐剂、生理盐水、盐、溶剂、糖类、悬浮剂、持续释放型基质、甜味剂、增稠剂、张力剂、载剂、驱水剂及湿润剂。
[0195]
医药组合物可含有通常见于医药组合物中的其他额外组分。此类额外组分包括(但不限于):止痒剂、收敛剂、局部麻醉剂或消炎剂(例如抗组胺剂、苯海拉明等)。还设想表达或包含本文所定义的rnai触发剂的细胞、组织或经分离器官可用作“医药组合物”。如本文所用,“药理学有效量”、“治疗有效量”或简单的“有效量”指产生预定药理学、治疗性或预防性结果的rnai触发剂的量。
[0196]
在一些实施方式中,所述hif2αrnai触发剂组合一种或多种额外治疗剂或疗法,包括(但不限于):第二hif2αrnai触发剂或其他rnai剂、小分子药物、抗体、抗体片段和/或疫苗。
[0197]
所述rnai触发剂及包含本文揭示的hif2αrnai触发剂的医药组合物可封装或包括于试剂盒、容器、包或分配器中。hif2αrnai触发剂及包含所述hif2αrnai 触发剂的医药组合物可封装于预填针筒或小瓶中。
[0198]
涵盖包括本文所述的hif2αrnai触发剂中的至少一种的细胞、组织及非人类生物体。通过本领域中可利用的任何方式将rnai触发剂递送至细胞、组织或非人类生物体来制得细胞、组织或非人类生物体。在一些实施方式中,细胞为哺乳动物细胞,包括(但不限于)人类细胞。细胞、组织或非人类生物体适用于研究或适用作研究工具(例如药物测试或诊断)。
[0199]
治疗方法
[0200]
在一些实施方式中,本文所述的hif2αrnai触发剂用于治疗患有会因hif2α表达的降低或抑制而受益的疾病或病症的对象。在一些实施方式中,所述hif2α rnai触发剂用以治疗或预防患有会因hif2α表达的降低或抑制而受益的疾病或病症的对象的至少一种症状。向该对象给予治疗有效量的所述rnai触发剂中的任何一种或多种,由此治疗该症状。
[0201]
在一些实施方式中,hif2αrnai触发剂用以治疗或处理临床表达,其中向需要此类治疗、预防或处理的对象给予治疗或预防有效量的本文所述的hif2αrnai 触发剂或含hif2αrnai触发剂的组合物中的一种或多种。在一些实施方式中,该方法包含将包含本文所述的
hif2αrnai触发剂分子的组合物给予待治疗的哺乳动物。
[0202]
因hif2α基因表达的降低和/或抑制而受益的代表性疾病包括(但不限于)癌症、肾癌、透明细胞肾细胞癌、非小细胞肺癌、星形细胞瘤(脑癌)、膀胱癌、乳癌、软骨肉瘤、结肠直肠癌、胃癌、神经胶母细胞瘤、头颈鳞状细胞癌、肝细胞癌、肺腺癌、神经母细胞瘤、黑素瘤、多发性骨髓瘤、卵巢癌、直肠癌、癌转移、齿龈炎、牛皮癣、卡波西氏肉瘤相关的疱疹病毒、子痫前症、炎症、慢性炎症、新生血管性疾病及类风湿性关节炎。
[0203]
在一些实施方式中,hif2αrnai触发剂可用以抑制hif2α于例如对象的细胞、细胞群或组织中的表达。在一些实施方式中,hif2αrnai触发剂可用以调配用于抑制hif2α于例如对象的细胞、细胞群或组织中的表达的组合物。在一些实施方式中,向对象给予治疗有效量的一类(或若干不同类型)的如本文所述的hif2αrnai 触发剂,由此抑制hif2α于对象中的表达(例如有效抑制hif2α于对象中的表达的量)。
[0204]
如本文所用,在提及hif2α基因时术语“沉默”、“降低”、“抑制”、“下调”或“敲减基因表达”表示当细胞、细胞群或组织经所述hif2αrnai触发剂处理时,与已或尚未如此处理的第二细胞、细胞群或组织相比或与相同细胞、细胞群或组织在给予hif2αrnai触发剂之前相比,如通过自基因中转录的rna的含量或转录hif2α基因的细胞、细胞群或组织中自mrna转译的多肽、蛋白或蛋白次单元的含量所测量,基因的表达降低。
[0205]
在一些实施方式中,相对于给予hif2αrnai触发剂前的对象或不接受hif2α rnai触发剂的对象,给予所述hif2αrnai触发剂的对象的基因表达量和/或hif2α的mrna含量降低至少约5%、10%、15%、20%、25%、30%、35%、40%、45%、 50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或98%。在对象的细胞、细胞群和/或组织中,对象的基因表达量和/或mrna含量可降低。在一些实施方式中,相对于给予hif2αrnai触发剂前的对象或不接受hif2αrnai触发剂的对象,给予所述hif2αrnai触发剂的对象的hif2α的蛋白含量降低至少约5%、10%、 15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、 80%、85%、90%、95%或98%。在对象的细胞、细胞群、组织、血液和/或其他体液中,对象的蛋白含量可降低。基因表达、mrna或蛋白质含量的降低可通过此项技术中已知的任何方法来评估。hif2αmrna含量和/或蛋白质含量的减少或降低在本文中统称为hif2α的减少或降低或抑制或减少hif2α表达。
[0206]
当提及rnai触发剂时,“引入细胞中”表示在功能上将rnai触发剂递送至细胞中。功能性递送表示将rnai触发剂递送至细胞中且具有预期的生物活性(例如基因表达的序列特异性抑制)。
[0207]
给药路径为通过使rnai触发剂与身体达成接触的路径。一般而言,给予药物及核酸以便治疗对象的方法在本领域中已熟知且可应用于本文所述的组合物给予。本文所述的化合物可经由任何适合的途径以特定途径适当定制的制剂给予。因此,本文所述的化合物可通过注射给予,例如静脉内、肌肉内、皮内、皮下或腹膜内注射。
[0208]
在一些实施方式中,本文所述的hif2αrnai触发剂分子或组合物可使用本领域中已知的寡核苷酸递送技术递送至细胞、细胞群、组织或对象中。一般而言,本领域中所认知的用于(体外或体内)递送核酸分子的任何适合方法可经调适以便联合本文中所述的hif2αrnai触发剂使用。举例而言,递送可通过以下实现:局部给予(例如直接注射、植入或表面给予)、全身给予或皮下、静脉内、经口、腹膜内或非经肠途径,包含颅内(例如室内、脑实质内
及鞘内)、肌肉内、经皮、气管(气雾剂)、经鼻、经直肠或表面(包含经颊及舌下)给予,在某些实施方式中,组合物通过皮下或静脉内输注或注射给予。
[0209]
上述所提供的实施方式及各项现利用以下非限制性实施例加以说明。
[0210]
实施例
[0211]
实施例1.rnai触发剂合成.
[0212]
a)合成.根据寡核苷酸合成中所用的固相氨基磷酸酯技术合成rnai触发剂分子。视规模而定,使用mermade96e(bioautomation公司)或 mermade12(bioautomation)。在由受控微孔玻璃(cpg,或获自primesynthesis公司,美国宾夕法尼亚州阿斯顿)制成的固体载体上进行合成。所有dna、2'-经修饰的rna及una氨基磷酸酯均购自thermo fisher scientific公司(美国威斯康辛州密尔沃基)。具体地,使用以下2'-o-甲基氨基磷酸酯:(5'-o-二甲氧基三苯甲基-n6-(苯甲酰基)-2'-o-甲基-腺苷-3'-o-(2-氰基乙基-n,n-二异丙基氨基)氨基磷酸酯、5'-o-二甲氧基-三苯甲基-n4-(乙酰基)-2'-o-甲基-胞苷-3'-o-(2-氰基乙基
ꢀ‑
n,n-二异丙基氨基)氨基磷酸酯、(5'-o-二甲氧基三苯甲基-n2-(异丁酰基)-2'-o-甲基-鸟苷-3'-o-(2-氰基-乙基-n,n-二异丙基氨基)氨基磷酸酯及5'-o-二甲氧基-三苯甲基-2'-o-甲基尿苷-3'-o-(2-氰基乙基-n,n-二异丙基氨基)氨基磷酸酯。2'-脱氧-2'-氟
‑ꢀ
氨基磷酸酯带有与2'-o-甲基rna氨基酸酯相同的保护基。使用以下una氨基磷酸酯:5'-(4,4'-二甲氧基三苯甲基)-n-苯甲酰基-2',3'-开环-腺苷、2'-苯甲酰基-3'-[(2
‑ꢀ
氰基乙基)-(n,n-二异丙基)]-氨基磷酸酯、5'-(4,4'-二甲氧基三苯甲基)-n-乙酰基
ꢀ‑
2',3'-开环-胞嘧啶、2'-苯甲酰基-3'-[(2-氰基乙基)-(n,n-二异丙基)]-氨基磷酸酯、 5'-(4,4'-二甲氧基三苯甲基)-n-异丁酰基-2',3'-开环-鸟苷、2'-苯甲酰基-3'-[(2-氰基乙基)-(n,n-二异丙基)]-氨基磷酸酯及5'-(4,4'-二甲氧基-三苯甲基)-2',3'-开环-尿苷、2'
‑ꢀ
苯甲酰基-3'-[(2-氰基乙基)-(n,n-二异丙基)]-氨基磷酸酯。将所有氨基酸酯溶解于无水乙腈(50mm)中且添加分子筛为将teg-胆固醇引入寡聚物的5'端,使用来自glen research公司(美国维吉尼亚州斯特灵)的1-二甲氧基三苯甲基氧基-3-o-(n
‑ꢀ
胆固醇基-3-氨基丙基)-三乙二醇-甘油基-2-o-(2-氰基乙基)-(n,n,-二异丙基)-氨基磷酸酯。引入5'-修饰,而非合成循环中的任何修饰。使用5-苯甲硫基-1h-四唑(btt, 250mm乙腈溶液)作为活化剂溶液。偶合时间为10分钟(rna)、180秒(胆固醇)、 90秒(2'ome及una)及60秒(2'f及dna)。为引入硫代磷酸酯键,使用100mm 3
‑ꢀ
苯基1,2,4-二噻唑啉-5-酮(pos,获自polyorg公司,美国马萨诸塞州莱姆斯特) 于无水乙腈中的溶液。参见表1至2及5中的特定序列。
[0213]
b.载体所结合的寡聚物的裂解及去保护.完成固相合成之后,在30℃用40wt%甲胺水溶液与28%氢氧化铵溶液(aldrich公司)的1:1体积溶液处理干燥的固体载体两小时。将溶液蒸发且固体残余物于水中重建(参见下文)。
[0214]
c.纯化.使用waters xbridge beh300 c4 5u制备型管柱及shimadzu lc-8系统,通过逆相hplc纯化含有粗胆固醇的寡聚物。缓冲液a为100mm teaa、ph 7.5 且含有5%乙腈且缓冲液b为100mm teaa且含有95%乙腈。记录260nm的uv 痕量。接着使适当馏分在尺寸排阻型hplc上流动,其使用装填有sephadex g25 介质的ge healthcare xk 16/40管柱,使用100mm碳酸氢铵(ph 6.7)及20%乙腈的操作缓冲液。使用tksgel superq-5pw 13u管柱及
shimadzu lc-8系统,通过阴离子交换hplc纯化其他粗寡聚物。缓冲液a为20mm tris、5mm edta ph 9.0且含有20%乙腈,且缓冲液b在添加1.5m氯化钠的情况下与缓冲液a相同。记录 260nm的uv痕量。合并适当馏分,接着在尺寸排阻型hplc上流动,如针对含有寡聚物的胆固醇所述。
[0215]
d.退火.通过将等摩尔浓度溶液(正义链及反义链)合并于0.2
×
pbs(磷酸盐缓冲盐水,1
×
,corning,cellgro)中来使互补链混合以形成rnai触发剂。将此溶液置放于70℃热混合器中,加热至95℃,在95℃保持5分钟且缓慢冷却至室温。将一些rnai触发剂冻干且储存于-15℃至-25℃。通过uv-vis光谱仪测量0.2
×
pbs 中的溶液吸光度来测定双链浓度。接着使260nm溶液吸光度乘以变换因子及稀释因子以确定双链浓度。除非另外说明,否则所有变换因子为0.037mg/(ml cm)。在一些实验中,变换因子从实验确定的消光系数计算。
[0216]
实施例2.合成apn 1170-100a(100a)、apn 1203-006(006)、apn 1203-064(064) 两性膜活性多胺.
[0217][0218]
a.材料.2,2'-偶氮二(2,4-二甲基戊腈)(v-65,自由基触发剂)购自wako pure化学工厂。丙烯酸丙酯购自polysciences公司。n-boc-乙氧基-乙胺丙烯酸酯获自 wuxi公司。2-(十二烷硫基-碳硫酰基硫基)-2-甲基丙酸(ddmat,raft剂)、1,1'
‑ꢀ
偶氮二-(环己烷甲腈)(achn)、1-乙基哌啶次磷酸酯(ephp)、五氟苯酚、n,n'-二环己基碳化二亚胺及n,n-二异丙基-乙胺购自sigma aldrich公司。o-(2-氨基乙基)-o'-(2-叠氮基乙基)三乙二醇(叠氮基-peg4-胺)购自biomatrik公司。
[0219]
b.n-boc-乙氧基乙胺丙烯酸酯与丙烯酸丙酯(eap)的raft共聚物.制备乙酸丁酯中的v-65(2mg/ml)及raft剂ddmat(10mg/ml)非人溶液。单体摩尔浓度的进料为52%n-boc-乙氧基乙胺丙烯酸酯、48%丙烯酸丙酯。理论mw为75,000。 raft剂(ddmat)与触发剂(v-65)的摩尔比为6.67:1。
[0220]
将n-boc-乙氧基乙胺丙烯酸酯(1.778g,6.86mmol)、丙烯酸丙酯(0.794ml, 0.722g,6.33mmol)、ddmat溶液(1.215ml,0.0333mmol)、v-65溶液(0.621ml, 0.005mmol)及乙酸丁酯(10.2ml)添加至具有搅拌棒的20ml玻璃瓶中。小瓶用含垫片盖密封且使用长针、用氮气对溶液进行鼓泡1小时,其中以第二针作为出口。移除针且在搅拌下将小瓶加热至50℃维持24h。使溶液冷却至室温且等量转移至两个 50ml离心管中,之后向两个管中添加己烷(35ml)。以4400rpm将溶液离心2分钟。小心倾析上清层且用己烷冲洗底层。接着将各管的底层再溶解于二氯甲烷(7ml)中,于己烷(40ml)中沉淀且再次离心。倾析上清层且用己烷冲洗底层,之后将各层合并至一个50ml离心管中,且减压干燥聚合物数小时。粗eap共聚物的产量为2.1g。对共聚物样品实施多角度光散射(mals)及1h-nmr。
[0221]
聚合物006:通过1h-nmr确定的组成为55%n-boc-乙氧基乙胺丙烯酸酯及 45%丙烯酸丙酯。通过mals确定的006的mw为58,600g/mol,多分散指数(pdi) 为1.04。
[0222]
聚合物100a:通过1h-nmr得到的组成:56%n-boc-乙氧基乙胺丙烯酸酯及 44%丙
烯酸丙酯。通过mals得到的mw:65,150,pdi为1.122。
[0223]
聚合物064:通过1h-nmr得到的组成:54%n-boc-乙氧基乙胺丙烯酸酯及 46%丙烯酸丙酯。通过mals确定的064的mw为57,957g/mol,多分散指数(pdi) 为1.07。
[0224]
c.自由基诱导的ω端基移除(聚合物006及064).制备甲苯中的1,1'-偶氮二-(环己烷甲腈)(achn,20mg/ml)及1-乙基哌啶次磷酸酯(ephp,100mg/ml)的溶液。将eap(2g,0.035mmol)、achn(0.213ml,0.5当量,0.0174mmol)、ephp(1.25ml, 20当量,0.697mmol)及甲苯(25.2ml)添加至具有搅拌棒的40ml玻璃瓶中。小瓶用含垫片盖密封且使用长针、用氮气对溶液进行鼓泡1小时,其中以第二针作为出口。移除针且将小瓶加热至100℃维持2h。使溶液冷却至室温且通过旋转蒸发移除约 20ml甲苯。将剩余溶液转移至50ml离心机小瓶中,且添加己烷(35ml)。以4400rpm 将溶液离心2分钟。小心倾析上清层且用己烷冲洗底层。接着将底层再溶解于二氯甲烷(7ml)中,于己烷(40ml)中沉淀且再次离心。倾析上清层且用己烷冲洗底层,之后将聚合物减压干燥约1h。将聚合物溶解于甲基叔丁基醚(80ml)中且转移至分液漏斗中。接着用3
×
30ml体积的h2o,之后通过3
×
30ml体积的饱和nacl洗涤溶液。接着聚合物溶液经硫酸钠干燥,且经由0.45μm ghp过滤器真空过滤。经由旋转及高真空蒸发移除mtbe。使用uv分光亮度计监测样品的端基移除。端基移除经计算为99%。对样品实施mals、gc-fid及1h-nmr。通过1h-nmr得到的006的组成为55%n-boc-乙氧基乙胺丙烯酸酯及45%丙烯酸丙酯。通过gc-fid确定006的转化为n-boc-乙氧基乙胺丙烯酸酯为81.4%且丙烯酸丙酯为 77.3%。通过gc-fid转化确定的100a的转化为n-boc-乙氧基乙胺丙烯酸酯为87%且丙烯酸丙酯为83%。通过mals确定的聚合物006的mw为57,700g/mol,多分散指数(pdi)为1.06。
[0225]
d.α-端基的五氟苯酚活化.将eap聚合物(2g,0.0347mmol)、五氟苯酚(63.8mg, 0.3466mmol)、n,n'-二环己基碳化二亚胺(71.5mg,0.3466mmol)及二氯甲烷(40ml) 添加至具有搅拌棒的100ml圆底烧瓶中。用橡胶隔膜塞住烧瓶且用氮气吹扫系统 15分钟。在室温下搅拌溶液16h。再添加五氟苯酚(63.8mg,0.3466mmol)及n,n'
‑ꢀ
二环己基碳化二亚胺(71.5mg,0.3466mmol),烧瓶用橡胶隔膜塞住,且用氮气吹扫系统15分钟。在室温下搅拌所得溶液3h。用己烷(约10倍体积)使聚合物沉淀,离心且倾析溶剂。将聚合物溶解于最小二氯甲烷中,用己烷(约10倍体积)沉淀,离心且倾析溶剂。将聚合物溶解于最小乙酸乙酯中,用己烷(约10倍体积)沉淀,离心且倾析溶剂。高真空干燥聚合物沉淀直至固体达到恒重。
[0226]
e.α端基的叠氮官能化.在配备有橡胶隔膜及搅拌棒的100ml圆底烧瓶中,将来自先前步骤的聚合物(1.9g,0.0329mmol)溶解于二氯甲烷(38ml)中。在搅拌下将叠氮基-peg4-胺(86.4mg,0.3293mmol)及n,n-二异丙基乙胺(46.8mg,63.1μl, 0.3622mmol)添加至烧瓶中。用氮气吹扫系统15分钟,且在室温下搅拌反应物隔夜。再将叠氮基peg4胺(86.4mg,0.3293mmol)及n,n-二异丙基乙胺(46.8mg,63.1μ l,0.3622mmol)添加至烧瓶中,用n2气体吹扫系统,且在室温下搅拌反应物3h。用己烷(约10倍体积)使聚合物沉淀,离心且倾析溶剂。将聚合物溶解于最小二氯甲烷中,用己烷(约10倍体积)沉淀,离心且倾析溶剂。高真空干燥聚合物沉淀直至固体达到恒重。叠氮官能化eap的产量为1.77g。对共聚物样品实施多角度光散射(mals)及1h-nmr。
[0227]
聚合物006:通过1h-nmr确定的组成为56%n-boc-乙氧基乙胺丙烯酸酯及 44%丙烯酸丙酯。通过mals确定的mw为60,330g/mol,多分散指数(pdi)为1.05。
[0228]
聚合物100a:通过1h-nmr得到的组成为56%n-boc-乙氧基乙胺丙烯酸酯及44%丙烯酸丙酯。通过mals确定的mw:64,430,pdi为1.217。
[0229]
聚合物064:通过1h-nmr得到的组成为54%n-boc-乙氧基乙胺丙烯酸酯及 46%丙烯酸丙酯。通过mals确定的mw:65,170,pdi为1.05。
[0230]
单叠氮化物:术语“单叠氮化物”或“单叠氮化物聚合物”指示进行上述程序的步骤d及e且将叠氮基团偶合成聚合物的α端基。
[0231]
f.去boc保护及切向流过滤.在100ml圆底烧瓶中,将2m hcl的乙酸溶液 (28ml)添加至叠氮官能化的eap共聚物(1.67g,0.0277mmol)中。在室温下搅拌反应物1h。添加去离子h2o(56ml)且搅拌10分钟。接着溶液立即使用配备有切向流过滤系统(krosflo research)的mpes 30kd 115cm2过滤器模块用10当量体积的 5mm磷酸盐-柠檬酸盐缓冲液(ph 5)交换。接着使用设备浓缩溶液,得到55ml最终体积。记录5.1的ph值。通过顶空气相层析法对样品进行浓度确定。将等分试样冻干且接着用浓度为10mg/ml的含33.3%乙腈-d的氧化氘重建以进行1h-nmr 分析。对于006及100a,理论mw分别计算为43,026g/mol、45,765g/mol。
[0232]
g.使用类似技术,可容易形成类似两性膜活性多胺。具体地,两性膜活性多胺的分子量(mw)为40-120k(经保护)(25k至85k(去保护)),pdi范围为1.03至1.2,且单体比率为35%胺单体/65%疏水性基团单体至70%胺单体/30%疏水性基团单体。
[0233]
实施例3.合成apn 1095-126(126).
[0234][0235]
与用于合成100a及006的三硫代碳酸酯部分raft剂及v-65raft触发剂相比,apn 1095-126的合成使用二硫代苯甲酸酯部分raft剂及aibn raft触发剂。用于此聚合反应的条件需要不同加热温度及时间。另外,此聚合物需要部分沉淀。聚合物未封端,但叠氮化物添加方法与100a及006相同。
[0236]
a.材料.丙烯酸丙酯购自polysciences公司。n-boc-乙氧基乙胺丙烯酸酯获自 wuxi公司。4-氰基-4-(苯基硫代甲酰硫基)戊酸(cpcpa,raft剂)、2,2'-偶氮二(2
‑ꢀ
甲基丙腈)(aibn,自由基触发剂)、五氟苯酚、n,n'-二环己基碳化二亚胺及n,n
‑ꢀ
二异丙基乙胺购自sigma aldrich公司。o-(2-氨基乙基)-o'-(2-叠氮基乙基)三乙二醇 (叠氮基-peg4-胺)购自biomatrik公司。
[0237]
b.n-boc-乙氧基乙胺丙烯酸酯与丙烯酸丙酯(eap)的raft共聚物.重复以下程序8次以产生总计4.5513g分离的eap共聚物。制备aibn(1.035mg/ml)及raft 剂cpcpa(50.54mg/ml)于乙酸丁酯中的溶液。单体摩尔浓度的进料为52%n-boc
‑ꢀ
乙氧基乙胺丙烯酸酯、48%丙烯酸丙酯。理论mw为75,000。raft剂(cpcpa)与触发剂(aibn)的摩尔比为6.67:1。
[0238]
将n-boc-乙氧基乙胺丙烯酸酯(1.7879g,6.9mmol)、丙烯酸丙酯(0.774ml,0.7121g,6.24mmol)、cpcpa溶液(0.184ml,0.0333mmol)、aibn溶液(0.793ml, 0.005mmol)及乙酸丁酯(11.02ml)添加至具有搅拌棒的20ml玻璃瓶中。小瓶用含垫片盖密封且使用长针、用氮气对溶液进行鼓泡1小时,其中以第二针作为出口。移除针且且在搅拌下将小瓶加热至50℃维持24h。使溶液冷却至室温且转移至 50ml离心管中,之后添加己烷(35ml)。以
4400rpm将溶液离心2分钟。小心倾析上清层且用己烷冲洗底层。接着将各管的底层再溶解于二氯甲烷(7ml)中,于己烷 (40ml)中沉淀且再次离心。倾析上清层且用己烷冲洗底层,的后将聚合物减压干燥数小时。粗eap共聚物的产量为1.734g。对粗共聚物样品实施多角度光散射 (mals)及1h-nmr。将经干燥的粗共聚物溶解于dcm(100mg/ml)中。添加己烷,直至刚好达到浊点的后。将所得乳白色溶液离心。萃取底层且完全沉淀至己烷中。将馏分离心,其后分离出共聚物,且真空干燥。分离的eap共聚物馏分的产率为 0.602g。对分离的共聚物的样品进行1h-nmr及mals。通过1h-nmr确定的组成为56%n-boc-乙氧基乙胺丙烯酸酯及44%丙烯酸丙酯。通过mals确定的mw 为62,010g/mol,多分散指数(pdi)为1.14。
[0239]
c.α-端基的五氟苯酚活化.将eap聚合物(2g,0.0347mmol)、五氟苯酚(63.8mg, 0.3466mmol)、n,n'-二环己基碳化二亚胺(71.5mg,0.3466mmol)及二氯甲烷(40ml) 添加至具有搅拌棒的100ml圆底烧瓶中。用橡胶隔膜塞住烧瓶且用氮气吹扫系统 15分钟。在室温下搅拌所得溶液16h。再添加五氟苯酚(63.8mg,0.3466mmol)及 n,n'-二环己基碳化二亚胺(71.5mg,0.3466mmol),烧瓶用橡胶隔膜塞住,且用氮气吹扫系统15分钟。在室温下搅拌所得溶液3h。用己烷(约10倍体积)使聚合物沉淀,离心且倾析溶剂。将聚合物溶解于最小二氯甲烷中,用己烷(约10倍体积)沉淀,离心且倾析溶剂。将聚合物溶解于最小乙酸乙酯中,用己烷(约10倍体积)沉淀,离心且倾析溶剂。高真空干燥聚合物沉淀直至固体达到恒重。
[0240]
d.α端基的叠氮官能化.在配备有橡胶隔膜及搅拌棒的100ml圆底烧瓶中,将来自先前步骤的聚合物(1.9g,0.0329mmol)溶解于二氯甲烷(38ml)中。在搅拌下将叠氮基-peg4-胺(86.4mg,0.3293mmol)及n,n-二异丙基乙胺(46.8mg,63.1μl, 0.3622mmol)添加至烧瓶中。用氮气吹扫系统15分钟,且在室温下搅拌反应物隔夜。再将叠氮基peg4胺(86.4mg,0.3293mmol)及n,n-二异丙基乙胺(46.8mg,63.1μl, 0.3622mmol)添加至烧瓶中,用n2气体吹扫系统,且在室温下搅拌反应物3h。用己烷(约10倍体积)使聚合物沉淀,离心且倾析溶剂。将聚合物溶解于最小二氯甲烷中,用己烷(约10倍体积)沉淀,离心且倾析溶剂。高真空干燥聚合物沉淀直至固体达到恒重。叠氮官能化eap的产量为1.77g。对共聚物样品实施多角度光散射 (mals)及1h-nmr。通过1h-nmr确定的组成为56%n-boc-乙氧基乙胺丙烯酸酯及44%丙烯酸丙酯。通过mals确定的mw为66,670g/mol,多分散指数(pdi)为 1.11。
[0241]
e.去boc保护及切向流过滤.在100ml圆底烧瓶中,将2m hcl的乙酸溶液 (28ml)添加至叠氮官能化eap共聚物(1.67g,0.0277mmol)中。在室温下搅拌反应物1小时。添加去离子h2o(56ml)且搅拌10分钟。接着溶液立即使用配备有切向流过滤系统(krosflo research)的mpes 30kd 115cm2过滤器模块用10当量体积的 5mm磷酸盐-柠檬酸盐缓冲液(ph 5)交换。接着使用设备浓缩溶液,得到55ml最终体积。记录5.1的ph值。通过顶空气相层析法对样品进行浓度确定。将等分试样冻干且接着用浓度为10mg/ml的含33.3%乙腈-d的氧化氘重建以进行1h-nmr 分析。理论mw计算为43,026g/mol。
[0242]
实施例4.聚合物分析.
[0243]
(i)mals分析.将约10mg共聚物溶解于0.5ml 75%二氯甲烷、20%四氢呋喃及5%乙腈中。使用jordi 5μm 7.8
×
300混合床层ls dvb管柱,使用连接至 shimadzu prominence hplc的wyatt heleos ii多角度光散射检测器测量分子量及多分散性(pdi)。脱出保护基前的分子量(聚合物006):60,330(pdi 1.05)。
[0244]
(ii)通过气相层析法得到单体转化.在混合(预先n2鼓泡)之后、在n2鼓泡之后且
在反应完成之后获得大致40μl共聚物溶液(b部分)。将样品100倍稀释至乙酸乙酯中。用配备有火焰电离检测器的shimadzu gc-2010plus使用phenomenexzebron毛细管柱(zb-5,30m,0.25mm id,0.5μm薄膜厚度)分析样品。使用预先 n2鼓泡的样品作为单一点校准,单体转化由比较反应后单体浓度与反应前/n2鼓泡后单体浓度来测量。
[0245]
(iii)使用顶空气相层析法(hs-gc)通过丙醇含量得到聚合物浓度.使用1-丁醇作为内标物将去保护的聚合物溶液(约20mg/ml)50倍稀释至3m naoh中。将反应管密封且振荡1h。接着在室温下培育反应物至少6h。在10ml顶空小瓶中,将水解测试制品(250μl)添加至饱和nacl(500μl)及hcl(4m,250μl)中且将系统密封。使用具有hs-20顶空取样器的shimadzu gc-2010plus使用phenomenex zb-waxplus gc管柱(30.0m,0.25mm id,0.25μm薄膜厚度)分析测试物品。接着使用外部标准曲线或含有相同nacl/hcl/naoh基质的丙醇定量丙醇浓度。接着通过丙醇浓度除以如通过单体合并所确定的每聚合物中丙醇的量计算聚合物浓度。
[0246]
(iv)使用uv光谱分析进行叠氮化物定量.用60mm mes,ph 6将去保护的聚合物溶液(约20mg/ml)稀释至约5mg/ml。接着在室温下使聚合物与dbco-胺(2.5摩尔当量)反应至少6h。计算310nm下的吸光度差且确定每聚合物中叠氮化物的含量。
[0247]
实施例5.切向流过滤及偶联物分析.在偶联物形成之后,即通过添加rgd及 peg修饰剂修饰聚合物及连接rnai触发剂(参见以下实施例9),偶联物溶液 (2mg/ml,10ml)用10当量体积的10mm磷酸盐-柠檬酸盐缓冲液(ph 5)使用配备有切向流过滤系统(krosflo research)的mpes 30kd 20cm2过滤器模块交换。记录 5.1的ph值。
[0248]
a.偶联物表征及分析.
[0249]
(i)在整个结合中的聚合物浓度.在偶联物的整个组合中使用与g(iii)部分相同的方法以监测聚合物浓度。
[0250]
(ii)通过hplc逆相层析进行杂质定量.用h2o将聚合物偶联物(在tff纯化之后)稀释至1mg/ml且注射于具有spd-20a uv检测器及waters xbridge c18 5μ m4.6
×
250mm管柱的shimadzu prominence hplc上。该方法使用由h2o/乙腈/0.1%甲酸组成的二元梯度,其中检测设定为247nm。使用外部标准物定量计算 peg
n-acit-paboh、rgd-peg
n-fcfp-cooh及pnp的浓度。
[0251]
(iii)经由氨基酸分析的rgd-peg
n-fcitfp-tfp及peg
n-acit-pabc-pnp修饰. 在110℃下于密封的水解管中于hcl(6m)中将正缬氨酸(norvaline)作为内标物的聚合物偶联物(在tff纯化之后)水解16h。接着用naoh中和水解溶液,用硼酸盐缓冲液(ph 10.1)稀释,且用苯二甲醛/3-巯基丙酸衍生。接着将样品注射于具有 sil-30a自动取样器、spd-20a光二极管数组检测器及waters xbridge c18 5μm 4.6
×
250mm管柱的shimadzu nexera hplc系统上。样品使用10mm四硼酸钠十水合物/10mm二元磷酸钠/5mm叠氮化钠及45%甲醇/45%乙腈/10%h2o二元梯度溶离。uv检测设定为338nm。使用外部标准曲线计算丙氨酸及苯丙氨酸浓度。使用丙氨酸及苯丙氨酸浓度以及聚合物浓度及单体并入计算总氨基修饰以及两种配体之间的比率。
[0252]
(iv)通过尺寸排阻层析得到的rna触发剂定量及偶联物纯度.组合配备有 spd-20a uv检测器的shimadzu prominence hplc及acclaim sec-300 4.6mm
×
300mm,5μm,尺寸排阻管柱(串联中的第1个)连接acclaim sec-1000 4.6mm
ꢀ×
300mm,7μm,
(串联中的第2个)尺寸排阻管柱。所用方法等度,其中 200mm nabr、10mm tris ph 8、1mm edta及20%乙腈作为移动相且在260nm下检测。将聚合物偶联物的样品(在rna触发剂添加之后)稀释至移动相中且注射于系统上。偶联物的另一样品采用相同稀释流程,但用200mm二硫苏糖醇处理2h,之后注射于系统上。两种样品的rna触发剂浓度使用外部标准曲线计算。结合 rna触发剂的量通过自未处理rna含量减去dtt处理的rna含量来计算。偶联物的tff后纯度还使用此方法来确定。
[0253]
实施例6.rgd配体(rgd模拟物).
[0254][0255]
a.rgd模拟物编号1-peg
n-hynic,mw 1272。
[0256][0257]
n=4-24(优选为8-12)
[0258]
b.rgd模拟物编号1a-hynic,mw 802.8。
[0259][0260]
c.rgd模拟物编号1b-hynic,mw 830.9(rgd)。
[0261][0262]
实施例7.rgd及peg修饰剂
[0263]
a.二肽rgd-二肽及peg-二肽修饰剂如us-2012-0172412-a1(wo2012/092373)及us 2015-0045573 a1(wo 2015/021092)中所述制备(其两者以引用的方式并入本文中)。图3-7。
[0264]
b.rgd-peg
n-fcitfp-tfp及peg
n-fcitfp-tfp修饰剂合成.修饰剂前体 (di-boc)rgd(otbu)-apba-peg
n-fcitfpro-cooh使用通用fmoc化学物质固相合成法,使用预装载fmoc-proline-oh的2-cl-trt树脂来制备。向树脂-pro-fmoc中依序添加(在各步骤去fmoc保护之后):fmoc-phe-oh、fmoc-cit-oh、fmoc-phe-oh、 fmoc-nh-peg
n-cooh、4-(n-fmoc-对氨基苯氧基)-丁酸(apba)、 fmoc-asp(otbu)-oh、fmoc-gly-oh及diboc-间胍基苯甲酸。
[0265]
将(diboc)rgd(otbu)-apba-peg
n-fcitfpro-cooh(458mg,0.200mmol)及 tfp(66.5mg,0.400mmol)溶解于无水dcm(5.0ml)中且于冰/水浴槽中冷却至0℃,同时在氩气下搅拌。添加edc(77mg,0.400mmol)且在0℃下于冰/水浴槽中搅拌反应混合物30分钟。通过tlc(8.5:1.5chcl3:meoh)监测反应进展且在90分钟之后完成,通过tlc观察到无起始物质。用dcm将反应混合物稀释至100ml总体积,用di h2o(ph=5)洗涤3
×
40ml,且用1
×
40ml饱和nacl水溶液洗涤。有机物接着经na2so4干燥且经旋转蒸发器浓缩以产生448mg(产率92%)褐色/橙色泡沫。结构通过1h nmr及esi ms确定(反应如上针对peg20所示(n=20))。
[0266][0267]
(双boc)rgd(otbu)-apba-peg
n-fcitfpro-tfp
[0268]
(针对n=20所示)
[0269]
将(双boc)rgd(otbu)-peg
n-fcitfpro-tfp(497mg,0.204mmol)溶解于[9.25: 0.75:0.50]tfa:h2o:苯硫基甲烷(5.0ml)中且在室温下于封闭烧瓶中搅拌45分钟。反应完成通过ms(esi,阴性扫描,300-3000)确定,未观察到与起始物质有关的物质或部分去保护的中间物。接着使反应混合物沉淀于45ml乙醚中,短暂离心,倾出上清层且2
×
10ml乙醚洗涤且高真空干燥隔夜。最终产物经制备型hplc使用thermo aquasil c18 5um半制备型管柱纯化,其中移动相为含0.1%tfa的h2o 及acn。各注射为溶解于3.0ml含0.1%tfa的[61:39]h2o:acn中的50mg粗物质,经(以b%指示)39-(5)-39-(35)-43-(5)-95-(10)-95-(2)-39-(5)-39的梯度操作。各注射样品在注射15分钟内制备(溶解),且将阳性馏分汇集于一个烧瓶中且于冷冻器中保持冷却直至最后注射日结束。阳性馏分接着经旋转蒸发器在32℃的浴温下浓缩至干燥,接着用acn/甲苯追踪2次,接着用acn 3次,且接着经高真空干燥隔夜。自257mg注射的粗物质中,分离180mg(70%)纯物质(反应如上针对peg20 所示(n=20))。
[0270][0271]
rgd-peg
n-fcitfpro-tfp
[0272]
(针对n=20所示)
[0273]
4-(n-fmoc-对氨基苯氧基)-丁酸1合成.使对硝基酚(2)(7.5g,53.9mmole)与4
‑ꢀ
溴丁酸乙酯(8.45ml,59mmol)及k2co3(7.5g,54mmole)于dmf(75ml)中组合。在 100℃下搅拌混合物2h。移除dmf且用2n naoh及甲醇的3:1混合物稀释粗产物且在室温下搅拌4h。反应混合物用6m hcl酸化。收集白色沉淀以产生4-(对硝基苯氧基)-丁酸3:(10.9g,产率90%)。
[0274]
将4-(对硝基苯氧基)-丁酸3(37.1g,165mmol)溶解于meoh(1l)中且添加甲酸铵(35g,555mmole)及10%pd/c(德固赛型)(3.5g)。在65℃下使混合物回流隔夜。用硅藻土过滤反应物,以产生淡红棕色固体,产物4-(对氨基苯氧基)-丁酸4(30.5g,产率95%)。
[0275]
将4-(对氨基苯氧基)-丁酸4(5.1g,26mmol)溶解于饱和nahco3水性(3.36g, 40mmol)于h2o(450ml)及thf(300ml)中的6:4混合物中,得到白色浆液。添加 fmoc-osu(8.82g,26.1mmol)且搅拌反应物4h。移除丙酮,将反应物酸化(hcl),且收集灰白色沉淀且用1n hcl湿磨以产生9.6g产物4-(n-fmoc-对氨基苯氧基)-丁酸 1(产率88%)。
[0276][0277]
根据riches ag等人,tetrahedron(2012)68,第9448-9455页合成双boc-间胍基-苯甲酸5。
[0278]
peg
n-fcitfp修饰剂使用类似化学方法制得。图1-2。
[0279]
实施例8.四肽键.
[0280]
a.四肽合成.所有四肽以相同方式使用标准固相fmoc程序合成。一些肽由含有脯氨酸、亮氨酸或丙氨酸的市售2-cl-trt树脂(emd millipore公司,马萨诸塞州比勒利卡)合成。对于其他肽,通过将含有氨基酸或peg(1当量)及diea(2当量) 的dmf的溶液添加至2-cl-trt树脂中维持16h而使2-cl-trt树脂负载有 fmoc-peg
n-co2h或fmoc-n-甲基-ala-co2h。完成后,树脂用meoh覆盖。逐步添加pybop(4当量)、氨基酸(4当量)及diea(8当量)以进行偶合且逐步添加含20%哌啶的dmf以去除fmoc保护基。
[0281]
肽合成之后,使四肽与2当量n-羟基丁二酰亚胺(nhs)活化的酯,经保护n
‑ꢀ
乙酰基-半乳糖胺、nag(oac)3(rozema db等人,“protease-triggered sirna deliveryvehicles.”j control release.2015第209:57-66卷及美国专利8802773)或pegn于含有4当量diea的dmf中反应。在nag(oac)3或peg连接之后,使用于dcm 中的hfip(30%)自树脂移除肽维持0.5h。在溶剂移除之后,用et2o湿磨残余物。
[0282]
四肽经纯化且偶联至活化酯以形成修饰剂或未经纯化即偶联至发色团n-(对硝基
苯基))乙二胺(pna)以形成用于生理不稳定测试的底物。在纯化之前,含有 nag(oac)3的底物通过用于水(45%)及meoh(20%)中的tea(35%)处理去乙酰化且在室温下搅拌。对于纯化,四肽底物通过hplc使用thermo scientific aquasil c18 逆相管柱(250
×
21.2,马萨诸塞州沃尔瑟姆)用经0.1%甲酸缓冲的乙腈及水的梯度溶离来分离。在纯化之后,将底物冻干。
[0283]
胺反应性基团连接至四肽.在0℃下,将1当量hplc纯化的肽以及于dmf 或dcm中的n端nag(r5=nag(oh)3或peg(r5=pegn)添加至火焰干燥的烧瓶,得到0.2m浓度的肽。添加nhs(3当量)及n,n'-二环己基碳化二亚胺(dcc)(3当量) 且在室温下在氩气下搅拌隔夜,产生修饰剂。混合物经部分浓缩,冷却至-20℃且过滤。接着真空移除所有溶剂。将残余物溶解于最少的dcm及meoh中,沉淀于冷et2o中且通过在离心之后倾析溶剂来收集。重复沉淀于et2o中,直至不可检测到残余dcu(二环已基脲)。所有制备的化合物随后未经进一步纯化即使用。
[0284]
实施例9.聚合物修饰.使用rgd-peg-hynic、rgd-peg-acit-pnp或 rdg-peg-fcitfp-tfp及peg-二肽修饰剂形成sirna递送偶联物。
[0285]
1)方案1.在室温下,使指示聚合物与smpt以1:0.015(聚合物:smpt)的重量比于5mm hepes ph 8.0缓冲液反应1h。接着使经smpt修饰的聚合物与醛
ꢀ‑
peg-二肽修饰剂(醛-peg12-fcit或醛-peg24-acit)以所需比率在室温下反应1h。接着在室温下使经修饰的聚合物与peg12-二肽修饰剂(peg12-fcit、peg12-acit 或peg24-acit)以1:2(聚合物:peg)的重量比于100mm hepes ph 9.0缓冲液中反应1h。接着在室温下使经修饰的聚合物与sata-rnai触发剂以1:0.2(聚合物: sata-rnai触发剂)的重量比于100mm hepes ph 9.0缓冲液中反应隔夜以使 rnai触发剂连接。接下来,在室温下,使经修饰的聚合物与蛋白酶可裂解 peg(peg12-fcit或peg12-acit或peg24-acit)以1:6(聚合物:peg)的重量比于 100mm hepes ph 9.0缓冲液中反应1h。使用sephadex g-50旋转管柱纯化所得偶联物。
[0286]
rgd-hynic(实施例6b)通过在室温下与经修饰的聚合物以1:0.7(聚合物: rgd-hynic模拟物)的重量比于50mm mes ph 5.0缓冲液中反应最少4h来连接至经修饰的聚合物以形成完整递送偶联物。使用sephadex g-50旋转管柱纯化偶联物。 rgd配体连接效率如上所述确定。
[0287]
2)方案2.在室温下,使指示聚合物与smpt以1:0.015(聚合物:smpt)的重量比于5mm hepes ph 8.0缓冲液反应1h。接着在室温下使经smpt修饰的聚合物与醛-peg-二肽修饰剂(醛-peg24-acit)以1:0.5(聚合物:peg)的重量比且与peg
‑ꢀ
二肽修饰剂(peg12-fcit、peg12-acit或peg24-acit)以1:2(聚合物:peg)的重量比于100mm hepes ph 9.0缓冲液中反应1h。接着在室温下使经修饰的聚合物与sata-rnai触发剂以1:0.2(聚合物:sata-rnai触发剂)的重量比于100mmhepes ph 9.0缓冲液中反应隔夜以使rnai触发剂连接。接下来,在室温下,使经修饰的聚合物与蛋白酶可裂解-peg(peg12-fcit或peg12-acit或peg24-acit) 以1:6(聚合物:peg)的重量比于100mm hepes ph 9.0缓冲液中反应1h。 rgd-hynic(实施例6)通过在室温下与经修饰的聚合物以1:0.7(聚合物: rgd-hynic)的重量比于69mm氯化氢溶液(hcl)中反应隔夜连接至经修饰的聚合物以形成完全偶联物。rgd配体连接效率如上所述确定。
[0288]
3)方案3.在室温下,使指示聚合物与smpt以1:0.015(聚合物:smpt)的重量比于
tfp)以1:1(聚合物:rgd)的重量比于50mm hepes ph 8.5 缓冲液中反应2h。接着在室温下使经修饰的聚合物与蛋白酶可裂解-peg剂 (peg12-acit-pabc-pnp)以1:8(聚合物:peg)的重量比于50mm hepes ph 8.5 缓冲液中反应2h。接着对经修饰的聚合物进行tff纯化。在37℃下以1:0.4(聚合物:炔烃-rnai触发剂)的重量比将炔烃-rnai触发剂添加至tff纯化聚合物中 3天。
[0293]
实施例10.hif2αrnai触发剂的体外分析.候选序列通过计算器分析确认且体外筛选为经化学修饰的规范sirnas。出于筛选的目的,合成人类 epas1(hif2α)cdna序列(登录号nm_001430)且克隆(dna 2.0,加利福尼亚州门洛帕克)至市售基于报告物的筛选质粒psicheck2(promega,威斯康星州麦迪逊)中,由此产生海肾荧光素酶/epas1融合mrna。对于rnai触发剂功效评估,将hep3b 细胞(人类肝细胞癌株)以约10,000个细胞/孔涂铺于96孔格式中。两个亚群中的187 epas1 rnai触发剂中的每一种以两个浓度1nm及0.1nm共转染,其中25ngepas1-psicheck2质粒dna/孔及0.2μl lipofectamine 2000(life technologies)/ 孔。通过使用双重荧光素酶报告物分析(promega,威斯康星州麦迪逊)表5测量相对于组成性表达的萤火虫荧光素酶(还存在于上psicheck-2质粒上)的含量归一化的海肾荧光素酶含量来确定基因表达的减少情况。
[0294]
表5a.未修饰的hif2αrnai触发剂反义链和正义链序列
[0295]
[0296]
[0297]
[0298]
[0299]
[0300][0301]
表5b.具有修饰的核苷酸的hif2αrnai触发剂序列
[0302]
[0303]
[0304]
[0305]
[0306][0307]
表5c.hif2αrnai触发剂的体外效力筛选结果,由双荧光素酶报告物试验所确定.
[0308]
[0309]
[0310][0311]
实施例11.hif2αrnai触发剂ec
50
确定.八个最佳规范序列通过确定ec
50
浓度进一步评估。在与上述相同的条件及分析下但在0.00051nm至10nm范围内的10 种不同浓度下评定各触发剂的基因表达减少。使用graphpad prism软件确定ec
50
。
[0312]
前五个规范序列中的每一个经修饰以在6及7位含有una。使用与上述相同的条件及分析,并列评估这些触发剂以及其亲本规范序列的ec
50
浓度确定,表6。
[0313]
表6.ec
50
所示rnai触发剂的体外确定的值(nm)
[0314][0315]
实施例12.表达seap的透明细胞肾细胞癌(ccrcc)a498细胞的产生.在cmv 启动子下表达报告物基因分泌的碱性磷酸酶(seap)的pcr3.1表达载体通过自科隆达氏(clontech's)pseap2-基础载体扩增的seap编码序列pcr的定向克隆来制备。将适宜限制性位置添加于用以扩增seap编码序列的引物上,以克隆至pcr3.1载体(invitrogen)中。使用所得构建体pcr3-seap产生表达seap的a498 ccrcc细胞株。简言之,通过电穿孔根据制造商
的建议将pcr3-seap质粒转染至a498 ccrcc细胞中。通过g418抗性选择稳定转染子。评估选择的a498-seap纯系的 seap表达及整合稳定性。
[0316]
实施例13.具有稳定表达seap的a498细胞的带有原位rcc肿瘤的小鼠.用约3%异氟烷将雌性无胸腺裸小鼠麻醉且以右侧卧位置放。在左侧作出0.5-1cm小纵向腹部切口。使用潮湿棉签,将左肾自腹膜取出且温和稳定。就在注入之前,1.0ml 注射器填充有细胞/基质胶混合物且将27号针管连接至注射器尖端。接着将填充的注射器连接至注射泵(harvard apparatus,phd2000型)且灌注以移除空气。将连接至注射器的27号针管的尖端刚好低于肾囊接近尾端处插入,且接着针的尖端沿囊 3-4mm小心向前推进。使用注射泵将含有约300,000个细胞的2:1(体积:体积) 细胞/基质胶混合物的10μl等分试样缓慢注入至肾脏软组织中。针留于肾脏中 15-20秒以确保注射完成。接着自肾脏移除针且将棉签置放于注射位点上方30秒以防止细胞漏出或出血。接着将肾脏逐渐置放于腹部后面且将腹壁封闭。在植入之后每7-14天收集血清以使用商业seap分析试剂盒监测肿瘤生长。对于大多数研究,在肿瘤量度通常为大约4-8mm时,在植入之后5-6周使用肿瘤小鼠。
[0317]
实施例14.评估带有原位rcc肿瘤的小鼠中的hif2α-rnai触发剂.rgd靶向 hif2α-rnai触发剂递送偶联物。递送聚合物使用rgd-peg-hynic、 rgd-peg-acit-pnp或rdg-peg-fcitfp-tfp及peg-二肽修饰剂修饰。指示量的聚合物126或100a聚合物用8
×
peg12-acit-pabc-pnp/0.5
×
醛
ꢀ‑
peg24-fcit-pabc-pnp(其中rgd模拟物编号1-peg-hynic,使用1号方案)及指示量的指示hif2αrnai触发剂修饰。聚合物064根据方案7修饰。带有肾脏rcc 肿瘤的小鼠如所描述产生且用单次尾静脉注射等张葡萄糖(g1)或指示hif2αrnai 触发剂递送聚合物结合物处理。在注射之后在指示时间将小鼠安乐死,且总rna 由肾脏肿瘤使用trizol试剂根据制造商的建议来制备。如下文所述通过rt-qpcr 测定相对hif2αmrna含量且与仅经递送缓冲液(等张葡萄糖)处理的小鼠进行比较。
[0318]
表7.hif2αrnai触发剂递送后的小鼠中的hif2α敲减。rnai触发剂偶联至所示的可逆修饰的递送聚合物。
[0319]
[0320]
[0321][0322]
定量实时pcr分析.准备进行定量pcr时,根据制造商的方案,自 trireagent(分子研究中心(molecular research center),俄亥俄州辛辛那提)中均质化的组织样品分离出总rna。使用高容量cdna逆转录试剂盒(life technologies)对约500ng rna进行反转录。对于人类(肿瘤)hif2α(epas1)表达而言,使用taqman 基因表达主混物(life technologies)或veriquest探针主混物(affymetrix),使用预制的针对人类hif2α(目录号4331182)及cyca(ppia,目录号:4326316e)的taqman 基因表达分析进行双显体(biplex)反应,一式三份。对于人类(肿瘤)vegfa(vegfa) 表达而言,使用taqman基因表达主混物(life technologies)或veriquest探针主混物(affymetrix),使用预制的针对人类vegfa(目录号4331182,分析id:hs00900055) 及cyca(零件号:4326316e)的taqman基因表达分析进行双
显体反应,一式三份。通过使用7500fast或steponeplus实时pcr系统(life technologies)进行定量pcr。利用
△△ct
方法计算相对基因表达。
[0323]
实施例15.多剂量hif2αrnai触发剂递送聚合物偶联物抑制带有原位rcc肿瘤的小鼠中的肿瘤生长。hif2αrnai触发剂递送聚合物偶联物使用1号方案用 rnai触发剂双链id ad01031及聚合物ant 126制备。接着对偶联物进行tff纯化且如上所述确定聚合物浓度、rnai触发剂、rgd及修饰结合效率。每周剂量的含有400μg(聚合物重量)或280μg(聚合物重量)的hif2αrnai触发剂递送聚合物偶联物静脉内给予至2个不同组的带有肿瘤的小鼠。接受等张葡萄糖(ig)的带有肿瘤的小鼠用作处理对照。在研究过程中给予总计3次每周剂量。肿瘤生长率通过治疗期间以5-7天时间间隔收集的血清seap来评估。验尸时确定肿瘤重量及体积。评估总肿瘤形态及h&e病理组织学。
[0324]
表8.hif2αrnai触发剂递送聚合物偶联物敲减hif2α和vegfa
[0325][0326]
与对照处理相比,hif2α于400μg或280μg hif2αrnai触发剂递送聚合物偶联物组中的表达分别降低82%及81%(表8)。vegfa(良好表征的下游hif2α调节的基因)的表达还分别降低55%及61%(表8)。
[0327]
总体而言,在3次每周hif2αrnai触发剂递送聚合物偶联物注射之后,在两种评估剂量中显着抑制肿瘤生长。此情况得到总体肿瘤尺寸及血清seap含量的支持(图8-9,表9)。在第三次注射后seap含量的下降趋势表明肿瘤开始消退。另外,h&e染色福尔马林固定石蜡部分的肿瘤病理组织学研究展示典型rcc管结构破坏。在处理组中凋亡细胞的数量增加。一些肿瘤样品含有大面积的肿瘤坏死(图10)。
[0328]
表9.处理期间的血清seap水平,g1和g2,n=4;g3,n=3
[0329][0330]
实施例16.评估带有原位rcc肿瘤的小鼠中的hif2α-rnai触发剂.使用聚合物126、100a或006形成rgd靶向hif2α-rnai触发剂递送聚合物偶联物。rnai 触发剂μg指示与聚合物反应的触发剂的数量。聚合物经如上所述的指示rgd模拟物及peg修饰剂修饰。带有肾脏rcc肿瘤的小鼠如所描述产生且用单次尾静脉注射等张葡萄糖(g1)或指示hif2αrnai触发剂递送聚合物偶联物处理。在注射之后72h(第4天)将小鼠安乐死,且总rna由肾脏肿瘤使用trizol试剂根据制造商的建议来制备。如所述通过rt-qpcr确定相对hif2αmrna含量且与仅经递送缓冲液(等张葡萄糖)处理的小鼠进行比较(表11)。
[0331]
实施例17.hif2αrnai触发剂/第二处理组合研究.hif2αrnai触发剂递送聚合物偶联物(125μg聚合物)使用方案7双id no.ad1884及聚合物064来制备。每 4周通过静脉内注射给药hif2αrnai触发剂递送聚合物偶联物,总体4剂量。将获自lc laboratories公司的舒尼替尼(sunitinib,苹果酸盐)悬浮于ora-plus/orasweet(50:50,体积:体积)中。舒尼替尼处理在给予第一hif2αrnai触发剂剂量之后2周起始。小鼠通过经口给予5天/周给药维持2周,接着停药2周,总计3 个循环。
[0332]
肿瘤生长率通过治疗期间以5-7天时间间隔收集的血清seap来评估。验尸时确定肿瘤重量及体积。评估总肿瘤形态及h&e病理组织学。在单独舒尼替尼、dpc 舒尼替尼及单独dpc处理的组中相对hif2α表达量分别降低11.4%、73.8%及 77.6%(表10a)。组合hif2αrnai触发剂及舒尼替尼处理导致肿瘤生长抑制反应增加。总体上较小的肿瘤尺寸较小且观察到较低总生长(如通过seap的总倍数增加所测量)(表10b)。
[0333]
表10a.在用舒尼替尼、hif2αrnai触发剂、或hif2αrnai触发剂 舒尼替尼处理的动物模型中rcc肿瘤中的hif2α表达
[0334][0335]
表10b.在用舒尼替尼、hif2αrnai触发剂、或hif2αrnai触发剂 舒尼替尼处理的动物模型中rcc肿瘤中的肿瘤尺寸和seap表达
[0336][0337]
其他实施方式:应理解,尽管本发明已结合其实施方式加以描述,但前述描述意欲说明且不限制由所附权利要求的范围定义的本发明的范围。其他方面、优点及修改属于以下权利要求的范围内。
[0338]
表11.hif2αrnai触发剂递送后的具rcc肿瘤小鼠中的rcc细胞中的hif2α表达
[0339][0340]
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。
