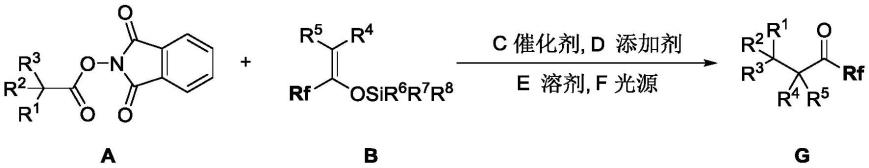
1.本发明涉及有机合成的技术领域,具体涉及一种氟烷基酮化合物的制备方法及其应用。
背景技术:
2.氟烷基酮是有机氟化合物的重要子类,由于氟原子的吸电子作用,使其具有独特的物理和化学性质,因此广泛应用于生物活性分子,天然产物和药物分子中,是一类非常重要的有机合成中间体。[a)c.han,a.e.salyer,e.h.kim,x.jiang,r.e.jarrard,m.s.powers,a.m.kirchhoff,t.k.salvador,j.a.chester,g.h.hockerman,d.a.colby,j.med.chem.2018,28,2697-2700.b)c.b.kelly,m.a.mercadante,n.e.leadbeater,chem.comm.2013,49,11133-11148.]氟烷基酮化合物的合成及其应用是非常重要的研究方向[a)g.pattison,eur.j.org.chem.2018,27-28,3496-3877.b)y.zeng,c.ni j.hu,chem.eur.j.2016,22,3210-3223.]目前,尽管在大多数情况下可以合成获得三氟甲基烷基酮[c.b.kelly,m.a.mercadante,n.e.leadbeater,chem.comm.2013,49,11133-11148.],但迄今为止,二氟甲基烷基酮的合成仍面临许多挑战。最为常见的方法主要有两种,一是通过亲电的氟试剂,逐步引入氟。二是将二氟化结构单元转移到适当的受体上,从而构成c-c键来合成二氟烷基酮。两种方法的官能团的容忍性和底物普适性都不是很好,很难应用于对复杂分子的后期修饰。因此,我们发展了一种简单高效的方法,可以一步合成二氟甲基烷基酮。此外,该方法不仅可以合成二氟烷基酮也可以应用于合成单氟甲基和三氟烷甲基烷基酮及其他各种含氟烷基酮。
技术实现要素:
[0003]
本发明的目的之一在于提供一种氟烷基酮化合物的制备方法,简单高效,可以一步合成二氟甲基烷基酮,还可以合成单氟甲基和三氟烷甲基烷基酮及其他各种含氟烷基酮。
[0004]
本发明的目的之二在于提供一种氟烷基酮化合物的应用。
[0005]
本发明实现目的之一所采用的方案是:一种氟烷基酮化合物的制备方法,将活性羧酸酯a、含氟烯醇硅醚b、光催化剂、有机溶剂和添加剂混合,得到混合溶液,在光照、-78℃到180℃的条件下搅拌反应后分离提纯,即可得到所述氟烷基酮化合物。
[0006]
所述反应的温度为-78℃到180℃。上述反应时间在3-24小时以内。加热过程可采用油浴(例如硅油、石蜡油等)或者其它加热方式。本发明在反应完成后对反应产物进行后处理,包括抽滤、浓缩、重结晶和柱层析等纯化方法。
[0007]
所述抽滤过程可使用砂芯漏斗在减压的条件下过滤。
[0008]
所述浓缩过程可采用常压蒸馏、减压蒸馏等方法,例如用旋转蒸发仪真空浓缩。
[0009]
所述纯化过程是通过柱层析得到纯净的产物。
[0010]
优选地,所述氟烷基酮化合物的分子结构式如下所示:
[0011][0012]
所述活性羧酸酯a的分子结构式为
[0013]
所述含氟烯醇硅醚b的分子结构式为:
[0014]
其中,r1、r2、r3为芳基、杂芳基、烷基、烯基、炔基、酯基、氰基、硝基、磺酰基、杂原子、氢原子中的任意一种,可以相同也可以不同;r4、r5为芳基、杂芳基、烷基、烯基、炔基、酯基、氰基、硝基、磺酰基、杂原子、氢原子中的任意一种,可以相同也可以不同;r6、r7、r8芳基、杂芳基、烷基、酯基、杂原子、氢原子中的任意一种,可以相同也可以不同;rf为cf2r9或cfr
10r11
,r9为卤素、芳基、杂芳基、烷基、烯基、炔基、酯基、氰基、硝基、磺酰基、羧基、杂原子、氢原子中的任意一种;r
10
、r
11
为芳基、杂芳基、烷基、烯基、炔基、酯基、氰基、硝基、磺酰基、杂原子、氢原子中的任意一种,可以相同也可以不同。
[0015]
本发明方法的反应式可表示如下:
[0016][0017]
其中,式a化合物代表活性羧酸酯,式b化合物代表各类烯醇硅醚,式g代表氟烷基酮化合物。
[0018]
优选地,所述烷基具有1-20个碳原子,为直链结构、环状结构或者支链结构。
[0019]
优选地,所述烷基带有一个或多个取代基,当具有多个取代基时,取代基可以相同也可以不同,位置可以相同也可以不相同。
[0020]
优选地,所述芳基带有一个或者多个取代基;当具有多个取代基时,取代基可以相同或不同。
[0021]
优选地,所述催化剂为三[2-苯基吡啶-c2,n]铱(iii)、二[2-(2,4-二氟苯基)-5-三氟甲基吡啶][2-2'-联(4-叔丁基吡啶)]铱二(六氟磷酸)盐、二[2-(2,4-二氟苯基)-5-甲基吡啶][2,2'-联(四叔丁基吡啶)]铱二(六氟磷酸)盐、二[2-(2,4-二氟苯基)-5-三氟甲基吡啶][2-2'-联吡啶]铱二(六氟磷酸)盐、[2,2'-联(4-叔丁基吡啶)]双[2-(2,4-二氟苯基)吡啶]铱(iii)六氟磷酸盐、(4,4'-二叔丁基-2,2'-联吡啶)双[(2-吡啶基)苯基]铱(iii)六氟磷酸盐、乙酰丙酮酸二(2-甲基-3-苯基吡嗪-c2,n)合铱、乙酰丙酮酸二(2,3-二苯基吡嗪-c2,n)合铱、乙酰丙酮酸二(2,3-二苯基喹喔啉)合铱、乙酰丙酮酸二(2-苯基嘧啶-c2,n)合铱、(2,2'-联吡啶)双[2-(4-氟苯基)吡啶]铱(iii)六氟磷酸盐、(2,2'-联吡啶)双[2-(2,4-二氟苯基)吡啶]铱(iii)六氟磷酸盐、(2,2'-联吡啶)双[2-(4-叔丁基苯基)吡啶]铱
(iii)六氟磷酸盐、(2-2'-联(4-叔丁基吡啶)双[2-(4-叔丁基苯基)吡啶]铱(iii)六氟磷酸盐、(1,10-菲罗啉)双[2-(4-叔丁基苯基)吡啶]铱(iii)六氟磷酸盐、三(2-(4-氟苯基)吡啶)合铱、三[2-(4,6-二氟苯基)吡啶-c2,n]铱(iii)、二[2-(3-叔丁基苯基)-4-叔丁基吡啶][2,2`-联(4-叔丁基吡啶)]合铱(iii)六氟磷酸盐、二氯四(2-(2-吡啶基)苯基)二铱(iii)、三(2-(4-三氟甲基苯基)吡啶)合铱、[2,2'-联(4-叔丁基吡啶)]双[2-(4-氟苯基)吡啶]铱(iii)六氟磷酸盐、罗丹明6g、三(1,10-菲咯啉)钌(ii)双(六氟磷酸盐)、三(4,4'-二甲基-2,2'-联吡啶)钌(iii)(六氟磷酸)盐、三(2,2'-联吡嗪)钌二(六氟膦酸)盐、三(2,2'-联吡啶)钌二(六氟磷酸)盐、三(2,2'-联吡啶)钌二(高氯酸)盐、三(2,2'-联吡啶)钌二(四氟硼酸)盐、三(2,2'-联吡啶)氯化钌(ii)六水合物、9-均三甲苯基-10-苯基吖啶-10-四氟硼酸盐、2,3,5,6-四(9-咔唑基)-对苯二腈、三(2,2'-联吡啶)氯化钌(ii)六水合物、溶剂红43中的任意一种。
[0022]
优选地,所述有机溶剂为甲醇、乙醇、异丙醇、叔丁醇、四氢呋喃、2-甲基四氢呋喃、乙醚、二甲基乙二醚、甲基叔丁基醚、1,4-环氧六烷、1,3-环氧六烷、二氯甲烷、1,2-二氯乙烷、氯仿、四氯化碳、c
4-12
的饱和烷烃、c
3-12
的氟代或者氯代烷烃、苯、甲苯、二甲苯、三甲苯、二甲亚砜、n,n-二甲基甲酰胺、n,n-二甲基乙酰胺、丙酮、n-甲基吡咯烷酮、乙腈、c
3-12
的饱和烷基腈中的至少一种。
[0023]
优选地,所述添加剂为甲酸、乙酸、丙酸、丁酸、苯甲酸、2-碘苯甲酸、乙二酸、三氟乙酸、二氟乙酸、单氟乙酸、三氟甲磺酸、对甲基苯磺酸、水、丙二酸、盐酸、硫酸、硝酸中的至少一种。
[0024]
优选地,所述活性羧酸酯a和烯醇硅醚b之间的摩尔比为1:1-6;催化剂的用量为活性羧酸酯a的摩尔量的1%~3%,添加剂与活性羧酸酯a之间的摩尔比为1:1-50;混合溶液中活性羧酸酯a的浓度在0.1m到1m之间。
[0025]
优选地,所述光照的光源为白光、蓝光、紫光、绿光中的任意一种,光源的功率为1w-60w之间。
[0026]
本发明实现目的之二所采用的方案是:所述的制备方法制备的氟烷基酮在合成含氟吡啶类化合物中的应用。
[0027]
本发明具有以下优点和有益效果:
[0028]
(1)本发明的制备方法实现了活性羧酸酯和含氟烯醇硅醚的自由基加成反应,是一种新的反应模式,为合成氟烷基酮提供一种简单、高效的方法,特别是二氟烷基酮的合成,具有非常大的应用前景,此外,该方法也可以应用于合成单氟甲基和三氟烷甲基烷基酮及其他各种含氟烷基酮。
[0029]
(2)本发明的制备方法在一个氧化还原中性的条件下进行,反应条件简单、高效、温和。
[0030]
(3)本发明的制备方法所涉及的反应条件具有良好的官能团容忍性和底物普适性,可以兼容酯基、卤素、羰基等各种官能团,各种直链或者支链的烷基也可以完成该反应。
[0031]
(4)本发明的制备方法可以对复杂生物活性分子及药物分子进行后期修饰,所合成氟烷基化合物也可用于合成含氟吡啶类化合物。
具体实施方式
[0032]
为更好的理解本发明,下面的实施例是对本发明的进一步说明,但本发明的内容不仅仅局限于下面的实施例。
[0033]
实施例1-30
[0034]
1,1-二氟-5-(4-氟苯基)戊烷-2-酮(简写为g1,结构式如下)的制备:
[0035]
将1,3-二氧异吲哚-2-基3-(4-氟苯基)丙酸酯和叔丁基((3,3-二氟丙-1-烯-2-基)氧基)二苯基硅烷,光催化剂,加入到25毫升的光反应管中,加入添加剂和有机溶剂,橡胶塞封住,插入一个氮气球,液氮冻抽3次,反应置于光源下在一定温度下反应。反应结束后,加入30微升的三氟乙酸,室温搅拌10分钟,然后加入10毫升水,乙酸乙酯萃取,盐水洗涤,无水硫酸钠干燥,过滤,旋干,粗产品用石油醚/乙酸乙酯=50:1(v/v)柱层析,旋干即得产品g1。1h nmr(400mhz,cdcl3)δ7.17
–
7.08(m,2h),7.04
–
6.92(m,2h),5.66(t,j=54.0,1h),2.72
–
2.59(m,4h),1.99
–
1.92(m,j=7.3hz,2h).
13
c nmr(101mhz,cdcl3)δ199.6(t,j=26.8hz)161.4(d,j=243.8hz),136.5(d,j=3.2hz),129.8(d,j=7.8hz),115.3(d,j=21.2hz),109.8(t,j=253.5hz),35.1,33.9,23.9.
19
f nmr(376mhz,cdcl3)δ
–
117.0
––
117.1(m,1f),
–
126.8(d,j=53.8hz,2f).ir(atr):2937,2863,1744,1603,1510,1342,1223,1159,1090,824cm-1
.hrms(esi,m/z):calcd for c
11h10
f3o-(m-h)-:215.0689;found:215.0691。反应原料及反应条件及产率具体见表1:
[0036]
表1实施例1-30的具体反应条件及产率
[0037]
[0038][0039]a为分离产率;b为fac-ir(ppy)3(1mmol%)。
[0040]
根据以上的条件优化,确定了最优的条件:物质a与物质b的最优比为1:6,最优的添加剂为水,最优当量为20当量,最优的溶剂为二甲亚砜,最优光源为蓝光,最优功率为6w,最优温度为25度。
[0041]
实例31-57都是在最优条件下进行的。
[0042]
实施例31
[0043]
1,1-二氟-5-(4-氟苯基)戊烷-2-酮(简写为g1,结构式如下)的制备:
[0044][0045]
将62.6毫克1,3-二氧异吲哚-2-基3-(4-氟苯基)丙酸酯,398.4毫克叔丁基((3,3-二氟丙-1-烯-2-基)氧基)二苯基硅烷,3.9毫克三(2-苯基吡啶)合铱,加入到25毫升的光反应管中,加入72毫克水和4毫升二甲基亚砜,橡胶塞封住,插入一个氮气球,液氮冻抽3次,反应置于蓝光(6w)下室温反应15小时。反应结束后,加入30微升的三氟乙酸,室温搅拌10分钟,然后加入10毫升水,乙酸乙酯萃取,盐水洗涤,无水硫酸钠干燥,过滤,旋干,粗产品用石
油醚/乙酸乙酯=50:1(v/v)柱层析,旋干即得产品g1(无色液体30.1mg,产率70%)。1h nmr(400mhz,cdcl3)δ7.17
–
7.08(m,2h),7.04
–
6.92(m,2h),5.66(t,j=54.0,1h),2.72
–
2.59(m,4h),1.99
–
1.92(m,j=7.3hz,2h).
13
c nmr(101mhz,cdcl3)δ199.6(t,j=26.8hz)161.4(d,j=243.8hz),136.5(d,j=3.2hz),129.8(d,j=7.8hz),115.3(d,j=21.2hz),109.8(t,j=253.5hz),35.1,33.9,23.9.
19
f nmr(376mhz,cdcl3)δ
–
117.0
––
117.1(m,1f),
–
126.8(d,j=53.8hz,2f).ir(atr):2937,2863,1744,1603,1510,1342,1223,1159,1090,824cm-1
.hrms(esi,m/z):calcd for c
11h10
f3o-(m-h)-:215.0689;found:215.0691。
[0046]
实施例32:
[0047]
1,1-二氟-5-苯基戊烷-2-酮(简写为g2,结构式如下)的制备:
[0048][0049]
将59.0毫克1,3-二氧异吲哚-2-基3-苯基丙酸酯,398.4毫克叔丁基((3,3-二氟丙-1-烯-2-基)氧基)二苯基硅烷,3.9毫克三(2-苯基吡啶)合铱,加入25到毫升的光反应管中,加入72毫克水和4毫升二甲基亚砜,橡胶塞封住,插入一个氮气球,液氮冻抽3次,反应置于蓝光(6w)下室温反应15小时。反应结束后,加入10毫升水,乙酸乙酯萃取,盐水洗涤,无水硫酸钠干燥,过滤,旋干(水浴大于45度),粗产品用石油醚/乙酸乙酯=50:1(v/v)柱层析,旋干即得产品g2(无色液体27.6mg,产率70%)。1h nmr(400mhz,cdcl3)δ7.34
–
7.27(m,2h),7.24
–
7.15(m,3h),5.66(t,j=54.0hz,1h),2.71
–
2.63(m,4h),2.03
–
1.95(m,2h).
13
c nmr(101mhz,cdcl3)δ199.6(t,j=26.1hz),140.9,128.5,128.4,109.8(t,j=252.7hz),35.2,34.7,23.8.
19
f nmr(376mhz,cdcl3)δ
–
126.85(d,j=54.7hz).ir(atr):3086,3027,2930,2863,1744,1603,1498,1342,1103,1062cm-1
.hrms(esi,m/z):calcd for c
11
h1f2o-(m-h)-:197.0783;found:197.0785。
[0050]
实施例33:
[0051]
5-(4-溴苯基)-1,1-二氟戊烷-2-酮(简写为g3,结构式如下)的制备:
[0052][0053]
将74.6毫克1,3-二氧异吲哚-2-基3-(4-溴苯基)丙酸酯,398.4毫克叔丁基((3,3-二氟丙-1-烯-2-基)氧基)二苯基硅烷,3.9毫克三(2-苯基吡啶)合铱,加入到25毫升的光反应管中,加入72毫克水和4毫升二甲基亚砜,橡胶塞封住,插入一个氮气球,液氮冻抽3次,反应置于蓝光(6w)下室温反应15小时。反应结束后,加入30微升的三氟乙酸,室温搅拌10分钟,然后加入10毫升水,乙酸乙酯萃取,盐水洗涤,无水硫酸钠干燥,过滤,旋干,粗产品用石油醚/乙酸乙酯=50:1(v/v)柱层析,旋干即得产品g3(淡黄色液体35.4mg,产率64%)。1h nmr(400mhz,cdcl3)δ7.45
–
7.38(m,2h),7.08
–
7.02(m,2h),5.66(t,j=54.0hz,1h),2.70
–
2.56(m,4h),1.99
–
1.92(m,2h).
13
c nmr(101mhz,cdcl3)δ199.5(t,j=26.2hz),131.6,130.2,119.9,109.8(t,j=253.0hz),35.0,34.1,23.6.139.9,131.6,130.2,119.9,109.8(t,j=253.0hz),35.0,34.2,23.6.
19
f nmr(376mhz,cdcl3)δ
–
126.9(d,j=54.7).ir(atr):
2926,2855,1748,1487,1402,1342,1100,1070,1010,794cm-1
.hrms(esi,m/z):calcd for c
11h12
brf2o
(m h)
:276.9668;found:276.9869。
[0054]
实施例34:
[0055]
1,1-二氟-4-苯氧基丁烷-2-酮(简写为g4,结构式如下)的制备:
[0056][0057]
将74.6毫克1,3-二氧异吲哚-2-基3-(4-溴苯基)丙酸酯,199.2毫克((3,3-二氟对-1-烯-2-基)氧基)三甲基硅烷,3.9毫克三(2-苯基吡啶)合铱,加入到25毫升的光反应管中,加入72毫克水和4毫升二甲基亚砜,橡胶塞封住,插入一个氮气球,液氮冻抽3次,反应置于蓝光(6w)下室温反应15小时。反应结束后,加入30微升的三氟乙酸,室温搅拌10分钟,然后加入10毫升水,乙酸乙酯萃取,盐水洗涤,无水硫酸钠干燥,过滤,旋干,粗产品用石油醚/乙酸乙酯=10:1(v/v)柱层析,旋干即得产品g4(无色液体,25.6mg,产率60%)。1h nmr(400mhz,cdcl3)δ7.32
–
7.26(m,2h),7.00
–
6.93(m,1h),6.92
–
6.86(m,2h),5.74(t,j=54.0hz,1h),4.01(t,j=5.9hz,2h),2.92
–
2.88(m,2h),2.19
–
2.10(m,2h).
13
c nmr(101mhz,cdcl3)δ199.4(t,j=26.1hz),158.6,129.5,120.9,114.4,109.8(t,j=252.6hz),66.1,32.9,22.4.
19
f nmr(376mhz,cdcl3)δ=
–
127.0(d,j=54.1hz).ir(atr):3034,2926,2878,1744,1599,1498,1245,1170,1103,1059,757cm-1
.hrms(esi,m/z):calcd for c
11h13
f2o
2
(m h)
:215.0878;found:215.0874。
[0058]
实施例35:
[0059]
1,1-二氟-5-(4-甲氧基苯基)戊烷-2-酮(简写为g5,结构式如下)的制备:
[0060][0061]
将65.0毫克1,3-二氧异吲哚-2-基3-(4-甲氧基苯基)丙酸酯,398.4毫克叔丁基((3,3-二氟丙-1-烯-2-基)氧基)二苯基硅烷,3.9毫克三(2-苯基吡啶)合铱,加入到25毫升的光反应管中,加入72毫克水和4毫升二甲基亚砜,橡胶塞封住,插入一个氮气球,液氮冻抽3次,反应置于蓝光(6w)下室温反应15小时。反应结束后,加入30微升的三氟乙酸,室温搅拌10分钟,然后加入10毫升水,乙酸乙酯萃取,盐水洗涤,无水硫酸钠干燥,过滤,旋干,粗产品用石油醚/乙酸乙酯=20:1(v/v)柱层析,旋干即得产品g5(无色液体,27.5mg,产率60%)。1h nmr(400mhz,cdcl3)δ7.12
–
7.05(m,2h),6.87
–
6.81(m,2h),5.65(t,j=54.0hz,1h),3.79(s,3h),2.70
–
2.56(m,4h),1.98
–
1.92(m,2h).
13
c nmr(101mhz,cdcl3)δ199.7(t,j=26.2hz),158.0,133.0,129.3,113.9,109.8(t,j=252.9hz),55.2,35.2,33.8,24.0.
19
f nmr(376mhz,cdcl3)δ
–
126.8(d,j=54.5hz).ir(atr):3004,2937,2840,1744,1610,1513,1461,1245,1779,1033,828cm-1
.hrms(esi,m/z):calcd for c
12h15
f2o
2
(m h)
:229.1035;found:229.1036。
[0062]
实施例:36:
[0063]
6,6-二氟-1-苯基己烷-1,5-二酮(简写为g6,结构式如下)的制备:
[0064][0065]
将64.6毫克1,3-二氧异吲哚-2-基4-氧-4-苯基丁酸酯,398.4毫克叔丁基((3,3-二氟丙-1-烯-2-基)氧基)二苯基硅烷,3.9毫克三(2-苯基吡啶)合铱,加入25到毫升的光反应管中,加入72毫克水和4毫升二甲基亚砜,橡胶塞封住,插入一个氮气球,液氮冻抽3次,反应置于蓝光(6w)下室温反应15小时。反应结束后,加入10毫升水,乙酸乙酯萃取,盐水洗涤,无水硫酸钠干燥,过滤,旋干(水浴大于45度),粗产品用石油醚/乙酸乙酯=5:1(v/v)柱层析,旋干即得产品g6(淡黄色固体36.1mg,产率80%)。1h nmr(400mhz,cdcl3)δ7.12
–
7.05(m,2h),6.87
–
6.81(m,2h),5.65(t,j=54.0,1h),3.79(s,3h),2.70
–
2.56(m,4h),1.98
–
1.92(m,2h).
13
c nmr(101mhz,cdcl3)δ199.5(t,j=26.3hz),199.1,136.6,133.2,128.6,128.0,109.7(t,j=253.5hz),36.9,35.2,16.7.
19
f nmr(376mhz,cdcl3)δ
–
127.0(d,j=53.8hz).ir(atr):2922,2885,1744,1681,1450,1401,1375,1279,1215,1103,738cm-1
.hrms(esi,m/z):calcd for c
12h13
f2o
2
(m h)
:227.0878;found:227.0874。
[0066]
实施例:37:
[0067]
6,6-二氟-1-(4-氟苯基)己烷-1,5-二酮(简写为g7,结构式如下)的制备:
[0068][0069]
将68.2毫克1,3-二氧代异吲哚啉-2-基4-(4-氟苯基)-4-氧代丁酸酯,398.4毫克叔丁基((3,3-二氟丙-1-烯-2-基)氧基)二苯基硅烷,3.9毫克三(2-苯基吡啶)合铱,加入25到毫升的光反应管中,加入72毫克水和4毫升二甲基亚砜,橡胶塞封住,插入一个氮气球,液氮冻抽3次,反应置于蓝光(6w)下室温反应15小时。反应结束后,加入10毫升水,乙酸乙酯萃取,盐水洗涤,无水硫酸钠干燥,过滤,旋干(水浴大于45度),粗产品用石油醚/乙酸乙酯=5:1(v/v)柱层析,旋干即得产品g7(淡黄色固体34.2mg,产率70%)。1h nmr(400mhz,cdcl3)δ8.02
–
7.87(m,2h),7.19
–
7.04(m,2h),5.71(t,j=54.0hz,1h),3.03(t,j=6.9hz,2h),2.82(t,j=6.9hz,2h),2.12
–
2.05(m,2h).
13
c nmr(101mhz,cdcl3)δ199.5(t,j=26.3hz),197.5,165.8(d,j=255.0hz),133.1(d,j=3.1hz),130.6(d,j=9.4hz),115.7(d,j=21.9hz),109.7(t,j=252.8hz),36.8,35.2,16.7.
19
f nmr(376mhz,cdcl3)δ
–
99.2
––
109.5(m,1f),
–
127.0(d,j=53.6hz,2f).ir(atr):3079,2963,1744,1637,1595,1507,1409,1372,1241,1163,1096cm-1
.gc-ms(ei,m/z):calcd for c
12h11
f3o2(m):244.07found:244.11。
[0070]
实施例:38:
[0071]
1,1-二氟壬二-2-酮(简写为g8,结构式如下)的制备:
[0072]
[0073]
将55毫克1,3-二氧异吲哚-2-基庚酸酯,398.4毫克叔丁基((3,3-二氟丙-1-烯-2-基)氧基)二苯基硅烷,3.9毫克三(2-苯基吡啶)合铱,加入到25毫升的光反应管中,加入72毫克水和4毫升二甲基亚砜,橡胶塞封住,插入一个氮气球,液氮冻抽3次,反应置于蓝光(6w)下室温反应15小时。反应结束后,加入30微升的三氟乙酸,室温搅拌10分钟,然后加入10毫升水,乙酸乙酯萃取,盐水洗涤,无水硫酸钠干燥,过滤,旋干,粗产品用石油醚柱层析,旋干即得产品g8(淡黄色液体,16.8mg,产率47%)。1h nmr(400mhz,cdcl3)δ5.67(t,j=54.0hz,1h),2.68
–
2.63(m,2h),1.70
–
1.59(m,2h),1.33
–
1.25(m,8h),0.90
–
0.87(m,3h).
13
c nmr(101mhz,cdcl3)δ200.0(t,j=26.8hz),109.9(t,j=253.0hz),36.0,31.6,28.90,28.88,22.6,22.3,14.0.
19
f nmr(376mhz,cdcl3)δ
–
126.9(d,j=53.6hz).ir(atr):3027,2930,2859,1744,1498,1454,1402,1342,1148,1100,701cm-1
.hrms(esi,m/z):calcd for c9h
15
f2o-(m-na)-:177.1096;found:177.1100。
[0074]
实施例39:
[0075]
8-氯-1,1-二氟辛烷-2-酮(简写为g9,结构式如下)的制备:
[0076][0077]
将55毫克1,3-二氧异吲哚-2-基6-氯己酸酯,398.4毫克叔丁基((3,3-二氟丙-1-烯-2-基)氧基)二苯基硅烷,3.9毫克三(2-苯基吡啶)合铱,加入到25毫升的光反应管中,加入72毫克水和4毫升二甲基亚砜,橡胶塞封住,插入一个氮气球,液氮冻抽3次,反应置于蓝光(6w)下室温反应15小时。反应结束后,加入30微升的三氟乙酸,室温搅拌10分钟,然后加入10毫升水,乙酸乙酯萃取,盐水洗涤,无水硫酸钠干燥,过滤,旋干,粗产品用石油醚/乙酸乙酯=50:1(v/v)柱层析,旋干即得产品g9(无色液体26.7mg,产率67%)。1h nmr(400mhz,cdcl3)δ5.67(t,j=54.0hz,1h),3.53(t,j=6.6hz,2h),2.69
–
2.65(m,2h),1.83
–
1.72(m,2h),1.70
–
1.62(m,2h),1.51
–
1.41(m,2h),1.41
–
1.31(m,2h).
13
c nmr(101mhz,cdcl3)δ199.8(t,j=26.8hz),109.9,44.9,35.8,32.3,28.1,26.5,22.1.
19
f nmr(376mhz,cdcl3)δ
–
126.8(d,j=53.8hz).ir(atr):2937,2863,1744,1461,1401,1342,1103,1047,865,805,727cm-1
.hrms(esi,m/z):calcd for c8h
11
clf2o-(m-h)-:197.0550;found:197.0553。
[0078]
实施例40:
[0079]
8-溴-1,1-二氟辛烷-2-酮(简写为g10,结构式如下)的制备:
[0080][0081]
将67.8毫克1,3-二氧异吲哚-2-基6-溴己酸酯,398.4毫克叔丁基((3,3-二氟丙-1-烯-2-基)氧基)二苯基硅烷,加入到25毫升的光反应管中,加入72毫克水和4毫升二甲基亚砜,橡胶塞封住,插入一个氮气球,液氮冻抽3次,反应置于蓝光(6w)下室温反应15小时。反应结束后,加入30微升的三氟乙酸,室温搅拌10分钟,然后加入10毫升水,乙酸乙酯萃取,盐水洗涤,无水硫酸钠干燥,过滤,旋干,粗产品用石油醚/乙酸乙酯=50:1(v/v),旋干即得产品g10(无色液体,26.4mg,产率58%)。1h nmr(400mhz,cdcl3)δ5.67(t,j=54.0hz,1h),
3.40(t,j=6.8hz,2h),2.69
–
2.65(m,2h),1.90
–
1.83(m,2h),1.70
–
1.62(m,2h),1.51
–
1.41(m,2h),1.39
–
1.31(m,2h).
13
c nmr(101mhz,cdcl3)δ199.7(t,j=26.1hz),109.8(t,j=252.9hz),35.8,33.6,32.4,28.0,27.7,22.1.
19
f nmr(376mhz,cdcl3)δ
–
126.8(d,j=54.2hz).ir(atr):2933,2859,1744,1461,1401,1342,1256,1159,1100,1044,723cm-1
.hrms(esi,m/z):calcd for c8h
11
brf2o-(m-h)-:287.0100;found:287.0104。
[0082]
实施例41:
[0083]
8,8-二氟-7-氧辛酸甲酯(简写为g11,结构式如下)的制备:
[0084][0085]
将70.0毫克1,3-二氧异吲哚-2-基己二酸甲酯,398.4毫克叔丁基((3,3-二氟丙-1-烯-2-基)氧基)二苯基硅烷,3.9毫克三(2-苯基吡啶)合铱,加入到25毫升的光反应管中,加入72毫克水和4毫升二甲基亚砜,橡胶塞封住,插入一个氮气球,液氮冻抽3次,反应置于蓝光(6w)下室温反应15小时。反应结束后,加入30微升的三氟乙酸,室温搅拌10分钟,然后加入10毫升水,乙酸乙酯萃取,盐水洗涤,无水硫酸钠干燥,过滤,旋干,粗产品用石油醚/乙酸乙酯=10:1(v/v)柱层析,旋干即得产品g11(淡黄色液体,27.1mg,产率65%)。1h nmr(400mhz,cdcl3)δ5.67(t,j=54.0hz,1h),3.65(s,3h),2.70
–
2.63(m,2h),2.31(t,j=7.4,2h),1.68
–
1.61(m,4h),1.41
–
1.31(m,2h).
13
c nmr(101mhz,cdcl3)δ199.7(t,j=26.2hz),173.9,109.8(t,j=252.8hz),51.5,35.7,33.7,28.3,24.5,21.9.
19
f nmr(376mhz,cdcl3)δ
–
126.90(d,j=53.7hz).ir(atr):2952,2866,1737,1439,1349,1252,1200,1174,1103,1047cm-1
.hrms(esi,m/z):calcd for c9h
13
f2o3(m-h)-:207.0838;found:207.0839。
[0086]
实施例42:
[0087]
1,1-二氟-3-(四氢-2h-吡喃-4-基)丙-2-酮(简写为g12,结构式如下)的制备:
[0088][0089]
将55.0毫克1,3-二氧杂异吲哚-2-基四氢-2h-吡喃-4-羧酸酯,398.4毫克叔丁基((3,3-二氟丙-1-烯-2-基)氧基)二苯基硅烷,3.9毫克三(2-苯基吡啶)合铱,加入到25毫升的光反应管中,加入72毫克水和4毫升二甲基亚砜,橡胶塞封住,插入一个氮气球,液氮冻抽3次,反应置于蓝光(6w)下室温反应15小时。反应结束后,加入30微升的三氟乙酸,室温搅拌10分钟,然后加入10毫升水,乙酸乙酯萃取,盐水洗涤,无水硫酸钠干燥,过滤,旋干,粗产品用石油醚/乙酸乙酯=10:1(v/v)柱层析,旋干即得产品g12(无色液体,23.6mg,产率66%)。1h nmr(400mhz,cdcl3)δ5.65(t,j=54.1hz,1h),4.00
–
3.89(m,2h),3.42(td,j=11.8,2.1hz,2h),2.60(dt,j=6.7,1.2hz,2h),2.21
–
2.10(m,1h),1.68
–
1.61(m,2h),1.40
–
1.28(m,2h).
13
c nmr(101mhz,cdcl3)δ198.8(t,j=26.8hz),109.8(t,j=254.0hz),67.6,42.7,32.6,29.8.
19
f nmr(376mhz,cdcl3)δ
–
126.9(d,j=53.8hz).ir(atr):2922,2848,1744,1446,1387,1342,1275,1241,1092,857cm-1
.hrms(esi,m/z):calcd for c8h
11
f2o
2-(m-h)-:177.0733;found:177.0736。
[0090]
实施例43:
[0091]
4-(3,3-二氟-2-氧丙基)哌啶-1-甲酸叔丁酯(简写为g13,结构式如下)的制备:
[0092][0093]
将74.8毫克1-(叔丁基)4-(1,3-二氧异吲哚-2-基)哌啶-1,4-二羧酸酯,398.4毫克叔丁基((3,3-二氟丙-1-烯-2-基)氧基)二苯基硅烷,3.9毫克三(2-苯基吡啶)合铱,加入25到毫升的光反应管中,加入72毫克水和4毫升二甲基亚砜,橡胶塞封住,插入一个氮气球,液氮冻抽3次,反应置于蓝光(6w)下室温反应15小时。反应结束后,加入10毫升水,乙酸乙酯萃取,盐水洗涤,无水硫酸钠干燥,过滤,旋干(水浴大于45度),粗产品用石油醚/乙酸乙酯=5:1(v/v)柱层析,旋干即得产品g13(无色液体,33.8mg,产率61%)。1h nmr(400mhz,cdcl3)δ5.65(t,j=54.1hz,1h),4.13
–
4.02(m,2h),2.73(t,j=12.3hz,2h),2.59(dt,j=6.7,1.2hz,2h),2.09
–
2.01(m,1h),1.71
–
1.63(m,2h),1.44(s,9h),1.20
–
1.10(m,2h).
13
c nmr(101mhz,cdcl3)δ198.6(t,j=26.7hz),154.74,109.75(t,j=253.0hz),79.44,42.31,31.70,30.82,28.40.
19
f nmr(376mhz,cdcl3)δ
–
126.9(d,j=53.8hz).ir(atr):2974,2930,2855,1744,1685,1424,1364,1286,1245,1163cm-1
.hrms(esi,m/z):calcd for c
13h21
f2nnao
3
(m na)
:300.1382;found:300.1380。
[0094]
实施例44:
[0095]
4-(3,3-二氟-2-氧丙基)哌啶-1-羧酸苄酯(简写为g14,结构式如下)的制备:
[0096][0097]
将81.6毫克1,3-二氧代异吲哚啉-2-基4-(4-氟苯基)-4-氧代丁酸酯,398.4毫克叔丁基((3,3-二氟丙-1-烯-2-基)氧基)二苯基硅烷,3.9毫克三(2-苯基吡啶)合铱,加入25到毫升的光反应管中,加入72毫克水和4毫升二甲基亚砜,橡胶塞封住,插入一个氮气球,液氮冻抽3次,反应置于蓝光(6w)下室温反应15小时。反应结束后,加入10毫升水,乙酸乙酯萃取,盐水洗涤,无水硫酸钠干燥,过滤,旋干(水浴大于45度),粗产品用石油醚/乙酸乙酯=5:1(v/v)柱层析,旋干即得产品g14(淡黄色液体,35.2mg,产率57%)。1h nmr(400mhz,cdcl3)δ7.39
–
7.29(m,5h),5.65(t,j=54.0hz,1h),5.12(s,2h),4.28
–
4.05(m,2h),2.92
–
2.71(m,2h),2.60(dt,j=6.7,1.2hz,2h),2.17
–
2.00(m,1h),1.78
–
1.64(m,2h),1.24
–
1.10(d,j=12.7hz,2h).
13
c nmr(101mhz,cdcl3)δ198.7(t,j=26.8hz),155.2,136.8,128.5,128.0,127.9,109.7(t,j=254.5hz),67.1,43.9,42.2,31.6,30.7.
19
f nmr(376mhz,cdcl3)δ
–
126.8(d,j=53.7hz).ir(atr):2922,2855,1744,1689,1431,1282,1241,1077,1017,798cm-1
.hrms(esi,m/z):calcd for c
16h19
f2no
3
(m h)
:312.1406;found:312.1406。
[0098]
实施例45:
[0099]
3-(2,3-二氢-1h-茚-2-基)-1,1-二氟丙烷-2-酮(简写为g15,结构式如下)的制备:
[0100][0101]
将61.4毫克1,3-二氧异吲哚-2-基2,3-二氢-1h-茚-2-羧酸酯,398.4毫克叔丁基((3,3-二氟丙-1-烯-2-基)氧基)二苯基硅烷,3.9毫克三(2-苯基吡啶)合铱,加入25到毫升的光反应管中,加入72毫克水和4毫升二甲基亚砜,橡胶塞封住,插入一个氮气球,液氮冻抽3次,反应置于蓝光(6w)下室温反应15小时。反应结束后,加入10毫升水,乙酸乙酯萃取,盐水洗涤,无水硫酸钠干燥,过滤,旋干(水浴大于45度),粗产品用石油醚/乙酸乙酯=50:1(v/v)柱层析,旋干即得产品g15(淡黄色液体,20.2mg,产率48%)。1h nmr(400mhz,cdcl3)δ7.24
–
7.12(m,4h),5.69(t,j=54.0hz,1h),3.23
–
3.17(m,2h),3.02
–
2.91(m,1h),2.89
–
2.86(m,2h),2.64
–
2.58(m,2h).
13
c nmr(101mhz,cdcl3)δ199.4,(t,j=26.3hz),142.3,126.4,124.5,109.8(t,j=254.0hz),41.8,38.9,33.7.
19
f nmr(376mhz,cdcl3)δ
–
126.7(d,j=53.6hz).ir(atr):2933,2844,1744,1603,1484,1402,1342,1103,1062,910,731cm-1
.hrms(esi,m/z):calcd for c
12h11
f2o-(m-h)-:209.0783;found:209.0784。
[0102]
实施例:46:
[0103]
3-(3,3-二氟-2-氧丙基)氮杂环丁烷-1-羧酸叔丁酯(简写为g16,结构式如下)的制备:
[0104][0105]
将69.2毫克1-(叔丁基)3-(1,3-二氧异吲哚-2-基)氮杂环丁烷-1,3-二羧酸酯,398.4毫克叔丁基((3,3-二氟丙-1-烯-2-基)氧基)二苯基硅烷,3.9毫克三(2-苯基吡啶)合铱,加入25到毫升的光反应管中,加入72毫克水和4毫升二甲基亚砜,橡胶塞封住,插入一个氮气球,液氮冻抽3次,反应置于蓝光(6w)下室温反应15小时。反应结束后,加入10毫升水,乙酸乙酯萃取,盐水洗涤,无水硫酸钠干燥,过滤,旋干(水浴大于45度),粗产品用石油醚/乙酸乙酯=3:1(v/v)柱层析,旋干即得产品g16(无色液体,28.4mg,产率57%)。1h nmr(400mhz,cdcl3)δ5.68(t,j=53.9hz,1h),4.16
–
4.10(m,2h),3.57
–
3.53(m,2h),3.05
–
2.99(m,2h),2.97
–
2.85(m,1h),1.42(s,9h).
13
c nmr(101mhz,cdcl3)δ198.3(t,j=26.9hz),156.1,109.6(t,j=252.8hz),79.6,40.4,28.3,23.2.
19
f nmr(376mhz,cdcl3)δ
–
126.7(d,j=53.5hz).ir(atr):2974,2885,1744,1672,1402,1252,1141,1066,861,775cm-1
.hrms(esi,m/z):calcd for c
12h11
f2nao
(m na)
:272.1069;found:272.1068。
[0106]
实施例47:
[0107]
3-((3r,5r,7r)-金刚烷-1-基)-1,1-二氟丙烷-2-酮(简写为g17,结构式如下)的制备:
[0108]
将65.0毫克1,3-二氧异异吲哚-2-基(3r,5r,7r)-金刚烷-1-羧酸酯,398.4毫克叔
丁基((3,3-二氟丙-1-烯-2-基)氧基)二苯基硅烷,3.9毫克三(2-苯基吡啶)合铱,加入25到毫升的光反应管中,加入72毫克水和4毫升二甲基亚砜,橡胶塞封住,插入一个氮气球,液氮冻抽3次,反应置于蓝光(6w)下室温反应24小时。反应结束后,加入30微升的三氟乙酸,室温搅拌10分钟,然后加入10毫升水,乙酸乙酯萃取,盐水洗涤,无水硫酸钠干燥,过滤,旋干,粗产品用石油醚柱层析,旋干即得产品g17(淡黄色色液体,28.7mg,产率63%)。1h nmr(400mhz,cdcl3)δ5.56(t,j=54.3hz,1h),2.40(d,j=1.7hz,2h),2.01
–
1.93(m,3h),1.74
–
1.61(m,12h).
13
c nmr(101mhz,cdcl3)δ199.2(t,j=25.8hz),109.8(t,j=255.0),48.8,42.2,36.6,33.8,28.5.
19
f nmr(376mhz,cdcl3)δ
–
126.7(d,j=54.7hz).ir(atr):2900,2848,1744,1454,1342,1144,1103,1059cm-1
.hrms(esi,m/z):calcd for c
13h17
f2o-(m-h)-:227.1253;found:227.1250。
[0109]
实施例48:
[0110]
1,1-二氟十六烷-2-酮(简写为g18,结构式如下)的制备:
[0111][0112]
将74.6毫克1,3-二氧异异吲哚-2-基十四烷酸酯,398.4毫克叔丁基((3,3-二氟丙-1-烯-2-基)氧基)二苯基硅烷,3.9毫克三(2-苯基吡啶)合铱,加入25到毫升的光反应管中,加入72毫克水和4毫升二甲基亚砜,橡胶塞封住,插入一个氮气球,液氮冻抽3次,反应置于蓝光(6w)下室温反应24小时。反应结束后,加入30微升的三氟乙酸,室温搅拌10分钟,然后加入10毫升水,乙酸乙酯萃取,盐水洗涤,无水硫酸钠干燥,过滤,旋干,粗产品用石油醚柱层析,旋干即得产品g18(白色固体,29.9mg产率57%)。1h nmr(400mhz,cdcl3)δ5.67(t,j=54.1hz,1h),2.70
–
2.61(m,2h),1.67
–
1.60(m,2h),1.26(s,22h),0.91
–
0.85(m,3h).
13
c nmr(101mhz,cdcl3)δ200.0(t,j=26.3hz),109.9(t,j=254.0hz),36.0,31.9,29.7,29.64,29.61,29.6,29.4,29.3,29.2,28.9,22.7,22.3,14.10.
19
f nmr(376mhz,cdcl3)δ
–
126.8(d,j=53.8hz).ir(atr):2915,2851,1741,1469,1402,1349,1264,1159,1103,1062,999cm-1
.hrms(esi,m/z):calcd for c
16h29
f2o-(m-h)-:275.2192;found:275.2193。
[0113]
实施例49:
[0114]
1,1-二氟十六烷-2-酮(简写为g19,结构式如下)的制备:
[0115][0116]
将79.8毫克1,3-二氧代异吲哚-2-基4-([[1,1'-联苯]-4-基)-4-氧代丁酸酯,398.4毫克叔丁基((3,3-二氟丙-1-烯-2-基)氧基)二苯基硅烷,3.9毫克三(2-苯基吡啶)合铱,加入25到毫升的光反应管中,加入72毫克水和4毫升二甲基亚砜,橡胶塞封住,插入一个氮气球,液氮冻抽3次,反应置于蓝光(6w)下室温反应24小时。反应结束后,加入10毫升水,乙酸乙酯萃取,盐水洗涤,无水硫酸钠干燥,过滤,旋干,粗产品用石油醚/乙酸乙酯=5:1(v/v)柱层析,旋干即得产品g19(白色固体,42.9mg,产率71%)。1h nmr(400mhz,cdcl3)δ8.10
–
7.99(m,2h),7.74
–
7.60(m,4h),7.51
–
7.45(m,2h),7.43
–
7.38(m,1h),5.73(t,j=
54.0hz,1h),3.09(t,j=7.0hz,2h),2.87
–
2.83(m,2h),2.16
–
2.09(m,1h).
13
c nmr(151mhz,cdcl3)δ199.6(t,j=26.1hz),198.7,145.9,139.8,135.3,129.0,128.6,128.3,127.3,127.2,109.8(t,j=252.8hz),36.9,35.3,16.8.
19
f nmr(376mhz,cdcl3)δ
–
126.9(d,j=55.1hz).ir(atr):2933,2889,1741,1677,1603,1487,1405,1275,1107,753cm-1
.hrms(esi,m/z):calcd for c
18h17
f2o
2
(m h)
:303.1191;found:303.1185。
[0117]
实施例50:
[0118]
(5s,8r,9s,10s,13r,16r)-16-(((s)-7,7-二氟-6-氧庚烷-2-基)-10,13-二甲基十二氢化-3h-环戊[a]菲-3,7,12(2h,4h)-三酮(简写为g20,结构式如下)的制备:
[0119][0120]
将109.4毫克1,3-二氧异吲哚-2-基(5s)-5-(((5s,8r,9s,10s,13r,16r)-10,13-二甲基-3,7,12-三氧十六烷基-1h-环戊[a]菲蒽-16-基)己酸酯,398.4毫克叔丁基((3,3-二氟丙-1-烯-2-基)氧基)二苯基硅烷,3.9毫克三(2-苯基吡啶)合铱,加入25到毫升的光反应管中,加入72毫克水和4毫升二甲基亚砜,橡胶塞封住,插入一个氮气球,液氮冻抽3次,反应置于蓝光(6w)下室温反应24小时。反应结束后,加入30微升的三氟乙酸,室温搅拌10分钟,然后加入10毫升水,乙酸乙酯萃取,盐水洗涤,无水硫酸钠干燥,过滤,旋干,粗产品用石油醚/乙酸乙酯=2:1(v/v)柱层析,旋干即得产品g20(白色固体,39.2mg,产率44%)。1h nmr(400mhz,cdcl3)δ5.67(t,j=54.1hz,1h),2.96
–
2.80(m,3h),2.67
–
2.60(m,2h),2.42
–
1.93(m,13h),1.88
–
1.51(m,4h),1.40(s,3h),1.30
–
1.22(m,4h),1.07(s,3h),0.86(d,j=6.6hz,3h).
13
c nmr(101mhz,cdcl3)δ212.0,209.1,208.8,199.9(t,j=26.3hz),109.9(t,j=254.0hz),56.8,51.7,49.0,46.8,45.6,45.5,45.0,42.8,38.6,36.5,36.3,36.0,35.9,35.2,34.7,27.7,25.1,21.9,19.5,18.8,11.8.
19
f nmr(376mhz,cdcl3)δ
–
126.8(d,j=54.1hz).ir(atr):2960,1752,1703,1461,1390,1301,1275,1088,999,738cm-1
.hrms(esi,m/z):calcd for c
26h36
f2o
4
(m h)
:451.2654;found:451.2657。
[0121]
实施例51:
[0122]
1-氟-5-(4-氟苯基)戊烷-2-酮(简写为g21,结构式如下)的制备:
[0123][0124]
将62.6毫克1,3-二氧代异吲哚啉-2-基4-(4-氟苯基)-4-氧代丁酸酯,376.8毫克叔丁基((3-氟丙-1-烯-2-基)氧基)二苯基硅烷,3.9毫克三(2-苯基吡啶)合铱,加入25到毫升的光反应管中,加入72毫克水和4毫升二甲基亚砜,橡胶塞封住,插入一个氮气球,液氮冻抽3次,反应置于蓝光(6w)下室温反应15小时。反应结束后,加入30微升的三氟乙酸,室温搅拌10分钟,加入10毫升水,乙酸乙酯萃取,盐水洗涤,无水硫酸钠干燥,过滤,旋干,粗产品用石油醚/乙酸乙酯=50:1(v/v)柱层析,旋干即得产品g21(无色液体,28.5mg,产率70%)。1h nmr(400mhz,cdcl3)δ8.02
–
7.87(m,2h),7.19
–
7.04(m,2h),5.71(t,j=54.0hz,1h),3.03(t,j=6.9hz,2h),2.82(t,j=6.9hz,2h),2.12
–
2.05(m,2h).
13
c nmr(101mhz,cdcl3)δ
199.5(t,j=26.3hz),197.5,165.8(d,j=255.0hz),133.1(d,j=3.1hz),130.6(d,j=9.4hz),115.7(d,j=21.9hz),109.7(t,j=252.8hz),36.8,35.2,16.7.
19
f nmr(376mhz,cdcl3)δ
–
99.2
––
109.5(m,1f),
–
127.0(d,j=53.6hz,2f).ir(atr):3079,2963,1744,1637,1595,1507,1409,1372,1241,1163,1096cm-1
.gc-ms(ei,m/z):calcd for c
11h12
f2o(m):198.09;found:198.11。
[0125]
实施例52:
[0126]
1,1,1-三氟-5-(4-氟苯基)戊烷-2-酮(简写为g22,结构式如下)的制备:
[0127][0128]
将62.6毫克1,3-二氧代异吲哚啉-2-基4-(4-氟苯基)-4-氧代丁酸酯,420.0毫克叔丁基((3-氟丙-1-烯-2-基)氧基)二苯基硅烷,3.9毫克三(2-苯基吡啶)合铱,加入25到毫升的光反应管中,加入72毫克水和4毫升二甲基亚砜,橡胶塞封住,插入一个氮气球,液氮冻抽3次,反应置于蓝光(6w)下室温反应15小时。反应结束后,加入30微升的三氟乙酸,室温搅拌10分钟,加入10毫升水,乙酸乙酯萃取,盐水洗涤,无水硫酸钠干燥,过滤,旋干,粗产品用石油醚/乙酸乙酯=50:1(v/v)柱层析,旋干即得产品g22(无色液体,14.2mg,产率30%)。1h nmr(400mhz,cdcl3)δ7.16
–
7.08(m,2h),7.03
–
6.95(m,2h),2.68(dt,j=26.5,7.4hz,4h),1.99(p,j=7.3hz,2h).
19
f nmr(376mhz,cdcl3)δ
–
79.2(s,1f),
–
116.8(dq,j=8.9,4.5hz).hrms(esi,m/z):calcd for c
11
h9f4o-(m-h)-:223.0595;found:223.0595。
[0129]
实施例53:
[0130]
1,1-二氟-5-(4-氟苯基)-3-甲基戊烷-2-酮(简写为g23,结构式如下)的制备:
[0131][0132]
将62.6毫克1,3-二氧代异吲哚啉-2-基4-(4-氟苯基)-4-氧代丁酸酯,376.8毫克叔丁基((3-氟丙-1-烯-2-基)氧基)二苯基硅烷,3.9毫克三(2-苯基吡啶)合铱,加入25到毫升的光反应管中,加入72毫克水和4毫升二甲基亚砜,橡胶塞封住,插入一个氮气球,液氮冻抽3次,反应置于蓝光(6w)下室温反应15小时。反应结束后,加入30微升的三氟乙酸,室温搅拌10分钟,加入10毫升水,乙酸乙酯萃取,盐水洗涤,无水硫酸钠干燥,过滤,旋干,粗产品用石油醚/乙酸乙酯=50:1(v/v)柱层析,旋干即得产品g23(无色液体,2.5mg,产率5%)。gc-ms(ei,m/z):calcd for c
12h13
f3o(m):230.09;found:230.37。
[0133]
实施例54:
[0134]
6-溴-1,1-二氟己烷-2-酮(简写为g24,结构式如下)的制备:
[0135][0136]
将62.0毫克1,3-二氧异异吲哚-2-基4-溴丁酸酯,398.4毫克叔丁基((3,3-二氟
丙-1-烯-2-基)氧基)二苯基硅烷,3.9毫克三(2-苯基吡啶)合铱,加入25到毫升的光反应管中,加入72毫克水和4毫升二甲基亚砜,橡胶塞封住,插入一个氮气球,液氮冻抽3次,反应置于蓝光(6w)下室温反应15小时。反应结束后,加入30微升的三氟乙酸,室温搅拌10分钟,加入10毫升水,乙酸乙酯萃取,盐水洗涤,无水硫酸钠干燥,过滤,旋干,粗产品用石油醚/乙酸乙酯=50:1(v/v)柱层析,旋干即得产品g24(无色液体,16.4mg,产率38%)。1h nmr(400mhz,cdcl3)δ5.69(t,j=54.0hz,1h),3.42(t,j=6.4hz,2h),2.75
–
2.65(m,2h),1.97
–
1.75(m,4h).
19
f nmr(376mhz,cdcl3)δ
–
126.7(d,j=53.7hz)。
[0137]
实施例55:
[0138]
7-(2,5-二甲基苯氧基)-1,1-二氟-4,4-二甲基庚烷-2-酮(简写为g25,结构式如下)的制备:
[0139][0140]
将79.0毫克1,3-二氧异吲哚-2-基5-(2,5-二甲基苯氧基)-2,2-二甲基戊酸酯,398.4毫克叔丁基((3,3-二氟丙-1-烯-2-基)氧基)二苯基硅烷,3.9毫克三(2-苯基吡啶)合铱,加入25到毫升的光反应管中,加入72毫克水和4毫升二甲基亚砜,橡胶塞封住,插入一个氮气球,液氮冻抽3次,反应置于蓝光(6w)下室温反应15小时。反应结束后,加入30微升的三氟乙酸,室温搅拌10分钟,加入10毫升水,乙酸乙酯萃取,盐水洗涤,无水硫酸钠干燥,过滤,旋干,粗产品用石油醚/乙酸乙酯=50:1(v/v)柱层析,旋干即得产品g25(淡黄色液体,17.1mg,产率29%)。1h nmr(400mhz,cdcl3)δ7.05
–
6.98(m,1h),6.69
–
6.60(m,2h),5.59(t,j=54.3hz,1h),3.93(t,j=6.3hz,2h),2.60(t,j=1.4hz,2h),2.31(s,3h),2.18(s,3h),1.80
–
1.72(m,2h),1.59
–
1.53(m,2h),1.08(s,6h).
19
f nmr(376mhz,cdcl3)δ-126.5(d,j=53.8hz)。
[0141]
实施例56:
[0142]
1,1-二氟-3-(1-甲基环己基)丙-2-酮(简写为g26,结构式如下)的制备:
[0143][0144]
将57.4毫克1,3-二氧杂多林-2-基-1-甲基环己烷-1-羧酸酯,398.4毫克毫克叔丁基((3,3-二氟丙-1-烯-2-基)氧基)二苯基硅烷,3.9毫克三(2-苯基吡啶)合铱,加入25到毫升的光反应管中,加入72毫克水和4毫升二甲基亚砜,橡胶塞封住,插入一个氮气球,液氮冻抽3次,反应置于蓝光(6w)下室温反应15小时。反应结束后,加入30微升的三氟乙酸,室温搅拌10分钟,加入10毫升水,乙酸乙酯萃取,盐水洗涤,无水硫酸钠干燥,过滤,旋干,粗产品用石油醚/乙酸乙酯=50:1(v/v)柱层析,旋干即得产品g26(无色液体,10.6mg,产率28%)。gc-ms(ei,m/z):calcd for c
10h16
f2o(m):190.12;found:189.93。
[0145]
实施例57:
[0146]
4-乙基-1,1-二氟辛烷-2-酮(简写为g27,结构式如下)的制备:
[0147][0148]
将57.8毫克1,3-二氧异异吲哚-2-基-2-乙基己酸酯,398.4毫克毫克叔丁基((3,3-二氟丙-1-烯-2-基)氧基)二苯基硅烷,3.9毫克三(2-苯基吡啶)合铱,加入25到毫升的光反应管中,加入72毫克水和4毫升二甲基亚砜,橡胶塞封住,插入一个氮气球,液氮冻抽3次,反应置于蓝光(6w)下室温反应15小时。反应结束后,加入30微升的三氟乙酸,室温搅拌10分钟,加入10毫升水,乙酸乙酯萃取,盐水洗涤,无水硫酸钠干燥,过滤,旋干,粗产品用石油醚/乙酸乙酯=50:1(v/v)柱层析,旋干即得产品g27(淡黄色液体,10.9mg,产率31%)。1h nmr(400mhz,cdcl3)δ5.64(t,j=54.2hz,1h),2.57(dq,j=6.2,1.1hz,2h),1.94(p,j=6.1hz,1h),1.40
–
1.20(m,8h),0.86(dt,j=10.8,7.2hz,6h).
19
f nmr(376mhz,cdcl3)δ-126.72(d,j=53.9hz)。
[0149]
氟烷基酮的应用:
[0150]
应用1:合成含氟吡啶类化合物
[0151][0152]
在惰性气体保护下,向干燥并装有磁力搅拌子的10.0ml反应管中加入45.2毫克6,6-二氟-1-苯基己烷-1,5-二酮,46.2毫克的醋酸铵,1ml醋酸,封紧封管,然后在120℃下加热过夜。然后冷却到室温,饱和碳酸氢钠调制中性,乙酸乙酯萃取,盐水洗涤,无水硫酸钠干燥,过滤,旋干,粗产品用石油醚/乙酸乙酯=50:1(v/v)柱层析,旋干即得产品2-(二氟甲基)-6-苯基吡啶(淡黄色液体,产率65%)。1h nmr(400mhz,cdcl3)δ8.06
–
7.99(m,2h),7.95
–
7.80(m,2h),7.60
–
7.58(dd,j=7.5,1.1hz,1h),7.54
–
7.41(m,3h),6.71(t,j=55.6hz,1h).
13
c nmr(151mhz,cdcl3)δ157.2,152.8(t,j=26.1hz),138.3,138.0,129.5,128.8,127.0,122.0(t,j=1.5hz),118.2(t,j=2.8hz),114.3(t,j=240.3hz).
19
f nmr(376mhz,cdcl3)δ
–
115.2(d,j=56.4hz).ir(atr):3064,2926,2851,1729,1584,1453,1357,1114,1040,760.hrms(esi,m/z):calcd for c
12h10
f2n
(m h)
:206.0776;found:206.0774。
[0153]
以上所述是本发明的优选实施方式而已,当然不能以此来限定本发明之权利范围,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和变动,这些改进和变动也视为本发明的保护范围。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。