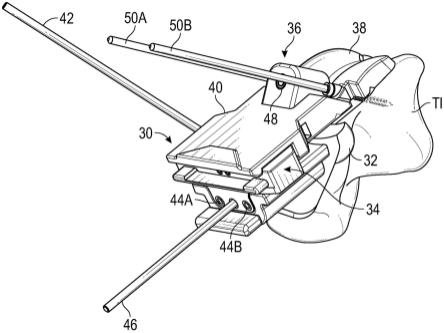
1.本发明的目的是一种新的氢化可的松半琥珀酸盐冻干物及其在制备用于预防或治疗早产儿支气管肺发育不良的静脉内或肠胃外注射溶液中的用途。
背景技术:
2.支气管肺发育不良(bpd)是一种慢性肺部疾病,常见于低出生体重的早产儿或极早产儿(即闭经不足32周的期限),并且作为急性呼吸窘迫综合征的一部分需要机械通气。它是早产儿或极早产儿的主要并发症之一,也是死亡和发病的主要原因之一。
3.在极早产儿中,肺泡的发育不完全,最轻微的攻击都可能会改变其成熟。这种情况在羊水感染期间尤为明显。
4.在早产儿中,它是新生儿死亡或神经系统后遗症的危险因素。儿童期发生呼吸系统问题的风险也会增加。通气功能可能受损,甚至在成年期也是如此。
5.静脉内施用皮质类固醇可降低早产儿或极早产儿发生支气管肺发育不良的风险。然而,要施用的低剂量通常需要对市场上的溶液进行高度稀释。在注射前制备溶液的这一步骤具有剂量错误或注射溶液的微生物污染的重大风险。
6.为了限制这些风险,欧洲药品管理局(ema)发布的关于用于儿科使用的药物开发的指令ema/chmp/qwp/805880/2012rev.2建议通过开发含有适当浓度的活性成分的制剂来避免这些稀释。
7.氢化可的松半琥珀酸盐,又称为氢化可的松琥珀酸氢、氢琥珀酸氢化可的松或简称氢化可的松琥珀酸盐,是一种合成皮质类固醇,作为治疗新生儿急性肾上腺功能不全、短暂性肾上腺功能不全和先天性肾上腺增生伴失盐综合征(debre-fibiger综合征)的药物在世界上许多国家销售。
8.由于氢化可的松和琥珀酸盐之间的酯键不稳定,这种活性成分在水性介质中会快速水解,以至于目前以含有100mg或500mg氢化可的松的冻干粉(或冻干物)和重构溶液的形式销售。
9.尽管如此,在预防或治疗早产儿或极早产儿支气管肺发育不良的背景下限定的剂量为头7天0.5mg氢化可的松/kg/12小时,然后接下来的3天0.5mg氢化可的松/kg/24小时,需要将从含有100mg氢化可的松的冻干物和重构溶液(2ml)重构后获得的溶液稀释50倍(使用5%葡萄糖溶液)以施用它。
10.在本发明之日,尚无能够以上述剂量和体积将氢化可的松静脉内(或肠胃外)施用于早产儿或极早产儿的制剂,所述制剂可通过简单地添加重构溶液而重构,而无需随后稀释。
11.因此,人们认识到需要这种组合物。然而,这种组合物的开发是非常复杂的。事实上,众所周知,冻干是一种复杂的方法,其中必须考虑几个参数以保证产品的一致性。尽管这种方法可以显著提高不稳定产品在水性介质中的稳定性,但必须特别注意配方的选择。特别是,配方中的ph、赋形剂的性质和用量等参数对最终制备的冻干物的稳定性有非常显
著的影响。此外,可获得关于不同赋形剂对活性药物成分稳定性的影响的相互矛盾的信息,这使得无法确定冻干物的结构与其稳定性之间的关系,更重要的是,取决于赋形剂的性质和比例,其组合可能会出乎意料地影响冻干物的稳定性。最后,在冻干物含有少(甚至非常少)量的活性成分的情况下,上述困难进一步增加。实际上,冻干物中低(甚至非常低)量的活性成分以大量填充剂的存在为前提,因此在开发稳定且易于重构的制剂方面存在额外困难。
12.然而,以一种完全出乎意料的方式发现,使用特定的填充剂与添加一定量的缓冲剂相结合,可以制备一种含有少(甚至非常少)量氢化可的松半琥珀酸盐的冻干物,这种冻干物随着时间的推移是稳定的,并且易溶于少量重构溶液,以制备可通过静脉内或肠胃外向早产儿或极早产儿注射的溶液。
技术实现要素:
13.因此,本发明的主题是用于制备静脉内或肠胃外注射溶液的冻干粉,所述冻干粉包括:
[0014]-1%至30%的氢化可的松半琥珀酸盐;
[0015]-40%至98%的填充剂,所述填充剂选自甘露糖醇、海藻糖、乳糖、蔗糖、棉子糖或山梨糖醇;
[0016]-1%至30%的缓冲剂。
[0017]
根据本发明的冻干粉在保持在5℃时随着时间的推移是稳定的,即使在保持在室温时也是如此。此外,它允许制备用于早产(甚至极早产)婴儿静脉内或肠胃外注射的溶液,以通过简单的重构来预防和治疗支气管肺发育不良,而无需随后稀释。
[0018]
在本发明的背景中:
[0019]
‑“
冻干粉”或“冻干物”是指任何含水量低于8%、优选低于5%以及通过任何允许达到该湿度水平的方法(特别是冻干)制备的粉末或干粉;
[0020]
‑“
氢化可的松半琥珀酸盐”是指11β,17α,21-三羟基孕甾-4-烯-3,20-二酮21-半琥珀酸盐(11β,17α,21-trihydroxypregn-4-ene-3,20-dione 21-hemisuccinate),cas编号为2203-97-6(一水合物形式)或83784-20-7(无水形式),化学结构如下:
[0021][0022]
以及其药学上可接受的盐(特别是其钠盐);
[0023]-活性成分的“药学上可接受的盐”是指所述活性成分与无机酸或有机酸在有机溶剂或水性溶剂(如醇、酮、醚或含氯溶剂)中在这种酸的作用下的任何加成盐,并且是药学上可接受的;和
[0024]
‑“
缓冲剂”是指允许将溶液的ph维持在稳定值( /-1,优选 /-0.5)的任何化合物
或化合物的组合。作为缓冲剂的实例,可以特别提及柠檬酸盐、磷酸盐、tris、组氨酸和hepes以及相关的盐。
[0025]
此外,在本发明的背景中,除非另有说明,否则以%表示的比例对应于相对于所考虑实体的总重量的质量百分比。
[0026]
因此,本发明的一个目的是包含如上定义的少(甚至非常少)量氢化可的松半琥珀酸盐、填充剂和缓冲剂的冻干粉。优选地,本发明的一个目的是如上定义的具有以下单独或组合考虑的特征的冻干粉:
[0027]-冻干粉含有2%至20%的氢化可的松半琥珀酸盐,更优选5%至15%的氢化可的松半琥珀酸盐,最优选8%至12%的氢化可的松半琥珀酸盐;
[0028]-填充剂选为甘露糖醇或海藻糖,更优选填充剂选为海藻糖;
[0029]-冻干粉含有50%至95%的填充剂,优选60%至90%的填充剂,最优选75%至85%的填充剂;
[0030]-缓冲剂选为磷酸盐或其盐之一,优选缓冲剂选为钠盐形式的磷酸盐,最优选缓冲剂选为磷酸一钠和磷酸二钠的混合物;
[0031]-冻干粉含有2%至20%的缓冲剂,优选5%至15%的缓冲剂,最优选8%至12%的缓冲剂;
[0032]-冻干粉还含有一种或多种允许调节ph的化合物,例如氢氧化钠或正磷酸。
[0033]
根据本发明的冻干粉可以根据本领域技术人员常规使用的任何方法制备。作为用于制备如上定义的冻干粉的方法的实例,可以特别提及包括以下步骤的方法:
[0034]-在室温下添加缓冲剂,所述缓冲剂的量为冻干前制备溶液所需的总水量的70%(v/v)至90%(v/v);
[0035]-添加氢化可的松半琥珀酸盐;
[0036]-将溶液的ph调节至7.0到8.0之间变化的值,优选7.0至7.4;
[0037]-添加填充剂;
[0038]-添加剩余的必要水;
[0039]-过滤溶液;
[0040]-将获得的溶液冻干。
[0041]
因此,可以通过简单地添加重构溶液将根据本发明的冻干粉用于制备用于早产儿或极早产儿静脉内或肠胃外注射的溶液。
[0042]
因此,本发明还涉及如上定义的冻干粉在制备用于早产儿或极早产儿静脉内或肠胃外注射的溶液中的用途。
[0043]
本发明还涉及用于制备用于早产儿或极早产儿静脉内或肠胃外注射的溶液的试剂盒,所述试剂盒包括:
[0044]-如前定义的冻干粉;和
[0045]-重构溶液。
[0046]
优选地,根据本发明的试剂盒具有以下单独或组合考虑的特征:
[0047]-试剂盒含有1mg至50mg的冻干粉,优选5mg至30mg的冻干粉,更优选10mg至20mg的冻干粉,最优选13mg的冻干粉;
[0048]-试剂盒含有0.1ml至10ml的重构溶液,优选0.2ml至5ml的重构溶液,更优选0.5ml
至2ml的重构溶液,最优选1ml的重构溶液;和/或
[0049]-重构溶液选为水或水和渗透剂的混合物,优选水和葡萄糖的混合物。
[0050]
因此,从根据本发明的试剂盒获得的静脉内或肠胃外注射溶液可以立即注射到早产(或极早产)婴儿中,用于预防或治疗支气管肺发育不良。因此,本发明还涉及从上述试剂盒获得的可注射溶液,用于预防或治疗早产儿或极早产儿支气管肺发育不良。
[0051]
最后,本发明还涉及用于预防或治疗早产儿或极早产儿支气管肺发育不良的方法,包括向所述儿童施用由上述试剂盒制备的溶液。
[0052]
本发明通过以下实施例进行说明,但不限于此。
具体实施方式
[0053]
实施例1-根据本发明的冻干粉的制备
[0054]
1.1冻干物l1
[0055]
根据下述方法制备冻干粉l1,其组成记载于下表1中。
[0056]
表1
–
冻干物l1
[0057]
成分%(w/w)氢化可的松半琥珀酸盐10.5%海藻糖(填充剂)79%磷酸钠(缓冲剂)1%磷酸二钠(缓冲剂)9.5%氢氧化钠(ph调节)适量至目标ph正磷酸(ph调节)适量至目标ph
[0058]
将0.23g磷酸钠和2.41g磷酸二钠溶于800ml水中,制成可在室温下注射的制剂。搅拌并完全溶解后,加入2.66g氢化可的松半琥珀酸盐,同时继续搅拌。将ph调节至7.4,直到活性成分完全溶解。然后将20g海藻糖加入溶液中。溶解所有粉末,将ph调节至目标,即7.0 /-0.1,并将水位加到1l。
[0059]
然后根据下表2中记载的循环进行冻干。
[0060]
表2
–
冻干循环
[0061]
编号步骤温度压力持续时间1冷冻-45℃大气压1小时2退火-25℃大气压5小时3初级干燥-30℃70μbar44小时4二次干燥 30℃25μbar10小时5限制在氮气中 5℃50mbarn/a
[0062]
1.2冻干物l2
[0063]
根据上述实施例1.1中描述的方法制备冻干粉l2,其组成记载于表3中。
[0064]
表3
–
冻干物l2
[0065]
成分%(w/w)氢化可的松半琥珀酸盐17.4%
甘露糖醇(填充剂)65.4%磷酸钠(缓冲剂)1.6%磷酸二钠(缓冲剂)15.7%氢氧化钠(ph调节)适量至目标ph正磷酸(ph调节)适量至目标ph
[0066]
1.3对照
[0067]
根据上述实施例1.1中描述的方法制备所谓的对照冻干粉“l
ref.”,其组成记载于表4中。
[0068]
表4
–
对照冻干物l
ref.
[0069]
成分%(w/w)氢化可的松半琥珀酸盐2%葡萄糖(填充剂)97%磷酸二钠(缓冲剂)1%盐酸适量至目标ph氢氧化钠适量至目标ph
[0070]
2.注射溶液的重构
[0071]
通过将1ml水/葡萄糖重构溶液(4.5/95.5)添加到含有1mg氢化可的松的冻干物(l1、l2或l
ref.
)中来进行注射溶液的重构。由此获得1ml 1mg/ml的氢化可的松溶液。
[0072]
对于冻干物l1和l2,在轻微搅拌小瓶以使溶液均化后立即进行重构。因此,重构没有任何困难,并且与目前市场上不含填充剂的冻干粉一样容易进行。
[0073]
然后可以使用注射器和针头或注射器和转移装置取出溶液进行注射,而无需进一步稀释。因此,与目前市场上的产品相比,可能导致剂量错误的计算或操作错误的风险以及微生物污染的风险大大降低。
[0074]
相反,对于冻干物l
ref.
,无论储存温度如何,都有明显的塌陷趋势,这使得重构更加困难。因此,当冻干物储存在5℃时,重构时间约为30秒,而当冻干物储存在25℃或40℃时,重构时间可长达150秒。此外,无论储存温度如何,这种明显的塌陷趋势揭示了冻干物随时间的不稳定性。
[0075]
3.冻干物的稳定性
[0076]
冻干物l1和l2储存在5℃、25℃的温度下和40℃的加速稳定性条件下。在t0、t0 1个月、t0 2个月和t0 3个月进行旨在确定杂质(即游离氢化可的松)水平以及因此制剂的物理化学稳定性的分析。
[0077]
结果记载于下表5中。
[0078]
表5
–
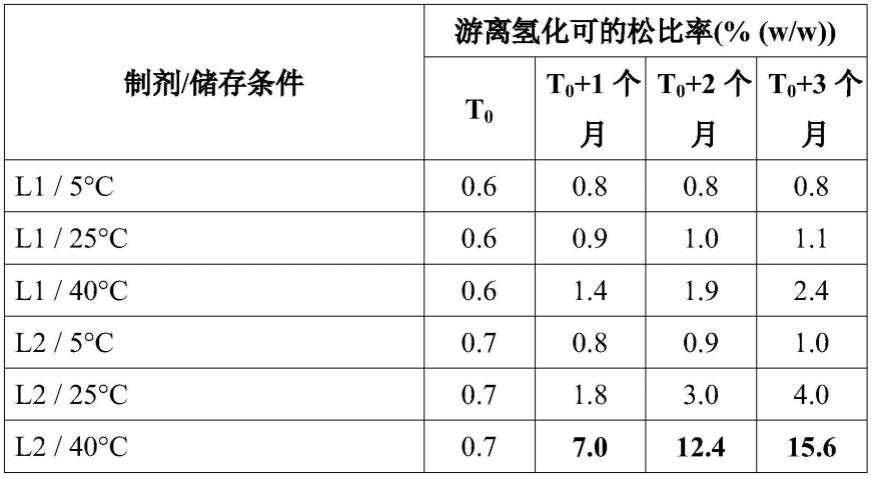
制剂l1和l2在t0、t0 1个月、t0 2个月和t0 3个月在5℃、25℃和40℃下的游离氢化可的松杂质的演变
[0079][0080]
允许的杂质限度比为6.7%(w/w)。
[0081]
应注意,在5℃和25℃在t0 3个月储存时,冻干物l1和l2是稳定的。即使在40℃的加速储存条件下储存,冻干物l1仍保持稳定。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。