1.本发明属于天然高分子技术领域,特别涉及一类桔霉素二聚体化合物及其制备方法和应用。
背景技术:
2.桔霉素(citrinin)是一种著名的聚酮类真菌毒素,最早是1931年从一株桔青霉penicillium citrinum中被分离得到。brown等在1948年首先提出桔霉素的平面结构,随后的研究阐明了桔霉素的绝对构型和互变异构现象(见式一)。桔霉素单体本身是一种著名的粮食污染物,许多报道证实它对牛、羊等牲畜具有肾毒性以及多种其他的慢性毒性,许多研究者试图通过热降解法减低其毒性的报道。同时桔霉素也具有抗菌、抗癌和抗氧化等广泛的生理活性。
[0003][0004]
由于桔霉素自身的不稳定性,其可在中性溶剂(甲醇、水)、酸性或碱性溶剂中发生结构改变。到目前为止桔霉素先后从青霉属、曲霉属及红曲霉属真菌中得到。然而关于桔霉素二聚体及多聚体的报道绝大多数来源于青霉属,仅有一株曲霉菌的报道。目前共有38个天然来源的桔霉素二聚体2分三聚体的报道,结构类型主要涉及氧原子参与的diels-alder型二聚体类、c7-c7碳桥接型二聚体、其他类型杂合二聚体和三聚体类。
[0005]
一、diels-alder型二聚体类:
[0006]
clark等在2006年推测一个o-quinone型桔霉素单体与p-quinone型桔霉素发生diels-alder反应后再经过脱羧,氧化还原,开环,水解等反应形成7,1
′‑
链接-8,8
′‑
氧桥接型二聚体。目前文献共报道此类结构22个该类型桔霉素二聚结构。除此外此类结构中常常一个桔霉素单体的吡喃环由于脱羧、关环等反应可以转化为呋喃环或者开链结构。
[0007][0008]
1973年首次得到桔霉素二聚体citrinin h1(化合物1,见式二),将桔霉素在水溶液中100℃加热30min得到产物。研究报道citrinin h1能够使诱导型一氧化氮合成和环氧合酶-2基因表达的降低,从而抑制脂多糖刺激的bv2小胶质细胞中一氧化氮和前列腺素e2的产生。此外,它还可抑制抑制剂κb-α的磷酸化,阻断核因子κb的核移位,降低p38丝裂原活化蛋白激酶的活性。随后从海洋来源的一株桔青霉真菌nlg-s01-p1中分离得到1-epi-citrinin h1(化合物2),该化合物对耐甲氧西林金黄色葡萄球菌具有抑菌作用。
[0009]
二、7,7'-碳桥接型二聚体
[0010]
目前文献只报道了7个7,7'-碳桥接型桔霉素二聚体,均来源于海洋青霉属真菌,其药理活性良好。从青霉属菌株p.citrinum中分离得到dicitrinones a-d(见式三),提出连接两个桔霉素单元的碳桥是来源于c-7上的羧基碳经脱羧、脱水、还原,与短链脂肪酸缩合等反应后得到,并推测该类化合物引入烷基侧链后由于其阻遏作用导致碳谱信号出现两组。但andrey等提出可能存在烯醇互变异构现象,并提出生物合成途径的假设。
[0011][0012]
三、其他类型桔霉素二聚体及三聚体
[0013]
除了桔霉素二聚体外,文献目前已报道了桔霉素杂合二聚体,主要为桔霉素与苯环、蒽醌、苄基取代、香豆素等结构连接。
[0014]
目前得到的桔霉素二聚体及多聚体普遍认为是在发酵物后续处理过程中得到的人工产物。
技术实现要素:
[0015]
为了克服上述现有技术的缺点与不足,本发明的首要目的在于提供一类桔霉素二聚体化合物。本发明化合物均由微生物分离得到,为天然产物。
[0016]
本发明的另一目的在于提供上述桔霉素二聚体化合物的制备方法。
[0017]
本发明的再一目的在于提供上述桔霉素二聚体化合物在制备抗菌药物领域中的
应用。本发明的桔霉素二聚体化合物具有优异的抗菌活性。
[0018]
本发明的目的通过下述方案实现:
[0019]
一类桔霉素二聚体化合物,为如下所示结构式中的一种:
[0020][0021][0022]
一种制备桔霉素二聚体化合物的方法,包括以下步骤:
[0023]
(一)当结构式为化合物
ⅰ‑
化合物viii时:
[0024]
将海洋来源真菌penicillium sp.ggf16-1-2gdmcc no:61080在液体培养基中进行发酵培养,所得发酵液用乙酸乙酯萃取,浓缩,得到发酵液etoac相浸膏;用硅胶柱层析进行分离,以体积比为100:0-0:100的石油醚/乙酸乙酯为洗脱液进行梯度洗脱,根据薄层层析结果区分合并,得到6个粗组分fr1-fr6;
[0025]
(1)选取v
pe
:v
etoac
=85:15-75:25的组分fr2进行sephdex lh-20柱层析,甲醇洗脱,薄层层析跟踪,得到fr2-1~fr2-5五个亚流份;
[0026]
对fr2-1亚流份进行hplc分离,流动相v
meoh
:v
水
=80:20,2.0ml/min,分离得到τr=56.960min的组分a和τr=49.143min的化合物
ⅴ
;对组分a再次进行hplc分离,流动相v
meoh
:v
水
=85:15,1.5ml/min,得到τr=48.960min的化合物ⅰ;
[0027]
对fr2-4亚流份进行hplc分离,流动相v
meoh
:v
水
=80:20,1.5ml/min,分离得到τr=
nobel公司。
[0047]
所述sephdex lh-20柱层析的参数为φ=3.0cm、l=200cm、lh-20(40-60μm)100g、高度160cm、柱体积300ml。
[0048]
所述发酵培养为本领域常规培养方法培养。
[0049]
所述发酵培养前优选为将菌株在pda培养基中进行活化。
[0050]
更具体的,所述活化可通过将菌种挑取到装有pda培养基的培养瓶中,置于28℃的恒温摇床(165r/min)中培养2天,获得种子液。250ml的培养瓶中,pda培养基的量优选为100ml。
[0051]
所述pda培养基的配方可为:每1l水中,马铃薯200g、葡萄糖20g、海盐35g。
[0052]
更具体的,所述在液体培养基中进行发酵培养可通过将已活化的种子液接种到液体培养基中,28℃室内静置培养60天。所述接种的量优选为1.5ml种子液/400ml液体培养基。优选为培养150l培养基。
[0053]
所述液体培养基的配方可为:每1l液体培养基中,麦芽糖40g、色氨酸5g、山梨醇50g、味精10g、kh2po
4 5g、mgso4·
7h2o 3g、酵母膏13g、陈海水余量,ph为6.5。
[0054]
(二)中,
[0055]
所述开放性ods柱层析的参数为400g,40-60μ,φ=5.5cm,l=43/62cm,柱体积800ml。
[0056]
所述hplc的色谱柱为pfp色谱柱:ace 10c-18-pfp,250mm
×
10mm。
[0057]
所述黄豆培养基的配方可为:50g(≧24目)黄豆粒、海盐33wt%、纯水85ml,ph自然。
[0058]
更具体的,所述在黄豆培养基中进行发酵培养可通过将已活化的种子液接种到黄豆培养基中,28℃室内静置培养45天。所述接种的量优选为5.0ml种子液/1l黄豆培养基,共培养10l。
[0059]
(一)中,所得的发酵液可通过加入甲醇进行灭活,更优选为400ml液体培养基中加入10-20ml甲醇进行灭活。灭活后过滤即可分离得到发酵液和菌丝体。
[0060]
所述发酵液优选由每150l浓缩至10l再进行萃取操作。
[0061]
所用乙酸乙酯优选与发酵液等体积;优选萃取3次。
[0062]
(二)中,所述浸泡提取所用乙酸乙酯的量优选为500ml每1l黄豆培养基。所述浸泡的时间优选为24h;优选浸泡提取3-5次,合并提取液。
[0063]
本发明的桔霉素二聚体化合物中,化合物i和化合ii为首个碳桥接型1位氧化的7-脱羧型桔霉素二聚体;化合物iii为首个碳桥接型1位为亚甲基的7-脱羧型桔霉素二聚体。
[0064]
本发明的桔霉素二聚体化合物具有优异的抑菌活性,可应用于制备抗菌药物领域中,特别是在制备防治木瓜炭疽病药物中的应用。
附图说明
[0065]
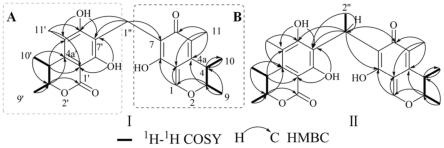
图1为化合物i和化合物ii的1h-1
h cosy和hmbc相关图。
[0066]
图2为化合物iii和化合物iv的1h-1
h cosy和hmbc相关图。
[0067]
图3为化合物v、化合物vi和化合物vii的cd曲线图。
具体实施方式
[0068]
下面结合实施例和附图对本发明作进一步详细的描述,但本发明的实施方式不限于此。下列实施例中涉及的物料若无特殊说明均可从商业渠道获得。所述方法若无特别说明均为常规方法。
[0069]
所述海洋来源真菌penicillium sp.ggf16-1-2从采自中国南海三亚东锣岛附近海域的16号海星样品分离得到,保藏于广东省微生物菌种保藏中心,简称gdmcc,地址:广州市先烈中路100号大院59号楼5楼广东省微生物研究所,保藏号为gdmcc no:61080,保藏日期:2020年7月7日。
[0070]
实施例1:桔霉素二聚体化合物的分离
[0071]
(1)菌株:penicillium sp.ggf16-1-2gdmcc no:61080。
[0072]
pda培养基:马铃薯200g、葡萄糖20g、海盐35g、纯水1l,ph自然;
[0073]
液体培养基:1l,麦芽糖40g、色氨酸5g、山梨醇50g、味精10g、kh2po45g、mgso4·
7h2o 3g、酵母膏13g、陈海水余量,ph为6.5;
[0074]
所述黄豆培养基的配方可为:50g(≧24目)黄豆粒、海盐33%、纯水85ml,ph自然。
[0075]
(2)菌种活化:用接种环从菌种管中挑取菌种到装有pda培养基的培养瓶中(100ml/250ml),将其放置于28℃的恒温摇床(165r/min)中培养2天,获得种子液。
[0076]
(3)接种:吸取已活化的种子培养液1.5ml至装有400ml液体培养基的1000ml培养瓶中,置于28℃的室内静置培养60天,共培养150l;
[0077]
或将已活化的种子培养液5.0ml至装有1l黄豆培养基的培养瓶中,置于28℃的室内静置培养45天,共培养10l。
[0078]
(4)提取:对装有液体培养基的每个培养瓶加10-20ml甲醇进行菌株灭活,纱布过滤,将发酵液和菌丝体分开;将得到的发酵液浓缩至10l,用等体积etoac萃取三次,得到的萃取液进行浓缩,最后得到发酵液etoac相浸膏;
[0079]
对装有黄豆培养基的培养瓶中加入500ml乙酸乙酯进行浸泡萃取,每次浸泡24h,浸泡3-5次,合并乙酸乙酯提取液,浓缩得到黄豆培养基etoac提取物(5.8g)。
[0080]
(5)分离:
[0081]
5-1:上述150l液体培养基中共获得etoac部位粗提物(发酵液etoac相浸膏111.9g)经硅胶柱层析(φ=10cm、l=110cm、硅胶h、165g拌样硅胶(高度7cm),装柱硅胶1.65kg(高度57cm)、柱体积3.85l)石油醚-乙酸乙酯体系洗脱(v
pe
:v
etoac
=100:0
→
0:100、1l/瓶),根据薄层tlc情况合并得到6个粗组分fr1-fr6。
[0082]
选择fr2(v
pe
:v
etoac
=85:15-75:25的组分)进行sephdex lh-20柱层析(φ=3.0cm、l=200cm、lh-20(40-60μm)、100g、高度160cm、柱体积300ml、纯甲醇洗脱),每次载样1.5g样品,25ml试管接液,tlc点板追踪,共得到fr2-1~fr2-5五个亚流份。其中,(展开剂v
pe
:v
etoac
=7:1)fr2-1(淡黄色溶液):tlc无明显斑点;fr2-2(深红色溶液):rf=0.1-0.45,254nm暗斑,365nm黄色斑点;fr2-3(亮黄色溶液):rf=0.3-0.8,254nm暗斑,365nm淡黄色斑点;fr2-4(黄色溶液):rf=0.3-0.9,254nm暗斑,365nm米黄
→
橙红色斑点(硫酸乙醇可显色);fr2-5(淡黄色溶液):rf=0.3-0.9,254nm暗斑,365nm黄色斑点。
[0083]
对fr2-1亚流份(339mg)进行hplc纯化(kromasil半制备色谱柱、10mm
×
250mm,5μm,瑞典akzo nobel公司),流动相v
meoh
:v
水
=80:20,2.0ml/min,分离得到τr=56.960min的组
1);6个甲基信号δ
h 1.14(3h,m,h-9)、1.19(3h,m,h-10)、1.97(3h,s,h-11)和1.31(3h,m,h-9
′
)、1.26(3h,m,h-10
′
)和2.11(3h,s,h-11
′
),δ
c 18.8(q,c-9)、20.1(q,c-10)、10.3(q,c-11)、19.8(q,c-9
′
)、18.2(q,c-10
′
)和10.6(q,c-11
′
);4个次甲基信号:δ
h 4.60(1h,q,6.4,h-3)、2.87(1h,q,7.2,h-4)、4.66(1h,q,6.8,h-3
′
)和2.95(1h,q,7.2,h-4
′
),δc80.4(d,c-3)、34.3(d,c-4)、80.6(d,c-3
′
)和30.6(d,c-4
′
);1个亚甲基信号δh3.71(2h,m,h-1”)和δc17.6/17.7(t,c-1
″
);3个活泼质子信号δ
h 12.20(1h,s,6'-oh)、12.88(1h,s,8'-oh)、8.94/9.10(1h,s,8-oh)。
13
c nmr中还显示存在1个共轭酮羰基(δ
c 187.8,s,c-6)、一个酯羰基[δ
c 169.5/169.6,s,c-1
′
)、3个连氧双键碳(δ
c 160.9(s,c-8)、162.8/162.9(s,c-6
′
)、157.6/157.7,(s,c-8
′
)]和8个四取代双键碳信息[δc136.1/136.3(s,c-4a)、126.1/126.2(s,c-5)、113.7/113.8,(s,c-7)、107.0/107.1(s,c-8a)、140.3(s,c-4a
′
)、116.7(s,c-5
′
)、111.9(s,c-7
′
)、98.6(s,c-8a
′
)]。表明其是一个不对称的桔霉素二聚体,且存在一个完整的7-脱羧桔霉素单体和一个1位氧化的7-脱羧桔霉素单体。
[0095]
hsqc对其nmr数据给予归属(见表1)。1h-1
h cosy给出两个片段(图1)和和hmbc给出δ
h 1.97(11-ch3)与δ
c 126.1/126.2(c-5)、187.8(c-6)、136.1/136.3(c-4a);δh2.87(h-4)与δc136.1/136.3(c-4a)、126.1/126.2(c-5)、107.0/107.1(c-8a);δh7.86(h-1)与δc107.0/107.1(c-8a)、136.1/136.3(c-4a)、34.3(c-4)、160.9(c-8);δ
h 1.97(8-oh)与δc160.9(c-8)、107.0/107.1(c-8a);δh4.60(h-3)与δc136.1/136.3(c-4a)、156.8/157.0(c-1);δh3.71(h-1
″
)与δc113.7/113.8(c-7)、187.8(c-6)、160.9(c-8)、111.9(c-7
′
)、162.8/162.9(c-6
′
)和157.6/157.7(c-8
′
);δh2.11(11
′‑
ch3)与δc116.7(c-5
′
)、162.8/162.9(c-6
′
)、140.3(c-4a
′
);δ
h 2.95(h-4
′
)与δc140.3(c-4a
′
)、116.7(c-5
′
)、98.6(c-8a
′
)的相关信息,说明化合物ⅰ中含有7-取代的脱羧桔霉素片段(图1中的a)和7-取代的脱羧且1位氧化的脱羧桔霉素片段(图1中的b),且二者有-ch
2-(c-1
″
)桥连。
[0096]
为了确定化合物ⅰ的相对构型,对其进行了noesy实验。在noesy实验中明显观察到δh1.19(h
3-10)与δh4.60(h-3)及δh1.26(h
3-10
′
)与δh4.66(h-3
′
)的相关,说明10-ch3与3-ch3、10
′‑
ch3与3
′‑
ch3均在异面。文献查阅确定桔霉素片段中c-3、c-4、c-3'、c-4'的绝对立体构型为3r、4s、3'r、4's。对化合物ⅰ进行旋光测试,其比旋光值为(c 0.10,meoh)。cd测试结果显示其在212nm、232nm以及275nm处为( )cotton效应,在331nm处为(-)cotton效应。与计算的3r、4s、3'r、4's的ecd相同,确定其绝对构型为3r、4s、3'r、4's。经scifinder检索以及文献调研发现该化合物未被报道,确定为新化合物,命名为dicitrinonee,为首个碳桥接型1位氧化的7-脱羧型桔霉素二聚体。
[0097]
表1化合物ⅰ和化合物ⅱ的nmr数据(cdcl3)
[0098][0099][0100]
注释:1h nmr(400mhz),
13
c nmr(100mhz),a表示重叠峰。
[0101]
(2)化合物ⅱ,橙黄色无定形粉末,正离子hresims给出的准分子离子峰m/z:455.2051[m h]
(计算值为m/z:455.2070[m h]
),确定其分子式为c
26h30
o7,不饱和度为12。紫外光谱中显示最大吸收波长为:202nm、280nm和320nm。红外光谱中显示有羟基(3259cm-1
)、羰基(1718cm-1
、1646cm-1
)以及苯环(1509cm-1
和1452cm-1
)基团。
[0102]
对比化合物ⅱ和ⅰ的nmr数据(见表1)二者极度相似,说明为同一类结构。唯一不同的是化合物ⅱ中的nmr图谱中亚甲基信号消失,出现一个甲基信号(δ
h 1.75,3h,m,h-2”;δc15.7/16.3,c-2
″
)和一个次甲基信息(δh4.66/4.89,1h,m,h-1”;δc,24.8/26.3,c-1
″
)。对比hmbc和1h-1
h cosy图谱的分析结果可知化合物ⅱ和ⅰ的平面结构类似,由桔霉素片段a和桔霉素片段b通过碳桥连接组成,只是在c-1”上增加了甲基取代(见图1)。
[0103]
与化合物ⅰ立体构型确定相同,化合物ⅱ通过noesy谱图以及文献查阅确定桔霉素片段中c-3、c-4、c-3'、c-4'的立体构型为3r、4s、3'r、4's。c-1”由于其距离c-3、c-4、c-3'和c-4'空间位置较远无法利用noesy、noe等确定其相对构型,亦无法确定该位置的立体构型。对其进行旋光测试以及cd实验,其比旋光值为(c 0.10,meoh)。cd测试结果显示在209以及279nm处为( )cotton效应,在332nm处为(-)cotton效应。经scifinder检索以及文献调研发现该化合物未被报道,确定为新化合物,命名为dicitrinonef。
[0104]
(3)化合物iii橙黄色胶状,正离子hresims给出的准分子离子峰m/z:427.2114[m h]
(计算值为m/z:427.2115[m h]
),确定其分子式为c
25h30
o6,不饱和度为11。紫外光谱中显示最大吸收波长为:280nm和343nm。
[0105]
当采用cdcl3溶剂对化合物ⅲ进行nmr测试(见表2),1h nmr谱图显示该化合物存在桔霉素结构片段a的特征信号以及3个甲基信号δ
h 1.12(3h,m,h-9')、1.18(3h,m,h-10')、2.13(3h,m,h-11'),2个次甲基信号δ
h 2.57(1h,m,h-4
′
)和δ
h 3.91(1h,q,6.4hz,h-3
′
)和1
6)、187.7/187.7(c-6')、116.5/116.6(c-7)、116.7/116.8(c-7')、163.4/164.0(c-8)和163.8/163.8(c-8')的hmbc相关信号,可知该片段链接在c-1
″
的位置,同时此次甲基δ
h 4.38/4.40(h-1”)又将两个桔霉素片段a通过c-7/7
′
连接起来(见图2)。
[0112]
通过noesy谱图确定c-3、c-4、c-3'和c-4'的相对构型,结合生源合成的角度确定其立体构型为3r、4s、3'r、4's。c-1”由于其距离c-3、c-4、c-3'和c-4'空间位置较远无法利用noesy、noe等确定其相对构型从而无法确定该位置的立体构型。对其进行旋光测试以及cd实验,该化合物比旋光值为cd实验,该化合物比旋光值为(c 0.11,meoh);cd测试结果显示在218nm处为( )cotton效应,在334nm处为(-)cotton效应。经scifinder检索以及文献调研发现该化合物未被报道,确定为新化合物,命名为dicitrinoneh。
[0113]
(5)化合物v,黄色固体,正离子hresims给出的准分子离子峰m/z:439.2113[m h]
(计算值为m/z:439.2115[m h]
),确定其分子式为c
26h30
o6,不饱和度为12。紫外光谱中显示最大吸收波长为:202nm、280nm和338nm。
[0114]
分析化合物
ⅴ
的nmr数据(见表3)可知化合物
ⅴ
与化合物ⅳ的nmr极度相似,仍是大多数nmr信号成对出现。
13
c nmr谱图出现47个碳信号,可能存在不可分离的阻转异构体。结合分子式可知该结构中含有12个季碳(包括2个酮羰基)、7个次甲基、7个甲基。化合物
ⅴ
的结构中同样存在两个桔霉素片段a。将其nmr数据与文献dicitrinone b([j].tetrahedron,2010,66(47):9286-9290.)的nmr数据进行对比,确定为dicitrinone b。该化合物中含有手性碳,旋光测试结果显示该化合物比旋光为(c 0.16,meoh)与文献基本一致,提示其立体构型相同,立体构型为3r、4s、3'r、4's。此外,首次报道该化合物的cd谱图(见图3),cd测试结果显示在219nm处为( )cotton效应,在332nm处为(-)cotton效应。
[0115]
表3化合物v和化合物vi的nmr数据(cdcl3)
[0116][0117]
注释:1h nmr(400mhz),
13
c nmr(100mhz),a表示重叠峰。
[0118]
(6)化合物vi,黄色固体,正离子hresims给出的准分子离子峰m/z:425.1955[m h]
(计算值为m/z:425.1959[m h]
),确定其分子式为c
25h28
o6,不饱和度为12。紫外光谱中显示最大吸收波长为:204、280和334nm。分析其nmr数据(见表3)与化合物
ⅴ
十分相似,只是少了一个甲基信息和一个次甲基信息,而增加了一个亚甲基信息(δh3.38 2h,s,h-1”和δc18.1,t,c-1”)。nmr谱图显示其成对出现,提示存在对称结构。将其nmr数据与文献dicitrinone c([j].tetrahedron,2010,66(47):9286-9290.)的数据对比二者十分相似,确定为dicitrinone c。
[0119]
该化合物中含有4个手性碳,旋光测试结果显示该化合物比旋光为该化合物中含有4个手性碳,旋光测试结果显示该化合物比旋光为(c 0.16,meoh)与文献基本一致,提示其立体构型相同,立体构型为3r、4s、3'r、4's。首次报道该化合物的cd谱图(见图3),其cd测试结果也在218nm处为( )cotton效应,在334nm处为(-)cotton效应。
[0120]
(7)化合物vii,红色无定形粉末状,易溶解于甲醇(溶液呈黄色)。正离子hr-esi-ms显示准分子离子峰m/z:427.1745[m h]
(计算值为427.1751[m h]
),分子式为c
24h26
o7,不饱和度12。紫外光谱中显示最大吸收波长为:206、270和322nm。
[0121]
nmr谱图显示6个甲基信号[δ
h 1.29(3h,t,5.6,h-9)、1.26(3h,t,6.8,h-10)、2.12(3h,s,h-11)、1.28(3h,t,6.2,h-9
′
)、1.36(3h,d,6.0,h-10
′
)、2.14(3h,s,h-11
′
)和δc 21.3(q,c-9)、22.8(q,c-10)、10.8(q,c-11)、15.6(q,c-9
′
)、19.3(q,c-10
′
)、12.5(q,c-11
′
)]及4个次甲基[δ
h 4.10(1h,qd,6.0,4.8,h-3)、2.89(1h,qd,7.2,4.4,h-4)、5.46(1h,qd,8.0,6.0,h-3
′
)、3.07(1h,qd,7.2,7.2,h-4
′
)和δc 79.9(d,c-3)、37.97(d,c-4)、73.2(d,c-3
′
)、40.5(d,c-4
′
)]信号提示结构中可能有桔霉素片段。此外与化合物ⅰ至ⅵ不同的是增加了一个芳香环上的质子信号[δh6.53,1h,s,h-7和δc100.9,d,c-7]、1个连氧次甲基的质子信号[δ
h 5.31,1h,s,h-1和δc 61.7,d,c-1]和1个醛基信息[δh7.78,1h,s,h-12'和δc 160.4,d)。同时缺少一个连氧次甲基信息(c-1
′
)。结合
13
c nmr和dept谱图可知存在11个季碳(包括3个羰基信号)、6个甲基和7个次甲基,推测该化合物可能含有一个开环且1位碳消失的桔霉素片段的二聚体(见表4)。
[0122]
将该化合物nmr数据与文献citrinin h1([j]journal of chemistry society perkin transactions.1,1993,2167-2171.)的数据进行对比,确定其平面结构为citrinin h1。将该化合物进行旋光测试,比旋光为(c 0.10,meoh)与文献1-epi-citrinin h1基本一致。由于该化合物为桔霉素类化合物,从生源合成角度可以确定c-3、c-4、c-3
′
和c-4
′
的其立体构型为3r、4s、3
′
r和4
′
s。noesy谱图显示h-1与h-3、h-10,h-4与h-9分别有相关,表明了c-1、c-3、c-4的相对构型分别为r*、r*、s*,初步确定c-1的立体构型为1r。cd实验结果(见图3)显示在221nm处为( )cotton效应,在281和334nm处为(-)cotton效应与文献报道的1-epi-citrinin h1的立体构型一致,确定为(1r、3r、4s、7's、8'r)-citrinin h1。
[0123]
表4化合物vii、化合物viii和化合物ix的nmr数据
[0124][0125]
注释:1h nmr(400mhz),
13
c nmr(100mhz),a表示重叠峰。
[0126]
(8)化合物viii,黄色油状(meoh),正离子hresims显示准分子离子峰m/z:403.2112[m h]
(计算值为m/z:403.2120[m h]
),分子式为c
23h30
o6,9个不饱和度。紫外光谱中显示最大吸收波长为:206nm、270nm和322nm。其nmr数据与化合物vii的相似,提示为桔霉素二聚体类化合物,只是少了三个不饱和度。nmr谱图显示同样具有桔霉素片段的特征信号:6个甲基信号以及4个次甲基碳上的氢信号(见表4),芳香环上的质子信号[δh6.17,1h,s,h-7和δc 102.0,d,c-7]及一个处于低场的质子信号[δh6.24,1h,s,h-1和δc 65.5,d,c-1]。但少了三个酮羰基信息,增加了一个芳香环上的质子信息[δ
h 6.32,1h,s,h-8a
′
和δc106.7,d,c-8a
′
]。结合
13
c nmr以及dept135谱图可知该结构有23个碳信号,分别为10个季碳、7个次甲基、6个甲基信号。结合分子式以及不饱和度推测该结构为7-取代脱羧桔霉素与一个开环的桔霉素片段相连。
[0127]
将该化合物nmr数据与文献的数据进行对比确定其平面结构为penidicitrinin b。文献([j].helvetica chimica acta,2010,93(11):2224-2230.)中nmr测试采用的溶剂为dmso-d6,由于实验得到的化合物量(3.0mg)较少,仅采集到1h nmr信息,与文献数据对比基本一致,
13
c nmr谱图中的碳信号太弱无法辨别。更换溶剂为cd3od并延长采集时间(碳谱10h),对1d nmr数据进行归属(见表4)。该化合物进行旋光测试,(c 0.08,meoh)与文献基本一致,确定其立体结构为1s、3r、4s、3
′
r、4
′
s。
[0128]
(9)化合物ix,橙黄色粉末,正离子hresims显示准分子离子峰m/z:403.1517[m na]
(计算值为403.1516[m h]
)、381.1694[m h]
(计算值为381.1697[m h]
)分子式为c
23h24
o5,不饱和度为12。其nmr数据与化合物vii化合物viii的nmr数据相似,提示为桔霉素二聚体类化合物。1h nmr谱图显示有桔霉素片段的特征信号:6个甲基信号以及4个次甲基碳上的氢信号(见表4),此外在还含有芳香环上的质子信号δ
h 6.35(1h,s,h-7)以及一个羟基质子信号8.34(1h,s,5'-oh)。结合
13
c nmr以及dept135谱图可知该结构有23个碳,分别为
12个季碳(包括1个酮羰基)、5个次甲基、6个甲基。将该化合物的nmr数据与penicitrinone a的文献数据([j].organic&biomolecular chemistry,2006,4(8):1520-1528.[j].journal of natural medicines,2006,60(4):279-284.)对照,基本一致,因此确定其平面结构为penicitrinone a(或dicitrinin a)。该化合物旋光(c 0.10,meoh)与文献基本一致,确定该化合物的立体构型为3r、4s、3'r、4's。
[0129]
实施例3:桔霉素二聚体化合物的抑菌性能测试:
[0130]
(1)菌丝生长速率法:配制不同浓度的化合物药液(每个浓度设3次重复),倒入培养皿中备用,以加入无菌水的pda培养基平板作对照。用无菌打孔器取培养好的病原菌菌饼,接种到pda培养基平板中央,置于28℃恒温培养箱中培养3天。阳性对照为多菌灵。十字交叉法测量菌落直径,计算菌丝生长抑制率。求出毒力回归方程,进一步算出lc
50
。
[0131]
菌丝生长抑制率=[(对照菌落直径-处理菌落直径)/(对照菌落直径-菌饼直径)]
×
100%。
[0132]
分别针对表皮葡萄球菌、金黄色葡萄球菌、耐甲氧西林金黄色葡萄球菌、大肠杆菌、铜绿假单胞菌和链球菌(菌株由广州微生物所提供)进行抑菌检测。
[0133]
结果显示,本发明桔霉素二聚体化合物具有显著的抑菌活性,详见表5。
[0134]
(2)对炭疽病菌的抑菌活性:
[0135]
配制不同浓度的化合物药液(每个浓度设3次重复),倒入培养皿中备用,以加入无菌水的pda培养基平板作对照。用无菌打孔器取培养好的病原菌菌饼(炭疽病菌株广东省农业科学院果树研究所提供),接种到pda培养基平板中央,置于28℃恒温培养箱中培养3天。阳性对照为多菌灵。十字交叉法测量菌落直径,计算菌丝生长抑制率。求出毒力回归方程,进一步算出lc
50
。
[0136]
菌丝生长抑制率=[(对照菌落直径-处理菌落直径)/(对照菌落直径-菌饼直径)]
×
100%。
[0137]
结果显示,本发明桔霉素二聚体化合物对木瓜炭疽病菌具有优异的抑菌活性(见表5),可应用于抗菌领域中,特别是在防治木瓜、苹果、香蕉、桔子等农作物和果树炭疽病中。
[0138]
表5、化合物1~ix抑菌活性(lc
50
、μg/ml)
[0139][0140][0141]
注:a表皮葡萄球菌、b金黄色葡萄球菌、c耐甲氧西林金黄色葡萄球菌、d大肠杆菌、
e铜绿假单胞菌和链球菌、f卡那霉素(阳性对照)、h炭疽病菌、i多菌灵(阳性对照)
[0142]
上述实施例为本发明较佳的实施方式,但本发明的实施方式并不受上述实施例的限制,其他的任何未背离本发明的精神实质与原理下所作的改变、修饰、替代、组合、简化,均应为等效的置换方式,都包含在本发明的保护范围之内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。