1.本发明涉及芯片技术领域,特别是聚合物、芯片及其制备方法和应用。
背景技术:
2.生物芯片通常是利用表面修饰技术,采用聚合物包被基底制成。表面修饰技术,从简单的二维修饰,到2.5维度的修饰,再到三维修饰,表面功能性基团的密度得到大幅度的提升。功能性基团的密度提升后,可用于生物芯片表面的高通量测试,比如基因芯片表面pcr、表面测序等等。
3.然而,目前已有的芯片仍存在诸多缺陷或限制,限制了其应用。例如,芯片基底能够承载的探针密度较低等,使得的芯片的制作工艺和应用较为受限。
技术实现要素:
4.基于此,有必要提供一种聚合物。该聚合物能够接枝于芯片的基底,使芯片能够更高密度地负载生物组分,满足不断发展的生物分子制备和/或分析需求。
5.具体技术方案如下:
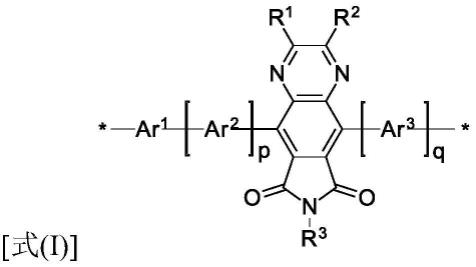
6.一种聚合物,所述聚合物包括重复单元a和重复单元b;
7.所述重复单元a具有如下所示结构特征:
8.x选自-o-或-nh-,r
01’、r
01”、r
01
”’
各自独立地选自:-h或c1~c3烷基;r0选自c1~c10烷基或-(c1-c5烷基)-nh-nhs-peg4,且r0被至少一个r
02
取代;r
02
各自独立地选自:环氧基、氨基或叠氮基;
9.所述重复单元b具有如下所示结构特征:
10.r
03’、r
03”、r
03
”’
、r
03
””
、r
04’、r
04”、r
04
””
、r
05’、r
05”、r
05
”’
各自独立地选自:-h、c1~c3烷基、酰胺基或酯基,l1选自c1~c3亚烷基或-c(o)-r
06-c(o)-;r
06
选自peg或烷基二胺。
11.在其中一个实施例中,x选自-o-。
12.在其中一个实施例中,r
01’、r
01”、r
01
”’
各自独立选自:-h或甲基;r0选自c1~c3烷基;
13.r
03’、r
03”、r
03
”’
、r
03
””
、r
04’、r
04”、r
04
”’
、r
05’、r
05”、r
05
”’
各自独立选自:-h、甲基、-c(o)nh2或-c(o)och3,l1选自-c(o)-peg-c(o)-或-c(o)-nh-ch
2-nh-c(o)-。
14.在其中一个实施例中,所述重复单元a选自如下所示重复单元中的一种:
[0015][0016]
在其中一个实施例中,
[0017]
所述重复单元b选自如下所示重复单元中的一种:
[0018][0019]
在其中一个实施例中,x选自-nh-。
[0020]
在其中一个实施例中,所述重复单元b具有如下所示结构特征:
[0021]r04’、r
04”、r
04
”’
、r
05’、r
05”、r
05
”’
各自独立地选自:-h、c1~c3烷基、酰胺基或酯基,l1选自c1~c3亚烷基或-c(o)-r
06-c(o)-;r
06
选自peg或烷基二胺。
[0022]
在其中一个实施例中,
[0023]r01’、r
01”、r
01
”’
各自独立选自:-h或甲基;r0选自c1~c3烷基或-(c1-c5烷基)-nh-nhs-peg4;
[0024]r04’、r
04”、r
04
”’
、r
05’、r
05”、r
05
”’
各自独立选自:-h、甲基、-c(o)nh2或-c(o)och3,l1选自-c(o)-peg-c(o)-或-c(o)-nh-ch
2-nh-c(o)-。
[0025]
在其中一个实施例中,
[0026]
所述重复单元a选自如下所示重复单元中的一种:
[0027][0028]
在其中一个实施例中,所述重复单元b选自如下所示重复单元中的一种:
[0029][0030]
在其中一个实施例中,所述重复单元b具有如下所示结构特征:
[0031]r03’、r
03”、r
03
”’
、r
03
””
各自独立地选自:-h、c1~c3烷基、酰胺基或酯基。
[0032]
在其中一个实施例中,所述重复单元b自如下所示重复单元中的一种:
[0033][0034]
在其中一个实施例中,r0选自-(c1-c5烷基)-nh-nhs-peg4-n3。
[0035]
在其中一个实施例中,所述重复单元a为
[0036]
在其中一个实施例中,所述聚合物的分子量为1万~12万。
[0037]
本发明还提供所述的聚合物的制备方法,包括如下步骤:
[0038]
以单体a和单体b进行共聚反应,制备所述聚合物;所述单体a形成所述重复单元a,所述单体b形成所述重复单元b。
[0039]
在其中一个实施例中,所述单体a和所述单体b的摩尔比为1:(1~30)。
[0040]
在其中一个实施例中,所述共聚反应是指所述单体a和所述单体b在引发剂的引发下,于30℃~60℃进行聚合反应。
[0041]
本发明还提供一种芯片,在其中一个实施例中,所述芯片包括基底,以及接枝于所述基底表面的聚合物;所述聚合物为如上所述的聚合物。
[0042]
在其中一个实施例中,所述基底修饰有活性基团,所述聚合物通过所述活性基团接枝于所述基底的表面;所述活性基团选自氨基、环氧基、炔基、氰基、乙烯基和丙烯基中的至少一种。
[0043]
在其中一个实施例中,所述芯片还包括生物组分;所述生物组分接枝于所述聚合物。
[0044]
在其中一个实施例中,所述生物组分选自核苷酸序列和氨基酸序列中的至少一种。
[0045]
本发明还提供一种芯片的制备方法,包括如下步骤:
[0046]
获取基底,将聚合物接枝至所述基底的表面;所述聚合物为如上所述的聚合物。
[0047]
在其中一个实施例中,先将所述基底的表面接枝活性基团,再将所述聚合物经所述活性基团接枝于所述基底的表面;所述活性基团选自氨基、环氧基、炔基、氰基、乙烯基和丙烯基中的至少一种。
[0048]
在其中一个实施例中,接枝所述活性基团是指采用硅烷偶联剂与所述基底进行反应;所述硅烷偶联剂选自3-氨丙基三甲氧基硅氧烷、3-(三乙氧基硅烷基)丙基]氨基甲酸2-丙炔酯、4-(三乙氧基)硅基丁腈和γ-(2,3-环氧丙氧)丙基三甲氧基硅烷中的至少一种。
[0049]
在其中一个实施例中,所述聚合物经所述活性基团接枝于所述基底的表面是指于40℃~50℃反应1~8h。
[0050]
在其中一个实施例中,还包括如下步骤:将生物组分接枝至所述高聚物。
[0051]
在其中一个实施例中,所述生物组分选自氨基酸序列和核苷酸序列中的至少一种。
[0052]
在其中一个实施例中,将所述生物组分接枝至所述高聚物是指于50℃~60℃反应1~5h。
[0053]
本发明还提供如上所述的聚合物,或如上所述的芯片,或如上所述的制备方法制备得到的芯片在生物分子制备或生物分子分析中的应用。
[0054]
与现有技术相比较,本发明具有如下有益效果:
[0055]
本发明一实施方案提供的聚合物,其包含特定重复单元,可以接枝于芯片的基底,形成密度较高、且反应活性高的修饰表面,由此能够更高密度地负载生物组分,满足不断发展的生物分子制备和/或分析需求。另外,该聚合物的稳定性好,还能够克服传统的芯片基底上修饰的聚合物大多具有空气敏感性,使得的芯片的制作工艺较为受限的技术缺陷。
附图说明
[0056]
图1为本发明一实施例所述生物芯片的制备方法的工艺流程图;
[0057]
图2为本发明实施例1制备的聚物的gpc分子量测试图;
[0058]
图3为本发明实施例1制备的生物芯片的表面质量检测的光强图;
[0059]
图4为本发明实施例1制备的生物芯片的生物应用的光强图;
[0060]
图5为本发明实施例2制备的聚物的gpc分子量测试图;
[0061]
图6为本发明实施例2制备的生物芯片的表面质量检测的光强图;
[0062]
图7为本发明实施例2制备的生物芯片的生物应用的光强图;
[0063]
图8为本发明实施例3制备的聚物的gpc分子量测试图;
[0064]
图9为本发明实施例3中叠氮基大分子核磁检测示意图;
[0065]
图10为本发明实施例3制备的生物芯片的表面质量检测的光强图;
[0066]
图11为本发明实施例3制备的生物芯片的生物应用的光强图;
[0067]
图12为本发明实施例4制备的聚物的gpc分子量测试图;
[0068]
图13为本发明实施例4制备的生物芯片的表面质量检测的光强图;
[0069]
图14为本发明实施例4制备的生物芯片的生物应用的光强图;
[0070]
图15为本发明实施例5制备的聚物的gpc分子量测试图;
[0071]
图16为本发明实施例5制备的生物芯片的表面质量检测的光强图;
[0072]
图17为本发明实施例5制备的生物芯片的生物应用的光强图;
[0073]
图18为本发明实施例6中文库的分子结构图;
[0074]
图19~23为本发明实施例1~5制备的生物芯片的的荧光强度检测图,其中,左图为原始图片,右图为使用imagej二值化处理后的图片。
具体实施方式
[0075]
以下结合具体实施例对本发明的生物芯片及其制备方法和应用作进一步详细的说明。本发明可以以许多不同的形式来实现,并不限于本文所描述的实施方式。相反地,提供这些实施方式的目的是使对本发明公开内容理解更加透彻全面。
[0076]
除非另有定义,本文所使用的所有的技术和科学术语与属于本发明的技术领域的技术人员通常理解的含义相同。本文中在本发明的说明书中所使用的术语只是为了描述具体的实施例的目的,不是旨在于限制本发明。本文所使用的术语“和/或”包括一个或多个相关的所列项目的任意的和所有的组合。
[0077]
本文所述芯片,可以为接枝有所述聚合物的基底,也可以为在所述聚合物上进一步接枝生物组分的基底。基底材料并不受特别限制,基底由玻璃、硅片、塑料、凝胶和尼龙膜中的至少之一形成。
[0078]
本文所述的“经
……
接枝于”、“修饰有
……”
可以表示直接接枝、修饰于对象之上,也可以表示进一步经过其他的过渡基团接枝、修饰于对象之上。
[0079]
术语“烷基”是指包含伯(正)碳原子、或仲碳原子、或叔碳原子、或季碳原子、或其组合的饱和烃。包含该术语的短语,例如,“c1~c
10
烷基”是指包含1~10个碳原子的烷基,每次出现时,可以互相独立地为c1烷基、c2烷基、c3烷基、c4烷基、c5烷基、c6烷基、c7烷基、c8烷基、c9烷基、c
10
烷基。合适的实例包括但不限于:甲基(me、-ch3)、乙基(et、-ch2ch3)、1-丙基(n-pr、n-丙基、-ch2ch2ch3)、2-丙基(i-pr、i-丙基、-ch(ch3)2)、1-丁基(n-bu、n-丁基、-ch2ch2ch2ch3)、2-甲基-1-丙基(i-bu、i-丁基、-ch2ch(ch3)2)、2-丁基(s-bu、s-丁基、-chr06-c(o)-;r
06
选自peg或烷基二胺。
[0090]
在其中一个具体的实施例中,x选自-o-。
[0091]
进一步地,r
01’、r
01”、r
01
”’
各自独立选自:-h或甲基;r0选自c1~c3烷基。
[0092]
进一步地,r
03’、r
03”、r
03
”’
、r
03
””
、r
04’、r
04”、r
04
”’
、r
05’、r
05”、r
05
”’
各自独立选自:-h、甲基、-c(o)nh2或-c(o)och3,l1选自-c(o)-peg-c(o)-或-c(o)-nh-ch
2-nh-c(o)-。
[0093]
具体地,所述重复单元a选自如下所示重复单元中的一种:
[0094][0095]
具体地,所述重复单元b选自如下所示重复单元中的一种:
[0096][0097]
在另外一个具体的实施例中,x选自-nh-。
[0098]
进一步地,所述重复单元b具有如下所示结构特征:
[0099]r04’、r
04”、r
04
”’
、r
05’、r
05”、r
05
”’
各自独立地选自:-h、c1~c3烷基、酰胺基或酯基,l1选自c1~c3亚烷基或-c(o)-r
06-c(o)-;r
06
选自peg或烷基二胺。
[0100]
更进一步地,r
01’、r
01”、r
01
”’
各自独立选自:-h或甲基;r0选自c1~c3烷基或-(c1-c5烷基)-nh-nhs-peg4;。
[0101]
更进一步地,r
04’、r
04”、r
04
”’
、r
05’、r
05”、r
05
”’
各自独立选自:-h、甲基、-c(o)nh2或-c(o)och3,l1选自-c(o)-peg-c(o)-或-c(o)-nh-ch
2-nh-c(o)-。
[0102]
具体地,所述重复单元a选自如下所示重复单元中的一种:
[0103][0104]
具体地,所述重复单元b选自如下所示重复单元中的一种:
[0105][0106]
另进一步地,所述重复单元b具有如下所示结构特征:
[0107]r03’、r
03”、r
03
”’
、r
03
””
各自独立地选自:-h、c1~c3烷基、酰胺基或酯基。
[0108]
具体地,所述重复单元b自如下所示重复单元中的一种:
[0109][0110]
更进一步地,r0选自-(c1-c5烷基)-nh-nhs-peg4-n3。
[0111]
具体地,所述重复单元a为
[0112]
另外,在其中一个具体的实施例中,所述聚合物的分子量为1万~12万。
[0113]
本发明的实施例还提供如上所述聚合物的制备方法,包括如下步骤:
[0114]
以单体a和单体b进行共聚反应,制备所述聚合物;所述单体a形成所述重复单元a,所述单体b形成所述重复单元b。
[0115]
在其中一个具体的实施例中,所述单体a和所述单体b的摩尔比为1:(1~30)。具体地,单体a和所述单体b的摩尔比为1:1、1:3、1:5、1:8、1:10、1:12、1:15、1:20、1:25、1:30。
[0116]
在其中一个具体的实施例中,所述共聚反应是指所述单体a和所述单体b在引发剂的引发下,于30~60℃(反应温度)进行聚合反应。具体地,所述反应温度可采用如下具体的温度值:30℃、35℃、36℃、37℃、38℃、40℃、41℃、42℃、43℃、45℃、50℃、52℃、54℃、55℃、56℃、58℃、60℃。
[0117]
在其中一个具体的实施例中,所述引发剂选自偶氮二异丁腈(aibn)、过硫酸钾(kps)中的至少一种。
[0118]
在其中一个具体的实施例中,所述聚合反应以氧气终止。
[0119]
在其中一个具体的实施例中,所述聚合反应所得产物以甲醇提取,再干燥,制备所述聚合物。
[0120]
本发明的实施例还提供一种芯片,所述芯片包括基底,以及接枝于所述基底表面的聚合物;所述聚合物为如上所述的聚合物。
[0121]
在其中一个具体的实施例中,所述基底修饰有活性基团,所述聚合物通过所述活性基团接枝于所述基底的表面;所述活性基团选自氨基、环氧基、炔基、氰基、乙烯基和丙烯基中的至少一种。
[0122]
在其中一个具体的实施例中,所述生物芯片还包括生物组分,所述生物组分接枝于所述聚合物。由此用于进一步的生物反应和应用。具体地,所述生物组分选自氨基酸序列和核苷酸序列中的至少一种。进一步地,氨基酸序列包含蛋白质、寡肽、多肽等;核苷酸序列包含寡核苷酸序列、多核苷酸序列等。
[0123]
本发明的实施例还提供一种芯片的制备方法,包括如下步骤:
[0124]
获取基底,将聚合物接枝至所述基底的表面;所述聚合物为权利要求1~15任一项所述的聚合物。该芯片的制备方法,无需严格的反应条件控制,工艺简单易控,利于芯片的推广应用。
[0125]
在其中一个具体的实施例中,先于所述基底的表面接枝活性基团,再将所述聚合物经所述活性基团接枝于所述基底的表面;所述活性基团选自氨基、环氧基、炔基、氰基、乙烯基和丙烯基中的至少一种。
[0126]
在其中一个具体的实施例中,接枝所述活性基团是指采用硅烷偶联剂与所述基底进行反应;所述硅烷偶联剂选自3-氨丙基三甲氧基硅氧烷、3-(三乙氧基硅烷基)丙基]氨基甲酸2-丙炔酯、4-(三乙氧基)硅基丁腈和γ-(2,3-环氧丙氧)丙基三甲氧基硅烷中的至少一种。
[0127]
在其中一个具体的实施例中,所述聚合物经所述活性基团接枝于所述基底的表面是指于40~50℃反应1~8h(反应温度*时间)。具体地,所述反应温度*时间可采用如下组合:40℃*4h、43℃*4h、44℃*4h、45℃*4h、46℃*4h、47℃*4h、50℃*4h、45℃*2h、45℃*6h、45℃*1h、45℃*8h。
[0128]
在其中一个具体的实施例中,接枝所述活性基团是指所述硅烷偶联剂与所述基底在20~30℃反应1~5h。
[0129]
另外,在其中一个具体的实施例中,所述制备方法还可以包括如下步骤:将生物组分接枝至所述高聚物。由此用于进一步的生物反应和应用。具体地,所述生物组分选自氨基酸序列和核苷酸序列中的至少一种。进一步地,氨基酸序列包含蛋白质、寡肽、多肽等;核苷酸序列包含寡核苷酸序列、多核苷酸序列等。
[0130]
在其中一个具体的实施例中,将所述生物组分接枝至所述高聚物是指于50℃~60℃反应0.5~5h(反应温度*时间)。具体地,所述反应温度*时间可采用如下组合:55℃*0.5h、55℃*1h、55℃*2h、55℃*3h、55℃*5h、54℃*1h、56℃*1h、52℃*1h、50℃*1h、58℃*1h、60℃*1h。
[0131]
另外,本发明的实施例提供如上所述的聚合物,或如上所述的芯片,或如上所述的制备方法制备得到的芯片在生物分子制备或生物分子分析中的应用。
[0132]
如下为具体的实施例,如无特别说明,实施例中采用的原料均为市售获得,“%”均指质量百分比。
[0133]
t20:tttttttttt tttttttttt tttttt(seq id no.1);
[0134]
pe:caacaacaac aacaacaaca acaacaa(seq id no.2);
[0135]
rd:ctgccccggg ttcctcattc tat(seq id no.3)。
[0136]
实施例1
[0137]
本实施例提供一种芯片,其制备方法如下(其工艺流程图参见图1):
[0138]
(1)聚合物制备
[0139]
以甲苯为溶剂,按照体积比,体系中加入5wt%的gma(甲基丙烯酸缩水甘油酯),0.1wt%的分子量为1000g/mol的pegda(聚乙二醇(二醇)二丙烯酸酯),0.1wt%的aibn(azodiisobutyronitrile;azobisisobutyronitrile,中文名称为偶氮二异丁腈)引发剂,通氮除氧后,在55℃下发生聚合反应。反应进行3h后,注入氧气终止反应,使用甲醇提取聚合物后,真空干燥获得体型的环氧基大分子,使用gpc检测(凝胶渗透色谱),检测结果如图2所示,获得峰位分子量为98215的环氧基大分子。
[0140][0141]
(2)基底表面修饰
[0142]
基底采用玻璃,玻璃使用溶液法进行表面氨基化镀膜,镀膜方法如下:
[0143]
将玻璃置于5%的aptms(氨丙基三甲氧基硅烷)乙醇溶液中25℃反应2h后,取出玻璃与烘箱中130℃烘烤2h,完成玻璃表面的氨基化。
[0144]
将氨基化镀膜后的玻璃置于0.1wt%的环氧基大分子的异丙醇溶液中,45℃反应4h后,得到接枝有环氧大分子的表面。
[0145]
利用nh2-cy3(采购自西安凯新生物科技有限公司)检测修饰环氧大分子的玻璃表面质量,具体检测过程如下:
[0146]
将20um浓度的nh2-cy3溶液通入到表面,55℃反应1h后,在荧光显微镜下,使用532nm波段激光,按照35mw,60ms参数进行拍照检测光强。光强检测结果如图3所示,经imagej信号统计,获得的表面平均亮度为21919a.u.。
[0147]
(3)寡核苷酸连接(a)将修饰有大分子的基底采用微流道封装技术,例如采用表面改性封装方式、热压键合封装或阳极键合微流道封装技术,在基底表面形成微流道。在微流道中加入nh2-oligo(nh
2-a
30
)5um溶液,在37℃下反应24h,使表面接枝有高密度oligo(寡核苷酸)序列,其中a
30
表示30个腺嘌呤核苷酸形成的寡核苷酸链。
[0148]
(b)用纯水将微流道表面冲洗干净后,加入5um t
20-cy3的溶液,在55℃下杂交30min。
[0149]
(c)在荧光显微镜下,使用532nm波段激光,按照35mw,60ms参数进行拍照检测光强。光强检测结果如图4所示,获得的平均亮度值为28267a.u.。
[0150]
实施例2
[0151]
本实施例提供一种芯片,其制备方法如下:
[0152]
(1)聚合物制备
[0153]
以水和dmf(二甲基甲酰胺)为溶剂,其中水和dmf的体积比未4:1。按照质量比,体系中加入2%的丙烯酰胺am、0.2%的gma单体、0.1%的kps(过硫酸钾)引发剂和0.01%的temed(四甲基乙二胺)凝胶促进剂,通氮除氧后,在42℃下发生聚合反应。反应进行3h后,注入氧气终止反应,使用甲醇提取聚合物后,真空干燥获得线性的环氧基大分子,经gpc检测(凝胶渗透色谱),检测结果如图5所示,获得峰位分子量为191619的环氧基大分子。
[0154][0155]
(2)基底表面修饰
[0156]
基底采用玻璃,玻璃使用溶液法进行表面氨基化镀膜,镀膜方法如下:
[0157]
将玻璃置于5%的aptms(氨丙基三甲氧基硅烷)乙醇溶液中,25℃反应2h后,取出玻璃与烘箱中130℃烘烤2h,完成玻璃表面的氨基化。
[0158]
将氨基化镀膜后的玻璃置于0.1wt%的环氧基大分子的异丙醇溶液中,45℃反应4h后,得到接枝有环氧大分子的表面。
[0159]
利用nh
2-cy3(采购自西安凯新生物科技有限公司)检测修饰环氧大分子的玻璃表面质量,具体检测过程如下:
[0160]
将20um浓度的nh
2-cy3溶液通入到表面,55℃反应1h后,在荧光显微镜下,使用532nm波段激光,按照35mw,60ms参数进行拍照检测光强。光强检测结果如图6所示,经imagej软件分析,获得的平均信号强度为13768a.u.。
[0161]
(3)寡核苷酸连接
[0162]
(a)将修饰有大分子的基底采用微流道封装技术在基底表面形成微流道。在微流
道中加入5um的nh
2-oligo(nh
2-t
35
)溶液,在37℃下反应24h,使表面接枝有高密度oligo(寡核苷酸)序列,其中t
35
表示35个胸腺嘧啶核苷酸形成的寡核苷酸链。
[0163]
(b)用纯水将微流道表面冲洗干净后,加入5um的a
30-cy3溶液,在55℃下杂交30min,其中a
30
表示30个腺嘌呤核苷酸形成的寡核苷酸链。
[0164]
(c)在荧光显微镜下,使用532nm波段激光,按照35mw,60ms参数进行拍照检测光强。光强图如图7所示,获得的平均信号强度为13039a.u.。
[0165]
实施例3
[0166]
本实施例提供一种芯片,其制备方法如下:
[0167]
(1)聚合物制备
[0168]
以水和dmf(二甲基甲酰胺)为溶剂,其中水和dmf的体积比未4:1。按照质量比,体系中加入2%的丙烯酰胺(am),1%的烯基叠氮单体(采购自西安凯新生物科技有限公司),0.1%的kps引发剂,0.01%的temed凝胶促进剂,通氮除氧后,在37℃下发生聚合反应。反应进行3h后,注入氧气终止反应,使用乙醇提取聚合物后,真空干燥获得线性的叠氮基大分子,经gpc检测(凝胶渗透色谱),检测结果如图8所示,获得峰位分子量为15167的叠氮基大分子。
[0169]
核磁测试如图9所示,在1.43、1.55、2.09处出现烯烃聚合后形成饱和链断的h吸收峰,在3.04-3.41范围出现分子内二胺内ch2上的h吸收峰,在3.93附近出现叠氮临近的peg链断内的h吸收峰,证明了叠氮大分子的形成。
[0170][0171]
(2)基底表面修饰
[0172]
基底采用玻璃,玻璃使用溶液法进行表面炔基化镀膜,镀膜方法如下:
[0173]
将玻璃置于1%的3-(三乙氧基硅烷基)丙基]氨基甲酸2-丙炔酯的甲苯溶液中,25℃反应2h后,取出玻璃于烘箱中130℃烘烤2h,完成玻璃表面的炔基化。
[0174]
将炔基化镀膜后的玻璃置于0.1wt%的叠氮基大分子的异丙醇溶液中,45℃反应4h后,得到接枝有叠氮大分子的表面。
[0175]
利用dbco(二苯并环辛炔)-cy3(采购自西安凯新生物科技有限公司)检测修饰叠氮大分子的玻璃表面质量,具体检测过程如下:
[0176]
将20um浓度的dbco-cy3溶液通入到表面,55℃反应1h后,在荧光显微镜下,使用532nm波段激光,按照35mw,60ms参数进行拍照检测光强。光强检测结果如图10所示,在imagej软件中进行分析,获得平均信号强度为19464a.u.的表面。
[0177]
(3)寡核苷酸连接
[0178]
(a)将修饰有大分子的基底采用微流道封装技术在基底表面形成微流道。在微流道中加入5um的dbco-oligo(dbco-t
35
)溶液,在37℃下反应24h,使表面接枝有高密度oligo(寡核苷酸)序列,其中t
35
表示35个胸腺嘧啶核苷酸。
[0179]
(b)将表面用纯水冲洗干净后,使用a
30-cy3的5um溶液在55℃下杂交30min,其中a
30
表示30个腺嘌呤核苷酸形成的寡核苷酸链。
[0180]
(c)在荧光显微镜下,使用532nm波段激光,按照35mw,60ms参数进行拍照检测光强。光强检测结果如图11所示,获得平均信号强度为14535a.u.。
[0181]
实施例4
[0182]
本实施例提供一种芯片,其制备方法如下:
[0183]
(1)聚合物制备
[0184]
以水为溶剂,按照质量比,体系中加入2%的烯基叠氮单体,0.1%的分子量为1000g/mol的pegda单体,0.1%的kps引发剂,0.01%的temed凝胶促进剂,通氮除氧后,在37℃下发生聚合反应。反应进行3h后,停止反应,使用乙醇提取聚合物后,真空干燥后获得体型的的叠氮基大分子,经gpc检测,检测结果如图12所示,获得其峰位分子量为129976的叠氮基大分子;
[0185][0186]
(2)基底表面修饰
[0187]
基底采用玻璃,玻璃使用溶液法进行表面氰基化镀膜,镀膜方法如下:
[0188]
将玻璃置于1%的4-(三乙氧基)硅基丁腈的甲苯溶液中,25℃反应2h后,取出玻璃于烘箱中130℃烘烤2h。完成玻璃表面的氰基化。
[0189]
将氰基化镀膜后的玻璃置于0.1wt%的叠氮基大分子的异丙醇溶液中,45℃反应4h后,得到接枝有叠氮大分子的表面。dbco-cy3(采购自西安凯新生物科技有限公司)检测修饰叠氮大分子的玻璃表面质量,具体检测过程如下:
[0190]
将20um浓度的dbco-cy3溶液通入到表面,55℃反应1h后,在荧光显微镜下,使用532nm波段激光,按照35mw,60ms参数进行拍照检测光强。光强检测结果如图13所示,经imagej软件分析,获得的平均信号强度为28531a.u.。
[0191]
(3)寡核苷酸连接
[0192]
(a)将修饰有大分子的基底采用微流道封装技术在基底表面形成微流道。在微流
道中加入5um的dbco-oligo(dbco-t
35
)溶液,在37℃下反应24h,使表面接枝有高密度oligo(寡核苷酸)序列,其中t
35
表示35个胸腺嘧啶核苷酸形成的寡核苷酸链。
[0193]
(b)将表面用纯水冲洗干净后,使用5um的a
30-cy3溶液在55℃下杂交30min。
[0194]
(c)在荧光显微镜下,使用532nm波段激光,按照35mw,60ms参数进行拍照检测光强。光强检测结果如图14所示,获得的平均信号强度为32108a.u.。
[0195]
实施例5
[0196]
本实施例提供一种芯片,其制备方法如下:
[0197]
(1)聚合物制备
[0198]
以甲苯为溶剂,按照体积比,体系中加入5%的n-(3-氨基丙基)甲基丙烯酸盐盐酸盐单体,0.1%的分子量为1000g/mol的pegda单体,0.1%的aibn引发剂,通氮除氧后,在55℃下发生聚合反应。反应进行3h后,注入氧气终止反应,使用甲醇提取聚合物后,真空干燥获得体型的氨基大分子,经gpc检测(凝胶渗透色谱),检测结果如图15,所示获得峰位分子量为99396的氨基大分子。
[0199][0200]
(2)基底表面修饰
[0201]
基底采用玻璃,玻璃使用溶液法进行表面环氧化镀膜,镀膜方法如下:
[0202]
将玻璃置于1%的γ-(2,3-环氧丙氧)丙基三甲氧基硅烷的甲苯溶液中,25℃反应2h后,取出玻璃与烘箱中130℃烘烤2h,完成玻璃表面的环氧化。
[0203]
将环氧化镀膜后的玻璃置于0.1wt%的氨基大分子的异丙醇溶液中,45℃反应4h后,得到接枝有叠氮大分子的表面。
[0204]
利用nhs-cy3(采购自西安凯新生物科技有限公司)检测修饰叠氮大分子的玻璃表面质量,具体检测过程如下:
[0205]
将20um浓度的nhs-cy3溶液通入到表面,55℃反应1h后,在荧光显微镜下,使用532nm波段激光,按照35mw,60ms参数进行拍照检测光强。光强检测结果如图16所示,在imagej软件中进行分析,获得的平均信号强度为25437a.u.。
[0206]
(3)制备得到的生物芯片的生物应用:
[0207]
(a)将修饰有大分子的玻璃用于芯片微流道封装。在封装后的微流道中加入nhs-oligo(nhs-t35)5um溶液,在37℃下反应24h,使表面接枝有高密度引物;
[0208]
(b)将表面用纯水冲洗干净后,使用a30-cy3的5um溶液在55℃下杂交30min
[0209]
(c)在荧光显微镜下,使用532nm波段激光,按照35mw,60ms参数进行拍照检测光强。光强检测结果如图17所示,获得的平均信号强度为33155a.u.。
[0210]
实施例6
[0211]
利用实施例1-5中制备的芯片进行文库杂交及检测,具体流程如下:
[0212]
1.dna杂交文库准备
[0213]
dna文库:片段长度为150-300bp双端含有已知序列的dna文库,文库的分子结构如图18所示,insertion:插入片段,来源于phi-x174标准菌株;t20、pe、rd分别为seq id no.1-3所示序列。
[0214]
将dna文库与52ul体积的去离子水混合,向其中加入18ul新鲜配制的0.2m naoh溶液,混合均匀后于室温静置变性8分钟,然后加入20ul体积ph8.0的400mmtris-hcl缓冲液终止反应,获得100ul体积的100pm变性dna文库。
[0215]
2.dna变性文库与芯片探针杂交
[0216]
使用ph 7.3含有3
×
ssc(是将20
×
ssc缓冲液用无核酸酶水(rnase-free水)稀释而成)杂交液将变性好的dna文库稀释至5pm,然后通入芯片通道中于42℃杂交反应30分钟,接着以250ul/min的速度流通160~260ulul体积的清洗试剂(5
×
ssc,0.05%吐温20,ph 7.0),完成杂交反应。
[0217]
3.模板初始延伸
[0218]
1)以500ul/min的速度流通芯片通道160~260ul体积的延伸缓冲试剂(20mm三羟甲基氨基甲烷(tris),10mm硫酸铵,2mm硫酸镁,1.5m甜菜碱,1.3%二甲基亚砜,0.45m n-甲基甲酰胺,1.5m甲酰胺(carboxamide),0.1%tritonx-100,ph 9.0);
[0219]
2)以500ul/min的速度流通芯片通道160~260ul体积的延伸试剂(延伸缓冲试剂,3ug/ml bst dna聚合酶,200um dntps),然后于50~60℃反应5min,完成模板初始延伸。
[0220]
4.dna簇生成
[0221]
利用文章isothermal amplification method for next-generation sequencing(zhaochun ma,et.al,pnas august 27,2013 110(35)14320-14323,https://doi.org/10.1073/pnas.1311334110)公开的template walking技术进行扩增,生成dna簇。
[0222]
5.检测dna簇(cluster)
[0223]
1)设置热循环温度为50~60℃;
[0224]
2)以500ul/min的速度流通芯片通道160~260ul体积的变性试剂甲酰胺,变性5分钟打开dna双螺旋结构;
[0225]
3)以500ul/min的速度流通芯片通道160~260ul体积的质控试剂(0.5um rd-cy3,3
×
ssc),其中rd-cy3中的cy3位于rd序列的5’端;
[0226]
4)设置热循环温度为25℃,反应15~30分钟;
[0227]
5)以500ul/min的速度流通芯片通道160~260ul体积的清洗试剂;
[0228]
6)利用20倍物镜的荧光检测系统,设置532nm波长激光功率为300mw,曝光时间为20ms,进行拍照观察。
[0229]
dna簇检测结果见图以及表1,图19~23对应的芯片分别为利用实施例1-5制备的芯片生成的dna簇检测结果。
[0230]
表1
[0231][0232]
由表1可知,利用实施例1~5制备的芯片可成功用于文库的杂交、dna簇的生成。
[0233]
以上所述实施例的各技术特征可以进行任意的组合,为使描述简洁,未对上述实施例中的各个技术特征所有可能的组合都进行描述,然而,只要这些技术特征的组合不存在矛盾,都应当认为是本说明书记载的范围。
[0234]
以上所述实施例仅表达了本发明的几种实施方式,其描述较为具体和详细,但并不能因此而理解为对发明专利范围的限制。应当指出的是,对于本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变形和改进,这些都属于本发明的保护范围。因此,本发明专利的保护范围应以所附权利要求为准。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。