一种人干血斑中维生素a和维生素e浓度的检测方法
技术领域
1.本发明涉及体外诊断技术领域,具体涉及一种人干血斑中维生素a和维生素e浓度的检测方法。
背景技术:
2.维生素a在视网膜的功能(对弱光的适应)起着至关重要的作用,是上皮组织生长和分化所必须的,也是骨骼生长,生殖和胚胎发育所必需,与某些类胡萝卜素一起,维生素a有增强免疫功能,减少患某些传染病。在维生素a缺乏症中通常可以观察到眼睛和皮肤的退化性变化。视力对黑暗的适应不良(夜盲症)是早期症状,也可伴随着视网膜的退化性变化。在发展中国家,维生素a缺乏时导致失明的主要原因。严重或长期缺乏可导致干眼(干眼症),可导致角膜溃疡、疤痕和失明。还有一种情况是摄入不足而导致的获得性免疫缺陷疾病,这种疾病的死亡率增加与维生素a摄入不足有关。并且维生素的不足与对疾病的易感性增加相关。在艾滋病患者中:维生素a缺乏与疾病的发展和死亡率增加相关。过量的维生素a摄入可能是有毒的,特别是慢性维生素a中毒,正常成人每天摄入超过15mg的维生素a儿童每天摄入超过6mg的维生素a,若在几个月中过量摄入会表现一些临床症状,临床症状具有多样性,其他包括皮肤干燥、唇裂、舌炎、呕吐、脱发、骨质脱矿和疼痛、高钙血症、淋巴结肿大、高血脂症、闭经、以及颅内压升高和乳头水肿的假性脑瘤特征。运费服用过量的维生素a会导致,门静脉高压症的肝纤维化也可能导致先天性畸形,如自然流产,颅面畸形和瓣膜性心脏病。因此,在怀孕期间,维生素a每日剂量不超过3mg。
3.维生素e有助于细胞膜,血管系统,及神经系统正常生理功能的维持,并为维生素a提供抗氧化保护作用;它起着抗氧化剂和自由基清除剂的作用,保护所有细胞生物膜中不饱和脂质的完整性,以及保护视黄醇免受氧化损伤。此外,维生素e可以促进内皮细胞中前列环素的形成,并抑制血小板中血栓烷的形成,从而最大限度地减少血小板在内皮表面的聚集,因此维生素e可能与冠状动脉粥样硬化和血栓形成有着非常重要的联系。儿童缺乏维生素e可导致可逆的运动和感觉神经病变,该问题在成年人中也可能存在;此外,维生素e可以预防早产儿支气管肺发育不良和牙后纤维增生等疾病。维生素e缺乏可能是由于营养不良或肠吸收不良造成的。儿童及患有肠病、胰腺病、及慢性胆汁淤积症等疾病的患者均容易出现维生素e缺乏的症状。婴儿胆管病,包括肝内和肝外胆道闭锁、肝内胆管狭窄、及动脉肝发育不良等,也会导致维生素e吸收不良。因此,对维生素e的浓度水平进行监测具有非常重要的临床指导意义。
4.目前,传统的维生素a和维生素e浓度检测方法中,常以血清为校准曲线及质控样本来源,而血清中本底较大,容易影响定量准确性,因此需要足够精确的取样量,同时还需保证采血量足够大;除此之外,传统检测方法的样本不稳定,需要冷链运输,致病性以及职业暴露的可能性都较高。
5.综上所述,本领域迫切需要一种稳定性好、所需样本量少、操作简便、准确性高且成本较低的血液中维生素a和维生素e浓度的检测方法。
技术实现要素:
6.为解决上述技术问题,本发明提供一种人干血斑中维生素a和维生素e浓度的检测方法,包括以下步骤:
7.1)配制校准品,所述校准品设置有七个,所述校准品的组成成分包括兔血、维生素va标准品、维生素ve标准品和甲醇;
8.2)配制质控品,所述质控品包括va组质控品和vb组质控品,所述va组质控品和vb组质控品均设置有三个,所述va组质控品包括va高浓度质控品、va中浓度质控品和va低浓度质控品,所述vb组质控品包括vb高浓度质控品、vb中浓度质控品和vb低浓度质控品,所述质控品的组成成分均包括兔血、维生素va标准品、维生素ve标准品和甲醇;
9.3)将配置好的校准品和质控品分别制作成干血片样品卡,并设置2个空白对照样品卡;
10.4)配制样品提取液,所述样品提取液的组成成分包括维生素va-d6、维生素ve-d6和甲醇,所述维生素va-d6的浓度为100ng/ml,所述维生素ve-d6的浓度为300ng/ml;
11.5)向前处理容器中加入配制好的校准品、质控品和待测样本,再加入配制好的样品提取液进行前处理,作为上样分析备用;
12.6)向空白样品中加入甲醇水溶液,进行所述前处理,作为空白对照;
13.7)使用超高效液相色谱串联质谱uplc-ms/ms系统,采用内外标结合法,对待测样本进行色谱质谱检测;
14.8)分析检测结果:
15.先通过7个校准品标示浓度(x),校准品中维生素a及维生素e与内标维生素va-d6及维生素ve-d6的峰面积比值(y),绘制标准曲线,并拟合标准曲线方程;
16.再将检测样品的维生素a及维生素e的峰面积与内标维生素va-d6及维生素ve-d6的峰面积比值,带入标准曲线方程,即可定量计算样本中维生素a及维生素e的浓度。
17.具体地,所述干血片样品卡的制备方法包括以下步骤:
18.s1、配置浓度为2.5mg/ml的维生素a储备液和浓度为10.0mg/ml的维生素e储备液,储存于-80℃下;
19.s2、将新鲜的兔血混合,调整混合后的兔血的红细胞比容值(hct)为35%-40%;
20.s3、取150μl维生素a储备液和375μl维生素e储备液,混合后进行梯度稀释,得到不同浓度的校准品和质控品;
21.s4、将配制好的校准品和质控品分别点制于采血管上,制成相应的干血片样品卡,以备检测。
22.具体地,所述甲醇均为hplc级甲醇,且所述甲醇中含有0.3%bht抗氧化剂。
23.具体地,所述校准品和质控品中均添加有防腐剂,所述防腐剂包括proclin300和proclin950。
24.具体地,所述校准品和质控品中还含有牛血清白蛋白、pbs缓冲液和l-抗坏血酸。
25.具体地,步骤5)中,所述前处理是指,于1500rpm下振荡混匀10min,再于12000rpm下离心5min,取上清液150μl于新的96孔板中,最后取15μl于超高效液相色谱串联质谱uplc-ms/ms系统中进样检测。
26.具体地,步骤5)中,所述样品提取液的加样量为250μl。
27.具体地,步骤6)中,所述甲醇水溶液中,甲醇与水的体积比为7:3,所述甲醇水溶液的加样量为300μl。
28.具体地,所述超高效液相色谱串联质谱uplc-ms/ms系统的色谱条件为:
29.色谱柱为waters acquity uplc beh c18,2.1mm
×
50mm,1.7μm;柱温为50℃;流速为0.4ml/min;流动相a为0.1%甲酸水溶液,流动相b为0.1%甲酸甲醇溶液;洗脱方式为梯度洗脱,所述梯度洗脱条件为:
30.0min流动相组成为30%a 70%b,0.5min流动相组成为30%a 70%b,1.0min流动相组成为1%a 99%b,2.5min流动相组成为1%a 99%b,2.51min流动相组成为30%a 70%b,3.0min流动相组成为30%a 70%b。
31.具体地,所述超高效液相色谱串联质谱uplc-ms/ms系统的质谱参数为:
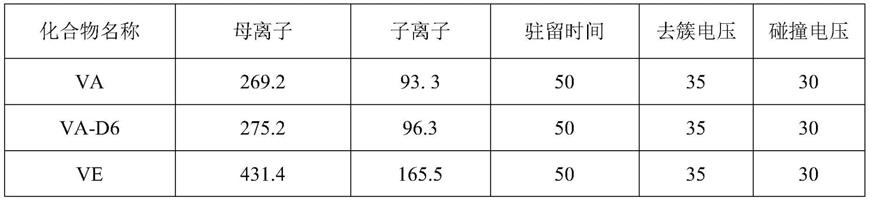
32.离子信息如下表所示:
[0033][0034][0035]
离子源为大气压化学电离源,气帘气为20psi,离子源温度为500℃,雾化气为55psi,碰撞气为9psi。
[0036]
与现有技术相比,本发明的有益效果在于:
[0037]
1.本发明提供的检测方法,采用兔血替代人全血,兔血的本底值较低,消除了人全血由于本底值较大而对检测准确度造成的影响,提升了检测的准确度,且所需的样本量无需太大。
[0038]
2.本发明提供的检测方法,提供了稳定性高的校准品、质控品和样品提取液,保证样品的稳定,降低了致病性和职业暴露的风险,同时提高了检测的准确度和灵敏度。
[0039]
3.本发明提供的检测方法利用液相色谱强大的分离能力,再结合串联质谱对样品中物质的质荷比进行检测,具有分析时间短、检测度准确、前处理简单和检测成本低等多个优点。
具体实施方式
[0040]
下面将对本发明的技术方案进行清楚、完整的描述,显然,所描述的实施例是本发明的一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动的前提下所获得的所有其他实施例,都属于本发明保护的范围。以下实施例中所使用的材料、仪器和试剂等,如无特殊说明,均可从商业途径得到。
[0041]
实施例一校准品、质控品和样品提取液的制备
[0042]
在一具体实施例中,校准品、质控品和样品提取液的配制具体操作如下:
[0043]
(一)标准溶液的配制
[0044]
精确称量25mg维生素va标准品,用甲醇(0.3%bht)溶解,配制成浓度为2.5mg/ml的储备液,编号为ssc-va。
[0045]
精确称量100mg维生素ve标准品,用甲醇(0.3%bht)溶解,配制成浓度为10mg/ml的储备液,编号为ssc-ve。
[0046]
(二)样品提取液配制
[0047]
va-d6储备液的配制:取1mg维生素va-d6标准品,用甲醇(0.3%bht)溶解,配制成浓度为0.1mg/ml的储备液,编号为ssc-va-d6。配制批号为当天日期,配制完的储备液保存在-90~-70℃。
[0048]
ve-d6储备液的配制:取10mg维生素ve-d6标准品,用甲醇(0.3%bht)溶解,配制成浓度为1mg/ml的储备液,编号为ssc-ve-d6。配制批号为当天日期,配制完的储备液保存在-90~-70℃,有效期12个月或至生产商声明的产品有效期。
[0049]
(三)校准样品卡和质控样品卡制备
[0050]
1)将新鲜采购的兔血混合好后,最终调整混合兔血的红细胞比容(hct)值在35%-40%之间。
[0051]
2)取用储存于-80℃配制的维生素a&维生素e储备液(2.5mg/ml;10.0mg/ml)按下表1配置出校准曲线(cc)高低浓度样品(cc-h/cc-l)。
[0052]
表1校准曲线高低浓度样品配置
[0053][0054]
3)按下表2互相稀释,得到校准曲线及质控样品。
[0055]
表2校准曲线及质控样品配置
[0056]
溶液名称c1c2c3c4c5c6c7lqcmqchqcc7(μl)1.63.24.891632484.819.238.4稀释液体积(μl)46.444.843.2393216043.228.89.6总体积48484848484848484848
[0057]
4)将校准品和质控品点制于采血管上。c1~c7表示7个校准品干斑点,hqc、mqc、lqc分别表示3个质控品干斑点。将点制后的采血管放置于生物安全柜中,室温干燥3-4小时。
[0058]
实施例二样品检测
[0059]
1.样品前处理:
[0060]
对空白样品进行前处理,具体操作步骤如下:
[0061]
1)在双空白样品中加入300μl甲醇:水(v:v 70:30)溶液,1500rpm振荡混匀10min。
[0062]
2)在12000rpm离心5min。
[0063]
3)取150μl上清液至新的96孔板中。
[0064]
4)在uplc-ms/ms系统中进样15μl。
[0065]
对待测样品进行前处理,具体操作步骤如下:
[0066]
1)在待测样品中加入250μl样品提取液,再加入内标液,补齐总体积至300μl,1500rpm振荡混匀10min。
[0067]
2)在12000rpm离心5min。
[0068]
3)取150μl上清液至新的96孔板中。
[0069]
4)在uplc-ms/ms系统中进样15μl。
[0070]
2.超高效液相色谱串联质谱uplc-ms/ms定量分析检测
[0071]
设置色谱柱为waters acquity uplc beh c18,2.1mm
×
50mm,1.7μm;柱温为50℃;流速为0.4ml/min;流动相a为0.1%甲酸水溶液,流动相b为0.1%甲酸甲醇溶液;洗脱方式为梯度洗脱,梯度洗脱条件为:
[0072]
0min流动相组成为30%a 70%b,0.5min流动相组成为30%a 70%b,1.0min流动相组成为1%a 99%b,2.5min流动相组成为1%a 99%b,2.51min流动相组成为30%a 70%b,3.0min流动相组成为30%a 70%b。
[0073]
超高效液相色谱串联质谱uplc-ms/ms系统的质谱参数为:
[0074]
离子信息如下表所示:
[0075]
化合物名称母离子子离子驻留时间去簇电压碰撞电压va269.293.3503530va-d6275.296.3503530ve431.4165.5503530ve-d6437.4171.3503530
[0076]
离子源为大气压化学电离源,气帘气为20psi,离子源温度为500℃,雾化气为55psi,碰撞气为9psi。
[0077]
进样分析结束后,对结果进行分析,先通过7个校准品标示浓度(x),校准品中维生素a及维生素e与内标维生素va-d6及维生素ve-d6的峰面积比值(y),绘制标准曲线,并拟合标准曲线方程;
[0078]
再将检测样品的维生素a及维生素e的峰面积与内标维生素va-d6及维生素ve-d6的峰面积比值,带入标准曲线方程,即可定量计算样本中维生素a及维生素e的浓度。
[0079]
此外,试剂盒附有高、中、低三个不同浓度的质控品对检测结果进行把控,并附有空白对照样品以对进样残留情况进行监测。
[0080]
综上所述,上述各实施例仅为本发明的较佳实施例而已,并不用以限定本发明的保护范围,凡在本发明的精神和原则之内,所做的任何修改、等同替换、改进等,皆应包含在本发明的保护范围内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。