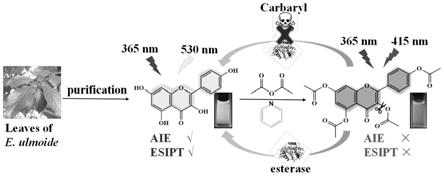
1.本技术涉及生物检测和分析领域,具体涉及一种外周血样本分析方法及相应的试剂盒和应用,可用于评估疫苗的有效性和免疫治疗的效果。
背景技术:
2.外周血的检测和分析是医学检查的一个重要方面。外周血是多种成分混合物,包括血浆和血细胞,易于从人体获得,主要从指尖、耳垂、肘部经脉抽取获得。血浆成分有代谢物、废物、激素、离子、蛋白质等,血细胞包括红细胞、白细胞、血小板等。临床上常应用外周血进行血常规、生化、血清免疫学检验,以此来诊断或者鉴别某些疾病。外周血的形态学检查和细胞学检查,对于各种血液病的诊断有重要意义。
3.单个细胞类型(single cell type)的基因表达是良好的生物标志物。为了获得外周血中单种细胞亚群的基因表达水平,传统方法需要事先分离指定细胞类型的亚群。最近,一种称为单细胞rna测序(single cell rna-sequencing,scrna-seq)的方法也可能获得单细胞的基因表达信息。单细胞rna测序通过使用价钱昂贵的设备和试剂,生成每个单细胞基因表达数据,这种昂贵的技术一般只在研究中使用,不适宜在临床中广泛应用。
4.一些方法可以直接测量细胞混合物样本中选定的单细胞亚群的特征性基因,而无需分离目标细胞亚群。它还避免了使用单细胞rna-seq的昂贵设备。具体参见专利文献cn103764848b(申请日2012年7月23日,公开日2014年4月30日);和us9589099b2(申请日2012年7月20日,公开日2017年3月7日)。这种新的检测方法称为“直接白血细胞亚群的转录本丰度”检测(direct leukocyte subpopulation transcript abundance assay,或简称direct ls-ta assay)。这些方法提供了不用事先对细胞进行分离而直接进行白血细胞亚群的转录本丰度测量的技术,测量速度和成本上具有很大优势。
5.免疫学是生物学的一个重要研究方面。通过免疫学研究,对人体和动物体的免疫系统有了进一步认识,对疾病预防和治疗提供了更多物质、手段和方法。免疫学近年有很大发展,各类疫苗不断涌现。疫苗预防疾病或者疫苗治疗疾病是当前一个发展较快的方面。但是,疫苗使用后的效果存在不确定性,及时获得疫苗使用效果或者确认疫苗使用效果是一个很重要的议题。
6.传染病是人类和动物的一个重大敌人。通过疫苗接种是控制感染的好方法。疫苗会使身体在感染之前启动获得性(又称为适应性或特异性)免疫系统,以产出针对病原体的抗体。在已经接种疫苗的个体中,病原体将得到快速控制,感染症状会大大减轻甚至无症状。常见的例子包括针对肝炎病毒和流感病毒的疫苗接种。由于流行性感冒病毒株频繁变化,因此在许多地方通常对不同的流行性感冒病毒株进行年度疫苗接种。现时covid-19是一种新的大流行感染,疫苗的开发也在进行中。
7.在针对流感病毒进行疫苗接种的情况下,并非所有接种疫苗的接种者都免受随后的感染,也不是每一个接种者都有抗体产生,这种保护不佳(低抗体产生)的人称为无反应者(non-responder,nr)。另一方面,疫苗接种的反应者(responder,r)会产生针对抗原的抗
体。抗体的产生是以针对特定抗原的抗体滴度(antibody titer)来衡量的,需要在接种后28天的血液样本中进行检测。一般来说,流感疫苗接种后的反应者比率少于接种者的50%。此外,获得性免疫系统需要较长时间产生针对新抗原的抗体,所以一般在疫苗接种后28天才分析抗体滴度的结果。以抗体出现为生物学标志物的测试确认试验,需要在接种后至少28天才能获得结果。
8.所以,疫苗使用需要配合有效检测才能真正做到及时预防和治疗疾病。快速和早期检测疫苗接种效果是疫苗使用中一个急需解决的问题。
9.因此,需要一种新的简单而快速的外周血分析方法,使得可以在预防性或治疗性疫苗接种后的早期进行,以评估疫苗接种的有效性和免疫治疗的效果。
技术实现要素:
10.总体而言,本技术提供了一种分析方法及相应的试剂盒和应用,可通过直接测量各种细胞混合物样本(例如外周血)中的特定b淋巴细胞类型的特征性基因(cell-type informative gene)的转录本丰度(transcript abundance,ta)来直接评估b淋巴细胞基因的表达,从而避免事先分离b淋巴细胞,也不需要使用昂贵的设备进行单细胞rna测序,通过该方法获得的生物标志物参数,用于预测接种疫苗的有效性和免疫治疗(例如癌症免疫治疗)的效果,从而有利于早期或者快速作出判断。
11.具体地,本技术一方面提供了一种外周血样本分析方法,包括测定外周血样本中的至少一种b淋巴细胞靶基因的转录本丰度和至少一种b淋巴细胞参考基因的转录本丰度;所述b淋巴细胞靶基因选自tnfrsf17、tnfrsf13b、txndc5、jchain中的至少一种,所述b淋巴细胞参考基因选自tnfrsf13c和fcrla。本技术还提供了用于测定基因转录本丰度的试剂成分在制备用于外周血样本分析方法的试剂盒中的用途,所述b淋巴细胞靶基因选自tnfrsf17、tnfrsf13b、txndc5和jchain,所述b淋巴细胞参考基因选自tnfrsf13c和fcrla。
12.在不背离本发明精神和实质的情况下,上述参考基因和靶基因还可以选择其他基因。
13.在一种实施方案中,上述方法可以包括如下步骤:
14.a).采集所述外周血样本;
15.b).测定所述外周血样本的所述至少一种b淋巴细胞靶基因的转录本丰度,以获得第一量;
16.c).测定所述外周血样本的所述至少一种b淋巴细胞参考基因的转录本丰度,以获得第二量;
17.d).计算生物标志物参数,即所述第一量与所述第二量的相对值。
18.在一种实施方案中,所述外周血样本为接种疫苗之前或接种疫苗之后的外周血样本。例如,所述外周血样本可以是接种疫苗5-12天后的样本。
19.在一种实施方案中,所述方法还包括将所述外周血样本的所述生物标志物参数与临界值进行比较。所述比较例如可以用于预测所述接种疫苗导致的抗体产生和/或癌症免疫治疗的效果。
20.在一种实施方案中,所述外周血样本包括接种疫苗之前获取的第一外周血样本,和接种疫苗后(例如接种5-12天后)获取的第二外周血样本;所述生物标志物参数包括由所
述第一外周血样本获得的第一生物标志物参数和由所述第二外周血样本获得的第二生物标志物参数。在进一步的实施方案中,所述方法还可包括计算所述第一生物标志物参数和第二生物标志物参数的变化值。所述变化值例如可以用于预测所述接种疫苗所导致的抗体产生和/或免疫治疗(例如癌症免疫治疗)的效果。
21.在一种实施方案中,所述生物标志物参数的计算和比较可以通过例如计算器系统来进行,例如通过计算机来进行。
22.在一种实施方案中,所述疫苗是预防性疫苗或者治疗性疫苗。例如,可以是预防传染病的疫苗或治疗癌症的疫苗。
23.在一种实施方案中,所述疫苗是已经上市的现有疫苗,也可以是新疫苗。
24.另一方面,本技术提供了一种试剂盒,其包含用于定量基因转录本丰度的试剂成分,所述基因可以选自tnfrsf17、tnfrsf13b、txndc5、jchain中的至少一种,以及tnfrsf13c和fcrla中的至少一种。在不背离本发明精神和实质的情况下,可以选择其他基因。
25.在一种实施方案中,所述试剂盒中含有具有如下序列的引物中的至少一种:
[0026][0027][0028]
另一方面,本技术提供了测定基因转录本丰度的试剂成分或试剂盒,其用于预测疫苗接种有效性和/或免疫治疗效果,其中所述基因选自tnfrsf17、tnfrsf13b、txndc5和jchain中的至少一种,以及tnfrsf13c和fcrla中的至少一种。再一方面,本技术提供了用于定量基因转录本丰度的试剂成分在制备用于预测疫苗接种有效性和/或免疫治疗效果的试剂盒或药物中的应用,其中所述基因选自tnfrsf17、tnfrsf13b、txndc5和jchain中的至少一种,以及tnfrsf13c和fcrla中的至少一种。
[0029]
在具体的实施方案中,所述试剂成分包括引物,所述引物的序列如seq id nos:1-14任一项所示。
[0030]
在具体的实施方案中,所述基因获自外周血样本,优选获自所述外周血样本的b淋巴细胞。在一种实施方案中,可以获得至少一次外周血样本,例如一次,两次,或者多次。
[0031]
在一种实施方案中,测定外周血中的b淋巴细胞的参考基因和靶基因的转录本的丰度可以采用cn103764848b所公开的方法。
[0032]
在一种实施方案中,本发明的方法用于分析疫苗接种所引起的免疫反应,从而评价疫苗的有效性或用于免疫治疗(例如癌症免疫治疗)的效果评估。
[0033]
传统疫苗的有效性或免疫疗法的预后评估多采用抗体滴定确认的方法,需要等抗体产生后才能进行,一般需要28天后进行。这种传统方法存在受制于抗体产生的生物学时限限制,尤其对急性传染病和发展快速的疾病治疗,确认时间太长。相比之下,本技术的方法显著缩短了疫苗有效性确认或免疫疗法的预后评估的时间。例如,本发明筛选得到了特定的b淋巴细胞靶基因和参考基因,通过对于这些特定基因的转录本进行分析测定,可以将对于疫苗有效性确认或免疫疗法的预后评估的时间大幅提前,例如可以提前至疫苗施用后的28天内,例如三个星期,例如两个星期,例如一个星期,甚至几天内,或者更短时间。
[0034]
附图的简要说明
[0035]
下面将结合附图对本发明作进一步说明,附图中:
[0036]
图1显示利用“直接b淋巴细胞亚群转录本丰度”检测(“direct b lymphocyte ls-ta”assay,简称“直接b淋巴细胞ls-ta”)获得的生物标志物的检测结果与传统方法在分离纯化b淋巴细胞中检测到的靶基因表达的相关性。图1中的x轴显示在分离纯化的b淋巴细胞中检定tnfrsf17的基因表达,使用了rpl32作为常规管家基因,这里x轴是黄金标准。如图1的y轴所示,在pbmc中利用“直接b淋巴细胞ls-ta”获得的生物标志物的检测结果(tnfrsf17:tnfrsf13c的相对值)与传统方法在分离纯化b淋巴细胞中检测到的靶基因表达有很好的相关性(相关系数,r》0.9)。
[0037]
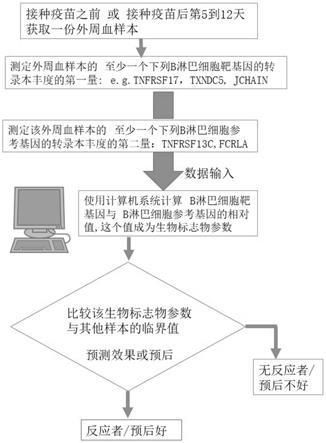
图2是本发明的疫苗使用效果评价方法的第一种实施方案。该方案只需要一个样本。
[0038]
图3是本发明的疫苗使用效果评价方法的第二种实施方案。该方案需要疫苗接种前、接种后的两个样本。
[0039]
图4a显示第7天的pbmc数据用于获得nr和r受试者的tnfrsf17的“直接b淋巴细胞ls-ta”生物标志物参数的原始值。图4b中显示为转换之后的mom值。
[0040]
图5a显示通过对第7天pbmc样本,“直接b淋巴细胞ls-ta”的tnfrsf17值进行roc分析(receiver operating characteristic curve,接收器工作特性曲线),用以确定“直接b淋巴细胞ls-ta”对疫苗接种后进行早期预测的能力。曲线下面积(auc)为0.85,表明该生物标记参数具有不错的预测能力。
[0041]
图5b显示用类似的方法,对另一个流感接种实验的数据集gse59635进行了roc分析,auc也达到0.73。
[0042]
图6a显示tnfrsf17的“直接b淋巴细胞-ls-ta”的增量。
[0043]
图6b显示为与图6a相同的数据转换为mom表示。在nr组中,生物标志物参数(d7-d0)的增量范围为从-1.01到0.67,增量中位数为0.066。反之,r组有更高的增量变化,其增量范围为从-0.13到3.39,增量中位数为1.11,nr组和r组之间的增量变化显著不同(配对测试,p值《0.01)。
[0044]
图7a显示进行了roc分析以确定第0天至第7天利用“直接b淋巴细胞ls-ta”检测tnfrsf17的增量在辨别r和nr组的能力。增量值的分辨能力也有高的auc(auc=0.85),和单
独使用第7天的“直接b淋巴细胞ls-ta”tnfrsf17的auc差不多。
[0045]
图7b显示在数据集gse59635 pbmc样本中,tnfrsf17的“直接b淋巴细胞ls-ta”的增量(d7-d0)的auc为0.7。
[0046]
图8a和图8b在数据集gse136163中,使用了针对黄热病接种者的全血样本的结果。其中,2个接种者被归为nr,因为它们的中和抗体(nab)滴度没有超过4倍的增加。nr组的tnfrsf17的“直接b淋巴细胞ls-ta”的中位数变化(d7-d0)为负数(-0.28)。相反地,r组的tnfrsf17的d7-d0“直接b淋巴细胞ls-ta”的增幅较高(中位数为0.38)。
[0047]
图8c显示进行了roc分析,单独使用第7天的“直接b淋巴细胞-ls-ta”tnfrsf17的auc为0.82。
[0048]
图8d显示第0天和第7天的“直接b淋巴细胞-ls-ta”tnfrsf17的增量的auc为0.88。
[0049]
图9a显示:在使用数据集gse59635中的txndc5基因数据时,nr和r组中生物标志物从d0到d7的增量。两组(nr和r)之间的差异是显著的(配对检验,p值《0.01)。
[0050]
图9b显示分析利用“直接b淋巴细胞ls-ta”检测txndc5的增量的roc,其auc为0.77。
[0051]
图9c显示使用数据集gse59635,单独使用第七天的样本,进行tnfrsf13b相对于tnfrsf13c的“直接b淋巴细胞ls-ta”检测,确定反应者(r组)有更高的生物指标参数(p值《0.05)。
[0052]
图9d显示roc分析,说明这个指标能够有效辨别两组(auc=0.81)。
[0053]
图10a显示r组比nr组具有更高的tnfrsf17:fcrla的“直接b淋巴细胞ls-ta”的增量(配对测试,p值<0.001)。
[0054]
图10b显示roc分析中,“直接b淋巴细胞ls-ta”(tnfrsf13c,fcrla)的增量的auc为0.82。
[0055]
图11a显示能够长时间存活的病人在疫苗接种前的“直接b淋巴细胞ls-ta”生物标志物参数较低(p值《0.05)。图11b显示roc分析表示,这个检测有一定的预测能力(auc=0.63)。
[0056]
图12a是生存分析(survival analysis)结果。使用考克斯回归(cox regression)计算三组病人的存活曲线(survival curve),把病人依据疫苗注射前的“直接b淋巴细胞ls-ta”生物标志物参数分为三组,使用分位数范围分为(a)低(指标低于25百分位),(b)中间区域(25百分位-75百分位),和(c)高(高于75百分位)的三组。三组生存曲线有明显的差别。存活机率最差的是“直接b淋巴细胞ls-ta”指标高的一组,大部分病人差不多都在一年内死亡(p值《0.01)。
[0057]
图12b显示只把生物标志物参数指标低(低于25百分位)和指标高(高于75百分位)的两组互相比较,存活曲线的差别更加明显(p值《0.001)。存活机率最差的是高“直接b淋巴细胞ls-ta”指标的一组,死亡危险几率(也叫作风险率或者风险比,hazard ratio)比生物标志物参数指标低的那一组高出差不多三倍(危险几率=2.95,置信区间=1.6-5.6)。
[0058]
图13a显示了nr和r组中生物标志物(jchain/tnfrsf13c)第七天表达的荟萃分析森林图(forest plot)。
[0059]
图13b显示了nr和r组中生物标志物(jchain/tnfrsf13c)从第0天到第7天的增量的荟萃分析森林图。
具体实施方案
[0060]
传统方法测定外周血中特定细胞的基因表达是首先分离特定细胞亚群,然后确定其基因表达水平。传统方法得出的细胞表达水平作为黄金标准。本技术提供了直接测定外周血样本(例如外周血单核细胞(pbmc))中特定细胞(例如b淋巴细胞)基因表达的方法,而不需要从其它血细胞中纯化特定细胞。比较传统方法得出的黄金标准和本文新方法得出的特定细胞基因表达水平以及它们的相关性,这样能确定新方法的效用。
[0061]
利用本技术的方法,能够直接在外周血(例如,pbmc)的细胞混合物样本中测定单细胞型(例如b淋巴细胞)的转录本丰度(ta),而不需要亚群分离。它适用于称为b细胞信息基因的一组基因。将在pbmc中获得的两个b细胞信息基因(靶基因和稳定表达的参考基因)的相对值用作新的生物标志物参数以代表纯化的b淋巴细胞中的靶基因表达。这种排除细胞分离的繁琐过程而直接测定外周血样品中白细胞亚群的ta的方法被称为直接ls-ta方法。例如,该方法可以被应用于在流感疫苗接种试验中收集的基因表达数据集来对血清转化进行早期预测。
[0062]
本技术提供了新的、易于分析的外周血生物标志物,其可以很容易地纳入常规临床实验室检查,或用于常规临床研究。所述外周血生物标志物可以预测流感疫苗接种后的早期血清转化状态(例如在第7天就可以预测疫苗接种后的抗体产生等)。由于获得性免疫的途径是针对流感和covid-19的疫苗接种所共有的,因此这些生物标志物也可用于预测新的covid-19疫苗的血清转化。直接b淋巴细胞ls-ta将成为实施个性化疫苗接种的有用检测。
[0063]
术语及定义
[0064]
术语“外周血样本”具有医学检验领域的通常含义,主要指取自指点、耳垂、手臂静脉等处的血液样本。例如,可以全血样本(whole blood,wb),也可以是外周血中多类型单核细胞的混合物样本(peripheral blood mononuclear cells,pbmc)。
[0065]
术语“直接测量”是指未经分离出其中的特定细胞(例如b淋巴细胞)而进行测量。也就是从血液样本中未经分离出要测定的特定细胞(例如b淋巴细胞)而进行直接测量。
[0066]
术语“基因表达水平”是指细胞(例如b淋巴细胞)的基因表达水平,以rna为测量对象,具体是mrna为测量对象,就是信使核糖核酸的数量水平。换句话说,是测量样本中细胞(例如b淋巴细胞)的基因的mrna水平。在技术上,它也被称为转录本丰度(ta)。
[0067]
术语“疫苗”指一种生物制品,是针对疾病的病原微生物或其蛋白质(多肽、肽)、多糖或者核酸,通过人工减毒、灭活、裂解、基因重组、提纯等方法制成,可以诱导机体产生相应的保护性的免疫物质,用于预防、控制相应疾病的发生和流行,或者可以调控机体内某一致害因素(如吸烟)和生理状态(如避孕)的特异性免疫反应,从而达到治疗或消除致害因素、避免生育为目的的生物制品。
[0068]
从功能上理解,疫苗就是刺激身体进行免疫反应,用于消灭特定感染生物、特定细胞,起到预防或者治疗作用的物质。疫苗成分包括活性成分和辅助成分。
[0069]
本技术中的所用的“疫苗”包括疫苗活性成分,以及加入了其他物质的组合物或者制剂,也就是适合用于人体和动物体刺激免疫反应的单一成分或者组合物或者制剂。疫苗所指代的是上述任何一种情形所指的物质。简单来说,是免疫反应刺激物,或者诱导有益免疫反应的物质。
[0070]
术语“癌症”是指一类疾病,即出现了癌基因表达或者有癌细胞扩增生长或者出现了实体瘤。临床上通过组织学、免疫学、蛋白质测定所做诊断的任何癌症,均在本词语含义内。
[0071]
术语“癌症免疫治疗”又称为癌症免疫疗法,是新一代的癌症治疗方案(wikipedia:(“癌症免疫疗法”2020)),此类疗法利用身体的免疫功能,去攻击肿瘤细胞。有不同的治疗方案去刺激机体的免疫效能。最常见的是使用pd-1或pd-l1抑制剂在大肠癌治疗就有很好的成效。癌症疫苗(cancer vaccine)是一个新的治疗手段。这里的癌症疫苗并不是指那些个体未出现癌症之前接种的预防性疫苗,例如可以预防肝癌的乙肝病毒(hbv)疫苗和预防子宫颈癌的人类乳突病毒(hpv)疫苗,而是指癌症出现之后,癌细胞拥有一些特征的抗原,可以通过刺激自体产生免疫反应来针对这些抗原和癌细胞。不同的治疗方案使用不同的候选抗原。本文的例子是使用接种个性化肽疫苗(personalized peptide vaccination,ppv)治疗前列腺癌(araki et al.2015)。
[0072]
术语“细胞混合物样本”是来自个体(例如人体)的细胞混合物。典型地,该细胞混合物样本可以来自外周血,例如可以是未经任何处理的外周血样本。
[0073]
术语“特征性基因(cell-type informative genes)”,是指特定细胞(例如b淋巴细胞)类型所特定表达的基因,测定其转录本丰度可以确定该特征性基因的活性。特征性基因可以包括靶基因和参考基因。由于在本专利申请使用的目标特定细胞是b细胞,b细胞特征性基因又可称为b细胞信息基因。在本专利申请中,特征性基因与信息基因可以互换使用。
[0074]
术语“生物标志物”和“生物指标”(biomarker)是指特定细胞(例如b淋巴细胞)的基因表达中的信使核糖核酸的量,包括相对量和绝对量可以用于记录生物标志物状态。在本专利申请中,生物标志物与生物指标可以互换使用。
[0075]
术语“白血球细胞亚群(leukocyte subpopulation,ls)”包括b淋巴细胞亚群。白血球细胞包括多类型细胞。外周血是典型的多类型细胞混合物样本,包含了各种白血球细胞亚群,例如嗜中性粒细胞(neutrophil),淋巴细胞(lymphocyte)和单核细胞(monocyte)等等。
[0076]
术语“转录本丰度(transcript abundance,ta)”是指通过检测样本得出的基因表达量(gene expression level)。转录本是指基因转录(gene transcription)之后的产物,一般为rna。例如蛋白质编码的基因会产出信使rna(messanger rna,mrna)。
[0077]
术语“直接b淋巴细胞亚群转录本丰度”检测(“direct b lymphocyte leukocyte subpopulation transcript abundance”assay,简称“直接b淋巴细胞ls-ta”检测)是一种新型的生物指标参数检测方案,针对多类型细胞混合物样本,不需要分离纯化当中的目标细胞类型亚群,就可以直接从混合物样本中评估目标细胞亚群的平均基因表达。本发明论述的目标细胞亚群就是在外周血的b淋巴细胞。所以该检测名为“直接b淋巴细胞亚群转录本丰度”检测。“直接b淋巴细胞ls-ta”的计算需要使用细胞亚群特征性靶基因和细胞亚群特征性参考基因。
[0078]
在一些实施方案中,直接b淋巴细胞ls-ta值可以通过使用细胞亚群特征性靶基因和细胞亚群特征性参考基因的比率计算得到,例如某一靶基因的“直接b淋巴细胞-ls-ta”=(pbmc中的该靶基因)/(pbmc中的相应参考基因)。在另一些实施方案中,使用log(比率)
来计算直接b淋巴细胞ls-ta值。例如,log(“直接b淋巴细胞-ls-ta”tnfrsf17)=log(pbmc中的tnfrsf17)-log(pbmc中的tnfrsf13c)。
[0079]
术语“细胞亚群特征性靶基因(subpopulation informative target gene)”是指在多细胞混合样本(例如wb,pbmc)中,其大部份的转录本都是来自于指定的目标细胞亚群的基因,亦即由该细胞亚群产生。例如,来自下列实施例中的b淋巴细胞的基因。
[0080]
术语“细胞亚群特征性参考基因(subpopulation informative reference gene)”是指在多细胞混合样本(例如wb,pbmc)中,其大部份的转录本都是来自于指定的目标细胞亚群,并且同时在目标细胞中稳定表达的基因。
[0081]
本技术的发明人提出了从各种外周血样本中直接测定特定细胞(例如b淋巴细胞)的基因表达,并意外地发现这些基因表达在预测疫苗接种和癌症免疫治疗效果中具有重要价值。
[0082]
本技术所述的方法还包括将外周血样本的所述生物标志物参数与临界值进行比较。在一些实施方案中,所述比较用于预测疫苗接种导致的抗体产生和/或免疫治疗的效果。
[0083]
术语“临界值”可以使用以下几种方法来定义。(1)临界值可以定义为对照组参考区间之外的值。对照组的参考区间通常取对照组的中间95%分布。超出此范围的值可以作为临界值来定义异常低或异常高的结果。(2)临界值还可以最好从roc图表中定义,如图5a所示。roc曲线上每个点上标记的值代表潜在临界值,y轴和x轴分别显示使用此临界值的相关灵敏度和特异性。因此,当0.6用作tnfrsf17与tnfrsf13c比率的第7天直接ls-ta值的临界值时,它预测疫苗接种反应的灵敏度为~0.8和特异性为~0.85(图5a)。(3)如果没有对照组可用,如实施例7和图12所示,患者组中直接ls-ta数据分布的百分位值可用作临界值。例如,由tnfrsf17与fcrla比率的直接ls-ta值的第75个百分位值(75th percentile value)定义临界值(图9b),直接ls-ta大于该临界值的癌症患者(图9b中的实线)与其他患者相比,对癌症疫苗治疗的反应较差,生存期较短。
[0084]
本发明使用的数据集列表:
[0085]
外周血和特定单细胞类型的基因表达数据集
[0086]
为了鉴定可预测疫苗接种反应的单一细胞类型特征性基因,使用了以下从外周血样本获得的基因表达数据集。
[0087]
这些数据集可从美国国立卫生研究院维护的“基因表达综合”(geo)中获得。详细信息可在其登录号下获得。获得的血液样本类型包括全血(wb)和外周血单核细胞(pbmc)。在某些数据集中还包括进一步分离和纯化的特定细胞类型,例如分离纯化的b淋巴细胞(例如gse45764)或t淋巴细胞。
[0088]
[0089][0090]
疫苗接种后的反应者(r)的标准定义是根据血清中针对特定抗原的抗体滴度,例如在流感疫苗接种之后,血凝抑制(hi)抗体水平(也称为hi滴度,titer in hemagglutination inhibition assay)的显著增加,代表了接种者对疫苗有反应。该标准是通过对接种前和接种后二十八天的受试者血清进行血凝抑制(hi)测定。欧洲人类医药产品委员会(chmp)将血清转化/显著增加(seroconversion/significant increase)定义为:(1)hi滴度在接种后至少是1:40和(b)有至少4倍上升(committee for medicinal products for human use.1997;mo et al.2017)。疫苗接种后的受试者不符合这些标准的情况定义为“无反应者(nr)”。
[0091]
除了流感疫苗之外,在数据集gse136163中,接种者进行了黄热病疫苗接种。正如其他研究中所使用的反应者定义那样,这里使用了疫苗接种后中和抗体(nab)滴度增加4倍来定义该数据集中的反应者(casey et al.2019)。在该数据有两个受试者定义为nr。
[0092]
在本说明书和权利要求书中,词语“包括”、“包含”和“含有”意指“包括但不限于”,
且并非意图排除其他部分、添加物、组分、或步骤。
[0093]
应该理解,在本技术的特定方面、实施方案或实施例中描述的特征、特性、组分或步骤,可适用于本文所描述的任何其他的方面、实施方案或实施例,除非与之矛盾。
[0094]
下面将结合本发明实施例中的附图对本技术实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本技术一部分实施例,而不是全部的实施例。下述实施例仅是说明性的,并不意图限制本技术实施方案的范围或者所附的权利要求的范围。基于本技术中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
[0095]
实施例
[0096]
实施例1
[0097]“直接b淋巴细胞的转录本丰度”(“direct b lymphocyte-ls-ta”,简称“直接b淋巴细胞ls-ta”)的生物指标参数
[0098]
使用细胞混合物样本中b淋巴细胞靶基因(例如tnfrsf17)和b淋巴细胞特征参考基因(例如tnfrsf13c)的ta相对值来计算一个生物指标参数以评估经过分离纯化后的b淋巴细胞的基因表达量。
[0099]
在数据集gse45764中,分别收集了5个接种者在不同天数的多个分离纯化的b淋巴细胞样本以及pbmc样本。pbmc细胞混合物样本中的两个指定的b淋巴细胞特征基因的相对值与纯化的b淋巴细胞样本中的靶基因的表达(黄金标准)的相关程度提供了对“直接b淋巴细胞ls-ta”方案的性能评估。
[0100]
在此实施例中,参考图1。指定的靶基因是tnfrsf17。指定的b淋巴细胞参考基因为tnfrsf13c。“直接b淋巴细胞ls-ta”标示在y轴。
[0101]
对于该实施例,常规管家基因只用于标准化已分离纯化的b淋巴细胞样本的基因表达结果。常规管家基因包括rpl31,rpl32,actb,gapdh和ubc。常规管家基因的选择参见eisenberg and levanon2013,也可在网站上获得,例如https://www.tau.ac.il/~elieis/hkg/。图1的x轴显示了分离纯化的b淋巴细胞中检定tnfrsf17的基因表达(黄金标准),使用rpl32作为常规管家基因。常规管家基因仅由制造商用于校准黄金标准和验证目的,而不是用于本发明的试剂盒或其实施方案中。
[0102]
如图1的y轴所示,在pbmc细胞混合物样本中测量的本发明的“直接b淋巴细胞ls-ta”生物标志物的结果(tnfrsf17:tnfrsf13c的相对值)与传统方法在分离纯化b淋巴细胞中检测到的靶基因表达(黄金标准)有很好的相关性(相关系数,r》0.9)。结果证实,该“直接b淋巴细胞ls-ta”生物标志物参数能够评估纯化的b淋巴细胞中的靶基因(tnfrsf17)表达;以及确定了单细胞类型基因表达测定,可以直接从多细胞混合物样本(包括pbmc或wb)获得,而不需要预先分离b淋巴细胞。
[0103]
其余的由b淋巴细胞靶基因(包括tnfrsf13b,txndc5,jchain)和b淋巴细胞参考基因(包括tnfrsf13c,fcrla)组成的“直接b淋巴细胞ls-ta”生物标志物也与它们各自的黄金标准有很好的相关性(相关系数,r》0.8)。
[0104]
在随后的实施例中,“直接b淋巴细胞-ls-ta”标志物会用于预测疫苗接种后的抗体产生状态。这里会使用两种方案,第一种方案只需要一个样本,实施流程见图2。第二个方案需要疫苗接种前、后两个样本,实施流程见图3。
[0105]
实施例2
[0106]
疫苗接种后第七天的“直接b淋巴细胞ls-ta”能够预测抗体产生反应
[0107]
在数据集gse29617中,两个指定的b淋巴细胞特征基因tnfrsf17和tnfrsf13c的转录物丰度(ta)已经对数转化。因此,log(tnfrsf17)减去log(tnfrsf13c)便可得出本技术所需的生物标志物参数(对数值)。该生物标志物参数代表pbmc的细胞混合物样本中的b淋巴细胞基因tnfrsf17的基因表达量。因为这个生物指标,无需事先分离b淋巴细胞即可获得,所以在图标中,它被标记为“直接b淋巴细胞转录本丰度”(“直接b淋巴细胞-ls-ta”)。
[0108]
因此,b淋巴细胞靶基因tnfrsf17的“直接b淋巴细胞-ls-ta”生物标志物参数,使用细胞亚群特征性靶基因和细胞亚群特征性参考基因的比率计算可得,可表示为:
[0109]
(“直接b淋巴细胞-ls-ta”tnfrsf17)=(pbmc中的tnfrsf17)/(pbmc中的tnfrsf13c)
[0110]
还可以为此生物标志物参数进行对数变换,即亦可表示为:
[0111]
log(“直接b淋巴细胞-ls-ta”tnfrsf17)=log(pbmc中的tnfrsf17)-log(pbmc中的tnfrsf13c)
[0112]
由于用不同的化验检测方法测定会产生不同单位的结果,因此需要一种方法来标准化从多种不同检测方法获得的结果。相对于正常对照组别的中位数(multiple of median of a reference group,mom)是一种常用的标准化手法。在该实施例中,接种前(第0天)的数据用于定义正常对照组别的中位数。然后所有个体(包括nr和r)的结果均表示为该正常中值的倍数。所以这种数据表示方法称为对照组中位数的倍数(mom)。它通常用于未经过大规模测定标准化的检测方法,例如用于确定sars-cov感染后不良结局风险的细胞因子测定(tang et al.2005)。使用mom的好处是它能够去除数据的单位限制,从而可以比较不同检测方案产生的结果。
[0113]
接种疫苗后第7天,r和nr组的外周血单核细胞混合样本(pbmc)中tnfrsf17基因的“直接b淋巴细胞ls-ta”的比较:
[0114]
将第7天的pbmc数据用于获得nr和r受试者的tnfrsf17的“直接b淋巴细胞ls-ta”生物标志物参数。在图4a和4b中显示为原始值和转换之后的mom值。结果证实r和nr组之间存在显著差异(wilcoxon检验,p值《0.01)。
[0115]
通过对第7天pbmc样本,“直接b淋巴细胞ls-ta”的tnfrsf17值进行roc分析(receiver operating characteristic curve,接收器工作特性曲线),用以确定“直接b淋巴细胞ls-ta”对疫苗接种有效性进行早期预测的能力(图5a)。曲线下面积(auc)为0.85,表明该生物标志物参数具有良好的预测能力。
[0116]
同样地,用类似的方法,对另一个流感接种实验的数据集gse59635进行了roc分析,auc也达到0.73(图5b)。
[0117]
实施例3
[0118]
第0天和第7天的“直接b淋巴细胞-ls-ta”tnfrsf17的增量变化值在r和nr组的比较
[0119]
使用数据集(gse29617),来计算第0天和第7天“直接b淋巴细胞-ls-ta”的增量,使用了第7天的数据“直接b淋巴细胞-ls-ta”tnfrsf17值和第0天(基线,接种前)的“直接b淋巴细胞-ls-ta”tnfrsf17值,由两个值相减得出的增量变化数值(delta,δ),可以用来预测
随后的抗体产生状态。即本实施例执行图3的流程。
[0120]
由于两个值均已进行对数转换,因此减值表示疫苗接种后倍数变化的对数值。它显示为以下公式:
[0121]
接种疫苗后tnfrsf17基因的“直接b淋巴细-ls-ta”的增量=第7天的“直接b淋巴细胞-ls-ta”tnfrsf17-第0天的“直接b淋巴细胞-ls-ta”tnfrsf17
[0122]
tnfrsf17的“直接b淋巴细胞-ls-ta”的增量如图6a所示。相同的数据转换为mom表示,如图6b所示。在nr组中,生物标志物参数(d7-d0)的增量范围为从-1.01到0.67,增量中位数为0.066。反之,r组有更高的增量变化,其增量范围为从-0.13到3.39,增量中位数为1.11,nr组和r组之间的增量变化显著不同(配对测试,p值《0.01)。
[0123]
进行了roc分析以确定第0天至第7天的“直接b淋巴细胞-ls-ta”tnfrsf17的增量区分r和nr组的能力(图7a)。增量值的分辨能力也有高的auc(auc=0.85),和单独使用第7天的“直接b淋巴细胞-ls-ta”tnfrsf17的auc差不多(auc=0.85,图5a作比较)。
[0124]
同样,在数据集gse59635 pbmc样本中,tnfrsf17的“直接b淋巴细胞-ls-ta”的增量(d7-d0)也提供了有用信息,auc为0.7(图7b)。
[0125]
实施例4
[0126]
全血样本中tnfrsf17的“直接b淋巴细胞-ls-ta”的d7-d0变化,以及在其他疫苗接种中也能有效区分r和nr两组的能力
[0127]
在数据集gse136163中,使用了针对黄热病接种者的全血样本。2个接种者被归为nr,因为它们的中和抗体(nab)滴度没有超过4倍的增加。nr组的tnfrsf17的“直接b淋巴细胞-ls-ta”的中位数变化(d7-d0)为负数(-0.28)。相反地,r组的tnfrsf17的d7-d0“直接b淋巴细胞-ls-ta”的增幅较高(中位数为0.38)。数据显示在图8a和图8b。
[0128]
进行了roc分析,单独使用第7天的“直接b淋巴细胞-ls-ta”tnfrsf17的auc为0.82(图8c),而第0天和第7天的“直接b淋巴细胞-ls-ta”tnfrsf17的增量的auc比较高,为0.88(图8d)。
[0129]
实施例5
[0130]
使用另外两个可用b淋巴细胞特征性靶基因的“直接b淋巴细胞ls-ta”的结果
[0131]
除tnfrsf17外,txndc5和tnfrsf13b基因是可用于“直接b淋巴细胞-ls-ta”的另外两个靶基因。在本实施例中,txndc5和tnfrsf13b相对于tnfrsf13c的相对表达用作生物标志物。
[0132]
在数据集gse59635中,包含txndc5基因的数据。因此用这一个数据集来分析。图9a显示了nr和r组中生物标志物从d0到d7的增量。两组(nr和r)之间的差异是显著的(配对检验,p值《0.01)。并且分析了“直接b淋巴细胞-ls-ta”txndc5的增量的roc,其auc为0.77(图9b)。
[0133]
同样地使用数据集gse59635,单独使用第七天的样本,进行tnfrsf13b相对于tnfrsf13c的“直接b淋巴细胞-ls-ta”检测,确定了反应者(r组)有更高的生物指标参数(图9c,p值《0.05)。roc分析显示这个指标能够有效地分辨r和nr两组(图9d,auc=0.81)。
[0134]
实施例6
[0135]
使用另一个b淋巴细胞特征性参考基因fcrla的“直接b淋巴细胞-ls-ta”的结果
[0136]
除了tnfrsf13c,fcrla还可以用作另一个b淋巴细胞参考基因。图10a和10b显示了
使用tnfrsf17和fcrla得出的“直接b淋巴细胞-ls-ta”的结果和分辨性能。
[0137]
图10a显示r组比nr组具有更高的tnfrsf17:fcrla的“直接b淋巴细胞-ls-ta”的增量(配对测试,p值<0.001)。图10b显示roc分析中,“直接b淋巴细胞-ls-ta”(tnfrsf13c,fcrla)的增量的auc为0.82(图10b)。
[0138]
实施例7
[0139]
癌症疫苗(ppv)接种前的“直接b淋巴细胞-ls-ta”能够预测前列腺病人的预后及存活机率
[0140]
gse53922数据库包含112位前列腺病人癌症疫苗接种前,外周血多类型单核细胞样本pmbc基因表达,预后和生存时间(overall survival,os)的数据。病人被分为两组,第一组为治疗后存活时间少于一年(365天)的病人。另一组为治疗效果较好,治疗后存活多于一年的病人。然后比较两组的病人ppv接种前的“直接b淋巴细胞-ls-ta”生物标志物参数。在本实施例中,使用pbmc样本中两个基因tnfrsf17和fcrla的相对值计算得出的“直接b淋巴细胞-ls-ta”的结果。
[0141]
图11a和图11b显示,治疗效果较好的病人组,在接种疫苗之前有比较低的“直接b淋巴细胞-ls-ta”生物标志物参数。图11a显示能够长时间存活的病人在疫苗接种前的“直接b淋巴细胞-ls-ta”生物标志物参数较低(p值《0.05)。roc分析表明,该检测具有一定的预测能力(auc=0.63)。
[0142]
图12a是生存分析(survival analysis),使用考克斯回归(cox regression)计算三组病人的存活曲线(survival curve),把病人依据疫苗注射前的“直接b淋巴细胞-ls-ta”生物标志物分为三组,使用分位数范围分为(a)低(指标低于25百分位),(b)中间区域(25百分位-75百分位),和(c)高(高于75百分位)的三组。三组生存曲线有明显的差别。存活机率最差的是接种前“直接b淋巴细胞-ls-ta”指标高的一组,大部分病人差不多都在一年内死亡(p值《0.01)。
[0143]
另外,只把指标低(低于25百分位)和指标高(高于75百分位)的两组互相比较,存活曲线的差别更加明显(图12b,p值《0.001)。存活机率最差的是高“直接b淋巴细胞-ls-ta”指标的一组,死亡危险几率(hazard ratio)比指标低的那一组高出差不多三倍(hazard ratio=2.95,置信区间=1.6至5.6)。
[0144]
以上结果显示,如果在ppv癌症疫苗接种前,前列腺病人已经有一定的b淋巴细胞活性(即“ls-ta”指标高的一组),为他们接种ppv疫苗对癌症的治疗帮助不大,即癌症疫苗对他们没有什么附加价值。反之,如果在ppv癌症疫苗接种前,病人没有(或只有低)的b淋巴细胞活性(即“ls-ta”指标低的一组),ppv疫苗对他们有帮助的机会更高,导致这一组别的预后存活机率大为上升。
[0145]
实施例8
[0146]
使用jchain基因作为b淋巴细胞特征性靶基因的“直接b淋巴细胞ls-ta”的结果
[0147]
除前面已经提及的b淋巴细胞特征性靶基因外,jchain基因也是可用于“直接b淋巴细胞-ls-ta”的靶基因。在本实施例中,将jchain相对于tnfrsf13c的相对表达用作生物标志物进行了流感疫苗接种者的荟萃分析(meta-analysis)。
[0148]
在荟萃分析中(参见图13),使用了7个数据集gse59654,gse59635,gse59743,gse101709,gse101710,gse29617,gse29614。荟萃分析共包括了65例nr和79例r流感疫苗接
种者。图13a显示了nr和r组中生物标志物(jchain/tnfrsf13c)第7天表达的荟萃分析森林图(forest plot),而图13b显示了nr和r组中该生物标志物从第0天到第7天的增量的荟萃分析森林图。这两种表达指标的荟萃分析在两组(nr和r)之间的差异是显著的,不论使用固定效应模型和随机效应模型均都得出大于零的标准化均数差(standardised mean difference,smd),而且可信区也确认大于零。例如图13a显示疫苗注射后第七天r组的jchain基因的“直接b淋巴细胞ls-ta”比nr组较高,smd=0.75(95%可信区=0.39-1.11)。
[0149]
实施例9
[0150]
定量b淋巴细胞基因转录本丰度的通用实验室程序和试剂盒组成
[0151]
在其他实施方案中,本领域技术人员将知道如何设计引物以确定这些b淋巴细胞信息基因的转录本丰度。
[0152]
本技术提供了一些可用于定量pcr(qpcr)的引物示例,以供参考。它们可以在qpcr反应中存在sybr green的情况下使用,以获取阈值循环(ct)数据,该数据可用于通过相对定量测定法确定delta-ct,delta-delta ct或效率校正的delta-ct作为生物标记参数。定量血液样本中rna的转录本丰度(dorak 2007)。其他的定量方法也可以实施。
[0153]
通用实验室程序:首先,使用trizol或类似试剂从各种血液样本中提取rna。商业试剂盒也可用于基于柱的rna提取。然后,通过逆转录酶将rna逆转录成cdna。特定基因通过用户选择的方法进行定量,包括qpcr、rna测序、dna微阵列(基因芯片)、分支链dna检测法(branched chain dna,bdna assay,us8426578b2,us7927798b2),纳米报告探针检测法(quantification using nanoreporters,us8415102b2)、数字pcr(us10465238b2)或杂交来测定。
[0154]
本技术教导了使用该方法的cdna样本可以同时用于b淋巴细胞的靶基因(如tnfrsf17,tnfrsf13b,txndc5或jchain)和b淋巴细胞参考基因(如tnfrsf13c,fcrla,cd79a,cd79b或ms4a1)的ta的测定,例如可以使用下面列出的引物。生物标志物参数由此类b淋巴细胞信息基因一对的qpcr结果的delta-ct,delta-delta ct或效率校正的delta-ct计算可得。这种“直接b淋巴细胞-ls-ta”分析产生的生物标志物参数提供了血液中各种细胞混合物样本(例如pbmc,wb)中b淋巴细胞基因表达水平的指标,而无需事先分离b淋巴细胞。
[0155]
在“直接b淋巴细胞-ls-ta”分析中用于qpcr分析的引物实例列表,参见下表。
enables early prediction of vaccine seroconversion.genes,12(7),971.https://doi.org/10.3390/genes12070971.
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。