1.本发明属于脑膜炎奈瑟菌检测技术领域,尤其涉及一种基于多交叉置换扩增检测脑膜炎奈瑟菌的引物和方法。
背景技术:
2.脑膜炎奈瑟菌,是流行性脑脊髓膜炎(简称流脑)的病原菌。肾形或豆形革兰阴性双球菌,两菌接触面平坦或略向内陷,直径0.6~0.8μm。人工培养后可成卵圆形或球状,排列较不规则,单个、成双或4个相连等。在孵育24h后的培养物中,常呈现衰退形态,菌体大小较不一致,着色亦深浅不匀。在患者脑脊液中,多位于中性粒细胞内,形态典型。
3.流行性脑脊髓膜炎,是一种由脑膜炎奈瑟菌(neisseria meningitidis)感染引起的以脑膜炎和败血症为主要临床表现的急性呼吸道传染病。即使患者在发病24-48小时内获得治疗,流脑的病死率仍然高达5%-10%,并且约10%-20%的幸存者会遗留精神异常及截肢等明显的后遗症。根据细菌的荚膜多糖结构,脑膜炎奈瑟菌可分为12个血清群,a、b、c、w135、x、y群是目前发现引起全球流脑流行的六种主要致病血清群。据我国近几年的流脑监测资料显示,我国目前脑膜炎奈瑟菌的流行以a、b、c、w135群为主要优势菌群,偶尔出现x群和y群脑膜炎奈瑟菌感染病例的报道。该菌以人类为其唯一的已知宿主,寄生在鼻咽部,通过呼吸道飞沫传播或者通过口腔分泌物接触传播。荟萃分析显示我国脑膜炎奈瑟菌的总体带菌率为2.7%。虽然仅部分携带者会出现临床症状,但无症状的带菌者被认为是流脑的主要传染源。因此,做好脑膜炎奈瑟菌及其血清群检测和鉴定的技术储备工作十分必要。
4.流脑发病急、进程快及病死率高与该病难以早期诊断有关。因此对于已经感染脑膜炎奈瑟菌或流脑发病的患者,尽快诊断并开始抗生素治疗是关键。
5.目前,临床上对脑膜炎奈瑟菌的血清学分群是在流脑确诊基础上,通过血清玻片凝集法对脑膜炎奈瑟菌进行血清群鉴定。此方法不仅需要培养出纯菌,费时费力,还因易受其他非特异因素的影响,导致检出率低,漏检率高,常延误诊断,耽误对患者病情的治疗及对流脑流行的有效控制。因此,建立快速、精准鉴定脑膜炎奈瑟菌及其血清群的分子检测方法,是及时有效诊断、控制与预防流脑传播的重要手段,对于流脑防治非常必要。
6.随着核酸诊断技术的快速发展,国内外已有部分实验室将以pcr为基础的检测技术,如普通pcr、荧光pcr等,用于快速鉴定脑膜炎奈瑟菌及其血清群。这些pcr方法与传统方法相比具有敏感性强、特异性高、快速等优点,但因依赖于特殊而昂贵的仪器设备、熟练地操作人员及后续的电泳操作,对于基层单位或条件落后的实验室难以推广,在一定程度上限制了这些技术的广泛应用。因此还需探讨更加便捷的方法,应对流脑暴发或流行。
7.近年发展起来的多种恒温扩增技术,较pcr技术而言,不依赖于热循环扩增设备,反应速度快,敏感性好。因此,有利于实现快速扩增,便捷检测及现场诊断。到目前为止,应用较为广泛的恒温扩增技术有滚环扩增(rca)、链置换扩增(sda)、解旋酶依赖的恒温扩增(hda)、环介导恒温扩增(lamp)、交叉扩增(cpa)及多交叉置换扩增(mcda)等。
技术实现要素:
8.本技术提供了一种基于多交叉置换扩增检测脑膜炎奈瑟菌的引物和方法,以解决现有检测脑膜炎奈瑟菌精度低的技术问题。
9.第一方面,本技术提供了一种基于多交叉置换扩增检测脑膜炎奈瑟菌的引物,所述引物包括第一引物,所述第一引物包括:如核苷酸序列如seq id no:1所示的置换引物f1和如核苷酸序列如seq id no:2所示的置换引物f2;
10.如核苷酸序列如seq id no:3所示的交叉内引物cp1和如核苷酸序列如seq id no:4所示的交叉内引物cp2;
11.如核苷酸序列如seq id no:5所示的扩增引物c1和如核苷酸序列如seq id n0:6所示的扩增引物c2;
12.如核苷酸序列如seq id no:7所示的扩增引物d1和如核苷酸序列如seq id no:8所示的扩增引物d2;
13.如核苷酸序列如seq id no:9所示的扩增引物r1和如核苷酸序列如seq id no:10所示的扩增引物r2。
14.可选的,所述引物还包括第二引物,用于脑膜炎奈瑟菌血清群检测,所述第二引物包括:第一组引物、第二组引物、第三组引物和第四组引物中的至少一组,所述第一组引物为特异基因sacb的引物,所述第二组引物为针对特异基因siad第一区域的引物,所述第三组引物为针对特异基因siad第二区域的引物,所述第四组引物为特异基因syng的引物。
15.可选的,所述第一组引物包括:核苷酸序列如seq id no:11-12所示的置换引物对a,核苷酸序列如seq id no:13-14所示的交叉内引物对a,核苷酸序列如seq id no:15-20所示的三组扩增引物对a;
16.可选的,所述第二组引物包括:核苷酸序列如seq id no:21-22所示的置换引物对b,核苷酸序列如seq id no:23-24所示的交叉内引物对b,核苷酸序列如seq id no:25-30所示的三组扩增引物对b;
17.可选的,所述第三组引物包括:核苷酸序列如seq id no:31-32所示的置换引物对c,核苷酸序列如seq id no:33-34所示的交叉内引物对c,核苷酸序列如seq id no:35-40所示的三组扩增引物对c;
18.可选的,所述第四组引物包括:核苷酸序列如seq id no:41-42所示的置换引物对w135,核苷酸序列如seq id no:43-44所示的交叉内引物对w135,核苷酸序列如seq id no:45-50所示的三组扩增引物对w135。
19.第二方面,本技术提供了一种基于多交叉置换扩增检测脑膜炎奈瑟菌的引物的使用方法,所述方法包括:将权利要求1所述的引物进行mcda扩增,所述mcda扩增的反应温度为62-67℃。
20.第三方面,本技术提供了一种基于多交叉置换扩增检测脑膜炎奈瑟菌的引物的使用方法,将权利要求1所述的第一引物进行mcda扩增,所述mcda扩增的目标基因片段模板浓度≥10fg。
21.第四方面,本技术提供了一种基于多交叉置换扩增检测脑膜炎奈瑟菌的检测器具,所述检测器具的组成部件包括:样品垫、金标垫、纤维膜、吸水垫及背板,所述样品垫、金标垫、纤维膜及吸水垫依次组装在背板上;
22.所述金标垫中物质包括:金纳米粒子偶联的链霉素亲和素;所述纤维膜中物质包括:含抗异硫氰酸荧光素的捕获抗体和生物素偶联的牛血清蛋白;所述检测器具还包括:如权利要求1-6任意一项所述的引物,用于对待检测物进行mcda扩增以使扩增产物滴入所述样品垫。
23.第五方面,本技术提供了一种基于多交叉置换扩增的脑膜炎奈瑟菌及其血清群的检测方法,所述方法包括以下步骤:
24.得到第一方面所述引物;
25.在所述引物的扩增引物中,任意一条扩增引物的5’端标记异硫氰酸荧光素,任意一条扩增引物的5’端标记生物素,得到标识有异硫氰酸荧光素和生物素的第三引物;
26.将待检测物与所述第三引物进行mcda扩增,得到双标mcda产物;
27.对所述双标mcda产物进行金纳米检测,判断所述待检测物是否有脑膜炎奈瑟菌其血清群。
28.本技术实施例提供的上述技术方案与现有技术相比具有如下优点:
29.本技术实施例提供的基于多交叉置换扩增检测脑膜炎奈瑟菌的引物,所述引物包括第一引物,所述第一引物的类型包括:交叉内引物对、置换引物对和三组扩增引物对;核苷酸序列如seq id no:1-10所示,所述第一引物针对脑膜炎奈瑟菌的特异基因ctra,经mcda扩增后,标识有异硫氰酸荧光素和生物素的产物与抗异硫氰酸荧光素捕获抗体和金纳米粒子偶联的链霉素亲和素结合并反应,并进行显色反应,实现脑膜炎奈瑟菌检测,所述方法便捷、快速、敏感、特异,适宜于推广应用于该特异核苷酸片段对应的病原菌的检测;mcda扩增技术对原始信号有指数级别的放大作用,提高检测脑膜炎奈瑟菌的精度,克服了在抗生素影响下,脑膜炎奈瑟菌被漏检的情况;可以简单快速客观实现反应产物的可视化检测;将mcda扩增技术和可视化检测技术结合则可对原始核酸序列起到指数级别的放大作用,极大提高检测精度,缩短检测时间,实现对目的分子的精准检测。
附图说明
30.此处的附图被并入说明书中并构成本说明书的一部分,示出了符合本发明的实施例,并与说明书一起用于解释本发明的原理。
31.为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单的介绍,显而易见地,对于本领域普通技术人员而言,在不付出创造性劳动性的前提下,还可以根据这些附图获得其他的附图。
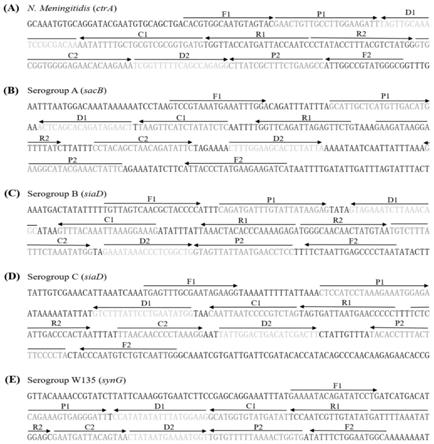
32.图1为本技术实施例提供的mcda引物设计的位置和方向示意图;
33.图2为本技术实施例提供的mcda扩增原理示意图;
34.图3为本技术实施例提供的金纳米生物传感器检测示意图;
35.图4为本技术实施例提供的mcda引物验证lfb检测结果图谱;
36.图5为本技术实施例提供的mcda引物验证电泳检测结果图谱;
37.图6为本技术实施例提供的mcda最佳反应温度测试结果图谱;
38.图7为本技术实施例提供的mcda检测脑膜炎奈瑟菌及其血清群的灵敏度的lfb检测结果图谱;
39.图8为本技术实施例提供的mcda检测脑膜炎奈瑟菌及其血清群的灵敏度的电泳检
测结果图谱。
具体实施方式
40.为使本技术实施例的目的、技术方案和优点更加清楚,下面将结合本技术实施例中的附图,对本技术实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例是本技术的一部分实施例,而不是全部的实施例。基于本技术中的实施例,本领域普通技术人员在没有做出创造性劳动的前提下所获得的所有其他实施例,都属于本技术保护的范围。
41.在整个说明书中,除非另有特别说明,本文使用的术语应理解为如本领域中通常所使用的含义。因此,除非另有定义,本文使用的所有技术和科学术语具有与本发明所属领域技术人员的一般理解相同的含义。若存在矛盾,本说明书优先。本文中所使用的专业术语只是为了描述具体实施例的目的,并不是旨在限制本发明的保护范围。例如,室温可以是指10~35℃区间内的温度。
42.除非另有特别说明,本发明中用到的各种原材料、试剂、仪器和设备等,均可通过市场购买得到或者可通过现有方法制备得到。
43.本技术实施例的技术方案为解决上述技术问题,总体思路如下:
44.根据本发明一种典型的实施方式,提供了一种基于多交叉置换扩增检测脑膜炎奈瑟菌的引物,所述引物包括第一引物,所述第一引物包括:如核苷酸序列如seq id no:1所示的置换引物f1和如核苷酸序列如seq id no:2所示的置换引物f2;
45.如核苷酸序列如seq id no:3所示的交叉内引物cp1和如核苷酸序列如seq id no:4所示的交叉内引物cp2;
46.如核苷酸序列如seq id no:5所示的扩增引物c1和如核苷酸序列如seq id n0:6所示的扩增引物c2;
47.如核苷酸序列如seq id no:7所示的扩增引物d1和如核苷酸序列如seq id no:8所示的扩增引物d2;
48.如核苷酸序列如seq id no:9所示的扩增引物r1和如核苷酸序列如seq id no:10所示的扩增引物r2。
49.具体地,所述三对扩增引物中,任意一条引物的5’端可以标记异硫氰酸荧光素,任意一条引物的5’端可以标记生物素,标记异硫氰酸荧光素和标记生物素的引物不是同一条引物。
50.本技术实施例中,基于多交叉置换扩增检测脑膜炎奈瑟菌的引物,比常规的引物,第一引物可识别靶基因的10个特定区域,具有更加灵敏、特异的优势。
51.在既定的恒温条件下,以c1*端标记异硫氰酸荧光素,d1*端标记生物素为例,第一引物的合成原理及流程包括:双链dna处于半解离和半结合的动态平衡状态中,任何一个引物向双链dna的互补部位进行碱基配对延伸时,另一条链就会解离,变成单链。
52.步骤1,在bstdna聚合酶的作用下,以交叉内引物cp1的p1区段的3
′
末端为起点,与对应的dna互补序列配对,启动链置换dna合成。置换引物f1与c1s前端f1s序列互补,以3
′
末端为起点,通过链置换活性dna聚合酶的作用,首先置换出交叉内引物cp1合成的dna链,同时合成自身dna。最终置换引物f1合成而得的dna链与模板dna形成双链。
53.步骤2,由交叉内引物cp1先合成的dna链被置换引物f1进行链置换产生一单链,该
单链的d1s,c1s,r1s,p2s,f2s区域能够依次与扩增引物d1*,c1*,r1,交叉内引物cp2及置换引物f2结合,并发挥链置换扩增作用。
54.步骤3:c1*引物扩增并置换d1*的扩增链,生成短片段c1s-d1产物,该产物能够与c1*和交叉内引物cp1结合,启动链置换扩增,进入循环扩增1。
55.步骤4,r1引物扩增并置换c1*的扩增链,生成短片段c1s-c1产物,该产物能够与c1*和交叉内引物cp1结合,启动链置换扩增,进入循环扩增2。在循环扩增2中,随着mcda扩增的进行,大量的双标产物被形成,该双标的产物能被金纳米生物器具(包括金纳米生物传感器)和琼脂糖凝胶电泳检测,从而进行可视检测。
56.因此,利用mcda-lfb技术进行靶序列检测时,可利用c1*和d1*扩增引物构建可检测产物,其中,c1*端标记异硫氰酸荧光素,d1*端标记生物素(图2),还可以利用扩增引物中的其他引物进行异硫氰酸荧光素或生物素标记。
57.第二方面,本技术提供了一种基于多交叉置换扩增检测脑膜炎奈瑟菌的引物的使用方法,所述方法包括:将权利要求1所述的引物进行mcda扩增,所述mcda扩增的反应温度为62-67℃。
58.具体地,所述mcda扩增中,所述反应为恒温反应。
59.以脑膜炎奈瑟菌-mcda为例:在标准反应体系条件下,加入针对脑膜炎奈瑟菌模板对应的mcda引物,模板量为10pg/反应。反应在不同的恒温条件下进行(62℃-67℃),结果运用实时浊度仪进行检测,可得到mcda引物的扩增动态曲线图(图6)。如图6所示,在不同的温度下均可见到稳健的扩增曲线。根据扩增曲线峰出现的最早时间,65℃作为适宜脑膜炎奈瑟菌-mcda扩增的最佳反应温度。
60.第三方面,本技术提供了一种基于多交叉置换扩增检测脑膜炎奈瑟菌的引物的使用方法,将权利要求1所述的第一引物进行mcda扩增,所述mcda扩增的目标基因片段模板浓度≥10fg。
61.在一些实施方式中,所述引物还包括第二引物,所述第二引物包括:第一组引物、第二组引物、第三组引物和第四组引物中的至少一组,所述第一组引物为特异基因sacb的引物,所述第二组引物为针对特异基因siad第一区域的引物,所述第三组引物为针对特异基因siad第二区域的引物,所述第四组引物为特异基因syng的引物。
62.具体地,所述第二组引物和所述第三组引物均是针对特异基因siad的引物,但,针对特异基因siad的不同区域,第一区域根据cp002424.1而来,第二区域根据am421808.1而来。
63.一般地来说,在进行了脑膜炎奈瑟菌特异基因ctra的判断和检测后,得到待检测物中含有脑膜炎奈瑟菌,可以进一步的对脑膜炎奈瑟菌的血清群作进一步的判断,判断脑膜炎奈瑟菌是属于哪种血清群,如血清群a、血清群b、血清群c、血清群w135-mcda等。可以将待检测物按照上述流程进行4组并行的检测,以判定血清群。
64.具体地,针对血清群a、血清群b、血清群c、血清群w135-mcda的特异基因依次为sacb、siad、siad和syng,针对血清群a、血清群b、血清群c、血清群w135-mcda的最佳mcda扩增的反应温度依次为61℃、59℃、60℃、56℃。
65.具体地,四组引物中,分别包括三对扩增引物,任意一条引物的5’端可以标记异硫氰酸荧光素,任意一条引物的5’端可以标记生物素,标记异硫氰酸荧光素和标记生物素的
引物不是同一条引物。
66.在一些实施方式中,所述第一组引物包括:核苷酸序列如seq id no:11-12所示的置换引物对a,核苷酸序列如seq id no:13-14所示的交叉内引物对a,核苷酸序列如seq id no:15-20所示的三组扩增引物对a;
67.本技术实施例中,比常规的引物,第一组引物可识别靶基因的10个特定区域,具有更加灵敏、特异的优势。
68.在一些实施方式中,所述第二组引物包括:核苷酸序列如seq id no:21-22所示的置换引物对b,核苷酸序列如seq id no:23-24所示的交叉内引物对b,核苷酸序列如seq id no:25-30所示的三组扩增引物对b;
69.本技术实施例中,比常规的引物,第二组引物可识别靶基因的10个特定区域,具有更加灵敏、特异的优势。
70.在一些实施方式中,所述第三组引物包括:核苷酸序列如seq id no:31-32所示的置换引物对c,核苷酸序列如seq id no:33-34所示的交叉内引物对c,核苷酸序列如seq id no:35-40所示的三组扩增引物对c;
71.本技术实施例中,比常规的引物,第三组引物可识别靶基因的10个特定区域,具有更加灵敏、特异的优势。
72.在一些实施方式中,所述第四组引物包括:核苷酸序列如seq id no:41-42所示的置换引物对w135,核苷酸序列如seq id no:43-44所示的交叉内引物对w135,核苷酸序列如seq id no:45-50所示的三组扩增引物对w135。
73.本技术实施例中,比常规的引物,第三组引物可识别靶基因的10个特定区域,具有更加灵敏、特异的优势。
74.具体地,第一组引物为针对特异基因sacb的引物,第二组引物为针对特异基因siad的第一区域,根据cp002424.1;第三组引物为针对特异基因siad的第二区域,根据am421808.1;第四组引物为针对特异基因syng的引物。检测时,可以对血清群的分型做几组平行实验,以检测脑膜炎奈瑟菌为哪种血清群。
75.根据本发明另一种典型的实施方式,提供了一种基于多交叉置换扩增检测脑膜炎奈瑟菌的检测器具,所述检测器具的组成部件包括:样品垫、金标垫、纤维膜、吸水垫及背板,所述样品垫、金标垫、纤维膜及吸水垫依次组装在背板上;
76.所述金标垫中物质包括:金纳米粒子偶联的链霉素亲和素;所述纤维膜中物质包括:含抗异硫氰酸荧光素的捕获抗体和生物素偶联的牛血清蛋白;所述检测器具还包括:如权利要求1-7任意一项所述的引物,用于对待检测物进行mcda扩增。
77.根据本发明另一种典型的实施方式,提供了一种基于多交叉置换扩增的脑膜炎奈瑟菌及其血清群的检测方法,所述方法包括以下步骤:
78.得到第一方面所述引物;
79.在所述引物的扩增引物中,任意一条扩增引物的5’端标记异硫氰酸荧光素,任意一条扩增引物的5’端标记生物素,得到标识有异硫氰酸荧光素和生物素的第三引物;
80.将待检测物与所述第三引物进行mcda扩增,得到双标mcda产物;
81.对所述双标mcda产物进行金纳米检测,判断所述待检测物是否有脑膜炎奈瑟菌及其血清群。
82.本技术的检测方法的原理在于:将第一mcda产物直接滴加到待检测区域,当第一mcda产物中的扩增产物的生物素标记端与金纳米粒子偶联的链霉素亲和素(sa-gnp)反应,当第一双标反应产物继续运动,第一双标反应产物的异硫氰酸荧光素标记端与检测线区域的捕获抗体结合,将反应后的双标产物固定在检测线区域,随着双标产物在检测线区域的积累,通过另一端的金纳米粒子偶联的链霉素亲和素(sa-gnp)进行显色反应,从而对mcda产物进行可视化检测。此外,过剩的金纳米粒子偶联的链霉素亲和素(sa-gnp)可与质控区域的生物素偶联的牛血清蛋白(b-bsa),进行直接显色反应,判断功能是否正常。
83.下面将结合实施例、对比例及实验数据对本发明的方法进行详细说明。
84.本技术中所涉及的试剂及设备:脱氧核糖核酸恒温扩增试剂盒(dnaamplificationkit)和金纳米生物传感器购于天津汇德鑫科技发展有限公司。dna提取试剂盒(dna mini kit)购于德国qiagen公司。d2000dna marker购于天根生化科技(北京)有限公司。其余试剂均为市售分型纯产品。
85.本技术实验中使用的主要仪器:恒温实时浊度仪la-320c(eiken chemical co.,ltd,japan)购于日本荣研公司;pcr仪为quantstudio 3,美国abi产品;电泳设备为北京君意东方电泳设备有限公司产品;凝胶成像系统为bio-radgeldoxxr,美国bio-rad产品。
86.本技术实验中所用菌株来自于北京大学首钢医院检验科和安徽省疾病预防控制中心分离培养鉴定后的保存菌株、标准菌株及北京市质控菌株(表1)。
87.表1。
88.[0089][0090]
实施例1引物设计
[0091]
针对脑膜炎奈瑟菌特异基因ctra和血清群a、血清群b、血清群c、血清群w135特异基因sacb、siad、siad、syng设计了五组引物用于mcda扩增,每组引物包括5对引物,包括:一对交叉内引物、一对置换引物、三对扩增引物,所述扩增引物中,任意一条引物的5’端标记异硫氰酸荧光素,任意一条引物的5’端标记生物素。设计示意图见图2。引物序列及修饰见表2。
[0092]
表2。
[0093]
[0094]
[0095]
[0096][0097]
表中,ad1*,5’端标记生物素(biotin);c1*,5’端标记异硫氰酸荧光素(fitc)。
[0098]bnt,nucleotide,核苷酸;mer,monomeric unit,单体单元。
[0099]
实施例3mcda扩增
[0100]
mcda扩增的标准mcda反应体系:置换引物f1和置换引物f2的浓度为0.4μm,扩增引物包括:c1*,c2,d1*,d2,r1和r2,扩增引物的浓度均为0.8μm,交叉内引物cp1和cp2的浓度为1.6μm,12.5μl的2
×
反应缓冲液,1.25μl的bstdna聚合酶(bst2.0),1μl的dna模板,补加去离子水至25μl。扩增引物c1*和扩增引物d1*,5’端分别标记有异硫氰酸荧光素和生物素。整个体系恒温反应60min(脑膜炎奈瑟菌和血清群a、血清群b、血清群c和血清群w135的恒温反应,反应的温度分别为65℃、61℃、59℃、60℃、56℃)。
[0101]
以脑膜炎奈瑟菌-mcda为例:在标准反应体系条件下,加入针对脑膜炎奈瑟菌模板对应的mcda引物,模板量为10pg/反应。反应在不同的恒温条件下进行(62℃-67℃),结果运用实时浊度仪进行检测,可得到mcda引物的扩增动态曲线图(图6)。如图6所示,在不同的温度下均可见到稳健的扩增曲线。根据扩增曲线峰出现的最早时间,推荐65℃作为适宜于本次专利涉及的脑膜炎奈瑟菌-mcda扩增的最佳反应温度。血清群a、血清群b、血清群c和血清群w135的最佳反应温度分别为61℃、59℃、60℃、56℃。
[0102]
实施例4基于多交叉置换扩增检测脑膜炎奈瑟菌的传感器
[0103]
传感器的组成部分:如图3所示,lfb包含五个部分,样品垫,金标垫,纤维膜,吸水垫及背板。首先将样品垫,金标垫,纤维膜及吸水垫依次组装在背板上。然后将金纳米粒子偶联的链霉素亲和素(sa-gnp),抗异硫氰酸荧光素抗体(anti-fitc),及生物素偶联的牛血清蛋白(b-bsa)依次包被在金标垫、检测线(tl)及控制线(cl),待干燥后备用。
[0104]
lfb的检测原理:将mcda产物0.5μl直接滴加到lfb的样品垫区域,然后将2-3滴检测缓冲液加到样品垫区域,mcda产物在虹吸作用下,从样品垫向吸收垫方向运动。当mcda产物达到金标垫后,双标产物的一端(即生物素标记端)与金纳米粒子偶联的链霉素亲和素(sa-gnp)反应。当产物继续运动,双标产物的另一端(即异硫氰酸荧光素标记端)与检测线区域的抗体结合,将双标产物固定在检测线区域。随着产物在检测线区域的积累,通过另一端的金纳米粒子偶联的链霉素亲和素(sa-gnp)进行显色反应,从而对mcda产物进行可视化检测。此外,过剩的金纳米粒子偶联的链霉素亲和素(sa-gnp)可与cl(质控线)区域的生物素偶联的牛血清蛋白(b-bsa),进行直接显色反应,判断lfb的功能是否正常。
[0105]
每次mcda反应体系包括:10条引物,识别靶序列的10个区域,包括2条交叉内引物,即cp1和cp2(cross primer,cp);2条置换引物,即f1和f2;6条扩增引物,即d1,c1,r1,d2,c2和r2。为了构建可检测产物,在引物c1的5’端标记半抗原如异硫氰酸荧光素(fitc),在引物d1的5’端标记生物素(biotin),新标记的引物被命名为c1*和d1*。cp1包含cls(c1区域的互补序列)和p1,即5
′‑
cls-p1;cp2包含c2s(c2区域的互补序列)和p2,即5
′‑
c2s-p2。两条交叉
内引物cp1和cp2是介导mcda扩增的主要引物;置换引物f1和f2在mcda反应中发挥置换作用,置换交叉内引物cp1和cp2;六条扩增引物d1*,c1*,r1,d2,c2和r2能够加速mcda反应及增加mcda产物量,见图2。
[0106]
双标产物能被金纳米生物传感器检测,从而进行可视检测(图3)。因此,利用mcda-lfb技术进行靶序列检测时,可利用c1*和d1*引物构建可检测产物。
[0107]
实施例5验证mcda引物的可行性
[0108]
mcda扩增之后,两种检测方法用于mcda扩增结果的判别(图4-5)。首先,通过lfb对产物进行检测。其次,mcda产物可以通过琼脂糖凝胶电泳后检测扩增子,由于产物中包含了不同大小的扩增片段,因此阳性扩增产物的电泳条带呈阶梯状,阴性反应不出现任何扩增条带。
[0109]
lfb检测:将mcda扩增产物进行lfb检测。由于针对靶基因的mcda引物c1和d1标记了异硫氰酸荧光素(fitc)和生物素(biotin),因此,当tl和cl区域均出现紫红色条带时表示靶基因检测阳性。通过lfb判读mcda扩增结果,阳性对照出现了预期的结果,而阴性对照和空白对照仅在cl区域出现紫红色条带,验证了本研究设计的mcda-lfb技术及mcda引物可行,可用于靶序列的扩增检测(图4)。
[0110]
电泳检测:将mcda扩增产物进行电泳检测,由于mcda扩增产物包含了许多大小不一的短片段及一系列反向重复的靶序列构成的茎环结构和多环花椰菜样结构的dna片段混合物,电泳后在凝胶上显现不同大小区带组成的阶梯式图谱,见图5。通过电泳检测法判读mcda扩增结果,阳性反应出现了预期的结果,而阴性反应和空白对照未出现任何扩增条带,进一步验证了本研究设计的mcda引物可行,可用于靶序列的扩增检测。
[0111]
实施例6mcda-lfb检测脑膜炎奈瑟菌及其血清群的灵敏度
[0112]
以脑膜炎奈瑟菌-mcda为例:运用连续稀释好的脑膜炎奈瑟菌基因组dna进行标准的mcda扩增反应后,两种检测方法用于mcda扩增结果判别。
[0113]
首先,通过lfb检测mcda产物(图7)。结果显示:脑膜炎奈瑟菌-mcda的检测范围低至10fg,在tl和cl区域均出现紫红色条带。而当反应体系中脑膜炎奈瑟菌基因组dna含量为1fg及以下,或无脑膜炎奈瑟菌基因组dna模板时,仅在cl区域出现紫红色条带,表示阴性结果。血清群a、b、c、w135-mcda的检测下限分别为10fg、100fg、100fg、100fg。
[0114]
其次,通过琼脂糖凝胶电泳检测mcda产物(图8)。由于产物中包含了大小不同的扩增片段,因此阳性扩增产物的电泳条带呈阶梯状,阴性反应则不出现任何扩增条带。电泳检测显示:脑膜炎奈瑟菌-mcda的检测范围低至10fg,阳性反应出现阶梯状条带。而当反应体系中脑膜炎奈瑟菌基因组dna含量为1fg及以下,或无脑膜炎奈瑟菌基因组dna模板时,则不出现任何扩增条带,为阴性结果。血清群a、b、c、w135-mcda的检测下限分别为10fg、100fg、100fg、100fg。
[0115]
实施例7测定mcd-lfb技术的特异性
[0116]
以脑膜炎奈瑟菌-mcda为例:以常见的致病菌及条件致病菌dna为模板评价mcda-lfb技术的特异性(菌株信息及检测结果详见表1)。表中1-4号为脑膜炎奈瑟菌血清群a、b、c、w135菌株,lfb检测结果为阳性;表中5-39号为非脑膜炎奈瑟菌菌株,lfb检测结果均为阴性。从表中可以看出mcda-lfb技术能准确的检测脑膜炎奈瑟菌,说明mcda-lfb技术具备较高的特异性。
[0117]
附图1-8的详细说明:
[0118]
如图1所示,为本技术实施例提供的mcda引物设计的位置和方向示意图,其中,展示了10条引物,分别为2条交叉内引物,即cp1和cp2;2条置换引物,即f1和f2;6条扩增引物,即d1,c1,r1,d2,c2和r2;并展示了每条引物的扩增方向,六条扩增引物能够加速mcda反应及增加mcda产物量。
[0119]
如图2所示,为本技术实施例提供的mcda扩增原理示意图,其中,利用c1*和d1*扩增引物构建可检测产物,进行mcda扩增后,所有可检测的产物均含有异硫氰酸荧光素和生物素,可以被检测到。
[0120]
如图3所示,为金纳米生物传感器检测示意图,其中,样品垫,金标垫,纤维膜,吸水垫及背板。首先将样品垫,金标垫,纤维膜及吸水垫依次组装在背板上。然后将金纳米粒子偶联的链霉素亲和素(sa-gnp),抗异硫氰酸荧光素抗体(anti-fitc),及生物素偶联的牛血清蛋白(b-bsa)依次包被在金标垫、检测线(tl)及控制线(cl),待干燥后备用。待检测物滴加于样品垫上。
[0121]
如图4所示,为本技术实施例提供的mcda引物验证lfb检测结果图谱,其中,横坐标中,mcda产物为用针对脑膜炎奈瑟菌或其血清群特异基因的5对引物与待检测物扩增的产物,a、b、c、w135、nc、nc和bc代表的意思为待检测物为血清群a菌株、血清群b菌株、血清群c菌株、血清群w135菌株、阴性对照菌株、阴性对照菌株和空白对照;纵坐标中,nm、a、b、c和w135代表的意思为脑膜炎奈瑟菌、血清群a、血清群b、血清群c和血清群w135-mcda,例如,纵坐标和横坐标均为a时,此时的金纳米生物传感器有两横,即tl和cl区域均出现紫红色条带,表示靶基因检测阳性,代表了血清群a-mcda可精准检测血清群a菌株,例如,纵坐标为a横坐标为b、c、w135、nc时,此时的金纳米生物传感器有一横,即tl区域未出现紫红色条带,代表了血清群a-mcda无法检出除血清群a菌株以外的其他血清群菌株和其他非脑膜炎奈瑟菌菌株,说明了血清群a-mcda引物可行,可用于精准检测血清群a。
[0122]
如图5所示,为本技术实施例提供的mcda引物验证电泳检测结果图谱,图中,a、b、c、w135、nc、nc和bc代表的意思为待检测物为血清群a菌株、血清群b菌株、血清群c菌株、血清群w135菌株、阴性对照菌株、阴性对照菌株和空白对照;图a、图b、图c、图d和图e代表的意思为脑膜炎奈瑟菌、血清群a、血清群b、血清群c和血清群w135-mcda,图a中,a、b、c、w135通过电泳检测法判读mcda扩增呈阳性,nc、nc和bc呈阴性,说明了脑膜炎奈瑟菌-mcda引物可行,可用于精准检测脑膜炎奈瑟菌;图b、图c、图d和图e中,依次只有相应的血清群具有阳性结果,说明了各血清群-mcda引物可行,可用于精准检测各血清群。
[0123]
如图6所示,本技术实施例提供的mcda最佳反应温度测试结果图谱,其中,横坐标为时间,单位为分钟:秒,纵坐标为浊度(650nm处),图a、图b、图c、图d、图e和图f中的mcda扩增温度依次为62℃、63℃、64℃、65℃、66℃和67℃,如图a-f所示,均可见稳健的扩增曲线,根据扩增曲线起峰时间及扩增曲线线型高度确定最佳反应温度,例如图d中,扩增曲线起峰时间最早,线型高度最高,因此选择65℃作为脑膜炎奈瑟菌-mcda的最佳反应温度。
[0124]
如图7所示,为本技术实施例提供的mcda检测脑膜炎奈瑟菌及其血清群的灵敏度的lfb检测结果图谱,图中,横纵标为1ng、100pg、10pg、1pg、100fg、10fg、1fg和bc,bc代表了空白对照,纵坐标中,nm、a、b、c和w135代表的意思为脑膜炎奈瑟菌、血清群a、血清群b、血清群c和血清群w135-mcda,例如,纵坐标为c,横坐标为10fg、1fg和bc,此时的金纳米生物传感
器有一横,即tl区域未出现紫红色条带,代表了模板量小于等于10fg时血清群c-mcda无法检出待检测物;例如,纵坐标为c,横坐标为100fg,此时的金纳米生物传感器有两横,即tl和cl区域均出现紫红色条带,代表了模板量大于等于100fg时血清群c-mcda可有效检出待检测物。
[0125]
如图8所示,本技术实施例提供的mcda检测脑膜炎奈瑟菌及其血清群的灵敏度的电泳检测结果图谱,图a、图b、图c、图d和图e分别代表了脑膜炎奈瑟菌、血清群a、血清群b、血清群c和血清群w135-mcda,图中,横坐标为待检测物的含量,依次为1ng、100pg、10pg、1pg、100fg、10fg、1fg和bc,bc代表了空白对照,纵坐标为dna分子量标准,由图a可知脑膜炎奈瑟菌-mcda的检测下限为10fg,由图b可知血清群a-mcda的检测下限为10fg,由图c可知血清群b-mcda的检测下限为100fg,由图d可知血清群c-mcda的检测下限为100fg,由图e可知血清群w135-mcda的检测下限为100fg。
[0126]
需要说明的是,在本文中,诸如“第一”和“第二”等之类的关系术语仅仅用来将一个实体或者操作与另一个实体或操作区分开来,而不一定要求或者暗示这些实体或操作之间存在任何这种实际的关系或者顺序。而且,术语“包括”、“包含”或者任何其他变体意在涵盖非排他性地包含,从而使得包括一系列要素的过程、方法、物品或者设备不仅包括那些要素,而且还包括没有明确列出的其他要素,或者还包括为这种过程、方法、物品或者设备所固有的要素。在没有更多限制的情况下,由语句“包括一个
……”
限定的要素,并不排除在包括所述要素的过程、方法、物品或者设备中还存在另外的相同要素。
[0127]
以上所述仅是本发明的具体实施方式,使本领域技术人员能够理解或实现本发明。对这些实施例的多种修改对本领域的技术人员来说将是显而易见的,本文中所定义的一般原理可以在不脱离本发明的精神或范围的情况下,在其他实施例中实现。因此,本发明将不会被限制于本文所示的这些实施例,而是要符合与本文所申请的原理和新颖特点相一致的最宽的范围。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。
