1.本发明涉及海洋天然产物领域,具体涉及氯代间苯二酚醛类化合物及其在制备破骨细胞分化抑制剂中的应用。
背景技术:
2.骨质疏松症是老龄化人群和绝经后女性中常见的溶骨性疾病。骨骼是一种高度动态的组织,会不断重塑,并通过破骨细胞负责的骨吸收和成骨细胞负责的骨形成过程达到代谢平衡。破骨细胞(osteoclasts,ocs)是由单核细胞/巨噬细胞造血谱系前体细胞融合形成的特殊细胞,是人体内唯一具有骨吸收功能的细胞。破骨细胞活性缺陷导致骨硬化和骨髓衰竭,过度激活可导致骨质疏松症、类风湿性关节炎、肿瘤骨转移等溶骨性疾病。因此,靶向抑制破骨细胞形成和骨吸收的分子成为防治骨破坏性相关疾病的研究热点。海洋微生物是发现新型药源分子的新理想资源,关于海洋微生物天然产物抗破骨细胞分化抑制剂的研究报道较少,故其抗破骨细胞分化潜力有待进一步挖掘。
3.破骨细胞的形成是一个逐步过程,由核因子-κb受体活化因子配体(receptor activator of nuclear kappa b ligand,rankl)的受体激活剂与其在单核细胞/巨噬细胞前体上的受体rank结合而启动。目前临床上运用的破骨细胞分化相关抑制剂主要为地诺昔单抗和双膦酸盐类药物,但都具有一定的并发症和副作用。因此,亟需寻找一种安全、有效、质量可控、经济的靶向抑制破骨细胞形成和骨吸收的药物,有效解决临床上对于破骨细胞分化抑制剂的巨大需求。
技术实现要素:
4.本发明的第一个目的是,针对上述问题,提供两个氯代间苯二酚醛类化合物orsaldechlorins a
–
b(1
–
2)。
5.为达到上述目的,本发明所采用的技术方案是:
6.本发明的化合物orsaldechlorins a
–
b(1
–
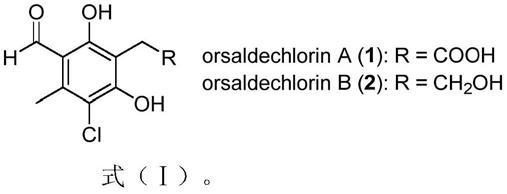
2)的结构式如式(ⅰ)所示:
[0007][0008]
本发明的第二个目的是,针对上述问题,提供一种制备化合物orsaldechlorins a
–
b(1
–
2)的方法,所述的化合物orsaldechlorins a
–
b(1
–
2)是从菌核生枝顶孢霉(acremonium sclerotigenum)c2f21的发酵培养物中制备分离得到的。
[0009]
在本发明中,进一步说明,所述的制备化合物orsaldechlorins a
–
b(1
–
2)的方法,具体步骤如下:
[0010]
a)、制备菌核生枝顶孢霉(acremonium sclerotigenum)c2f21的发酵培养物,用乙酸乙酯浸泡发酵培养物,将发酵物切成小块,超声提取15min,用布氏漏斗过滤,滤液经蒸馏浓缩后得到浸膏a;滤渣继续用乙酸乙酯提取3遍,经蒸馏浓缩后得到浸膏b;
[0011]
b)、将浸膏a和浸膏b合并的粗提物经中压正相液相色谱,用石油醚/二氯甲烷作为洗脱剂,从体积比100:0~0:100进行梯度洗脱,收集石油醚/二氯甲烷体积比70:30梯度洗脱下来的流份,继续过中压反相c
18
柱色谱,用甲醇/水作为洗脱剂,从体积比10:90~100:0进行梯度洗脱,收集甲醇/水体积比25:75梯度洗脱下来的流份,收集流份再经纯化后得到化合物orsaldechlorins a
–
b(1
–
2)。
[0012]
在本发明中,进一步说明,所述的步骤a)的制备菌核生枝顶孢霉(acremonium sclerotigenum)c2f21的发酵培养物是将活化的菌核生枝顶孢霉(acremonium sclerotigenum)c2f21接入种子培养基中,25℃,180rpm,培养72h制得种子液,将种子液以5%的接种量接入到发酵培养基中,25℃,静态培养30天制得发酵培养物。
[0013]
在本发明中,进一步说明,所述的种子培养基配方为每1l升培养基中含有:麦芽提取粉15g,粗海盐20g,余量为水,ph 7.5。
[0014]
在本发明中,进一步说明,所述的发酵培养基的配方为每1l三角瓶培养基中含有:大米120g,细菌学蛋白胨1.5g,粗海盐3g,水150ml,ph 7.5。
[0015]
本发明的第三个目的是提供菌核生枝顶孢霉(acremonium sclerotigenum)c2f21在制备化合物orsaldechlorins a
–
b(1
–
2)中的应用。
[0016]
本发明通过实验得到:化合物orsaldechlorins a
–
b(1
–
2)对lps诱导的nf-κb荧光素酶具有显著抑制作用,半抑制浓度(ic
50
值)分别为15μm和19μm,可以作为研制nf-κb核因子表达抑制剂的先导化合物。
[0017]
本发明通过实验得到:化合物orsaldechlorins a
–
b(1
–
2)呈浓度梯度地抑制rankl诱导的bmms(bone marrow macrophage cells,骨髓巨噬细胞)细胞分化成破骨细胞,且对bmms细胞无明显细胞毒性,因此可望开发成为安全有效的新型破骨细胞分化抑制剂药物。
[0018]
本发明的第四个目的是提供化合物orsaldechlorins a
–
b(1
–
2)或其药用盐在制备nf-κb核因子表达抑制剂或破骨细胞分化抑制剂药物中的应用。
[0019]
本发明的第五个目的是提供两个nf-κb核因子表达抑制剂或破骨细胞分化抑制剂药物,包括有效量的作为活性成份的化合物orsaldechlorins a
–
b(1
–
2)或其药用盐,和药学上可以接受的载体或辅剂。
[0020]
由于采用上述技术方案,本发明具有以下有益效果:
[0021]
本发明在对广西北部湾鹿角杯形珊瑚(pocillopora damicornis)共附生菌核生枝顶孢霉(acremonium sclerotigenum)c2f21的次生代谢产物的研究过程中,分离获得两个新颖氯代间苯二酚醛类化合物orsaldechlorins a
–
b(1
–
2),其对lps诱导的nf-κb荧光素酶具显著抑制作用(ic
50
值分别为15μm和19μm),呈浓度梯度下抑制rankl诱导的bmms细胞分化成破骨细胞,因此是开发成为新型nf-κb核因子表达抑制剂或破骨细胞分化抑制剂药物的理想候选化合物。
附图说明
[0022]
图1是化合物orsaldechlorins a
–
b(1
–
2)的化学结构及其关键的hmbc(箭头)相关图;其中a)为orsaldechlorins a
–
b(1
–
2)的化学结构说明,b)为hmbc关键相关说明;
[0023]
图2是化合物orsaldechlorin a(1)的铜靶单晶衍射示意图;
[0024]
图3是化合物orsaldechlorins a
–
b(1
–
2)(20μm)对在raw264.7细胞经脂多糖(lps)诱导的nf-κb荧光素酶的抑制活性对比图,其中,图中标号1为化合物orsaldechlorin a(1),标号2为化合物orsaldechlorin b(2),
###
表示p《0.001vs.control group;***表示p《0.001vs.lps group;
[0025]
图4是化合物orsaldechlorins a
–
b(1
–
2)对破骨前体bmms细胞分化的trap染色结果示意图;
[0026]
图5是化合物orsaldechlorins a
–
b(1
–
2)对破骨前体bmms细胞分化的影响结果图;
[0027]
图6是化合物orsaldechlorins a
–
b(1
–
2)对破骨前体bmms细胞活力图(72h)。
具体实施方式
[0028]
为了使本发明的目的、技术方案及优点更加清楚明白,以下结合实施例和附图,对本发明进行进一步详细说明。应当理解,此处所描述的具体实施例仅仅用以解释本发明,并不用于限定本发明。
[0029]
实施例1菌核生枝顶孢霉(acremonium sclerotigenum)c2f21
[0030]
从采自中国广西北部湾的鹿角杯形珊瑚(pocillopora damicornis)分离得到菌核生枝顶孢霉(acremonium sclerotigenum)c2f21,于2019年05月20日保藏于广东省微生物菌种保藏中心(gdmcc),地址:广东省广州市先烈中路100号广东省微生物研究所59号楼五楼,广东省微生物研究所,保藏编号为:gdmcc no.60670。
[0031]
实施例2化合物orsaldechlorins a
–
b(1
–
2)的制备和分离
[0032]
1、培养
[0033]
1.1、种子培养基:每1l升培养基中含有麦芽提取粉15g,粗海盐20g,余量为水,ph7.5。按上述组份和含量混合均匀,然后121℃,灭菌30min备用。
[0034]
1.2、发酵培养基:每1l三角瓶培养基中含有:大米120g,细菌学蛋白胨1.5g,粗海盐3g,水150ml,ph 7.5。按上述组份和含量混合均匀,然后121℃,灭菌30min备用。
[0035]
2、发酵
[0036]
2.1、种子培养:将活化的菌核生枝顶孢霉(acremonium sclerotigenum)c2f21接入每瓶含有300ml种子培养基的1l的三角培养瓶中,25℃,180rpm,培养72h制得种子液。
[0037]
2.2、发酵培养:将种子液以5%的接种量(体积百分比)接入到48瓶发酵培养基三角瓶中,25℃,静态培养30d,制得发酵培养物。
[0038]
3、提取:用乙酸乙酯浸泡发酵培养物,将发酵培养物切成小块,超声破碎提取15min,采用布氏漏斗过滤,滤液经蒸馏浓缩后得到浸膏a;滤渣继续用乙酸乙酯提取3遍,经蒸馏浓缩后得到浸膏b,合并浸膏a和浸膏b得总提取物(100g)。
[0039]
4、化合物orsaldechlorins a
–
b(1
–
2)的分离纯化
[0040]
将浸膏a和浸膏b合并的粗提物(100g)经中压正相柱层析液相色谱(mplc),用石油
醚/二氯甲烷作为洗脱剂,从体积比100:0~0:100进行梯度洗脱,收集石油醚/二氯甲烷体积比为70:30洗脱的流份(2.5g),继续过中压反相c
18
柱色谱,用甲醇/水作为洗脱剂,从体积比10:90~100:0进行梯度洗脱,收集甲醇/水体积比25:75梯度洗脱下来的流份,收集流份采用hplc-dad检测收集最大吸收波长在220和290nm左右吸收的流份,该流份最后用半制备高效液相精细分离,在洗脱体系为甲醇/水(体积比50:50,ymc-pack ods-a色谱柱,10
×
250mm,5μm,2ml/min)进行纯化后得到化合物orsaldechlorin a(1)(6mg)和orsaldechlorin b(2)(2mg)。
[0041]
实施例3化合物orsaldechlorins a
–
b(1
–
2)的结构鉴定
[0042]
结构鉴定:化合物orsaldechlorin a(1)为无色针状晶体。高分辨质谱hr-esims给出一个m/z 245.0199[m h]
(calcd for c
10h10
clo5,245.0217)的准分子离子峰,推测其分子式为c
10
h9clo5。其核磁数据归属如表1所示,显示为含氯取代的间苯二酚醛结构,包括1个单峰甲基(δ
h/c 2.58/14.5),1个亚甲基(δ
h/c 3.53/28.5),1个醛基(δ
h/c 10.12/195.1),1个羟基(δ
h 12.84),1个羰基(δ
c 171.8)以及6个芳香碳[(δ
c 112.5,108.8,113.7,139.6)和2个连氧的(δ
c 161.4,158.9)]。hmbc谱图(图1)中h
2-9/c-2,c-3,c-4,c-10相关说明苯环3位所连的亚甲基与1个羰基相连,结合其分子式判断其为一个羧基。以上推断出的结构最后通过x-ray单晶衍射分析加以证实(图2)。
[0043]
结构鉴定:化合物orsaldechlorin b(2)为白色固体。高分辨质谱hr-esims给出一个m/z 253.0238[m na]
(calcd for c
10h11
clo4na,253.0244)的准分子离子峰,推测其分子式为c
10h11
clo4,含5个不饱和度。其核磁数据归属如表1所示,将其与化合物orsaldechlorin a(1)的核磁数据进行对比,发现两者具有极其相似的化学结构,主要区别是化合物orsaldechlorin b(2)中10位连羟基的亚甲基(δ
h/c 3.96/63.4)取代了化合物orsaldechlorin a(1)中的羧基(δc171.8),此推断被hmbc谱图中h
2-10/c-9,c-3相关信号及减少的1个不饱和度所证实。具体结构式见图1所示。
[0044]
表1.化合物orsaldechlorins a
–
b(1
–
2)的1h-和
13
c-nmr数据归属。
[0045][0046]
a 175mhz,
b 700mhz,
c 150mhz,
d 600mhz
[0047]
化合物orsaldechlorin a(1):无色针状晶体;uv(meoh)λ
max
(logε)335(3.60),291(3.86),226(3.97),211(3.93)nm;ir(film)ν
max 3392,2947,1716,1697,1653,1635,1616,
1575,1558,1506,1456,1251,1205cm-1
;hr-esims m/z 245.0199[m h]
(calcd for c
10h10
clo5,245.0217),267.0017[m na]
(calcd for c
10
h9clnao5,267.0036).
[0048]
化合物orsaldechlorin a(1)的单晶数据:2
·c10
h9clo5·
ch3oh,mr=521.28,crystal size 0.05
×
0.08
×
0.03mm3,orthorhombic,α=90
°
,β=90
°
,γ=90
°
,t=104(7)k,space group pbca,z=8,μ(cukα)=3.229mm-1
,12912reflections collected,4284independent reflections(r
int
=0.1029).the final r
1 values were0.1217(i》2σ(i)).the final wr(f2)values were 0.3401(i》2σ(i)).the final r
1 values were 0.1675(all data).the final wr(f2)values were 0.3853(all data).the goodness of fit on f
2 was 1.334.化合物orsaldechlorin a(1)的x-射线单晶衍射图见图2。
[0049]
化合物orsaldechlorin b(2):白色固体;uv(meoh)λ
max
(logε)345(3.01),292(3.07),209(4.01)nm;hr-esims m/z 253.0238[m na]
(calcd for c
10h11
clo4na,253.0244).
[0050]
实施例4化合物orsaldechlorins a
–
b(1
–
2)对lps诱导的nf-κb荧光素酶抑制活性测定nf-κb荧光素酶抑制活性测定主要参考文献(british journal of pharmacology,2020,177:4242
–
4260)。
[0051]
取稳定转染nf-κb荧光素酶报告基因的raw264.7细胞接种于96孔板中(1
×
104个/孔),每孔加入含10%胎牛血清、100iu/ml青霉素和链霉素和0.1μg/ml的g418的dmem培养基200μl,待细胞贴壁稳定后,加入化合物orsaldechlorins a
–
b(1
–
2),设置6个复孔。继续孵育4h后,除阴性对照组外,每个化合物组(3孔)和阳性对照组(nf-κb抑制剂,bay11-7082,5μm)分别加入lps和rankl,使其每孔终浓度为100ng/ml,两者刺激8h后,弃掉上清液,每孔加入细胞裂解液25μl,低速震荡10min以充分裂解细胞,然后取20μl转移至白板中,每孔加入荧光素溶液50μl,用多功能酶标仪检测luciferase值。
[0052]
试验结论:研究发现与lps空白组对比,化合物orsaldechlorins a
–
b(1
–
2)在20μm对lps诱导的nf-κb荧光素酶具有显著抑制作用(p《0.001)(图3),半抑制浓度(ic
50
值)分别为15μm和19μm。
[0053]
实施例5化合物orsaldechlorins a
–
b(1
–
2)对rankl诱导的破骨前体bmms细胞分化的影响
[0054]
rankl诱导的破骨前体bmms细胞分化抑制活性测定主要参考文献(british journal of pharmacology,2020,177:4242
–
4260)。
[0055]
取生长状态良好的raw264.7细胞以1
×
103个/孔的密度接种于96孔板中,每孔加入含10%胎牛血清以及100iu/ml青霉素和100iu/ml链霉素的dmem培养基至200μl,然后将96孔板置于37℃、5%co2的细胞培养箱进行孵育,待细胞过夜贴壁稳定后,分别加入化合物orsaldechlorins a
–
b(1
–
2)(5和15μm),每组设3个复孔。4h后,除了阴性对照组外,其余各组都加入rankl,使其终浓度为100ng/ml每孔,每两天换一次液,rankl刺激4-5d后,弃去上清,进行trap染色。在倒置显微镜下拍照并计数,其中细胞核大于3个的trap阳性细胞即为破骨细胞。
[0056]
试验结果:研究发现与rankl组相比,化合物orsaldechlorins a
–
b(1
–
2)呈浓度梯
度地抑制rankl诱导的bmms细胞分化成破骨细胞(图4和图5),且对bmms细胞无明显细胞毒性(图6)。
[0057]
结果讨论:化合物orsaldechlorins a
–
b(1
–
2)对lps诱导的nf-κb荧光素酶具显著抑制作用(ic
50
值分别为15μm和19μm),且在15μm浓度下能显著抑制rankl诱导的bmms细胞分化成破骨细胞,且对bmms细胞无明显毒性作用。可以作为新型破骨细胞分化抑制剂或nf-κb核因子表达抑制剂进行开发,用于防治骨质疏松症等骨溶性疾病。
[0058]
综上,本发明为研制新的破骨细胞分化抑制剂或nf-κb核因子表达抑制剂药物提供了新的候选化合物,对中国自主知识产权的新药开发具有重要的意义。
[0059]
上述说明是针对本发明较佳可行实施例的详细说明,但实施例并非用以限定本发明的专利申请范围。凡本发明所提示的技术构思下所完成的同等变化或修饰变更,均应属于本发明所涵盖专利范围。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。
