一类具有硝基还原酶响应的
β-咔啉喹啉鎓盐及其制备方法和应用
技术领域
1.本发明涉及生物医药技术领域,具体涉及一类具有硝基还原酶响应的β-咔啉喹啉鎓盐及其制备方法和应用。
背景技术:
2.在许多类型的实体肿瘤及其微环境中突出显示的缺氧特征,这些缺氧特性会降低放射疗法或化学疗法的疗效。在肿瘤微环境中,缺氧可以增加肿瘤细胞内很多生物还原反应并导致肿瘤细胞内硝基还原酶(nitroreductase)的过表达。在缺氧条件下,硝基还原酶可利用还原辅酶nadh/nadph提供的电子将芳香硝基类化合物还原为芳香胺类化合物。因此,利用肿瘤组织内过表达的硝基还原酶开发在肿瘤疾病检测的荧光探针具有重要意义。
3.线粒体是细胞内进行有氧呼吸的场所,是细胞中制造能量的细胞器。线粒体通过产生由电子传递链产生的膜电位梯度来驱动atp的合成,从而维持氧化磷酸化作用。线粒体对于肿瘤的发生和维持肿瘤细胞的生长是必不可少的。肿瘤细胞由于线粒体的功能障碍,使得其线粒体比正常细胞具有更高的线粒体膜电位,从而使得亲脂性阳离子对肿瘤更具有选择性。因此,线粒体靶向可被开发用于癌症疾病的诊断和治疗,研究肿瘤细胞或组织内线粒体生理学和功能。
4.同时考虑到激发光源的波长越长,组织穿透能力越强。传统荧光探针仅适用于单光子激发这就使得其传统深度受到一定的限制。具有双光子吸收能力的荧光探针可被两个近红外光子同时激发。因此,与单光子激发的荧光探针相比,具有双光子吸收能力的荧光探针具有更深的组织穿透能力,因而可用于较深处肿瘤成像,同时避免组织自身荧光的干扰。
技术实现要素:
5.本发明提供了一类具有硝基还原酶响应的β-咔啉喹啉鎓盐及其制备方法和应用,该β-咔啉喹啉鎓盐通过在单光子和/或双光子激发下实现体内外肿瘤细胞线粒体靶向和硝基还原酶响应的荧光成像的医药用途,特别是在制备肿瘤荧光成像诊断试剂中的应用。
6.为了实现上述目的,本发明采用的技术方案如下:
7.一类具有硝基还原酶响应的β-咔啉喹啉鎓盐,具有通式ⅰ所示结构:
[0008][0009]
其中,r1表示h、c1-c6烷基、炔基取代的c1-c6烷基、卤代c1-c6烷基、甲氧基取代的c1-c6烷基和吗啉取代的c1-c6烷基中的一种;r2表示h、c1-c6烷基和甲氧基取代的苯基中
的一种;r3表示c1-c6烷基、炔基取代的c1-c6烷基和卤代c1-c6烷基中的一种;y-表示卤负离子、六氟磷酸根负离子、磺酸负离子和甲磺酸负离子中的一种。
[0010]
优选的,所述r1表示h、ch3或ch2ch3;r2表示h、ch3、c(ch3)3或3,4,5-三甲氧基苯基;r3表示ch3、ch2ch3或炔丙基;y-代表卤负离子、六氟磷酸根负离子、磺酸负离子或者甲磺酸负离子。
[0011]
优选的,所述β-咔啉喹啉鎓盐的通式ⅰ部分化合物代号及其对应的结构如下:
[0012]
表1通式ⅰ部分化合物代号及其对应的结构
[0013][0014]
i1:(e)-4-(2-(1,9-二甲基-6-硝基-9h-吡啶并[3,4-b]吲哚-3-基)乙烯基)-1-甲基喹啉-1-鎓碘盐;
[0015]
i2:(e)-4-(2-(1,9-二甲基-6-硝基-9h-吡啶并[3,4-b]吲哚-3-基)乙烯基)-1-(丙-2-炔-1-基)喹啉-1-鎓溴盐;
[0016]
i3:(e)-4-(2-(1-甲基-9-乙基-6-硝基-9h-吡啶并[3,4-b]吲哚-3-基)乙烯基)-1-甲基喹啉-1-鎓六氟磷酸盐;
[0017]
i4:(e)-4-(2-(1-叔丁基-9-甲基-6-硝基-9h-吡啶并[3,4-b]吲哚-3-基)乙烯基)-1-甲基喹啉-1-鎓甲磺酸盐;
[0018]
i5:(e)-4-(2-(1-(3,4,5-三甲氧基苯基)-6-硝基-9h-吡啶并[3,4-b]吲哚-3-基)乙烯基)-1-甲基喹啉-1-鎓碘盐。
[0019]
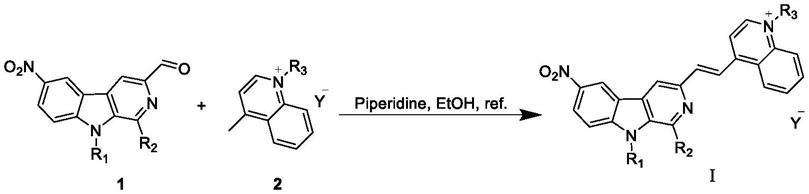
本发明的另一目的是提供一类具有硝基还原酶响应的β-咔啉喹啉鎓盐的制备方法,将9-r
1-6-硝基-1-r
2-9h-吡啶并[3,4-b]吲哚-3-甲醛(化合物1)与喹啉鎓盐(化合物2)在加热条件下发生knoevenagel缩合反应得到。
[0020]
优选的,所述制备方法具体为:
[0021]
将9-r
1-6-硝基-1-r
2-9h-吡啶并[3,4-b]吲哚-3-甲醛(1)与喹啉鎓盐(2)溶于无水乙醇中,滴加催化量的哌啶,回流反应,经重结晶或柱分离纯化得到β-咔啉喹啉鎓盐化合物ⅰ;
[0022]
合成路线如下所示:
[0023][0024]
其中,r1表示h、c1-c6烷基、炔基取代的c1-c6烷基、卤代c1-c6烷基、甲氧基取代的c1-c6烷基和吗啉取代的c1-c6烷基中的一种;r2表示h、c1-c6烷基和甲氧基取代的苯基中的一种;r3表示c1-c6烷基、炔基取代的c1-c6烷基和卤代c1-c6烷基中的一种;y-表示卤负离子、六氟磷酸根负离子、磺酸负离子和甲磺酸负离子中的一种。
[0025]
本发明还提供了一类具有硝基还原酶响应的β-咔啉喹啉鎓盐在制备线粒体靶向和硝基还原酶响应荧光探针中的应用。
[0026]
优选的,所述线粒体靶向和硝基还原酶响应荧光探针可通过在单光子和/或双光子激发下实现线粒体靶向和硝基还原酶响应产生荧光。
[0027]
本发明还提供了一类具有硝基还原酶响应的β-咔啉喹啉鎓盐在制备靶向肿瘤细胞线粒体的荧光成像诊断试剂中的应用。
[0028]
优选的,所述β-咔啉喹啉鎓盐通过硝基还原酶响应,在单光子和/或双光子激发下发挥肿瘤细胞和组织选择性荧光成像。
[0029]
优选的,所述肿瘤为肝癌、结肠癌、乳腺癌、肺癌和宫颈癌中的一种。
[0030]
本发明有益效果:
[0031]
1、本发明在β-咔啉母环的3位通过knoevenagel缩合引入亲脂性阳离子,从而形成具有d-π-a型的结构,进一步延长β-咔啉母环共轭体系,同时在β-咔啉母环的6位引入吸电子基团硝基,且可被肿瘤细胞内硝基还原酶还原从而产生显著荧光,发挥线粒体靶向和硝基还原响应的作用。
[0032]
2、本发明根据肿瘤细胞内硝基还原酶过表达,开发新型具有肿瘤细胞和组织选择性荧光成像的β-咔啉喹啉鎓盐的小分子荧光探针,且具有较好的单光子和双光子吸收性质,实现深层次肿瘤组织选择性荧光成像诊断应用,指导临床术中切除肿瘤,将具有重要的
医药用途前景。
附图说明
[0033]
图1为本发明中化合物经硝基还原酶还原机制;
[0034]
图2为本发明化合物经硝基还原酶激活响应的荧光发射光谱;
[0035]
图3为本发明化合物在硝基还原酶响应还原下的双光子吸收截面图;
[0036]
图4为本发明化合物在肿瘤细胞中的荧光成像;
[0037]
图5为本发明化合物在正常细胞中的荧光成像。
具体实施方式
[0038]
为了进一步阐明本发明,下面给出一系列实施例,这些实施例完全是例证性的,它们仅用来对本发明具体描述,不应当理解为对本发明的限制。
[0039]
实施例1:(e)-4-(2-(1,9-二甲基-6-硝基-9h-吡啶并[3,4-b]吲哚-3-基)乙烯基)-1-甲基喹啉-1-鎓碘盐(i1)的制备;
[0040]
将1,9-二甲基-6-硝基-9h-吡啶并[3,4-b]吲哚-3-甲醛(2.69g,10mmol)和1,4-二甲基喹啉-1-鎓碘盐(2.85g,10mmol)加入单口瓶中,加入5ml无水乙醇,随后加入1滴哌啶,回流过夜。tlc监测反应至完全,冷却至室温,减压浓缩,经柱层析纯化,得到β-咔啉喹啉鎓盐化合物红色固体(i1),产率为61.1%。
[0041]
(i1)谱图数据为:esi-ms(m/z):409[m]
;1h nmr(d
6-dmso,400mhz):δ9.36(d,j=6.5hz,1h,arh),9.30(d,j=2.3hz,1h,arh),8.93(m,2h,2arh),8.61(d,j=6.5hz,1h,arh),8.49(m,2h,2arh),8.31(s,1h,arh),8.12(s,1h,arh),7.98(m,2h,2arh),7.71(m,1h,arh),4.57(s,3h,ch3),4.30(s,3h,ch3),3.17(s,3h,ch3).
[0042]
实施例2:(e)-4-(2-(1,9-二甲基-6-硝基-9h-吡啶并[3,4-b]吲哚-3-基)乙烯基)-1-(丙-2-炔-1-基)喹啉-1-鎓溴盐(i2)的制备;
[0043]
参照实施例1中(i1)的合成方法,由4-甲基-1-(丙-2-炔-1-基)喹啉-1-鎓溴盐代替方法中的1,4-二甲基喹啉-1-鎓碘盐,最后得到红色固体(i2),产率为52.9%。
[0044]
(i2)谱图数据为:esi-ms(m/z):433[m]
;1h nmr(d
6-dmso,400mhz):δ9.29(d,j=6.5hz,1h,ar-h),8.86(d,j=8.5hz,1h,ar-h),8.56
–
8.37(m,3h,ar-h,ch),8.34
–
8.20(m,3h,ar-h,ch),8.12
–
8.04(m,1h,ar-h),7.77(d,j=8.4hz,1h,ar-h),7.72
–
7.63(m,1h,ar-h),7.38
–
7.34(m,1h,ar-h),5.57(m,2h,ch2),4.50(s,3h,ch3),3.15(s,3h,ch3),2.83(s,1h,ch).
[0045]
实施例3:(e)-4-(2-(1-甲基-9-乙基-6-硝基-9h-吡啶并[3,4-b]吲哚-3-基)乙烯基)-1-甲基喹啉-1-鎓六氟磷酸盐(i3)的制备;
[0046]
参照实施例1中(i1)的合成方法,由1-甲基-9-乙基-6-硝基-9h-吡啶并[3,4-b]吲哚-3-甲醛代替方法中的1,9-二甲基-6-硝基-9h-吡啶并[3,4-b]吲哚-3-甲醛,由1,4-二甲基喹啉-1-鎓六氟磷酸盐代替方法中的1,4-二甲基喹啉-1-鎓碘盐,最后得到红色固体(i3),产率为58.3%。
[0047]
(i3)谱图数据为:esi-ms(m/z):423[m]
;1h nmr(d
6-dmso,400mhz):δ9.29(d,j=6.5hz,1h,ar-h),8.86(d,j=8.5hz,1h,ar-h),8.56
–
8.37(m,3h,ar-h,ch),8.34
–
8.20(m,
3h,ar-h,ch),8.12
–
8.04(m,1h,ar-h),7.77(d,j=8.4hz,1h,ar-h),7.72
–
7.63(m,1h,ar-h),7.38
–
7.34(m,1h,ar-h),5.57(m,2h,ch2),4.53(m,2h,ch2),3.15(s,3h,ch3),2.83(s,1h,ch),1.29(s,3h,ch3).
[0048]
实施例4:(e)-4-(2-(1-叔丁基-9-甲基-6-硝基-9h-吡啶并[3,4-b]吲哚-3-基)乙烯基)-1-甲基喹啉-1-鎓甲磺酸盐(i4)的制备;
[0049]
参照实施例1中(i1)的合成方法,由1-叔丁基-9-甲基-6-硝基-9h-吡啶并[3,4-b]吲哚-3-甲醛代替方法中的1,9-二甲基-6-硝基-9h-吡啶并[3,4-b]吲哚-3-甲醛,最后得到红色固体(4),产率为53.7%。
[0050]
(i4)谱图数据为:esi-ms(m/z):451[m]
;1h nmr(d
6-dmso,400mhz):δ9.36(d,j=6.5hz,1h,arh),9.30(d,j=2.3hz,1h,arh),8.93(m,2h,2arh),8.61(d,j=6.5hz,1h,arh),8.49(m,2h,2arh),8.31(s,1h,arh),8.12(s,1h,arh),7.98(m,2h,2arh),7.71(m,1h,arh),4.57(s,3h,ch3),4.30(s,3h,ch3),1.35(s,9h,3ch3).
[0051]
实施例5:(e)-4-(2-(1-(3,4,5-三甲氧基苯基)-6-硝基-9h-吡啶并[3,4-b]吲哚-3-基)乙烯基)-1-甲基喹啉-1-鎓碘盐(i5)的制备;
[0052]
参照实施例1中(i1)的合成方法,由1-(3,4,5-三甲氧基苯基)-6-硝基-9h-吡啶并[3,4-b]吲哚-3-甲醛代替方法中的1,9-二甲基-6-硝基-9h-吡啶并[3,4-b]吲哚-3-甲醛,最后得到红色固体(i5),产率为50.4%。
[0053]
(i5)谱图数据为:esi-ms(m/z):547[m]
;1h nmr(d
6-dmso,400mhz):δ10.1(s,1h,nh),9.36(d,j=6.5hz,1h,arh),9.30(d,j=2.3hz,1h,arh),8.93(m,2h,2arh),8.61(d,j=6.5hz,1h,arh),8.49(m,2h,2arh),8.31(s,1h,arh),8.12(s,1h,arh),7.98(m,2h,2arh),7.71(m,1h,arh),7.45(s,1h,arh),7.32(s,1h,arh),4.30(s,3h,ch3),3.83(s,9h,3och3).
[0054]
实施例6:本发明化合物基于硝基还原酶响应的荧光光谱测试;
[0055]
将本发明化合物i1,i2,i3溶于含1%dmso的水溶液中,可以经硝基还原酶响应下还原硝基基团,生成相应的氨基还原产物(酶响应机制如图1),i1,i2,i3的还原产物经质谱确证其正离子峰分别为379、403、393[m]
。且在630~680nm左右的荧光峰值在硝基还原酶处理后明显增强,其峰值与酶响应之前相差5~8倍(图2);此外,化合物i1在630nm左右的荧光峰值随硝基还原酶处理时间增加而不断增强,结果表明本发明荧光化合物具有硝基还原酶响应的荧光。
[0056]
实施例7:采用飞秒荧光测量技术检测硝基还原酶响应下的双光子吸收截面
[0057]
将本发明化合物i1溶于含有硝基还原酶的pbs缓冲液中(5μm),经硝基还原酶的响应还原,检测其经酶响应溶液和对照化合物ru(bpy)
32
从900nm到1060nm的双光子激发下的荧光强度。利用公式:δ=δr
×
(fs
×
фr
×
nr)/(fr
×
фs
×
ns),其中,δ,f,ф和n分别是双光子吸收截面,光谱积分面积,量子产率和浓度;s和r分别代表了本发明化合物经酶响应溶液和对照化合物。计算不同波长下本发明化合物的双光子吸收截面,计算结果表明,本发明化合物经酶响应后,在1000nm具有最大的双光子吸收截面(δmax=114gm)(图3),而在未经酶响应的双光子吸收截面仅有32gm,由此说明本发明化合物具有硝基还原酶响应的双光子激发的荧光特性。
[0058]
实施例8:采用共聚焦显微镜进行线粒体定位实验;
[0059]
采用共聚焦显微镜进行线粒体定位实验,将人肺癌细胞a549、卵巢癌细胞hela、乳腺癌mcf-7、肝癌细胞hepg2和人正常肝细胞lo2、人上肺上皮细胞hfl-1分别由deme培养液在激光共聚焦皿中培养12~24h,再向细胞中加入1~25μm的受试化合物(i1,i2,i4或i5),将其放置置于37℃、含5%co2的细胞培养箱中孵育2~8小时。接着用ph=7.4的磷酸盐缓冲溶液洗涤3次后,再加入1μm的线粒体染色剂mitotracker green溶液并继续孵育半小时后用ph=7.4的磷酸盐缓冲溶液洗涤3次,将孵育好的细胞置于共聚焦显微镜的载物台上进行共聚焦荧光成像,设置mitotracker green:λex=488nm,λem=500-550nm;设置受试化合物激发波长:λex=552nm,λem=550-650nm。结果表明本发明所述化合物(红)能选择性地点亮肿瘤细胞(图4),并在肿瘤细胞中与线粒体染色剂mitotracker green(绿)荧光共定位图像重叠良好,皮尔森系数均比较高(图4),但在正常细胞中荧光成像很弱(图5)。由此表明本发明化合物具有线粒体靶向作用,并且通过硝基还原酶响应发挥肿瘤细胞选择性荧光成像。
[0060]
实施例9:将本发明化合物通过双光子激发对肿瘤组织荧光成像
[0061]
从ht29荷瘤裸鼠制备肿瘤组织切片,将组织切片与本发明化合物i1共培养3h,然后使用dpbs缓冲液洗涤,随后将切片转移到玻璃培养皿中,利用双光子荧光显微镜在双光子960~1080nm激发波长下对肿瘤组织切片进行双光子荧光成像,结果表明本发明化合物i1对肿瘤组织成像深度可达195~250μm,远超过其在单光子激发下对肿瘤组织成像深度(《100μm)。
[0062]
以上对本发明的实施例进行了详细说明,但所述内容仅为本发明的较佳实施例,不能被认为用于限定本发明的实施范围。凡依本发明申请范围所作的均等变化与改进等,均应仍归属于本发明的专利涵盖范围之内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。
