应用消毒剂组合物进行病毒的传播预防
1.关于联邦资金的声明
2.本发明是依据美国国防高级研究计划局(darpa)颁布的hr0011-19-3-0006在政府支持下进行的。美国政府拥有本发明的某些权利。
背景技术:
3.病毒诸如流感,尤其是大规模流行的流感病毒可能在群体中引发包括显著发病率和生产能力损失在内的问题。已经证明,使用疫苗接种难以控制甲型流感。平均每年疫苗仅59%有效,并且通常显著更低。虽然流感病毒本身可能导致死亡,但大多数流感相关的死亡是由于肺炎链球菌、金黄色葡萄球菌、或流感嗜血菌(和其它)(来自一种或多种这些病原体的鼻咽储存器)的肺侵袭(经由流感损伤的气管)由病毒后细菌肺炎导致的。
技术实现要素:
4.本公开的方面涉及一种防止有包膜rna病毒传播的方法。该方法包括根据处理方案向基本上未被有包膜rna病毒定殖的第一哺乳动物受试者的黏膜组织施用有效量的消毒剂组合物或其药学上可接受的盐。基本上未被有包膜rna病毒定殖的第一哺乳动物受试者与被该有包膜rna病毒以第一病毒载量定殖的第二哺乳动物受试者互动。第一哺乳动物受试者具有基于该互动的第二病毒载量。在该处理方案的持续时间内,相比于该初始病毒载量,该第二病毒载量不大于0.5log增加。该黏膜组织在该哺乳动物受试者的鼻咽、口咽、鼻腔、鼻窦或前鼻孔中。消毒剂组合物包含碘、碘伏或它们的组合。在至少一个示例中,不大于0.5log的增加可以如曲线下面积所定义。在另一个示例中,不大于0.5log的增加可以意指对比第0天,在任何给定日第二病毒载量不可能大于0.5log。
5.在另一方面,处理方案可以包括多次(即,多次施用)将消毒剂组合物施用至(第一和/或第二)哺乳动物受试者。
6.在另一方面,将消毒剂组合物施用至第一哺乳动物受试者可以包括在与第二哺乳动物受试者互动之前在任何时间段(例如,至少1小时、至少4小时、至少8小时、至少24小时或大于24小时)向第一哺乳动物受试者施用消毒剂组合物。
7.本公开的其他方面涉及一种防止有包膜rna病毒从哺乳动物受试者传播的方法。该方法可以包括将有效量的消毒剂组合物或该消毒剂组合物的药学上可接受的盐施用至具有第一病毒载量的哺乳动物受试者的黏膜组织持续处理方案的持续时间。该黏膜组织可以在该哺乳动物受试者的鼻咽、口咽、鼻腔、鼻窦或前鼻孔中。该方法可以包括允许有包膜rna病毒因与消毒剂组合物接触而附聚在黏膜组织中或黏膜组织上。当基本上未被有包膜rna病毒定殖的第二哺乳动物受试者与所述哺乳动物受试者互动时,所述哺乳动物受试者在所述处理方案的持续时间期间不将所述有包膜rna病毒传播至所述第二哺乳动物受试者。该消毒剂组合物包含碘、碘伏或它们的组合和增稠剂。该消毒剂组合物可包含10重量%的碘伏。该增稠剂可以被配置成允许消毒剂组合物持久保留在黏膜组织上。
8.本公开的其他方面涉及一种防止病毒传播(诸如有包膜rna病毒,例如,流感或冠
状病毒)的方法。该方法包括根据处理方案在环境温度下向被病毒以第一病毒载量定殖的第一哺乳动物受试者的黏膜组织施用有效量的消毒剂组合物或其药学上可接受的盐,其中该第一哺乳动物受试者被病毒以第一病毒载量定殖。在一些示例中,第一病毒载量不会导致第一哺乳动物受试者的症状。在一些示例中,第一哺乳动物受试者是受体,并且第二哺乳动物受试者是供体,或反之亦然。该方法还可以包括允许被病毒以第二病毒载量定殖的第二哺乳动物受试者与该第一哺乳动物受试者互动,其中该第一哺乳动物受试者被病毒以基于该互动的第三病毒载量定殖。在该处理方案的过程内,相比于该第一病毒载量,该第三病毒载量不大于0.5log增加。
附图说明
9.为了容易地识别对任何特定元件或动作的讨论,参考标号中的一个或多个最高有效数位是指首先引入该元件的附图标号。
10.图1示出了根据一个实施方案的图表。
11.图2示出了根据一个实施方案的图表。
12.图3示出了根据一个实施方案的实验配置。
13.图4示出了根据一个实施方案的图表。
14.图5示出了根据一个实施方案的图表。
具体实施方式
15.本公开的方面可以涉及一种使用成膜含碘组合物处理或预防病毒(诸如流感)的方法。即使在使用成膜聚维酮-碘组合物处理一只哺乳动物后,在一只哺乳动物的鼻孔中的病毒数量增加或基本上保持相同时,成膜含碘组合物可以减少病毒从一只哺乳动物到另一只哺乳动物的传播。
[0016]“环境温度”是指进行本发明方法的环境中的温度。通常,环境温度将为约10℃至约30℃,并且更具体地15℃至25℃。
[0017]“消毒剂”是指杀灭或灭活病原性和非病原性微生物(包括例如细菌和病毒)的化学剂。消毒剂可以是杀细菌剂、杀病毒剂和/或杀真菌剂,其分别杀灭细菌、灭活病毒和杀灭真菌。消毒剂通常广泛地干扰细胞代谢和/或细胞外被膜。抗菌剂有时被称为消毒剂,尤其是当用于处理硬质表面时。
[0018]“抗病毒剂”是指灭活病毒或抑制其复制能力的试剂。许多抗病毒剂是已知的。这些抗病毒剂包括金刚胺(其阻断甲型流感病毒中的病毒颗粒的脱壳)以及干扰核酸合成的多种核苷类似物。核苷类似物的示例包括azt、阿昔洛韦、更昔洛韦和阿糖腺苷。这些药物需要病毒复制以进行灭活。合适的抗病毒剂的示例可以包括奥司他韦、扎那米韦和病毒唑,其可商购获得。
[0019]“有效碘”是指碘伏的碘,其最终作为游离碘(i2)从聚合物释放后是可用的。因此,其包括溶液中的游离碘、可从三碘化物离子获得的双原子碘以及保持在由聚合物结构形成的储存器内的双原子碘。有效碘不包括碘离子。根据美国和英国药典专著,通过硫代硫酸盐滴定测量有效碘。
[0020]“定殖”或“定殖的”是指具有一些病毒存在,无论无症状的、症状发生前的或有症
状的。
[0021]“有效量”是指药物组合物和/或增强剂组分的量,其作为整体提供了减少、防止或消除一种或多种病毒的杀病毒活性,从而导致可接受水平的病毒载量。
[0022]
通常,有效量的消毒剂导致在与病毒或细菌接触30分钟的时间之后,优选地在与病毒或细菌仅接触10分钟的时间之后,最优选地在与病毒或细菌仅接触5分钟的时间之后,至少0.5log下降、至少1log下降、至少1.5log下降或更优选至少2log下降。
[0023]
应当理解,在本文所述的组合物中组分的浓度或含量(当分别考虑时)灭活病毒时可能不能达到可接受的水平,或者可能不能灭活那样广谱的病毒,或可能不如组合物那么快地灭活病毒;然而,当一起使用时,此类组分提供增强的(优选协同的)杀病毒活性(如与在相同条件下单独使用的相同成分相比)。
[0024]“有包膜rna病毒”是指具有病毒包膜的rna病毒。有包膜rna病毒的示例包括黄病毒、甲病毒、披膜病毒、冠状病毒、丁型肝炎、正黏液病毒(包括流感)、副粘病毒、弹状病毒、布尼亚病毒和线状病毒。
[0025]“成膜”是指当允许在环境条件(例如,23℃和50%相对湿度(rh))下在完整皮肤上干燥时形成连续层的组合物,该连续层在组织简单屈曲之后不剥落。
[0026]“感染”是指宿主中病毒的存在和对病毒的宿主响应的组合。感染通常可以导致来自宿主的症状响应。
[0027]“流感”是指甲、乙、丙、丁型流感病毒。甲型流感病毒至少包括h1n1、h2n2、h3n2、h5n1、h7n7、h1n2、h9n2、h7n2、h7n3、h10n7、h7n9、h6n1。
[0028]“接种”是指将病原体诸如病毒引入活生物体中的动作或过程。接种通常可以指将哺乳动物受试者直接(包括经由从另一动物的接触传输)或间接或被动(包括经由来自另一动物的空气传播)地暴露于病毒。接种发生在哺乳动物受试者中可观察到症状之前。
[0029]“互动”是指接触传播,或者在至少两个动物受试者之间的空气传播,或者将病原体从病原体负载表面传播到动物。
[0030]“检测限”是指给出至少三倍基线噪声平均值的响应的病毒的最低浓度。
[0031]“哺乳动物受试者”是指人、绵羊、马、牛、猪、狗、猫、豚鼠、鼬、大鼠、大鼠、小鼠、蝙蝠或其他哺乳动物。
[0032]“黏膜组织”是指鼻腔(包括前鼻孔、鼻咽等)、阴道和其它类似组织的产生粘液的膜状表面。示例包括黏膜,诸如鼻腔、直肠、尿道、输尿管、阴道、子宫颈和子宫的黏膜。
[0033]“保留”是指在正常生理活动期间(例如,呼吸、喷嚏、咳嗽、吐痰)在黏膜组织内或黏膜组织上继续保持病毒的作用。保留可以通过截留、附聚、细胞内存在病毒或它们的组合来进行。“附聚物”或“附聚”是指在感染期间病毒颗粒从细胞释放后不存在将病毒颗粒彼此分离的有效方法时(例如,在不存在流感病毒感染中的有效神经氨酸酶的情况下)可能发生的病毒颗粒的集结。
[0034]“耐久(substantive)”是指消毒剂组合物(或溶液中的成膜聚合物),当被作为均匀湿润膜以大约4毫克/平方厘米(4mg/cm2)内前臂上清洁干燥皮肤的量施用至人类皮肤,并且被彻底干燥(例如在23℃和50%相对湿度下持续至少10分钟)时,其抵抗在流动自来水下的去除,所述流动自来水在约23℃至约24℃的温度以约2.4-2.5升/分钟(l/min)的流速下,从15厘米(cm)的高度落下,冲击干燥组合物正上方的皮肤(而不直接冲在干燥组合物
上),然后流过干燥组合物,持续至少约15秒。
[0035]“症状”是指指示疾病病症的生理特征。流感的症状可以包括流鼻涕、发烧、肌肉酸痛、头痛、发冷、出汗、干咳、疲劳、鼻塞、喉咙痛或它们的组合。症状发作时流感的病毒载量可以是病毒种属依赖性和宿主种属依赖性的。例如,在人类中,病毒载量为至少100000pfu/ml、至少500000pfu/ml或至少1000000pfu/ml可以出现甲型流感的症状。在小鼠中,症状发作时甲型流感的病毒载量可以为至少100pfu/ml。
[0036]“增稠剂”是指增加液体粘度而基本上不改变其其他特性的物质。增稠剂可以是阴离子、阳离子或中性离子。增稠的消毒剂组合物不包括交联的聚合物(即,凝胶)。
[0037]“处理方案”是指一系列的处理。“处理”(“treat”或“treatment”)意指通常根据病症的临床症状或病毒或细菌载量改善受试者有关痛苦的状况。
[0038]“上限摄入水平”是指如由leung am、avram am、brenner av等人所建立的碘的安全摄入水平。过量碘摄入和暴露的潜在风险:由美国甲状腺协会公共卫生委员会(american thyroid association public health committee)声明thyroid.2015;25(2):145-146。
[0039]
本公开的方面涉及通过被感染的个体减少病毒(例如,流感)传播并且通过提供对健康个体感染的保护性屏障(即,预防)来减少病毒(例如,流感)传播。
[0040]
应当理解(除非另外指明),列出的所有组分的浓度为“即用型”或“已用型”组合物的浓度。组合物可为浓缩形式。即,组合物的某些实施方案可为浓缩物形式,所述浓缩物形式由使用者用适当的载体进行稀释。然而,这对于目前的应用而言通常不方便。
[0041]
术语“包括”及其变型在说明书和权利要求书中出现这些术语的地方不具有限制的含义。
[0042]
如本文所用,“一个(种)”、“该/所述”、“至少一个(种)”和“一个(种)或多个(种)”可互换使用。术语“和/或”是指所列出的要素(例如,预防和/或处理感染是指预防、处理或既处理又预防进一步的感染)中的一个或全部。
[0043]
另外,在本文中,通过端点表述的数值范围包含该范围内所含的所有数值(例如,1至5包含1、1.5、2、2.75、3、3.80、4、5等)。
[0044]
本发明的上述发明内容并非旨在描述本发明的每个公开的实施方案或每种实施方式。以下描述更具体地举例说明了例示性实施方案。在本技术全文的若干处,通过实施例列表提供了指导,这些实施例能够以各种组合使用。在每种情况下,所引用的列表都只用作代表性的组,并且不应被理解为排他性列表。
[0045]
本公开的药物组合物可以包括消毒剂组合物和抗病毒组合物。一些消毒剂组合物和抗病毒组合物是已知的并且在本文中描述。
[0046]
消毒剂组合物的示例可包括美国专利公开号20180207122和美国专利号8808722中所描述的那些,将它们以引用的方式并入本文。优选的消毒剂组合物是成膜的。例如,成膜聚合物可以将活性抗微生物组分保留在痛苦的位点和/或在感染开始的位点(例如,鼻孔)持续更长的时间段。这对于某些应用可为所期望的。例如,一些成膜聚合物可以在施用和干燥之后产生不能轻松地洗脱的组合物。
[0047]
在至少一个实施方案中,可以使用含有广谱消毒剂的药物组合物,诸如碘或碘伏、过氧化氢、次氯酸盐、氯己定盐、聚(六亚甲基双胍)、三氯生、小分子季胺(诸如苄索氯铵、甲苄索氯铵、苯扎氯铵和奥替尼啶)、抗微生物金属(诸如银)以及它们的组合,任选地具有增
强剂组分。
[0048]
优选地,采用使用碘或碘伏(例如,pvp-i)的消毒剂组合物。一些消毒剂组合物也是耐久的。耐久的消毒剂组合物的示例可按以下商品名商购:明尼苏达州圣保罗的3m公司(3m,st paul,mn)的3m皮肤和鼻腔消毒剂。3m皮肤和鼻腔消毒剂包含约0.5%有效碘,并且为约5重量%的pvp-i。3m皮肤和鼻腔消毒剂可包含增稠剂,诸如羟乙基纤维素、表面活性剂和缓冲剂。其他合适的消毒剂组合物可按以下商品名商购:来自aviro health的betadine、来自pdi healthcare的profend或来自global life technologies的nozin。
[0049]
合适的碘伏浓度可以在占消毒剂组合物的0.25重量%至10重量%、2.5重量%至10.5重量%、3.5重量%至10.5重量%、或4.5重量%至5.5重量%的范围内。这些浓度被认为对各种有包封(有包膜)rna病毒有效,诸如流感、诺罗病毒、鼻病毒、冠状病毒、副流感病毒、呼吸道合胞体病毒(rsv)以及它们的组合。在至少一个实施方案中,碘伏的浓度可为不超过5.5重量%的碘伏。
[0050]
在至少一个实施方案中,可以根据处理方案施用药物组合物。处理方案可以包括用于在用病毒接种之后和之前(预防)处理的选项。例如,在一个处理方案中,药物组合物可以在接种之前(经由哺乳动物受试者的鼻孔)施用于哺乳动物受试者。在另一个处理方案中,药物组合物可以在接种病毒之后(例如,在任何症状的发作时)施用。在另一个处理方案中,可以响应于另一哺乳动物受试者表现出症状而施用药物组合物(即,预防),以防止病毒从表现出症状的哺乳动物受试者传播到所述哺乳动物受试者。在另一个处理方案中,药物组合物可以施用于表现出症状的一个或多个哺乳动物受试者和与表现出一种或多种症状的一个或多个哺乳动物受试者直接接触和/或间接(通过空气流动)接触的一个或多个哺乳动物受试者。
[0051]
在至少一个实施方案中,暴露于由病毒定殖的哺乳动物受试者的哺乳动物受试者不应出现病毒感染的症状。在至少一个实施方案中,在暴露于被病毒定殖的哺乳动物受试者之后,哺乳动物受试者出现症状的延迟可以为至少1天,或可以为至少2天或更多。
[0052]
在至少一个实施方案中,该处理方案可以在持续时间内发生。该持续时间可为至少6小时、至少1天、至少3天、至少5天或至少7天。
[0053]
处理方案可以包括在持续时间期间消毒剂组合物的多次施用。处理频率可以在每72小时一次到每天1次至12次之间的范围内。举例来说,处理频率可为每72小时一次、每60小时一次、每48小时一次、每36小时一次、每25小时一次、每24.5小时一次(即,在施用之间经过超过24小时)、每24小时一次、每12小时一次、每8小时一次、每6小时一次或每天5次、每天6次、每天7次或每天8次。处理频率可以在整天大致均匀地发生。在至少一个实施方案中,该处理可以包括在当天期间较短间隔期间作为浓缩物(即,高度浓缩的剂量)给药。在至少一个实施方案中,剂量和处理频率的组合将向哺乳动物受试者递送小于药物组合物的上限摄入水平。此外,该处理方案将不允许有效碘超过成年男性的碘的毒性(例如,2g/天)。
[0054]
在至少一个实施方案中,该处理方案可以包括将药物组合物施用至哺乳动物受试者的黏膜组织。施用消毒剂组合物的方面由scholz等人,美国专利公开号20180207122(发布于2018年7月26日)提供,将其以引用的方式全文并入本文。优选地,该黏膜组织是指鼻孔、鼻咽、口腔的黏膜组织或鼻腔和/或前鼻孔的黏膜组织。药物组合物的施用可以包括将浸渍有药物组合物的拭子插入在鼻腔中并且沿着鼻腔的直径扩散药物组合物。在至少一个
实施方案中,该消毒剂组合物可以以任何深度施用至鼻孔。例如,可以在距鼻尖至少1cm的深度处将消毒剂组合物施用至后鼻孔。在至少一个实施方案中,还可以在第一药物组合物之后施用第二药物组合物。例如,在施用消毒剂之后,然后可以将抗病毒剂与消毒剂结合使用(即局部、口服或注射)持续一段时间。
[0055]
在至少一个实施方案中,消毒剂化合物的施用可以引起有包膜rna病毒的保留,使得哺乳动物受试者不将有包膜rna病毒传播到另一哺乳动物受试者。
[0056]
在至少一个实施方案中,“基本上未被病毒定殖”意指哺乳动物受试者未表现出因病毒引起的症状(即无症状的或症状发生前的)。基本上未被病毒感染或基本上未被病毒定殖还可以意指哺乳动物受试者基本上未被有包膜rna病毒定殖。在至少一个实施方案中,基本上未被定殖可以意指受体哺乳动物受试者(没有病毒)可以具有在低于检测限或小于100pfu/ml的水平的病毒载量。
[0057]
在至少一个实施方案中,当疾病的存在和/或疾病的严重程度与病毒载量有关时,病毒可以以高于检测限但低于引发疾病的水平定殖于哺乳动物受试者。在至少一个实施方案中,被有包膜rna病毒定殖的哺乳动物受试者可以具有至少1000pfu/ml、至少5000pfu/ml或至少10000pfu/ml的病毒载量,或以其它方式具有有包膜rna病毒的症状。
[0058]
实施例:
[0059]
在以下实施例中,3m皮肤和鼻腔消毒剂(包含5重量%的聚维酮-碘)的消毒剂组合物(在本文中称为“鼻腔制剂”)可购自明尼苏达州圣保罗的3m公司。磷酸盐缓冲盐水(pbs),ph=7.4,可从赛默飞世尔科技公司(thermo fisher scientific)商购获得(目录号10010023)。从商业实验动物供应商获得无疾病的动物。
[0060]
实施例1:通过用消毒剂组合物处理来预防小鼠感染流感病毒。
[0061]
对于用小鼠进行的以下实施例,使用以下附加材料:
[0062]
·
28只雌性c567bl/6小鼠8-10周龄,可购自无疾病动物的商业供应商
[0063]
·
甲型流感病毒/pr/8/38(h1n1)。
[0064]
将小鼠分成三组;第1组、第2组和第3组。第1组有12只小鼠,第2组有12只小鼠,并且第3组有4只小鼠。将第1组中的小鼠用消毒剂组合物处理。将第2组中的小鼠用pbs(作为安慰剂)处理。第3组中的小鼠充当未处理的对照。在用消毒剂组合物或安慰剂进行初始处理后(或在未处理的对照组中无处理之后)0、6或24小时,给小鼠接种25,000个噬斑形成单位(pfu)的甲型流感/pr/8/38(h1n1)。感染后三天,将小鼠安乐死,使用pbs对安乐死的小鼠进行鼻腔冲洗,并且通过噬斑试验确定病毒水平。
[0065]
实施例1:
[0066]
用氯胺酮麻醉小鼠,然后施用3m皮肤和鼻腔消毒剂,然后接种病毒。对于第1组中的每只小鼠,使用2μl移液器尖端通过将大约5μl的3m皮肤和鼻腔消毒剂扩散到两个鼻孔的内表面施用3m皮肤和鼻腔消毒剂。然后在以下时间点之一用流感病毒(总共25000pfu)接种第1组中每只小鼠的鼻孔:在使用3m皮肤和鼻腔消毒剂鼻内处理后立刻(4只动物)、鼻内处理后6小时(4只动物)以及鼻内处理后24小时(4只动物)。在接种病毒后三天,将动物安乐死并且通过使用鼻腔冲洗液的噬斑试验确定病毒水平。
[0067]
比较例1:
[0068]
用氯胺酮麻醉小鼠,然后施用3m皮肤和鼻腔消毒剂,然后接种病毒。对于第2组中
的每只小鼠,使用2μl移液器尖端通过将大约5μl的pbs扩散到两个鼻孔的内表面施用pbs。然后在以下时间点之一用流感病毒(25000pfu)接种每只小鼠的鼻孔:鼻内处理后立刻(4只动物)、鼻内处理后6小时(4只动物)以及鼻内处理后24小时(4只动物)。在接种病毒后三天,将动物安乐死并且通过使用鼻腔冲洗液的噬斑试验确定病毒水平。
[0069]
比较例2:
[0070]
在接种病毒之前用氯胺酮麻醉小鼠。用流感病毒(25000pfu)接种第3组中每只小鼠的鼻孔。在接种病毒后三天,将动物安乐死并且通过使用鼻腔冲洗液的噬斑试验确定病毒水平。
[0071]
图1是指示不考虑用3m皮肤和鼻腔消毒剂进行处理和接种病毒之间的时间长度(至多24小时),从第1组中的任何小鼠中均未回收到活病毒的条形图。图1还示出了从第2组回收活病毒,该组的个体在施用pbs后6小时和24小时用病毒接种。图1还示出了从第3组回收活病毒,该组的个体在接种病毒之前未经处理。图1指示使用3m皮肤和鼻腔消毒剂的单次施用24小时预防流感感染。
[0072]
图2是指示第2组当在施用pbs之后6小时接种病毒时在鼻孔中具有50pfu/ml活病毒,以及在施用pbs后24小时接种病毒时在鼻孔中具有100pfu/ml活病毒的图表。第3组在接种流感病毒后24小时在鼻孔中具有200pfu/ml活病毒。因此,第1组动物在用3m皮肤和鼻腔消毒剂处理然后用流感病毒接种至多24小时后在其鼻孔中不具有任何活病毒。
[0073]
实施例2:预防豚鼠的流感病毒的空气传播。
[0074]
五至六周龄的雌性哈氏天竺鼠种豚鼠可购自查尔斯河实验室(马萨诸塞州威明顿市(charles river laboratories,wilmington,ma)。动物重量为350g至400g之间。允许动物自由采食食品和水,并且在12小时光暗循环中饲养。
[0075]
豚鼠的感染和监测:肌内施用175-μl的氯胺酮(30mg/kg体重)和甲苯噻嗪(5mg/kg)的混合物麻醉豚鼠。通过向每个鼻孔施用一定体积的流感病毒的原液溶液(3
×
104pfu/ml a/panama/2007/1999(h3n2))鼻内滴注“pan99”甲型流感病毒的接种物。
[0076]
豚鼠鼻腔冲洗液样品的收集:在收集鼻腔冲洗液样品之前,如上所述麻醉豚鼠。通过将总共1ml的磷酸盐缓冲盐水(pbs)滴注入豚鼠的鼻孔中进行鼻腔冲洗,并允许其排出到无菌有盖培养皿中。在通过噬斑试验分析之前,将上清液储存在-80℃。
[0077]
处理:使用鼻腔制剂和pbs(磷酸盐缓冲盐水)的处理。
[0078]
实验:实验中使用十六只动物。每只动物被鉴定为一对动物中的一只,其中每队的笼子通过导管连接,该导管使得能够在两个笼子之间交换空气,如图3所述。
[0079]
对于空气传播的传播实验,病毒供体和病毒受体动物通过空气可渗透屏障物理分离,所述空气可渗透屏障排除直接接触传输,同时允许通过空气传播途径(液滴和气溶胶)从供体动物扩散到受体动物。
[0080]
用甲型流感/panama/2007/1999(h3n2)病毒感染每对动物中的一只,并且随后根据下文所描述的处理方案处理动物。
[0081]
第-1天:在实验的
“‑
1”天,将动物分成对并指定如下:
[0082]
四只动物指定为“供体,鼻腔制剂”,指示如此指定的那些动物将用流感病毒接种并且用消毒剂组合物处理。
[0083]
四只动物被指定为“受体,鼻腔制剂”,指示那些四只动物中的每一只与“供体,鼻
腔制剂”动物之一构成“对”。将受体、鼻腔制剂动物用消毒剂组合物处理,并且经由通过来自供体、鼻腔制剂动物的导管的空气暴露于任何流感病毒。
[0084]
将四只动物指定为“供体,安慰剂(pbs)”,指示如此指定的那些动物将用流感病毒接种并且用pbs处理。
[0085]
四只动物被指定为“受体,安慰剂(pbs)”,指示那些四只动物中的每一只与“供体,安慰剂(pbs)”动物之一构成“对”。将受体、安慰剂(pbs)动物用pbs处理,并且经由通过来自供体、安慰剂(pbs)动物笼子的导管的空气暴露于任何流感病毒。
[0086]
在第-1天,通过将50微升的消毒剂组合物滴注到清醒直立动物的每个鼻孔中,将所有被指定为“鼻腔制剂”的动物用消毒剂组合物处理。另外,将指定为“安慰剂(pbs)”的所有动物通过将50微升pbs滴注到清醒、直立动物的每个鼻孔中用pbs进行处理。
[0087]
在第0天,将所有标记为“供体”的动物在氯胺酮麻醉下(如上所述)每个鼻孔接种75微升的“pan 99”流感病毒(如上所述)。三小时后,根据实验对其的指定,用pbs或消毒剂组合物处理所有动物(如上所述)。
[0088]
在第 1天、第 3天、第 5天和第 7天,将所有动物麻醉,经历鼻腔冲洗(通过将1ml pbs取样溶液滴注入鼻孔(俯卧时)),允许其苏醒并且然后根据实验对其处理的指定,用消毒剂组合物或安慰剂(pbs)处理。
[0089]
在第 2天、第 4天和第 6天,根据实验对其处理的指定,用消毒剂组合物或安慰剂(pbs)处理所有动物。
[0090]
在收集后立即用pbs稀释(1至10倍)在第 1天、第 3天、第 5天和第 7天收集的鼻腔冲洗液。(早些的体外实验表明,1至10倍稀释度足以防止残留的碘(在鼻腔冲洗期间从鼻子中冲洗出的)在通过噬斑试验进行滴定之前在鼻腔冲洗液样品中灭活病毒。)为了定量活病毒,将鼻腔冲洗液样品连续稀释并且铺板到mdck细胞上以定量病毒。病毒量报告为噬斑形成单位(pfu)。图4中示出了传播实验的结果。
[0091]
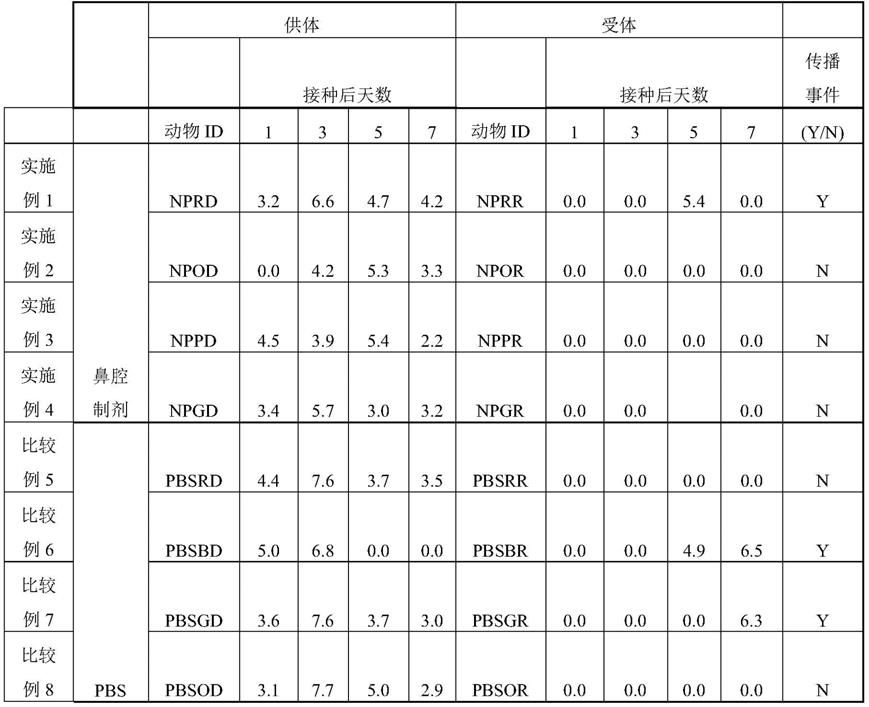
结果:图4示出了跨4个豚鼠群体的病毒滴度的平均值的图,其中lod是噬斑试验的检测限。表1中的实验的结果(其中单位为[log(pfu/ml)])显示,使用消毒剂组合物的处理防止了4个经测试的受体动物中的3个受体动物的流感病毒经由空气传播的传播,而使用安慰剂(pbs)的处理防止了4个经测试的受体动物中的仅2个受体动物的空气传播。
[0092]
表1-豚鼠传播数据
[0093][0094]
另外,使用消毒剂组合物处理通过流感病毒的空气传播感染的单个受体动物在感染发生后48小时内将被感染的受体的病毒载量(鼻孔中病毒的量)降低到检测限以下,而使用pbs的处理在相同的48小时时间段期间使病毒传播到的pbs处理的动物中的至少一个动物的病毒载量继续升高。
[0095]
另外,接种后3天,用鼻腔制剂(实施例1-4)处理的供体与安慰剂(比较例5-8)相比病毒滴度浓度低至少1.5log。
[0096]
实施例3:用鼻腔制剂处理后的豚鼠的鼻孔中的病毒数评估。
[0097]
豚鼠的感染和监测:在感染流感病毒之前,肌内施用175-μl的氯胺酮(30mg/kg体重)和甲苯噻嗪(5mg/kg)的混合物麻醉豚鼠。通过向每个鼻孔施用一定体积的流感病毒的原液溶液(3
×
104pfu/ml a/panama/2007/1999(h3n2))鼻内滴注“pan99”甲型流感病毒的接种物。(对于下文描述的每个实验,分别指示了所施用的体积)。
[0098]
豚鼠鼻腔冲洗液样品的收集:在收集鼻腔冲洗液样品之前,如上所述麻醉豚鼠。通过将总共1ml的磷酸盐缓冲盐水(pbs)滴注入豚鼠的鼻孔中进行鼻腔冲洗,并允许其排出到无菌有盖培养皿中。在通过噬斑试验分析之前,将上清液储存在-80℃。
[0099]
处理:使用鼻腔制剂、载体(不含聚维酮碘和碘化钠的3m
tm
皮肤和鼻腔消毒剂)和pbs(磷酸盐缓冲盐水)处理动物。
[0100]
第-1天:在此实验的第
“‑
1”天中,如下处理十只豚鼠:
[0101]
使用移液管用鼻腔制剂处理四只豚鼠(在清醒和直立时),并且将50μl鼻腔制剂递送到每个鼻孔(每只豚鼠100μl)。
[0102]
使用移液管用载体处理四只豚鼠(在清醒和直立时),并且将50μl载体递送到每个
鼻孔(每只豚鼠100μl)。
[0103]
使用移液管用pbs处理两只豚鼠(在清醒和直立时),并且将50μl pbs递送到每个鼻孔(每只豚鼠100μl)。
[0104]
第0天:麻醉所有豚鼠,然后接种150μl(75μl/鼻孔)的稀释的pan99甲型流感病毒原液溶液,浓度为6.7
×
103pfu/ml,等同于每只动物接受1
×
103pfu的流感病毒。6小时后,在豚鼠已经完全从麻醉中苏醒后,如上所述重新施用处理(第-1天)。
[0105]
第 1天、第 3天、第 5天和第 7天:将所有豚鼠麻醉,经历鼻腔冲洗(1ml pbs采样溶液),并且然后允许其苏醒。在第1天、第3天和第5天,苏醒后,如上所述(第-1天)用鼻腔制剂、载体或pbs处理豚鼠。
[0106]
第2天、第4天、第6天:如上所述(第-1天),用鼻腔制剂、载体或pbs处理所有豚鼠。
[0107]
将鼻腔冲洗液稀释并且铺板到可从sigma-aldrich(密苏里州圣路易市)商购获得的maden darby canine kidney细胞上以用于定量活病毒。
[0108]
图5中示出实施例3的结果。
[0109]
实施例3的结果表明,对于鼻腔制剂处理的动物(502,n=4只动物),从第1天到第7天活病毒的量稳定增加,并且对于载体处理的动物(506,n=4只动物)和pbs处理的动物(504,n=2只动物),该时间段活病毒的量持续减少。
[0110]
用实施例2的结果获得的实施例3的结果示出了令人惊讶的结果,即用于处理方法中的聚维酮-碘组合物防止了病毒的传播。不受理论的束缚,怀疑病毒颗粒可能通过在存在增稠的聚维酮碘组合物的情况下在鼻孔中凝聚而保留,并且不能容易地从一只动物转移到另一只动物,还怀疑在鼻孔取样期间鼻腔冲洗破坏了假定的附聚,并且允许病毒体在mdck细胞中复制,这导致mdck群落上的病毒引起的噬斑。
[0111]
实施例4-鼻腔制剂针对sars-cov-2病毒的体外功效。
[0112]
过程:
[0113]
病毒、培养基和细胞
[0114]
通过在vero 76细胞中生长病毒来制备sars-cov-2病毒原液。测试培养基是补充有2%fbs和50μg/ml庆大霉素的mem。
[0115]
杀病毒测定
[0116]
使用无菌水作为稀释剂,并以三次另外的连续10倍稀释液在全部效力下测试鼻腔制剂(90%鼻腔制剂和10%病毒溶液)。将sars-cov-2病毒原液添加到每个制备的浓度(以1/10的稀释度制备的)的三个管中,使得测试的鼻腔制剂的最终浓度为全部效力的90%(0.45%w/w有效碘)、全部效力的9%(0.045%w/w有效碘)、全部效力的0.9%(0.0045%w/w有效碘)和全部效力的0.09%(0.00045%w/w有效碘)。将培养基添加到每个制备的浓度的鼻腔制剂的仅一个管中,以用作细胞毒性对照。平行测试乙醇(63%)(可从sigma aldrich商购获得)作为杀病毒活性的阳性对照,并且仅测试水用作病毒对照。将溶液和病毒在室温下孵育持续在30秒、1分钟和2分钟的三次接触时间期间。在接触期之后,使用测试培养基中的0.5%硫代硫酸钠的1/10稀释度将每种溶液“中和”。(硫代硫酸钠,na2s2o3,还原分子碘(i2)至无色碘化物阴离子(i-),其不具有体外杀病毒活性。)
[0117]
病毒定量
[0118]
在测试培养基中使用八个半对数稀释液连续稀释中和样品。将每种稀释液添加到
96孔板的四个孔中,所述孔是80%-100%融合的vero76细胞。将毒性对照添加到另外的四个孔中,其中两个被病毒感染以用作中和对照,确保在铺板的个体滴度测定中保留的任何残留测试样品不抑制存活病毒的生长和检测。将所有板在37
±
2℃下在5%co2下孵育。
[0119]
在感染后第6天,对板存在或不存在病毒细胞病变作用(cpe)进行评分。reed-muench方法用于确定样品的终点滴度(50%细胞培养感染剂量,ccid
50
)并计算与阴性(水)对照相比的化合物的log下降值(lrv)。使用graphpad prism(第8版)软件通过单因素方差分析与dunnett多重比较测试将样品结果与未经处理的对照进行比较。
[0120]
对照
[0121]
在水中测试病毒对照,并将测试孔中病毒的减少与病毒对照进行比较,并且计算为log下降值(lrv)。使用不含病毒的培养基测试毒性对照,以确定样品是否对细胞有毒。测试中和对照以确保病毒灭活在指定的接触时间之后未继续,并且滴度测定板中剩余的任何残留样品未抑制存活病毒的生长和检测;这是通过添加毒性样品到滴度测试板,然后用少量病毒体(在孵育期间产生可观察到程度的细胞病变效应程度)掺入每个孔中完成的。
[0122]
结果
[0123]
针对sars-cov-2病毒的鼻腔制剂的病毒滴度和log下降值显示在表2中。
[0124]
在3m
tm
皮肤和鼻腔消毒剂的最高浓度(90%的效力)的八个半对数稀释液中的两个(1/10和1/100稀释度)中和在3m
tm
皮肤和鼻腔消毒剂的9%的效力的1/10稀释度中观察到对vero 76细胞的完全毒性。由于这种毒性,在这些孔中不能排除存在活病毒,因此检测限为2.7log
10
和1.7log
10 ccid
50
病毒/0.1ml。类似地,乙醇在1/10稀释度下引起毒性。在室温下与病毒接触30秒、1分钟或2分钟的时间之后,鼻腔制剂的9%溶液减少病毒计数至低于检测限,即》2log
10 ccid
50
/0.1ml(》99%,p《0.001)。尽管不灭活所有存在的病毒,但是0.9%溶液减少病毒》2log
10 ccid
50
/0.1ml(99%,p《0.0001)(在1或2分钟接触时间之后)和》1log
10 ccid
50
/0.1ml(90%,p《0.01)(在30秒接触时间之后)。
[0125]
由于细胞毒性,对于所有三个接触时间,通过鼻腔制剂的90%溶液的减少病毒的水平限于》1log
10 ccid
50
/0.1ml(90%,p《0.05)。在测试的接触时间期间鼻腔制剂的0.09%溶液不会减少病毒。
[0126]
中和对照表明,中和样品中的任何残留的碘不会抑制病毒生长,也不会在未显示细胞毒性的孔中的终点滴度测定中检测到病毒。病毒对照和阳性对照如预期进行。
[0127]
因此,在低至30秒持续时间的接触时间期间,鼻腔制剂对sars-cov-2的杀病毒效力低至0.9%(0.0045%w/w有效碘)。
[0128]
表2:在22
±
2℃孵育病毒后,鼻腔制剂针对sars-cov-2的杀病毒功效。
[0129][0130][0131]
每毫升病毒的log
10 ccid
50
,3次重复的平均值,“《”意指检测下限
[0132]
b lrv(log下降值)是病毒与病毒对照相比的减少
[0133]
例示性实施方案的列表:
[0134]
1.一种处理或预防哺乳动物受试者的有包膜rna病毒的方法,包括:
[0135]
将有效量的消毒剂组合物或所述消毒剂组合物的药学上可接受的盐施用至具有第一病毒载量的所述哺乳动物受试者的黏膜组织;
[0136]
允许所述第一病毒载量在处理方案的持续时间内减少至第二病毒载量,
[0137]
其中在所述处理方案的所述持续时间期间,与使用安慰剂相比,使用所述消毒剂组合物出现所述第二病毒载量的至少0.5log下降,
[0138]
其中所述消毒剂组合物包含碘、碘伏或它们的组合和增稠剂。
[0139]
2.根据实施方案1所述的方法,其中所述第一病毒载量与所述病毒的症状发作相关联。
[0140]
3.根据前述实施方案中任一项所述的方法,还包括:向所述哺乳动物受试者施用有效量的抗病毒剂。
[0141]
4.根据前述实施方案中任一项所述的方法,其中所述安慰剂是磷酸盐缓冲盐水。
[0142]
5.根据前述实施方案中任一项所述的方法,其中所述碘或碘伏以足够的浓度存在以提供0.0045重量%至0.55重量%的有效碘浓度。
[0143]
6.根据实施方案5所述的方法,其中所述pvp-i的浓度不大于10重量%(100mg/
ml)。
[0144]
7.根据实施方案6所述的方法,其中所述pvp-i的浓度为4.5重量%至5.5重量%(45mg/ml至55mg/ml)。
[0145]
8.根据前述实施方案中任一项所述的方法,其中所述消毒剂组合物包含水、表面活性剂和缓冲液。
[0146]
9.根据实施方案8所述的方法,其中所述消毒剂组合物包含以至少2.5重量%的浓度存在的羟基羧酸;氧化胺;和碘化物盐,其以至少2.0重量%的浓度并且以不大于10重量%的量存在,其中所述组合物为即用型,并且其中所述组合物在40℃储存约6个月时表现出不大于5%重量/重量的有效碘的降低。
[0147]
10.根据实施方案9所述的方法,其中所述羟基羧酸以大于5重量%的量存在。
[0148]
11.根据实施方案9所述的方法,其中所述氧化胺以0.25重量%至1.5重量%的浓度存在。
[0149]
12.根据实施方案9所述的方法,其中所述消毒剂组合物还包含单糖、糖醇或它们的组合,其中所述单糖、糖醇或它们的组合以大于5%重量/重量的浓度存在。
[0150]
13.根据实施方案9所述的方法,其中所述消毒剂组合物包含表面活性剂;其中所述表面活性剂包括阴离子表面活性剂、两性表面活性剂、非离子表面活性剂、两性离子表面活性剂或它们的组合;其中所述阴离子表面活性剂包括磷酸盐、膦酸盐、硫酸盐、磺酸盐或它们的组合。
[0151]
14.根据实施方案9所述的方法,其中所述消毒剂组合物包含载体,其中所述载体包含水和重均分子量小于1500的聚乙二醇。
[0152]
15.根据前述实施方案中任一项所述的方法,其中所述消毒剂组合物包含增稠剂。
[0153]
16.根据前述实施方案中任一项所述的方法,其中所述消毒剂组合物不含有脂质体。
[0154]
17.根据前述实施方案中任一项所述的方法,其中所述处理方案包括以每天1至12次的频率施用所述消毒剂组合物。
[0155]
18.根据前述实施方案中任一项所述的方法,其中所述处理方案不超过所述消毒剂组合物的上限摄入水平。
[0156]
19.根据前述实施方案中任一项所述的方法,其中在所述处理方案中,在施用之间经过至少24小时。
[0157]
20.根据前述实施方案中任一项所述的方法,其中所述持续时间为1天、3天、5天或7天。
[0158]
21.根据实施方案18所述的方法,其中所述处理方案中的所述消毒剂组合物的每个后续处理增加了所述消毒剂的浓度。
[0159]
22.根据实施方案18所述的方法,其中所述处理方案中的所述消毒剂组合物的每个后续剂量降低了所述消毒剂的浓度。
[0160]
23.根据前述实施方案中任一项所述的方法,其中将所述消毒剂组合物施用到鼻腔中超过1cm。
[0161]
23a.根据前述实施方案中任一项所述的方法,其中将所述消毒剂组合物施用到鼻腔中小于1cm。
[0162]
24.根据前述实施方案中任一项所述的方法,其中所述有包膜rna病毒是流感或冠状病毒。
[0163]
25.根据前述实施方案中任一项所述的方法,其中所述第一病毒载量为每毫升至少1000个噬斑形成单位(pfu)。
[0164]
26.根据前述实施方案中任一项所述的方法,其中所述第二病毒载量不大于每毫升32个噬斑形成单位(pfu)。
[0165]
27.根据前述实施方案中任一项所述的方法,其中所述第一病毒载量不大于每毫升32pfu。
[0166]
28.根据实施方案27所述的方法,其中所述第二病毒载量不大于每毫升100pfu。
[0167]
29.根据前述实施方案中任一项所述的方法,还包括:
[0168]
在暴露于所述哺乳动物受试者之前并且根据所述处理方案将有效量的消毒剂组合物或所述消毒剂组合物的药学上可接受的盐施用至第二哺乳动物受试者的黏膜组织;
[0169]
允许所述哺乳动物受试者与所述第二哺乳动物受试者互动一段时间,其中所述第二哺乳动物受试者在所述处理方案期间具有不大于0.5log的病毒载量增加。
[0170]
30.根据实施方案29所述的方法,其中所述时间段为至少1小时、至少2小时、至少3小时或至少4小时。
[0171]
31.根据前述实施方案中任一项所述的方法,其中互动意指与任何身体部位接触。
[0172]
32.根据前述实施方案中任一项所述的方法,其中互动意指允许所述有包膜rna病毒的空气传播。
[0173]
33.根据前述实施方案中任一项所述的方法,还包括:在施用所述药物组合物之前清洁鼻孔的内部。
[0174]
34.根据前述实施方案中任一项所述的方法,其中施用包括在所述黏膜组织上扩散所述消毒剂组合物。
[0175]
35.根据前述实施方案中任一项所述的方法,其中施用包括用拭子将所述消毒剂组合物分配到所述黏膜组织上。
[0176]
36.根据实施方案35所述的方法,其中所述拭子是棉签涂药器或刷子。
[0177]
37.根据实施方案35所述的方法,其中施用包括允许所述消毒剂组合物保持在所述黏膜组织中持续至少1分钟、至少5分钟或至少10分钟。
[0178]
38.一种防止有包膜rna病毒传播的方法,包括:
[0179]
根据处理方案向基本上未被所述有包膜rna病毒定殖的第一哺乳动物受试者的黏膜组织施用有效量的消毒剂组合物或其药学上可接受的盐;
[0180]
允许基本上未被所述有包膜rna病毒定殖的所述第一哺乳动物受试者与被所述有包膜rna病毒以第一病毒载量定殖的第二哺乳动物受试者互动,所述第一哺乳动物受试者具有基于所述互动的第二病毒载量;
[0181]
其中在所述处理方案的持续时间内,相比于初始病毒载量,所述第二病毒载量不大于0.5log增加;
[0182]
其中所述黏膜组织在该哺乳动物受试者的鼻咽、鼻腔或前鼻孔中;
[0183]
其中所述消毒剂组合物包含碘、碘伏或它们的组合和增稠剂。
[0184]
39.根据实施方案38所述的方法,还包括:
[0185]
根据所述处理方案向具有所述第一病毒载量的有包膜rna病毒的所述第二哺乳动物受试者的所述黏膜组织施用有效量的所述消毒剂组合物或其药学上可接受的盐。
[0186]
40.一种防止有包膜rna病毒从哺乳动物受试者传播的方法,包括:
[0187]
将有效量的消毒剂组合物或所述消毒剂组合物的药学上可接受的盐施用至具有第一病毒载量的所述哺乳动物受试者的黏膜组织中持续处理方案的持续时间,其中所述黏膜组织在所述哺乳动物受试者的鼻咽、鼻腔或前鼻孔中;
[0188]
允许有包膜rna病毒因与所述消毒剂组合物接触而保留在所述黏膜组织中;
[0189]
其中当基本上未被所述有包膜rna病毒定殖的第二哺乳动物受试者与所述哺乳动物受试者互动时,所述哺乳动物受试者在所述处理方案的持续时间期间不将所述有包膜rna病毒传播至所述第二哺乳动物受试者;
[0190]
其中所述消毒剂组合物包含碘、碘伏或它们的组合和增稠剂。
[0191]
41.根据实施方案38或实施方案40所述的方法,其中基本上未被有包膜rna病毒定殖意指所述有包膜rna病毒的病毒浓度低于检测限。
[0192]
42.根据实施方案41所述的方法,其中基本上未被有包膜rna病毒定殖意指所述第一哺乳动物受试者或第二哺乳动物受试者未表现出所述有包膜rna病毒的症状。
[0193]
43.根据实施方案38或实施方案40所述的方法,其中所述第一病毒载量与所述有包膜rna病毒的症状发作相关联。
[0194]
44.根据实施方案38或实施方案40所述的方法,其中所述第一病毒载量为每毫升至少1000pfu。
[0195]
45.根据实施方案44所述的方法,其中所述第一病毒载量为每毫升至少10000pfu。
[0196]
46.根据实施方案38或实施方案40所述的方法,其中所述持续时间为至少3天。
[0197]
47.根据实施方案46所述的方法,其中在所述处理方案中,在施用之间经过超过24小时。
[0198]
48.根据实施方案46所述的方法,其中所述有包膜rna病毒选自流感或冠状病毒。
[0199]
49.一种使用消毒剂组合物或其药学上可接受的盐的方法,其包含0.25%至10.5重量百分比之间的碘伏,包括端值在内,用作预防流感,该方法包括根据处理方案将所述消毒剂组合物施用至哺乳动物受试者的黏膜组织。
[0200]
49a.根据实施方案49所述的方法,其中所述消毒剂组合物或其药学上可接受的盐包含在3.5重量百分比至10.5重量百分比之间。
[0201]
50.根据实施方案49所述的方法,其中所述处理方案包括在流感接种之前至少6小时进行所述消毒剂组合物的施用。
[0202]
51.根据前述实施方案中任一项所述的方法,其中所述处理方案包括在流感接种之前至少12小时进行所述消毒剂组合物的施用。
[0203]
52.根据前述实施方案中任一项所述的方法,其中所述处理方案包括在流感接种之前至少24小时进行所述消毒剂组合物的施用。
[0204]
53.根据前述实施方案中任一项所述的方法,其中所述消毒剂组合物包含4.5重量百分比至5.5重量百分比之间的碘伏,包括端值在内。
[0205]
54.根据实施方案53所述的方法,其中所述消毒剂组合物是成膜的。
[0206]
55.根据实施方案53所述的方法,其中所述消毒剂组合物是耐久的。
[0207]
56.根据前述实施方案中任一项所述的方法,其中所述黏膜组织是前鼻孔。
[0208]
57.根据前述实施方案中任一项所述的方法,其中流感为h1n1。
[0209]
58.根据前述实施方案中任一项所述的方法,其中在流感接种后24小时未发生病毒载量的可观察到的增加。
[0210]
59.一种处理或预防哺乳动物受试者的病毒的方法,包括:
[0211]
将有效量的药物组合物或其药学上可接受的盐施用至具有第一病毒载量的哺乳动物受试者的黏膜组织;
[0212]
允许所述第一病毒载量在处理方案的持续时间内减少至第二病毒载量,其中与安慰剂相比,使用所述药物组合物出现病毒载量的至少0.5log下降。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。