1.本发明属于医药技术领域,具体涉及植物草珊瑚中制备新龙胆酸混源杂萜类化合物的方法及这类化合物在抗神经炎症方面的应用。
背景技术:
2.草珊瑚:草珊瑚[sarcandra glabra(thunb.)nakai]又名肿节风,属于金粟兰科草珊瑚属的多年生常绿草本或亚灌木植物。草珊瑚主要分布于我国的广西、江西、贵州等地,且资源丰富。其具有悠久的入药历史,性平,味辛、苦,有小毒,具有清热解毒,活血化瘀,祛风疏络,接骨,抗癌等药用价值。常用于菌痢、肺炎、骨折、阑尾炎等疾病的治疗。药理学研究表明草珊瑚具有一定的抗菌消炎作用、抗肿瘤作用、抑制流感病毒的作用、促进骨折的愈合等生物活性。
[0003]
随着全球人口老龄化的进程,神经退行性疾病受到越来越多的关注,其中阿尔茨海默氏症和帕金森症等正成为导致中老年人死亡的主要杀手。近年来的研究表明,小胶质细胞(bv2)主导的神经炎症在神经退行性疾病的发展过程中发挥重要的作用。抑制神经炎症反应可以延缓神经退行性疾病的进程,同时能够防止神经元发生病变,对于治疗神经退行性疾病有着很好的前景。
技术实现要素:
[0004]
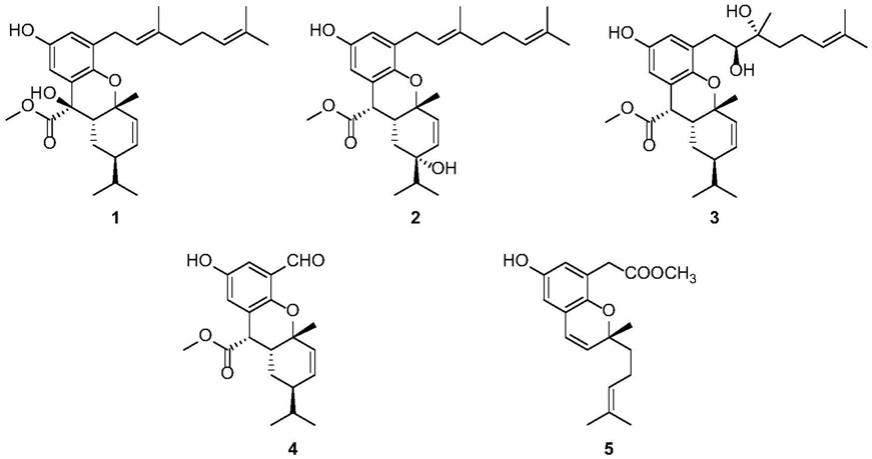
本发明提供五种从金粟兰科草珊瑚属植物草珊瑚[sarcandra glabra(thunb.)nakai]中分离得到的新龙胆酸混源杂萜类化合物,具体结构如下所示:
[0005][0006]
本发明的制备技术方案包括如下步骤:
[0007]
取干燥的草珊瑚全草以80%工业乙醇提取,合并提取液浓缩得浸膏,浸膏采用乙酸乙酯萃取并将所得组分经硅胶柱色谱,以二氯甲烷-甲醇系统100:0-0:100进行等度梯度洗脱,共收集到4个馏分(a-d);
6;根据δh3.71与δc176.5有相关,提示c-1
′
连有乙酰酯基部分,由此,化合物的平面结构被确定下来。
[0021]
在noesy谱中,h-6"(δh2.16)与ch
3-7"(δh1.41)相关,h-6"(δh2.16)与h-8"(δh1.63)相关,h-6"(δh2.16)与h-9"(δh0.95)相关,提示h-6"、ch
3-7"与异丙基处于同侧。在b3lyp/6-311 g(d,p)基组水平及连续极化模式条件下对(1
′
s*,1"r*,4"r*,6"r*)和(1
′
r*,1"r*,4"r*,6"r*)两种构型进行了理论
13
c nmr计算。结果显示,计算的1
′
r*,1"r*,4"r*,6"r*构型的碳核磁数据与实测的数据比较,经dp4 概率分析得出99.94%的可能性,因此确定化合物1的相对构型为1
′
r*,1"r*,4"r*,6"r*。该化合物的绝对构型是通过比较实验ecd与计算ecd的方法确定的,计算的1
′
r,1"r,4"r,6"r构型与实测的ecd的图谱吻合度较高,故确定该化合物的绝对构型为1
′
r,1"r,4"r,6"r。
[0022]
化合物1的1h(600mhz)与
13
c(150mhz)nmr数据(cdcl3)
[0023][0024][0025]
sarcandralideb(2):黄色油状;(c 0.10meoh);hresims给出准分子离子峰m/z491.2765[m na]
(calcd for c
29h40
nao5,491.2768),确定该化合物的分子量为468,分子式为c
29h40
o5,计算不饱和度为10。
[0026]1h-nmr(600mhz,cdcl3)中,低场区给出δ
h 6.57(1h,d,j=2.9hz,h-5),6.49(1h,d,j=2.9hz,h-3),提示可能为两个间位偶合的芳香质子信号;δ
h 5.87(1h,dd,j=10.0,3.8hz,h-2
″
),5.74(1h,d,j=10.0,1.2hz,h-3
″
)分别为一个顺式双键上的两组烯氢质子信号。δ
h 5.22(1h,t,j=7.4hz,h-8),δ
h 5.08(1h,t,j=6.9hz,h-12)提示为两个三取代双键上的氢。高场区,δ
h 3.81(3h,s)提示为一个甲氧基上的质子信号。δ
h 1.67(3h,s),1.65(3h,
s),1.59(3h,s)提示为三个烯甲基氢。由δ
h 0.84(3h,d,j=6.8hz,h-9
″
),0.88(3h,d,j=6.8hz,h-10
″
)两组甲基质子信号可知,该化合物中含有一个异丙基
–
ch(ch3)2片段。另外,高场区还出现一个角甲基上的氢信号δ
h 1.33(3h,s,h-7
″
)。
[0027]
13
c-nmr(150mhz,cdcl3)中共有29个碳信号,其中δ
c 173.5提示为羰基碳信号,δc148.6,144.6,136.0,134.4,134.1,131.5,131.4,124.5,122.3,116.7,116.3,113.5为12个sp2杂化碳信号,结合其氢谱推测该结构中含有一个四取代的苯环和三个双键(包括一个顺式双键),高场区给出16个脂肪族碳信号。通过二维谱数据分析进一步对其结构进行了确定。
[0028]
在hmbc谱中,h-3
″
与c-1
″
/c-5
″
存在相关,h-2
″
与c-4
″
/c-6
″
存在相关,h-5
″
与c-1
″
存在相关,h-6
″
与c-4
″
存在相关,h-7
″
与c-2
″
/c-6
″
存在相关,h-9
″
/h-10
″
与c-4
″
/c-8
″
存在相关,提示该结构中含有一个连有异丙基的环己烯结构片段。根据h-6
″
与c-2/c-1
′
存在相关,h-3与c-1
′
存在相关,表明该自旋系统的一端是通过c-1
′
与苯环的c-2位之间相连。结合化合物分子量推测c-1(δc144.6),c-1
″
(δc71.9)通过一个氧桥连结,结合1h-1
h cosy相关确定c-4
′
(δc73.1)处连有羟基取代。根据h-5与c-7有相关,h-8与c-10/c-6/c(9-me)有相关,h-10与c-11/c-12有相关,h-11与c-13有相关,h(13-me)/h-14与c-12有相关,提示结构中c-9、c-13位连有烯甲基,并且该脂肪链连于c-6;根据δh3.81与δc173.5有相关,提示c-1
′
连有甲氧羰基部分,由此,化合物的平面结构被确定下来。
[0029]
通过noesy谱确定了化合物2的相对构型,h-1'(δh4.22)与h-7"(δh1.33)相关,h-1'(δh4.22)与h-6"(δh2.47)相关,h-6"(δh2.47)与h-7"(δh1.33)相关,h-6"(δh2.47)与h-10"(δh0.88)相关,h-1'(δh4.22)与h-10"(δh0.88)相关。因此确定化合物2的相对构型为1s*,1"r*,4"s*,6"r*。该化合物的绝对构型是通过比较实验ecd与计算ecd的方法确定的,故该化合物的绝对构型为1
′
s,1"r,4"s,6"r。
[0030]
化合物2的1h(600mhz)与
13
c(150mhz)nmr数据(cdcl3)
[0031][0032]
sarcandralidec(3):黄色油状;(c 0.10meoh);hresims给出准分子离子峰m/z487.3057[m h]
(calcd for c
29h43
o6,487.3054),确定该化合物的分子量为486,分子式为c
29h42
o6,计算不饱和度为9。
[0033]1h-nmr(600mhz,cdcl3)中,低场区给出δ
h 6.58(1h,d,j=2.7hz,h-5),6.60(1h,d,j=2.7hz,h-3),提示可能为两个间位偶合的芳香质子信号;δ
h 5.76(1h,dd,j=10.0,1.6hz,h-2
″
),5.97(1h,d,j=10.0,4.5hz,h-3
″
)分别为一个顺式双键上的两组烯氢质子信号。δ
h 5.16(1h,t,j=7.1hz,h-12)提示为一个三取代双键上的氢。高场区,δ
h 3.80(3h,s)提示为一个甲氧基上的质子信号。δ
h 1.70(3h,s),1.64(3h,s)提示为两个烯甲基氢。由δ
h 0.88(3h,d,j=6.8hz,h-9
″
),0.94(3h,d,j=6.8hz,h-10
″
)两组甲基质子信号可知,该化合物中含有一个异丙基
–
ch(ch3)2片段。另外,高场区还出现一个角甲基上的氢信号δ
h 1.31(3h,s,h-7
″
)。
[0034]
13
c-nmr(150mhz,cdcl3)中共有29个碳信号,其中δ
c 173.4提示为羰基碳信号,δc149.0,144.0,135.2,131.8,131.0,128.9,124.9,117.9,117.3,114.9为10个sp2杂化碳信号,结合其氢谱推测该结构中含有一个四取代的苯环和两个双键(包括一个顺式双键)。高场区给出18个脂肪族碳信号,比化合物2多两个连氧碳信号δc79.2(c-8),74.7(c-9),通过二维谱数据分析进一步对其结构进行了确定。
[0035]
在hmbc谱中,h-3
″
与c-1
″
/c-5
″
存在相关,h-2
″
与c-4
″
/c-6
″
存在相关,h-5
″
与c-1
″
存在相关,h-6
″
与c-4
″
存在相关,h-7
″
与c-2
″
/c-6
″
存在相关,h-9
″
/h-10
″
与c-4
″
/c-8
″
存在相关,提示该结构中含有一个连有异丙基的环己烯结构片段。根据h-6
″
与c-2/c-1
′
存在相关,h-3与c-1
′
存在相关,表明该自旋系统的一端是通过c-1
′
与苯环的c-2位之间相连。结合化合物分子量推测c-1(δc144.0),c-1
″
(δc73.1)通过一个氧桥连结,结合1h-1
h cosy以及
hsqc相关确定c-8(δc79.2),c-9(δc74.7)处连有羟基取代。根据h-5与c-7有相关,h-8与c-6/c-10/c(9-me)有相关,h-10与c-11/c-12有相关,h-11与c-13有相关,h(13-me)/h-14与c-12有相关,提示结构中c-13位连有烯甲基,并且该脂肪链连于c-6;根据δh3.80与δc173.4有相关,提示c-1
′
连有甲氧羰基部分,由此,化合物的平面结构被确定下来。
[0036]
通过noesy谱确定了化合物3的c-1,c-1",c-4",c-6"位相对构型,h-1'(δh4.13)与h-9"(δh0.88)相关,h-1'(δh4.13)与h-7"(δh1.31)相关,h-6"(δh2.26)与h-7"(δh1.31)相关,h-6"(δh2.26)与h-9"(δh0.88)相关。由于该结构的脂肪链中含有一个邻二醇单元,我们采用mo盐诱导的方法,观察到333nm处的正cotton效应,确定8,9位邻二醇的相对构型为苏式,同时利用计算nmr的方式,确定化合物3的相对构型为1
′
s*,1"r*,4"r*,6"r*,8s*,9r*。该化合物的绝对构型是通过比较实验ecd与计算ecd的方法确定的,故该化合物的绝对构型为1
′
s,1"r,4"s,6"r,8s,9r。
[0037]
化合物3的1h(600mhz)与
13
c(150mhz)nmr数据(cdcl3)
[0038][0039]
sarcandralide d(4):白色不定型粉末;hresims给出准分子离子峰m/z 367.1494[m na]
(calcd for c
20h24
nao5,367.1521),确定该化合物的分子量为344,分子式为c
20h24
o5,计算不饱和度为9。
[0040]1h-nmr(400mhz,cdcl3)中,低场区给出δ
h 7.19(1h,d,j=2.9hz,h-5),7.07(1h,d,j=2.9hz,h-6),提示可能为两个间位偶合的芳香质子信号;δ
h 6.01(1h,dd,j=9.8,4.6hz,h-3
″
),5.82(1h,d,j=9.8,1.4hz,h-2
″
)分别为一个顺式双键上的两组烯氢质子信号。此外,低场区还存在一个醛基信号δ
h 10.36(1h,s,h-7)。较高场区,δ
h 4.17(1h,d,j=6.2hz,h-1
′
),2.36(1h,ddd,j=13.5,6.2,2.9hz,h-1
″
)提示其为相互偶合的
–
chch
–
片段。
δ
h 3.83(3h,s)为一个甲氧基上的质子信号。由δ
h 0.91(3h,d,j=6.8hz,h-9
″
),0.97(3h,d,j=6.8hz,h-10
″
)两组甲基质子信号可知,该化合物中含有一个异丙基
–
ch(ch3)2片段。高场区还出现一个角甲基上的氢信号δ
h 1.40(3h,s,h-7
″
)。
[0041]
13
c-nmr(100mhz,cdcl3)中,一共显示出20个共振碳信号,其中δ
c 189.9和172.9分别为醛基上和酯(羧)基上的碳信号;δ
c 150.1,149.1,135.1,130.8,125.0,124.5,119.6,112.9为芳香区的8个碳信号,结合其氢谱推测该结构中含有一个四取代的苯环和一个顺式双键。δc150.1,149.1表明苯环上含有邻二连氧取代的片段。高场区给出10个脂肪族碳信号。通过hsqc谱,我们对化合物中直接相连的碳氢信号进行了归属。
[0042]
在hmbc谱中,h-7与c-5,c-6相关,提示醛基是通过c-6与苯环相连;h-1
″
与c-1,c-2相关,以及h-1
′
与c-2相关,表明该自旋系统的一端是通过c-1
′
与苯环的c-2位之间相连。δc172.9的碳信号分别与h-1
′
和甲氧基上的氢信号相关,提示结构中含有一个甲酯基连在c-1
′
位。h-7
″
与c-1
″
,c-2
″
,c-3
″
相关,提示该甲氧基是通过c-2
″
与c-1
″
和c-3
″
连接起来的,且由c-2
″
的化学位移值为δc73.8,提示c-2
″
是一个与氧原子相连的季碳。结合hr-esims给出分子式为c
20h24
o5,去掉醛基和酯基中的3个氧原子,剩余两个氧原子应为对应苯环中δc150.1,149.1的两个碳上氧原子。由此,化合物4的平面结构被确定下来。
[0043]
其相对构型是通过noesy实验并结合相关氢之间的偶合常数确定下来的。在noesy谱中,h-1
″
与h-9
″
以及h-1
′
与h-7
″
有相关,提示h-1
′
与ch
3-7
″
处于同侧,h-1
″
与异丙基是处于同侧。此外,noesy谱中高场区信号干扰强烈,由ch
3-7
″
与h-1
″
之间的noe相关微弱不足以说明分子整体的相对构型,因此我们借助结构中b环与c环中部分质子之间的偶合常数来对整个分子结构的相对构型加以判断。在氢谱中,h-1
″
与h-6
″
上的两个质子的偶合常数分别为13.5hz和2.9hz,提示h-1
″
应该在六元环c系统中处于直立键。而又因h-1
″
与h-1
′
之间的偶合常数较小,约为6.2hz,推测h-1
′
应该处于b环的平伏键。该化合物的绝对构型是通过比较实验ecd与计算ecd的方法确定的,计算的1
′
s,1"r,4"s,6"r构型与实测的ecd的图谱吻合度较高,故确定该化合物的绝对构型为1
′
s,1"r,4"s,6"r。
[0044]
化合物4的1h(600mhz)与
13
c(150mhz)nmr数据(cdcl3)
[0045][0046]
sarcandralide e(5):淡黄色油状物;hr-esims给出准分子离子峰m/z 339.1519
[m na]
(calcd for c
19h24
nao4,339.1572),确定该化合物的分子量为316,分子式为c
19h24
o4,计算不饱和度为8。
[0047]1h-nmr(400mhz,cdcl3)中,低场区给出δ
h 6.54(1h,d,j=2.9hz,h-5),6.42(1h,d,j=2.9hz,h-3),提示可能为两个间位偶合的芳香质子信号;δ
h 6.26(1h,dd,j=9.9hz,h-5
″
),5.58(1h,d,j=9.9hz,h-6
″
)为一组顺式双键上的两个烯氢质子信号。较高场区,δ
h 3.57(1h,d,j=15.8hz,h-1
′
),3.50(1h,d,j=15.8hz,h-1
′
)提示其为一组亚甲基上的同碳偕偶的两个氢信号。此外,氢谱中还显示出一组甲氧基上的氢信号δ
h 3.83(3h,s)和三个明显的角甲基的氢信号δh1.31(3h,s,h-7
″
),1.58(3h,s,h-10
″
),1.66(3h,s,h-9
″
)。
[0048]
13
c-nmr(100mhz,cdcl3)中,一共显示出19个共振碳信号,包括11个sp2杂化的碳信号和8个脂肪区的碳信号。其中δc172.2为一个酯(羧)基上的碳信号;δ
c 148.8,145.1,131.8,131.0,124.3,122.7,122.6,121.8,117.1,112.2为另外sp2杂化的10个碳信号,再结合其氢谱推测该结构中含有一个1,3,4,5-四取代的苯环和两个双键(包括一个顺式双键)。
[0049]
在hmbc谱中,h-9
″
与c-4
″
/c-8
″
/c-10
″
存在相关,h-10
″
与c-4
″
/c-8
″
/c-9
″
存在相关,提示该结构中含有一个异丙基的结构片段连接在c-4
″
位。结合化合物分子量推测c-1(δc148.8),c-1
″
(δc78.6)通过一个氧桥连结。根据h-7
″
与c-1
″
有相关,确定了甲基的连接位置。根据δh3.68与δc172.2有相关,提示c-1
′
连有乙酰酯基部分,由此,化合物的平面结构被确定下来。
[0050]
由于化合物分子中只含有一个手性原子,因此对其绝对构型采用计算ecd的方式进行确定。计算的1"s构型与实测的ecd的图谱吻合度较高,故确定该化合物的绝对构型为1"s。
[0051]
化合物5的1h(600mhz)与
13
c(150mhz)nmr数据(cdcl3)
[0052][0053]
对发明所述五个新化合物的抗神经炎症活性进行了考察,其中在脂多糖(lps)诱导的小胶质细胞(bv2)模型中,在10μg/ml的浓度下,5个化合物均具备一定的抗神经炎症活性,其中化合物4和5抑制no生成作用与阳性对照药相当,因此本发明所述的新龙胆酸混源杂萜类化合物能应用于预防和治疗神经炎症药物的前景。
[0054]
本发明还提供一种药物组合物,包含所述的新龙胆酸混源杂萜类化合物和药学上
可接受的载体。所述的药物组合物用于预防和治疗神经炎症药物中。
[0055]
本发明的优点在于,所述化合物均为新化合物,结构新颖,且均为立体构型确定的光学纯化合物,同时其抗神经炎症活性强,具有进一步开发的价值。
附图说明
[0056]
图1化合物1的hr-esims谱;
[0057]
图2化合物1的1h-nmr谱(600mhz,cdcl3);
[0058]
图3化合物1的
13
c-nmr谱(150mhz,cdcl3);
[0059]
图4化合物1的hsqc谱(600mhz,cdcl3);
[0060]
图5化合物1的hmbc谱(600mhz,cdcl3);
[0061]
图6化合物1的1h-1
hcosy谱(600mhz,cdcl3);
[0062]
图7化合物1的noesy谱(600mhz,cdcl3);
[0063]
图8化合物2的hr-esims谱;
[0064]
图9化合物2的1h-nmr谱(600mhz,cdcl3);
[0065]
图10化合物2的
13
c-nmr谱(150mhz,cdcl3);
[0066]
图11化合物2的hsqc谱(600mhz,cdcl3);
[0067]
图12化合物2的hmbc谱(600mhz,cdcl3);
[0068]
图13化合物2的1h-1
hcosy谱(600mhz,cdcl3);
[0069]
图14化合物2的noesy谱(600mhz,cdcl3);
[0070]
图15化合物3的hr-esims谱;
[0071]
图16化合物3的1h-nmr谱(600mhz,cdcl3);
[0072]
图17化合物3的
13
c-nmr谱(150mhz,cdcl3);
[0073]
图18化合物3的hsqc谱(600mhz,cdcl3);
[0074]
图19化合物3的hmbc谱(600mhz,cdcl3);
[0075]
图20化合物3的1h-1
hcosy谱(600mhz,cdcl3);
[0076]
图21化合物3的noesy谱(600mhz,cdcl3);
[0077]
图22化合物4的hr-esims谱;
[0078]
图23化合物4的1h-nmr谱(600mhz,cdcl3);
[0079]
图24化合物4的
13
c-nmr谱(150mhz,cdcl3);
[0080]
图25化合物4的hsqc谱(600mhz,cdcl3);
[0081]
图26化合物4的hmbc谱(600mhz,cdcl3);
[0082]
图27化合物4的1h-1
hcosy谱(600mhz,cdcl3);
[0083]
图28化合物4的noesy谱(600mhz,cdcl3);
[0084]
图29化合物5的hr-esims谱;
[0085]
图30化合物5的1h-nmr谱(600mhz,cdcl3);
[0086]
图31化合物5的
13
c-nmr谱(150mhz,cdcl3);
[0087]
图32化合物5的hsqc谱(600mhz,cdcl3);
[0088]
图33化合物5的hmbc谱(600mhz,cdcl3);
[0089]
图34化合物5的1h-1
hcosy谱(600mhz,cdcl3)。
具体实施方式
[0090]
下面所列实施例有助于本领域技术人员更好地理解本发明,但不以任何方式限制本发明。
[0091]
实施例1
[0092]
化合物1-5的制备,具体包括以下步骤:
[0093]
取干燥的草珊瑚全草以80%工业乙醇回流提取2次,每次提取时间为2h,合并提取液浓缩得浸膏,浸膏采用乙酸乙酯萃取并将所得组分经硅胶柱色谱,以二氯甲烷-甲醇系统100:0,80:20,50:50,20:80进行等度梯度洗脱,共收集到4个馏分(a-d)。
[0094]
馏分b(二氯甲烷-甲醇80:20洗脱下来部分)经hp20柱色谱,以乙醇-水系统30:70,60:40,90:10,100:0进行梯度洗脱,得4个组分b1、b2、b3和b4。利用ods柱色谱将b2组分(乙醇-水系统60:40)以乙醇-水系统10:90,40:60,50:50,60:40,70:30,80:20,90:10进行梯度洗脱,得5个组分(a-e)。
[0095]
所得组分c(乙醇-水系统60:40洗脱下来部分)经硅胶柱色谱以石油醚-乙酸乙酯系统100:1,50:1,30:1,20:1,10:1在tlc分析的基础上得到5个亚组分(c1-c5)。
[0096]
在制备性反相高效液相色谱上使用甲醇-水(70:30,v/v)的流动相来分离c3(石油醚-乙酸乙酯30:1洗脱下来部分)和c4(石油醚-乙酸乙酯20:1洗脱下来部分)得到了化合物1-5。
[0097]
实施例2
[0098]
化合物1-5的抗神经炎症的活性考察。
[0099]
bv2细胞在温度为37℃、co2浓度为5%的细胞培养箱中用高糖培养基dmem培养至对数增殖期,备用。待测化合物使用dmso配成10μm。细胞浓度调节为106/ml,96孔板每孔接种200μl。细胞孵育1h后用1μg/l的lps处理,加入10μg/l的待测物处理24h。用griess反应法测定了bv-2细胞培养上清液中no
2-浓度间接反映no浓度。在测试浓度下,没有一种测试化合物显示出明显的细胞毒性。
[0100][0101]a以地塞米松作为阳性对照药
[0102]
活性结果表明,5个新龙胆酸混源杂萜类化合物均具备一定的抗神经炎症活性,可用于抗神经炎症的药物开发。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。