1.本发明涉及钌配合物的诊疗作用,还涉及脂质体修饰的钌配合物和狂犬病毒衍生肽(rabies virus derived peptide,rdp,ytiwmpenprpgtpcdiftnsrgkrasngggg(d)rrrrrr rrr)修饰的钌配合物脂质体及其制备方法和rdp在靶向诊疗真菌性疾病(如隐球菌性脑膜炎)中的应用。
背景技术:
2.致病菌(如隐球菌)在机体免疫力低下时乘机感染机体的各个器官和组织(如脑膜和/或脑实质,等)。由于发病症状隐蔽,不容易发现,特别是不能得到及时有效的治疗,真菌感染的发病率较高。近年来,随着广谱抗生素、激素以及免疫抑制药的大规模广泛应用,使致病菌的基因发生了突变而产生了广泛的耐药性,导致现有治疗新生隐球菌的药物治疗效果不理想。目前现有的治疗真菌的药物有两性毒素b、氟胞嘧啶、氟康唑以及伊曲康唑,药物开发较早,且长期使用的副作用较大,因此有必要开发新的治疗真菌感染的药物。
技术实现要素:
3.为了解决现有技术中的问题,根据本发明的第一方面,本发明提供一种多吡啶钌配合物,该多吡啶钌配合物能够用于预防或诊疗真菌(如隐球菌)感染。
4.为实现上述目的,本发明的技术方案为:
5.本发明所述钌配合物,结构式如下:
[0006][0007]
本发明所述钌配合物在制备预防或诊疗真菌(如隐球菌)感染疾病药物中的应用。
[0008]
根据本发明的一个实施方案,所述隐球菌感染疾病为隐球菌性脑膜炎。
[0009]
脂质体是一种囊泡体,它能够将药物包封于其类脂质双分子层内。其中,两层磷脂分子的疏水部组成的脂质夹层疏水端可装载疏水性药物,而亲水性的内部囊腔可装载水溶性药物。由于被包封在脂质体内部,能起到一定的缓释作用达到延长药物作用时间的作用,且脂质体具有可以和细胞膜融合的特性,药物的稳定性被大大提高。此外脂质体还表现出能够提高药物溶解性、提高生物利用度等优点,因而可通过与一些药物的结合形成药物载体。
[0010]
第二方面,本发明提供上述钌配合物的脂质体。
[0011]
上述钌配合物的脂质体,其特征在于:所述脂质体由包括胆固醇、钌配合物、维生
素e、吐温80和磷脂在内的原料制得。
[0012]
所述胆固醇、钌配合物、维生素e、吐温80和磷脂的用量为胆固醇1-3份,钌配合物1份,维生素e 2-5份,吐温80 2-5份,磷脂16-30份。优选胆固醇1份,钌配合物1份,维生素e 2份,吐温80 2份,磷脂20份。
[0013]
第三方面,本发明提供rdp修饰的钌配合物的脂质体。
[0014]
rdp修饰的钌配合物的脂质体,其特征在于:所述脂质体由包括胆固醇、钌配合物、维生素e、吐温80、rdp和磷脂在内的原料制得。
[0015]
所述胆固醇、钌配合物、维生素e、吐温80、rdp和磷脂的用量为胆固醇1-3份,钌配合物1份,维生素e 2-5份,吐温80 2-5份,rdp 3-6份,磷脂16-30份。优选胆固醇1,钌配合物1份,维生素e 2份,吐温80 2份,rdp 3份,磷脂20份。
[0016]
按照上述处方精密称取各种脂材放在茄形瓶中,加入氯仿溶解,35-37℃减压旋蒸15-20min,使其在瓶壁上均匀地形成薄膜,加入去离子水在35-37℃摇床中水化45min-60min形成悬浮液,超声150-200s,过220nm的膜使粒径分布均匀,保存在4℃冰箱内。
[0017]
第四方面,本发明提供上述钌配合物的脂质体或rdp修饰的钌配合物的脂质体在制备预防或治疗隐球菌性脑膜炎药物中的应用。
[0018]
有益效果:
[0019]
本发明提供一种新的钌配合物,并提供该钌配合物在制备预防或诊疗隐球菌感染药物中的应用。本发明还提供钌配合物的脂质体及rdp-脂质体修饰的钌配合物。本发明通过隐球菌与两种新型钌配合物在体外培养的条件下共同孵育,对其进行抑菌活性的检测。使用荧光分光光度计对隐球菌体内钌配合物的吸收进行测定,然后通过荧光显微镜下观察进行验证。利用配合物自身的荧光特性以及rdp的靶脑特性,在体外实验的基础上进行脑膜炎模型小鼠的脂质体治疗并观察其活体成像结果。
[0020]
本实验通过对rdp-脂质体修饰的钌配合物的分散度和稳定性研究确定了脂质体制备的最佳配方,通过小鼠的体内药效学实验对隐球菌性脑膜炎的治疗方面提供了理论研究。本发明制备出了钌配合物和rdp-脂质体修饰的钌配合物,并对其粒径分布、zeta电位、分散度、包封率、稳定性等物理化学性质进行了表征,结果表明制备的钌配合物和rdp-脂质体修饰的钌配合物脂质体平均粒径都在100nm以内,包封率大于80%,分散度良好。
[0021]
本实验中小鼠的活体成像实验以及离体器官荧光观察均表明了制备的经rdp-脂质体修饰的钌配合物具有明显的靶脑作用,体内药效学实验结果可知rdp-脂质体修饰的钌配合物治疗组最久的可达20天,比普通脂质体治疗组存活时间最多延长了5天,平均存活时间延长了2天。为侵袭性真菌感染的治疗提供了依据。
附图说明
[0022]
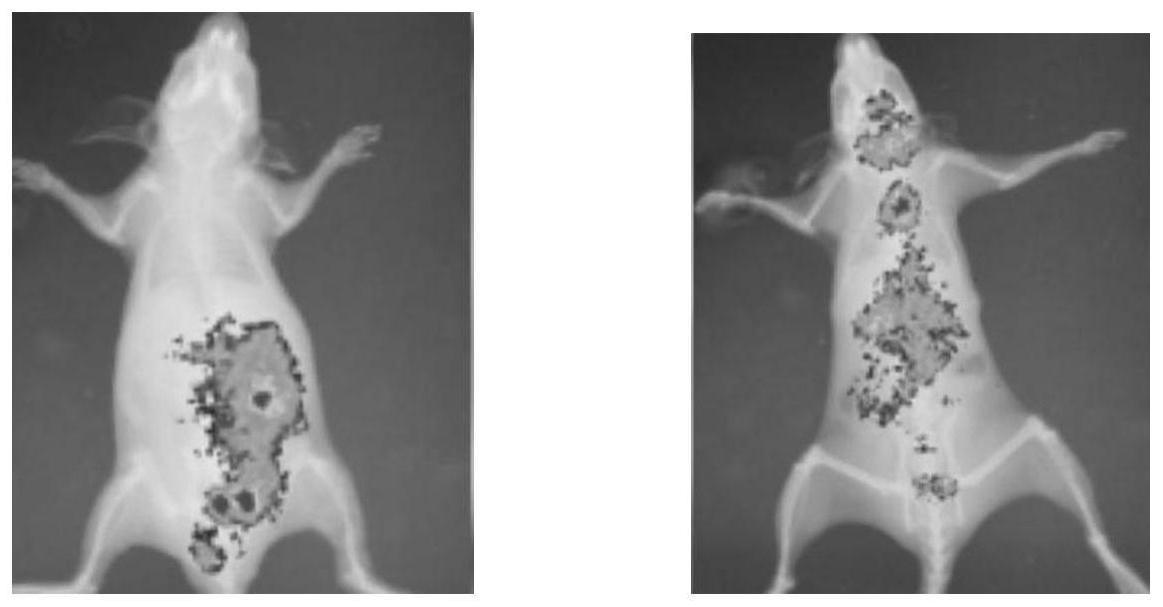
图1是本发明钌配合物的普通脂质体与rdp修饰的钌配合物脂质体分别对实验小鼠活体成像结果图;体内钌配合物分布主要在肺、肾、肝、脾等器官(图1左),而经rdp-脂质体修饰过后,钌配合物明显入脑(图1右),实验结果表现出了rdp-脂质体钌配合物具有很强的靶脑治疗作用。
[0023]
图2是本发明钌配合物的普通脂质体和rdp-脂质体修饰的钌配合物两种药物治疗组结果比对图,对照组为使用生理盐水治疗,空白组为没有经过任何处理,采用相同质量的
钌配合物治疗小鼠,没有加入rdp-脂质体的为钌配合物组,而加入rdp-脂质体的为钌配合物脂质体组。
[0024]
图3是使用钌配合物有助于诊断组织匀浆中的病原菌;3a.是显微镜下的病原菌,3b是加了钌配合物的病原菌;3c是加了钌配合物的病原菌。
具体实施方式
[0025]
下面通过具体实施例对本发明进行具体描述,在此指出以下实施例只用于对本发明进行进一步说明,不能理解为对本发明保护范围的限制,本领域的技术熟练人员可以根据上述发明内容对本发明作出一些非本质的改进和调整。除特殊说明外,本发明所述份数均为重量份,所述百分比均为质量百分比。
[0026]
本发明所用原料及试剂均为市售产品。
[0027]
实验室自主合成的新型多吡啶钌配合物,蛋白胨(安琪酵母股份有限公司),酵母浸粉(安琪酵母股份有限公司),葡萄糖(成都市科龙化工试剂厂),琼脂粉(成都市科龙化工试剂厂),kc-39(吉尔生化上海有限公司),氯化钠注射液(石家庄四药有限公司),卵磷脂(山东西亚化学工业有限公司),胆固醇(合肥博美生物科技有限责任公司),n,n-二甲基甲酰胺(合肥博美生物科技有限责任公司),三氯甲烷(成都市科龙化工试剂厂),tween-80(成都市新都区木兰镇工业开发区),n-甲基吗啡啉,血细胞计数板,显微镜盖玻片(江苏世泰实验器材有限公司),印度墨汁,15ml茄形瓶等。
[0028]
实施例1本发明钌配合物的制备
[0029]
本发明钌配合物结构式为:
[0030][0031]
制备步骤为:
[0032]
第一步:将rucl3(2.0mmol)和2-苯基吡啶(4.4mmol)混合在250ml圆底烧瓶中,加入乙二醇乙醚(60ml)和水(20ml)并加热到140℃回流24h,冷却至室温后抽滤,抽滤过程中用丙酮和乙醇的混合溶液洗涤(60ml:60ml),真空干燥得到黄色固体[(bpy)2ru(μ-cl)2]2(无需进一步纯化)0.85g,产率约为60%。
[0033]
第二步:称取[(bpy)2ru(μ-cl)2]2(0.076mmol)和1,10菲咯啉-5,6二酮(0.195mmol)于装有隔膜的封闭棕色小瓶中,加入乙二醇8ml,加热到130℃搅拌反应15h,冷却至室温后将反应溶液加入到含35ml水的离心管中并混匀,加入过量的六氟磷酸铵(nh4pf6)将产物沉淀出来,离心去掉澄清的溶液再加水清洗两次,用硅胶柱层析提纯,洗脱剂为乙腈:水:饱和硝酸钾溶液=150:3:1,减压蒸发溶剂至1ml时,加入过量的水将产物沉淀出来,并用水洗涤(除去洗脱剂中的硝酸钾),真空干燥得到粉红色固体43mg,产率约为46%。在核磁共振波谱仪brukeradvance iii上记录其1h和13c核谱,以确定其成分。核磁表
征为:δ(ppm)8.52(s,1h),8.50(s,1h),8.485(d,j=2.0hz,1h),8.475(d,j=2.0hz,1h),8.345(d,j=2.7hz,1h),8.328(d,j=2.7hz,1h),8.05(m,2h),7.86(m,2h),7.73(m,2h),7.61(d,j=6.1hz,1h),7.59(d,j=6.0hz,1h),7.48(m,1h),7.44(m,1h),7.41(m,4h),2.207(s,3h),2.198(s,3h),1.426(s,9h),1.412(s,9h).13c-nmr(75mhz,cd3cn):δ(ppm)152.6,152.52,152.47,152.4,152.2,151.96,151.94,139.28,139.22,139.1,138.67,138.64,138.49,138.46,128.6,128.5,128.4,125.7,125.6,125.5,125.2,124.2,122.61,122.57,36.3,30.52,30.50,18.62,18.56.6.ir(neat):ν(cm-1
)2960,2872,1615,1466,1414,1244,828,762,606,555,419.cd(δε/m-1
cm-1
,mecn):279nm(-138),293.5nm( 315)。通过高分辨质谱计算出其分子式为c40h44f6n6pru(m-pf6),分子量为855.2298。
[0034]
实施例2钌配合物的抗隐球菌活性的研究
[0035]
隐球菌的实验室培养方法:1.配制ypd固体培养基、液体培养基;2.在高压蒸汽灭菌锅中对配制好的培养基进行高温灭菌;3.冷却ypd固体培养基,烘干容器表面的水份;4.取少量隐球菌接种在ypd固体培养基中培养;5.把接种好的培养皿放在30℃的恒温培养箱中进行培养(倒置培养);6.将ypd固体培养基中生长到对数生长期的菌种接到少量ypd液体培养基中扩大培养(低速振摇)。
[0036]
多吡啶钌配合物的最低抑菌浓度(mic)和半数抑制浓度(ic50)的测定:
[0037]
最低抑菌浓度(mic)测定实验:
[0038]
首先通过纸片法对本实验中的药物的最低抑菌浓度做一个预实验:用无菌棉签蘸取校正好浓度为0.5比浊浓度的隐球菌菌悬液充分且均匀地涂布在整个ypd固体培养基表面。待水分挥发完全后贴含钌配合物药物的纸片。用无菌镊子将药敏纸片贴在培养基表面,每个平板上贴6张纸片,纸片间距应不少于24mm,纸片中心距培养皿边缘不少于15mm。在菌接种完15min内贴完纸片。将培养皿倒置,30℃下恒温孵育18-24h。
[0039]
多吡啶钌配合物药物最低抑菌浓度测定方法:1.每孔加100μl液体培养基;2.第一孔加100μl药液(2.5mg/ml);3.取第一孔的液体100μl加入第二个孔,依次稀释;4.再在各孔加入100μl的扩大培养后的隐球菌菌液(2*104个/ml);5.药物的起始浓度是1.25mg/ml,培养48h,观察各孔内是否有白点出现。开始出现白点的孔记录下来作为抑制真菌生长的起始点,出现白点的上一个点即为最低抑菌浓度点,重复上述实验三次,可以根据药物的初始浓度得到最低抑菌浓度(mic)值。
[0040]
多吡啶钌配合物药物半数抑制浓度(ic50)测定实验步骤[11]:1.每孔加100μl扩大培养后的隐球菌菌液(2*104个/ml),培育24h,待细胞贴壁生长50%以上;2.第一孔加100μl药液(2.5mg/ml),取第一孔100μl加入第二个孔,依次稀释,等待药物作用48h;3.弃去原来培养液和药液,加入100μl新鲜培养液,每孔加入20μlmtt溶液(本课题组配制的,终浓度为10%),继续培养;4.在mtt溶液加入培养4h后,结晶充分形成。此时将96孔板轻轻倒置,放在事先铺在桌面的几张滤纸上,这样便可以将上清吸走;5.接下来在每孔中分别加入100μl二甲基亚砜,放在低速摇床上振荡10min左右,使mtt与dna结合生成的结晶物得以充分溶解。最后于490nm处酶联免疫检测仪下测量各孔的吸光度值(即od值)。
[0041]
多吡啶钌配合物在隐球菌体内的代谢活性观察:
[0042]
使用f-7000荧光分光光度计测定多吡啶钌配合物的浓度。同浓度的两种钌配合物药物1μl分别与1ml隔夜培养的隐球菌菌悬液,共同孵育2h后,用无菌生理盐水冲洗三次并
离心,利用荧光显微镜观察多吡啶钌配合物与隐球菌菌体是否有结合。
[0043]
多吡啶钌配合物的体外抗隐球菌活性结果:
[0044]
隐球菌的一般实验室培养结果:
[0045]
隐球菌具备贴壁生长的特性,在固体培养基上菌落呈油脂状,表面光滑、粘稠,菌落边缘有缺损,菌落颜色呈乳白色;在液体培养基中以沉淀生长的方式繁殖。
[0046]
纸片法对钌配合物药物的最低抑菌浓度的预实验结果:
[0047]
纸片周围抑菌浓度范围内的隐球菌不会继续生长,而抑菌浓度范围外的菌株则继续生长,从而在纸片的周围形成一层透明的抑菌圈,在浓度为1.25mg/ml和2.5mg/ml下的钌配合物药物抑菌圈均大于氟康唑药物,且浓度越高抑菌圈越大越明显,为接下来的最低抑菌浓度(mic)值的测定提供了参考。
[0048]
钌配合物药物最低抑菌浓度(mic)测定实验结果:
[0049]
依据最低抑菌浓度的测定方法三次重复试验得到钌配合物药物的mic为1.25*2-3
mg/ml。
[0050]
钌配合物药物半数抑制浓度(ic50)测定实验结果:
[0051]
经bliss法计算得到钌配合物药物的半数抑菌浓度(ic50)值:0.005655878μmol/ml。
[0052]
吡啶钌配合物在隐球菌菌体内的代谢活性测定结果:
[0053]
本实验中多吡啶钌配合物与隐球菌有很好的结合作用,钌配合物与隐球菌结合结合能力要强于氟康唑。在高倍镜下可观察到药物与隐球菌菌体内细胞核结合,由此可知实验药物可以穿透隐球菌的坚硬外壳,与隐球菌结合。通过以上的研究还发现实验室自主合成的多吡啶钌配合物有很强的荧光,利用这一特性为后续的靶向治疗提供了便利。
[0054]
实施例3
[0055]
钌配合物脂质体的制备和表征
[0056]
处方:胆固醇1mg,钌配合物1mg,维生素e 2mg,吐温802mg,磷脂20mg。
[0057]
按照上述处方精密称取各种脂材放在预先准备好的15ml茄形瓶中,加入4-4.5ml氯仿溶解,37℃减压旋蒸15min,使其在瓶壁上均匀地形成一层薄膜,加入去离子水2ml,在37℃摇床中水化45min-60min,形成悬浮液,间歇超声180s,过220nm的膜使粒径分布均匀,保存在4℃冰箱内。
[0058]
发明人考察了处方和制备工艺对钌配合物脂质体的制备的影响,结果如下。
[0059]
1.药脂比对包封率有较大影响。当磷脂用量增大时,能够包封更多的内水相,相应地能够包封更多的药物(钌配合物)。但是磷脂的浓度不能过高,否则无法形成稳定均一的脂质体。结果表明,当药脂比达到1∶16(质量比)时已可达到最高的包封率,药脂比继续增加时,包封率不再增加。
[0060]
2.载药温度主动载药法载药时,需给予一定的温度,以增强脂质体双分子层的通透性,并使药物分子能够跨过一定的能垒穿过磷脂双分子层。实验结果表明,温度在37℃左右时可达到最高的包封率。而温度进一步升高时,包封率有一定程度的下降,推测原因为随着温度的升高,脂质体膜的通透性增加,当增加到一定程度时,会导致膜的破裂,致使膜内的h 渗漏,削弱了离子梯度;同时,也会导致药物的渗漏率增加。综合考虑温度对脂质体稳定性的影响,选择载药温度为37℃。
[0061]
3.载药时的加热时间主动载药时,将药物加入到脂质体的外水相,药物在离子梯度的驱使下进入脂质体内部,很快达到平衡;同时应考虑到温度对脂质体稳定性的影响,因此载药过程应控制在较短的时间内。当加热时间过短时,则药物还未达到分配平衡,因此包封率较低。而当药物分配达到平衡后,随着加热时间的延长,包封率不会进一步提高,相反,在高温下药物会有一定的渗漏。因此,当加热时间延长至20min时,包封率略有下降。
[0062]
实施例4
[0063]
rdp修饰的钌配合物脂质体的制备参照实施例3的方法制备rdp-脂质体修饰的钌配合物。
[0064]
处方:胆固醇1mg,钌配合物1mg,维生素e 2mg,吐温802mg,rdp 3mg,磷脂20mg。
[0065]
实验所用的多肽rdp是狂犬病毒衍生肽(rabies virus derivedpeptide,rdp,ytiwmpenprpgtpcdiftnsrgkrasngggg(d)rrrrrr rrr),由一种连接物dspe-peg-nhs与来源于狂犬病毒糖蛋白中的rvg通过物理搅拌的方式连接得到的一种能靶向脑部中枢神经的衍生肽(wang qinghua,cheng shang,qin fen,fuailing.and fu chen.applicationprogress ofrvgpeptides to facilitate the delivery oftherapeutic agents into the central nervous system.rscadvances,2021,11(15),pp.8505-8515.)。
[0066]
实施例5
[0067]
对实施例3-4制备的脂质体进行表征
[0068]
粒径测定:取1ml的脂质体溶液于马尔文激光粒度仪上进行测定;
[0069]
电位测定:取1ml的脂质体溶液于马尔文zeta电位分析仪上进行测定;
[0070]
采用透析破乳法结合f-7000荧光分光光度计测脂质体包封率:实验分成两份(每份500μl),一份用200ml无水乙醇透析液(1:1)透析6h,收集脂质体部分,加1滴tween-80破乳,用荧光分光光度法测定包裹在脂质体内的药物浓度c1;另一份加1滴tween-80直接破乳,经荧光分光光度法测定钌配合物脂质体得到c2,按照如下公式计算,包封率=c1/c2×
100%计算。
[0071]
实施例3制备的钌配合物理化性质脂质体的表征:
[0072]
制得的钌配合物平均粒径在43nm左右,电位-24.8mv,分散度良好,荧光光度法测其包封率在88%左右。4℃冰箱保存,溶液澄清透明呈褐黄色乳光。以上结果表明,所制得的钌配合物粒径在100nm以内,分散度良好。4℃冰箱放置60天后,外观依旧澄清透明并分别呈现其特色乳光,与刚刚制备时相比无明显变化。对其包封率进行测定,60天时包封率依然接近80%,表现出了很好的稳定性。
[0073]
实施例4制备的rdp-脂质体修饰的钌配合物的表征:
[0074]
制得的rdp-脂质体修饰的钌配合物平均粒径在43nm左右,电位-26.5mv,分散度良好,荧光光度法测其包封率在87%左右。4℃冰箱保存,溶液澄清透明呈淡黄色乳光,时间可持续四周左右。
[0075]
研究表明,脂质体粒径在100nm以内对细胞膜有高度穿透性,且能在炎症组织中停留更长的时间。在本实验的处方条件下制备出的rdp-脂质体修饰的钌配合物粒径均在100nm以内,且分散度良好。4℃冰箱放置60天后,包封率仍然在80%左右,可见其稳定性良好。
[0076]
实施例6
[0077]
四组治疗和处理方式对于小鼠治疗效果的研究:
[0078]
实验动物
[0079]
昆明种小鼠,体重(24
±
5)g,饲养于西南大学药学院spf级小鼠饲养室,固定温度、湿度条件,自由进食、进水。
[0080]
隐球菌性脑膜炎模型的建立以及实验药物诊疗效果的评价
[0081]
隐球菌性脑膜炎模型建立实验步骤:
[0082]
菌悬液的配制:
[0083]
取无菌生理盐水1ml于无菌试管,无菌接种环挑取适量隐球菌菌落于试管中,缓缓振荡,这样就配制好了菌悬液。将血细胞计数板盖上盖玻片后,吸取一滴菌悬液,从盖玻片侧边缓慢注入
[7]
,显微镜下计数(共数5个方格),计算浓度:
[0084][0085]
重复上述步骤,直至配成终浓度为4.0*107个/ml的隐球菌生理盐水悬液,注意现配现用。
[0086]
动物处理:
[0087]
选择实验小鼠腹腔注射环磷酰胺注射用水溶液(浓度10mg/ml,剂量10μl/g体重);24h后每只小鼠用0.2ml 4%的水合氯醛麻醉。取对数生长期的菌种用生理盐水稀释得到4.0*107个/ml浓度为隐球菌生理盐水悬液,每只小鼠注射6μl菌悬液,小鼠苏醒后正常饲养,记录生长期。
[0088]
动物(隐球菌脑膜炎小鼠)分组及处理:
[0089]
确认感染隐球菌性脑膜炎的小鼠随机分组,每组选取9只生理状况相同、体重相近的雄性小鼠,共4组,(其中空白组为正常小鼠不注射任何试剂),除空白组、对照组外每天尾静脉注射1ml的0.2mg/ml钌配合物药液进行治疗。一旦有小鼠死亡,立即记录时间(单位:天),收录在excel表格中以便之后数据处理。
[0090]
a、空白组没有任何处理
[0091]
b、对照组:注射1ml生理盐水
[0092]
c、钌配合物治疗组
[0093]
d、rdp-脂质体修饰的钌配合物治疗组
[0094]
钌配合物及rdp-脂质体修饰的钌配合物治疗的小鼠活体成像结果:
[0095]
使用小动物活体成像仪发现体内钌配合物分布主要在肺、肾、肝、脾等器官(图1左)。而经rdp-脂质体修饰过后,钌配合物明显入脑(图1右),实验结果表明rdp-脂质体钌配合物具有很强的靶脑治疗作用。
[0096]
对小鼠解剖取各个器官后的离体分析,普通脂质体的钌配合物主要分布在肝、肺等器官,脑中分布很少,rdp-脂质体修饰的钌配合物在肾中有少量分布,主要分布在脑、肝、肺等器官,脑中荧光强度明显高于其他器官,此部分更加直观地表明了rdp的靶脑作用。rdp-脂质体修饰的钌配合物对于隐球菌性脑膜炎起到了良好的靶向治疗效果。
[0097]
隐球菌性脑膜炎模型的建立以及实验药物治疗效果的评价结果:
[0098]
通过图2统计图表可直观的得到不同治疗方式下小鼠的存活情况。对照组为使用生理盐水治疗。空白组为没有经过任何处理。采用相同质量的钌配合物治疗小鼠,没有加入
rdp-脂质体的为钌配合物组,而加入rdp-脂质体的为钌配合物脂质体组。实验结果发现对照组小鼠存活时间最短,而rdp-脂质体修饰的钌配合物组的小鼠存活时间最长。其中钌配合物组治疗组存活时间比对照组小鼠的平均存活时间要多2天左右,rdp-脂质体修饰的钌配合物治疗组则要比对照组疾病模型小鼠的平均存活时间多5天左右。rdp-脂质体修饰的钌配合物治疗组治疗效果最好,最久可存活20天。上述实验结果证明了钌配合物对动物疾病模型有治疗作用,也证明了rdp-脂质体在钌配合物脂质体治疗的过程中起到了一定的缓释和靶向治疗作用,从而延长了疾病模型小鼠的存活时间。
[0099]
实施例7
[0100]
使用钌配合物有助于诊断组织匀浆中的病原菌。组织匀浆提取自安乐死后的小鼠,使用印度墨汁染色。检测方法是:首先将一滴用生理盐水稀释的10%组织匀浆液放在载玻片上;2.将少量印度墨汁也添加到组织匀浆液中。3.将一小滴钌配合物(最终浓度约为1%)也与载玻片上的匀浆混合。4.放置盖玻片,并使用荧光显微镜(日本奥林巴斯)观察组织匀浆,使用钌配合物帮助检测组织匀浆中的病原菌。在显微镜下,如果匀浆液体发出明亮的圆点则明确地诊断出了病原菌的感染(图3)。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。