1.本发明涉及药物制剂领域。本发明提供一种具备良好稳定性的女性避孕或治疗、预防更年期综合征药物组合物。
背景技术:
2.口服避孕药通常由人工合成的孕激素和雌激素配伍而成。这两种激素类化合物均具有促进女性附性器官成熟及第二性征出现,并维持正常性欲及生殖功能的作用。雌激素炔雌醇与孕激素醋酸炔诺酮(旋光度-32
°
至-38
°
)组合的复方制剂能够用于女性避孕及治疗或预防更年期综合征。
3.炔雌醇是一种口服生物有效的雌激素,在几乎所有的现代复方口服避孕药配方中使用,在单剂量产品中的含量通常在100
µ
g以下用量较少,暴露在空气后容易发生氧化降解,导致药物的效果下降。因此,复方制剂中需要额外关注炔雌醇的稳定性以保障药物的安全性和有效性。
技术实现要素:
4.本发明提供一种包含炔雌醇和醋酸炔诺酮的组合物,通过使用抗氧化剂维生素e控制炔雌醇的氧化降解;经过研究,本技术意外地发现将维生素e的量控制在一定范围内,不仅能保证炔雌醇的稳定性,同时还能降低另外两个降解物质的产生,从而使复方制剂在整体上获得了更好的稳定性效果。
5.一方面,本发明提供一种药物组合物,包含以下组分:a)活成成分包含炔雌醇和醋酸炔诺酮,并且炔雌醇与醋酸炔诺酮以相接触的方式存在于单位制剂中,b)维生素e,c)以及其他药学上可接受的辅料。
6.在一些实施方案中,组合物中维生素e的用量为组合物总重量的0.005%-0.02%。
7.在一些实施方案中,组合物中炔雌醇:醋酸炔诺酮:维生素e的重量比为0.004-0.008:0.756-1.515:0.01-0.04。炔雌醇:醋酸炔诺酮:维生素e的具体的重量比可以选择0.004:0.756:0.01-0.02,或0.008:1.515:0.02-0.04。
8.在一些实施方案中,组合物中通过hplc测定相对于炔雌醇保留时间1.41
±
0.02处杂质的量低于总峰面积的0.5%。
9.在一些实施方案中,组合物中通过hplc测定相对于炔雌醇保留时间1.41
±
0.02处杂质的量低于总峰面积的0.25%。具体的数值还可以低于0.23%。
10.在一些实施方案中,组合物中通过hplc测定相对于炔雌醇保留时间2.21
±
0.02处杂质的量低于总峰面积的0.5%。
11.在一些实施方案中,组合物中通过hplc测定相对于炔雌醇保留时间2.21
±
0.02处杂质的量低于总峰面积的0.25%。具体的数值还可以低于0.22%或0.05%。
12.在一些实施方案中,组合物中杂质的总量低于2.0%、1.8%、1.7%、1.6%、1.5%、1.4%、1.3%、或1.2%。
13.在一些实施方案中,所述组合物为片剂或胶囊剂,其中所述其他药学上可接受的辅料包括稀释剂、粘合剂、润滑剂、崩解剂、额外稳定剂中的一种或多种。
14.在一些实施方案中,稀释剂选自碳酸钙、碳酸钠、磷酸钙、磷酸二钙、硫酸钙、磷酸氢钙、磷酸钠、乳糖、蔗糖、微晶纤维素、甘露醇、山梨醇、淀粉、预胶化淀粉、玉米淀粉、部分预胶化淀粉、糖粉、乙基纤维素、异麦芽酮糖醇及其混合物。在一些实施方案中,稀释剂为乳糖和淀粉的混合物。应当理解,除非明确相反说明,否则本文中使用的术语稀释剂或填充剂可互换使用。
15.在一些实施方案中,润滑剂选自硬酯酸镁、硬酯酸钙、硬酯酸锌、蔗糖硬酯酸酯、硬酯酸、二氧化硅、滑石粉、山嵛酸甘油酯、氢化植物油、聚乙二醇、硬酯基富马酸钠。在一些实施方案中,润滑剂是硬脂酸镁。
16.在一些实施方案中,药物组合物包含以下组分或由以下组分组成:炔雌醇0.004-0.008份,醋酸炔诺酮 0.756-1.515份,维生素e 0.01-0.04份,稀释剂95-100份,润滑剂0.25-0.75份。
17.在一些实施方案中,药物组合物由以下成分组成或由以下组分组成:炔雌醇0.004-0.008份,醋酸炔诺酮0.756-1.515份,维生素e 0.01-0.04份, 乳糖87-88份,淀粉8-12份,硬脂酸镁0.25-0.75份。
18.在一些实施方案中,药物组合物包含以下组分或由以下组分组成:炔雌醇0.004-0.008份,醋酸炔诺酮0.756-1.5156份,维生素e 0.01-0.02份, 乳糖88.7-88.8份,淀粉10份,硬脂酸镁0.5份。
19.在一些实施方案中,药物组合物包含以下组分或由以下组分组成:炔雌醇0.004份,醋酸炔诺酮0.756份,维生素e 0.01-0.02份, 乳糖88.7-88.8份,淀粉10份,硬脂酸镁0.5份。
20.在一些实施方案中,药物组合物包含以下组分或由以下组分组成:炔雌醇0.008份,醋酸炔诺酮1.515份,维生素e 0.02-0.04份, 乳糖88.7-88.8份,淀粉10份,硬脂酸镁0.5份。
21.在一些实施方案中,本文提供的药物组合物为片剂形式,并可包含包衣剂,例如薄膜包衣剂。包衣材料可以选择聚乙烯醇。包衣剂中可进一步包含颜料。
22.另一方面,本发明提供一种上述药物组合物的制备方法。在制备方法中使用湿法制粒工艺。其中的制粒溶剂为乙醇和/或三氯甲烷。
23.另一方面,本发明提供一种上述药物组合物作为女性避孕药物或治疗或预防更年期综合征药物的用途。
24.另一方面,本发明提供一种上述药物组合物在制备女性避孕药物或治疗、预防更年期综合征药物的用途。
25.定义本文所采用术语“包括”意指词组“包括(但不限于)”,并可与其交换使用。本文所采用术语“包含”意指词组“包含(但不限于)”,并可与其交换使用。本专利中的使用“包括”或“包含”的技术方案,可以进一步限定成“组成”或“构成”。
26.本文中使用的“%”指作为计算单个成分重量百分比的基础的总重量的百分比。对于单个口服剂型,单个组分的%可以计算为单个口服剂型所有组分的总重量的百分比。例如,当单个口服剂型为片剂时,总重量可以是片剂所有组分的总重量。无特殊说明时,%均为重量%,当使用固体和液体混合时为重量体积百分比。
27.本文所采用术语“或”意指“和/或”,并可与其交换使用,除非另有说明。
28.本文中使用的数值除了数值本身之外,还包括本领域能够接受的测量或操作误差范围。除特别定义之外,本技术的误差范围可以选择具体数值的
±
10%。
29.术语“药学上可接受的辅料”是指无毒的载体、辅剂或载体,其不会对与其一起配制的化合物的药理活性产生不利影响,并且对人类使用也是安全的。
30.术语“相对于炔雌醇保留时间”是指检测到的该杂质的保留时间与活性成分炔雌醇的保留时间的比值。例如,“相对于炔雌醇保留时间2.21
±
0.02”是指hplc测定该物质的保留时间为炔雌醇保留时间的2.21
±
0.02倍;“相对于炔雌醇保留时间1.41
±
0.02”是指hplc测定该物质的保留时间为炔雌醇保留时间的1.41
±
0.02倍。
31.有益效果1.本发明通过使用抗氧化剂维生素e控制了包含炔雌醇和醋酸炔诺酮的复方组合物中炔雌醇的氧化降解。
32.2.本发明发现炔雌醇和醋酸炔诺酮的复方制剂中抗氧化剂维生素e的用量与稳定性的提高并非线性正比关系。本发明通过将维生素e的用量控制在特定的范围内,不仅保证了炔雌醇的稳定性,还同时降低另外两个降解物质的产生(相对于炔雌醇保留时间为1.41
±
0.02和2.21
±
0.02),进一步提高了复方制剂的总体稳定性。
33.3.相对于通过复杂包装提高制剂的稳定性,本发明提高炔雌醇和醋酸炔诺酮复方制剂稳定性的方法更为简单并且易于工业化生产,能够有效降低产品的包装成本并提高工厂的生产效率。
附图说明
34.图1 实施例1制剂0天的hplc图谱。
35.图2 实施例1制剂在40
°
c/75%rt保存3个月的hplc图谱。
36.图3 实施例2制剂0天的hplc图谱。
37.图4 实施例2制剂在40
°
c/75%rt保存3个月的hplc图谱。
38.图5 实施例3制剂0天的hplc图谱。
39.图6 实施例3制剂在40
°
c/75%rt保存3个月的hplc图谱。
40.图7 实施例4制剂0天的hplc图谱。
41.图8 实施例4制剂在40
°
c/75%rt保存3个月的hplc图谱。
42.图9 实施例5制剂0天的hplc图谱。
43.图10 实施例5制剂在40
°
c/75%rt保存3个月的hplc图谱。
具体实施方式
44.为使本发明实施例的目的、技术方案和优点更加清楚,下面将对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例是本发明一个模块实施例,而不
是全部的实施例。在本发明的一种实施方式中描述的元素和特征可以与一个或更多个其它实施方式中示出的元素和特征相结合。应当注意,为了清楚的目的,说明中省略了与本发明无关的、本领域普通技术人员已知的部件和处理的表示和描述。基于本发明中的实施例,本领域普通技术人员在没有付出创造性劳动的前提下所获得的所有其他实施例,都属于本发明保护的范围。
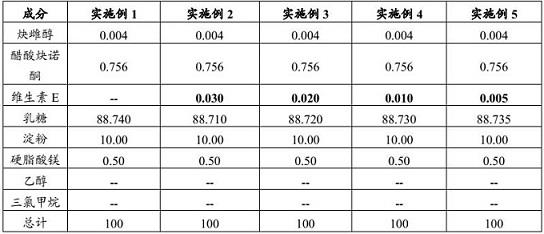
45.实施例1-5采用流化床湿法制粒压片技术制备炔雌醇和醋酸炔诺酮的复方片剂,工艺步骤如下:称量:按表1处方称取各成分。
46.主药溶液配制:将炔雌醇、醋酸炔诺酮、维生素e溶解于乙醇和三氯甲烷1:1(v/v)的混合溶剂;过筛:将乳糖、淀粉过孔径为20目的筛网;制粒及干燥:将过筛后物料放入流化床制粒锅中,在流化状态下喷入主药溶液,然后在40℃条件下流化烘干;过筛:将烘干后物料过孔径为20目的筛网;总混、压片:向过筛后的颗粒中加入处方量的硬脂酸镁混合均匀后压制成5mm圆形片。
47.表1实施例1-5片剂处方实施例6有关物质的测定将实施例1-5制备的片剂在40
°
c/75%rh条件下保存3个月,包装条件为热封的高密度聚乙烯瓶,使用高效液相色谱法分别测定0天和3个月样品中有关物质的量,测定结果参见表3。
48.hplc色谱条件为:用辛烷基键合硅胶为填充剂;以含0.5%磷酸的乙腈为流动相a,含0.5%磷酸的乙腈:水=1:3为流动相b,按表2进行线性梯度洗脱;流速为每分钟1.6ml;fldex285nm,em350nm(6α-羟基炔雌醇,6β-羟基炔雌醇和δ9,11-炔雌醇),uv210nm(其他杂质);柱温:40
º
c;进样体积:30
µ
l。
49.表2梯度洗脱参数设定
表3 实施例1-5有关物质的测定结果实施例1结果表明,组合物中不加维生素e时,炔雌醇的有关物质在加速条件下将显著性增长,其中6β-羟基炔雌醇和δ9,11-炔雌醇3个月后已接近或超过ich规定的不得过1.0%限度。
50.实施例2结果表明,当组合物中加入0.03%的维生素e时,在加速条件下炔雌醇的有关物质得到了较好的控制。但是出现两个未知杂质(相对于炔雌醇保留时间:1.41
±
0.02和2.21
±
0.02),两种未知杂质在3个月加速条件下杂质的量达到0.66%和1.05%,已超可接受
限度(《0.5%);并且复方制剂的杂质总量也显著增加,达到3.2%。
51.实施例3和4的结果表明,组合物中加入0.01%和0.02%的维生素e时,在加速条件下不仅炔雌醇有关物质得到了较好的控制,未知杂质(相对于炔雌醇保留时间:1.41
±
0.02和2.21
±
0.02)可以控制在限度以下(《0.5%),并且复方制剂的杂质总量也维持在1.7%或1.2%的更低的水平。
52.实施例5的结果表明,即使组合物中加入0.005%的维生素e时,在加速条件下炔雌醇有关物质还是得到了较好的控制,未知杂质(相对于炔雌醇保留时间:1.41
±
0.02和2.21
±
0.02)也可以控制在限度以下(《0.5%),并且复方制剂的杂质总量仍维持在1.2%的低水平。
53.上述结果表明,在炔雌醇和醋酸炔诺酮的复方制剂中抗氧化剂维生素e的用量与稳定性的提高并非线性正比关系。当抗氧化剂维生素e用量大于0.03%时,复方制剂中的有关物质总杂增加,稳定性降低。当抗氧化剂维生素e用量控制在0.005-0.02%范围时,复方制剂的总杂和特定单杂维持在可控的理想水平内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。