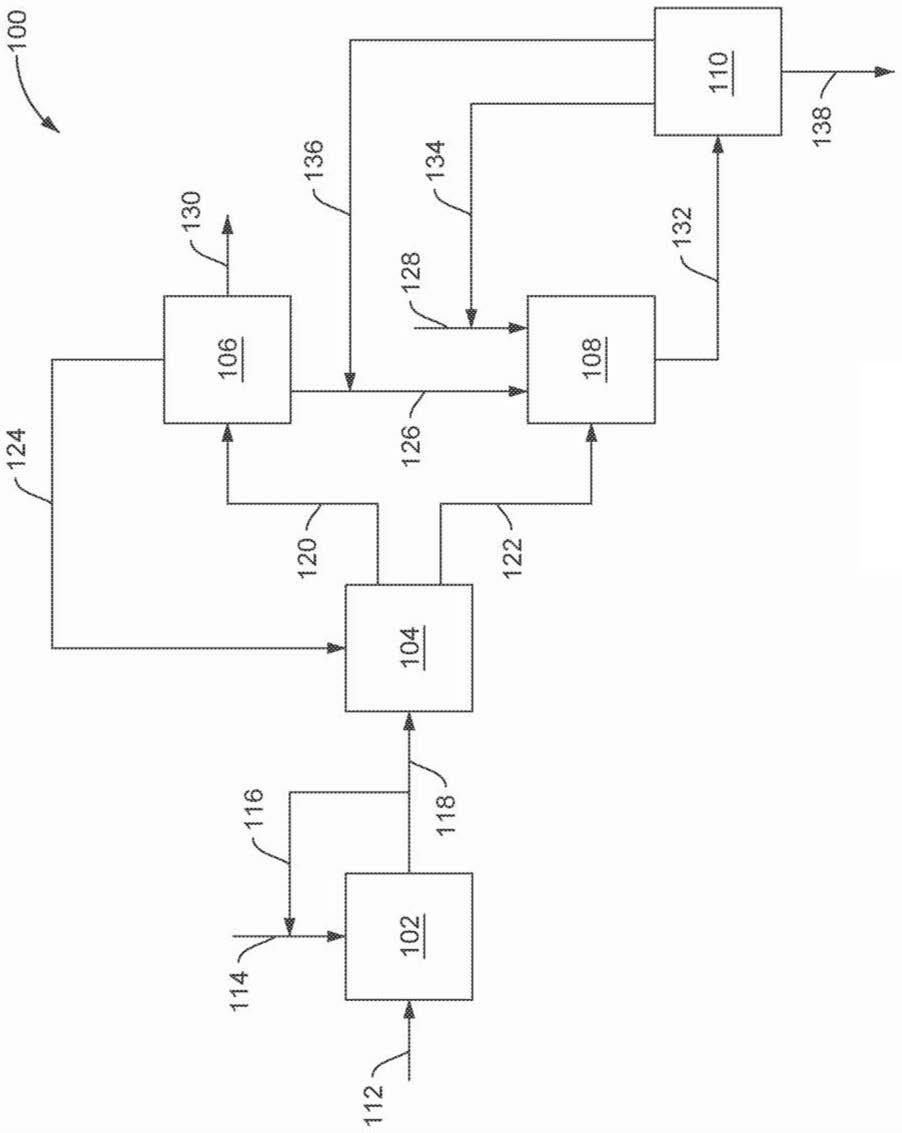
制备邻位金属化金属化合物的方法
1.本发明涉及一种由简单的铱反应物制备环金属化铱化合物的方法。
2.有机金属铱化合物在可广泛地归属于电子工业的许多不同应用中用作功能材料,尤其是作为有机电致发光器件中的磷光发光体。这需要有效合成获得相应的高纯度铱化合物。考虑到ir的稀缺性,这对于此类化合物的资源节约利用至关重要。
3.用于制备环金属化有机铱化合物的各种方法是已知的。其中的共同因素是它们在有机溶剂或有机溶剂与水的混合物中,常常在高温下进行,并且反应时间长。当使用含氯的铱反应物时,这里常常使用银盐来消除氯化物,但这导致铱络合物的纯化问题。因此,不希望使用银盐。
4.例如,已知的方法在具有高熔点质子化合物例如氢醌、苯酚、萘酚、间苯二酚、儿茶酚、聚乙二醇及其混合物的熔体中进行。已发现这些化合物是良好的反应介质,尤其是对于与多足配体(例如根据wo2016/124304)或者相应的双核络合物(例如根据wo 2018/041769)的环金属化反应。在熔体中高于240℃的邻位金属化反应快速、选择性地进行并且没有明显的副反应。由于反应产物不溶于水溶性和醇溶性反应介质,因此这些介质的去除效果优异。因此,在实验室操作中,反应可以以非常好的时空产率进行。相比之下,发现技术上很难在生产规模上对在分批反应器操作中的该方法升级,因为在技术上很难快速加热相对较大的体积并且不会过热至》240℃的所需温度,或者在反应后将其再次冷却。此外,已发现反应混合物在冷却时固化是不利的,这导致搅拌和后处理的问题。另一个因素是这种高温过程中的特定安全要求使得实践中对工厂和建筑基础设施的要求非常高,例如由于大的防爆区(爆炸危险区)而要求单独的建筑物。此外,在方法升级过程中,在一些情况下观察到自燃铱的形成,这会导致粗产品在空气中吸干时自燃,从而构成相当大的安全风险。因此,这里仍然需要改进。
5.因此,本发明的根本问题在于提供一种广泛适用的方法,所述方法可以在温和的条件和良好的产率下,从易得的铱反应物(例如卤化铱(iii)水合物或乙酸铱(iii))中以简单的方式和高产率合成环金属化铱络合物,尤其是多足环金属化铱络合物,以及相应的多核络合物。具体问题是提供一种广泛适用的多足环金属化络合物和相应的多核络合物的合成方法,其中应避免添加银盐。此外,在所述方法中不会形成自燃副产物。此外,反应物和反应介质应无毒且具有良好的商业可用性。本发明解决的另一个问题是提供一种不仅可以从卤化铱而且可以从无卤素、尤其是无氯的反应物进行的方法,因为在这种情况下反应也可以在不锈钢反应器中进行,而在使用含氯反应物的情况下,反应应在惰性反应器例如玻璃或搪瓷反应器中进行。
6.令人惊讶地发现,由各种铱(iii)或铱(i)反应物,例如卤化铱、乙酸铱或其它铱反应物开始的环金属化铱络合物的合成,可以在无水有机羧酸中以高产率和纯度进行。这里的反应在相对温和的条件下,即在温度《190℃和低压下进行。
7.因此,本发明提供了一种制备环金属化铱络合物的方法,所述方法通过使铱化合物与一种或多种在环金属化下与铱配位的配体反应来制备,其特征在于所述方法在羧酸存在下在无水介质中进行。
8.本发明上下文中的环金属化铱络合物是具有至少一个双齿环金属化配体或亚配体的铱络合物。这里的铱络合物可以是单核的或多核的,例如双核或三核的。其优选为具有三个双齿环金属化配体或亚配体的三环金属化铱络合物。在本发明的上下文中,术语“环金属化铱络合物”还包括其中三个双齿配体(其中至少一个是环金属化的)经由桥彼此共价键合以形成任一种三足六齿配体的铱络合物。多核络合物也是如此。在本发明的上下文中,环金属化配体是与其配位的金属形成金属环的配体,在配体和金属之间存在至少一个金属-碳键。
9.取决于配体,可以合成均配或杂配金属络合物。均配络合物应理解为是指其中只有相同的配体与金属键合的化合物。杂配络合物是不同配体与金属键合的络合物。这既涉及具有不同配体基础结构的配体,也涉及具有相同基础结构但被不同取代的配体。
10.在本发明的一个优选的实施方式中,当三个双齿配体不经由桥共价连接形成六齿三足配体时,环金属化铱络合物是均配络合物。当三个双齿配体经由桥共价键合形成六齿三足配体时,同样优选其中三足配体的各个双齿亚配体是彼此不同的络合物。
11.在本发明的另一个优选的实施方式中,环金属化铱络合物是络合物的面式异构体。本技术上下文中的面式或经式配位描述了具有六个供体原子的铱的八面体环境。当三个相同的供体原子占据(伪)八面体配位多面体中的三角形表面并且除第一供体原子以外的三个相同的供体原子占据(伪)八面体配位多面体中的另一个三角形表面时,配位是面式的。在经式配位的情况下,三个相同的供体原子占据(伪)八面体配位多面体中的一个经线,并且除第一供体原子以外的三个相同的供体原子占据(伪)八面体配位多面体中的另一个经线。下面以三个供体氮原子和三个供体碳原子的配位为例(方案1)显示了这一点。由于该定义是指供体原子而不是提供这些供体原子的双齿配体,因此三个双齿环金属化配体可以相同或不同,但在本技术的上下文中仍然符合面式或经式配位。相同的供体原子被理解为是指由相同元素(例如碳或氮)组成的那些,无论这些元素是否并入到不同的结构中。
[0012][0013]
可通过本发明的方法获得的铱络合物优选具有下式(1)、(2)或(3)的结构:
[0014][0015]
其中:
[0016]
l在每种情况下相同或不同并且在式(2)中是双齿环金属化配体或在式(1)和(3)
中是双齿环金属化亚配体;
[0017]
l'在每种情况下相同或不同并且在式(2)中是双齿配体或在式(1)和(3)中是双齿亚配体;
[0018]
l”是与两个铱原子配位的双(双齿)环金属化亚配体;
[0019]
v在每种情况下相同或不同并且是桥接单元,其在式(1)中将亚配体l和l'相互连接以形成三足六齿配体,并且在式(3)中将亚配体l'和l”相互连接以总体形成十二齿配体。
[0020]
本发明方法中使用的配体,对于式(1)的络合物,对应于式(4)的化合物,
[0021][0022]
其中符号具有上文给出的定义并且亚配体l具有碳-氢键而不是碳-铱键,并且亚配体l'具有氢原子而不是与铱连接的键。
[0023]
本发明方法中使用的配体,对于式(2)的络合物,对应于l和l',其中配体l具有碳-氢键而不是碳-铱键,并且配体l'具有氢原子而不是与铱连接的键。
[0024]
本发明方法中使用的配体,对于式(3)的络合物,对应于式(5)的化合物,
[0025][0026]
其中符号具有上文给出的定义并且亚配体l”具有碳-氢键而不是碳-铱键,并且亚配体l'具有氢原子而不是与铱连接的键。
[0027]
这里的双齿配体或亚配体l'可以是环金属化的或非环金属化的,并且当l'是环金属化配体时,式(1)和(2)中的l和l'也可以相同。
[0028]
在本发明的一个优选的实施方式中,l和l'是单阴离子配体,并且l”是双阴离子配体。
[0029]
式(1)络合物中的式(4)配体是具有可相同或不同的三个双齿亚配体l和l'的六齿三足配体。“双齿”是指络合物中的特定亚配体经由两个配位位点与铱配位或结合。“三足”是指配体具有三个与桥v键合的亚配体。由于配体具有三个双齿亚配体,因此总体结果是六齿配体,即经由六个配位位点与铱配位或结合的配体。在本技术上下文中的表述“双齿亚配体”是指如果不存在桥v,则l和l'将各自是双齿配体。然而,由于在形式上从该双齿配体中提取氢原子并连接到桥v,它不再是一个单独的配体,而是由此产生的六齿配体的一部分,因此对此使用术语“亚配体”。
[0030]
式(3)络合物中的式(5)配体是与两个铱原子配位的十二齿双(三足)配体。这里的配体含有两个双齿亚配体l',其各自与两部分中的每一者中的两个铱原子之一配位,并含有与两个铱原子配位的双(双齿)亚配体l”。
[0031]
在本发明的一个优选的实施方式中,配体l'是双齿环金属化配体或亚配体。因此,可通过本发明的方法获得的金属络合物优选具有下式(1a)、(2a)或(3a)的结构:
[0032][0033]
其中使用的符号具有上文给出的定义。
[0034]
以下是对双齿环金属化配体或亚配体l的描述。当l'是双齿环金属化配体或亚配体时,随后的优选特征也适用于l'。配体或亚配体l经由一个碳原子和一个氮原子或经由两个碳原子与铱配位。当l经由两个碳原子与铱配位时,两个碳原子之一是卡宾(carbene)碳原子。在本发明的一个优选的实施方式中,至少两个配体或亚配体l和l'是相同的。在式(2)的络合物中,优选所有配体l和l'都是相同的,因此络合物是均配络合物。
[0035]
更优选地,每个配体或亚配体l和l'具有一个碳原子和一个氮原子作为配位原子。
[0036]
进一步优选的是,由铱和配体或亚配体l或l'形成的金属环是五元环。这在下文中示意性地示出:
[0037][0038]
其中n代表配位氮原子并且c代表配位碳原子,并且所示的碳原子代表配体或亚配体l或l'的原子。
[0039]
在本发明的一个优选的实施方式中,配体或亚配体l,和如果适当,l'在每种情况下相同或不同,并且是下式(l-1)和(l-2)的结构:
[0040][0041]
其中虚线键在式(1)或(3)中代表亚配体与桥v的键,而对于式(2)是不存在的,并且其中使用的其它符号如下:
[0042]
cyc在每种情况下相同或不同并且是取代或未取代的具有5至14个芳族环原子的芳基或杂芳基基团,并且cyc在每种情况下经由碳原子与金属配位并且经由共价键与cyd键合;
[0043]
cyd在每种情况下相同或不同并且是取代或未取代的具有5至14个芳族环原子的杂芳基基团,并且cyd经由氮原子或经由卡宾碳原子与金属配位并且经由共价键与cyc键合;
[0044]
同时,两个或更多个任选的取代基一起可以形成环系;所述任选的基团优选地选自下文定义的r基团。
[0045]
cyd经由不带电荷的氮原子或经由卡宾碳原子配位,并且cyc经由阴离子碳原子配
位。
[0046]
对于cyc和cyd上的r基团,优选的情况是:
[0047]
r在每种情况下相同或不同并且是h,d,f,cl,br,i,n(r1)2,or1,sr1,cn,no2,coor1,c(=o)n(r1)2,si(r1)3,b(or1)2,c(=o)r1,p(=o)(r1)2,s(=o)r1,s(=o)2r1,oso2r1,具有1至20个碳原子的直链烷基基团,或具有2至20个碳原子的烯基或炔基基团,或具有3至20个碳原子的支链或环状的烷基基团,其中所述烷基、烯基或炔基基团在每种情况下可以被一个或多个r1基团取代并且其中一个或多个非相邻的ch2基团可以被si(r1)2、c=o、nr1、o、s或conr1代替,或具有5至40个芳族环原子并且在每种情况下可以被一个或多个r1基团取代的芳族或杂芳族环系;同时,两个r基团一起也可以形成环系;
[0048]
r1在每种情况下相同或不同并且是h,d,f,cl,br,i,n(r2)2,or2,sr2,cn,no2,si(r2)3,b(or2)2,c(=o)r2,p(=o)(r2)2,s(=o)r2,s(=o)2r2,oso2r2,具有1至20个碳原子的直链烷基基团,或具有2至20个碳原子的烯基或炔基基团,或具有3至20个碳原子的支链或环状的烷基基团,其中所述烷基、烯基或炔基基团在每种情况下可以被一个或多个r2基团取代并且其中一个或多个非相邻的ch2基团可以被si(r2)2、c=o、nr2、o、s或conr2代替,或具有5至40个芳族环原子并且在每种情况下可以被一个或多个r2基团取代的芳族或杂芳族环系;同时,两个或更多个r1基团一起可以形成环系;
[0049]
r2在每种情况下相同或不同并且是h,d,f或具有1至20个碳原子的脂族有机基团,尤其是烃基基团,其中一个或多个氢原子也可以被f代替。
[0050]
当两个r或r1基团一起形成环系时,它可以是单环或多环的脂族、杂脂族、芳族或杂芳族的。在这种情况下,一起形成环系的这些基团可以是相邻的,意味着这些基团键合至同一碳原子或键合至相互直接键合的碳原子,或者它们可以进一步彼此远离。此外,cyc和cyd上的取代基也可以一起形成环,因此cyc和cyd也可以一起形成单个稠合芳基或杂芳基基团作为双齿配体。
[0051]
在本说明书的上下文中,两个或更多个基团一起可以形成环的措辞应当被理解为尤其是指,两个基团通过化学键相互连接,形式上消除两个氢原子。这由以下方案说明:
[0052][0053]
此外,上述措辞也应理解为是指,如果两个基团之一是氢,则第二个基团与氢原子键合的位置结合,从而形成环。这将通过以下方案来说明:
[0054][0055]
此外,上述措辞也应理解为是指,如果两个基团是烯基基团,则所述基团一起形成环,从而形成稠合的芳基基团。类似地,在芳氧基取代基的情况下可以形成稠合的苯并呋喃基团,并且在芳氨基取代基的情况下可以形成稠合的吲哚基团。这将通过以下方案来说明:
[0056][0057]
在本发明的上下文中,术语“烷基基团”用作直链或支链的烷基基团和环状的烷基基团的概括性术语。类似地,术语“烯基基团”和“炔基基团”用作直链或支链的烯基或炔基基团和环状的炔基基团的概括性术语。
[0058]
在本发明上下文中的环状的烷基、烷氧基或硫代烷氧基基团应理解为是指单环、双环或多环基团。
[0059]
在本发明的上下文中,其中个别氢原子或ch2基团还可以被上述基团取代的c1至c
20
烷基基团应理解为是指例如甲基、乙基、正丙基、异丙基、环丙基、正丁基、异丁基、仲丁基、叔丁基、环丁基、2-甲基丁基、正戊基、仲戊基、叔戊基、2-戊基、新戊基、环戊基、正己基、仲己基、叔己基、2-己基、3-己基、新己基、环己基、1-甲基环戊基、2-甲基戊基、正庚基、2-庚基、3-庚基、4-庚基、环庚基、1-甲基环己基、正辛基、2-乙基己基、环辛基、1-双环[2.2.2]辛基、2-双环[2.2.2]辛基、2-(2,6-二甲基)辛基、3-(3,7-二甲基)辛基、金刚烷基、三氟甲基、五氟乙基、2,2,2-三氟乙基、1,1-二甲基-正己-1-基、1,1-二甲基-正庚-1-基、1,1-二甲基-正辛-1-基、1,1-二甲基-正癸-1-基、1,1-二甲基-正十二烷-1-基、1,1-二甲基-正十四烷-1-基、1,1-二甲基-正十六烷-1-基、1,1-二甲基-正十八烷-1-基、1,1-二乙基-正己-1-基、1,1-二乙基-正庚-1-基、1,1-二乙基-正辛-1-基、1,1-二乙基-正癸-1-基、1,1-二乙基-正十二烷-1-基、1,1-二乙基-正十四烷-1-基、1,1-二乙基-正十六烷-1-基、1,1-二乙基-正十八烷-1-基、1-(正丙基)环己-1-基、1-(正丁基)环己-1-基、1-(正己基)环己-1-基、1-(正辛基)环己-1-基和1-(正癸基)环己-1-基基团。烯基基团应理解为是指例如乙烯基、丙烯基、丁烯基、戊烯基、环戊烯基、己烯基、环己烯基、庚烯基、环庚烯基、辛烯基、环辛烯基或环辛二烯基。炔基基团应理解为是指例如乙炔基、丙炔基、丁炔基、戊炔基、己炔基、庚炔基或辛炔基。or1基团应理解为是指例如甲氧基、三氟甲氧基、乙氧基、正丙氧基、异丙氧基、正丁氧基、异丁氧基、仲丁氧基、叔丁氧基或2-甲基丁氧基。
[0060]
在本发明上下文中的芳基基团含有6至30个碳原子;在本发明上下文中的杂芳基基团含有2至30个碳原子和至少一个杂原子,条件是碳原子和杂原子的总和为至少5个。所述杂原子优选地选自n、o和/或s。这里,芳基基团或杂芳基基团应理解为是指简单的芳族环,即苯,或简单的杂芳族环,例如吡啶、嘧啶、噻吩等,或缩合的(稠合的)芳基或杂芳基基团,例如萘、蒽、菲、喹啉、异喹啉等。相比之下,通过单键相互连接的芳族体系例如联苯不被称为芳基或杂芳基基团,而是被称为芳族环系。
[0061]
在本发明上下文中的芳族环系在环系中含有6至40个碳原子,优选6至30个碳原子。在本发明上下文中的杂芳族环系在环系中含有2至40个碳原子,优选2至30个碳原子和
至少一个杂原子,条件是碳原子和杂原子的总和为至少5个。所述杂原子优选地选自n、o和/或s。在本发明上下文中的芳族或杂芳族环系应被理解为是指以下体系:不必仅含有芳基或杂芳基基团,而是其中两个或更多个芳基或杂芳基基团还可通过非芳族单元例如碳、氮或氧原子连接。这些同样应理解为是指其中两个或更多个芳基或杂芳基基团直接相互连接的体系,例如联苯、三联苯、联吡啶或苯基吡啶。例如,诸如芴、9,9'-螺二芴、9,9-二芳基芴、三芳基胺、二芳基醚、茋等的体系还应被视为在本发明上下文中的芳族环系,以及其中两个或更多个芳基基团例如通过短的烷基基团连接的体系同样如此。优选的芳族或杂芳族环系是简单的芳基或杂芳基基团以及其中两个或更多个芳基或杂芳基基团直接相互连接的基团,例如联苯或联吡啶,以及芴或螺二芴。
[0062]
具有5-40个芳族环原子并且在每种情况下还可以被上述r2基团或烃基基团取代并且可经由任何希望的位置与所述芳族或杂芳族体系连接的芳族或杂芳族环系,应理解为尤其是指衍生自如下物质的基团:苯、萘、蒽、苯并蒽、菲、芘、苣、苝、荧蒽、并四苯、并五苯、苯并芘、联苯、联二苯叉、三联苯、联三苯叉、芴、螺二芴、二氢菲、二氢芘、四氢芘、顺式或反式茚并芴、顺式或反式茚并咔唑、顺式或反式吲哚并咔唑、三聚茚、异三聚茚、螺三聚茚、螺异三聚茚、呋喃、苯并呋喃、异苯并呋喃、二苯并呋喃、噻吩、苯并噻吩、异苯并噻吩、二苯并噻吩、吡咯、吲哚、异吲哚、咔唑、吡啶、喹啉、异喹啉、吖啶、菲啶、苯并-5,6-喹啉、苯并-6,7-喹啉、苯并-7,8-喹啉、吩噻嗪、吩嗪、吡唑、吲唑、咪唑、苯并咪唑、萘并咪唑、菲并咪唑、吡啶并咪唑、吡嗪并咪唑、喹喔啉并咪唑、唑、苯并唑、萘并唑、蒽并唑、菲并唑、异唑、1,2-噻唑、1,3-噻唑、苯并噻唑、哒嗪、六氮杂苯并菲、苯并哒嗪、嘧啶、苯并嘧啶、喹喔啉、1,5-二氮杂蒽、2,7-二氮杂芘、2,3-二氮杂芘、1,6-二氮杂芘、1,8-二氮杂芘、4,5-二氮杂芘、4,5,9,10-四氮杂苝、吡嗪、吩嗪、吩嗪、吩噻嗪、荧红环、萘啶、氮杂咔唑、苯并咔啉、菲咯啉、1,2,3-三唑、1,2,4-三唑、苯并三唑、1,2,3-二唑、1,2,4-二唑、1,2,5-二唑、1,3,4-二唑、1,2,3-噻二唑、1,2,4-噻二唑、1,2,5-噻二唑、1,3,4-噻二唑、1,3,5-三嗪、1,2,4-三嗪、1,2,3-三嗪、四唑、1,2,4,5-四嗪、1,2,3,4-四嗪、1,2,3,5-四嗪、嘌呤、蝶啶、吲哚嗪和苯并噻二唑,或衍生自这些体系的组合的基团。
[0063]
优选地,所有配体或亚配体l,以及如果适当,l'具有式(l-1)的结构,或者所有配体或亚配体l,以及如果适当,l'具有式(l-2)的结构。
[0064]
在本发明的一个优选的实施方式中,cyc是具有6至13个芳族环原子,更优选具有6至10个芳族环原子,最优选具有6个芳族环原子的芳基或杂芳基基团,所述基团经由碳原子与金属配位,其可以被一个或多个r基团取代并且所述基团经由共价键与cyd键合。
[0065]
cyc基团的优选实施方式是下式(cyc-1)至(cyc-20)的结构,其中cyc基团在每种情况下在由#表示的位置与cyd结合并在由*表示的位置与铱配位,
[0066][0067]
其中r如上文所定义,并且此外:
[0068]
x在每种情况下相同或不同并且是cr或n,条件是每个环不超过两个符号x是n;
[0069]
w在每种情况下相同或不同并且是nr、o、s或br;
[0070]
条件是,当在式(1)或(3)中桥v与cyc键合时,一个符号x是c并且所述桥v与该碳原子键合。当cyc基团与桥v键合时,所述键优选经由上述式中标记为“o”的位置,因此在这种情况下标记为“o”的符号x优选为c。不含任何标记为“o”的符号x的上述结构优选不直接键合至桥v,因为这样键合至桥出于空间原因是不利的。
[0071]
优选地,cyc中不超过一个符号x是n,并且更优选地所有符号x都是cr,条件是,当
在式(1)中桥v与cyc键合时,一个符号x是c并且所述桥v与该碳原子键合。
[0072]
优选的cyc基团是下式(cyc-1a)至(cyc-20a)的基团:
[0073]
[0074]
[0075][0076]
其中使用的符号具有上文给出的定义,并且在式(1)或(3)中当桥v与cyc键合时,不存在一个r基团并且桥v与相应的碳原子键合。当cyc基团与桥v键合时,所述键优选经由上述式中标记为“o”的位置,因此在这种情况下该位置的r基团优选不存在。不含任何标记为“o”的碳原子的上述结构优选不直接与桥v键合。
[0077]
(cyc-1)至(cyc-19)基团中的优选基团是(cyc-1)、(cyc-3)、(cyc-8)、(cyc-10)、(cyc-12)、(cyc-13)和(cyc-16)基团,并且特别优选(cyc-1a)、(cyc-3a)、(cyc-8a)、(cyc-10a)、(cyc-12a)、(cyc-13a)和(cyc-16a)基团。
[0078]
在本发明的另一个优选的实施方式中,cyd是具有5至13个芳族环原子,更优选具有6至10个芳族环原子的杂芳基基团,所述基团经由不带电荷的氮原子或经由卡宾碳原子与金属配位并且其可以被一个或多个r基团取代并且所述基团经由共价键与cyc键合。
[0079]
cyd基团的优选实施方式是下式(cyd-1)至(cyd-12)的结构,其中cyd基团在每种情况下在由#表示的位置与cyc结合并在由*表示的位置与铱配位,
[0080][0081][0082]
其中x、w和r具有上文给出的定义,条件是,当式(1)或(3)中的桥v与cyd键合时,一个符号x是c并且所述桥v与该碳原子键合。当cyd基团与桥v键合时,所述键优选经由上述式中标记为“o”的位置,因此在这种情况下标记为“o”的符号x优选是c。不含任何标记为“o”的符号x的上述结构优选不直接键合至桥v,因为这样键合至桥出于空间原因是不利的。
[0083]
在这种情况下,(cyd-1)至(cyd-4)和(cyd-7)至(cyd-12)基团经由不带电荷的氮
原子与铱配位,并且(cyd-5)和(cyd-6)基团经由卡宾碳原子与铱配位。
[0084]
优选地,cyd中不超过一个符号x是n,并且更优选地所有符号x都是cr,条件是,当在式(1)或(3)中桥v键合至cyd时,一个符号x是c并且所述桥v与该碳原子键合。
[0085]
特别优选的cyd基团是下式(cyd-1a)至(cyd-12b)的基团:
[0086][0087][0088]
其中使用的符号具有上文给出的定义,并且当在式(1)或(3)中桥v与cyd键合时,不存在一个r基团并且桥v与相应的碳原子键合。当cyd基团与桥v键合时,所述键优选经由上述式中标记为“o”的位置,因此在这种情况下该位置的r基团优选不存在。不含任何标记为“o”的碳原子的上述结构优选不直接与桥v键合。
[0089]
(cyd-1)至(cyd-12)基团中的优选基团是(cyd-1)、(cyd-2)、(cyd-3)、(cyd-4)、(cyd-5)和(cyd-6)基团,尤其是(cyd-1)、(cyd-2)和(cyd-3),并且特别优选(cyd-1a)、(cyd-2a)、(cyd-3a)、(cyd-4a)、(cyd-5a)和(cyd-6a)基团,尤其是(cyd-1a)、(cyd-2a)和(cyd-3a)。
[0090]
在本发明的一个优选的实施方式中,cyc是具有6至13个芳族环原子的芳基或杂芳基基团,并且同时cyd是具有5至13个芳族环原子的杂芳基基团。更优选地,cyc是具有6至10个芳族环原子的芳基或杂芳基基团,并且同时cyd是具有5至10个芳族环原子的杂芳基基团。最优选地,cyc是具有6个芳族环原子的芳基或杂芳基基团,并且cyd是具有6至10个芳族环原子的杂芳基基团。同时,cyc和cyd可以各自被一个或多个r基团取代。
[0091]
上述优选的基团(cyc-1)至(cyc-20)和(cyd-1)至(cyd-12)可以根据需要彼此组合。对于式(1)或(3)的化合物,在此必要的是,cyc或cyd基团中的至少一者具有与桥v的合适的键联位点,其中上述式中的合适的键联位点由“o”标识。
[0092]
尤其优选的是,上文提及为优选的cyc和cyd基团,即式(cyc-1a)至(cyc-20a)的基
团和式(cyd-1a)至(cyd-14b)的基团相互组合。
[0093]
非常特别优选的是,(cyc-1)、(cyc-3)、(cyc-8)、(cyc-10)、(cyc-12)、(cyc-13)和(cyc-16)基团之一,尤其是(cyc-1a)、(cyc-3a)、(cyc-8a)、(cyc-10a)、(cyc-12a)、(cyc-13a)和(cyc-16a)基团,与(cyd-1)、(cyd-2)和(cyd-3)基团之一组合,尤其是与(cyd-1a)、(cyd-2a)和(cyd-3a)基团之一组合。
[0094]
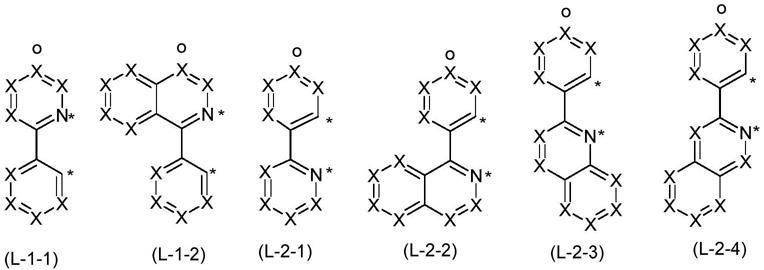
优选的亚配体(l-1)是式(l-1-1)和(l-1-2)的结构,并且优选的亚配体(l-2)是式(l-2-1)至(l-2-4)的结构:
[0095][0096]
其中使用的符号具有上文给出的定义,并且式(1)或(3)化合物中的“o”代表与桥v的键合位置,在这种情况下,相应的x是c。
[0097]
特别优选的亚配体(l-1)是式(l-1-1a)和(l-1-2b)的结构,并且特别优选的亚配体(l-2)是式(l-2-1a)至(l-2-4a)的结构
[0098][0099]
其中使用的符号具有上文给出的定义,并且式(1)或(3)中的“o”代表与桥v的键合位置,在这种情况下不存在相应的r基团。
[0100]
当两个r基团(其中一个与cyc键合并且另一个与cyd键合)一起形成环系时,这会导致桥接配体或亚配体l或l',在这种情况下,这些桥接亚配体中的一些总体形成单个较大的杂芳基基团,例如苯并[h]喹啉等。cyc和cyd上的取代基之间的环优选由下式(6)至(15)
之一的基团形成:
[0101][0102]
其中r1具有上文给出的定义,并且虚线键表示与cyc和cyd连接的键。上文提到的那些不对称基团在这里可以以两种方式中的任何一种结合。例如,在式(15)的基团的情况下,氧原子可以与cyc基团结合并且羰基基团与cyd基团结合,或者氧原子可以与cyd基团结合并且羰基基团与cyc基团结合。
[0103]
同时,当这导致环形成得到六元环时,特别优选式(12)的基团,如下文例如下式(l-21)和(l-22)所示。
[0104]
通过在不同环上的两个r基团之间形成环而产生的优选配体是如下所示的式(l-3)至(l-30)的结构:
[0105]
[0106][0107]
其中使用的符号具有上文给出的定义并且式(1)或(3)中的“o”表示亚配体与v基团连接的位置,并且相应的符号x则为c。
[0108]
在式(l-3)至(l-30)的配体或亚配体的一个优选的实施方式中,总共一个符号x是n并且其它符号x是cr,或者所有符号x都是cr。
[0109]
在本发明的另一个实施方式中,优选的是,在基团(cyc-1)至(cyc-20)或(cyd-1)至(cyd-14)中或者在配体或亚配体(l-1-1)至(l-30)中,当作为与该氮原子相邻的取代基键合的r基团不是氢或氘时,原子x之一是n。这类似地适用于优选的结构(cyc-1a)至(cyc-20a)或(cyd-1a)至(cyd-14b),其中与非配位氮原子相邻键合的取代基优选是不为氢或氘的r基团。在这种情况下,该取代基r优选是选自以下的基团:cf3,ocf3,具有1至10个碳原子的烷基基团,尤其是具有3至10个碳原子的支链或环状的烷基基团,or1,其中r1是具有1至10个碳原子的烷基基团,尤其是具有3至10个碳原子的支链或环状的烷基基团,具有2至10个
碳原子的二烷基氨基基团或具有5至10个芳族环原子的芳基或杂芳基基团。这些基团是空间要求高的基团。更优选地,该r基团还可以与相邻的r基团形成环。
[0110]
其它合适的双齿配体或亚配体是下式(l-31)或(l-32)的配体或亚配体:
[0111][0112]
其中r具有上文给出的定义,*代表与铱的配位位置,式(1)或(3)中的“o”代表亚配体与v的键联位置,并且使用的其它符号如下:
[0113]
x在每种情况下相同或不同并且是cr或n,条件是每个环不超过一个x符号是n。
[0114]
当配体或亚配体(l-31)和(l-32)中与相邻碳原子键合的两个r基团彼此形成芳族环时,该环与两个相邻碳原子一起优选为下式(16)的结构:
[0115][0116]
其中虚线键表示该基团在配体或亚配体内的键联,并且y在每种情况下相同或不同并且是cr1或n,并且优选不超过一个符号y是n。
[0117]
在配体或亚配体(l-31)或(l-32)的一个优选的实施方式中,存在不超过一个这样的稠合基团。所述配体或亚配体因此优选具有下式(l-33)至(l-38)的结构:
[0118][0119]
其中x在每种情况下相同或不同并且是cr或n,但r基团一起不形成芳族或杂芳族环系,并且其它符号具有上文给出的定义。
[0120]
在本发明的一个优选的实施方式中,在式(l-31)至(l-38)的配体或亚配体中,总共0、1或2个符号x和可能存在的y是n。更优选地,总共0或1个符号x和可能存在的y是n。
[0121]
式(l-33)至(l-38)的优选实施方式是下式(l-33a)至(l-38f)的结构:
[0122]
[0123]
[0124][0125]
其中使用的符号具有上文给出的定义,并且式(1)或(3)中的“o”表示与桥v的键联位置,在这种情况下不存在相应的r基团。
[0126]
在本发明的一个优选的实施方式中,与金属配位的邻位的x基团是cr。在与金属配位的邻位键合的r基团优选地选自h、d、f和甲基。
[0127]
在本发明的另一个实施方式中,当与该氮原子相邻键合的取代基是不为h或d的r基团时,优选原子x之一是n。在这种情况下,该取代基r优选是选自以下的基团:cf3,ocf3,具有1至10个碳原子的烷基基团,尤其是具有3至10个碳原子的支链或环状的烷基基团,or1,其中r1是具有1至10个碳原子的烷基基团,尤其是具有3至10个碳原子的支链或环状的烷基基团,具有2至10个碳原子的二烷基氨基基团,或具有5至10个芳族环原子的芳基或杂芳基基团。这些基团是空间要求高的基团。进一步优选地,该r基团还可以与相邻的r基团形成环。
[0128]
在本发明的一个优选的实施方式中,配体或亚配体l或l'中的恰好一个是下式(l-39)的配体或亚配体,其经由两个d基团与铱配位:
[0129][0130]
其中式(1)或(3)中的“o”表示与桥v的键合位置,在这种情况下相应的x是c;并且此外:
[0131]
d是c或n,条件是一个d是c并且另一个d是n;
[0132]
x在每种情况下相同或不同并且是cr或n;
[0133]
z是cr'、cr或n,条件是恰好一个z是cr'并且另一个z是cr或n;
[0134]
其中每个环总共最多一个符号x或z是n;
[0135]
r'是下式(17)或(18)的基团:
[0136][0137]
其中虚线键表示所述基团的连接;
[0138]
r”在每种情况下相同或不同并且是h,d,f,cn,具有1至10个碳原子的直链烷基基团,其中一个或多个氢原子也可以被d或f代替,或具有3至10个碳原子的支链或环状的烷基基团,其中一个或多个氢原子也可以被d或f代替,或具有2至10个碳原子的烯基基团,其中一个或多个氢原子也可以被d或f代替;同时,两个相邻r”基团或相邻苯基基团上的两个r”基团一起也可以形成环系;或者相邻苯基基团上的两个r”一起为选自c(r1)2、nr1、o和s的基团,使得两个苯环与桥接基团一起是咔唑、芴、二苯并呋喃或二苯并噻吩,并且其它r”如上文所定义;
[0139]
n是0、1、2、3、4或5。
[0140]
在相邻苯基基团上的两个取代基r”形成环的情况下,结果因此也可以是芴或菲或联三苯叉。同样可能的是,如上所述,相邻苯基基团上的两个r”一起是选自nr1、o和s的基团,使得两个苯环与桥接基团一起是咔唑、二苯并呋喃或二苯并噻吩。
[0141]
在本发明的一个优选的实施方式中,x在每种情况下相同或不同并且是cr。进一步优选地,一个z基团是cr并且另一个z基团是cr'。更优选地,在式(l-39)的配体或亚配体中,
x基团在每种情况下相同或不同并且是cr,并且同时一个z基团是cr而另一个z基团是cr'。配体或亚配体l或l'优选具有下式(l-39a)或(l-39b)之一的结构,其中式(l-39)的多足结构与桥v的键联是经由由“o”标识的位置并且没有r基团键合在该位置,
[0142][0143]
其中使用的符号具有上文给出的定义,并且当式(1)或(3)中的亚配体经由由“o”标识的位置与桥头v结合时,r基团不存在。
[0144]
更优选地,式(l-39)的亚配体l具有下式(l-39a')或(l-39b')之一的结构,其中式(l-39)的多足结构与桥v的键联是经由由“o”标识的位置并且没有r基团键合在该位置,
[0145][0146]
其中使用的符号具有上文给出的定义。
[0147]
式(l-39)或式(l-39a)、(l-39b)、(l-39a')和(l-39d')的亚配体l中的r基团优选地选自h,d,cn,or1,具有1至6个碳原子,优选具有1、2或3个碳原子的直链烷基基团,或具有3、4、5或6个碳原子的支链或环状的烷基基团,或具有2至6个碳原子,优选2、3或4个碳原子的烯基基团,所述基团中的每个可以被一个或多个r1基团取代,或者可以被一个或多个非芳族r1基团取代的苯基基团。两个或更多个相邻的r基团在这里也可以一起形成环系。
[0148]
在这种情况下,在邻位与配位原子键合的取代基r优选地选自h、d、f和甲基,更优选h、d和甲基并且尤其是h和d。
[0149]
此外,优选的是r'邻位的所有取代基r都是h或d。
[0150]
当式(l-39)的亚配体l中的r基团一起形成环系时,其优选为脂族、杂脂族或杂芳族环系。此外,优选在亚配体l或l'的两个环上的两个r基团之间形成环,优选形成菲啶,或者还可以含有更多氮原子的菲啶。当r基团一起形成杂芳族环系时,这优选形成选自喹啉、异喹啉、二苯并呋喃、二苯并噻吩和咔唑的结构,其中的每个都可以被一个或多个r1基团取代,并且其中二苯并呋喃、二苯并噻吩和咔唑中的个别碳原子也可以被n代替。特别优选喹啉、异喹啉、二苯并呋喃和氮杂二苯并呋喃。这里稠合结构可以在任何可能的位置键合。优选的具有稠合苯并基团的亚配体l或l'是下文列出的式(l-39c)至(l-39j)的结构,其中式(l-39)的多足结构与桥v的键联是经由由“o”标识的位置:
[0151][0152][0153]
其中所述配体各自还可以被一个或多个另外的r基团取代并且稠合结构可以被一个或多个r1基团取代。优选地,不存在另外的r或r1基团。
[0154]
优选的具有稠合苯并呋喃或氮杂苯并呋喃基团的式(l-39)的亚配体l或l'是下文列出的式(l-39k)至(l-39z)的结构,其中式(l-39)的多足结构与桥v的键联是经由由“o”标识的位置:
[0155]
[0156][0157]
其中所述配体各自还可以被一个或多个另外的r基团取代并且稠合结构可以被一个或多个r1基团取代。优选地,不存在另外的r或r1基团。同样这些结构中的o可以被s或nr1代替。
[0158]
如上所述,r'是式(17)或(18)的基团。这里两个基团的区别仅在于式(17)的基团与配体或亚配体l或l'在对位键合,而式(18)的基团与配体或亚配体l或l'在间位键合。
[0159]
在本发明的一个优选的实施方式中,n=0、1或2,优选为0或1并且最优选为0。
[0160]
在本发明的另一个优选的实施方式中,在邻位与碳原子键合(式(17)或(18)的基团由此与苯基吡啶配体键合)的两个取代基r”相同或不同并且是h或d。
[0161]
式(17)结构的优选实施方式是式(17a)至(17h)的结构,并且式(18)结构的优选实施方式是式(18a)至(18h)的结构:
[0162]
[0163][0164]
其中e是c(r1)2、nr1、o或s,并且使用的其它符号具有上文给出的定义。这里,当e=c(r1)2时,r1优选地在每种情况下相同或不同并且是具有1至6个碳原子、优选具有1至4个碳原子的烷基基团,更优选为甲基。此外,当e=nr1时,r1优选为具有5至30个芳族环原子,优选具有6至24个芳族环原子,更优选具有6至12个芳族环原子的芳族或杂芳族环系,尤其是苯基。
[0165]
式(17)或(18)或优选实施方式的基团上的优选取代基r”选自h、d、cn和具有1至4个碳原子的烷基基团,更优选h、d或甲基。
[0166]
亚配体l”是与两个铱原子配位的双(双齿)环金属化亚配体。在本发明的一个优选的实施方式中,该亚配体具有下式(19)或(20)的结构:
[0167][0168]
其中x具有上文给出的定义,虚线键表示与v连接的键,*表示与铱原子的配位,并且此外:
8)、(q-11)或(q-14)的基团,即经由碳原子与两个铱原子中的每一者配位,则两个d基团优选为氮原子。如果q基团代表式(q-3)、(q-6)、(q-9)、(q-12)或(q-15)的基团,即经由一个碳原子和一个氮原子与两个铱原子配位,则优选地两个d基团之一是氮原子并且另一个d基团是碳原子,使得每个铱原子由一个碳原子和一个氮原子配位。
[0177]
此外,在本发明的一个优选的实施方式中,式(19)或(20)中所示的符号x在每种情况下相同或不同并且是cr,尤其是ch或cd。
[0178]
如果l'是非环金属化配体或亚配体,则l'的优选实施方式是乙酰丙酮阴离子或其衍生物、吡啶甲酸或其衍生物、吡唑基硼酸阴离子或羟基喹啉或其衍生物。
[0179]
式(1)和(3)的络合物是具有六齿或十二齿配体的络合物,其中式(1)中的三个亚配体l和l'通过一个桥接单元v彼此共价键合,并且式(3)中的三个亚配体l'和l”通过两个桥接单元v彼此共价键合。
[0180]
在本发明的一个优选的实施方式中,桥接单元v是下式(21)的基团,其中虚线键在式(1)中代表亚配体l或l'的键联位置或者在式(3)中代表l'和l”的键联位置:
[0181][0182]
其中:
[0183]
x1在每种情况下相同或不同并且是cr或n;
[0184]
x2在每种情况下相同或不同并且是cr或n;
[0185]
a在每种情况下相同或不同并且是cr
2-cr2、cr
2-o、cr
2-nr、c(=o)-o、c(=o)-nr或下式(22)的基团:
[0186][0187]
其中在每种情况下的虚线键代表式(1)中的双齿亚配体l或l'或式(3)中的l'和l”与该结构的键合位置,*代表式(21)的单元与中心三价芳基或杂芳基基团的键联位置。
[0188]
当x2=cr时,式(22)的基团中的优选取代基选自上述取代基r。
[0189]
在本发明的一个优选的实施方式中,a在每种情况下相同或不同并且是cr
2-cr2或式(22)的基团。这里优选以下实施方式:
[0190]-所有三个a基团都是相同的式(22)的基团;
[0191]-两个a基团是相同的式(22)的基团,并且第三个a基团是cr
2-cr2;
[0192]-一个a基团是式(22)的基团,并且另外两个a基团是相同的cr
2-cr2基团;或者
[0193]-所有三个a基团都是相同的cr
2-cr2基团。
[0194]
这里“相同的式(22)的基团”是指这些基团都具有相同的基础骨架和相同的取代。此外,“相同的cr
2-cr2基团”是指这些基团都具有相同的取代。
[0195]
当a是cr
2-cr2时,r优选在每种情况下相同或不同并且是h或d,更优选h。
[0196]
式(22)的基团是芳族或杂芳族六元环。在本发明的一个优选的实施方式中,式(22)的基团在芳基或杂芳基基团中含有不超过一个杂原子。这并不意味着与该基团键合的任何取代基也不能含有杂原子。此外,该定义并不意味着通过取代基形成的环不会产生稠合的芳族或杂芳族结构,例如萘、苯并咪唑等。式(22)的基团优选地选自苯、吡啶、嘧啶、吡嗪和哒嗪,尤其是苯。
[0197]
式(22)的基团的优选实施方式是下式(22a)至(22h)的结构:
[0198][0199]
其中使用的符号具有上文给出的定义。
[0200]
特别优选式(22a)至(22e)的任选取代的六元芳族环和六元杂芳族环。非常特别优选邻苯亚基,即式(22a)的基团。
[0201]
同时,也如上文取代基描述中详述的,相邻的取代基也可以一起形成环系,使得可以形成稠合结构,包括稠合的芳基和杂芳基基团,例如萘、喹啉、苯并咪唑、咔唑、二苯并呋喃或二苯并噻吩。
[0202]
下文陈述的是桥头v的优选实施方式,即式(21)的结构。式(21)的基团的优选实施方式是下式(23)至(26)的结构:
[0203][0204]
其中使用的符号具有上文给出的定义。
[0205]
更优选地,式(23)至(26)的中心环中的所有取代基r均为h,因此所述结构优选地选自式(23a)至(26a)
[0206][0207]
其中使用的符号具有上文给出的定义。
[0208]
更优选地,式(23)至(26)的基团选自下式(23b)至(26b)的结构:
[0209][0210]
其中r在每种情况下相同或不同并且是h或d,优选h。
[0211]
合适的桥头v的其它实例是如下所示的结构:
[0212][0213]
[0214]
下面描述了可存在于上述亚配体l、l'和l”上,也可存在于式(21)结构中的二价芳亚基或杂芳亚基基团上,即在式(22)的结构中的优选取代基。
[0215]
在本发明的一个实施方式中,金属络合物含有两个r取代基或两个r1取代基,它们与相邻的碳原子键合并一起形成根据下文描述的式之一的脂族环。在这种情况下,形成该脂族环的两个r取代基可以存在于式(21)的桥上和/或一个或多个双齿亚配体或配体上。由两个r取代基一起成环而形成的脂族环优选由下式(27)至(33)之一描述:
[0216][0217]
其中r1和r2具有上文给出的定义,虚线键表示配体中两个碳原子的连接,并且此外:
[0218]
g是具有1、2或3个碳原子并且可以被一个或多个r2基团取代的烷亚基基团,-cr2=cr
2-或具有5或6个芳族环原子并且可以被一个或多个r2基团取代的邻位键合的芳亚基或杂芳亚基基团;
[0219]
r3在每种情况下相同或不同并且是h,f,or2,具有1至10个碳原子的直链烷基基团,具有3至10个碳原子的支链或环状的烷基基团,其中所述烷基基团在每种情况下可以被一个或多个r2基团取代,其中一个或多个非相邻的ch2基团可以被r2c=cr2、c≡c、si(r2)2、c=o、nr2、o、s或conr2代替,或具有5或6个芳族环原子并且在每种情况下可以被一个或多个r2基团取代的芳基或杂芳基基团;同时,与同一碳原子键合的两个r3基团可以一起形成脂族环系,并因此形成螺环系;此外,r3与相邻的r或r1基团可以形成脂族环系。
[0220]
在上述式(27)至(33)的结构中,在两个碳原子之间在形式意义上描绘了双键。当这两个碳原子结合到芳族或杂芳族体系中并且因此这两个碳原子之间的键在形式上介于单键键合水平与双键键合水平之间时,这是化学结构的简化。
[0221]
式(27)至(33)的基团的优选实施方式可以见于专利申请wo2014/023377、wo 2015/104045和wo 2015/117718中。
[0222]
当r基团键合在双齿配体或亚配体l、l'或l”内或键合在式(21)或优选实施方式内键合的式(22)的二价芳亚基或杂芳亚基基团内时,这些r基团在每种情况下相同或不同,并且优选地选自h,d,f,br,i,n(r1)2,cn,si(r1)3,b(or1)2,c(=o)r1,具有1至10个碳原子的直链烷基基团,或具有2至10个碳原子的烯基基团,或具有3至10个碳原子的支链或环状的烷基基团,其中所述烷基或烯基基团在每种情况下可以被一个或多个r1基团取代,或具有6至24个芳族环原子并且在每种情况下可以被一个或多个r1基团取代的芳族或杂芳族环系;同时,两个相邻的r基团一起或者r与r1一起也可以形成单环或多环的脂族或芳族环系。更优
选地,这些r基团在每种情况下相同或不同并且选自h,d,f,n(r1)2,具有1至6个碳原子的直链烷基基团或具有3至10个碳原子的支链或环状的烷基基团,其中一个或多个氢原子可以被d或f代替,或具有6至18个芳族环原子、尤其是6至13个芳族环原子并且可以被一个或多个r1基团取代的芳族或杂芳族环系;同时,两个相邻的r基团一起或者r与r1一起也可以形成单环或多环的脂族或芳族环系。
[0223]
优选的r1基团在每种情况下相同或不同并且是h,d,f,n(r2)2,cn,具有1至10个碳原子的直链烷基基团,或具有2至10个碳原子的烯基基团,或具有3至10个碳原子的支链或环状的烷基基团,其中所述烷基基团在每种情况下可以被一个或多个r2基团取代,或具有6至24个芳族环原子并且可以被一个或多个r2基团取代的芳族或杂芳族环系;同时,两个或更多个相邻的r1基团一起可以形成单环或多环的脂族环系。特别优选的与r键合的r1基团在每种情况下相同或不同并且是h、f、cn、具有1至5个碳原子的直链烷基基团或具有3至5个碳原子的支链或环状的烷基基团,所述基团中的每个可以被一个或多个r2基团取代,或具有6至18个芳族环原子、尤其是6至13个芳族环原子并且可以被一个或多个r2基团取代的芳族或杂芳族环系;同时,两个或更多个相邻的r1基团一起可以形成单环或多环的脂族环系。
[0224]
优选的r2基团在每种情况下相同或不同并且是h、f或具有1至5个碳原子的脂族烃基基团或具有6至12个碳原子的芳族烃基基团;同时,两个或更多个r2取代基一起也可以形成单环或多环的脂族环系。
[0225]
上述优选实施方式可以根据需要相互组合。在本发明的一个特别优选的实施方式中,上述优选实施方式同时适用。
[0226]
一般来说,通过本发明的方法,可获得如根据现有技术在有机电致发光器件中使用的所有环金属化铱络合物。例如,可获得的络合物包括在申请wo 00/70655、wo 2001/41512、wo 2002/02714、wo 2002/15645、ep 1191613、ep 1191612、ep 1191614、wo 05/033244、wo 05/019373、us 2005/0258742、wo 2009/146770、wo 2010/015307、wo 2010/031485、wo 2010/054731、wo 2010/054728、wo 2010/086089、wo 2010/099852、wo 2010/102709、wo 2011/032626、wo 2011/066898、wo 2011/157339、wo 2012/007086、wo 2014/008982、wo 2014/023377、wo 2014/094961、wo 2014/094960、wo 2015/036074、wo 2015/104045、wo 2015/117718、wo 2016/015815、wo 2016/124304、wo 2017/032439、wo 2018/011186、wo 2018/001990、wo 2018/019687、wo 2018/019688、wo 2018/041769、wo 2018/054798、wo 2018/069196、wo 2018/069197、wo 2018/069273、wo 2018/178001、wo 2018/177981、wo 2019/020538、wo 2019/115423、wo 2019/158453、wo 2019/179909和us 2020/0048290以及尚未公开的申请ep19156381.6中公开的络合物。
[0227]
一般来说,在用于有机电致发光器件的环金属化络合物中常用的所有配体均可用于根据本发明的方法中。
[0228]
在本发明的方法中可用作反应物的有用的铱化合物包括各种化合物。优选的铱反应物是卤化铱,尤其是氯化铱、羧酸铱,尤其是乙酸铱、铱-cod络合物、铱酮酮合物和下文详述的化合物。
[0229]
可在本发明方法中用作反应物的优选铱化合物是下式(34)至(39)的化合物,
[0230][0231]
其中r、cyc和cyd具有上文给出的定义并且使用的其它符号如下:
[0232]
hal在每种情况下相同或不同并且是f、cl、br或i;
[0233]
kat在每种情况下相同或不同并且是碱金属阳离子、铵阳离子、具有4至40个碳原子的四烷基铵阳离子或具有4至40个碳原子的四烷基阳离子;
[0234]
z是0至100;
[0235]
y是0至100。
[0236]
此外合适的是cod-铱(i)化合物,例如[(cod)ircl]2(cas[12112-67-3])或(cod)ir(ind)(cas[102525-11-1]),其中cod代表环辛二烯并且ind代表茚基。
[0237]
式(34)的卤化铱水合物、尤其是氯化铱水合物,不是定义的化合物,因为它是可能含有不同量的hcl和/或水的吸湿性化合物。批料的水含量通常在这里经由铱含量报告。本发明上下文中的术语“卤化铱”或“卤化铱水合物”包括所有这些化合物,而与存在的水和卤化氢的量无关。
[0238]
式(36)的羧酸铱,例如乙酸铱,也不是完美的化学计量或定义的化合物,并且有用的化合物包括可能含有不同量的乙酸、水和氢氧化物的各种羧酸铱,例如化合物cas[37598-27-9]、[126310-98-3]或[52705-52-9]。在本发明上下文中的术语“羧酸铱”包括所有这些化合物,而不管它们的确切组成如何。
[0239]
式(36)、(37)和(38)中的r优选为具有1至10个碳原子的烷基基团或具有5至12个芳族环原子并且可以被一个或多个基团r1取代的芳族或杂芳族环系。更优选地,式(36)、(37)和(38)中的r是具有1至5个碳原子的烷基基团,尤其是甲基或叔丁基。
[0240]
优选的式(34)化合物是标记z为1至10,更优选2至4的那些。优选的式(34)化合物也是标记y为0至10,更优选0至3的那些。更优选地,同时,z=2至4并且y=0至3。
[0241]
优选的式(35)化合物是标记z为0至10,更优选0至3的那些。优选的式(35)化合物也是标记y为0至10,更优选0至3,甚至更优选0的那些。更优选地,同时,z=0至3并且y=0至3。
[0242]
标记z和y不必是整数,因为反应物还可以包含非化学计量量的水和卤化氢。由于涉及吸湿性金属盐,每个批料中的水含量特别地可以变化。
[0243]
优选的式(34)、(35)、(38)和(39)的化合物也是其中符号hal在每种情况下相同或不同并且是cl或br、更优选cl的那些。
[0244]
根据本发明,所述方法在至少一种羧酸存在下在无水介质中进行。羧酸是带有一个或多个羧基基团(-cooh)的有机化合物。合适的羧酸是在室温下为液体的羧酸和在室温下为固体但在反应条件下熔化的羧酸。
[0245]
本发明的一个优选的实施方式涉及式r
4-cooh的单羧酸或式hooc-r
5-cooh的双羧酸。这里r4选自具有1至20个碳原子的直链烷基基团,或具有3至20个碳原子的支链或环状的烷基基团,其中所述烷基基团在每种情况下可以被一个或多个r1基团取代,或具有2至20个碳原子并且可以被一个或多个r1基团取代的烯基或炔基基团,具有5至40个芳族环原子并且在每种情况下可以被一个或多个非芳族r1基团取代的芳族或杂芳族环系,或具有5至20个芳族环原子并且在每种情况下可以被一个或多个r1基团取代的芳烷基或杂芳烷基基团。r5选自具有1至20个碳原子的直链烷亚基基团或具有3至20个碳原子的支链或环状的烷亚基基团,其中所述烷亚基基团在每种情况下可以被一个或多个r1基团取代,或具有2至20个碳原子并且可以被一个或多个r1基团取代的烯基或炔基基团,具有5至40个芳族环原子并且在每种情况下可以被一个或多个非芳族r1基团取代的二价芳族或杂芳族环系,或具有5至20个芳族环原子并且在每种情况下可以被一个或多个r1基团取代的二价芳烷基或杂芳烷基基团。这里的r1具有上文给出的定义。
[0246]
在本发明的一个优选的实施方式中,r4选自具有1至10个碳原子,更优选具有1、2、3或4个碳原子的直链烷基基团,或具有3至10个碳原子,更优选具有3、4、5或6个碳原子的支链或环状的烷基基团,其中所述烷基基团在每种情况下可以被苯基基团取代,或具有6至12个芳族环原子的芳族或杂芳族环系,优选地苯基基团,所述芳族或杂芳族环系在每种情况下可以被一个或多个具有1至4个碳原子的烷基基团取代,或具有6至12个芳族环原子的芳烷基基团。
[0247]
在本发明的另一个优选的实施方式中,r5选自具有1至10个碳原子,更优选具有1、2、3或4个碳原子的直链烷亚基基团,或具有3至10个碳原子,更优选具有3、4、5或6个碳原子的支链或环状的烷亚基基团,其中所述烷亚基基团在每种情况下可以被苯基基团取代,或具有6至12个芳族环原子的二价芳族或杂芳族环系,优选地苯亚基基团,所述二价芳族或杂芳族环系在每种情况下可以被一个或多个具有1至4个碳原子的烷基基团取代,或具有6至12个芳族碳原子的二价芳烷基基团。
[0248]
优选的羧酸是乙酸、丙酸、新戊酸、苯甲酸、苯乙酸、己二酸及其混合物。特别优选乙酸、新戊酸、苯甲酸、水杨酸或苯乙酸及其混合物。
[0249]
例如,一些配体微溶于冰醋酸中。在这种情况下,有利的是使用或添加具有芳族结构部分的羧酸,例如苯甲酸、水杨酸或苯乙酸。
[0250]
同样合适的是二羧酸,例如马来酸、富马酸、丙二酸、邻苯二甲酸、间苯二甲酸或对苯二甲酸。其它合适的羧酸是氨基酸,尤其是α-、β-、γ-、δ-或ε-氨基酸,例如甘氨酸、丙氨酸、苯丙氨酸或ε-氨基己酸,以及羟基羧酸,尤其是α-、β-、γ-、δ-或ε-羟基羧酸,例如苹果酸、d-酒石酸、l-酒石酸或内消旋酒石酸、柠檬酸、乙醇酸、d-扁桃酸或l-扁桃酸或乳酸。
[0251]
在本发明的一个实施方式中,羧酸或两种或更多种羧酸的混合物被用作唯一溶剂。在本发明的另一个实施方式中,所用溶剂是一种或多种羧酸和一种或多种惰性有机溶剂的混合物,例如二烷、甲苯、苯甲醚、二甲苯、均三甲苯或各种乙二醇醚。这里“惰性”是指溶剂不与所用的羧酸反应并且不具有任何酸性质子,尤其是任何羟基基团。惰性溶剂的
特征在于pka》15。使用有机溶剂可有助于提高配体的溶解性。此外,有机溶剂的使用简化了反应状况,尤其是在生产规模上。
[0252]
所用羧酸的量优选相对于每毫摩尔的铱反应物为1g至100g,更优选相对于每毫摩尔的铱反应物为10g至50g。
[0253]
取决于铱反应物,可优选向反应混合物中添加其它添加剂。
[0254]
尤其是当所用的铱反应物是水合物,例如氯化铱水合物时,可优选加入水清除剂。在本发明上下文中的水清除剂是在反应条件下与水发生化学反应并因此将水从反应混合物中除去的化合物。这里优选的是,选择水清除剂以使得其与水在反应条件下发生化学反应,充分完全反应使得反应混合物的水含量(通过karl fischer滴定确定,如例如chemie in unserer zeit 2000,no.3中所述)小于10ppm。本领域技术人员通常知道哪些化合物与水反应并因此能够从反应混合物中除去水。
[0255]
合适的水清除剂是例如羧酸酐、羰基卤(尤其是羰基氯)、原羧酸三烷基酯或碳二亚胺,以及与水反应的无机化合物,例如五氧化二磷(p4o
10
)、亚硫酰氯或磷酰氯。合适的羧酸酐和羰基卤的实例对应于反应混合物中所用的羧酸,即,例如,当使用乙酸时为乙酸酐或乙酰氯,当使用新戊酸时为新戊酸酐或新戊酰氯,当使用苯甲酸时为苯甲酸酐或苯甲酰氯,当使用苯乙酸时为苯乙酸酐或苯乙酰氯等。另外合适的羰基卤是草酰氯。例如,还可以使用乙酸酐或乙酰氯,同时使用更高熔点或更高沸点的羧酸。建议蒸馏掉反应期间形成的乙酸。合适的原羧酸三烷基酯的实例是原甲酸三甲酯和原乙酸三乙酯。合适的碳二亚胺的一个实例是二环己基碳二亚胺(dci)。在本技术的上下文中,所有这些化合物都是水清除剂。
[0256]
水清除剂的量优选为3当量至30当量,更优选为5当量至20当量并且最优选为10当量至20当量,其中当量是基于所用铱反应物的摩尔量。
[0257]
在无水铱反应物的情况下,添加水清除剂不会提供任何进一步的益处。
[0258]
尤其是当卤化物用作铱反应物时,例如氯化铱水合物或[(cod)ircl]2,添加盐也可有帮助。怀疑该盐充当卤化物清除剂,在本发明上下文中的卤化物清除剂是在反应介质中与铱反应物的卤化物形成微溶盐的化合物。然而,与现有技术相比,不需要添加银盐,因为许多盐微溶于羧酸,因此可以避免形成难以分离的卤化银。合适的卤化物清除剂是例如碱金属盐、碱土金属盐、铵盐或锌盐,尤其是在反应介质中使用的羧酸的相应盐。此外,相应的乙酸盐也是合适的,即使当使用更高熔点或更高沸点的羧酸时也是如此,在这种情况下,形成的乙酸优选在反应期间被蒸馏掉。合适的碱金属盐是例如锂盐、钠盐或钾盐,优选钠盐或钾盐并且更优选钾盐。因此,例如,当使用乙酸时优选使用乙酸钾,而且当使用其它羧酸时也如此,当使用新戊酸时优选使用新戊酸钾,当使用苯甲酸时优选使用苯甲酸钾,当使用水杨酸时优选使用水杨酸钾,等等。在本技术的上下文中,所有这些化合物都是卤化物清除剂。
[0259]
用作卤化物清除剂的添加盐的量优选为10当量至100当量,更优选为10当量至50当量并且最优选为20当量至40当量,其中当量是基于所用铱反应物的摩尔量。
[0260]
在不含卤化物的铱反应物的情况下,添加卤化物清除剂不会提供任何进一步的益处。
[0261]
反应优选在室温至250℃、优选60℃至230℃、更优选80℃至200℃、甚至更优选100℃至180℃并且尤其优选120℃至160℃的温度范围内进行,其中该温度是反应容器的夹套
温度。反应温度还取决于所用的铱反应物。例如,在反应性铱反应物例如(cod)ir(ind)的情况下,即使《100℃的反应温度也足以实现非常好的产率,而例如,在使用氯化铱水合物的情况下,在120℃至160℃范围内的反应温度下可实现更好的产率。
[0262]
在本发明的一个优选的实施方式中,反应在保护气体气氛中进行,尤其是在氮气或氩气下进行。
[0263]
在本发明的一个实施方式中,反应在环境压力和回流下进行。在另一个实施方式中,反应在封闭系统中,例如在封闭安瓿或高压釜中在回流下进行。这里的压力对应于溶液上方的蒸气压。
[0264]
铱与反应介质中使用的配体的优选摩尔比取决于所用的铱反应物和所用的配体。当三足六齿配体用于式(1)的络合物时,ir与配体的比率为1:0.9至1:5是优选的,尤其是1:1至1:1.05的比率。对于式(2)的络合物,优选使用ir与配体的比率为1:1至1:20,更优选1:3至1:15,最优选1:10至1:13。对于式(3)的络合物,优选使用ir与配体的比率为1.5:1至10:1,优选为1.9:1至3:1并且最优选为1.9:1至2:1。
[0265]
反应优选在1h至1000h内进行,更优选在5h至500h内进行,最优选在10h至200h内进行。
[0266]
当使用含卤素的铱反应物时,进一步优选的是所使用的反应容器不是钢罐,而是例如由玻璃、搪瓷或teflon制成的反应容器。
[0267]
使用微波辐射可以进一步加速反应。环金属化反应通常可以在微波中进行的方式描述于例如wo 2004/108738中。
[0268]
在本发明的方法中,反应混合物的后处理很简单,因为环金属化铱化合物通常在反应中部分或完全沉淀出来。这可以通过用不溶解铱化合物的溶剂,例如用醇(例如乙醇)、水、或醇和水的混合物进行沉淀来完成。还可建议另外加入有机溶剂,例如甲苯、二甲苯或二烷,以从产物中溶解过量的配体。然后可以通过过滤和用使其不溶的溶剂,例如用水、醇(例如乙醇)或、醇和水的混合物洗涤来分离和纯化产物。如果需要,可以通过对于此类铱络合物通常常用的方法,例如重结晶、色谱法、热萃取、升华和/或热处理来实现进一步纯化。
[0269]
可通过本发明的方法获得的络合物是通常以外消旋形式获得的手性化合物。还可以通过使用手性对映异构纯的羧酸来合成对映异构富集或对映异构纯的络合物。适用于此目的的实例是使用α-氨基羧酸,其中多种是可用的,例如丙氨酸、苯丙氨酸等。此外合适的是羟基羧酸,例如苹果酸或酒石酸。
[0270]
本发明的方法与现有技术相比提供以下优点:
[0271]
1.本发明的方法能够从易得的卤化铱以及其它铱反应物以一个步骤并以非常好的产率获得环金属化铱络合物,尤其是三环金属化铱络合物,而根据现有技术的许多方法从更复杂的反应物例如铱酮酮合物络合物或氯桥接二聚铱络合物开始,和/或实现较差的产率。
[0272]
2.本发明方法中使用的羧酸可以在有机生产中以标准方式使用,而不需要超出正常有机生产的特殊安全措施。
[0273]
3.高达190℃的方法温度和高达6巴的压力在有机生产的常规范围内,因此所述目的不需要特殊的技术措施。这对于在约120℃和环境压力下回流的优选区域中的反应方案
尤其如此。
[0274]
4.加热和冷却时间可以在常规有机生产中毫无困难地实施并且在方法中不是关键的。
[0275]
5.后处理仅包括典型的简单方法步骤,例如过滤、离心、洗涤和/或干燥以及通过重结晶、色谱法、升华和/或热处理进行纯化。
[0276]
6.没有观察到形成呈铱镜或铱黑形式的金属铱。更特别是,没有观察到自燃元素铱的形成,这构成了反应安全性的显著改进。
[0277]
更特别是,根据以上详述的优点,本发明的方法也非常适合以生产规模而不只是实验室规模制备环金属化铱络合物。
[0278]
本发明将通过以下实施例进一步说明,但不旨在限于所述实施例。对于有机和有机金属合成领域的技术人员而言,无需进一步的创造性技能就可以在其它体系中进行本发明的反应。更特别地,所述方法可以在不付出创造性劳动的情况下在不同取代的体系上或者在含有其它芳基或杂芳基基团作为配位基团而不是苯基或吡啶的体系上进行。本领域技术人员同样能够在添加羧酸、其它水清除剂和/或其它盐的情况下进行本发明的方法。
实施例:
[0279]
除非另有说明,否则随后的合成在保护气体气氛下在干燥溶剂中进行。金属络合物另外在避光下或在黄光下处理。溶剂和试剂可以例如购自sigma-aldrich或abcr。方括号中的相应数字或个别化合物引用的数字与文献中已知的化合物的cas编号有关。在化合物可以显示多种对映异构、非对映异构或互变异构形式的情况下,以代表性方式显示一种形式。
[0280]
1)一般程序
[0281]
三足六齿配体、铱反应物和反应介质r,以及如果适当,则添加剂a(干燥剂、水清除剂)和添加剂b(羧酸盐,用作卤化物清除剂)的混合物,其最初在可封闭的耐压反应容器(例如带隔垫盖的颈缩瓶)中在氩气气氛下装入并在加热块中加热至指定温度(=加热块温度)。在指定的时间取样并经由1h nmr光谱法和/或hplc进行分析。对于1h nmr光谱分析,将2滴反应混合物用0.75ml dmso-d6稀释,并且加热混合物直至形成澄清溶液,然后照常分析。随后,将反应混合物的光谱与相应配体的光谱和在dmso-d6中的络合物的光谱进行比较,并经由积分进行量化。这种方法的误差估计为 /-5%。hplc通过已建立的标准方法进行(hplc柱:chromolith-performance rp-18e,100-4.6mm,梯度:水-乙腈,检测254nm)。所报告的转化率是基于配体峰和络合物峰的面积%。下文指定的实验以摩尔量1eq=100μmol进行。
[0282]
结果整理在表1中。单独标题各自显示哪些参数发生了变化。缩写在表格下方阐明。
[0283]
表1
[0284]
[0285]
[0286]
[0287][0288]
1)δ,δ-/λ,λ-和δ,λ-非对映异构体混合物约1:1
[0289]
2)添加100eq丙氨酸用于手性诱导,δ,δ-/λ,λ-和δ,λ-非对映异构体混合物约1:4
[0290]
缩写:
[0291]
hoac:无水乙酸、冰醋酸[64-19-7]
[0292]
hopiv:新戊酸[75-98-9]
[0293]
hobnz:苯甲酸[65-85-0]
[0294]
hophe:苯乙酸[103-82-2]
[0295]
ac2o:乙酸酐[108-24-7]
[0296]
piv2o:新戊酸酐[1538-75-6]
[0297]
bnz2o:苯甲酸酐[93-97-0]
[0298]
accl:乙酰氯[75-36-5]
[0299]
tmof:原甲酸三甲酯[149-73-5]
[0300]
teoa:原乙酸三乙酯[78-39-7]
[0301]
p4o
10
:十氧化四磷[1314-56-3]
[0302]
lioac:无水乙酸锂[546-89-4]
[0303]
naoac:无水乙酸钠[127-09-3]
[0304]
koac:无水乙酸钾[127-08-2]
[0305]
nh4oac:乙酸铵[631-61-8]
[0306]
zn(oac)2:无水乙酸锌[557-34-6]
[0307]
kopiv:无水新戊酸钾[19455-23-3]
[0308]
kobnz:无水苯甲酸钾[582-25-2]
[0309]
l-丙氨酸:l-丙氨酸[56-41-7]
[0310]
ircl
3 x h2o:三氯化铱水合物,在本发明的上下文中,用于下文列出的化合物的统称性术语,其化学计量根据所用化合物的ir含量进行调整:
[0311]
ircl
3 x 3 h2o:[13569-57-8]
[0312]
ircl
3 x x h2o:[14996-61-3]
[0313]
ircl
3 x 4 h2o:[16938-21-9]
[0314]
ircl
3 x 1 h2o:[1542203-90-6]
[0315]
ircl
3 x 2 h2o:[1593479-74-3]
[0316]
ircl
3 x hcl x h2o:[717927-65-6]
[0317]
ir(oac)3:乙酸铱,在本发明的上下文中,用于下文列出的化合物的统称性术语,其化学计量根据所用化合物的ir含量进行调整:
[0318]
ir(oac)
x
:[37598-27-9]
[0319]
[ir3c
12h24o16
]ch3o2:[52705-52-8]
[0320]
[ir(cod)cl)2:环-1,5-辛二烯基铱(i)氯化物二聚体[12112-67-3]
[0321]
(ind)ir(cod):(1,5-环辛二烯)(η5-茚基)铱(i)[102525-11-1]
[0322]
u.e.:在密闭反应容器中在反应混合物的自生压力下在规定温度下g.a.:与大气相比,被氩气覆盖的颈缩瓶相比于实验室气氛,温度图:在反应混合物中测得的温度
[0323]
使用l1为例,在制备规模上进行所述方法:
[0324][0325]
a:在冰醋酸中利用乙酸酐和乙酸钾
[0326]
在氩气气氛下在带有teflon插件的搅拌高压釜中装入9.18g(10mmol)的配体l1、3.53g(10mmol)的ircl
3 x 3 h2o、29.45g(300mmol)的无水乙酸钾、300ml的冰醋酸和9.47ml(100mmol)的乙酸酐,密闭并加热至160℃,同时充分搅拌48h(压力:4.3巴)。冷却后,将黄色悬浮液在搅拌下倒入1000ml软化水中,并且抽滤出黄色固体,用每次200ml水洗涤三次并用每次50ml乙醇洗涤两次,并减压干燥。将固体悬浮在300ml温热的二氯甲烷(dcm)中1h,然后在300g硅胶60(merck)上用dcm进行色谱分离。选择黄色主要部分(rf~0.9),并且在旋转蒸发器上在50℃水浴温度和标准压力下蒸馏出dcm,通过加入etoh连续替换蒸馏出的dcm体积。dcm蒸馏结束后,将混合物减压浓缩至约100ml,利用双头玻璃原料过滤出黄色固体,并且将残余物用每次50ml乙醇洗涤两次并首先在氩气流中干燥,然后减压干燥(p~10-3
毫巴,t~100℃)。产量:10.19g(9.20mmol);理论值的92%;纯度:》99.5%,根据1h nmr和hplc。如wo 2016/124304中所述,由此获得的产物可以通过热萃取和分级升华进一步纯化。
[0327]
b:在新戊酸中利用新戊酸酐和新戊酸钾
[0328]
如a)中所述的程序,不同之处在于使用新戊酸而不是乙酸,使用新戊酸酐而不是乙酸酐并且使用新戊酸钾而不是乙酸钾,以及在带有精密玻璃搅拌器、回流冷凝器和氩气覆盖的2l四颈圆底烧瓶中进行反应。内部温度~165℃。产量:10.44g(9.43mmol);理论值的94%;纯度:》99.5%,根据1h nmr和hplc。
[0329]
c:在新戊酸中利用乙酸酐和乙酸钾
[0330]
如b)中所述的程序,不同之处在于使用乙酸酐而不是新戊酸酐并且使用乙酸钾而不是新戊酸钾,以及在带有精密玻璃搅拌器、水分离器、回流冷凝器和氩气覆盖的2l四颈圆底烧瓶中进行反应。不时排出收集在水分离器中的乙酸。内部温度~155℃。产量:10.51g(9.50mmol);理论值的95%;纯度:》99.5%,根据1h nmr和hplc。
[0331]
d:在苯甲酸中利用苯甲酸酐和苯甲酸钾
[0332]
如a)中所述的程序,不同之处在于使用苯甲酸而不是乙酸,使用苯甲酸酐而不是乙酸酐并且使用苯甲酸钾而不是乙酸钾,以及在带有精密玻璃搅拌器、回流冷凝器和氩气覆盖的2l四颈圆底烧瓶中进行反应。内部温度~168℃。对于后处理,将温热的、仍为液态的反应混合物倒入水中。产量:10.51g(9.49mmol);理论值的95%;纯度:》99.5%,根据1h nmr和hplc。
[0333]
e:在苯乙酸中利用乙酸酐和乙酸钾
[0334]
如c)中所述的程序,使用苯乙酸而不是新戊酸。内部温度~152℃。对于后处理,将温热的、仍为液态的反应混合物倒入水中。产量:10.84g(9.80mmol);理论值的98%;纯度:》99.5%,根据1h nmr和hplc。
[0335]
f:在水杨酸/均三甲苯中利用ir(oac)3[0336]
在氩气气氛下在具有精密玻璃搅拌器、水分离器(10ml储液器)、回流冷凝器和氩气覆盖的500ml四颈烧瓶中装入9.18g(10mmol)的配体l1、3.69g(10mmol)的乙酸铱(iii)ir(oac)3、40g水杨酸和40ml均三甲苯,并且将平缓回流(内部温度约158℃)加热22h。最初的蓝色溶液随着时间变成黄色悬浮液;将开始时还分离出的一些乙酸排出。22h后,使混合物冷却至90℃,小心滴加200ml乙醇,在搅拌下将混合物冷却至40℃,并且抽滤出黄色固体,用每次30ml甲醇洗涤三次并减压干燥。如a中所述进一步纯化。产量:10.86g(9.20mmol);理论值的98%;纯度:》99.5%,根据1h nmr和hplc。如wo 2016/124304中所述,由此获得的产物可以通过热萃取和分级升华进一步纯化。
[0337]
除了均三甲苯,还可以使用苯甲醚。
[0338]
配体:
[0339]
表2显示了所用的配体。
[0340]
表2:
[0341]
[0342]
[0343]
[0344]
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。