1.本发明涉及包含治疗有效量的马西替坦、糖醇稀释剂和表面活性剂的压缩组合物。本发明还涉及获得所述压缩组合物的方法、包含它们的口服药物组合物以及它们在治疗肺动脉高压中的用途。
背景技术:
2.马西替坦为化合物n-[5-(4-溴苯基)-6-[2-[(5-溴-2-嘧啶基)氧]乙氧基]-4-嘧啶基]-n'丙磺酰胺的国际非专有名称(inn),也被称为代号act-064992。其分子式为c
19h20
br2n6o4s并且其分子量为588.27g.mol-1
。其具有以下结构式:
[0003][0004]
马西替坦是目前批准的内皮素受体拮抗剂(era),并且并以商标opsumit在欧洲(eu和其它国家/地区)、美国和日本销售,用于治疗肺动脉高压。马西替坦是选择性抑制et-1与eta和etb有受体的结合的双内皮素(et)受体拮抗剂。马西替坦抑制由这些受体介导的效应。
[0005]
马西替坦在室温下在ph 1.2、4、6.8、7、9的水溶液中不溶,并且在有机溶剂甲醇和乙醇中仅微溶。它是生物药剂学分类系统(bcs)ii类化合物,特征在于高渗透性和低溶解性。其溶剂化速率限制了体内表现出的生物利用度。
[0006]
mct-ima是马西替坦通过氧化或水解形成的最普遍的杂质。它也是排泄在粪便中的主要代谢物。(yerra,n.v.et al.rapid commun mass spectrum 2018,15,32,(13),1075-1084;thummar,m.et al.chromatographia2018,81,3,525-531)(bruderer,s.et al.xenobiotica,2012,1-10)。
[0007]
文献wo 2002053557 a1公开了马西替坦及其制备方法。
[0008]
文献wo 2007031933和us8367685b2公开了马西替坦的固体口服药物组合物。结果表明,在所有测试的可能性中,表现出更好行为的组合物是包含高剂量乳糖或乳糖一水合物作为填料的组合物。
[0009]
文献in 201641023754公开了包含乳糖作为填料的马西替坦组合物。
[0010]
文献wo 2014173805公开了包含特定多晶型的马西替坦组合物。特别地,文献wo 2014173805公开了包含结晶马西替坦游离碱的药物组合物的制备。
[0011]
文献wo 2018153925公开了不含表面活性剂的马西替坦组合物。
[0012]
文献in 201641002749公开了通过挤出方法获得的马西替坦组合物。
[0013]
文献cn107913256涉及含有以下组分比率的马西替坦-崩解片:马西替坦-5-10%,崩解剂5-20%,粘合剂0.5-20%,润滑剂0.5-5%,调味剂2-5%,填料65-75mg。
[0014]
文献cn109260163 a涉及一种稳定的马西替坦片剂组合物,以提供定性临床药物。
[0015]
文献wo 2010054845 a1涉及一种制备碳酸钙片剂的方法,该方法导致片剂在溶出方面具有改善的储存稳定性。
[0016]
公开这些事实是为了说明本公开所解决的技术问题。
技术实现要素:
[0017]
鉴于现有技术的缺点,我们在此公开了包含治疗有效量马西替坦的固体口服药物组合物,其同时表现出改善的稳定性特性和适当的溶出曲线。
[0018]
本公开涉及包含治疗有效量马西替坦、糖醇稀释剂和表面活性剂的压缩组合物。其还涉及获得所述压缩组合物的方法,包含它们的口服药物组合物以及它们在治疗肺动脉高压中的用途。
[0019]
本公开还涉及包含治疗有效量马西替的固体口服药物组合物,其同时显示出改进的稳定性和适当的溶出曲线。
[0020]
本公开还涉及压缩组合物,其包含治疗有效量的马西替坦;选自由以下项组成的列表中的糖醇稀释剂:麦芽糖醇,木糖醇,甘露糖醇或它们的混合物;和选自由以下项组成的列表中的表面活性剂:十二烷基硫酸钠(sds),聚山梨醇酯80(tween 80)或它们的混合物。
[0021]
在一个实施方式中,所述压缩组合物包含治疗有效量的马西替坦、糖醇稀释剂和表面活性剂。
[0022]
在一个实施方式中,所述表面活性剂是指聚山梨醇酯20(聚氧乙烯(20)脱水山梨糖醇单月桂酸酯)、聚山梨醇酯40(聚氧乙烯(20)脱水山梨糖醇单棕榈酸酯)、聚山梨醇酯60(聚氧乙烯(20)脱水山梨糖醇单硬脂酸酯)、聚山梨醇酯80(聚氧乙烯(20)脱水山梨糖醇单油酸酯)或sds(十二烷基硫酸钠)。优选地,所述表面活性剂可以选自聚山梨醇酯80(聚氧乙烯(20)脱水山梨糖醇单油酸酯)或sds(十二烷基硫酸钠)。
[0023]
在一个实施方式中,为了更好的结果,所述表面活性剂为十二烷基硫酸钠、聚山梨醇酯80或它们的混合物。
[0024]
在一个实施方式中,所述糖醇稀释剂是指乙二醇、丙三醇、赤藓糖醇、苏糖醇、阿糖醇、木糖醇、核糖醇、甘露糖醇、山梨糖醇、半乳糖醇、果糖醇、艾杜糖醇、纤维醇、庚七醇、异麦芽酮糖醇、麦芽糖醇、乳糖醇、马罗三醇(marotriol)、麦芽四糖醇或聚葡萄糖醇。
[0025]
在一个实施方式中,为了更好的结果,所述糖醇稀释剂选自麦芽糖醇、木糖醇、甘露糖醇或它们的混合物。
[0026]
在一个实施方式中,为了更好的结果,所述糖醇稀释剂为麦芽糖醇、木糖醇或它们的混合物。
[0027]
在优选的实施方式中,所述表面活性剂为十二烷基硫酸钠(sds)。
[0028]
在优选的实施方式中,所述表面活性剂为聚山梨醇酯80(tween 80)。
[0029]
在一个实施方式中,本公开的压缩组合物可以进一步包含从非糖醇稀释剂、崩解剂、粘合剂和润滑剂中选择的至少一种赋形剂,优选所述非糖醇稀释剂为微晶纤维素。
[0030]
在优选的实施方式中,本公开的压缩组合物可以包含0.1%至15%(wt
表面活性剂
/wt
总
)的表面活性剂,优选0.5%至10%(wt
表面活性剂
/wt
总
),更优选0.5%至5%(wt
表面活性剂
/wt
总
);甚至
更优选0.5至2%(wt
表面活性剂
/wt
总
)的表面活性剂。
[0031]
在优选的实施方式中,本公开的压缩组合物可以包含0.9%至10%(wt
表面活性剂
/wt
总
)的表面活性剂,优选2%至10%(wt
表面活性剂
/wt
总
),更优选2%至5%(wt
表面活性剂
/wt
总
)。
[0032]
在优选的实施方式中,本公开的压缩组合物可以包含:
[0033]
作为糖醇稀释剂的麦芽糖醇和作为表面活性剂的十二烷基硫酸钠;或
[0034]
作为糖醇稀释剂的麦芽糖醇和作为表面活性剂的聚山梨醇酯80;
[0035]
作为糖醇稀释剂的木糖醇和作为表面活性剂的十二烷基硫酸钠;或
[0036]
作为糖醇稀释剂的木糖醇和作为表面活性剂的聚山梨醇酯80;
[0037]
作为糖醇稀释剂的甘露糖醇和作为表面活性剂的十二烷基硫酸钠;或
[0038]
作为糖醇稀释剂的甘露糖醇和作为表面活性剂的聚山梨醇酯80。
[0039]
在优选的实施方式中,本公开的压缩组合物可以包含15%至85%(wt
糖醇稀释剂
/wt
总
)的糖醇稀释剂,优选25%至75%(wt
糖醇稀释剂
/wt
总
),更优选35%至65%(wt
糖醇稀释剂
/wt
总
)。
[0040]
在优选的实施方式中,本公开的压缩组合物可以包含1%至45%(wt
马西替坦
/wt
总
)的马西替坦,优选5%至35%(wt
马西替坦
/wt
总
),更优选5%至25%(wt
马西替坦
/wt
总
)。
[0041]
在优选的实施方式中,本公开的压缩组合物可以包含5%至65%(wt
非糖醇稀释剂
/wt
总
)的非糖醇稀释剂,优选10%至50%(wt
非糖醇稀释剂
/wt
总
),更优选15%至35%(wt
非糖醇稀释剂
/wt
总
)。
[0042]
在一个实施方式中,所述压缩组合物包含5%至25%(wt
马西替坦
/wt
总
)的马西替坦,35%至65%(wt
糖醇稀释剂
/wt
总
)的糖醇稀释剂和0.5%至5%(wt
表面活性剂
/wt
总
)的表面活性剂。
[0043]
在一个实施方式中,所述压缩组合物进一步包含从非糖醇稀释剂、崩解剂、粘合剂和润滑剂中选择的至少一种赋形剂。
[0044]
在一个实施方式中,所述非糖醇稀释剂为微晶纤维素,所述崩解剂为交聚维酮,所述粘合剂为聚维酮并且所述润滑剂为硬脂酸镁。
[0045]
在一个实施方式中,所述非糖醇稀释剂为微晶纤维素,所述崩解剂为羟基乙酸淀粉钠,所述粘合剂为聚维酮并且所述润滑剂为硬脂酸镁。
[0046]
本公开的一个方面涉及通过湿法制粒制备的压缩组合物。
[0047]
本公开的一个方面涉及一种用于在治疗肺动脉高压中使用的压缩组合物。
[0048]
本公开的一个方面涉及包含压缩的马西替坦组合物的固体口服药物组合物。
[0049]
本公开的一个方面涉及用于在治疗肺动脉高压中使用的包含压缩的马西替坦组合物的固体口服药物组合物。
[0050]
本公开的另一方面涉及一种用于制备压缩组合物的方法,包含:
[0051]
混合马西替坦、糖醇稀释剂与任选地从非糖醇稀释剂、崩解剂、粘合剂、助流剂中选择的一种或多种赋形剂;
[0052]
使用表面活性剂的水溶液将前一步骤中获得的混合物造粒,其中所述表面活性剂为十二烷基硫酸钠或聚山梨醇酯80或它们的组合。
[0053]
使用硬脂酸镁润滑前一步骤中获得的颗粒;
[0054]
压缩前一步骤中获得的经润滑的颗粒。
[0055]
本公开的另一方面涉及一种固体口服药物组合物,包含根据包含以下步骤的方法制备的压缩组合物:
[0056]
混合马西替坦、糖醇稀释剂与任选地从非糖醇稀释剂、崩解剂、粘合剂、助流剂中
选择的一种或多种赋形剂;
[0057]
使用表面活性剂的水溶液将前一步骤中获得的混合物造粒,其中所述表面活性剂为十二烷基硫酸钠或聚山梨醇酯80或它们的组合;
[0058]
使用硬脂酸镁润滑前一步骤中获得的颗粒;
[0059]
压缩前一步骤中获得的经润滑的颗粒。
[0060]
本公开的另一方面涉及一种用于在治疗肺动脉高压中使用的固体口服药物组合物,其包含根据包含以下步骤的方法制备的压缩组合物:
[0061]
混合马西替坦、糖醇稀释剂与任选地从非糖醇稀释剂、崩解剂、粘合剂、助流剂中选择的一种或多种赋形剂;
[0062]
使用表面活性剂的水溶液将前一步骤中获得的混合物造粒,其中所述表面活性剂为十二烷基硫酸钠或聚山梨醇酯80或它们的组合;
[0063]
优选使用硬脂酸镁,润滑前一步骤中获得的颗粒;
[0064]
压缩前一步骤中获得的经润滑的颗粒。
[0065]
在一个实施方式中,所述制备压缩组合物或用于在治疗肺动脉高压中使用的固体口服药物组合物的方法,其中所述糖醇稀释剂为麦芽糖醇、木糖醇或甘露糖醇。
[0066]
在一个实施方式中,所述用于制备压缩组合物、用于在肺动脉高压的治疗中使用的固体口服药物组合物的方法,其中所述非糖醇稀释剂为微晶纤维素。
[0067]
在一个实施方式中,所述用于制备压缩组合物、在肺动脉高压的治疗中使用的固体口服药物组合物的方法,其中所述崩解剂为交聚维酮或羟基乙酸淀粉钠或它们的混合物。
[0068]
所述用于制备压缩组合物、用于在肺动脉高压的治疗中使用的固体口服药物组合物的方法,其中所述粘合剂为聚维酮、共聚维酮或它们的混合物。
[0069]
在一个实施方式中,所述非糖醇稀释剂是指微晶纤维素。
[0070]
在一个实施方式中,所述崩解剂是指羟基乙酸淀粉钠、或交聚维酮或它们的混合物。
[0071]
在一个实施方式中,所述粘合剂是指聚维酮、共聚维酮或它们的混合物。优选地,所述粘合剂为聚维酮。
[0072]
在一个实施方式中,所述润滑剂是指硬脂酸钙、硬脂酸、硬脂富马酸钠或硬脂酸镁或它们的混合物。优选地,所述润滑剂为硬脂酸镁。
[0073]
在一个实施方式中,所述助流剂是指胶体无水二氧化硅或滑石粉。优选地,所述助流剂为无水胶体二氧化硅。
[0074]
在一个实施方式中,已经发现,与含有10mg马西替坦、乳糖一水合物、微晶纤维素、羟基乙酸淀粉钠、聚维酮、硬脂酸镁和聚山梨醇酯80的压缩组合物相比,所述压缩组合物显示出更高的稳定性和快速溶出曲线。
[0075]
在本公开的上下文中,压缩组合物包含任何组合物,该组合物包含马西替坦和药物赋形剂,诸如片芯、微片、囊片、珠粒、颗粒等。优选所述压缩组合物为片芯。
[0076]
在一个实施方式中,包含压缩的马西替坦组合物的所述固体口服药物组合物为预用于药剂的药物递送的任何固体口服组合物的形式,优选为片剂、微片、囊片,或为容纳在胶囊中的珠粒,或为用于提供单位剂型的小袋中的颗粒。最优选地,所述固体口服药物组合
物为片剂的形式。
附图说明
[0077]
以下附图提供了用于说明描述的优选实施方式,并且不应被视为限制本发明的范围。
[0078]
图1示出了与参考产品的溶出曲线相比,所公开的组合物(实施例1、2、3和5)的溶出曲线。
具体实施方式
[0079]
本发明涉及包含治疗有效量马西替坦、糖醇稀释剂和表面活性剂的压缩组合物。本发明还涉及获得所述压缩组合物的方法,包含它们的口服药物组合物和它们在治疗肺动脉高压中的用途。
[0080]
本公开涉及包含治疗有效量马西替坦的固体口服药物组合物,其同时展现出改进的稳定性和适当的溶出曲线。
[0081]
在一个实施方式中,根据以下方式制备压缩的马西替坦组合物(实施例1,组成细节见表1):
[0082]
a)在适当的设备中混合马西替坦、木糖醇、聚维酮、微晶纤维素、无水二氧化硅胶体和羟基乙酸淀粉钠粉末。
[0083]
b)使用由sds和水制备的造粒液将所述混合物造粒。
[0084]
c)颗粒在40℃下干燥并用1mm的筛孔校准.
[0085]
d)用硬脂酸镁润滑校准后的颗粒,然后压缩。
[0086]
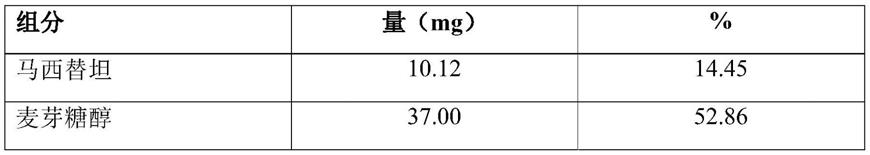
表1:实施例1的压缩的马西替坦组合物
[0087]
组分量(mg)%马西替坦10.1214.45木糖醇37.0052.86微晶纤维素15.8822.69羟基乙酸淀粉钠2.103.00聚维酮2.103.00sds1.402.00无水二氧化硅胶体0.701.00硬脂酸镁0.701.00总计70100.00
[0088]
在一个实施方式中,通过将木糖醇替换为麦芽糖醇,类似于实施例1的组合物,制备了一种压缩的马西替坦组合物(实施例2,组成细节见表2)。
[0089]
表2:实施例2的压缩的马西替坦组合物
[0090]
组分量(mg)%马西替坦10.1214.45麦芽糖醇37.0052.86
微晶纤维素15.8822.69羟基乙酸淀粉钠2.103.00聚维酮2.103.00sds1.402.00无水二氧化硅胶体0.701.00硬脂酸镁0.701.00总计70100.00
[0091]
在一个实施方式中,根据以下方法制备了压缩的马西替坦组合物(实施例3,组成细节见表3):
[0092]
a)在适当的设备中混合马西替坦、木糖醇、聚维酮、微晶纤维素和羟基乙酸淀粉钠粉末。
[0093]
b)使用以聚山梨醇酯80和水制备的造粒液将所述混合物造粒。
[0094]
c)颗粒在40℃下干燥并用1mm的筛孔校准。
[0095]
d)使用硬脂酸镁润滑校准后的颗粒,然后压缩。
[0096]
表3:实施例3的压缩的马西替坦组合物
[0097]
组分量(mg)%马西替坦10.1214.45木糖醇37.0052.86微晶纤维素16.5823.69羟基乙酸淀粉钠2.103.00聚维酮2.103.00聚山梨醇酯801.402.00硬脂酸镁0.701.00总计70100.00
[0098]
在一个实施方式中,通过将木糖醇替换为麦芽糖醇,类似于实施例3的组合物,制备了压缩的马西替坦组合物(实施例4,组成细节见表4)。
[0099]
表4:实施例4的压缩的马西替坦组合物
[0100]
[0101][0102]
在一个实施方式中,通过将木糖醇替换为甘露糖醇,类似于实施例1的组合物,制备了压缩的马西替坦组合物(实施例5,组成细节见表5)。
[0103]
表5:实施例5的压缩的马西替坦组合物
[0104]
组分量(mg)%马西替坦10.1214.45甘露糖醇37.0052.86微晶纤维素15.8822.69羟基乙酸淀粉钠2.103.00聚维酮2.103.00sds1.402.00无水二氧化硅胶体0.701.00硬脂酸镁0.701.00总计70100.00
[0105]
在一个实施方式中,类似于实施例3的组合物,制备了压缩的马西替坦组合物(实施例6,组成细节见表6)。
[0106]
表6:实施例6的压缩的马西替坦组合物
[0107][0108][0109]
在一个实施方式中,类似于实施例3的组合物,制备了压缩的马西替坦组合物(实施例7,组成细节见表7)。
[0110]
表7:实施例7的压缩的马西替坦组合物
[0111]
组分量(mg)%马西替坦10.1214.45甘露糖醇37.0052.86微晶纤维素16.5823.69羟基乙酸淀粉钠2.103.00聚维酮2.103.00tween 801.402.00硬脂酸镁0.701.00总计70100.00
[0112]
在一个实施方式中,类似于实施例3的组合物,制备了压缩的马西替坦组合物(实施例8,组成细节见表8)。
[0113]
表8:实施例8的压缩的马西替坦组合物
[0114][0115][0116]
根据以下方法制备了一种比较压缩的马西替坦组合物(组成细节见表9):
[0117]
a)在适当的设备中混合马西替坦、乳糖一水合物、聚维酮、微晶纤维素和羟基乙酸淀粉钠粉末。
[0118]
b)使用以聚山梨醇酯80和水制备的造粒液将所述混合物造粒。颗粒在40℃下干燥并用1mm的筛孔校准。
[0119]
c)使用硬脂酸镁润滑校准后的颗粒并且压缩。
[0120]
表9:压缩的马西替坦组合物(比较例)
[0121]
组分量(mg)%马西替坦10.1214.45乳糖一水合物37.0052.86微晶纤维素16.5823.69羟基乙酸淀粉钠2.103.00聚维酮2.103.00
聚山梨醇酯801.402.00硬脂酸镁0.701.00总计70100.00
[0122]
在一个实施方式中,分析了所述组合物的稳定性。将实施例1至4和7中描述的组合物和比较例的组合物置于压力条件下,以研究整个时间的产品行为和降解曲线。将测试批次储存在密闭瓶中并放置在两种不同的条件下,(a)40℃与75%相对湿度,(b)85%相对湿度。每个测试批次在暴露1.5个月后和/或暴露3个月后进行分析。
[0123]
在一个实施方式中,使用配备uv检测器的高效液相色谱系统在260nm下分析每种组合物。对于样品分析,使用经过验证的稳定性指示方法,并使用表征的工作标准进行量化。对马西替坦的普遍杂质mct-ima杂质以及杂质总量进行定量。
[0124]
表10:数据涉及具有sds或聚山梨醇酯和麦芽糖醇、木糖醇、甘露糖醇的实施例1-4和7以及比较例(细节见表9)的组合物在75%rh(相对湿度)和40℃下的稳定性
[0125][0126]
表11:数据涉及具有sds或聚山梨醇酯和麦芽糖醇、木糖醇、甘露糖醇的实施例1-4和7以及比较例(细节见表9)的组合物在85%rh下的稳定性
[0127][0128]
在一个实施方式中,与比较例(细节见表9)的组合物相比,实施例1至4和7的压缩的马西替坦组合物表现出增强的稳定性。表10显示,在40℃与75%相对湿度下3个月后,与比较例的组合物相比,实施例1至4和7的组合物表现出较低的mct-ima杂质水平和较低的总杂质水平。表11显示,在85%相对湿度下3个月后,实施例1至4和7的组合物表现出比比较例的组合物更低的总杂质水平。
[0129]
在一个实施方式中,分析了组合物的稳定性。将实施例1、2和5中描述的组合物以及比较例的组合物置于压力条件下,以研究整个时间的产品行为和降解曲线。将测试批次储存在密闭瓶中并保持在60℃下。每个测试批次分析两次,一次在暴露1.5个月后,且一次在暴露3个月后。
[0130]
在一个实施方式中,使用配备有uv检测器的高效液相色谱系统在260nm下分析各组合物。对于样品分析,使用经过验证的稳定性指示方法,并使用表征的工作标准进行量
化。对马西替坦的普遍杂质mct-ima杂质及杂质总量进行定量。
[0131]
表12:数据涉及具有sds和木糖醇、麦芽糖醇或甘露糖醇的实施例1、2、5以及比较例的组合物在60℃下的稳定性
[0132][0133]
表12显示,在60℃下,与比较例(细节见表9)的组合物相比,实施例1、2和5的压缩的马西替坦组合物表现出增强的稳定性。在60℃下1.5个月和3个月后,实施例1、2和5的组合物表现出的mct-ima杂质水平和总杂质水平低于比较例的组合物。
[0134]
表13:数据涉及实施例6的组合物在40℃和30℃下的稳定性
[0135][0136]
表13显示,在40℃或30℃下,与比较例(细节见表9)的组合物相比,实施例6的压缩的马西替坦组合物表现出增强的稳定性。
[0137]
还进行了溶出测试。在所公开实施例的溶出测试中,在900ml溶出介质中使用usp仪器2(桨)方法在50rpm转速下在37℃
±
0.5℃下进行。在测试开始后5、10、20、30、45、60和90分钟后取出样品,并使用合适的hplc方法在260nm下分析溶解的马西替坦。已经使用ph 6.8磷酸盐缓冲剂 0.1%ctab作为溶出介质,有足够的分辨能力。报告的溶出度结果是六个片剂的平均值。
[0138]
表14示出了与参考药物产品()相比的实施例组合物的溶出曲线。使用相似因子(f2)在相同条件下进行溶出测试。相似因子(f2)是衡量两条曲线之间溶出百分比相似性的指标。当f2值≥50时,认为两条溶出曲线相似。
[0139]
表14:数据涉及实施例1、2、3、5的口服固体组合物以及片剂的组合物的溶出曲线
[0140][0141]
在与包含马西替坦的商业固体口服组合物(片剂)相比时,所测试的压缩的马西替坦组合物显示出良好的相似度。
[0142]
表15:数据测试实施例6的口服固体组合物在0.1n hcl中的溶出曲线
[0143]
时间(min)%
00548106715743084458860909092
[0144]
表16:数据涉及实施例6的口服固体组合物在磷酸盐缓冲剂ph 6.8,0.02%ctab中和50rpm下的溶出曲线
[0145][0146]
表17:数据涉及实施例6、7和8的口服固体组合物在磷酸盐缓冲剂ph 6.8,0.1%ctab中和50rpm下溶出曲线
[0147][0148]
表18:数据涉及实施例6、7和8的口服固体组合物以及片的组合物的溶
出曲线
[0149][0150]
在给出范围的情况下,包括端点。另外,应当理解的是,除非另有说明或从上下文和/或本领域普通技术人员的理解中明显看出,表达为范围的值可以具有本发明不同实施方式中规定范围内的任何特定值,直至该范围下限单位的十分之一,除非上下文另有明确规定。还应当理解的是,除非另有说明或从上下文和/或本领域普通技术人员的理解中明显看出,表达为范围的值可以具有给定范围内的任何子范围,其中所述子范围的端点以与所述范围下限单位的十分之一相同的精度表示。
[0151]
无论何时,本文件中使用的术语“包含”旨在表示存在所陈述的特征、整数、步骤、组分,但不排除存在或添加一个或多个其它特征、整数、步骤、组分或其组。
[0152]
上述实施方式是可组合的。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。