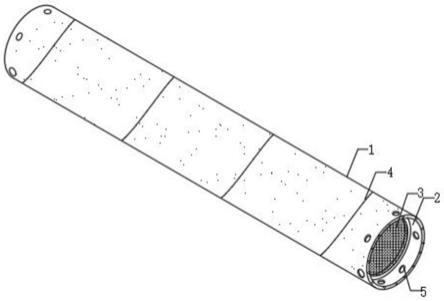
用于制备组织粘附片的方法
1.本发明的技术领域
2.本发明涉及制备组织粘附片的方法,所述方法包括:
3.·
提供包括三维互连间隙空间的纤维片;
4.·
提供反应性聚合物颗粒,所述反应性聚合物颗粒包括携带至少3个反应性亲电基团的水溶性亲电聚合物,所述反应性亲电基团能够在形成共价键的情况下与血液中的胺基团反应;
5.·
将纤维片和反应性聚合物颗粒置于两个电极之间;
6.·
同时使纤维片和反应性聚合物颗粒经受0.1至40kv/mm的电场以用反应性聚合物颗粒浸渍纤维片的互连间隙空间。
7.本发明的方法能够使反应性聚合物颗粒有效地分布在纤维片内,并能够生产具有优异粘附性能的组织粘附片。
8.本发明的背景
9.在对薄壁组织进行外科手术程序期间的一个主要挑战是实现对出血的控制。缝合控制、电灼和超声密封通常在例如肝或肾的手术期间是不够的。因此,像肝切除或部分肾切除术的程序需要替代的方法来控制出血。为此,已经开发了多种局部止血产品并且在临床上使用。
10.boerman等人(next generation hemostatic materials based on nhs-ester functionalized poly(2-oxazoline)s,biomacromolecules(2017),18,2529-2538)描述了通过将n-羟基琥珀酰亚胺酯(nhs)官能化聚(2-噁唑啉)(nhs-pox)涂覆到明胶贴片上获得的合成的非生物活性止血产品,其通过在聚合物、宿主血蛋白、明胶和组织之间形成共价交联来密封伤口部位并防止外科手术期间出血。
11.us 2010/0233246描述了生物相容性聚合物装置,其包括用两部分反应性聚乙二醇粉末浸渍的胶原海绵或片,其中所述反应性粉末包括具有亲核基团的第一聚乙二醇和具有亲电基团的第二聚乙二醇,其中所述聚乙二醇粉末在干燥状态下保持非反应性。
12.us 2011/0250257描述了无水纤维片,其包含第一组分的纤维聚合物和第二组分,所述聚合物含有亲电基团或亲核基团,当所述片暴露于与生物组织接触的水性介质时,所述第二组分能够交联所述第一组分以形成交联水凝胶,所述交联水凝胶粘附至所述生物组织;其中第二组分是纤维聚合物,并且如果第一组分含有亲核基团,则所述第二组分含有亲电基团,或者如果第一组分含有亲电基团,则所述第二组分含有亲核基团;或者
13.第二组分是第一组分的纤维聚合物上的涂层,其中如果第一组分含有亲核基团,则所述涂层含有亲电基团,或者如果第一组分含有亲电基团,则所述涂层含有亲核基团;或者
14.第二组分是分散和截留在第一组分的纤维聚合物的间隙内的干燥粉末,其中如果第一组分含有亲核基团,则所述粉末含有亲电基团,或者如果第一组分含有亲电基团,则所述粉末含有亲核基团。
15.wo 2011/124640描述了制造止血海绵的方法,其包括:
16.a)提供包含干燥形式的生物材料基质的海绵,
17.b)提供干燥粉末形式的一种反应性聚合材料,
18.c)使a)和b)接触,使得b)的材料存在于所述海绵的至少一个表面上,以及
19.d)将b)的材料固定在a)的海绵上。
20.固定可以通过熔化足够长的时间段来实现。
21.wo 2012/057628描述了包含至少1重量%亲电活化聚噁唑啉(el-pox)的干物质的组织粘附性医疗产品,所述el-pox包含至少2个反应性亲电基团,包括至少一个侧基亲电基团。除了el-pox之外,医疗产品可以包含亲核活化的聚噁唑啉(nu-pox)。组织粘附性产品的实例包括粘附组织带、组织密封剂、止血多孔材料和植入物。
22.wo 2016/056901描述了粘附剂止血产品,其选自经涂覆的网、经涂覆的泡沫或经涂覆的粉末,所述止血产品包含:
23.·
多孔固体基材,其具有至少5vol.%的孔隙率并且包括外表面,所述外表面包含含有反应性亲核基团的亲核聚合物;
24.·
覆盖固体基材的至少一部分的粘附性涂层,所述涂层包含亲电活化的聚噁唑啉(el-pox),所述el-pox平均包含至少1个反应性亲电基团。
25.粘附性止血产品通过包括以下步骤的方法生产:提供多孔固体基材;用包含el-pox和溶剂的涂覆液涂覆基材;以及去除溶剂。
26.us 6,733,845描述了用粉末静电浸渍到纤维状或丝状网络中的方法,用于生产包括刚性或柔性基质的复合材料,所述网络与所述刚性或柔性基质紧密接触,其中所述粉末和所述纤维或丝的网络置于两个电极之间,所述电极彼此电绝缘,并且所述电极分别连接到ac电压静电发生器的带相反电荷的极,以便同时使位于所述电极之间的所述粉末和所述纤维状或丝状网络经受静电场,其ac电压为至少5kv,持续至少2秒的时间。
技术实现要素:
27.本发明人已经开发了用于制备组织粘附片的方法,所述组织粘附片可以在外科手术程序期间适当地用作可植入的止血或密封构建物。
28.本方法包括:
29.·
提供包括三维互连间隙空间的纤维片;
30.·
提供反应性聚合物颗粒,所述反应性聚合物颗粒包含携带至少3个反应性亲电基团的水溶性亲电聚合物,所述反应性亲电基团能够在形成共价键的情况下与血液中的胺基团反应;
31.·
将所述纤维片和所述反应性聚合物颗粒置于两个电极之间;
32.·
同时使所述纤维片和所述反应性聚合物颗粒经受0.1至40kv/mm的电场以用所述反应性聚合物颗粒浸渍所述纤维片的互连间隙空间。
33.当血液进入间隙空间时,血液被本发明的组织粘附片吸收,片内的反应性聚合物颗粒一旦被血液“润湿”就开始溶解,从而允许亲电聚合物与血液和组织中的反应性亲核基团反应,导致血液凝固和组织密封,这两者均有助于止血。含有反应性聚合物颗粒的纤维片的止血性能受益于反应性聚合物颗粒在纤维片内的“深度”浸渍和均匀分布。本发明的方法可以实现这两个目的。
34.此外,本方法提供的优点在于,与用液体浸渍不同,它不影响纤维片的结构完整性或机械性能。此外,与使用摇动或振动的机械浸渍方法相比,本发明的方法不施加机械应力并实现更有效的浸渍,特别是对非常小(《100μm)的反应性聚合物颗粒。
35.本发明的另一方面涉及通过本方法获得的组织粘附片。
具体实施方式
36.本发明的第一方面涉及制备组织粘附片的方法,所述方法包括:
37.·
提供包括三维互连间隙空间的纤维片;
38.·
提供反应性聚合物颗粒,所述反应性聚合物颗粒包含携带至少3个反应性亲电基团的水溶性亲电聚合物,所述反应性亲电基团能够在形成共价键的情况下与血液中的胺基团反应;
39.·
将纤维片和反应性聚合物颗粒置于两个电极之间;
40.·
同时使纤维片和反应性聚合物颗粒经受0.1至40kv/mm的电场以用反应性聚合物颗粒浸渍纤维片的互连间隙空间。
41.如本文使用的术语“组织粘附性”是指组织粘附片由于在片与组织之间形成共价键而附着至组织的能力。这些共价键的形成通常需要水的存在。
42.如本文使用的术语“间隙空间”是指纤维片内的空隙(“空的”)空间。纤维片内的间隙空间允许将反应性聚合物颗粒引入片中。而且,血液和其它体液可以进入间隙空间,允许反应性聚合物颗粒内的水溶性亲电聚合物溶解。
43.根据本发明使用的“携带反应性亲电基团的水溶性亲电聚合物”携带能够在形成共价键的情况下与组织和血液中的胺基团反应的至少三个反应性基团。该水溶性亲电聚合物具有至少1kda的分子量和至少50g/l的在20℃的蒸馏水中的溶解度。
44.如本文使用的术语“吸水能力”是组织粘附片吸收水的能力的量度。通过以下方法测定吸水能力:称量干燥片的样品(重量=wd),然后将样品浸入蒸馏水(37℃),持续45分钟。然后,将样品从水中取出,并去除附着在基材外部的水,然后再次称量样品(重量=ww)。吸水能力=100%x(w
w-wd)/wd。吸水能力表示基材的孔隙率以及其在水的存在下溶胀的能力。
45.如本文使用的术语“胶原”是指动物体内各种结缔组织的细胞外间隙中的主要结构蛋白。胶原形成三条多肽链的特征性三螺旋。根据矿化程度,胶原组织可以是刚性的(骨)或顺应性的(腱)或具有从刚性至顺应性的梯度(软骨)。除非另外说明,术语“胶原”也包括明胶以外的改性胶原。
46.如本文使用的术语“明胶”是指通过从诸如家养的牛、鸡、猪和鱼的动物的皮肤、骨和结缔组织提取的胶原的部分水解产生的肽和蛋白质的混合物。在水解期间,各胶原链之间的天然分子键被分解成更容易重排的形式。
47.如本文使用的术语“聚噁唑啉”是指聚(n-酰基亚烷基亚胺)或聚(芳酰基亚烷基亚胺),并且还被称为pox。pox的实例是聚(2-乙基-2-噁唑啉)。术语“聚噁唑啉”也包括pox共聚物。
48.反应性聚合物颗粒可以均匀地分布在纤维片的间隙空间内,这意味着颗粒密度在整个片中基本上相同。反应性聚合物颗粒可以在片的整个厚度上不均匀地分布。对于某些
应用,如果反应性聚合物颗粒的密度显示出梯度,则可能是有利的,例如,反应性聚合物颗粒的密度在旨在应用于出血伤口的片的一侧附近最低,并且在片的另一侧附近最高。
49.反应性聚合物颗粒的直径分布可以适当地通过使用malvern mastersizer 2000结合不锈钢样品分散单元的激光衍射来测定。样品分散单元填充有约120ml的环己烷,其在1800rpm的搅拌速度下稳定5至10分钟,随后进行背景测量(空白测量)。摇动样品管并水平转动20次。然后,将约50mg分散在含有环己烷的样品分散单元中。在将样品引入分散单元之后,在进行测量之前,将样品在1800rpm下搅拌1.5分钟以确保所有颗粒被适当地分散。对分散的颗粒不进行超声处理。平均粒度表示为d[4,3],体积加权平均直径表示为(σnidi4)/(σnidi3)。
[0050]
在优选实施方案中,本方法包括用5至90%,更优选10至80%,甚至更优选20至75%,最优选50至70%的反应性聚合物颗粒浸渍纤维片,所述百分比按纤维片的重量计。
[0051]
根据特别优选的实施方案,本发明的组织粘附片是生物可吸收的,意味着该片、反应性聚合物颗粒和组织粘附片的任何其它组分最终被吸收在体内。片和反应性聚合物颗粒的吸收通常需要包含在其中的聚合物的化学分解(例如水解)。人体对组织粘附片的完全生物吸收通常在1至10周内,优选在2至8周内实现。
[0052]
本发明的组织粘附片优选是无菌的。
[0053]
本发明的组织粘附片通常具有0.5至25mm的非压缩平均厚度。更优选地,非压缩平均厚度为1至10mm,最优选1.5至5mm。
[0054]
组织粘附片优选具有小于200mg/cm3,更优选小于150mg/cm3,最优选10至100mg/cm3的非压缩密度。
[0055]
本发明的组织粘附片优选基本上是无水的。通常,组织粘附片的水含量不超过5wt.%,更优选不超过2wt.%,最优选不超过1wt.%。
[0056]
组织粘附片的吸水能力优选为至少50%,更优选100%至800%,最优选200%至500%。
[0057]
本方法中使用的纤维片优选是耐水性的,即该片不是水溶性的,并且在中性ph条件(ph7)和37℃的温度下不会在水中崩解。
[0058]
纤维片中的纤维优选具有1至500μm,更优选2至300μm,最优选5至200μm的平均直径。纤维的平均直径可以适当地使用显微镜来确定。
[0059]
典型地,纤维片中的至少50wt.%,更优选至少80wt.%的纤维具有1至300μm的直径和至少1mm的长度。
[0060]
优选地,纤维片中的至少50wt.%,更优选至少80wt.%的纤维具有至少1000的纵横比(长度与直径的比率)。
[0061]
纤维片优选包含至少50wt.%,更优选至少80wt.%,最优选至少90wt.%的含有明胶、胶原、纤维素、改性纤维、羧甲基葡聚糖、plga、透明质酸钠/羧甲基纤维素、聚乙烯醇、壳聚糖或其组合的纤维。
[0062]
在本发明的实施方案中,纤维状载体结构不包含氧化的再生纤维素。
[0063]
优选的纤维片具有开孔结构,其对空气的渗透率为至少0.1l/min
×
cm2,更优选至少0.5l/min
×
cm2。根据en iso 9237:1995(纺织品-织物对空气的渗透率的测定)测定空气渗透率。
[0064]
纤维片中的纤维可以通过本领域已知的方法生产,例如电纺、电吹纺和高速旋转喷雾器纺丝。us 2015/0010612中描述了通过高速旋转喷雾器纺丝生产纤维片。也可以使用市售的止血纤维片作为纤维片。
[0065]
本发明方法中使用的反应性聚合物颗粒优选含有至少10wt.%的水溶性亲电聚合物。更优选地,反应性聚合物颗粒含有至少50wt.%,更优选至少90wt.%的水溶性亲电聚合物。
[0066]
本发明方法提供的优点在于,与使用振动或摇动的浸渍技术不同,它可以将非常小的反应性聚合物颗粒有效地分布到纤维片中。这对于小颗粒是有利的,因为表面积/体积比高,溶解快于较大颗粒。因此,含有非常小的反应性聚合物颗粒的组织粘附片的止血性能通常优于含有较大反应性聚合物颗粒的组织粘附片。因此,在非常优选的实施方案中,反应性聚合物颗粒的体积加权平均直径(d[4,3],(∑nid4)/(∑nid3))为10至100μm,更优选15至80μm,最优选20至70μm。
[0067]
根据特别优选的实施方案,至少80vol.%的反应性聚合物颗粒的直径为5至200μm,更优选10至120μm,最优选12至100μm。
[0068]
本发明的反应性聚合物颗粒可以以各种方式制备,例如通过研磨,通过喷雾干燥聚合物溶液,通过冷冻干燥,通过喷雾冷却聚合物熔体,通过造粒粉末混合物,或者通过流化床涂覆。
[0069]
包含在反应性聚合物颗粒中的水溶性亲电聚合物的分子量通常为至少2kda,更优选至少5kda,最优选10至100kda。
[0070]
水溶性亲电聚合物在20℃的蒸馏水中的溶解度优选为至少100g/l,更优选至少200g/l。
[0071]
根据本发明使用的水溶性亲电聚合物优选含有至少4个反应性亲电基团,更优选至少8个反应性亲电基团,甚至更优选至少16个反应性亲电基团,最优选至少32个反应性亲电基团。
[0072]
存在于反应性聚合物颗粒中的水溶性亲电聚合物优选选自聚噁唑啉、聚乙二醇、聚乙烯吡咯烷酮、聚氨基甲酸酯(例如,如wo2017/171551中所述)及其组合。甚至更优选地,亲电聚合物选自聚噁唑啉、聚乙二醇及其组合。最优选地,亲电聚合物是聚噁唑啉。
[0073]
包含反应性亲电基团的聚噁唑啉优选衍生自其重复单元由下式(i)表示的聚噁唑啉:
[0074]
(chr1)mncor2[0075]
其中r2和每个r1独立地选自h、任选取代的c
1-22
烷基、任选取代的环烷基、任选取代的芳烷基、任选取代的芳基;并且m是2或3。
[0076]
优选地,式(i)中的r1和r2选自h和c
1-8
烷基,甚至更优选选自h和c
1-4
烷基。r1最优选为h。式(i)中的整数m优选等于2。
[0077]
根据优选实施方案,聚噁唑啉是聚合物,甚至更优选是2-烷基-2-噁唑啉的均聚物,所述2-烷基-2-噁唑啉选自2-甲基-2-噁唑啉、2-乙基-2-噁唑啉、2-丙基-2-噁唑啉、2-丁基-2-噁唑啉及其组合。优选地,聚噁唑啉是2-丙基-2-噁唑啉或2-乙基-噁唑啉的均聚物。最优选地,聚噁唑啉是2-乙基-噁唑啉的均聚物。
[0078]
根据特别优选的实施方案,水溶性亲电聚合物包含至少20个噁唑啉单元,更优选
至少30个噁唑啉单元,最优选至少80个噁唑啉单元。亲电聚合物优选包含每个噁唑啉残基平均至少0.05个反应性亲电基团。甚至更优选地,亲电聚合物包含每个噁唑啉残基平均至少0.1个反应性亲电基团。最优选地,亲电聚合物包含每个噁唑啉残基平均0.12至0.5个反应性亲电基团。
[0079]
水溶性亲电聚合物通常平均携带至少10个,更优选至少20个反应性亲电基团。
[0080]
聚噁唑啉可以在其侧链中携带反应性亲电基团(侧基反应性亲电基团),在其末端处携带反应性亲电基团,或在其侧链和末端携带反应性亲电基团。根据本发明使用的聚噁唑啉有利地包含一个或多个侧基反应性亲电基团。通常,聚噁唑啉含有每个单体0.03至0.5个侧基反应性亲电基团,更优选含有每个单体0.04至0.35个侧基反应性亲电基团,甚至更优选含有每个单体0.05至0.25个侧基反应性亲电基团。
[0081]
根据本发明应用的包含反应性亲电基团的聚乙二醇(peg)优选是多臂peg或星形peg,其包含至少3个臂,更优选至少4个臂,所述臂用反应性亲电基团封端。
[0082]
组织粘附片中的反应性聚合物颗粒优选包含携带反应性亲电基团的水溶性亲电聚合物,所述反应性亲电基团选自羧酸酯、磺酸酯、膦酸酯、五氟苯基酯、对硝基苯基酯、对硝基噻吩基酯、酰卤基团、酸酐、酮、醛、异氰酸根合、硫代异氰酸根合、异氰基、环氧化物、活化羟基基团、烯烃、缩水甘油醚、羧基、琥珀酰亚胺基酯、磺基琥珀酰亚胺基酯、马来酰亚氨基(马来酰亚胺基)、乙烯磺酰基、酰亚氨基酯、乙酰乙酸酯、卤代缩醛、邻二硫吡啶、二羟基-苯基衍生物、乙烯基、丙烯酸酯、丙烯酰胺、碘乙酰胺及其组合。更优选地,反应性亲电基团选自羧酸酯、磺酸酯、膦酸酯、五氟苯基酯、对硝基苯基酯、对硝基噻吩基酯、酰卤基团、酸酐、酮、醛、异氰酸根合、硫代异氰酸根合、异氰基、环氧化物、活化羟基基团、缩水甘油醚、羧基、琥珀酰亚胺基酯、磺基琥珀酰亚胺基酯、酰亚氨基酯、二羟基-苯基衍生物及其组合。甚至更优选地,反应性亲电基团选自卤代缩醛、邻二硫吡啶、马来酰亚胺、乙烯砜、二羟基苯基衍生物、乙烯基、丙烯酸酯、丙烯酰胺、碘乙酰胺、琥珀酰亚胺基酯及其组合。最优选地,反应性亲电基团选自马来酰亚胺、乙烯基、丙烯酸酯、丙烯酰胺、琥珀酰亚胺基酯、磺基琥珀酰亚胺基酯及其组合。
[0083]
可使用的琥珀酰亚胺基酯的实例包括琥珀酰亚胺基戊二酸酯、琥珀酰亚胺基丙酸酯、琥珀酰亚胺基琥珀酰胺、琥珀酰亚胺基碳酸酯、二琥珀酰亚胺基辛二酸酯、双(磺基琥珀酰亚胺基)辛二酸酯、二硫代双(琥珀酰亚胺基丙酸酯)、双(2-琥珀酰亚氨基氧基羰氧基)乙基砜、3,3'-二硫代双(磺基琥珀酰亚胺基丙酸酯)、琥珀酰亚胺基氨基甲酸酯、磺基琥珀酰亚胺基(4-碘乙酰基)氨基苯甲酸酯、双(磺基琥珀酰亚胺基)辛二酸酯、磺基琥珀酰亚胺基-4-(n-马来酰亚氨基甲基)-环己烷-1-甲酸酯、二硫代双-磺基琥珀酰亚胺基丙酸酯、二磺基琥珀酰亚胺基酒石酸酯;双[2-(磺基-琥珀酰亚胺基氧羰基氧乙基砜)]、乙二醇双(磺基琥珀酰亚胺基琥珀酸酯)、二硫代双(琥珀酰亚胺基丙酸酯)。
[0084]
可以使用的二羟基苯基衍生物的实例包括二羟基苯基丙氨酸、3,4-二羟基苯基丙氨酸(dopa)、多巴胺、3,4-二羟基氢化肉桂酸(doha)、去甲肾上腺素、肾上腺素和儿茶酚。
[0085]
在本发明的有利实施方案中,除了水溶性亲电聚合物之外,反应性聚合物颗粒还包含亲核交联剂,所述亲核交联剂包含至少两个反应性亲核基团,所述亲核基团能够在形成共价键的情况下与水溶性亲电聚合物的反应性亲电基团反应。亲核交联剂的引入提供了以下优点:可以改善片的止血和粘附性能,因为当血液进入片时水溶性亲电聚合物将与亲
核交联剂反应。这种交联反应将导致形成固定血流的水凝胶,并且由于水凝胶中的反应性亲电基团与组织中的胺/硫醇基团之间形成共价键,这种水凝胶将粘附到组织上。通过将水溶性亲电聚合物和亲核交联剂组合在单个颗粒中,确保了这两种反应性组分可以均匀地分布在整个止血片中,在运输和处理期间不发生分离,并且当颗粒与血液接触时这些组分可以彼此立即反应。
[0086]
含有携带反应性亲电基团的水溶性聚合物和亲核交联剂的组合的反应性聚合物颗粒(即反应性杂化颗粒)可以经由湿法制粒和随后干燥(优选在减压下)来生产。应选择粒化液体,使得在水溶性亲电聚合物与亲核交联剂之间的粒化期间很少或不发生反应。这可以例如通过使用这两种组分中的至少一种不溶于其中的粒化液体来实现。最优选地,携带反应性亲电基团的水溶性聚合物不溶于粒化液体。
[0087]
根据特别优选的实施方案,反应性聚合物颗粒是颗粒附聚物,其包含:(i)含有水溶性亲电聚合物的亲电颗粒;以及(ii)含有亲核交联剂的亲核颗粒。
[0088]
亲电颗粒优选含有至少30wt.%,更优选至少50wt.%,最优选至少80wt.%的水溶性亲电聚合物。
[0089]
亲核颗粒优选含有至少30wt.%,更优选至少50wt.%,最优选至少80wt.%的亲核交联剂。
[0090]
亲核交联剂优选含有至少3个反应性亲核基团。亲核交联剂的反应性亲核基团优选选自胺基团、硫醇基团及其组合。更优选地,这些反应性亲核基团是胺基团。根据优选实施方案,亲核交联剂中存在的反应性亲核基团是伯胺基团。
[0091]
优选地,亲核交联剂选自蛋白质、壳聚糖、携带反应性亲核基团的合成聚合物、携带反应性亲核基团的碳水化合物聚合物及其组合。甚至更优选地,亲核交联剂选自明胶、胶原、壳聚糖及其组合。
[0092]
在本发明方法中,纤维片和反应性聚合物颗粒优选同时经受0.5至30kv/mm的电场,更优选经受1至10kv/mm的电场。
[0093]
根据特别优选的实施方案,纤维片和反应性聚合物颗粒同时经受交变电场。优选地,电场以至少10s-1
的频率交替,更优选以至少50s-1
的频率交替,最优选以100s-1
的频率交替。
[0094]
在本发明方法中,通过产生与纤维片相邻的反应性聚合物颗粒层和通过将纤维片和相邻的反应性聚合物颗粒层置于两个电极之间,可以有效地实现纤维片的浸渍。浸渍还可以通过产生包含由反应性聚合物颗粒层分开的两个或更多个纤维片的层叠体以及通过将该层叠体置于两个电极之间来实现。
[0095]
在本方法的优选实施方案中,将纤维片和反应性聚合物颗粒放置在下电极与上电极之间,这些电极通过电介质彼此电绝缘并且连接到ac发电机的相应极,以便同时使纤维片和反应性聚合物颗粒经受电场。
[0096]
纤维片和反应性聚合物颗粒优选在下电极与上电极之间通过,同时使纤维片和反应性聚合物颗粒经受电场。因此,可以通过本发明的方法以半连续的方式用反应性聚合物颗粒适当地浸渍一卷纤维片。
[0097]
在优选实施方案中,纤维片和反应性聚合物颗粒同时暴露于电场持续至少0.1秒,更优选至少5秒,最优选至少30秒。
[0098]
本发明的另一方面涉及通过本文以上所述的方法获得的组织粘附片。
[0099]
通过以下非限制性实施例进一步说明本发明。
[0100]
实施例
[0101]
通常:在任何未明确提及干燥后(在干燥粉末、颗粒和/或纤维片中)的残余水分含量之处,水平低于2.0%w/w。
[0102]
具有40μm或更小的d[4,3]的粉末通过研磨,随后经250目筛(haver和boecker,序列号47181315)筛分来生产。再次研磨未通过筛的颗粒并再次筛分直到所有粉末均低于250目。
[0103]
水溶性亲电聚合物(nhs-pox)的制备
[0104]
含有20%nhs-酯基团的nhs侧链活化的聚[2-(乙基/羟基-乙基-酰胺-乙基/nhs-酯-乙基-酯-乙基-酰胺-乙基)-2-噁唑啉]三元共聚物(=el-pox,20%nhs)如下合成:
[0105]
使用60%2-乙基-2-噁唑啉(etox)和40%2-甲氧基羰基-乙基-2-噁唑啉(mestox)通过crop合成聚[2-(乙基/甲氧基-羰基-乙基)-2-噁唑啉]共聚物(dp= /-100)。获得含有40%2-甲氧基羰基-乙基基团的统计共聚物(1h-nmr)。其次,含有40%2-甲氧基羰基-乙基基团的聚合物与乙醇胺反应,得到具有40%2-羟基-乙基-酰胺-乙基基团的共聚物(1h-nmr)。此后,根据1h-nmr,使一半的2-羟基-乙基-酰胺-乙基基团与琥珀酸酐反应,得到具有60%2-乙基基团、20%2-羟基-乙基-酰胺-乙基基团和20%2-羧基-乙基-酯-乙基-酰胺-乙基基团的三元共聚物。最后,用n-羟基琥珀酰亚胺(nhs)和二异丙基碳二亚胺(dic)活化2-羧基-乙基-酯-乙基-酰胺-乙基基团,得到el-pox,20%nhs。根据1h-nmr,nhs-pox含有20%nhs-酯基团。将nhs-pox在2℃至8℃下溶解在水中(60g在300ml中),在-80℃冷却半小时并冷冻干燥。将如此获得的冷冻干燥的粉末在旋转蒸发器中在40℃下干燥直至通过karl fischer滴定测定的水含量低于0.8%w/w。使用具有12齿推入配合转子组合具有0.25mm的梯形孔的距离筛的retsch ultra centrifugal mill zm 200研磨该干燥(白色)粉末,直至平均粒度不超过35μm(d[4,3]),或者使用台式咖啡研磨机研磨这种干燥(白色)粉末,直至平均粒度为约70μm(d[4,3]),并且真空密封在alu-alu袋中。
[0106]
nhs-pox粉末的染色
[0107]
将20g的nhs-pox粉末溶解在水中,并且使用高性能分散仪器(ultra-turrax,ika)与50mg brilliant blue fcf(sigma aldrich)混合。在混合(2分钟)后立即将溶液在-78℃下冷冻,随后冷冻干燥过夜。将如此获得的冷冻干燥的粉末在旋转蒸发器中在40℃下干燥直至通过karl fischer滴定测定的残余水含量低于0.8%w/w。然后,使用retsch ultra centrifugal mill zm 200研磨干燥的(蓝色)粉末,直至蓝色染色的nhs-pox粉末具有不超过35μm(d[4,3])的平均粒度,并且真空密封在alu-alu袋中。
[0108]
亲核交联剂(nu-pox)的制备
[0109]
通过etox和mestox的crop合成在烷基侧链中含有乙基和胺基团的聚噁唑啉,随后用乙二胺对甲基酯侧链进行酰胺化以得到聚(2-乙基/氨基乙基酰氨基乙基-2-噁唑啉)共聚物(nu-pox)。根据1h-nmr,nu-pox含有10%nh2。将nu-pox在2℃至8℃下溶解在水中(60g在300ml中),在-80℃冷却半小时并冷冻干燥。将如此获得的冷冻干燥的粉末在旋转蒸发器中在40℃下干燥直至通过karl fischer滴定测定的水含量低于0.8%w/w。使用retsch ultra centrifugal mill zm 200研磨干燥粉末,直至平均粒度不超过35μm(d[4,3]),并且真空密
封在alu-alu袋中。
[0110]
反应性聚合物颗粒(nhs-pox/nu-pox颗粒)的制备
[0111]
在高剪切混合器中用异丙醇(ipa)润湿蓝色或白色(未染色的)nhs-pox粉末,直至获得含有约1至2%w/w ipa的均匀雪花状粉末。此后,添加nu-pox粉末并且混合。将润湿的蓝色nhs-pox粉末与nu-pox粉末以1:1的摩尔比混合,所述摩尔比是指由nhs-pox提供的nhs基团的数量与由nu-pox提供的胺基团的数量的比率。
[0112]
混合后,将湿颗粒在减压下干燥直至ipa含量小于0.1%w/w,如经由1h-nmr测定的。使用retsch ultra centrifugal mill zm 200研磨干燥的颗粒,直至平均粒度不超过50μm或35μm(d[4,3]),并且真空密封在alu-alu袋中。
[0113]
使用1h-nmr光谱分析nhs-pox/nu-pox颗粒(1:1)。将25mg的颗粒通过超声20分钟溶解在三氟乙酸(0.20ml)中。在颗粒完全溶解后,用含有马来酸(2.5mg/ml)作为内标的氘化二甲亚砜(dmso-d6)(0.80ml)稀释样品,转移至nmr管并且记录1h-nmr光谱。
[0114]
根据获得的光谱,可以计算与nhs-pox结合的nhs的量,以及颗粒中存在的nhs和胺基团的摩尔比。颗粒中与nhs-pox结合的nhs的量等于与nhs-pox起始材料结合的nhs的量,表明在粒化期间没有衰减或交联。
[0115]
使用已知量的内标(马来酸)和由不同浓度的nhs-pox和nu-pox记录的1h-nmr光谱构建的校准曲线测定nmr样品中的总聚合物回收率,即nhs-pox和nu-pox的组合。测得总聚合物回收率为99%,表明没有形成不溶性交联材料。
[0116]
通过尺寸排阻色谱法进一步分析nhs-pox/nu-pox颗粒(1:1)。将20mg的颗粒用乙酸酐(1.00ml)在50℃下处理1小时。随后,添加甲醇(2.00ml),并且将混合物在50℃下再搅拌1小时。取等分试样(0.75ml),并且在减压下去除所有挥发物。将样品吸收在含有50mm氯化锂的n,n-二甲基乙酰胺(2.50ml)中,其为用于sec分析的洗脱液。相对于聚(甲基丙烯酸甲酯)标准物测量sec,并且根据获得的尺寸排阻色谱图确定mn、mw和pdi。pdi不超过1.5,表明在粒化期间没有发生交联。该尺寸排阻色谱方法的分析验证表明0.05mol%水平的nhs-pox与nu-pox的有意交联将pdi增加至超过2.5。
[0117]
反应性聚合物颗粒(nhs-pox/nu-pox/p188颗粒)的制备
[0118]
如前所述制备反应性nhs-pox/nu-pox颗粒。随后,通过在高剪切混合器中在65℃下将nhs-pox/nu-pox颗粒与p188粉末一起加热10分钟,然后冷却至环境条件来制备1.5%、2.5%、3.5%、5%和10%w/w p188涂覆的反应性nhs-pox/nu-pox颗粒。使用retsch ultra centrifugal mill zm 200研磨涂覆的颗粒,直至平均粒度不超过40μm(d[4,3]),并且真空密封在alu-alu袋中。
[0119]
如此获得的颗粒的粒度分布为约:90vol.%《80μm,50vol.%《40μm并且10vol.%《10μm。
[0120]
使用1h-nmr光谱分析nhs-pox/nu-pox/p188颗粒。将25mg的粉末通过超声20分钟溶解在三氟乙酸(0.20ml)中。在颗粒完全溶解后,用氘化二甲亚砜(dmso-d6)(0.80ml)稀释样品,转移至nmr管并且记录1h-nmr光谱。根据获得的光谱,与nhs-pox相比计算未反应的nhs的量为98%。
[0121]
通过尺寸排阻色谱法进一步分析nhs-pox/nu-pox/p188颗粒。将20mg的颗粒用乙酸酐(1.00ml)在50℃下处理1小时。随后,添加甲醇(2.00ml),并且将混合物在50℃下再搅
拌1小时。取等分试样(0.75ml),并且在减压下去除所有挥发物。将样品吸收在含有50mm氯化锂的n,n-二甲基乙酰胺(2.50ml)中,其为用于sec分析的洗脱液。相对于聚(甲基丙烯酸甲酯)标准物测量sec,并且从获得的尺寸排阻色谱图确定mn、mw和pdi。pdi不超过1.5,表明在粒化期间没有发生交联。
[0122]
反应性聚合物颗粒(nhs-pox/gelita spon颗粒)的制备使用高剪切混合器在20,000rpm下操作20分钟,将水含量小于0.2%w/w的7.01g的预干燥明胶粉末(购自gelitamedical gmbh)分散在二氯甲烷(200ml)中。随后,添加nhs-pox(7.02g)并且继续搅拌5分钟。nhs-pox不溶解。在减压下从悬浮液中去除所有挥发物。使用咖啡研磨机研磨获得的粉末直至平均粒度不超过95μm(d[4,3])并且真空密封在alu-alu袋中,进一步在减压下干燥并且真空密封在alu-alu袋中。
[0123]
如此获得的颗粒的粒度分布为约:90vol.%《190μm,50vol.%《80μm并且10vol.%《15μm。
[0124]
通过1h-nmr光谱分析来分析颗粒。为此,将含有5%(v/v)乙酸的氘化氯仿(cdcl3)(1.0ml)添加至25mg的颗粒中。通过超声处理样品20分钟选择性地提取nhs-pox。使分散体通过0.22μm过滤器,转移至nmr管并且记录1h-nmr光谱。根据获得的光谱,与nhs-pox相比计算未反应的nhs的量为97%。
[0125]
通过尺寸排阻色谱(sec)分析进一步分析颗粒。将上述过滤的nhs-pox提取物的等分试样(0.15ml)用含有50mm氯化锂的n,n-二甲基乙酰胺(1.00ml)稀释,其为用于sec分析的洗脱液。通过sec对聚(甲基丙烯酸甲酯)标准物分析样品,并且pdi为1.45,表明没有发生交联。
[0126]
反应性聚合物颗粒(nhs-pox/nu-pox/peg 3000颗粒)的制备
[0127]
如前所述制备反应性nhs-pox/nu-pox颗粒。随后,通过将nhs-pox/nu-pox颗粒与peg(mw 3kda)粉末一起在高剪切混合器中在65℃加热10分钟,然后冷却至环境条件,制备5%和10%w/w peg 3000涂覆的反应性nhs-pox/nu-pox颗粒。使用retsch ultra centrifugal mill zm 200研磨涂覆的颗粒,并且真空密封在alu-alu袋中。
[0128]
使用1h-nmr光谱分析nhs-pox/nu-pox/peg 3000颗粒。将25mg的粉末通过超声20分钟溶解在三氟乙酸(0.20ml)中。在颗粒完全溶解后,用氘化二甲亚砜(dmso-d6)(0.80ml)稀释样品,转移至nmr管中并且记录1h-nmr光谱。根据获得的光谱,与nhs-pox相比计算未反应的nhs的量为96%。
[0129]
通过尺寸排阻色谱法进一步分析nhs-pox/nu-pox/peg颗粒。将20mg的颗粒用乙酸酐(1.00ml)在50℃下处理1小时。随后,添加甲醇(2.00ml),并且将混合物在50℃下再搅拌1小时。取等分试样(0.75ml),并在减压下去除所有挥发物。将样品吸收在含有50mm氯化锂的n,n-二甲基乙酰胺(2.50ml)中,其为用于sec分析的洗脱液。相对于聚(甲基丙烯酸甲酯)标准物测量sec,并且根据获得的尺寸排阻色谱图确定mn、mw和pdi。pdi不超过1.5,表明在粒化期间没有发生交联。
[0130]
反应性聚合物颗粒(nhs-pox/nu-peg)的制备
[0131]
通过将nhs-pox(d[4,3]≤35μm)与peg二胺(mw 10kda)粉末一起在高剪切混合器中在65℃加热10分钟,然后冷却至环境条件,制备5%w/w nu-peg涂覆的nhs-pox。使用retsch ultra centrifugal mill zm 200研磨涂覆的颗粒,并且真空密封在alu-alu袋中。
[0132]
使用1h-nmr光谱分析nhs-pox/nu-peg反应性聚合物颗粒。将25mg的粉末通过超声20分钟溶解在三氟乙酸(0.20ml)中。在颗粒完全溶解后,用氘化二甲亚砜(dmso-d6)(0.80ml)稀释样品,转移至nmr管中并且记录1h-nmr光谱。根据获得的光谱,与nhs-pox相比计算未反应的nhs的量为95%。
[0133]
通过尺寸排阻色谱法进一步分析nhs-pox/nu-peg反应性聚合物颗粒。将20mg的粉末用乙酸酐(1.00ml)在50℃下处理1小时。随后,添加甲醇(2.00ml),并且将混合物在50℃下再搅拌1小时。取等分试样(0.75ml),并在减压下去除所有挥发物。将样品吸收在含有50mm氯化锂的n,n-二甲基乙酰胺(2.50ml)中,其为用于sec分析的洗脱液。相对于聚(甲基丙烯酸甲酯)标准物测量sec,并且根据获得的尺寸排阻色谱图确定mn、mw和pdi。pdi不超过1.5,表明在粒化期间没有发生交联。
[0134]
纤维片
[0135]
选择以下可商购的止血产品用作在根据本发明制备组织粘附片中的纤维片:
[0136]
·
gelita由八层减少交联的凝胶泡沫纤维组成的粘性纤维片。每层约2mm厚度的八个层具有50mm
×
75mm的尺寸。gelita的水含量不超过15%。将产物在真空烘箱中在40℃下干燥数小时以将水含量降低至不超过2.0%w/w(通过重量分析法测定),然后将其用附聚物颗粒进行浸渍。
[0137]
·
snow
tm
:由通过再生纤维素(orc)的受控氧化制备的可吸收的非织造织物组成的粘性纤维片。尺寸为5.1cm
×
10.2cm,水含量不超过2.0%w/w
[0138]
·
snow
tm-hybrid:通过再生纤维素(orc)的受控氧化制备的纤维的致密编织可吸收织物,其以若干尺寸(例如,15.2cm
×
22.9cm)缝合到snow
tm
上,切割成5.1cm
×
10.2cm的尺寸。
[0139]
·
pem:如下制备由氧化的再生纤维素(orc)和polyglactin 910组成的粘性纤维片,其尺寸(长度,宽度)为97.0至102.5mm,厚度为1.40至2.50mm。将聚(乙交酯-共-丙交酯)(pgl,90/10mol/mol)熔纺成纤维。将80旦尼尔复丝纱线固结成800旦尼尔固结的纱线。将固结的纱线在约110℃下卷曲。将卷曲的纱线切成长度为约1.25”的短纤维。精确称量20g的卷曲的短纤维并且均匀地放置在多辊梳理机的进料传送带上。控制环境条件(温度:21℃/55%rh)。然后对短纤维进行梳理以产生非织造絮。将絮从拾取辊上取下并切成4个相等的部分。将它们重新送入垂直于收集方向的梳理机。在第二次通过之后,将絮称重(19.8g:99%织物产率),然后压实成毡。将压实的毡精确地铺在orc织物上,并通过针刺设备的2次通过牢固地连接。将多层织物修整并在3个离散的异丙醇浴中冲洗以去除纺丝整理剂和任何机油。将洗过的多层织物在烘箱中在70℃下干燥30分钟,冷却并称重。含水量不超过2.0%w/w
[0140]
浸渍方法
[0141]
机器
[0142]
fibroline sl-preg实验室机器通过以高达200hz的频率施加高达40kv的电压持续高达60秒的时间在电极之间移动颗粒。两个电极板具有约50
×
40cm的尺寸。顶板接地。
[0143]
使用以下标准设置:40kv,100hz,20至30秒。
[0144]
阵列
[0145]
在阵列已经安装到底部电极板上之后,将粉末通过重量计量配量到3d印刷的pmma阵列中。使用刮板纸盒或金属刮刀用反应性聚合物粉末填充阵列。阵列测量为50
×
75
×
4mm并且含有22
×
33=726个正方形孔(每个孔的内部尺寸:2
×2×
2mm)。726个孔的合并体积为约5.8ml。
[0146]
间隔物
[0147]
将间隔物遮盖物置于阵列的顶部。当经受交变电场时,间隔物用于允许颗粒上下移动。如果不使用间隔物,则通过载体的渗透和分布受到限制。
[0148]
对于不同的基材,需要不同的间隔物高度。对于tuft-it和snow,这是3mm的遮盖物。这导致电极的3 4mm=7mm的距离。对于nu-knit/snow-hybrid,这是1.5mm的遮盖物。这导致电极的1.5
±
4mm=5.5mm的距离
[0149]
出血实验
[0150]
使用标准化的离体和体内猪出血模型来评估止血功效。所有模型使用肝素将血液的凝固时间增加至活化凝固时间(act)的约2至3倍。
[0151]
离体模型:将来自屠宰场的肝素化新鲜血液灌注具有新鲜肝的活的离体猪模型,以尽可能接近地模拟真实的体内情况。将肝安装在灌注机上,通过灌注机进行氧合作用,将血液的ph、温度和血压保持在体内边界内。在屠宰场收集两个肝和10升肝素化血液(5000单位/l)。肝用冰运输;血液在环境温度下运输。在收集后2小时内,检查用手套和氰基丙烯酸酯胶封闭的肝的损伤。
[0152]
·
灌注参数:流速600ml/min;压力10至12mmhg;温度37℃( /-1℃);卡波原0.25升/分钟
[0153]
·
使用平的圆形旋转磨具,在肝表面上形成圆形出血伤口(8mm直径),使用橡胶上置物,使得穿孔出血的深度总是3mm
[0154]
·
在肝适当灌注(颜色和温度检查)后,根据以下程序测试样品:将样品切割成正确的尺寸(2.7
×
2.7cm);照相机打开;照相机上的位点数量;活检穿孔8mm;切下活组织;用纱布(2x)从出血中去除血液;在预称重的纱布中收集血液30秒;对出血进行评分(由2位研究人员评分);将样品用预润湿的纱布(盐水)放置在出血处上,并且在小压力下保持1分钟;观察5分钟(检查并评分粘附性和止血)并且在30分钟后重复。
[0155]
猪体内模型:在经麻醉的猪(家猪,雌性,体重范围:40kg,成年)中造成标准化组合的穿透性脾破裂。进行中线剖腹术以通达脾和其它器官。当使用该模型时,执行几种类型的外科手术程序:
[0156]
·
使用圆形活组织检查穿孔器,在肝和/或脾中形成囊下标准化损伤(0.8mm直径)。使用约2
×
2cm的测试制品以便覆盖损伤并施加手动压塞。
[0157]
·
使用手术刀,在肝和/或脾中形成囊下标准化损伤。使用标准技术切除所需的肝叶或脾的边缘,使切割的横截面表面暴露。使用7.5
×
5cm或10
×
5cm的测试制品以便覆盖切除表面并施加手动压塞。
[0158]
·
使用迟钝的和尖锐的解剖的组合来识别和隔离右肾和左肾。解剖右肾和左肾,允许用一只手抓住肾,并且用手术刀以切刀方式切除肾的尾极(约2.5
±
1cm直径乘以1
±
0.5cm深度)。在将测试制品应用于活动性出血部位之前,立即抽吸目标应用部位并清除血液。使用7.5
×
5cm或10
×
5cm的测试制品以便覆盖切除表面并应用手动压塞。在肾脏的颅极
中重复相同的程序。
[0159]
大鼠体内模型:使用100只雄性wistar(wu)大鼠,体重范围为270至300克。在手术前至少15分钟用0.02mg/kg丁丙诺啡皮下处理所有大鼠。通过吸入在加压空气和氧气的1:1混合物中的5%异氟烷在诱导室中进行诱导麻醉。维持剂量为3.5%异氟烷(也在加压空气和氧气的1:1混合物中),通过鼻部面具给药。通过剃刮、用碘和无菌覆盖物皮肤消毒制备大鼠。将大鼠固定在15度倾斜的桌子上,头部高于尾部(murakimi 2008)。用加热垫和灯将体温保持在38℃,然后使用严格无菌技术通过4至5cm中线剖腹术操作。腹部中线切开开腹,分离左外侧肝叶。将该叶放置在坚固的纸张上并进行切除。用手术刀切除肝叶的远端部分,距边缘约3mm。将一片贴片(15mm
×
25mm)轻轻地应用于左侧肝叶上的伤口周围,然后在1分钟内用湿纱布施加手动压塞。然后制备肝中叶的右侧部分,进行部分切除,并且以相同的方式应用相同尺寸的第二贴片。
[0160]
在本文所述的所有离体和体内程序中,通过预润湿的纱布(盐水)用温和的压力应用止血产品并保持1分钟。在应用产品后,对凝固和对组织的粘附性进行评分。
[0161]
用于贴片的评分体系:凝固
[0162]
在压塞后立即实现
[0163]
在压塞后《10秒实现
[0164]
在压塞后《30秒实现
[0165]
在压塞后3分钟内实现
[0166]
/-在3分钟后,应用第二次压塞实现
[0167]-未实现
[0168]
用于贴片的评分体系:应用后10分钟的粘附性
[0169]
非常强的粘附性(在移除时贴片断裂)
[0170]
强粘附性(在移除时贴片断裂)
[0171]
强粘附性(贴片可以在不断裂的情况下移除)
[0172]
中等粘附性(贴片可以在不断裂的情况下移除)
[0173]
/-轻微粘附性(贴片可以在不断裂的情况下移除)
[0174]-未实现
[0175]
实施例1
[0176]
用70μm nhs-pox或35μm染色的nhs-pox浸渍tuft-it
[0177]
用70μm nhs-pox(n=186)浸渍tuft-it。
[0178]
·
未浸渍的tuft-it的平均重量为0.74g
[0179]
·
平均浸渍为0.93g,对应于约56%的总浸渍效率平均浸渍为0.93g,对应于约56%的总浸渍效率
[0180]
·
考虑到从阵列中回收34%的nhs-pox并重新用于浸渍,平均损失为8.9%w/w。
[0181]
未浸渍片的重量与浸渍水平(以克计)之间未观察到相关性。
[0182]
用35μm蓝色nhs-pox(n=26)浸渍双tuft-it
[0183]
·
未浸渍的tuft-it的平均重量为1.55g
[0184]
·
平均浸渍为2.78g,对应于约64%的总浸渍效率
[0185]
·
平均损失为约10%,而不需要从阵列中回收nhs-pox以再次用于浸渍。
[0186]
同样地,未浸渍片的重量与浸渍水平(以克计)之间没有观察到相关性。
[0187]
实施例2
[0188]
用50μm或35μm反应性nhs-pox/nu-pox浸渍pem
[0189]
用50μm nhs-pox/nu-pox颗粒(n=186)浸渍pem
[0190]
·
未浸渍的pem的平均重量为0.71g
[0191]
·
平均浸渍为1.65g,对应于约70%的总浸渍效率。
[0192]
·
平均损失为约10%,而不需要从阵列回收聚合物以再用于浸渍。
[0193]
未浸渍片的重量与浸渍水平(以克计)之间未观察到相关性。
[0194]
用35μm nhs-pox/nu-pox颗粒(n=20)浸渍pem
[0195]
·
未浸渍的pem的平均重量为0.72g
[0196]
·
平均浸渍为1.53g,对应于约68%的总浸渍效率。
[0197]
·
平均损失为约5%,而不需要从阵列中回收聚合物以再次用于浸渍。
[0198]
未浸渍片的重量与浸渍水平(以克计)之间未观察到相关性。
[0199]
实施例3
[0200]
用50μm或35μm反应性nhs-pox/nu-pox浸渍nu-knit/snow-hybrid
[0201]
用50μm nhs-pox/nu-pox颗粒(n=5)浸渍nu-knit/snow-hybrid
[0202]
·
未浸渍的nu-knit/snow-hybrid的平均重量为1.56g
[0203]
·
平均浸渍为3.47g,对应于约55%的总浸渍效率
[0204]
·
平均损失为约10%,而不需要从阵列中回收聚合物以再次用于浸渍。
[0205]
未浸渍片的重量与浸渍水平(以克计)之间未观察到相关性。
[0206]
用35μm nhs-pox/nu-pox颗粒(n=12)浸渍nu-knit/snow-hybrid
[0207]
·
未浸渍的nu-knit/snow-hybrid的平均重量为1.52g
[0208]
·
平均浸渍为2.87g,对应于约65%的总浸渍效率
[0209]
·
平均损失为约5%,而不需要从阵列中回收聚合物以再次用于浸渍。
[0210]
未浸渍片的重量与浸渍水平(以克计)之间未观察到相关性。
[0211]
实施例4
[0212]
用40μm nhs-pox/nu-pox/p188(5%和10%)颗粒浸渍pem
[0213]
5%p188:
[0214]
·
未浸渍的pem的平均重量为1.04g(n=11)
[0215]
·
平均浸渍为2.50g,对应于约70%的总浸渍效率
[0216]
10%p188
[0217]
·
未浸渍的pem的平均重量为1.03g(n=6)
[0218]
·
平均浸渍为2.56g,对应于约71%的总浸渍效率
[0219]
5%peg 3000:
[0220]
·
未浸渍的pem的重量为0.96g(n=1)
[0221]
·
浸渍为2.19g,对应于约70%的总浸渍效率
[0222]
10%peg 3000:
[0223]
·
未浸渍的pem的重量为1.02g(n=1)
[0224]
·
浸渍为2.48g,对应于约71%的总浸渍效率
[0225]
nhs-pox/nu-peg:
[0226]
·
未浸渍的pem的重量为1.01g(n=1)
[0227]
·
浸渍为1.47g,对应于约59%的总浸渍效率
[0228]
实施例5
[0229]
用40μm nhs-pox/nu-pox/p188(1.5%、2.5%、3.5%、5%和10%)颗粒浸渍nu-knit/snow-hybrid
[0230]
1.5%p188:
[0231]
·
未浸渍的nu-knit/snow-hybrid的平均重量为1.55g(n=1)
[0232]
·
平均浸渍为1.90g,对应于约55%的总浸渍效率
[0233]
2.5%p188:
[0234]
·
未浸渍的nu-knit/snow-hybrid的平均重量为1.53g(n=1)
[0235]
·
平均浸渍为1.77g,对应于约54%的总浸渍效率
[0236]
3.5%p188:
[0237]
·
未浸渍的nu-knit/snow-hybrid的平均重量为1.45g(n=1)
[0238]
·
平均浸渍为1.19g,对应于约45%的总浸渍效率
[0239]
5%p188:
[0240]
·
未浸渍的nu-knit/snow-hybrid的平均重量为1.52g(n=12)
[0241]
·
平均浸渍为2.87g,对应于约65%的总浸渍效率
[0242]
10%p188:
[0243]
·
未浸渍的nu-knit/snow-hybrid的平均重量为1.52g
[0244]
·
平均浸渍为2.61g,对应于约63%的总浸渍效率
[0245]
实施例6
[0246]
用100μm反应性nhs-pox/gelita spon颗粒浸渍pem
[0247]
·
未浸渍的pem的平均重量为0.79g(n=1)
[0248]
·
2次循环(一次20秒和一次30秒)后的平均浸渍为1.15g,对应于约60%的总浸渍效率
[0249]
颗粒是蓬松的,因此可以在阵列中应用有限量的颗粒。为了实现合理的浸渍效率(或负载-%),需要2个循环。
[0250]
实施例7
[0251]
tuft-it由0.75克的明胶纤维制成并且能够保持最大1克的nhs-pox(参见实施例1)。为了增加超过1g nhs-pox的负载容量,所谓的“tuft-it-plus”由标准tuft-it通过在n=8层之间均匀分散0.5克的标准gelita spon制成。
[0252]
增加tuft-it的密度导致两个主要结果:[1]更松散的材料以实现更好的止血 [2]增加了保持更多nhs-pox用于改善止血的能力。
[0253]
用70μm nhs-pox浸渍tuft-it-plus。可以使用双隔离物(双遮盖物各3mm,导致3 3 4mm的粉末阵列厚度并且电极之间的总高度为10mm)将nhs-pox的负载增加到每载体1.5g。
[0254]
实施例8
[0255]
使用实施例1至7中所述的浸渍片进行出血实验。
[0256]
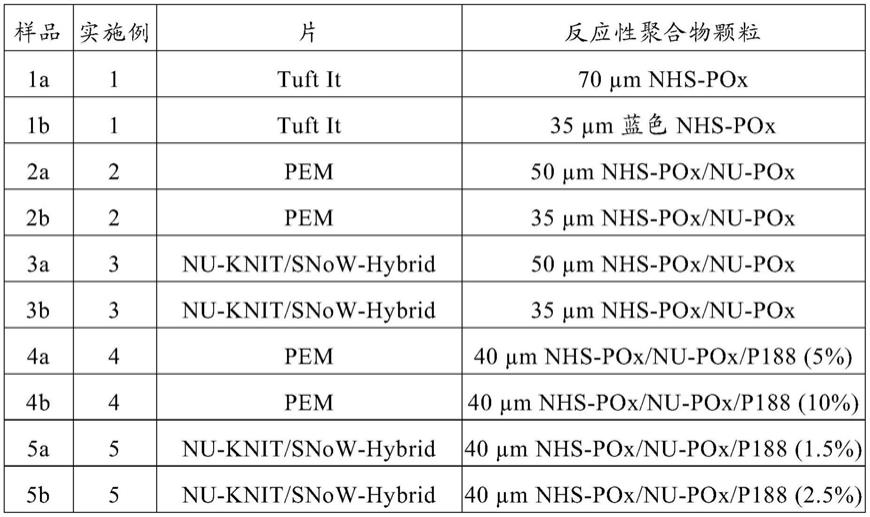
表1中显示了测试样品的概况。
[0257]
表1
[0258][0259][0260]
出血测试的结果总结在表2和表3中(nt=未测试)。
[0261]
表2(非肝素化的)
[0262][0263]
表3(肝素化的)
[0264][0265][0266]
实施例9
[0267]
进行实验以确定反应性nhs-pox/nu-pox颗粒的nu-pox含量对止血贴片的体内性能的影响。
[0268]
浸渍方法
[0269]
将止血贴片(gelita50x75mm,约0.7g)用通过丙酮粒化制备的反应性nhs-pox/nu-pox颗粒以1:0.10、1:0.20和1:0.40的摩尔比浸渍,所述摩尔比是指由nhs-pox提供的nhs基团的数量与由nu-pox提供的胺基团的数量的比率。同样的止血贴片也用反应性nhs-pox粉末浸渍。
[0270]
使用fibroline sl-preg实验室机器将1克颗粒/粉末分布在整个贴片中。然后,将止血贴片固定、干燥和包装在含有1g的二氧化硅的alu-alu袋中并且真空密封。
[0271]
机器
[0272]
fibroline sl-preg实验室机器通过以高达200hz的频率施加高达40kv的电压持续高达60秒的时间在电极之间移动颗粒。两个电极板具有约50
×
40cm的尺寸。顶板接地。
[0273]
使用以下标准设置:40kv,100hz,20秒。
[0274]
阵列
[0275]
在阵列已经安装到底部电极板上后,将粉末通过重量计量配量到3d印刷的pmma阵列中。使用刮纸盒或金属刮刀用反应性聚合物粉末填充阵列。阵列测量为50
×
75
×
4mm并且含有22
×
33=726个正方形孔(每个孔的内部尺寸:2
×2×
2mm)。726个孔的合并体积为约5.8ml。
[0276]
间隔物
[0277]
将间隔物遮盖物置于阵列的顶部。当经受交变电场时,间隔物用于允许颗粒上下移动。如果不使用间隔物,则通过载体的渗透和分布受到限制。对于tuft-it,这是3mm的遮盖物。这导致电极的3 4mm=7mm的距离。
[0278]
在非肝素化的体内猪模型中评估含有nhs-pox:nu-pox颗粒(来自nu-pox的0%、10%、20%和40%的胺基团,基于由nhs-pox提供的nhs基团的数量计算百分比)或nhs-pox粉末的止血贴片的体内性能。测试的贴片的细节显示在表4中。
[0279]
表4
[0280][0281]
体内测试
[0282]
对成年雌性家猪(40至50kg)进行测试,没有应用抗凝剂。在脾和肝上测试贴片性能。随着测试阶段的进行,脾或肝根据需要被定位和外化,并且通过用盐水浸泡的海绵覆盖它们来保持它们的自然湿度。
[0283]
产生不同类型的损伤:
[0284]
·
肝:擦伤、活检穿孔和切除
[0285]
·
脾:切除
[0286]
将适当大小的肝薄壁组织刮擦/打孔以引起中度至重度出血。通过手术刀和1
×
1cm2的模板以及使用8mm圆形活检穿孔的圆形穿孔产生肝擦伤。使用手术刀进行肝和脾切除。
[0287]
在组织切除或划痕之后立即应用贴片:
[0288]-用于活检穿孔和擦伤的2
×
2cm的片
[0289]-用于切除的完整7.5
×
5cm贴片
[0290]
将测试的贴片应用于出血组织上并使用用盐水溶液预润湿的纱布通过压缩而轻轻地向下压。将压塞应用10秒的初始时间,随后是30秒的间隔,直至总共5分钟。
[0291]
未浸渍的tuft-it贴片用作参考物(称为tuft-it)。
[0292]
体内测试的结果概述在表5中。
[0293]
表5
[0294][0295]
贴片1至贴片4显示出非常强的组织粘附性,而对于tuft-it贴片仅观察到轻微的粘附性。
[0296]
贴片1和贴片2在应用后仅显示出非常有限的溶胀。贴片3至贴片4显示出更多但仍可接受的溶胀。
[0297]
实施例10
[0298]
将止血贴片(gelita50x75mm,约0.7g)用nhs-pox的溶液、nhs-pox粉末或nhs-pox/nu-pox颗粒浸渍。使用的nhs-pox/nu-pox颗粒通过丙酮粒化以1:0.20的摩尔比制备(参见实施例9)。
[0299]
通过将nhs-pox溶解在异丙醇和二氯甲烷(200g/l)的1:1混合物中来制备含有nhs-pox的喷雾溶液。使用玻璃实验室喷雾器和加压空气在单个喷雾循环中用5ml的这种喷雾溶液浸渍贴片。以这种方式递送的nhs-pox的总量为1克/每贴片。在浸渍之后,使贴片在40℃的烘箱内干燥2小时,然后将它们在干燥器中储存2天,然后包装在含有1g的二氧化硅的alu-alu袋中并且真空密封。
[0300]
此外,使用实施例9中所述的程序,用1克的nhs-pox粉末或1克的nhs-pox/nu-pox颗粒浸渍贴片。
[0301]
如此制备的贴片的性能在离体肝灌注模型中在温和出血(《20ml/min)和严重出血(》50ml/min)条件下一式三份地测试。使用平的圆形旋转磨具,在肝表面上产生圆形出血伤口(8mm直径),使用橡胶上置物,使得穿孔出血的深度总是3mm。结果显示在表6中。
[0302]
表6
[0303]
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。