本发明涉及锂离子二次电池用正极活性物质的制造方法。
背景技术
近年来,随着手机终端、笔记本型个人电脑等便携式电子设备的普及,强烈希望开发出具有高能量密度、耐久性的小型且轻量的非水系电解质二次电池。此外,作为电动工具、以混动汽车为代表的电动汽车用的电池,强烈期望开发出高输出的二次电池。
作为满足这样的要求的二次电池,有锂离子二次电池等非水系电解质二次电池。使用具有层状或尖晶石型晶体结构的锂金属复合氧化物作为正极活性物质的锂离子二次电池能够获得4V级的高电压,因此作为具有高能量密度的电池而正在推进实用化。
作为锂金属复合氧化物,提出了合成比较容易的锂钴复合氧化物(LiCoO2)、使用比钴便宜的镍的锂镍复合氧化物(LiNiO2)、锂镍钴锰复合氧化物(LiNi1/3Co1/3Mn1/3O2)、使用锰的锂锰复合氧化物(LiMn2O4)、锂镍锰复合氧化物(LiNi0.5Mn0.5O2)等。
另外,锂离子二次电池在使用非水系电解质作为电池材料的情况下,要求高的热稳定性。例如,在锂离子二次电池的内部发生短路的情况下,会因急剧的电流而产生发热,因此要求更高的热稳定性。
因此,关注了热稳定性优异的锂镍钴锰复合氧化物、锂镍锰复合氧化物等。锂镍钴锰复合氧化物与锂钴复合氧化物、锂镍复合氧化物等相同地,是层状化合物,将过渡金属点位上的镍、钴和锰的组成比为1:1:1的比例的物质称为三元系正极活性物质。
特别是,近年来关注了以高容量化为目标的三元系正极活性物质、使锂镍锰复合氧化物的镍比率增加了的、镍比率高的正极活性物质(Hi-Ni正极材料)。但是,由镍比率带来的电池容量增加与热稳定性的降低是此消彼长的,因此要求兼具作为锂离子二次电池的高性能(高循环特性、高容量、高输出)与耐短路性、热稳定性的正极活性物质。
为了提高热稳定性,提出了一些在锂金属复合氧化物中添加铌的技术。例如,专利文献1中提出了一种非水系二次电池用正极活性物质,其包含由通式:LiaNi1-x-y-zCoxMyNbzOb(其中,M为选自由Mn、Fe和Al所组成的组中的一种以上元素,1≤a≤1.1、0.1≤x≤0.3、0≤y≤0.1、0.01≤z≤0.05、2≤b≤2.2)所表示的含有锂、镍、钴、元素M、铌和氧的至少一种以上化合物构成的组合物。根据专利文献1,由于存在于粒子的表面附近或内部的Li-Nb-O系化合物具有高的热稳定性,因此能够获得具有高的热稳定性和大放电容量的正极活性物质。
此外,专利文献2中提出了一种非水系电解质二次电池用正极活性物质,其包含通式(1):LidNi1-a-b-cMnaMbNbcO2 γ(上述通式(1)中,M为选自Co、W、Mo、V、Mg、Ca、Al、Ti、Cr、Zr和Ta中的至少1种元素,0.05≤a≤0.60、0≤b≤0.60、0.0003≤c≤0.03、0.95≤d≤1.20、0≤γ≤0.5。)所表示的锂镍锰复合氧化物,锂镍锰复合氧化物中的铌的至少一部分固溶于一次粒子。根据专利文献2,能够获得以高水平兼具高能量密度和优异的输出特性以及因导电性降低导致的短路时的热稳定性的非水系二次电池。
现有技术文献
专利文献
专利文献1:日本特开2002-151071号公报
专利文献2:国际公开第2018/043669号
专利文献3:日本特开2008-017729号公报
专利文献4:日本专利第4807467号
专利文献5:日本特开2006-147499号公报
专利文献6:日本特开2007-265784号公报
专利文献7:日本特开2008-257902号公报
技术实现要素:
发明所要解决的课题
上述专利文献1、2中虽然记载了,其所记载的正极活性物质通过以特定的形态包含铌从而提高热稳定性,但对于具有高镍比率的锂镍锰复合氧化物,要求进一步提高热稳定性。此外,由于铌的价格高,因此要求能够以更低成本实现高的热稳定性的正极活性物质的制造方法。
本发明是鉴于这些情况而完成的,其目的在于,对于含有具有高镍比率的锂镍锰复合氧化物的正极活性物质而言,提供能够在工业规模的生产中容易地制造能以低成本实现更高的热稳定性的正极活性物质的方法。
另外,为了获得具有高电池特性的正极活性物质,例如,提出了一些在锂金属复合氧化物中添加钛的技术。根据专利文献3~7,包含锂镍钴钛复合氧化物的正极活性物质的热稳定性良好,具有高电池容量。
此外,在锂离子二次电池的内部发生短路的情况下,作为抑制短路导致的急剧的电流的方法之一,例如,如上述专利文献2所记载的那样,认为降低在被压缩而存在于正极的状态下的正极活性物质的导电性、或者提高体积电阻率是有效的。
但是,上述专利文献1~7中完全没有记载在锂镍锰复合氧化物中组合含有铌和钛作为异种元素所带来的效果,此外,上述专利文献1、3~7中也完全没有记载在被压缩而存在于正极的状态下的正极活性物质的导电率或体积电阻率。
用于解决课题的方法
本发明的第一方式中,提供一种锂离子二次电池用正极活性物质的制造方法,其具备混合物调制工序以及烧成工序,上述锂离子二次电池用正极活性物质包含具有六方晶系的层状结构、且由多个一次粒子凝聚而成的二次粒子构成的锂镍锰复合氧化物,上述混合物调制工序中,调制至少包含镍锰复合化合物和锂化合物、且任意地包含钛化合物和铌化合物中的一者或两者的混合物,上述烧成工序中,将混合物在750℃以上1000℃以下进行烧成而获得锂镍锰复合氧化物,镍锰复合化合物含有镍(Ni)和锰(Mn)、且任意地含有选自由Co、V、Mg、Mo、Ca、Cr、Ta、Na、W、Fe、Zn、B、Si、P、Zr和Al所组成的组中的至少1种元素即元素M(M)、钛(Ti)和铌(Nb),各个元素的物质量之比由Ni:Mn:M:Ti:Nb=(1-x-y):x:y:z’:w’(其中,0.03≤x≤0.30、0≤y≤0.30、0≤z’≤0.05、0≤w’≤0.03)表示,混合物中,相对于镍、锰、元素M、钛和铌的物质量的合计,钛的物质量的比例(z)和铌的物质量的比例(w)满足0.005≤z≤0.05、0.001<w≤0.03、(z w)≤0.06且z>w,锂镍锰复合氧化物中的铌的至少一部分在一次粒子间的粒界偏析。
本发明的第二方式中,提供一种锂离子二次电池用正极活性物质的制造方法,其具备混合物调制工序以及烧成工序,上述锂离子二次电池用正极活性物质包含具有六方晶系的层状结构、且由多个一次粒子凝聚而成的二次粒子构成的锂镍锰复合氧化物,上述混合物调制工序中,至少将镍锰复合化合物、钛化合物、铌化合物以及锂化合物混合而调制混合物,上述烧成工序中,将混合物在750℃以上1000℃以下进行烧成而获得锂镍锰复合氧化物,镍锰复合化合物含有镍(Ni)和锰(Mn)、且任意地含有选自Co、V、Mg、Mo、Ca、Cr、Ta、Na、W、Fe、Zn、B、Si、P、Zr和Al中的至少1种元素即元素M(M),各个元素的物质量之比由Ni:Mn:M=(1-x-y):x:y(其中,0.03≤x≤0.30、0≤y≤0.30)表示,混合物中,相对于镍、锰、元素M、钛和铌的物质量的合计,钛的物质量的比例(z)和铌的物质量的比例(w)满足0.005≤z≤0.05、0.001<w≤0.03、(z w)≤0.06且z>w,锂镍锰复合氧化物中的铌的至少一部分在一次粒子间的粒界偏析。
此外,上述第一方式或第二方式中,可以具备水洗工序以及干燥工序,上述水洗工序中,相对于烧成后得到的上述锂镍锰复合氧化物150重量份,以50重量份以上200重量份以下的比例混合水,搅拌后进行固液分离,上述干燥工序中,将水洗后的锂镍锰复合氧化物进行干燥。此外,混合物中,相对于镍、锰、元素M、钛和铌的物质量的合计,钛的物质量的比例(z)和铌的物质量的比例(w)可以满足0.005≤z≤0.05、0.002≤w≤0.03、(z w)≤0.06且z>w。
此外,混合物调制工序中,可以至少将含钛的镍锰复合化合物、铌化合物以及锂化合物混合,镍锰复合化合物含有镍(Ni)、锰(Mn)和钛(Ti)、且任意地含有选自Co、V、Mg、Mo、Ca、Cr、Ta、Na、W、Fe、Zn、B、Si、P、Zr和Al中的至少1种元素即元素M(M),各个元素的物质量之比由Ni:Mn:M:Ti=(1-x-y-z’):x:y:z’(其中,0.03≤x≤0.30、0≤y≤0.30、0.005≤z’≤0.05)表示。
此外,含钛的镍锰复合化合物可以通过晶析来获得。此外,含钛的镍锰复合化合物也可以通过将含钛的化合物被覆于由晶析得到的镍锰复合化合物来获得。
此外,混合物调制工序中,可以至少将含铌的镍锰复合化合物、锂化合物以及钛化合物混合,含铌的镍锰复合化合物含有镍(Ni)、锰(Mn)和铌(Nb)、且任意地含有选自由Co、V、Mg、Mo、Ca、Cr、Ta、Na、W、Fe、Zn、B、Si、P、Zr和Al所组成的组中的至少1种元素即元素M(M),各个上述元素的物质量之比由Ni:Mn:M:Nb=(1-x-y):x:y:w’(其中,0.03≤x≤0.30、0≤y≤0.30、0.001<w’≤0.03)表示。
此外,含铌的镍锰复合化合物可以通过将含铌的化合物被覆于由晶析得到的镍锰复合化合物来获得。此外,含铌的镍锰复合化合物中的上述元素的物质量之比由Ni:Mn:M:Nb=(1-x-y):x:y:w’(其中,0.03≤x≤0.30、0≤y≤0.30、0.002≤w’≤0.03)表示。
此外,烧成工序优选在氧浓度为80体积%以上100体积%以下的气氛下进行。此外,锂镍锰复合氧化物中的钛优选存在于一次粒子的内部。此外,钛化合物优选为氧化钛。此外,铌化合物优选为氧化铌、铌酸或它们的混合物。此外,烧成后得到的锂镍锰复合氧化物的、通过压粉电阻测定求出的压缩至4.0g/cm3时的体积电阻率优选为5.0×102Ω·cm以上1.0×105Ω·cm以下。
发明效果
根据本发明,能够提供能以低成本实现非常高的热稳定性的正极活性物质的制造方法。此外,本发明能够在工业规模的生产中容易地制造这样的正极活性物质,可以说具有极大的工业价值。
附图说明
[图1]图1是示出比较例1A、2A、3A以及实施例2A中得到的正极活性物质的最大氧产生峰值温度的图表。
[图2]图2是示出比较例1A、2A、3A以及实施例2A中得到的正极活性物质的压缩时的体积电阻率的图表。
[图3]图3是示出实施例2A、6A中得到的正极活性物质的放电容量的图表。
[图4]图4是示出比较例1A、2A、3A、实施例2A以及实施例11A中得到的正极活性物质的最大氧产生峰值温度的图表。
[图5]图5是示出实施例2A、实施例11A中得到的正极活性物质的放电容量的图表。
[图6]图6是示出本实施方式的正极活性物质的制造方法的一例的图。
[图7]图7的(A)和图7的(B)是示出本实施方式的镍锰复合化合物的制造方法的一例的图。
[图8]图8是示出本实施方式的正极活性物质的制造方法的一例的图。
[图9]图9的(A)和图9的(B)是示出本实施方式的含钛的镍锰复合化合物的制造方法的一例的图。
[图10]图10是示出本实施方式的含钛的镍锰复合化合物的制造方法的一例的图。
[图11]图11是示出本实施方式的正极活性物质的制造方法的一例的图。
[图12]图12是示出本实施方式的含铌的镍锰复合化合物的制造方法的一例的图。
[图13]图13是示出本实施方式的正极活性物质的制造方法的一例(包括水洗工序以及干燥工序)的图。
[图14]图14是示出本实施方式的正极活性物质的制造方法的一例(包括水洗工序以及干燥工序)的图。
[图15]图15是示出本实施方式的正极活性物质的制造方法的一例(包括水洗工序以及干燥工序)的图。
[图16]图16是电池评价中使用的纽扣型电池的概略截面图。
[图17]图17的(A)是示出正极活性物质的截面照片的一例的图,图17的(B)和图17的(C)是分别示出实施例2A和实施例2B的正极活性物质的一次粒子内部的STEM-EDX的评价结果的一例的图。
[图18]图18的(A)是示出正极活性物质的截面照片的一例的图,图18的(B)和图18的(C)是分别示出实施例2A和实施例2B的正极活性物质的一次粒子间粒界的STEM-EDX的评价结果的一例的图。
具体实施方式
以下,首先,对利用本实施方式的制造方法得到的锂离子二次电池用正极活性物质进行说明,接着,对本实施方式的锂离子二次电池用正极活性物质的制造方法以及使用该正极活性物质的锂离子二次电池进行说明。
1.锂离子二次电池用正极活性物质
本实施方式的锂离子二次电池用正极活性物质(以下,也称为“正极活性物质”。)优选包含具有六方晶系的层状结构、且由多个一次粒子凝聚而成的二次粒子构成的锂镍锰复合氧化物。锂镍锰复合氧化物中,作为氧以外的元素,含有锂(Li)、镍(Ni)、锰(Mn)、钛(Ti)和铌(Nb)、且任意地含有选自Co、V、Mg、Mo、Ca、Cr、Ta、Na、W、Fe、Zn、B、Si、P、Zr和Al中的至少1种元素即元素M(M)。
尤其在使用可燃性非水系电解质作为锂离子二次电池的构成材料的情况下,对锂离子二次电池要求高的热稳定性。此外,在锂离子二次电池中,在充电状态下正极与负极间发生短路的情况下,有时产生如下的连锁效应:正极活性物质由于因电流急剧流过所产生的大量的热而分解,进而进行发热。因此,通过在正极中受到压缩的条件下使用具有高体积电阻率的正极活性物质,从而能够抑制由于短路而发生的急剧的电流升高,能够更加提高短路时的热稳定性。
本发明人等进行了深入研究,结果发现,通过在用于正极活性物质的锂镍锰复合氧化物中,以特定的分布含有特定量的钛(Ti)和铌(Nb),从而正极活性物质可以具有非常高的体积电阻率,并且能够通过抑制过充电时的氧释放而实现高的热稳定性,从而完成了本发明。
以下,参照图1~5来说明在本实施方式的锂镍锰复合氧化物中包含钛(Ti)和铌(Nb)所带来的效果。需说明的是,图1~5是基于后述的实施例和比较例中得到的正极活性物质以及二次电池的评价结果而制作的。
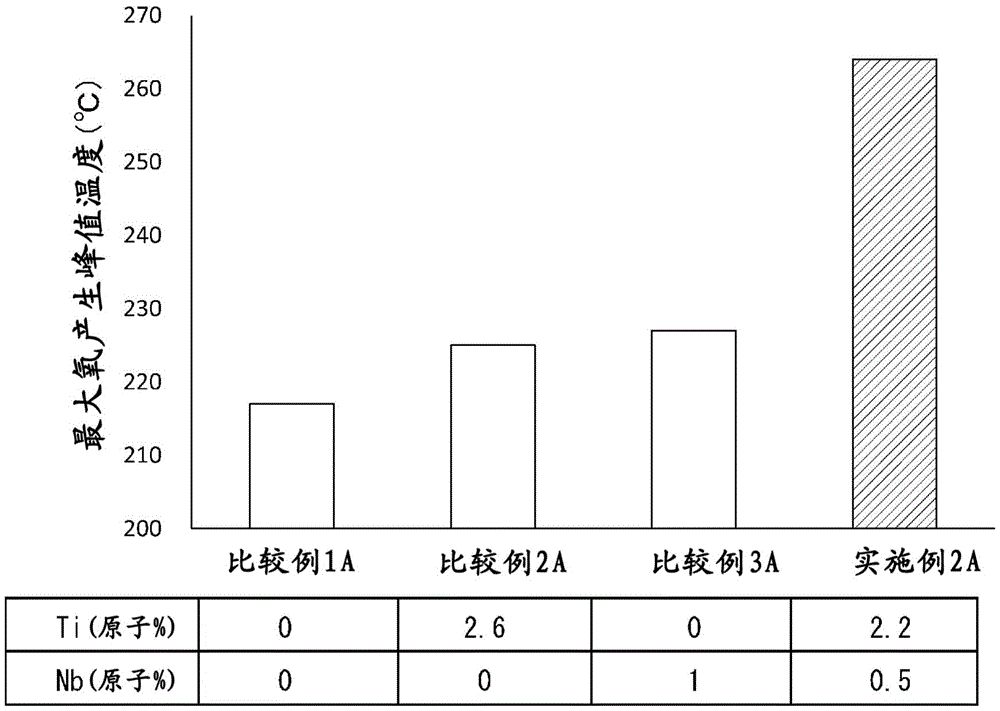
图1是示出将锂镍锰复合氧化物(正极活性物质)设为过充电状态,并测定从室温升温至450℃时的氧量而得到的最大氧产生峰值温度(℃)的图表。
图1的图表中,从左开始示出不含钛和铌的比较例1A、单独含有钛的比较例2A(Ti:2.6原子%)、单独含有铌的比较例3(Nb:1原子%)、以及含有钛和铌的实施例2(Ti:2.2原子%、Nb:0.5原子%)的最大氧产生峰值温度。
如图1所示,与不含钛和铌的比较例1A相比,仅含有钛的比较例2A(Ti:2.6原子%)和仅含有铌的比较例3(Nb:1原子%)中,最大氧产生峰值温度升高。而且,含有钛和铌这两者的实施例2A(Ti:2.2原子%、Nb:0.5原子%)中,与比较例2A、3A相比,最大氧产生峰值温度进一步升高。
此外,实施例2A中,仅通过与Ti一起含有0.5原子%的Nb,就显示出高于比较例3A(Nb:1原子%)的最大氧产生峰值温度。因此,本实施方式的正极活性物质能够将过充电时的氧产生以更高的水平抑制,同时降低高价的铌的使用量。
图2是示出将锂镍锰复合氧化物(正极活性物质)压缩至4.0g/cm3时的体积电阻率(Ω·cm)的图表。
如图2所示,与不含钛和铌的比较例1A相比,仅含有钛的比较例2A(Ti:2.6原子%)和仅含有铌的比较例3(Nb:1原子%)中,体积电阻率在一定程度上增加。但是,含有钛和铌这两者的实施例2(Ti:2.2原子%、Nb:0.5原子%)中,即使与比较例2、3相比,体积电阻率增加得非常明显。因此,本实施方式的正极活性物质通过含有钛和铌,从而压缩时的体积电阻率显著增加,因此短路时的热稳定性优异。
此外,图3是示出除了变更了烧成工序中的气氛的氧浓度以外在同样的条件下制造的实施例2A和实施例6A(Ti:2.2原子%、Nb:0.5原子%)的放电容量(mAh/g)的图表。如图3所示,在将烧成时的氧浓度设为80体积%以上的实施例2A(氧浓度:90体积%)中,与将烧成时的氧浓度设为60体积%的实施例6A相比,放电容量提高。
因此,虽然通常认为难以兼具高体积电阻率和高电池容量,但本实施方式的正极活性物质通过调整制造条件(例如,烧成工序时的氧浓度等),从而即使具有非常高的体积电阻率(4.0g/cm3压缩时),也能够具有高的电池容量,能够以低成本兼具高的热稳定性和高电池容量。
由以上内容可以明确,本实施方式的正极活性物质(i)通过锂镍锰复合氧化物组合含有钛和铌,从而能够以低成本实现过充电时的高的热稳定性和压缩时的非常高的体积电阻率,且短路时的热稳定性优异,此外,(ii)通过调整制造条件,能够兼具高电池容量和高的热稳定性。
本发明人等进行了更加深入的研究,结果发现,在用于正极活性物质的锂镍锰复合氧化物中,iii)通过将锂镍锰复合氧化物水洗以及干燥,从而能够具有高的热稳定性,并且更加提高电池容量。
以下,参照图4、5来说明在本实施方式的锂镍锰复合氧化物中由水洗以及干燥带来的效果。
图4是示出将锂镍锰复合氧化物(正极活性物质)设为过充电状态,并测定从室温升温至450℃时的氧量而得到的最大氧产生峰值温度(℃)的图表。
图4的图表中从左开始示出了不含钛和铌的比较例1A、单独含有钛的比较例2A(Ti:2.6原子%)、单独含有铌的比较例3A(Nb:1原子%)、含有钛和铌的实施例2A(Ti:2.2原子%、Nb:0.5原子%)、以及将实施例2A水洗以及干燥而得到的实施例11A(Ti:2.2原子%、Nb:0.5原子%)的最大氧产生峰值温度。
如图4所示,与不含钛和铌的比较例1A相比,仅含有钛的比较例2A(Ti:2.6原子%)和仅含有铌的比较例3(Nb:1原子%)中,最大氧产生峰值温度升高。此外,含有钛和铌这两者的实施例2A和实施例11A(Ti:2.2原子%、Nb:0.5原子%)中,与比较例2A相比,最大氧产生峰值温度升高,显示出与比较例3A相同程度或比它更高的最大氧产生峰值温度。
此外,实施例11A和实施例2A中,仅通过与Ti一起含有0.5原子%的Nb,就显示出高于比较例2A(Ti:2.6原子%)和比较例3A(Nb:1原子%)的最大发热峰值温度。因此,明确了本实施方式的正极活性物质能够将过充电时的氧产生以更高的水平抑制,同时降低高价的铌的使用量。
图5是示出含有钛和铌的实施例2A(Ti:2.2原子%、Nb:0.5原子%)以及将实施例2A水洗和干燥而得到的实施例11的电池容量(初始放电容量)的图表。如图5所示,与未进行水洗的实施例2A相比,进行了水洗的实施例11A的电池容量提高。
因此,虽然锂镍锰复合氧化物的电池容量有时由于含有作为异种元素的钛和铌而略有下降,但是,本实施方式的正极活性物质如后述那样通过在烧成后进行水洗以及干燥,能够兼具高的热稳定性和更高的电池容量。以下,详细说明本实施方式的正极活性物质的优选构成。
[锂镍锰复合氧化物]
正极活性物质所含有的锂镍锰复合氧化物由多个一次粒子凝聚而成的二次粒子构成。此外,锂镍锰复合氧化物优选具有六方晶系的层状结构。
锂镍锰复合氧化物中,作为氧以外的元素,含有锂(Li)、镍(Ni)、锰(Mn)、钛(Ti)和铌(Nb),且任意地含有选自Co、V、Mg、Mo、Ca、Cr、Ta、Na、W、Fe、Zn、B、Si、P、Zr和Al中的至少1种元素即元素M(M)。
锂镍锰复合氧化物所含有的上述元素的物质量之比(摩尔比)没有特别限定,从高电池容量的观点出发,优选由Li:Ni:Mn:M:Ti:Nb=a:(1-x-y-z-w):x:y:z:w(其中,0.97≤a≤1.25、0.03≤x≤0.30、0≤y≤0.30、0.005≤z≤0.05、0.001<w≤0.03)表示。此外,上述物质量比中,表示钛(Ti)的物质量比的z和表示铌(Nb)的物质量比的w满足(z w)≤0.06且z>w的关系。以下,对各元素的优选的组成进行说明。
(锂)
上述物质量比中,Li以外的上述元素的物质量比的合计成为1,因此表示Li的物质量比的a对应于锂与锂以外的上述元素(Me)的物质量比(以下也称为“Li/Me”。)。此外,a的范围为0.97≤a≤1.25,优选为1.00≤a≤1.15。在a的值为上述范围的情况下,正极的反应电阻降低而能够提高电池的输出。此外,a的范围可以为1.00≤a≤1.05。
(锰)
上述物质量比中,表示Mn的物质量之比的x的范围为0.03≤x≤0.30,优选为0.05≤x≤0.15,更优选为0.05≤x≤0.10。在x的值为上述范围的情况下,能够具有高电池容量和高的热稳定性。另一方面,在x的值小于0.03的情况下,无法获得热稳定性的改善效果。此外,在x的值大于0.30的情况下,电池容量降低。此外,通过以上述范围包含锰,从而能够在后述的烧成工序(S20)中提高烧成温度,能够促进钛等的分散。
(元素M)
上述物质量比中,元素M是选自Co、V、Mg、Mo、Ca、Cr、Ta、Na、W、Fe、Zn、B、Si、P、Zr和Al中的至少1种元素。此外,表示元素M的物质量比的y的范围为0≤y≤0.30,优选为0≤y≤0.15。在y为0以上的情况下,能够改善热稳定性、保存特性以及电池特性等。另一方面,在y大于0.30的情况下,存在晶体结构变得不稳定而无法形成具有层状的晶体结构的化合物的情况、由于Ni、Mn的比率相对下降而导致电池容量降低的情况。例如,在M包含Co的情况下,电池容量和输出特性更为优异。在M为Co的情况下,优选为0≤y≤0.10。此外,在将元素M所含的Co的物质量比设为y1的情况下,优选为0<y1≤0.10,更优选为0.01≤y1≤0.10。
(钛)
上述物质量比中,表示Ti的物质量比的z的范围为0.005≤z≤0.05。如上所述,在与铌一起以上述范围包含钛的情况下,能够显著增加锂镍锰复合氧化物的压缩时的体积电阻率,并且能够在用于二次电池的正极时抑制氧释放,获得高的热稳定性。另一方面,在z的值小于0.005的情况下,热稳定性的改善效果不充分。此外,在z的值大于0.05的情况下,Ni、Mn的比率相对降低,或者晶体结构不稳定而容易发生阳离子混排,因此电池容量有时会大幅降低。
(铌)
上述物质量比中,表示Nb的物质量比的w的范围为0.001<w≤0.03,优选为0.002≤w≤0.03,更优选为0.002≤w≤0.02,进一步优选为0.002≤w≤0.01。如上所述,通过与钛一起以上述范围包含铌,从而即使铌的含量少,也能够显著增加锂镍锰复合氧化物的压缩时的体积电阻率,并且能够在用于二次电池的正极时抑制氧释放,具有高的热稳定性。
此外,上述物质量比中,钛的物质量比(z)与铌的物质量比(w)的合计(z w)为0.06以下,优选为0.05以下,更优选为0.03以下。在z w为上述范围的情况下,能够具有高的热稳定性,同时获得更高的电池容量。
此外,上述物质量比中,铌的物质量比(w)小于钛的物质量比(z)(z>w),优选为z≥2w,更优选为z≥3w,进一步优选为z≥4w。铌是与钛相比高价的元素,因此通过使其含量少于钛,从而能够降低制造成本,并且通过与钛组合而能够具有高的热稳定性。
(镍)
上述物质量比中,表示Ni的物质量比的(1-x-y-z-w)为0.34以上,优选为0.5以上,更优选为0.65以上,更优选为0.70以上,进一步优选为0.80以上,可以为0.90以上。在镍的物质量比为上述范围的情况下,能够获得具有高电池容量的二次电池。在镍的物质量比高的情况下,虽然电池容量提高,但有时热稳定性会下降。但是,本实施方式的锂镍锰复合氧化物通过具有如上的组成,从而即使镍比高,也能够具有高的热稳定性。
需说明的是,锂镍锰复合氧化物的组成可以通过利用电感耦合等离子体(ICP)发光分析法的定量分析来测定。
(铌的分布)
本实施方式的锂镍锰复合氧化物所含的铌(Nb)的至少一部分优选在一次粒子间的粒界偏析。铌的偏析例如可以如下确认:利用扫描透射电子显微镜(S-TEM)的能量分散型X射线光谱法(EDX),对一次粒子截面的组成进行面分析/线分析,从而检测出铌在一次粒子间的粒界的至少一部分中的浓缩。需说明的是,铌的至少一部分可以存在于一次粒子的内部。
此外,利用STEM-EDX求出的、一次粒子间的粒界处的铌浓度相对于一次粒子内部的铌浓度优选为1.3倍以上,更优选为1.5倍以上。需说明的是,铌浓度的上限没有特别限定,例如为5倍以下。
需说明的是,一次粒子的内部或粒界处的铌的浓度可以如下确认:利用扫描透射电子显微镜(S-TEM)的EDX测定,对多个二次粒子的截面的组成进行面分析/线分析/点分析。
例如,一次粒子间的粒界的铌浓度可以如下获得:从多个二次粒子的截面随机选择20个包含一次粒子间的粒界的区域(例如,如图18所示的130nm×130nm的测定区域,以粒界横切区域内的方式包含的区域),通过点分析来确认各个区域的组成,并算出其平均值。此外,一次粒子内的铌浓度同样可以如下获得:随机选择20个一次粒内的内部区域(例如,130nm×130nm的不含粒界的区域:参照图17),对各个区域的组成进行分析,并算出其平均值。
(钛的分布)
本实施方式的锂镍锰复合氧化物所含的钛(Ti)的分布没有特别限定,可以存在于一次粒子的表面和粒界的至少一方,也可以固溶于一次粒子的内部,从提高二次电池中的电池容量这样的观点出发,优选钛进行固溶。这里,钛进行固溶是指,例如,通过使用S-TEM中的EDX进行二次粒子截面的面分析,在一次粒子的内部检测到钛,且没有确认到钛在一次粒子的界面的浓缩的状态,优选在一次粒子内部的整面检测到钛。
例如,利用STEM-EDX求出的、一次粒子间的粒界处的钛浓度相对于一次粒子内部的钛浓度优选小于1.3倍,优选为1.2倍以下,优选为1.1倍以下,可以为1.0倍以下。此外,一次粒子间的粒界处的钛浓度相对于一次粒子内部的钛浓度的下限可以为0.6倍以上,可以为0.7倍以上,例如可以为0.8倍以上1.2倍以下,可以为0.9以上1.1倍以下。需说明的是,钛浓度与上述的铌浓度同样地,能够通过S-TEM的EDX的面分析等来测定。
需说明的是,本实施方式的锂镍锰复合氧化物中,上述铌(Nb)和钛(Ti)以外的金属元素的分布没有特别限定,例如,在包含Ni、Mn以及作为元素M的Co的情况下,这些金属元素优选在构成二次粒子的多个一次粒子的内部的整面被检测到。
[体积平均粒径(Mv)]
本实施方式的正极活性物质的体积平均粒径(Mv)优选为8μm以上20μm以下,更优选为10μm以上17μm以下。在体积平均粒径(Mv)为上述范围的情况下,在将正极活性物质用于二次电池的正极时,能够兼具高输出特性和电池容量、以及向正极中的高填充性。
另一方面,在体积平均粒径(Mv)小于8μm的情况下,有时无法获得向正极中的高填充性。此外,如果体积平均粒径(Mv)大于20μm,则有时无法获得高的输出特性、电池容量。需说明的是,体积平均粒径(Mv)例如可以由利用激光衍射散射式粒度分布计测定的体积积分值求出。
[(D90-D10)/Mv](离散指数)
本实施方式的正极活性物质的[(D90-D10)/Mv]优选为0.80以上1.20以下。需说明的是,[(D90-D10)/Mv]表示由利用激光衍射散射法得到的粒度分布中的D90和D10(以粒度分布曲线中的粒子量的体积积分计90%时的粒径和10%时的粒径)以及体积平均粒径(Mv)算出的、构成正极活性物质的粒子的粒径的离散指数。
构成正极活性物质的粒子的粒度分布宽的情况下,存在许多粒径小于体积平均粒径(Mv)的微小粒子、粒径大于平均粒径的粗大粒子。在离散指数为上述范围的情况下,微小粒子、粗大粒子适度混在一起而填充密度变高,能够提高单位体积的能量密度。此外,从提高单位体积的能量密度的观点出发,[(D90-D10)/Mv]可以为0.90以上,可以为0.95以上。
另一方面,在正极活性物质的离散指数小于0.80的情况下,体积能量密度有时降低。此外,在使用本实施方式的正极活性物质的制造方法的情况下,上限为1.20左右。需说明的是,后述的烧成工序(S20)中,如果烧成温度大于1000℃,则粒径的离散指数有时会大于1.20。该情况下,有时会在形成正极活性物质时比表面积降低而正极的电阻升高,从而电池容量降低。
[压缩至4.0g/cm3时的体积电阻率]
烧成工序(S20)后得到的正极活性物质的由压粉电阻测定求出的、压缩至4.0g/cm3时的体积电阻率为5.0×102Ω·cm以上1.0×105Ω·cm以下,优选为1.0×103Ω·cm以上1.0×104Ω·cm以下,更优选为2.0×103Ω·cm以上1.0×104Ω·cm以下。在正极活性物质的体积电阻率为上述范围的情况下,能够获得短路时的高的热稳定性。通常,正极活性物质的导电率越高,则认为是电化学反应中的电阻越低的优异的活性物质,但在考虑短路时的热稳定性的情况下,通过体积电阻率适度高,从而能够抑制短路时产生急剧的电流。
需说明的是,体积电阻率例如可以如下求出:在4.5g以上5.5g以下的范围内称量正极活性物质,以成为4.0g/cm3的方式加压成型为直径20mm的圆柱状后,以加压的状态由依据JIS K 7194:1994的利用4探针法的电阻率试验方法进行测定。
[最大氧产生峰值温度]
烧成工序(S20)后得到的正极活性物质在过充电状态下的升温时的最大氧产生峰值温度优选为250℃以上,更优选为260℃以上。升温时的最大氧产生峰值温度的上限没有特别限定,为300℃以下的程度。
此外,进行水洗工序(S30)以及干燥工序(S40)后得到的正极活性物质在过充电状态下的升温时的最大氧产生峰值温度优选为250℃以上。
升温时的最大氧产生峰值温度的上限没有特别限定,为300℃以下的程度。需说明的是,最大氧产生峰值温度可以通过实施例中记载的方法来测定。此外,最大氧产生峰值温度是指,升温时所产生的氧达到极大且最大的峰的温度。
[溶出锂量]
本实施方式的正极活性物质在浸渍于水时在水中溶出的锂量(溶出锂量)优选小于除了没有进行后述的水洗工序(S30)以及干燥工序(S40)以外在同样的条件下制造的正极活性物质的溶出锂量。通过将溶出锂量降低至特定量,从而能够提高正极活性物质的结晶性、提高放电容量,同时抑制制作二次电池的极板时的正极合材糊剂的凝胶化。
进行水洗工序(S30)以及干燥工序(S40)后得到的正极活性物质在浸渍于水时在水中溶出的锂量(溶出锂量)相对于正极活性物质整体优选为0.20质量%以下,更优选为0.10质量%以下,可以为0.08质量%以下,可以为0.06质量%以下。此外,溶出锂量的下限没有特别限定,例如为0.01质量%以上。在溶出锂量为上述范围的情况下,能够引出锂镍锰复合氧化物中的剩余锂而抑制正极合剂糊剂的凝胶化等的发生。需说明的是,在溶出锂量小于0.01质量%的情况下,在水洗时锂有时会从锂镍锰复合氧化物中被过度引出,该情况下,电池特性会下降。
需说明的是,溶出锂量可以如下测定:取2g正极活性物质,投入至利用搅拌器搅拌的室温的纯水125ml中,在投入活性物质后立即使用HCl水溶液进行滴定。滴定通过Warder法进行评价,算出氢氧化锂(LiOH)量和碳酸锂(Li2CO3)量,将这些锂量之和作为溶出锂算出。
需说明的是,本实施方式的锂镍锰复合氧化物可以在不损害本发明的效果的范围内包含少量除上述金属元素(Li、Ni、Mn、元素M、Nb、Ti)和氧以外的元素。此外,作为正极活性物质所含的锂镍锰复合氧化物,除了二次粒子以外,还可以包含少量单独的一次粒子。此外,正极活性物质可以包含上述锂镍锰复合氧化物以外的化合物。
2.锂离子二次电池用正极活性物质的制造方法
图6~图15是示出本实施方式的锂离子二次电池用正极活性物质的制造方法(以下,也称为“正极活性物质的制造方法”)的一例的图。通过本实施方式的制造方法,能够以工业规模容易地获得包含上述锂镍锰复合氧化物的正极活性物质。
本实施方式的正极活性物质的制造方法具备混合物调制工序(S10)以及烧成工序(S20),上述混合物调制工序(S10)中,调制至少包含镍锰复合化合物和锂化合物且任意地包含钛化合物和铌化合物中的一者或两者的混合物,上述烧成工序(S20)中,将混合物烧成而获得锂镍锰复合氧化物,镍锰复合化合物含有镍(Ni)和锰(Mn)且任意地含有元素M(M)、钛(Ti)以及铌(Nb),上述元素M(M)为选自由Co、V、Mg、Mo、Ca、Cr、Ta、Na、W、Fe、Zn、B、Si、P、Zr和Al所组成的组中的至少1种元素,各个上述元素的物质量之比由Ni:Mn:M:Ti:Nb=(1-x-y):x:y:z’:w’(其中,0.03≤x≤0.30、0≤y≤0.30、0≤z’≤0.05、0≤w’≤0.03)表示,混合物调制工序中调制的混合物中,相对于镍、锰、元素M、钛和铌的物质量的合计,钛的物质量的比例(z)以及铌的物质量的比例(w)满足0.005≤z≤0.05、0.001<w≤0.03、(z w)≤0.06且z>w。
本实施方式的制造方法例如如图6所示可以具备:将镍锰复合化合物、钛化合物、铌化合物以及锂化合物混合而调制混合物的混合物调制工序(S10A);以及将混合物烧成而得到锂镍锰复合氧化物的烧成工序(S20)。
此外,本实施方式的制造方法例如如图8所示可以具备:至少将含钛的镍锰复合化合物、铌化合物和锂化合物混合而调制混合物的混合物调制工序(S10B);以及将混合物烧成而获得锂镍锰复合氧化物的烧成工序(S20)。
此外,本实施方式的制造方法例如如图11所示可以具备:至少将含铌的镍锰复合化合物、钛化合物和锂化合物混合而调制混合物的混合物调制工序(S10C);以及将混合物烧成而获得锂镍锰复合氧化物的烧成工序(S20)。
此外,混合物调制工序(S10D)中,混合物可以至少将含钛和铌的镍锰复合化合物与锂化合物混合进行调制。
此外,本实施方式的制造方法例如如图13所示可以具备:至少将镍锰复合化合物、钛化合物、铌化合物和锂化合物混合而调制混合物的混合物调制工序(S10A);将混合物烧成而获得上述锂镍锰复合氧化物的烧成工序(S20);将所得的锂镍锰复合氧化物与水混合并搅拌后进行固液分离的水洗工序(S30);以及将水洗后的锂镍锰复合氧化物(沉淀物)干燥的干燥工序(S40)。
此外,本实施方式的制造方法例如如图14所示可以具备:至少将含钛的镍锰复合化合物、铌化合物和锂化合物混合而调制混合物的混合物调制工序(S10B);将混合物烧成而获得锂镍锰复合氧化物的烧成工序(S20);将所得的锂镍锰复合氧化物与水混合并搅拌后进行固液分离的水洗工序(S30);以及将水洗后的锂镍锰复合氧化物(沉淀物)干燥的干燥工序(S40)。
此外,本实施方式的制造方法例如如图15所示可以具备:至少将含铌的镍锰复合化合物、钛化合物和锂化合物混合而调制混合物的混合物调制工序(S10C);将混合物烧成而获得锂镍锰复合氧化物的烧成工序(S20);将所得的锂镍锰复合氧化物与水混合并搅拌后进行固液分离的水洗工序(S30);以及将水洗后的锂镍锰复合氧化物(沉淀物)干燥的干燥工序(S40)。
以下,按照每个工序来详细说明本实施方式的制造方法。需说明的是,以下的说明是本实施方式的制造方法的一例,并不限定制造方法。
[晶析工序(S1A、S1B)]
混合物调制工序(S10A)中所使用的镍锰复合化合物例如如图7(A)和图7(B)所示那样优选通过具备晶析工序(S1A)和/或热处理工序(S2)的方法来获得。
此外,混合物调制工序(S10B)中所使用的含钛的镍锰复合化合物例如如图9(A)、图9(B)所示那样优选通过具备晶析工序(S1B)和/或热处理工序(S2)的方法来获得。
此外,混合物调制工序(S10C)中所使用的含铌的镍锰复合化合物例如可以通过将图9(A)所示的钛盐变更为铌盐来获得。此外,混合物调制工序(S10D)中所使用的含钛和铌的镍锰复合化合物例如可以通过与图9(A)所示的钛盐一起添加铌盐来获得。
晶析工序(S1A)中所得的镍锰复合氢氧化物中,作为羟基(OH)以外的元素,含有镍(Ni)和锰(Mn),且任意地含有选自Co、V、Mg、Mo、Ca、Cr、Ta、Na、W、Fe、Zn、B、Si、P、Zr和Al中的至少1种元素即元素M(M),各自的物质量之比(A)优选由Ni:Mn:M=(1-x-y):x:y(其中,0.03≤x≤0.30、0≤y≤0.30)表示。
晶析工序(S1B)中所得的镍锰复合氢氧化物中,作为羟基(OH)以外的元素,含有镍(Ni)、锰(Mn)和钛(Ti),且任意地含有选自Co、V、Mg、Mo、Ca、Cr、Ta、Na、W、Fe、Zn、B、Si、P、Zr和Al中的至少1种元素即元素M(M),各个元素的物质量之比(B)优选由Ni:Mn:M:Ti=(1-x-y-z’):x:y:z’(其中,0.03≤x≤0.30、0≤y≤0.30、0.005≤z’≤0.05)表示。需说明的是,晶析工序(S1B)中,除了以含钛的盐(钛盐)作为原料进行添加来获得含钛的镍锰复合氢氧化物以外,可以在与晶析工序(S1A)同样的条件下进行。
此外,含铌的镍锰复合氢氧化物中,作为羟基(OH)以外的元素,含有镍(Ni)、锰(Mn)和铌(Nb),且任意地含有选自Co、V、Mg、Mo、Ca、Cr、Ta、Na、W、Fe、Zn、B、Si、P、Zr和Al中至少1种元素即元素M(M),各个元素的物质量之比(C)优选由Ni:Mn:M:Nb=(1-x-y-w’):x:y:w’(其中,0.03≤x≤0.30、0≤y≤0.30、0.001<w’≤0.03)表示。需说明的是,关于含铌的镍锰复合氢氧化物,在晶析工序(S1B)中,除了将含铌的盐(铌盐)替换钛盐作为原料进行添加来获得含铌的镍锰复合氢氧化物以外,可以在与晶析工序(S1B)同样的条件下进行。
关于晶析工序(S1A)以及(S1B),只要能够获得具有上述物质量比(摩尔比)的镍锰复合氢氧化物,就可以通过公知的晶析方法来进行。以下,对于通过晶析来获得镍锰复合氢氧化物的晶析工序的一例进行说明。
例如,在反应槽内,将至少包含镍和锰的混合水溶液一边以恒定速度进行搅拌一边加入中和剂而形成反应水溶液,通过中和来控制反应水溶液的pH,从而通过共沉淀(晶析)生成镍锰复合氢氧化物。
包含镍和锰的混合水溶液可以使用含镍盐和锰盐的水溶液,例如镍和锰的硫酸盐溶液、硝酸盐溶液、氯化物溶液等。需说明的是,可以在分别调制含镍的水溶液和含锰的水溶液后,分别供给于反应槽内,从而制成包含镍和锰的混合水溶液。
此外,混合水溶液可以如后述那样包含元素M。此外,在获得含钛和/或铌的镍锰复合氢氧化物的情况下,混合水溶液可以包含钛和/或铌。混合水溶液所含的各金属元素的组成与所得的镍锰复合氢氧化物所含的各金属元素的组成大体一致。因此,可以按照成为与目标镍锰复合氢氧化物的各金属元素的组成相同的方式调制混合水溶液的金属元素的组成。
中和剂可以使用碱水溶液,例如,可以使用氢氧化钠、氢氧化钾等。
此外,优选与中和剂一起将络合剂添加于反应水溶液。络合剂只要能够在反应槽内的反应水溶液中与镍离子、其他金属离子结合而形成络合物就没有特别限定,可以使用公知的物质,例如,可以使用铵离子供体。作为铵离子供体,没有特别限定,例如,可以使用氨、硫酸铵、氯化铵、碳酸铵、氟化铵等。通过添加络合剂,能够调整反应水溶液中的金属离子的溶解度。
在晶析工序(S1A)或(S1B)中,在不使用络合剂的情况下,对于反应水溶液的温度而言,优选将温度(液温)设为大于60℃且为80℃以下的范围,并且上述温度下的反应水溶液的pH优选为10以上12以下(25℃基准)。在反应水溶液的pH大于12的情况下,所得的镍锰复合氢氧化物可能形成细小的粒子,过滤性也变差,无法得到球状粒子。另一方面,在反应水溶液的pH小于10的情况下,镍锰复合氢氧化物的生成速度显著变慢,滤液中残留Ni,Ni的沉淀量偏离目标组成,可能无法获得目标比率的镍锰复合氢氧化物。
此外,在反应水溶液的温度大于60℃的情况下,Ni的溶解度提高,能够避免Ni的沉淀量偏离目标组成而不形成共沉的现象。另一方面,如果反应水溶液的温度大于80℃,则可能发生由于水分的蒸发量多而浆料浓度(反应水溶液浓度)变高,Ni的溶解度降低,以及滤液中产生硫酸钠等的结晶,杂质浓度升高等,从而正极活性物质的充放电容量降低。
在晶析工序(S1A)或(S1B)中,在使用铵离子供体等络合剂的情况下,为了使反应水溶液中的Ni的溶解度升高,反应水溶液的温度优选为30℃以上60℃以下,并且反应水溶液的pH优选为10以上13以下(25℃基准),更优选为12以上13以下。
此外,反应水溶液中的氨浓度优选在3g/L以上25g/L以下的范围内保持在恒定值。在氨浓度小于3g/L的情况下,无法恒定地保持金属离子的溶解度,因此可能不会形成形状和粒径整齐的复合氢氧化物的一次粒子。此外,由于容易生成凝胶状的核,因此所得的镍锰复合氢氧化物的粒度分布也容易变宽。另一方面,如果氨浓度大于25g/L,则金属离子的溶解度变得过大,反应水溶液中残存的金属离子量增加,容易引起所得的镍锰复合氢氧化物的组成的偏离等。需说明的是,如氨浓度发生变动,则金属离子的溶解度发生变动,不会形成均匀的氢氧化物粒子,因此优选保持在恒定值。例如,关于氨浓度,优选将上限与下限的幅度设为5g/L左右而保持在期望的浓度。
此外,通过晶析得到的镍锰复合氢氧化物包含选自Co、V、Mg、Mo、Ca、Cr、Ta、Na、W、Fe、Zn、B、Si、P、Zr和Al中的至少1种元素即元素M的情况下,作为在镍锰复合氢氧化物中配合元素M的方法,没有特别限定,可以使用公知的方法。例如,从提高生产率这样的观点出发,优选为在反应槽内的包含镍和锰的混合水溶液中添加包含元素M的水溶液,使包含元素M的镍锰复合氢氧化物共沉淀的方法。
此外,通过晶析得到的镍锰复合氢氧化物包含钛和/或铌的情况下,作为在镍锰复合氢氧化物中配合钛和/或铌的方法,没有特别限定,可以使用公知的方法。例如,从提高生产率这样的观点出发,优选在反应槽内的包含镍和锰的混合水溶液中添加包含钛和/或铌的水溶液、且使包含钛和/或铌的镍锰复合氢氧化物共沉淀的方法。
作为包含元素M的水溶液,例如,可以使用包含硫酸钴、氯化氧钒、硫酸氧钒、硫酸镁、氯化镁、氯化钼、氯化钙、氯化铬、钽酸钠、氢氧化钠、钨酸钠、氧化钨、硫酸铁、氯化锌、硫酸锌、硼酸、硼酸铵、溴化硅、磷酸、硫酸锆、硝酸锆、硫酸铝、铝酸钠等的水溶液。此外,作为包含钛的水溶液,可以使用包含钛盐的水溶液,例如包含硫酸钛的水溶液等。此外,作为包含铌的水溶液,可以使用包含铌盐的水溶液,例如,将氢氧化铌、五氯化二铌、铌酸等溶解于氢氧化钾或盐酸而得到的水溶液等。
此外,从将晶析条件最佳化而容易控制组成比这样的观点出发,可以在由晶析工序(S1A)得到镍锰复合氢氧化物后,进一步设置将元素M被覆于所得的镍锰复合氢氧化物的工序。元素M的被覆方法没有特别限定,可以使用公知的方法。
此外,在获得包含钛和/或铌的镍锰复合氢氧化物的情况下,如图10和图12所示,可以在由晶析工序(S1A)或(S1B)得到镍锰复合氢氧化物后,具备用包含钛和/或铌的化合物进行被覆的被覆工序(S3)。钛和/或铌的被覆方法没有特别限定,可以使用公知的方法。钛和/或铌的被覆方法也与元素M的被覆方法同样,没有特别限定,可以使用公知的方法。
以下,对钛、铌和元素M中的至少一种元素(以下,统称为“添加元素”。)的被覆方法的一例进行说明。首先,使通过晶析得到的镍锰复合氢氧化物分散于纯水,制成浆料。接着,将含有对应于目标被覆量的添加元素的水溶液与上述浆料混合,并以成为预定的pH的方式滴加中和剂(酸或碱)进行调整。作为酸,例如,可使用硫酸、盐酸、硝酸等。作为碱,例如,可使用氢氧化钠、氢氧化钾等。接着,将浆料按照预定的时间混合后,进行浆料的过滤以及干燥,从而能够得到被覆有添加元素的镍锰复合氢氧化物。需说明的是,作为其他被覆方法,可举出将含有包含添加元素的化合物的溶液喷雾于镍锰复合氢氧化物后进行干燥的喷雾干燥法、使含有包含元素M的化合物的溶液含浸于镍锰复合氢氧化物的方法等。
需说明的是,将添加元素与镍锰复合氢氧化物配合的方法可以包括将添加元素混合于上述混合水溶液中、以及将添加元素被覆于镍锰复合氢氧化物中的一者或两者。
例如,1)可以在包含镍和锰的混合水溶液(其中,不包含添加元素)中加入碱水溶液进行晶析而得到镍锰复合氢氧化物,将添加元素被覆于该镍锰复合氢氧化物;2)也可以制作包含镍、锰以及添加元素中的一部分的混合水溶液,使镍锰复合氢氧化物(包含添加元素)共沉淀,进而将添加元素被覆于共沉淀物来调整添加元素的含量。
例如,作为含钛的镍锰复合氢氧化物的制造方法,如图10所示,例如,1)可以包括在包含镍和锰的混合水溶液(其中,不包含钛)中加入碱水溶液进行晶析而得到镍锰复合氢氧化物(S1A),以及将钛被覆于所得的镍锰复合氢氧化物(S3);2)也可以包括制作包含镍、锰和钛的混合水溶液,加入碱水溶液进行晶析,使其共沉淀而得到包含钛的镍锰复合氢氧化物(S1B),以及将钛被覆于所得的包含钛的镍锰复合氢氧化物(共沉淀物)(S3)。在包括晶析工序(S1B)以及被覆工序(S3)的情况下,可以按照这些工序中添加的钛量的合计达到上述物质量之比(B)的范围内的方式调整钛的含量。
需说明的是,作为包含铌的镍锰复合氢氧化物的制造方法,如图12所示,除了将图10所示的钛变更为铌以外,可以使用与上述包含钛的镍锰复合氢氧化物的制造方法同样的方法。
需说明的是,晶析工序(S1A)、(S1B)可以采用1)利用分批式晶析的制法(分批式晶析法),也可以采用2)利用连续式晶析的制法(连续晶析法)。例如,在分批式晶析法的情况下,能够通过在反应槽内的反应水溶液成为稳定状态后收集沉淀物并进行过滤、水洗,从而得到镍锰复合氢氧化物。此外,在连续晶析法的情况下,能够通过连续供给混合水溶液和碱水溶液、或视情况连续供给包含铵离子供体的水溶液,并使其从反应槽溢流来收集沉淀物、并进行过滤、水洗,从而得到镍锰复合氢氧化物。
本实施方式的正极活性物质的制造方法中,从得到用于二次电池时显示高体积能量密度的正极活性物质这样的观点出发,优选使用连续晶析法。利用连续式晶析的制造中,能够容易地得到离散指数高、粒度分布的幅度宽、填充性高的正极活性物质。此外,连续晶析法与分批式晶析法相比生产率也更高,更适合以工业规模生产。
[热处理工序(S2)]
如图7(B)和图9(B)所示,镍锰复合化合物可以通过在晶析工序(S1A)或(S1B)之后、进而具备热处理工序(S2)的方法来得到。此外,镍锰复合化合物可以通过在图10和图12所示的被覆工序(S3)之后、具备上述热处理工序(S2)的方法来得到。
热处理工序(S2)是将镍锰复合氢氧化物所含的水分的至少一部分通过热处理进行去除的工序。在具备热处理工序(S2)的情况下,通过将残留在镍锰复合氢氧化物中的水分的至少一部分去除,从而能够防止后述的烧成工序(步骤S20)中得到的正极活性物质的Li/Me产生偏差。
热处理工序(S2)只要能够将镍锰复合氢氧化物中的水分去除至正极活性物质的Li/Me不产生偏差的程度即可,从更加降低Li/Me的偏差这样的观点出发,优选使镍锰复合氢氧化物充分氧化而转换至镍锰复合氧化物。需说明的是,没必要将全部镍锰复合氢氧化物转化成镍锰复合氧化物。
此外,在具备热处理工序(S2)的情况下,可以在混合物调制工序(S10)中使用通过热处理工序(S2)得到的镍锰复合氢氧化物和镍锰复合氧化物中的至少一者作为镍锰复合化合物。此外,在利用添加元素(钛、铌和元素M中的至少1种元素)被覆镍锰复合氢氧化物的情况下,可以在将包含添加元素的化合物被覆于镍锰复合氢氧化物后,进行热处理工序(S2),也可以将包含添加元素的化合物被覆于通过热处理工序(S2)得到的镍锰复合氢氧化物和镍锰复合氧化物中的至少一者。
热处理只要在去除镍锰复合氢氧化物中的残留水分的条件下进行加热即可,例如,热处理的温度优选为105℃以上700℃以下。在将镍锰复合氢氧化物以105℃以上进行加热的情况下,可以容易地去除残留水分的至少一部分。需说明的是,在热处理的温度小于105℃的情况下,需要花费长时间来去除残留水分,在工业上不适合。另一方面,在热处理的温度大于700℃的情况下,转换成镍锰复合氧化物后的粒子有时会烧结而凝聚。例如,在将镍锰复合氢氧化物的大部分转换至镍锰复合氧化物的情况下,热处理的温度优选为350℃以上700℃以下。
热处理的气氛没有特别限定,例如,从容易进行操作这样的观点出发,优选为空气气流中。此外,热处理的时间没有特别限定,例如,可以设为1小时以上。在热处理的时间小于1小时的情况下,有时无法充分进行镍锰复合氢氧化物的粒子中的残留水分的去除。此外,热处理的时间优选为5小时以上15小时以下。此外,热处理中所使用的设备没有特别限定,只要能够将镍锰复合氢氧化物在空气气流中进行加热即可,例如,可以合适地使用送风干燥器、不产生气体的电炉等。
需说明的是,图7(B)中,对晶析工序(S1)后的镍锰复合氢氧化物进行了热处理,但也可以对在晶析工序(S1)以外的工序中得到的镍锰复合氢氧化物进行热处理。该情况下,也可以通过去除镍锰复合氢氧化物中的水分的至少一部分来获得上述效果。
[混合物调制工序(S10)]
混合物调制工序(S10)是调制至少包含镍锰复合化合物和锂化合物、且任意地包含钛化合物和铌化合物中的一者或两者的混合物的工序。以下,对于混合物调制工序(S10)的一例分别进行说明。需说明的是,以下的说明是混合物调制工序(S10)的一例,混合物调制工序(S10)也可以利用以下记载的方法以外的方法来调制混合物。
如图6所示,混合物调制工序(S10A)是至少将镍锰复合化合物、钛化合物、铌化合物以及锂化合物混合而调制混合物的工序。此外,混合物调制工序(S10)中,可以混合上述化合物以外的化合物,例如,可以混合包含元素M的化合物。
此外,如图8所示,混合物调制工序(S10B)是至少将含有钛的镍锰复合化合物、铌化合物以及锂化合物混合而调制混合物的工序。需说明的是,混合物调制工序(S10B)中,可以混合上述化合物以外的化合物,例如,可以进一步混合钛化合物,也可以混合包含元素M的化合物。
此外,如图11所示,混合物调制工序(S10C)是至少将含有铌的镍锰复合化合物、钛化合物以及锂化合物混合,从而调制混合物的工序。需说明的是,混合物调制工序(S10C)中,可以混合上述化合物以外的化合物,例如,可以进一步混合铌化合物,也可以混合包含元素M的化合物。
混合物调制工序(S10)中,可以将各个化合物例如以粉末(固相)添加、混合。以下,对于混合物调制工序(S10)中所使用的各材料进行说明。
(镍锰复合化合物)
混合物调制工序(S10A)中所使用的镍锰复合化合物中,作为氢(H)和氧(O)以外的元素,含有镍(Ni)和锰(Mn),且任意地含有作为选自Co、V、Mg、Mo、Ca、Cr、Ta、Na、W、Fe、Zn、B、Si、P、Zr和Al中的至少1种元素的元素M(M)。此外,所含有的上述元素的物质量之比优选由Ni:Mn:M=(1-x-y):x:y(其中,0≤x≤0.30、0≤y≤0.30)表示。此外,镍锰复合化合物可以为氢氧化物和氧化物中的至少一者。
混合物调制工序(S10B)中所使用的含钛的镍锰复合化合物中,作为氢(H)和氧(O)以外的元素,含有镍(Ni)、锰(Mn)和钛(Ti),且任意地含有作为选自Co、V、Mg、Mo、Ca、Cr、Zr、Ta、Na、W、Fe、Zn、B、Si、P和Al中的至少1种元素的元素M(M)。此外,所含有的上述元素的物质量之比优选由Ni:Mn:M:Ti=(1-x-y-z'):x:y:z'(其中,0≤x≤0.30、0≤y≤0.30、0.005≤z'≤0.05)表示。此外,含钛的镍锰复合化合物可以为氢氧化物和氧化物中的至少一者。
混合物调制工序(S10C)中所使用的含铌的镍锰复合氢氧化物中,作为羟基(OH)以外的元素,含有镍(Ni)、锰(Mn)和铌(Nb),且任意地含有作为选自Co、V、Mg、Mo、Ca、Cr、Ta、Na、W、Fe、Zn、B、Si、P、Zr和Al中的至少1种元素的元素M(M)。此外,所含有的上述元素的物质量之比优选由Ni:Mn:M:Nb=(1-x-y-w’):x:y:w’(其中,0.03≤x≤0.30、0≤y≤0.30、0.001<w’≤0.03)表示。此外,含铌的镍锰复合化合物可以为氢氧化物和氧化物中的至少一者。
镍锰复合化合物中的各个元素(Ni、Mn、M)的含量(组成)在锂镍锰复合氧化物的粒子中也会被大体维持,因此各元素(Ni、Mn、M)的含量优选为与上述锂镍锰复合氧化物中的含量同样的范围。需说明的是,本实施方式中所使用的镍锰复合化合物可以在不损害本发明的效果的范围内少量含有除上述元素(Ni、Mn、M)、氢以及氧以外的元素。
作为镍锰复合化合物,如上所述,可以使用通过晶析工序(S1A)或(S1B)得到的镍锰复合氢氧化物,也可以使用通过被覆工序(S3)得到的镍锰复合氢氧化物。此外,可以使用在热处理工序(S2)后得到的镍锰复合氢氧化物和镍锰复合氧化物中的至少一者。需说明的是,镍锰复合化合物可以通过上述晶析工序(S1A、S1B)和/或热处理工序(S2)等来获得,但也可以通过其他的方法获得。
此外,镍锰复合化合物优选在其粒子内分别均匀地含有镍和锰。例如,在使用将镍氢氧化物粒子与锰化合物分别混合而成的混合物、由锰化合物被覆的镍氢氧化物粒子等作为原料的情况下,有时所得的正极活性物质中的锰的分布不均匀而无法充分获得由于含有锰而得到的效果。
(钛化合物)
作为钛化合物,可以使用含钛的公知的化合物,例如,可以使用氧化钛、硫酸钛、四溴化钛、四氯化钛、硅化钛等。需说明的是,钛化合物可以使用1种,也可以使用2种以上。
它们中,从获取的容易性、避免杂质混入至锂镍锰复合氧化物中这样的观点出发,优选为氧化钛。需说明的是,在锂镍锰复合氧化物中混入了杂质的情况下,可能导致所得的二次电池的热稳定性、电池容量、循环特性的降低。
钛化合物优选以粒子(固相)混合。在将钛进行固相添加的情况下,烧成工序(S20)中的反应性会因钛化合物的粒径而发生变化,因此所使用的钛化合物的粒径是重要的要素之一。钛化合物的平均粒径优选为0.01μm以上5μm以下,更优选为0.05μm以上3μm以下,进一步优选为0.08μm以上1μm以下。在平均粒径小于0.01μm的情况下,可能发生粉末的操作变得非常困难这样的问题、混合物调制工序(S10)以及烧成工序(S20)中钛化合物飞散而在活性物质中无法添加目标组成的问题。另一方面,在平均粒径大于5μm的情况下,有可能钛在烧成后的锂镍锰复合氧化物中分布不均匀而电池容量降低。需说明的是,平均粒径是体积平均粒径(Mv),例如,可以从由激光衍射散射式粒度分布计测定的体积积分值求出。
钛化合物可以预先使用球磨机、行星式球磨机、喷射式磨机/纳米喷射式磨机、珠磨机、钉盘式磨机等各种粉碎机而粉碎成上述范围的粒径。此外,钛化合物视需要可以通过干式分级器、过筛来进行分级。例如,可以使用干式分级器来获得接近于1μm的粒子。
(铌化合物)
作为铌化合物,可以使用含铌的公知的化合物,例如,可以使用铌酸、氧化铌、硝酸铌、五氯化二铌、硝酸铌等。它们中,从获取的容易性、避免杂质混入至锂镍锰复合氧化物中这样的观点出发,铌化合物优选为氧化铌、铌酸或它们的混合物。需说明的是,在锂镍锰复合氧化物中混入了杂质的情况下,可能导致所得的二次电池的热稳定性、电池容量、循环特性的降低。
铌化合物优选以粒子(固相)混合。在将铌进行固相添加的情况下,后续的烧成工序(步骤S20)中的反应性会因铌化合物的粒径而发生变化,因此所使用的铌化合物的粒径是重要的要素之一。铌化合物的平均粒径优选为0.01μm以上20μm以下,更优选为0.08μm以上5μm以下,进一步优选为0.10μm以上3μm以下。在平均粒径小于0.01μm的情况下,可能发生粉末的操作变得非常困难这样的问题、混合物调制工序(S10)以及烧成工序(S20)中铌化合物飞散而在活性物质中无法添加目标组成的问题。另一方面,在平均粒径大于10μm的情况下,有可能Nb在烧成后的锂镍锰复合氧化物中分布不均匀而无法确保热稳定性。需说明的是,平均粒径是体积平均粒径(Mv),例如,可以从由激光衍射散射式粒度分布计测定的体积积分值求出。
铌化合物可以预先使用球磨机、行星式球磨机、喷射式磨机/纳米喷射式磨机、珠磨机、钉盘式磨机等各种粉碎机而粉碎成上述范围的粒径。此外,铌化合物视需要可以通过干式分级器、过筛来进行分级。例如,可以使用干式分级器来获得平均粒径接近于0.05μm的粒子。
(包含元素M的化合物)
作为包含元素M的化合物,可以使用包含元素M的公知的化合物,例如,可以使用氧化钴、五氧化二钒、氧化镁、氧化钼、氧化钙、碳酸钙、氧化铬、五氧化二钽、碳酸钠、三氧化钨、氧化铁、氧化锌、硼酸、氧化硼、氧化硅、磷酸、氧化锆等。需说明的是,在锂镍锰复合氧化物中混入了杂质的情况下,可能导致所得的二次电池的热稳定性、电池容量、循环特性的降低。
元素M可以使用包含元素M的化合物以粒子(固相)进行混合,也可以通过前述的方法包含在镍锰复合氢氧化物中。在将包含元素M的化合物进行固相添加的情况下,后续的烧成工序(步骤S20)中的反应性会因包含元素M的化合物的粒径而发生变化,因此优选适宜调整所使用的包含元素M的化合物的粒径。此外,在混合物调制工序(S10)中混合包含元素M的化合物的情况下,优选以镍锰复合化合物和包含元素M的化合物中所含有的元素M的物质量的合计成为上述锂镍锰复合化合物中的元素M的物质量之比的范围的方式混合包含元素M的化合物。
包含元素M的化合物可以预先使用球磨机、行星式球磨机、喷射式磨机/纳米喷射式磨机、珠磨机、钉盘式磨机等各种粉碎机而粉碎成上述范围的粒径。此外,包含元素M的化合物视需要可以通过干式分级器、过筛来进行分级。
(锂化合物)
锂化合物没有特别限定,可以使用包含锂的公知的化合物,例如,可使用碳酸锂、氢氧化锂、硝酸锂或它们的混合物等。它们中,从残留杂质的影响小、在烧成温度下溶解这样的观点出发,优选为碳酸锂、氢氧化锂或它们的混合物。
(混合方法)
上述化合物的混合方法没有特别限定,只要以使这些粒子的骨架不被破坏的程度将这些粒子充分混合即可。作为混合方法,例如,可以使用一般的混合机进行混合,例如,可以使用振动混合器、罗迪格(Lodige)混合机、Julia混合机、V式掺混机等进行混合。需说明的是,钛混合物优选在后述的烧成工序前已充分混合。在混合不充分的情况下,有时会发生在正极活性物质的各个粒子间Li与Li以外的金属元素(Me:本实施方式中Me=Ni Mn 元素M Ti Nb)的物质量比(原子%比)即Li/Me产生偏差,无法获得充分的电池特性等问题。
在不进行后述的水洗工序(S30)的情况下,锂化合物以混合物中的Li/Me成为0.97以上1.25以下的方式混合。即,以混合物中的Li/Me成为与要获得的正极活性物质中的Li/Me相同的方式混合。这是因为,在烧成工序(S20)前后,Li/Me以及各金属元素的摩尔比不会变化,因此混合物调制工序(S10)中的混合物的Li/Me就是正极活性物质的Li/Me。
此外,在进行水洗工序(S30)的情况下,锂镍复合氧化物的表面存在的剩余锂成分的一部分溶解于水,因此与烧成工序(S20)后的锂镍复合氧化物相比,Li/Me比可能会降低。该Li/Me比的降低幅度根据锂镍复合氧化物的组成、物性、以及水洗条件而变化,本实施方式的制造方法的一例中,由于水洗工序(S30)而降低大致0.02左右。
此外,混合物中,以相对于除了锂以外的上述金属元素的物质量(Ni、Mn、元素M、Ti和Nb)的合计,钛的物质量的比例(z)以及铌的物质量的比例(w)满足0.005≤z≤0.05、0.001<w≤0.03、(z w)≤0.06且z>w的方式调整钛化合物和铌化合物的混合量。此外,混合物中,铌的物质量的比例(c)可以为0.002≤c≤0.03。
需说明的是,混合物中的铌(Nb)和钛(Ti)的含量(比例)在锂镍锰复合氧化物中也被大体维持。因此,混合物调制工序(S10A)中的铌化合物和钛化合物的混合量优选为与上述锂镍锰复合氧化物中的铌和钛的含量同样的范围。
此外,混合物调制工序(S10B)中的、混合物整体所含的钛的物质量可以与含钛的镍锰复合化合物中所含的钛的物质量相同。此外,在混合物调制工序(S10B)中进一步混合钛化合物的情况下,可以与含钛的镍锰复合化合物和混合的钛化合物所含的钛的物质量的合计相同。
此外,混合物调制工序(S10C)中的、混合物整体所含的铌的物质量可以与含铌的镍锰复合化合物中所含的铌的物质量相同。此外,在混合物调制工序(S10C)中进一步混合铌化合物的情况下,可以与含铌的镍锰复合化合物和混合的铌化合物所含的铌的物质量的合计相同。
[烧成工序(S20)]
烧成工序(S20)是将混合物调制工序(S10)中得到的混合物进行烧成而获得锂镍锰复合氧化物的工序。
如果将混合物烧成,则锂化合物中的锂会在镍锰复合化合物中扩散,因此形成由多晶结构的粒子构成的锂镍锰复合氧化物。锂化合物在烧成时的温度下熔融,渗透至镍锰复合化合物内而形成锂镍锰复合氧化物。锂化合物在烧成时的温度下熔融,渗透至镍锰复合化合物内而形成锂镍锰复合氧化物。此时,锂混合物中所含的铌、钛也与熔融的锂化合物一起渗透至二次粒子内部,如果在一次粒子中存在晶界等,则也认为会发生渗透。
烧成气氛优选氧浓度为80体积%以上100体积%以下,更优选氧浓度为90体积%以上100体积%以下。镍比率高的锂镍锰复合氧化物中,容易发生Ni等过渡金属元素在层状化合物中的Li点位进行排列的、所谓阳离子混排。此外,层状化合物的结晶性降低,原子分布容易发生错乱。由于这种结构的错乱,认为钛等无法在Me点位(过渡金属元素点位)均匀固溶,电池容量降低。另一方面,以上述氧浓度范围进行烧成的情况下,能够获得在维持高电池容量的同时提高热稳定性,兼具高电池容量和热稳定性的正极活性物质。
烧成温度在氧化气氛中为750℃以上1000℃以下,优选为750℃以上950℃以下。在以上述温度进行烧成的情况下,发生锂化合物的熔融,促进钛的渗透和扩散。此外,混合物通过包含锰,从而能够提高烧成温度。烧成温度能够在上述范围内适宜调整,通过提高烧成温度,可促进钛和铌的扩散。进一步,锂镍锰复合氧化物的结晶性变高,能够更加提高电池容量。
另一方面,在烧成温度小于750℃的情况下,锂、钛、锰向镍锰复合化合物中的扩散不会充分进行,剩余的锂、未反应的粒子残留,或者晶体结构不够整齐,从而产生无法获得充分的电池特性这样的问题。此外,在烧成温度大于1000℃的情况下,在所形成的锂镍锰复合氧化物的粒子间剧烈地发生烧结,并且有可能发生异常粒子生长。如果发生异常粒子生长,则产生如下问题:烧成后的粒子会变得粗大,在形成正极活性物质时填充性降低,此外,由于晶体结构的错乱而反应电阻增加,放电容量降低。
烧成时间优选设为至少3小时以上,更优选为6小时以上24小时以下。在烧成时间小于3小时的情况下,有可能无法充分进行锂镍锰复合氧化物的生成。此外,烧成中所使用的炉没有特别限定,只要能够在氧气流中将钛混合物烧成即可,优选使用不产生气体的电炉,可以使用分批式或连续式炉中的任一种。
[压缩至4.0g/cm3时的体积电阻率]
烧成后得到的锂镍锰复合氧化物的压缩至4.0g/cm3时的体积电阻率为5.0×102Ω·cm以上1.0×105Ω·cm以下,优选为1.0×103Ω·cm以上1.0×104Ω·cm以下,更优选为2.0×103Ω·cm以上1.0×104Ω·cm以下。在锂镍锰复合氧化物的体积电阻率为上述范围的情况下,能够获得短路时的高的热稳定性。
需说明的是,关于体积电阻率,例如,可以在4.5g以上5.5g以下的范围内称量正极活性物质,以成为4.0g/cm3的方式加压成型为直径20mm的圆柱状后,以加压的状态由依据JIS K 7194:1994的利用4探针法的电阻率试验方法进行测定而求出。
[预烧]
需说明的是,烧成工序(S20)中,在以750℃以上1000℃以下的温度进行烧成前,可以进一步包括以比上述烧成温度更低的温度进行预烧的工序。预烧优选在混合物中的锂化合物发生熔融、且可与镍锰复合化合物发生反应的温度下进行。预烧的温度例如可以设为350℃以上且比烧成温度更低的温度。此外,预烧的温度的下限优选为400℃以上。通过以上述温度范围保持(预烧)混合物,从而锂化合物能够渗透至镍锰复合化合物中,充分进行锂的扩散,获得均匀的锂镍锰复合氧化物。例如,在使用氢氧化锂作为锂化合物的情况下,预烧优选通过在400℃以上550℃以下的温度下保持1小时以上10小时左右来进行。
[破碎]
需说明的是,烧成工序(S20)后得到的锂镍锰复合氧化物虽然抑制了粒子间的烧结,但有时会由弱的烧结、凝聚而形成粗大的粒子。在这样的情况下,可以通过破碎来解除上述烧结、凝聚从而调整粒度分布。
此外,本实施方式的制造方法可以如以下说明的那样在烧成工序(S20)后具备水洗工序(S30)以及干燥工序(S40)。通过具备这些工序,从而能够提高放电容量,由此能够兼具高的热稳定性和更高的电池容量。以下,对各工序进行说明。
[水洗工序(S30)]
水洗工序(S30)是将烧成工序(S20)中得到的锂镍锰复合氧化物与水混合并进行搅拌(以下,称为“水搅拌”。)后,进行固液分离的工序。
本实施方式的制造方法通过具备水洗工序(S30)以及后述的干燥工序(S40),从而正极活性物质的结晶性提高,且放电容量提高。虽然其详细情况并不明确,但认为例如在通过水搅拌而引出正极活性物质中的锂时,由于原子排列的错乱得到缓和而正极活性物质的结晶性提高,显示出高放电容量。此外,通过利用水洗工序(S30)将表面的剩余锂成分溶解于水而去除,能够抑制制作二次电池的极板时的正极合材糊剂的凝胶化。
水洗工序(S30)中所混合的水的量相对于锂镍锰复合氧化物150质量份优选为50质量份以上200质量份以下。在水的混合比例为200质量份以上的情况下,会从正极活性物质中引出过量的锂,有可能会引起电池容量的下降、反应电阻的升高。另一方面,在水的混合比例小于50质量份的情况下,提高结晶性的效果、剩余锂成分的去除会不充分,有可能会引起电池容量的下降、正极合材糊剂的凝胶化。此外,水洗工序(S30)中所混合的水的量相对于锂镍锰复合氧化物100质量份可以为50质量份以上200质量份以下。
水洗的时间没有特别限定,例如为1分钟以上2小时以下的程度,可以为5分钟以上50分钟以下。
在将锂镍锰复合氧化物进行水搅拌后,进行固液分离而获得锂镍锰复合氧化物(沉淀物)。固液分离的方法没有特别限定,可以使用公知的方法。例如,可以使用选自Nutsche过滤器(布氏漏斗)等吸滤机、压滤机、离心分离机等中的1种以上来进行固液分离。
[干燥工序(S40)]
干燥工序(S40)是使由上述水洗工序(S30)得到的锂镍锰复合氧化物(沉淀物)干燥而获得锂金属复合氧化物的粉末(干燥粉末)的工序。
干燥条件优选在氧化性气氛或真空气氛中在100℃以上250℃以下的温度下进行热处理。在干燥温度为100℃以上的情况下,能够使沉淀物中的水分充分蒸发。此外,在干燥温度为250℃以下的情况下,可以使用紧凑的干燥装置,适合于工业规模的实施。
干燥时的气氛优选为不含水蒸气、二氧化碳的气氛以避免气氛中的水分、碳酸与所得的正极活性物质的反应,具体优选设为氧气气氛等那样的氧化性气氛或真空气氛。此外,从能够快速排出由干燥产生的水蒸气这样的观点出发,优选在干燥装置上附加排气机构。
干燥时间没有特别限定,为了使原料混合物的水分充分蒸发,优选设为在干燥时的最高达到温度下0.5小时以上。此外,从生产率的观点出发,干燥时间的上限优选设为48小时以下。
3.锂离子二次电池
本实施方式的锂离子二次电池(以下,也称为“二次电池”。)具备包含上述正极活性物质的正极、负极以及非水系电解质。二次电池例如具备正极、负极以及非水系电解液。此外,二次电池例如可以具备正极、负极以及固态电解质。此外,二次电池只要是通过锂离子的脱离和嵌入而进行充放电的二次电池即可,例如,可以为非水系电解液二次电池,也可以为全固态锂二次电池。需说明的是,以下说明的实施方式仅为例示,本实施方式的二次电池也可以适用于以本说明书中记载的实施方式为基础实施了各种变更、改良的形态。
[正极]
使用上述的正极活性物质制作二次电池的正极。以下,对正极的制造方法的一例进行说明。
首先,将上述正极活性物质、导电材料和粘结剂混合,进而视需要添加活性炭、以粘度调节等为目的的溶剂,将它们混炼而制作正极合材糊剂。此时,可以根据作为目标的二次电池的性能来适宜调整正极合材糊剂中的各自的混合比。例如,在将除溶剂以外的正极合材的固体成分设为100质量份的情况下,可以将正极活性物质的含量设为60质量份以上95质量份以下,将导电材料的含量设为1质量份以上20质量份以下,将粘结剂的含量设为1质量份以上20质量份以下。
将所得的正极合材糊剂例如涂布于铝箔制的集电体的表面,干燥而使溶剂飞散,制作片状的正极。根据需要,有时也利用辊压机等进行加压以提高电极密度。如此得到的片状的正极可以根据作为目标的电池而以适当的大小进行裁切等,供于电池的制作。但是,正极的制作方法不限于上述例示,也可以依据其他方法。
作为导电材料,例如,可以使用石墨(天然石墨、人造石墨以及膨胀石墨等)、乙炔黑、科琴黑等炭黑系材料等。
作为粘结剂(粘合剂),起到将活性物质粒子连结在一起的作用,例如,可以使用聚偏二氟乙烯(PVDF)、聚四氟乙烯(PTFE)、氟橡胶、乙烯丙烯二烯橡胶、苯乙烯丁二烯、纤维素系树脂以及聚丙烯酸等。
根据需要,在正极合材中添加使正极活性物质、导电材料以及活性炭分散且溶解粘结剂的溶剂。作为溶剂,具体可以使用N-甲基-2-吡咯烷酮等有机溶剂。此外,正极合材中可以添加活性炭以使双电层容量增加。
[负极]
作为负极,可以使用金属锂、锂合金等。此外,作为负极,可以使用如下形成的负极,即:在能够吸藏和脱离锂离子的负极活性物质中混合粘结剂,加入适当的溶剂而制成糊剂状的负极合材,将该负极合材涂布于铜等金属箔集电体的表面,进行干燥,根据需要进行压缩以提高电极密度,从而形成负极。
作为负极活性物质,例如,可以使用天然石墨、人造石墨和酚醛树脂等的有机化合物烧成体、以及焦炭等碳物质的粉状体。该情况下,作为负极粘结剂,与正极同样,可以使用PVDF等含氟树脂,作为使这些活性物质和粘结剂分散的溶剂,可以使用N-甲基-2-吡咯烷酮等有机溶剂。
[隔膜]
在正极与负极之间,夹着隔膜进行配置。隔膜用于将正极与负极分离,并保持电解质,可以使用公知的物质,例如,可以使用聚乙烯、聚丙烯等薄的膜、且具有大量微小的孔的膜。
[非水系电解质]
作为非水系电解质,例如可以使用非水系电解液。非水系电解液是将作为支持盐的锂盐溶解于有机溶剂而得到的溶液。此外,作为非水系电解液,可以使用在离子液体中溶解有锂盐的溶液。需说明的是,离子液体是指,由锂离子以外的阳离子和阴离子构成且在常温下也为液体状的盐。
作为有机溶剂,可以单独使用选自碳酸亚乙酯、碳酸亚丙酯、碳酸亚丁酯和三氟碳酸亚丙酯等环状碳酸酯、以及碳酸二乙酯、碳酸二甲酯、碳酸甲乙酯和碳酸二丙酯等链状碳酸酯、以及四氢呋喃、2-甲基四氢呋喃和二甲氧基乙烷等醚化合物、甲基乙基砜、丁烷磺酸内酯等硫化合物、磷酸三乙酯、磷酸三辛酯等磷化合物等中的1种,或者可以混合使用2种以上。
作为支持盐,可以使用LiPF6、LiBF4、LiClO4、LiAsF6、LiN(CF3SO2)2以及它们的复合盐等。进一步,非水系电解液也可以包含自由基捕获剂、表面活性剂以及阻燃剂等。
此外,作为非水系电解质,也可以使用固态电解质。固态电解质具有可耐受高电压的性质。作为固态电解质,可举出无机固态电解质、有机固态电解质。
作为无机固态电解质,可举出氧化物系固态电解质、硫化物系固态电解质等。
作为氧化物系固态电解质,没有特别限定,可以合适地使用例如含有氧(O)且具有锂离子传导性和电子绝缘性的电解质。作为氧化物系固态电解质,例如,可以使用选自磷酸锂(Li3PO4)、Li3PO4NX、LiBO2NX、LiNbO3、LiTaO3、Li2SiO3、Li4SiO4-Li3PO4、Li4SiO4-Li3VO4、Li2O-B2O3-P2O5、Li2O-SiO2、Li2O-B2O3-ZnO、Li1 XAlXTi2-X(PO4)3(0≤X≤1)、Li1 XAlXGe2-X(PO4)3(0≤X≤1)、LiTi2(PO4)3、Li3XLa2/3-XTiO3(0≤X≤2/3)、Li5La3Ta2O12、Li7La3Zr2O12、Li6BaLa2Ta2O12、Li3.6Si0.6P0.4O4等中的1种以上。
作为硫化物系固态电解质,没有特别限定,可以合适地使用例如含有硫(S)且具有锂离子传导性和电子绝缘性的电解质。作为硫化物系固态电解质,例如,可以使用选自Li2S-P2S5、Li2S-SiS2、LiI-Li2S-SiS2、LiI-Li2S-P2S5、LiI-Li2S-B2S3、Li3PO4-Li2S-Si2S、Li3PO4-Li2S-SiS2、LiPO4-Li2S-SiS、LiI-Li2S-P2O5、LiI-Li3PO4-P2S5等中的1种以上。
需说明的是,作为无机固态电解质,也可以使用上述以外的物质,例如,可以使用Li3N、LiI、Li3N-LiI-LiOH等。作为有机固态电解质,只要是显示离子传导性的高分子化合物就没有特别限定,例如,可以使用聚环氧乙烷、聚环氧丙烷、它们的共聚物等。此外,有机固态电解质也可以包含支持盐(锂盐)。
需说明的是,也可以使用固态电解质代替非水系电解液来构成二次电池。固态电解质即使在高电位下也不会分解,因此不会如在非水系电解液中看到的那样在充电时由于电解液的分解而导致产生气体、热失控,因此具有高的热稳定性。因此,在用于使用了本发明的正极活性物质的锂离子二次电池的情况下,能够获得热稳定性更高的二次电池。
[二次电池的形状、构成]
二次电池的构成没有特别限定,如上所述,可以由正极、负极、隔膜、非水系电解质等构成,也可以由正极、负极、固态电解质等构成。此外,二次电池的形状没有特别限定,可以制成圆筒形、层叠形等各种各样的形状。
例如,在二次电池为非水系电解液二次电池的情况下,使正极和负极隔着隔膜层叠而制成电极体,使非水系电解液含浸于所得的电极体,使用集电用引线等将正极集电体与通向外部的正极端子之间以及负极集电体与通向外部的负极端子之间连接,并密封于电池盒,从而完成二次电池。
需说明的是,本实施方式的二次电池不限定于使用非水系电解液作为非水系电解质的形态,也可以制成例如使用固体的非水系电解质的二次电池,即全固态电池。在制成全固态电池的情况下,正极活性物质以外的构成可以根据需要进行变更。
本实施方式的二次电池能够以低成本实现高的热稳定性。此外,用于二次电池的正极活性物质可以通过上述工业性制造方法来获得。此外,二次电池适合于总是要求高容量的小型便携式电子设备(笔记本型个人电脑、手机终端等)的电源。此外,二次电池与以往使用锂钴系氧化物或锂镍系氧化物的正极活性物质的电池相比,不仅是容量优异,耐久性和过充电时的热稳定性也优异。因此,由于能够小型化、高容量化,因而适合作为搭载空间受到制约的电动汽车用电源。需说明的是,二次电池不仅可以用作纯粹以电能驱动的电动汽车用电源,还可以用作与汽油发动机、柴油发动机等燃烧机构并用的所谓的混动汽车用电源。
实施例
以下,利用本发明的实施例和比较例来进一步详细说明本发明,但本发明不受这些实施例的任何限定。需说明的是,实施例和比较例中的正极活性物质所含有的金属的分析方法以及正极活性物质的各种评价方法如下。
(1)组成的分析:通过ICP发光分析法测定。
(2)体积平均粒径(Mv)以及粒径的离散指数〔(D90-D10)/平均体积粒径〕:利用激光衍射散射式粒度分布测定装置(日机装株式会社制,MICROTRAC HRA)按照体积基准来进行。
(3)各元素的浓度
将正极活性物质加工成能够利用S-TEM进行一次粒子的截面分析。从正极活性物质所含的多个二次粒子中任意选择20个一次粒子,利用S-TEM的EDX对各个包含一次粒子截面的内部和粒界的区域(130nm×130nm)的组成进行点分析。
(4)体积电阻率:将5g正极活性物质以成为4.0g/cm3的方式加压成型为直径20mm的圆柱状后,以加压的状态由依据JIS K 7194:1994的利用4探针法的电阻率试验方法进行测定而求出。
(5)溶出锂量:
取2g正极活性物质,投入至利用搅拌器搅拌的室温的纯水125ml中,在投入活性物质后立即使用浓度1mol/L的HCl水溶液进行滴定。滴定使用自动滴定装置COM-1750(平沼产业株式会社制)按照以下的条件实施。
终点检测方法:拐点检测
检测灵敏度:2500
滴管型号:H-1700
滴管速度:2
最小滴加量:0.013mL
通过Warder法评价滴定结果,算出氢氧化锂(LiOH)和碳酸锂(Li2CO3),将这些锂量之和作为溶出锂来算出。
(6)初始放电容量:
关于初始充电容量和初始放电容量,按照以下方法制作图16所示的纽扣型电池CBA后放置24小时左右,开路电压OCV(open circuit voltage)稳定后,以对于正极的电流密度为0.1mA/cm2进行充电直至截止电压4.3V,设为初始充电容量,暂停1小时后,将放电至截止电压3.0V时的容量设为初始放电容量。放电容量的测定中,使用多通道电压/电流发生器(株式会社Advantest制、R6741A)。
(纽扣型电池的制作)
将所得的正极活性物质52.5mg、乙炔黑15mg和聚四氟乙烯树脂(PTFE)7.5mg混合,以100MPa的压力加压成型为直径11mm、厚度100μm,制作图16所示的正极(评价用电极)PE。将所制作的正极PE在真空干燥机中以120℃干燥12小时后,使用该正极PE在露点被管理在-80℃的Ar气氛的手套箱内制作2032型纽扣型电池CBA。作为负极NE,使用直径17mm厚度1mm的锂(Li)金属,作为电解液,使用以1M的LiClO4作为支持电解质的碳酸亚乙酯(EC)与碳酸二乙酯(DEC)的等量混合液(富山药品工业株式会社制)。作为隔膜SE,使用膜厚25μm的聚乙烯多孔膜。此外,纽扣型电池CBA是通过配置垫圈GA和波形垫片WW,且利用正极壳PC和负极壳NC而组装成纽扣型的电池。
(7)最大氧产生峰值温度
正极的热稳定性评价如下进行:使正极活性物质成为过充电状态并进行加热,对由此释放出的氧量进行定量。与(5)同样地制作纽扣型电池,以0.05C速率进行CC充电(恒流-恒压充电)至截止电压4.3V。然后,将纽扣电池拆解,小心地仅取出正极以免短路,利用DMC(碳酸二甲酯)清洗,并进行干燥。量取约2mg干燥后的正极,使用气相色谱质谱仪(GCMS,岛津制作所,QP-2010plus),以升温速度10℃/min从室温升温至450℃。将氦气用作载气。测定加热时产生的氧(m/z=32)的产生行为,得到最大氧产生峰值温度。
(实施例1A)
[晶析工序]
在反应槽(60L)中加入预定量纯水,在搅拌的同时将槽内温度设定在49℃。此时,在反应槽内通入N2气体以使反应槽液中的溶解氧浓度成为0.8mg/L。向该反应槽内,将以镍:锰:钴的摩尔比成为85:10:5的方式配合的硫酸镍、硫酸锰、硫酸钴的2.0M的混合水溶液以及作为碱溶液的25质量%氢氧化钠溶液、作为络合剂的25质量%氨水同时地连续地添加于反应槽,通过连续晶析法进行晶析。
此时以混合水溶液的停留时间成为8小时的方式控制流量,将反应槽内的pH调整为12.0~12.6,将氨浓度调整为10~14g/L。反应槽稳定后,从溢流口回收包含镍锰钴复合氢氧化物的浆料后,进行过滤,得到镍锰钴复合氢氧化物的滤饼。对于进行了过滤后的滤布(Denver)内的镍锰钴复合氢氧化物140g通液1L的纯水,从而进行杂质的清洗。将过滤后的粉末干燥,得到镍、锰、钴的物质量之比由Ni:Mn:Co=0.85:0.10:0.05表示的镍锰钴复合氢氧化物的粒子。
[混合物调制工序]
以锂:(镍 锰 钴):钛:铌的物质量之比成为1.01:0.973:0.022:0.005的方式称量所得的镍锰钴复合氢氧化物的粒子、氢氧化锂、氧化钛(TiO2)以及铌酸(Nb2O5·4H2O)后,使用振动混合器装置(Willy A Bachofen(WAB)公司制TURBULA T2C型)进行充分混合,得到锂混合物。
[烧成工序]
将所得的锂混合物在氧(氧浓度:90容量%)气流中以850℃保持10小时进行烧成,然后破碎而得到锂镍锰钴复合氧化物的粒子(正极活性物质)。
[评价]
将正极活性物质的制造条件示于表1中,将对于所得的正极活性物质由上述评价方法进行评价得到的结果示于表2中。需说明的是,对于下表的各元素的物质量比,示出将测定值的小数第四位进行四舍五入而得的数值,对于Ti/Nb物质量比,示出将由Ti和Nb的物质量比的测定值算出的比率的小数第二位进行四舍五入而得的数值。
(实施例2A)
在烧成工序中,将烧成温度设为870℃,除此以外,与实施例1A同样地得到正极活性物质并进行评价。将正极活性物质的制造条件以及评价结果示于表1、2中。
(实施例3A)
在烧成工序中,将烧成温度设为890℃,除此以外,与实施例1A同样地得到正极活性物质并进行评价。将正极活性物质的制造条件以及评价结果示于表1、2中。
(实施例4A)
在混合物调制工序中,以锂:(镍 锰 钴):钛:铌的物质量之比成为1.02:0.975:0.022:0.003的方式称量所得的镍锰钴复合氢氧化物的粒子、氢氧化锂、氧化钛(TiO2)以及铌酸(Nb2O5·4H2O),除此以外,与实施例2A同样地得到正极活性物质并进行评价。将正极活性物质的制造条件以及评价结果示于表1、2中。
(实施例5A)
在混合物调制工序中,使用氧化铌(Nb2O5)作为铌化合物,除此以外,与实施例2A同样地得到正极活性物质并进行评价。将正极活性物质的制造条件以及评价结果示于表1、2中。
(实施例6A)
在烧成工序中,在氧(氧浓度:60容量%)气流中进行烧成,除此以外,与实施例2A同样地得到正极活性物质并进行评价。将正极活性物质的制造条件以及评价结果示于表1、2中。
(比较例1A)
在混合物调制工序中,不准备钛化合物和铌化合物而以锂:镍:锰:钴的物质量之比成为1.02:0.85:0.10:0.05的方式称量所得的镍锰钴复合氢氧化物的粒子以及氢氧化锂,且在烧成工序中,将烧成温度设为800℃,除此以外,与实施例1A同样地得到正极活性物质并进行评价。将正极活性物质的制造条件以及评价结果示于表1、2中。
(比较例2A)
在混合物调制工序中,不准备铌化合物而以锂:(镍 锰 钴):钛的物质量之比成为1.02:0.974:0.026的方式称量所得的镍锰钴复合氢氧化物的粒子、氢氧化锂以及氧化钛(TiO2),且在烧成工序中,将烧成温度设为830℃,除此以外,与实施例1A同样地得到正极活性物质并进行评价。将正极活性物质的制造条件以及评价结果示于表1、2中。
(比较例3A)
在混合物调制工序中,不准备钛化合物而以锂:(镍 锰 钴):铌的物质量之比成为1.02:0.99:0.010的方式称量所得的镍锰钴复合氢氧化物的粒子、氢氧化锂以及铌酸(Nb2O5·4H2O),且在烧成工序中,将烧成温度设为850℃,除此以外,与实施例1A同样地得到正极活性物质并进行评价。将正极活性物质的制造条件以及评价结果示于表1、2中。
(比较例4A)
在混合物调制工序中,以锂:(镍 锰 钴):钛:铌的物质量之比成为1.01:0.977:0.022:0.001的方式称量所得的镍锰钴复合氢氧化物的粒子、氢氧化锂、氧化钛(TiO2)以及铌酸(Nb2O5·4H2O),且在烧成工序中,将烧成温度设为840℃,除此以外,与实施例1A同样地得到正极活性物质并进行评价。将正极活性物质的制造条件以及评价结果示于表1、2中。
[表1]
[表2]
(实施例1B)
[晶析工序]
在反应槽(60L)中加入预定量纯水,在搅拌的同时将槽内温度设定在49℃。此时,在反应槽内通入N2气体以使反应槽液中的溶解氧浓度成为0.8mg/L。向该反应槽内,将以镍:锰:钴:钛的摩尔比成为0.833:0.095:0.050:0.022的方式配合的硫酸镍、硫酸锰、硫酸钴、硫酸钛的2.0M的混合水溶液以及作为碱溶液的25质量%氢氧化钠溶液、作为络合剂的25质量%氨水同时地连续地添加于反应槽,通过连续晶析法进行晶析。
此时以混合水溶液的停留时间成为8小时的方式控制流量,将反应槽内的pH调整为12.0~12.6,将氨浓度调整为10~14g/L。反应槽稳定后,从溢流口回收包含镍锰钴钛复合氢氧化物的浆料后,进行过滤,得到镍锰钴钛复合氢氧化物的滤饼。对于进行了过滤后的滤布内的镍锰钴钛复合氢氧化物140g通液1L的纯水,从而进行杂质的清洗。将过滤后的粉末干燥,得到镍、锰、钴、钛的物质量之比由Ni:Mn:Co:Ti=0.833:0.095:0.050:0.022表示的镍锰钴钛复合氢氧化物的粒子。
[混合物调制工序]
以锂:(镍 锰 钴 钛):铌的物质量之比成为1.01:0.995:0.005的方式称量所得的镍锰钴钛复合氢氧化物的粒子、氢氧化锂以及铌酸(Nb2O5·4H2O)后,使用振动混合器装置(Willy A Bachofen(WAB)公司制TURBULA T2C型)进行充分混合,得到锂混合物。
[烧成工序]
将所得的锂混合物在氧(氧浓度:90容量%)气流中以850℃保持10小时进行烧成,然后破碎而得到锂镍锰钴复合氧化物的粒子(正极活性物质)。
[评价]
将正极活性物质的制造条件示于表3中,将对于所得的正极活性物质由上述评价方法评价的结果示于表4中。
(实施例2B)
在烧成工序中,将烧成温度设为870℃,除此以外,与实施例1B同样地得到正极活性物质并进行评价。将正极活性物质的制造条件以及评价结果示于表3、4中。
(实施例3B)
在烧成工序中,将烧成温度设为890℃,除此以外,与实施例1B同样地得到正极活性物质并进行评价。将正极活性物质的制造条件以及评价结果示于表3、4中。
(实施例4B)
在混合物调制工序中,以锂:(镍 锰 钴 钛):铌的物质量之比成为1.01:0.997:0.003的方式称量所得的镍锰钴钛复合氢氧化物的粒子、氢氧化锂以及铌酸(Nb2O5·4H2O),除此以外,与实施例2B同样地得到正极活性物质并进行评价。将正极活性物质的制造条件以及评价结果示于表3、4中。
(实施例5B)
在混合物调制工序中,使用氧化铌(Nb2O5)作为铌化合物,除此以外,与实施例2B同样地得到正极活性物质并进行评价。将正极活性物质的制造条件以及评价结果示于表3、4中。
(实施例6B)
在烧成工序中,在氧(氧浓度:60容量%)气流中进行烧成,除此以外,与实施例2B同样地得到正极活性物质并进行评价。将正极活性物质的制造条件以及评价结果示于表3、4中。
(实施例1C)
[晶析工序]
在晶析工序中,使添加于反应槽内的2.0M的混合水溶液中不含硫酸钛而以镍:锰:钴的摩尔比成为0.85:0.10:0.05的方式配合硫酸镍、硫酸锰、硫酸钴,除此以外,与实施例1B同样地进行晶析,获得过滤后得到的镍锰钴复合氢氧化物的滤饼。
[被覆工序]
将所得的镍锰钴复合氢氧化物的滤饼分散在纯水中,使用硫酸调整至pH8.2后,以镍:锰:钴:铌的摩尔比成为0.847:0.098:0.050:0.005的方式添加溶解于氢氧化钾溶液的铌酸,将铌化合物被覆于镍锰钴复合氢氧化物。
[混合物调制工序]
以锂:(镍 锰 钴 铌):钛的物质量之比成为1.01:0.978:0.022的方式称量所得的镍锰钴铌复合氢氧化物的粒子、氢氧化锂以及氧化钛(TiO2),除此以外,与实施例1B同样地混合,得到锂混合物。
[烧成工序]
在与实施例2B同样的条件下进行烧成,得到正极活性物质并进行评价。将正极活性物质的制造条件以及评价结果示于表3、4中。
(实施例2C)
在被覆工序中,以镍:锰:钴:铌的摩尔比成为0.848:0.097:0.052:0.003的方式添加溶解于氢氧化钾溶液的铌酸,除此以外,与实施例1C同样地得到正极活性物质并进行评价。将正极活性物质的制造条件以及评价结果示于表3、4中。
(比较例1B)
在晶析工序中不准备硫酸钛水溶液,在混合物调制工序中不准备铌化合物而以锂:镍:锰:钴的物质量之比成为1.01:0.85:0.10:0.05的方式称量所得的镍锰钴复合氢氧化物的粒子以及氢氧化锂,且在烧成工序中,将烧成温度设为800℃,除此以外,与实施例1B同样地得到正极活性物质并进行评价。将正极活性物质的制造条件以及评价结果示于表3、4中。
(比较例2B)
在混合物调制工序中,不准备铌化合物而以锂:(镍 锰 钴 钛)的物质量之比成为1.01:1的方式称量所得的镍锰钴钛复合氢氧化物的粒子以及氢氧化锂,且在烧成工序中,将烧成温度设为830℃,除此以外,与实施例1B同样地得到正极活性物质并进行评价。将正极活性物质的制造条件以及评价结果示于表3、4中。
(比较例3B)
在晶析工序中,不准备硫酸钛水溶液而以锂:(镍 锰 钴):铌的物质量之比成为1.01:0.990:0.010的方式称量所得的镍锰钴复合氢氧化物的粒子、氢氧化锂以及铌酸(Nb2O5·4H2O),且在烧成工序中,将烧成温度设为850℃,除此以外,与实施例1B同样地得到正极活性物质并进行评价。将正极活性物质的制造条件以及评价结果示于表3、4中。
(比较例4B)
在混合物调制工序中,以锂:(镍 锰 钴 钛):铌的物质量之比成为1.01:0.999:0.001的方式称量所得的镍锰钴钛复合氢氧化物的粒子、氢氧化锂以及铌酸(Nb2O5·4H2O),且在烧成工序中,将烧成温度设为840℃,除此以外,与实施例1B同样地得到正极活性物质并进行评价。将正极活性物质的制造条件以及评价结果示于表3、4中。
[表3]
[表4]
(评价结果1)
如表1~4以及图1、2所示,实施例中得到的正极活性物质的压缩时的体积电阻率为5×102Ω·cm以上,并且最大氧产生峰值温度为250℃以上,表明具有高的热稳定性,抑制过充电时的氧释放。
此外,如表1~4、图3所示,在氧浓度为80体积%的气氛下进行烧成的实施例1A~5A、1B~5B、1C、2C中,得到具有184mAh/g以上的高放电容量、且在具有高的热稳定性的同时具有高电池容量的正极活性物质。
图17的(A)、图18的(A)是示出正极活性物质的截面照片的图,这些图中的正方形所包围的部分示出了分析中所使用的位置的一例,通过使用STEM-EDX的点分析来解析正方形所包围的部分中的各元素的浓度(原子%)。图17的(B)、图17的(C)以及图18的(B)、图18的(C)是示出通过使用STEM-EDX的点分析对实施例2A、2B中得到的正极活性物质的截面中的一次粒子的内部(图17的(B):实施例2A、图17的(C):实施例2B)和粒界(图18的(B):实施例2B、图18的(B):实施例2B)的组成进行评价的结果的一例的图。
如图17的(B)、图17的(C)以及图18的(B)、图18的(C)所示,实施例中得到的正极活性物质中,铌在一次粒子间的粒界偏析。此外,如表2、4所示,一次粒子间的粒界处的铌浓度相对于一次粒子内部的铌浓度(粒界的铌浓度/粒内的铌浓度)为1.3倍以上。此外,对于钛而言,没有确认到在一次粒子间的粒界的偏析,一次粒子间的粒界处的钛浓度相对于一次粒子内部的钛浓度(粒界的钛浓度/粒内的钛浓度)小于1.3倍(具体为0.8倍以上1.1倍以下)。
另一方面,比较例1A、1B的正极活性物质中,由于不含钛和铌,因此压缩时的体积电阻率以及最大氧产生峰值温度低,热稳定性不充分。
此外,比较例2A、3A以及2B、3B的正极活性物质中,仅含有钛或铌中的任一者,因此最大氧产生峰值温度以及压缩时的体积电阻率与比较例1相比变得稍高,但比实施例低,不能说短路时的热稳定性是充分的。
此外,比较例4A、4B的正极活性物质中,铌的含量为0.001以下,因此压缩时的体积电阻率以及最大氧产生峰值温度低,热稳定性不充分。
以下,对于进行水洗工序以及干燥工序的实施例11A~实施例11C进行说明。
[实施例11A]
相对于在与实施例2A同样的条件下得到的锂镍锰钴钛复合氧化物150质量份,以100质量份的比例混合水,在水搅拌后使用Nutsche过滤器进行吸滤,得到沉淀物(水洗工序)。将所得的沉淀物放入SUS制容器中,使用真空干燥机加热至100℃静置干燥12小时,加热至190℃静置干燥10小时,从而得到正极活性物质(干燥工序)。将正极活性物质的制造条件以及评价结果示于表5~表7中。需说明的是,在表5~7中作为参考一起示出了实施例2A、比较例1A~4A的正极活性物质的制造条件以及评价结果。
[表5]
[表6]
[表7]
(实施例7B)
[晶析工序]
在反应槽(60L)中加入预定量纯水,在搅拌的同时将槽内温度设定在49℃。此时,在反应槽内通入N2气体以使反应槽液中的溶解氧浓度成为0.8mg/L。向该反应槽内,将以镍:锰:钴:钛的摩尔比成为0.829:0.098:0.050:0.023的硫酸镍、硫酸锰、硫酸钴、硫酸钛的2.0M的混合水溶液以及作为碱溶液的25质量%氢氧化钠溶液、作为络合剂的25质量%氨水同时地连续地添加于反应槽,通过连续晶析法进行晶析。
此时以混合水溶液的停留时间成为8小时的方式控制流量,将反应槽内的pH调整为12.0~12.6,将氨浓度调整为10~14g/L。反应槽稳定后,从溢流口回收包含镍锰钴钛复合氢氧化物的浆料后,进行过滤,得到镍锰钴钛复合氢氧化物的滤饼。对于进行了过滤后的滤布内的镍锰钴钛复合氢氧化物140g通液1L的纯水,从而进行杂质的清洗。将过滤后的粉末干燥,得到镍、锰、钴、钛的物质量之比由Ni:Mn:Co:Ti=0.829:0.098:0.050:0.023表示的含有钛的镍锰钴钛复合氢氧化物的粒子。
[混合物调制工序]
以锂:(镍 锰 钴 钛):铌的物质量之比成为1.01:0.995:0.005的方式称量所得的含有钛的镍锰钴钛复合氢氧化物的粒子、氢氧化锂以及铌酸(Nb2O5·4H2O)后,使用振动混合器装置(Willy A Bachofen(WAB)公司制TURBULA T2C型)进行充分混合,得到锂混合物。
[烧成工序]
将所得的锂混合物在氧(氧浓度:90容量%)气流中以870℃保持10小时进行烧成,然后破碎而得到锂镍锰钴复合氧化物的粒子(正极活性物质)。
[评价]
将正极活性物质的制造条件示于表8中,将所得的正极活性物质的评价结果示于表9、10中。此外,所得的正极活性物质的4.0g/cm3压缩时的体积电阻率为3.5×103(Ω·cm)。
(实施例11B)
相对于在与实施例7B同样的条件下得到的锂镍锰钴钛复合氧化物150质量份,以100质量份的比例混合水,在水搅拌后使用Nutsche过滤器进行吸滤,得到沉淀物(水洗工序)。将所得的沉淀物放入SUS制容器中,使用真空干燥机加热至100℃静置干燥12小时,加热至190℃静置干燥10小时,从而得到正极活性物质(干燥工序)。将正极活性物质的制造条件以及评价结果示于表8~表10中。
(实施例11C)
[晶析工序]
晶析工序中,使添加于反应槽内的2.0M的混合水溶液中不含硫酸钛,而以镍:锰:钴的摩尔比成为0.85:0.10:0.05的方式配合硫酸镍、硫酸锰、硫酸钴,除此以外,与实施例11B同样地进行晶析工序,获得过滤后得到的镍锰钴复合氢氧化物的滤饼。
[被覆工序]
将所得的镍锰钴复合氢氧化物的滤饼分散在纯水中,使用硫酸调整正pH8.2后,以镍:锰:钴:铌的摩尔比成为0.845:0.100:0.050:0.005的方式添加溶解于氢氧化钾溶液的铌酸,将铌化合物被覆于镍锰钴复合氢氧化物。
[混合物调制工序]
以锂:(镍 锰 钴 铌):钛的物质量之比成为1.01:0.978:0.022的方式称量所得的镍锰钴铌复合氢氧化物的粒子、氢氧化锂以及氧化钛(TiO2),除此以外,与实施例1B同样地混合,得到锂混合物。
[烧成工序]
在与实施例11B同样的条件下进行烧成、水洗、干燥,得到正极活性物质并进行评价。将正极活性物质的制造条件以及评价结果示于表8~10中。
(比较例5B)
晶析工序中不准备硫酸钛水溶液,混合物调制工序中不准备铌化合物而以锂:镍:锰:钴的物质量之比成为1.02:0.85:0.10:0.05的方式称量所得的镍锰钴复合氢氧化物的粒子以及氢氧化锂,且在烧成工序中,将烧成温度设为800℃,除此以外,与实施例7B同样地得到正极活性物质并进行评价。所得的正极活性物质的压缩至4.0g/cm3时的体积电阻率为8.5×101Ω·cm。将正极活性物质的制造条件以及评价结果示于表8、9中。
(比较例6B)
在混合物调制工序中不准备铌化合物而以锂:(镍 锰 钴 钛)的物质量之比成为1.02:1的方式称量所得的含有钛的镍锰钴复合氢氧化物的粒子以及氢氧化锂,且在烧成工序中,将烧成温度设为830℃,除此以外,与实施例7B同样地得到正极活性物质并进行评价。所得的正极活性物质的压缩至4.0g/cm3时的体积电阻率为2.1×102Ω·cm。将正极活性物质的制造条件以及评价结果示于表8、9中。
(比较例7B)
在晶析工序中不准备硫酸钛水溶液而以锂:(镍 锰 钴):铌的物质量之比成为1.01:0.991:0.009的方式称量所得的镍锰钴复合氢氧化物的粒子、氢氧化锂以及铌酸(Nb2O5·4H2O),且在烧成工序中,将烧成温度设为850℃,除此以外,与实施例7B同样地得到正极活性物质并进行评价。所得的正极活性物质的压缩至4.0g/cm3时的体积电阻率为3.4×102Ω·cm。将正极活性物质的制造条件以及评价结果示于表8、9中。
(比较例8B)
在混合物调制工序中,以锂:(镍 锰 钴 钛):铌的物质量之比成为1.01:0.999:0.001的方式称量所得的含有钛的镍锰钴复合氢氧化物的粒子、氢氧化锂以及铌酸(Nb2O5·4H2O),且在烧成工序中,将烧成温度设为840℃,除此以外,与实施例7B同样地得到正极活性物质并进行评价。所得的正极活性物质的压缩至4.0g/cm3时的体积电阻率为3.3×102Ω·cm。将正极活性物质的制造条件以及评价结果示于表8、9中。
[表8]
[表9]
[表10]
(评价结果2)
如表6、9以及图4所示,实施例11A~11C中得到的正极活性物质的最大氧产生峰值温度为250℃以上,表明具有高的热稳定性,可抑制过充电时的氧释放。
此外,如表6、9以及图5所示,与未进行水洗以及干燥的实施例2A、实施例7B相比,进行了水洗以及干燥的实施例11A、11B中得到了具有高放电容量、且在具有高的热稳定性的同时具有更高的电池容量的正极活性物质。
此外,如表7、10所示,未进行水洗以及干燥的实施例2A、实施例7B中,溶出锂量大于0.20质量%,而实施例11A、11B、11C中,溶出锂量为0.20质量%以下,显示出剩余锂减少。
另一方面,比较例1A、5B的正极活性物质中,不含钛和铌,因此最大氧产生峰值温度低,热稳定性不充分。
此外,比较例4A、8B的正极活性物质中,铌的含量为0.001以下,因此最大氧产生峰值温度低,热稳定性不充分。
产业上的可利用性
本实施方式中,能够通过工业性制造方法获得具有高的热稳定性和优异的电池特性的锂离子二次电池用正极活性物质。该锂离子二次电池适合于总是要求高容量的小型便携式电子设备(笔记本型个人电脑、手机终端等)的电源。
此外,使用本实施方式的正极活性物质的二次电池与以往使用锂镍系氧化物的正极活性物质的电池相比,热稳定性优异,进而容量方面优异。因此,由于能够小型化,因而适合作为搭载空间受到制约的电动汽车用电源。
此外,使用本实施方式的正极活性物质的二次电池不仅可以用作纯粹以电能驱动的电动汽车用电源,还可以用作与汽油发动机、柴油发动机等燃烧机构并用的所谓的混动汽车用电源、定置型蓄电池。
需说明的是,本发明的技术范围不限定于上述实施方式等中说明的形态。有时会省略上述实施方式等中说明的要件中的1个以上。此外,上述实施方式等中说明的要件可以适宜组合。此外,在法律允许的范围内,援用作为日本专利申请的日本特愿2019-127259、日本特愿2019-236895、日本特愿2020-092692、日本特愿2019-127258、日本特愿2019-236896、日本特愿2020-092693以及本说明书中引用的全部文献内容作为本文的记载的一部分。
符号说明
CBA…纽扣型电池(评价用)
PE…正极(评价用电极)
NE…负极
SE…隔膜
GA…垫圈
WW…波形垫片
PC…正极壳
NC…负极壳
G…空隙。
本文用于企业家、创业者技术爱好者查询,结果仅供参考。