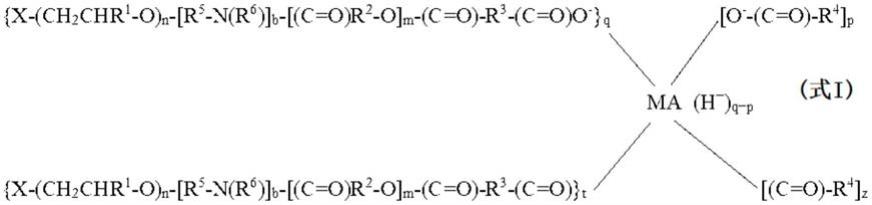1.本发明涉及与聚酯和/或聚醚链反应的多胺物质(聚胺,如聚乙烯亚胺)的分散剂和经由酸酐中间体制备所述分散剂的方法。
背景技术:
2.通常认为聚胺衍生的分散剂作为颜料分散剂是有效的。这些分散剂的空间稳定链的组成和分子量对于有效地将固体分散在极性和非极性的连续介质中来说是重要的。许多配置物(如油墨、油漆、研磨浆和塑料材料)需要分散剂以将颗粒状固体均匀地分布在有机介质中。因此,颜料分散体最好与不同的油墨或涂料配置物相容。
3.还发现具有盐键和酰胺键的混合物的多胺基分散剂提供了更有效的分散剂。然而,使用醇封端的聚合物难以制造这些分散剂。最理想的是具有含有内盐键和酰胺键的分散剂,但它们可以方便地由基于醇封端的聚醚和/或聚酯的聚合物制备。
技术实现要素:
4.本发明提供了一种由醇封端的聚合物制备具有式
5.的分散剂的方法。制备式i分散剂的方法包括以下步骤:(a)提供式x
‑
(ch2chr1‑
o)
n
‑
[r5‑
n(r6)]
b
‑
[(c=o)r2‑
o]
m
‑
h(式ii)的醇封端的聚合物,(b)使醇封端的聚合物与环状酸酐反应以提供酸封端的聚合物,(c)使酸封端的聚合物与非环状酸酐反应提供酸酐混合物,以及(d)使酸酐混合物与多胺物质反应,其中多胺物质具有300至20000的数均分子量以形成分散剂分子,其中q和t是各自至少为一,使得分散剂同时包含酰胺键和盐键。在式ii中,x代表r
‑
q或环状仲胺。当x为r
‑
q时,r为含有1至50个碳原子的支链或直链、饱和或不饱和环烃链,q为o、或nr7、或nh,条件是当n为0和b是0时,q只能是nh,并且r7是包含1至18个碳原子的直链或支链、饱和或不饱和烃链,其可任选地包含醚、酯或酰胺官能团或卤化物取代基。或者,x也可以是衍生自一种或多种环状仲胺的环状胺结构。在式ii中,r1是h、甲基、或乙基,r5是含有最多3个碳原子的直链或支链烃链;r6为氢、含1至22个碳原子的烃基、或(甲基)丙烯酸烷基酯或烷基(甲基)丙烯酰胺的残基。变量b是0或1,条件是当n和m都至少为1时,b只能是1。r2是含1至15个碳原子的直链或支链、饱和或不饱和烃链,或
‑
r8(c=o)yr9‑
,其中y是o或nh或nr
10
,r8是含1至10个碳原子的烃链,r9为含有2至10个碳原子的烃链,r
10
为含有1至20个碳原子的烃链。在一些实施例中,r
10
可包括酯基、醚基或酰胺基。当r2为含有1至15个碳原子的烃链时,在一个实施例中,r2可为含有1至10个碳原子的直链或支链、饱和或不饱和烃链,而
在另一实施例中,r2可为含有2至15个碳原子的烃链,其包括具有式
‑
n(r
11
)
‑
(c=o)
‑
的酰胺官能团,其中r
11
是h或含有1至4个碳原子的烃链。在式ii中,n是0到65之间的任何整数,m是0到35之间的任何整数,条件是m n至少为3。
[0006]
本发明还提供一种具有式i结构的分散剂,其中x为r
‑
q或环状胺。其中,x为r
‑
q,r为含1至50个碳原子的烃链,q为o、或nr7、或nh,条件是当n为0且b为0时,q只能为nh,且r7为含有1至18个碳原子的直链或支链烃链,其可任选地包含醚、酯或酰胺官能团或卤化物取代基。x也可以代表环状仲胺。在式i中,r1为h、甲基或乙基;r5是含有最多3个碳原子的直链或支链烃链;r6为氢、含1至50个碳原子的烃基或(甲基)丙烯酸烷基酯或烷基(甲基)丙烯酰胺的残基;b是0或1,条件是当n和m都至少为1时,b只能是1;r2是含1至15个碳原子的直链或支链、饱和或不饱和烃链或
‑
r8(c=o)yr9‑
,其中y是o、或nh、或nr
10
,r8是含1至10个碳原子的烃链,r9为含有1至10个碳原子的烃链,且r
10
为含有1至20个碳原子的烃链,其可包括酯基、醚基或酰胺基。当r2为含有1至15个碳原子的烃链时,在一个实施例中,r2可为含有1至10个碳原子的直链或支链、饱和或不饱和烃链,而在另一实施例中,r2可为含有2至15个碳原子的烃链,其包括具有式
‑
n(r
11
)
‑
(c=o)
‑
的酰胺官能团,其中r
11
是h或含有1至4个碳原子的烃链。变量n是0到65之间的任何整数,变量m是0到35之间的任何整数,条件是m n至少为3。r3是含有2至80个碳的直链或支链、饱和或不饱和烃。变量q和t各自至少为1,而q t可以是2到150之间的任何整数。ma为数均分子量为300g/mol到20000g/mol的多胺物质。变量p或z可以各自为0,或者p z可以为0,或从1或2到200的任何整数;r4是包含1至4个碳(例如1至3个碳)的直链或支链的饱和碳链。在一个实施例中,在式i中,n是0。在另一个实施例中,在式i中,n为3至65的任何整数且m为0。在另一个实施例中,在式i中,m是0。在另一个实施例中,在式i中,m是3至35的任何整数,例如5至16,并且n是0。在另一个实施例中,在式i中,n和m都是正整数并且n m为3到65,例如5到30。
具体实施方式
[0007]
在以下的说明书和权利要求中,术语“烃基”将指一价烃基团,其可任选地包括常规或指定量的其它杂原子(如o和n),如基团中每两个或每十个碳原子包含一个氧和/或氮,但优选仅为碳和氢。当在本文中广泛使用时,术语“烃链”将指包含碳和氢的化合物,其包括为支链、直链、饱和、不饱和或环状结构的变体。烃链可以任选地包括其他原子,例如杂原子,其包括醚基形式的氧、或酰胺基形式的氮。
[0008]
本发明是针对具有以下结构的分散剂:
[0009][0010]
分散剂分子尤其可以包括聚醚种类、聚酯种类或聚醚和聚酯两者的组合。此外,分散剂分子将包含酰胺键和盐键。
[0011]
在一个实施例中,在式i中,x代表r
‑
q基团或环状胺基。当x为r
‑
q时,r表示含有1至
50个碳原子(例如1至30个碳原子)的支链或直链、饱和或不饱和烃链。在一个实施例中,r可以任选地包括卤素(如cl或f)或杂原子(如n或o),它们作为叔胺基或醚基或其混合物存在。在一些实施例中,烃链可选自烷基、芳基、芳烷基或烷芳基烃链。在一个实施例中,r是芳基,其包括萘基、苯基或联苯基。在一个实施例中,r是芳烷基,其包括2
‑
苯乙基或苄基。在一个实施例中,r可以是烷芳基,包括辛基苯基或壬基苯基。在另一个实施例中,r是环烷基,包括c3‑8‑
环烷基,例如环丙基或环己基。
[0012]
在式i中,q代表o、nr7或nh,条件是当n为0且b为0时,q只能是nh。r7可以是含有1至18个碳原子的直链或支链、饱和或不饱和烃链,其可任选地包含醚、酯或酰胺官能团,或卤化物取代基。在一些实施例中,r7还可衍生自丙烯酸酯、甲基丙烯酸酯、丙烯酰胺或甲基丙烯酰胺。
[0013]
在另一个实施例中,r
‑
q衍生自醇或胺或其混合物。有用的醇包括但不限于甲醇、乙醇、正丙醇、正丁醇、新戊醇、正己醇、正庚醇、正辛醇、正癸醇、正十二醇、正十四醇、正十六醇、油醇、正十八醇、异丙醇、异丁醇、叔丁醇、2
‑
乙基丁醇、2
‑
乙基己醇、3
‑
庚醇、3,5,5
‑
三甲基己醇、3,7
‑
二甲基辛醇、环己醇、环戊醇、环戊烷甲醇、环己基甲醇、4
‑
环己基
‑1‑
丁醇、4
‑
乙基环己醇、环庚醇、苯酚、邻甲酚、2
‑
乙基苯酚、2
‑
丙基苯酚、4
‑
乙基苯酚、辛基苯酚、壬基苯酚、十二烷基苯酚、二
‑
和三
‑
苯乙烯基苯酚、苯甲醇、2
‑
苯乙醇、1
‑
萘酚、2
‑
萘酚、2
‑
苯基苯酚、4
‑
苯基苯酚、聚异丁烯苯酚、仲苯乙醇、4
‑
乙基苯甲醇、4
‑
丁基苯甲醇、2
‑
萘甲醇、3
‑
苯基
‑1‑
丙醇、4
‑
苯基
‑1‑
丁醇、肉桂醇和4
‑
丙氧基苯酚、2
‑
二甲氨基乙醇、2
‑
二乙氨基乙醇、2
‑
二丁氨基乙醇、2
‑
丙烯
‑1‑
醇、烯丙醇、4
‑
戊烯
‑1‑
醇、2
‑
己烯
‑1‑
醇、3
‑
壬烯
‑1‑
醇、7
‑
十二烯
‑1‑
醇、2
‑
烯丙氧基乙醇、2
‑
烯丙基苯酚、2
‑
乙烯氧基乙醇、甲基丙烯酸2
‑
羟乙酯、甲基丙烯酸羟丙酯、甲基丙烯酸羟丁酯、以商品名unilin,从贝克休斯(baker hughes)商购获得的饱和直链醇和饱和支链醇,例如以商品名isofol,从沙索化学有限公司(sasol gmbh)商购获得的“格尔伯”醇,包括它们的混合物。市售格尔伯醇的具体实例是isofol 12、14t、16、18t、18e、20、24、28、32、32t和36。有用的胺包括但不限于伯胺:甲胺、乙胺、丙胺、丁胺、戊胺、己胺、庚胺、辛胺、壬胺、癸胺、十一胺、十二胺、十三胺、1
‑
十四胺、十五胺、1
‑
十六胺、十八胺、异丙胺、仲丁胺、异丁胺、叔丁胺、1
‑
甲基丁胺、1,3
‑
二甲基丁胺、3,3
‑
二甲基丁胺、2
‑
乙基己胺、3
‑
二甲基氨基丙胺、n
‑
甲基乙二胺、n,n'
‑
二甲基乙二胺、环戊胺、环己胺、环己烷甲胺、环庚胺、烯丙胺和油胺、苯胺、2
‑
乙基苯胺、4
‑
丁基苯胺、4
‑
环己基苯胺、4
‑
氨基联苯、1
‑
氨基萘、2
‑
氨基萘、苄胺、苯乙胺、3
‑
苯基
‑1‑
丙胺、3
‑‑
氨基丙基咪唑、苯基
‑4‑
丁胺、间氨基苯甲醚和对乙氧基苯胺;和仲胺:二甲胺、n
‑
乙基甲胺、二乙胺、二丙胺、二异丙胺、n
‑
甲基丁胺、n
‑
甲基
‑
叔丁胺、二丁胺、二己胺、二(2
‑
乙基己基)胺、二异丁胺、二壬胺、二戊胺,二
‑
十二胺、二辛胺、双十二胺、n
‑
甲基十八胺、n
‑
甲基环己胺、n
‑
乙基环己胺、二环己胺、双(2
‑
甲氧基乙基)胺、n
‑
甲基烯丙胺、二烯丙胺、n
‑
甲基苯胺、n
‑
乙基苯胺、n
‑
丁基苯胺、二苯胺、n
‑
乙基
‑1‑
萘胺、n
‑
苄基甲胺、二苄基胺、n
‑
乙基苄基胺和n
‑
甲基苯胺,包括它们的混合物。
[0014]
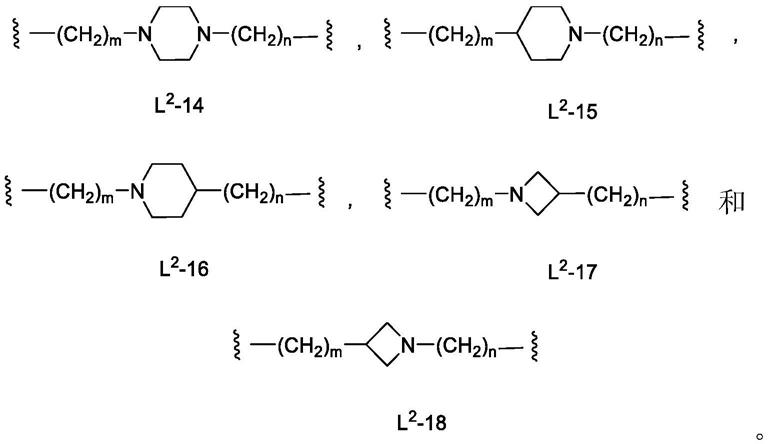
当x是环状胺时,它衍生自环状仲胺。有用的环状仲胺包括但不限于哌啶、吗啉、4
‑
甲基哌啶、4
‑
苯基哌啶、硫代吗啉、杂氮环丁烷、1
‑
甲基哌嗪、2
‑
甲基哌嗪和吡咯烷,包括它们的混合物。
[0015]
在本发明中,式i的分散剂分子可以含有聚醚链、聚酯链、聚酯酰胺链或每种链的组合,例如其聚醚
‑
共
‑
聚酯链、聚醚
‑
共
‑
聚酯酰胺链、聚醚
‑
共
‑
聚酯
‑
共
‑
聚酯酰胺链或聚
酯
‑
共
‑
聚酯酰胺链。因此,在一实施例中,本发明中的变量之和,m n至少为3。例如,m n可以是3到65,例如,5到50。在本发明的一个实施例中,n可以是从0到65的任何整数。在另一个实施例中,n是从1到65的任何整数,例如,至少2、3、4或者更多的例如,5到50。在另一个实施例中,n是0。变量m可以是0到35之间的任何整数。在一个实施例中,m可以是从1到35的任何整数,例如至少2、3、4或者更多的例如,5到16。在另一个实施例中,m是0。
[0016]
在包含聚醚链段(即其中n为1或更大)的式i的实施例中,r1可以是h、甲基或乙基。聚醚链段衍生自例如环氧乙烷、环氧丙烷、环氧丁烷或其混合物等环氧烷烃的开环反应。在本发明的一个实施例中,n可以是从0到65的任何整数。在另一个实施例中,n是从1到65的任何整数,例如至少2、3、4或者更多的例如,5到30。在另一个实施例中,n是0。聚醚链段可以通过本领域技术人员已知的任何方法合成,包括但不限于在一元醇或仲胺存在下的环氧烷烃聚合以引发聚醚链的延长。聚合可在碱催化剂(如氢氧化钾或氢氧化钠)的存在下,于50℃至150℃或70℃至140℃的温度下,优选在压力下方便地进行,以防止易挥发的环氧烷烃的损失。在一个实施例中,式ii的聚醚一元醇化合物是可商购的,其中n为3或更大,且b和m均为零。实施例包括但不限于来自默克(aldrich)或来自陶氏化学(dow)以synalox为商标名称或来自科莱恩化工(clariant)的polyglykol的各种分子量的聚(丙二醇)单丁醚、聚(乙二醇
‑
ran
‑
丙二醇)单丁基醚(poly(ethyleneglycol
‑
ran
‑
propyleneglycol)monobutyl ethers)或聚乙二醇单甲醚。synalox
tm 的具体实例是100
‑
d20、100
‑
40b、100
‑
50b、100
‑
d95和100
‑
150b。polyglykoltm的具体实例是b01/20、b01/40、b01/80、b01/120和b01/240。聚丙二醇单异十三烷基醚醚(polypropyleneglycol monoisotridecylether ether)可从科莱恩化工(clariant)以polyglykol tm为商标名称获得,具体实例为t01/35。聚环氧乙烷的其他单取代烷(烯)基醚、环烷基醚或芳基醚也可从多种来源获得,例如默克(sigma
‑
aldrich)、禾大(croda)、科莱恩化工(clariant)、巴斯夫(basf)、陶氏化学(dow)和英力士(ineos)。
[0017]
在式i的实施例中,变量b是0或1,条件是当n和m都至少为1时,b只能是1。在一个实施例中,b是1并且变量的总和,m n至少是4。r5代表含有最多3个碳原子的直链或支链烃链,r6代表氢(h),具有1至22个碳原子的烃基,其可任选地含有醚、酯、叔胺或酰胺官能团。在一个实施例中,r6可以衍生自(甲基)丙烯酸烷基酯或烷基(甲基)丙烯酰胺。在一个实施例中,r6包含(甲基)丙烯酸烷基酯的残基,或其混合物。在一个实施例中,r6是丙烯酸烷基酯,并且在另一个实施例中,r6是甲基丙烯酸烷基酯。在一个实施例中,r6是烷基丙烯酰胺,并且在另一个实施例中,r6是烷基甲基丙烯酰胺。在一个实施例中,r6是h。合适的(甲基)丙烯酸烷基酯或烷基(甲基)丙烯酰胺的实例包括那些(甲基)丙烯酸酯或烷基(甲基)丙烯酰胺化合物,其中烷基是甲基、乙基、丙基、异丙基、丁基、戊基、己基、庚基、辛基、2
‑
乙基己基、壬基、癸基、十二烷基、十四烷基、十六烷基、十八烷基、二十烷基、2
‑
二甲基氨基乙基、3
‑
二甲基氨基丙基或其混合物。如本文所用,表述(甲基)丙烯酸酯或烷基(甲基)丙烯酰胺包括丙烯酸酯或甲基丙烯酸酯或其混合物或丙烯酰胺或甲基丙烯酰胺或其混合物。
[0018]
在包含聚醚链段(即其中n为1或更大)和聚酯或聚酯酰胺链段或其混合物(即其中m为1或更大)并且b为0的式i的一些实施例中,聚醚链段可以是衍生自环氧烷烃在单醇或仲胺存在下的开环反应以引发聚醚链延长,或衍生自早先公开的市售聚醚单醇。
[0019]
在包含聚醚链段(即其中n为1或更大)和聚酯或聚酯酰胺链段或其混合物(即其中
m为1或更大)并且b为1的式i的其他实施例中,聚合物式ii的残基,即x
‑
(ch2chr1‑
o)
n
‑
[r5‑
n(r6)]
b
‑
可以包括聚醚胺,例如聚环氧烷单烷基(polyalkyleneoxide monoalkyl)或芳基醚单胺(aryl ether monoamine)。该聚醚胺可以通过本领域技术人员已知的任何方法合成,包括但不限于在一元醇引发剂的存在下环氧烷烃如环氧乙烷、环氧丙烷或环氧丁烷或其混合物的开环反应以形成醇封端的聚醚链,然后在如us 3654370、us 4618717、us4960942和us 5457147中所述的那些金属催化剂的存在下使用已知的胺化反应条件(如,氨)将醇封端的聚醚链转化为胺。在一个实施例中,聚醚胺可通过氨基醇的烷氧基化获得,如us 5879445中所述(特别是第2栏第50行至第7栏第50行中的公开内容)。在另一个实施例中,聚醚胺可通过将醇封端的聚醚链碱催化加成到丙烯腈并随后氢化得到胺封端的聚醚链来获得。聚醚胺可以商标名称jeffamine
tm m
‑
系列或surfonamine
tm b和l系列单胺从huntsman corporation商购。jeffamine
tm
胺的具体实例是m
‑
600(9,1,600)、m
‑
1000(3,19,1000)、m
‑
2005(29,6,2000)、m2095(4,41,2000)和m
‑
2070(10,31,2000)。surfonamine
tm
胺的具体实例是b
‑
60(9,1,600)、l
‑
100(3,19,1000)、b
‑
200(29,6,2000)、b100(12.5,0,1000)、l200(4,41,2000)、l207(10,31,2000)和l300(8,58,3000)。括号中的数字分别是环氧丙烷,环氧乙烷和数均分子量的近似重复单位。可通过本领域技术人员理解的方式将可商购的聚醚胺,例如本文所列的那些,并入式ii的醇封端的聚合物中。
[0020]
在含有聚酯链段(即其中m为1或更大)的式i的实施例中,r2可以是含有1至10个碳原子(例如2至7个碳原子)的支链或直链、饱和或不饱和烃链,或
‑
r8(c=o)yr9‑
,其中y为氧,且r8为含1至10个碳原子的支链或直链、饱和或不饱和烃链,且r9为含有2至10个碳原子的支链或直链、饱和或不饱和烃链,并且还可以包括杂原子,例如作为醚基存在的氧。变量m可以是0到35之间的任何整数。在一个实施例中,m可以是从1到35的任何整数,例如至少2、3、4或者更多的例如,5到16。在另一个实施例中,m是0。聚酯链段可以通过本领域技术人员已知的任何方法合成,包括但不限于(i)在一元醇或胺的存在下,内酯和/或羟基羧酸聚合以引发聚酯链的延长,或(ii)在化学计量量的一元醇或胺存在下,二醇与二元酸或其衍生物(如酰氯(acid chloride)、酸酐或二烷基酯)的聚合反应控制分子量并抑制二羧酸聚酯(dicarboxylic polyester)的形成;并且可以方便地在50℃至250℃或70℃至200℃的温度下,任选地在酯化反应催化剂的存在下和在惰性气氛中进行。惰性气氛可以由元素周期表中的任何惰性气体提供,但通常为氮气。酯化反应催化剂可以是本领域之前已知的任何酯化反应催化剂并且可以包括但不限于钛酸四烷基酯(例如钛酸四丁酯),有机酸的锌盐(例如乙酸锌),脂族醇的锆盐(例如异丙氧基锆或丁氧基锆),甲磺酸,甲苯磺酸,磷酸二苯酯,或强有机酸如三氟乙酸。
[0021]
在另一个实施例中,在不脱离本发明范围的情况下,聚酯链段的合成可以通过任何已知的或以后开发的方法来完成。例如,聚酯链段可以通过羟基羧酸和/或内酯在一元醇或胺的存在下聚合以引发聚酯链的延长来合成。所使用的原材料还可以包括那些现在已知或以后开发的原材料。合适的羟基羧酸的具体实例是乙醇酸和乳酸,包括它们的环状二聚体、乙交酯和丙交酯、6
‑
羟基己酸、5
‑
羟基戊酸、5
‑
羟基癸酸、10
‑
羟基十一烷酸和4
‑
羟基癸酸或其混合物。内酯的实例包括c1
‑
4烷基取代的ε
‑
己内酯或任选取代的c1
‑
4烷基δ
‑
戊内酯和β
‑
丙内酯或其混合物。所述ε
‑
己内酯和δ
‑
戊内酯中的烷基取代基可以是c1
‑
4烷基并且可以是直链或支链的。合适的内酯的实例是ε
‑
己内酯和7
‑
甲基
‑
、2
‑
甲基
‑
、3
‑
甲基
‑
、5
‑
甲基
‑
、
6
‑
甲基
‑
、4
‑
甲基、5
‑
叔丁基
‑
、4,4,6
‑
三甲基
‑
和4,6,6
‑
三甲基
‑
类似物和δ
‑
戊内酯及其β
‑
甲基
‑
δ
‑
戊内酯类似物。
[0022]
在另一个实施例中,聚酯链段可以通过在化学计量量的一元醇或胺的存在下,二醇与二元酸或其衍生物(例如酰氯、酸酐或二烷基酯)的聚合反应来合成,以控制分子量并抑制形成二羧酸聚酯。产生上述r9烃链的合适二醇的具体实例包括亚烷基二醇,例如乙二醇、丙二醇、新戊二醇、1,4
‑
丁二醇、1,6
‑
己二醇、顺式和反式1,2
‑
环己烷二甲醇和1,4
‑
环己烷二甲醇,具有醚键的二醇,例如二甘醇、二丙二醇、三丙二醇和三甘醇,聚亚烷基二醇,例如聚乙二醇、聚丙二醇、聚丁二醇,数均分子量(mw)小于1000的聚乙二醇和聚丙二醇的混合嵌段和无规共聚物(pluronic
tm
和反向pluronic
tm ex basf)。产生上述r8烃链的合适的二元酸、二酯和酸酐的具体实例包括马来酸酐、琥珀酸酐、戊二酸、富马酸、丙二酸、己二酸、癸二酸、邻苯二甲酸酐、庚二酸、二聚脂肪酸和其氢化版本,以及环己烷二羧酸酐。用于引发聚酯链段聚合的醇和胺的具体实例已在前面公开。
[0023]
在包含聚酯酰胺链段(即其中m为1或更大)的式i的实施例中,r2可以是包含2至15个碳原子的烃链,其包含酰胺官能团
‑
n(r
11
)
‑
(c=o)
‑
,其中r
11
为h或含有1至4个碳原子的烃链,或r2可为
‑
r8(c=o)yr9‑
,其中y为氮,且r8为含有1至10个碳原子的支链或直链、饱和或不饱和烃链,并且r9是含有2至10个碳原子的支链或直链、饱和或不饱和烃链,并且还可以包括杂原子,例如作为醚基存在的氧。变量m可以是0到35之间的任何整数。在一个实施例中,m可以是从1到35的任何整数,例如至少2、3、4或者更多的例如,5到16。在另一个实施例中,m是0。聚酯酰胺链段可以通过本领域技术人员已知的任何方法合成,包括但不限于(i)在一元醇或胺的存在下,内酯与氨基羧酸聚合以引发聚酯酰胺链的延长,或(ii)在化学计量量的一元醇或胺存在下,氨基醇与二元酸或其衍生物(如酰氯(acid chloride)、酸酐或二烷基酯)的聚合反应控制分子量并抑制二羧酸聚酯(dicarboxylic polyester)的形成。
[0024]
在另一个实施例中,在不脱离本发明范围的情况下,聚酯酰胺链段的合成可以通过任何现在已知的或以后开发的方法来完成。例如,聚酯酰胺链段可以通过内酯与氨基羧酸在单醇或胺的存在下聚合以引发聚酯酰胺链延长来合成,并且可以方便地在50℃到250℃或70℃到200℃的温度下,任选地在酯化反应催化剂存在下并在惰性气氛中进行。惰性气氛和酯化反应催化剂可以是本领域先前已知的并且包括但不限于早先公开的那些。所使用的原材料还可以包括那些现在已知或以后开发的原材料。合适的氨基羧酸(或氨基酸)的具体实例包括11
‑
氨基十一烷酸、12
‑
氨基十二烷酸、6
‑
氨基己酸、4
‑
氨基丁酸、β
‑
丙氨酸、甘氨酸和肌氨酸。可以使用氨基羧酸的混合物。合适的内酯、醇和胺的具体实例已在前面公开。
[0025]
在另一个实施例中,聚酯酰胺链段的合成可以在化学计量的一元醇或胺的存在下,通过氨基醇与二元酸或其衍生物(例如酰氯、酸酐或二烷基酯)的聚合反应来完成以控制分子量并抑制二羧酸聚酯的形成。氨基醇可以是c2
‑
10
‑
氨基醇并且还可以包括杂原子,例如作为醚基存在的氧。合适的氨基醇的具体实例包括乙醇胺、3
‑
氨基
‑1‑
丙醇、4
‑
氨基丁醇、2
‑
氨基丁醇、2
‑
氨基
‑2‑
甲基
‑1‑
丙醇、5
‑
氨基
‑1‑
戊醇、5
‑
氨基
‑2‑
戊醇、2
‑
氨基
‑3‑
甲基
‑1‑
丁醇、6
‑
氨基
‑1‑
己醇、2
‑
氨基
‑1‑
己醇、丝氨醇、4
‑
氨基环己醇、2
‑
(2
‑
氨基乙氧基)乙醇或其混合物。合适的二元酸、二酯和酸酐、醇和胺的具体实例已在前面公开。
[0026]
在式i中,r3包含含有2至80个碳原子的支链或直链、饱和或不饱和烃链。在一个实施例中,r3是包含20个碳的直链饱和碳链。在另一个实施例中,r3衍生自环状酸酐。
[0027]
在式i中,变量q和t各自至少为1,使得每个分散剂分子包含盐和酰胺键的混合物。在一个实施例中,q t是从2到200的任何整数,例如2到150,其中q大于或等于t。
[0028]
在式i中,ma代表多胺物质(multi
‑
amine species)。在一个实施例中,本发明中使用的多胺物质可能含有通过沸点升高法分析测量的数均分子量(mn),所述数均分子量可在300g/mol和20000g/mol之间,例如300g/mol到10000g/mol。在另一个实施例中,ma包括至少四种胺。在一个实施例中,ma为聚胺且选自聚乙烯亚胺、改性聚乙烯亚胺、聚烯丙基胺、改性聚烯丙基胺、聚乙烯胺、改性聚乙烯胺或其混合物。在一个实施例中,至少70重量%、80重量%、90重量%或95重量%的多胺物质为聚乙烯亚胺。
[0029]
ma可为直链或支链。直链聚乙烯亚胺可通过水解聚(n
‑
酰基)亚烷基亚胺来制备,如例如takeo saegusa等人在《大分子(macromolecules)》,1972,第5卷,第4470页中所描述。分子量不同的支链聚乙烯亚胺可从巴斯夫(basf)和日本触媒公司(nihon shokubai)商购获得。不同分子量的聚烯丙胺和聚(n
‑
烷基)烯丙胺可从日东纺织(nitto boseki)商购获得。不同分子量的聚乙烯胺可从三菱开赛公司(mitsubishi kasai)获得。聚(丙烯亚胺)树枝状大分子可从dsm精细化工公司(dsm fine chemicals)商购获得,并且聚(酰氨基胺)树枝状大分子可从奥德里奇化学(aldrich chemical)公司以“starburst”树枝状大分子获得。在一个实施例中,ma为聚(c2
‑6‑
亚烷基亚胺)和/或聚乙烯亚胺。
[0030]
在另一个实施方案中,ma可以通过使它的伯和/或仲氨基的一部分与酯(如乙酸乙酯或乙酸丁酯),异氰酸酯(如异氰酸苯酯),内酯(如ε
‑
己内酯和δ
‑
戊内酯),酸酐(如琥珀酸酐、马来酸酐、邻苯二甲酸酐、靛红酸酐、1,2
‑
萘二甲酸酐、1,8
‑
萘二甲酸酐或1,2,4
‑
苯三羧酸酐),环状碳酸酯(如碳酸亚乙酯),(甲基)丙烯酸酯(如丙烯酸乙酯或丙烯酸2
‑
羟乙酯),或环氧化物(如苯基缩水甘油醚)反应而被改性,同时确保改性多胺仍存在未改性的伯氨基和/或仲氨基,因此仍为胺形式。
[0031]
在另一个实施例中,ma可能是聚乙烯亚胺。聚乙烯亚胺可通过用c2
‑
4烷氧基单元取代nh单元的一个或多个质子来改性。聚乙烯亚胺可使用c2
‑
4环氧烷烃(如环氧乙烷、环氧丙烷、环氧丁烷或其混合物)通过烷氧基化来改性。烷氧基化聚乙烯亚胺的实例可从巴斯夫和日本触媒公司商购获得。在此实施例中,如此改性的ma将仍含有未改性且仍处于胺形式的伯和/或仲氨基,以形成本文所述的分散剂聚合物。
[0032]
ma的改性可以在本领域技术人员通常理解的反应条件下进行,无论是现在存在的还是以后开发的。应当理解,在加入链以产生分散剂之前对ma的改性可以在分散剂分子形成后可能不可行的反应条件(例如更高的温度)下进行。
[0033]
在式i中,h
表示当酸酐与多胺ma反应生成酰胺键和盐键时生成的质子物质(proton species)。h 物质连接到ma的胺基的一个氮原子上以生成铵阳离子。在一个实施例中,h
物质的数量等于q p的总和,因此,总的来说,式i的分散剂分子不带电荷。
[0034]
在公式i中,变量p和z可以是0,或1或更大。在一个实施例中,p z是从1到200的任何整数。在另一个实施例中,p z是从2到200的任何整数。
[0035]
在式i中,r4可以是包含1至4个碳原子(例如1个或2个)的直链或支链饱和碳链。在一个实施例中,r4衍生自非环状酸酐。
[0036]
本发明的分散剂(例如式i)使用包括以下步骤的新方法制备:(a)提供式x
‑
(ch2chr1‑
o)
n
‑
[r5‑
n(r6)]
b
‑
[(c=o)r2‑
o]
m
‑
h(式ii)的醇封端的聚合物,(b)使醇封端的聚合
物与环酐反应以提供酸封端的聚合物,(c)使酸封端的聚合物与非环状酸酐以提供酸酐混合物,以及(d)使酸酐混合物与多胺物质反应,其中多胺物质具有300至20000的数均分子量以形成分散剂分子,其中q和t各自至少为一,使得分散剂同时包含酰胺键和盐键。在式ii中,x代表r
‑
q或环状仲胺。当x为r
‑
q时,r为含有1至50个碳原子的支链或直链、饱和或不饱和环烃链,q为o、或nr7、或nh,条件是当n为0和b是0时,q只能是nh,并且r7是包含1至18个碳原子的直链或支链、饱和或不饱和烃链,其可任选地包含醚、酯或酰胺官能团或卤化物取代基。x也可以是衍生自一种或多种环状仲胺的环状胺结构。在式ii中,r1是h、甲基、或乙基,r5是含有最多3个碳原子的直链或支链烃链;r6为氢、含1至22个碳原子的烃基、或(甲基)丙烯酸烷基酯或烷基(甲基)丙烯酰胺的残基。变量b是0或1,条件是当n和m都至少为1时,b只能是1。r2是直链或支链、饱和或不饱和的、含1至15个碳原子的烃链或
‑
r8(c=o)yr9‑
,其中y是o或nh或nr
10
,r8是含1至10个碳原子的烃链,r9为含有1至10个碳原子的烃链,且r
10
为含有1至20个碳原子的烃链,其可包括酯基、醚基或酰胺基。当r2是含有1至15个碳原子的烃链时,在一个实施例中,r2可以是含有1至10个碳原子(例如2至7个)的、直链或支链、饱和或不饱和烃链,并且在另一个实施例中,r2可以是含有2至15个碳原子的烃链,其包括具有下式的酰胺官能团,
‑
n(r
11
)
‑
(c=o)
‑
,其中r
11
是h或含有1至4个碳原子的烃链。在式ii中,n是0到65之间的任何整数,m是0到35之间的任何整数,条件是m n至少为3。
[0037]
在一实施例中,醇封端的聚合物的数均分子量为300g/mol至5000g/mol,例如500g/mol至3000g/mol。
[0038]
在一个实施例中,醇封端的聚合物和环状酸酐以大约1︰1的摩尔比混合并在足够高的温度下反应以溶解环状酸酐。例如,在一个实施例中,大约130℃的温度可能是合适的。在一个实施例中,反应可以在2至48小时内发生并且可以方便地在50℃至150℃或70℃至140℃的温度下于惰性气氛中,任选地在催化剂(例如磷酸)的存在下进行。合适的环状酸酐的例子包括,例如,戊二酸酐、1,2
‑
环己烷二羧酸酐、高邻苯二甲酸酐(homophthalic anhydride)、琥珀酸酐、二甘醇酸酐、聚异丁烯琥珀酸酐、2
‑
苯基琥珀酸酐或烷(烯)基琥珀酸酐。
[0039]
随后的酸封端的聚合物随后与非环状酸酐反应。合适的非环状酸酐包括丁酸酐、异丁酸酐、丙酸酐和乙酸酐或其混合物。在一个实施例中,该反应提供杂酸酐产物和均酸酐产物的混合物,其中杂酸酐是一半来自聚合物而另一半来自非环酸酐的酸酐,并且其中均酸酐是两半均由聚合物或残留的非环状酸酐制成的酸酐。在一个实施例中,酸封端的聚合物和非环状酸酐以1﹕0.5和1﹕2之间的摩尔比组合。
[0040]
上述反应步骤使用允许从反应容器中除去过量酸酐和酸副产物的装置进行。在一个实施例中,该反应在高于产生的酸的沸点但低于非环状酸酐的沸点的反应温度下进行2至10个小时。例如,当使用乙酸酐时,120℃左右的温度是合适的。然后,将反应温度升高至高于非环状酸酐的沸点的温度(例如,当使用乙酸酐时为约150℃)并且反应再进行1至72个小时。这里所描述的反应可以在大气压下进行。本领域技术人员应当理解,反应可以在减压下进行,例如在真空下进行,这可以降低反应温度和反应时间。
[0041]
然后将所得酸酐混合物与本文所述的多胺物质反应。所述的酸酐混合物和多胺组分以1﹕1至25﹕1之间(例如3﹕1至18﹕1)的重量比组合。该反应在低于100℃、优选低于80℃的温度下于惰性气氛中进行1/4至6个小时。
[0042]
制备本发明分散剂的方法包括以下步骤:(a)提供式x
‑
(ch2chr1‑
o)
n
‑
[r5‑
n(r6)]
b
‑
[(c=o)r2‑
o]
m
‑
h(式ii)的醇封端的聚合物,(b)使醇封端的聚合物与环状酸酐反应以提供酸封端的聚合物,(c)使酸封端的聚合物与非环状酸酐反应提供酸酐混合物,以及(d)使酸酐混合物与多胺物质反应,其中多胺物质具有300至20.000的数均分子量以形成分散剂分子,所述分散剂分子具有式i:
[0043][0044]
该方法包括制备具有式i的分散剂,其中x是r
‑
q或环状胺,其中当x是r
‑
q时,r是支链或直链、饱和或不饱和的烷基、芳基、芳烷基或烷芳基烃链,任选地被卤素(例如cl和f)取代或被杂原子(例如作为叔胺基或醚基存在的n和o)取代,并且q是o、或nr7或nh,条件是当n是0且b是0时,q只能是nh。x可以替代地为环状仲胺,衍生自胺,例如哌啶、吗啉、4
‑
甲基哌啶、4
‑
苯基哌啶、硫代吗啉、氮杂环丁烷、1
‑
甲基哌嗪、2
‑
甲基哌嗪和吡咯烷,包括它们的混合物。r1是h、甲基或乙基。r5是含有最多3个碳原子的直链或支链烃链。r6为氢、含有1至22个碳原子的烃基,或(甲基)丙烯酸烷基酯或烷基(甲基)丙烯酰胺的残基。b是0或1,条件是当n和m都至少为1时,b只能是1。r2是含1至15个碳原子的直链或支链、饱和或不饱和烃链,或
‑
r8(c=o)yr9‑
,其中y是o或nh或nr
10
,r8是含1至10个碳原子的烃链,r9为含有1至10个碳原子的烃链,且r
10
为含有1至20个碳原子的烃链,其可包括酯基、醚基或酰胺基。当r2为含有1至15个碳原子的烃链时,在一个实施例中,r2可为含有1至10个碳原子的直链或支链、饱和或不饱和烃链,而在另一实施例中,r2可为含有2至15个碳原子的烃链,其包括具有式
‑
n(r
11
)
‑
(c=o)
‑
的酰胺官能团,其中r
11
是h或含有1至4个碳原子的烃链。变量n是0到65之间的任意整数,变量m是0到35之间的任意整数,条件是m n至少为3。r3是含有2至80个碳的直链或支链、饱和或不饱和烃。变量q和t各自至少为1,而q t可以是2到150之间的任何整数。ma是数均分子量为300g/mol至20000g/mol的多胺物质。p z可为0,或1或2至200的任何整数;r4是包含1至4个碳,优选1至3个碳的直链或支链饱和碳链。在一个实施例中,在式i中,n是0。在另一个实施例中,在式i中,n为3至65的任何整数且m为0。在另一个实施例中,在式i中,m是0。在另一个实施例中,在式i中,m是3至35的任何整数,例如5至16,并且n是0。在另一个实施例中,在式i中,n和m都是正整数并且n m为3到65,例如5到30。
[0045]
在一个实施例中,如上公开的制备分散剂的方法产生式i的分散剂,其中n为0且m为至少3。在另一个实施例中,如上公开的制备分散剂的方法产生式i的分散剂,其中m为0且n为至少3。在另一个实施例中,如上公开的制备分散剂的方法产生式i的分散剂,其中m或n为0,但m n为至少3。在另一个实施例中,如上公开的制备分散剂的方法产生式i的分散剂,其中m n是3至65的任何整数,例如5至30。
[0046]
在一个实施例中,式i的分散剂可进一步官能化以使其特性和应用性能适应特定的要求。下文描述的这些改性反应在下文列出的各种试剂和上面详述的聚醚和/或聚酯和/或聚酯酰胺基反应的聚胺物质的胺之间。任何剩余氨基的改性可以所属领域的技术人员已
知的任何方式进行。举例来说,当氨基将与掺入颜料分散体或糊剂的黏结剂(binder)体系反应并引起絮凝时,这类改性为期望的。这种修饰可以在本领域技术人员通常理解的反应传导(reaction conduction)下进行,无论是现在存在的还是以后开发的。对于在如本文所述将多胺(ma)物质并入分散剂分子后制备的胺的改性,应理解可能需要在受控温度下进行此类改性,例如100℃或降低。
[0047]
所陈述的改性是本发明的有利实施例,并且可以通过以下方式实现:
[0048]
a)使聚胺物质的一个或多个剩余的游离伯氨基和仲氨基与异氰酸酯、内酯、酸酐、环氧化物、环状碳酸酯或(甲基)丙烯酸酯反应。合适的异氰酸酯的具体实例包括异氰酸苯酯。合适的内酯的具体实例包括己内酯和戊内酯。在美国6,878,799和7,767,750中公开了聚胺物质的一个或多个剩余的游离伯氨基和仲氨基与酸酐的反应。合适的酸酐的具体实例包括马来酸酐、琥珀酸酐、邻苯二甲酸酐、四氢邻苯二甲酸酐、甲基四氢邻苯二甲酸酐、六氢邻苯二甲酸酐、甲基六氢邻苯二甲酸酐、1,8
‑
萘二甲酸酐,其任选地被硝基或卤素取代基(如cl和br)、靛红酸酐、偏苯三酸酐、c1‑
20
烯基和烷基琥珀酸酐取代。jp4031471中公开了聚胺物质的一个或多个剩余的游离伯氨基和仲氨基与环氧化物的反应。合适的环氧化物的具体实例包括氧化苯乙烯、环氧丙烷和环氧乙烷。合适的环状碳酸酯的具体实例包括碳酸亚乙酯和碳酸2,2
‑
二甲基三亚甲基酯。适合的(甲基)丙烯酸酯的具体实例包括丙烯酸乙酯和丙烯酸2
‑
羟乙酯;
[0049]
b)聚胺物质的一个或多个剩余的游离伯氨基、仲氨基或叔氨基与一元或多元羧酸、无机酸、含有磷和多金属氧酸盐的酸或强酸的成盐作用和/或反应。用于此目的的合适的试剂包括盐酸、乙酸、硫酸、烷基磺酸、烷基硫酸氢盐或芳基磺酸。jp9157374,美国2010/0017973和美国2013/0126804中公开了胺基聚胺物质的一个或多个剩余的游离氨基与一元或多元羧酸或含有磷的酸的成盐作用和/或反应。合适的一元羧酸的具体实例包括任选取代的c1
‑
50脂族一元羧酸(如乙酸、丙酸、己酸、辛酸、2
‑
乙基己酸、壬酸、癸酸、月桂酸、肉豆蔻酸、棕榈酸、油酸、亚油酸、硬脂酸、花生酸、芥酸、二十二烷酸、甲氧基乙酸)、天然来源油(如葵花籽油、菜籽油、蓖麻油和橄榄油)衍生的脂肪酸混合物、以商标isocarb
tm
(ex sasol)获得的支链烷基羧酸、unicid
tm
酸(其是从贝克休斯公司(baker hughes)商购的线性c25
‑
50合成伯酸)以及芳族羧酸(如苯甲酸、水杨酸和萘甲酸)。合适的多元羧酸的具体实例包括琥珀酸、丙二酸、己二酸、癸二酸、苹果酸、富马酸、柠檬酸和酒石酸。合适的含有磷的酸的具体实例包括磷酸和亚磷酸。合适的含有多金属氧酸盐的酸的具体实例包括磷钼酸、磷钨酸和硅钼酸;
[0050]
c)将聚胺物质的一个或多个剩余的游离伯氨基、仲氨基或叔氨基氧化为氮氧化物;
[0051]
d)将聚胺物质的一个或多个剩余的游离叔氨基季铵化。这可以使用烷基硫酸盐、烷基或芳烷基卤化物、卤代羧酸酯、草酸烷基酯或环氧化物来实现。用于此目的的合适的试剂包括硫酸二甲酯、苄基氯、甲基卤化物(如氯、溴和碘)、草酸二甲酯、环氧乙烷、环氧丙烷和在酸的存在下的氧化苯乙烯,以及丙烷(或丁烷)磺内酯;以及
[0052]
e)使聚胺物质的一个或多个剩余的游离伯氨基、仲氨基或叔氨基与一个或多个mw150至3000的单氨基反应性基团封端的聚合物反应。在美国4,224,212、4,861,380、5,700,395、5,760,257、6,197,877、8,202,935、jp4866255、jp8010601、jp9157361、wo2006/
113258和wo 2007/039605中公开了羧酸封端的聚酯、聚酯酰胺和聚酰胺聚合物的合适的实例。在jp4248207、美国7,767,750、7,671,119、7,872,070、8,076,409和8,168,713中公开了羧酸封端的聚醚聚合物的合适的实例。在美国4,861,380和6,197,877中公开了磷酸盐、硫酸盐和磺酸盐封端的聚酯聚合物的合适的实例。在ep713894、jp3488001、jp2010
‑
222522和美国8,202,935中公开了(甲基)丙烯酸酯封端的聚酯、聚酯酰胺和聚酰胺聚合物的合适的实例。在美国7,923,474和jp2010
‑
222522中公开了(甲基)丙烯酸酯封端的聚醚聚合物的合适的实例。在美国5,130,463、5,151,218、6,111,054、6,310,123、7,595,416和8,202,935中公开了磷酸盐、硫酸盐和磺酸盐封端的聚醚、聚醚/聚酯、聚醚/聚氨酯和聚醚/聚酯/聚氨酯聚合物的合适的实例。在jp4031471、jp7149855和wo 2007/039605中公开了异氰酸酯封端的聚酯和聚醚聚合物的合适的实例。在美国5,100,969中公开了环氧化物或乙酰乙酰氧基或环碳酸酯封端的聚丙烯酸酯聚合物的合适的实例。
[0053]
本发明的一个目的是提供能够改善色强度或其它着色性能、增加颗粒状固体负荷和/或形成改善的分散体,并具有改善的最终组合物亮度的化合物。在达到此目的的同时,还制备了具有降低的粘度、良好的分散稳定性、降低的粒度和降低的粒度分布、降低的雾度,改善的光泽度和增加的喷射性的组合物(特别是当组合物为黑色时)。本发明的组合物还可以在环境储存条件,和在高温储存条件下稳定并且还可以减少最终涂层的变色/泛黄。
[0054]
本文的本发明聚合物可用作各种小颗粒分散体的分散剂,例如各种极性和非极性介质中的可悬浮颜料和颗粒。各种颗粒、分散剂和连续相的组合物可用作油墨、涂层、涂料和用于对油墨、涂层和涂料着色的研磨浆。
[0055]
工业应用
[0056]
存在于组合物中的颗粒状固体可以是任何无机或有机固体材料,其在相关温度下基本上不溶于有机介质,并且期望以细碎形式稳定在其中。所述颗粒固体可以是粒状材料、纤维、薄片的形式,或者是粉末的形式,所述粉末的形式通常是吹制粉末(blown powder)。在一个实施例中,所述颗粒固体是颜料。
[0057]
通过光散射测量,颗粒固体(通常是颜料或填料)可以具有10纳米至10微米,或10纳米至1、2、3或5微米或20纳米至1、2、3或5微米的平均粒度。
[0058]
合适的固体的实例是用于溶剂型油墨的颜料;用于涂料和塑料材料的颜料、增量剂、填料、发泡剂和阻燃剂;染料,特别是分散染料;用于溶剂型染浴的光学增白剂和纺织助剂;用于油墨、墨粉和其它溶剂型应用体系的颜料;用于油基和反相乳液钻井泥浆的固体;干洗液中的灰尘和固体颗粒;金属;用于陶瓷、压电陶瓷印刷、耐火材料、研磨剂、铸造、电容器、燃料电池、铁液、导电油墨、磁记录介质,水处理和碳氢化合物土壤修复的颗粒陶瓷材料和磁性材料;有机和无机单分散固体;用于电池电极的金属、金属氧化物和碳,用于复合材料纤维(如木材、纸张、玻璃、钢、碳和硼);以及在有机介质中用作分散剂的杀生物剂、农药和药物。
[0059]
在一个实施例中,固体是来自任何公认的颜料类别的有机颜料,所述颜料类别例如在《比色指数(colour index)》(1971)的第三版中及其后续修订版和补充版中在标题为“颜料(pigments)”的一章中描述。有机颜料的实例是来自偶氮、双偶氮、三偶氮、缩合偶氮、偶氮色淀、萘酚颜料、蒽嵌蒽醌、蒽素嘧啶、蒽醌、苯并咪唑酮、咔唑、吡咯并吡咯二酮、黄烷士林、靛蓝颜料、靛蒽醌、异蒽酮紫、异茚满蒽酮、异吲哚啉酮、异吲哚啉酮、异蒽酮紫、金属
络合物颜料、嗪、二萘嵌苯、环酮、皮蒽酮染料、吡唑并喹唑酮、喹吖啶酮、喹啉黄、硫靛、三芳基碳(triarylcarbonium)颜料、三苯基二恶嗪(triphendioxazine)、氧杂蒽和酞化青染料系列,特别是铜酞菁及其核卤代衍生物,以及酸性、碱性和媒染染料色淀。尽管严格地说炭黑是无机的,但在其分散性能上却更像有机颜料。在一个实施例中,有机颜料是酞菁,特别是铜酞菁、单偶氮、双偶氮、靛蒽醌、蒽缔蒽酮、喹吖啶酮、吡咯并吡咯二酮、二萘嵌苯和炭黑。
[0060]
无机颜料的实例包括金属氧化物,如二氧化钛、金红石二氧化钛和表面涂覆的二氧化钛、不同颜色的氧化钛(如黄色和黑色)、不同颜色的氧化铁(如黄色、红色、棕色和黑色)、氧化锌、氧化锆、氧化铝、含氧金属化合物(如钒酸铋、铝酸钴、锡酸钴、锌酸钴、铬酸锌和锰、镍、钛、铬、锑、镁、镨、钴、铁或铝中两种或多种的混合金属氧化物)、普鲁士蓝、朱砂、群青、磷酸锌、硫化锌、钙和锌的钼酸盐和铬酸盐,金属效果颜料(如薄铝片、铜和铜/锌合金、如碳酸铅和氯氧化铋的珠光薄片)。
[0061]
无机固体包括增量剂和填料,如研磨和沉淀的碳酸钙、硫酸钙、氧化钙、草酸钙、磷酸钙、钙膦酸酯、硫酸钡、碳酸钡、氧化镁、氢氧化镁、天然氢氧化镁或水镁石、沉淀的氢氧化镁、碳酸镁、白云石、氢氧化铝、氢过氧化铝或勃姆石、硅酸钙和硅酸镁、铝硅酸盐,其包括纳米粘土、高岭土、蒙脱石(包括膨润土、水辉石和皂石)、球形粘土(包括天然、合成和可膨胀的云母)、滑石(包括白云母、金云母),锂云母和绿泥石、白垩、合成和沉淀二氧化硅、气相法二氧化硅、金属纤维和粉末、锌、铝、玻璃纤维、耐火纤维、炭黑(包括单壁和多壁碳纳米管)、增强和非增强炭黑、石墨、富勒烯、沥青质、石墨烯、金刚石、氧化铝、石英、珍珠岩、伟晶石、硅胶、木粉、包括软木和硬木的木薄片、锯末、粉状纸/纤维、纤维素纤维(如洋麻、麻、剑麻、亚麻、棉、棉短绒、黄麻、苎麻、稻壳或果壳、酒椰叶、伤寒芦苇、椰子纤维、椰壳纤维、油棕纤维、木棉、香蕉叶、卡罗、curaua、龙舌兰纤维叶、亚麻叶、蕉麻、蔗渣、甘蔗渣、秸秆、竹条、小麦粉、mdf等)、蛭石、沸石、水滑石、发电厂的粉煤灰、焚化的污水污泥灰、火山灰、高炉矿渣、石棉、温石棉、直闪石、青石棉、硅灰石、凹凸棒石等、颗粒陶瓷材料如氧化铝、氧化锆、二氧化钛、二氧化铈、氮化硅、氮化铝、氮化硼、碳化硅、碳化硼、硅铝氮化物和金属钛酸盐的混合物;颗粒磁性材料,如过渡金属(通常是铁和铬)的磁性氧化物,例如γ
‑
fe2o3、fe3o4和钴掺杂的氧化铁、铁氧体(例如钡铁氧体)和金属颗粒(例如金属铝、铁、镍、钴、铜、银、金、钯和铂及其合金)。
[0062]
其它可用的固体材料包括阻燃剂(诸如五溴二苯醚、八溴二苯醚、十溴二苯醚、六溴环十二烷、聚磷酸铵、三聚氰胺、氰尿酸三聚氰胺、氧化锑和硼酸盐);杀生物剂或工业微生物制剂,诸如《柯克
‑
奥斯特默化学技术百科全书(kirk
‑
othmer’s encyclopedia of chemical technology)》第13卷,1981,第3版“工业微生物制剂(industrial microbial agents)”一章中表2、3、4、5、6、7、8和9中提及的微生物制剂,以及农用化学品(诸如氟三嗪杀真菌剂(fungicides flutriafen)、多菌灵、百菌清和代森锰锌)。
[0063]
在一个实施例中,本发明的组合物中存在的有机介质是塑料材料,在另一实施例中是有机液体。有机液体可以是非极性或极性有机液体。相对于有机液体,术语“极性”是指有机液体能够形成中等至强键,如crowley等人在《涂料技术杂志(journal of paint technology)》第38卷,1966,第269页题为“三维溶解度方法(a three dimensional approach to solubility)”中所描述。如以上提及的文章中所定义,此类有机液体通常具
有5个或更多的氢键数。
[0064]
合适的极性有机液体的实例是胺、醚,特别是较低的烷基醚、有机酸、酯、酮、乙二醇、乙二醇醚、乙二醇酯、醇和酰胺。ibert mellan在题为“兼容性和溶解度(compatibility and solubility)”的书(由诺伊斯发展公司(noyes development corporation)于1968年出版)中在第39
‑
40页的表2.14中给出了这种中强氢键液体的多个具体实例,并且这些液体全都落入本文使用的术语极性有机液体的范围内。
[0065]
在一个实施例中,极性有机液体是二烷基酮、烷烃羧酸的烷基酯和链烯醇,尤其是包含最多且包括总共6个碳原子的这类液体。作为极性有机液体的实例,其包括二烷基和环烷基酮,如丙酮、甲乙酮、二乙基甲酮、二异丙基甲酮、甲基异丁基甲酮、二异丁基甲酮、甲基异戊基甲酮、甲基正戊基酮和环己酮;烷基酯,如乙酸甲酯、乙酸乙酯、乙酸异丙酯、乙酸丁酯、甲酸乙酯、丙酸甲酯、乙酸甲氧基丙酯和丁酸乙酯;乙二醇和乙二醇酯以及醚,如乙二醇、2
‑
乙氧基乙醇、3
‑
甲氧基丙基丙醇、3
‑
乙氧基丙基丙醇、2
‑
丁氧基乙酸乙酯、3
‑
甲氧基丙基乙酸酯、3
‑
乙氧基丙基乙酸酯和2
‑
乙氧基乙酸乙酯;链烯醇,如甲醇、乙醇、正丙醇、异丙醇、正丁醇和异丁醇(也称为2
‑
甲基丙醇)、松油醇和二烷基,以及环醚,如乙醚和四氢呋喃。在一个实施例中,溶剂是链烯醇、链烷羧酸和链烷羧酸的酯。在一个实施例中,本发明适用于基本上不可溶于水性介质的有机液体。此外,本领域的技术人员将认识到,只要整体有机液体基本上不溶于水性介质,则有机液体中可以存在少量的水性介质(如乙二醇、乙二醇醚、乙二醇酯和醇)。
[0066]
可用作极性有机液体的有机液体的实例是成膜树脂,如适合于制备用于各种应用的油墨、油漆和碎屑,如油漆和油墨。这种树脂的实例包含聚酰胺,如versamid
tm
和wolfamid
tm
以及纤维素醚,如乙基纤维素和乙基羟乙基纤维素、硝化纤维素和乙酸丁酸纤维素树脂,包含其混合物。涂料树脂的实例包括短油醇酸树脂/三聚氰胺
‑
甲醛树脂、聚酯树脂/三聚氰胺
‑
甲醛树脂、热固性丙烯酸树脂/三聚氰胺
‑
甲醛树脂、长油醇酸树脂、中油醇酸树脂、短油醇酸树脂、聚醚多元醇树脂和多媒体树脂(multi
‑
media resin)(如丙烯酸和脲/醛)。
[0067]
有机液体可以是多元醇,即具有两个或更多个羟基的有机液体。在一个实施例中,多元醇包括α
‑
ω二醇或α
‑
ω二醇乙氧基化物。
[0068]
在一个实施例中,非极性有机液体是含有脂族基、芳族基或其混合物的化合物。非极性有机液体包括非卤代芳族烃(例如甲苯和二甲苯)、卤代芳族烃(例如氯苯、二氯苯、氯甲苯)、非卤代脂族烃(例如含六个或更多个碳原子的完全或部分饱和的直链和支链脂族烃)、卤代脂肪烃(例如二氯甲烷、四氯化碳、氯仿、三氯乙烷)以及天然非极性有机物(例如植物油、葵花籽油、菜籽油、亚麻籽油、萜烯和甘油酯)。
[0069]
在一个实施例中,以全部有机液体计,有机液体包含至少0.1重量%或1重量%或更多的极性有机液体。在一个实施例中,有机液体不含水。
[0070]
所述塑料材料可以是热固性树脂。可用于本发明的热固性树脂包含在加热、催化或经受紫外线、激光、红外线、阳离子、电子束或微波辐射时发生化学反应并变得相对不熔的树脂。热固性树脂中的典型反应包含不饱和双键的氧化、涉及环氧树脂/胺、环氧树脂/羰基、环氧树脂/羟基的反应、环氧树脂与路易斯酸(lewis acid)或路易斯碱(lewis base)、聚异氰酸酯/羟基、氨基树脂/羟基部分的反应、自由基反应或聚丙烯酸酯、环氧树脂和乙烯
基醚的阳离子聚合以及硅烷醇的缩合。不饱和树脂的实例包含通过一种或多种二酸或酸酐与一种或多种二醇反应制得的聚酯树脂。这种树脂通常以与反应性单体(如苯乙烯或乙烯基甲苯)的混合物形式提供并且通常被称为邻苯二甲酸树脂和间苯二甲酸树脂。另外的实例包含在聚酯链中使用二环戊二烯(dcpd)作为共反应剂的树脂。另外的实例还包含双酚a二缩水甘油醚与不饱和羧酸如甲基丙烯酸的反应产物,随后以在苯乙烯中的溶液形式提供,通常称为乙烯基酯树脂。
[0071]
在一个实施例中,热固性复合材料或热固性塑料可以是聚酯、聚乙酸乙烯酯、苯乙烯中的聚酯树脂、聚苯乙烯或其混合物。
[0072]
具有羟基官能团的聚合物(通常是多元醇)广泛用于热固性体系中,以与氨基树脂或聚异氰酸酯交联。多元醇包含丙烯酸多元醇、醇酸多元醇、聚酯多元醇、聚醚多元醇和聚氨酯多元醇。典型的氨基树脂包含三聚氰胺甲醛树脂、苯代三聚氰胺甲醛树脂、脲甲醛树脂和甘脲甲醛树脂。聚异氰酸酯是具有两个或更多个异氰酸酯基的树脂,包含单体脂肪族二异氰酸酯、单体芳香族二异氰酸酯以及其聚合物。典型的脂族二异氰酸酯包括己二异氰酸酯、异佛尔酮二异氰酸酯和氢化二苯基甲烷二异氰酸酯。典型的芳族异氰酸酯包括甲苯二异氰酸酯和二苯基甲烷二异氰酸酯。
[0073]
如果需要,本发明的组合物可以包含其它成分,例如树脂(其中这些树脂尚未构成有机介质)、黏结剂、共溶剂、交联剂、流化剂、润湿剂、抗沉淀剂、增塑剂、表面活性剂、除本发明化合物以外的分散剂、保湿剂、消泡剂、抗缩孔剂、流变改性剂、热稳定剂、抗光剂、uv吸收剂、抗氧化剂、匀染剂、光泽改性剂、杀生物剂和防腐剂。
[0074]
组合物通常包含1重量%至95重量%的颗粒状固体,精确量取决于固体的性质,并且数量取决于固体的性质以及固体和极性有机液体的相对密度。举例来说,其中固体是有机材料的组合物,如有机颜料,在一个实施例中包含按重量计15%至60%的固体,而其中固体是无机材料的组合物,如无机颜料、填料或增量剂,在一个实施例中包含按组合物的总重量计40%到90%的固体。
[0075]
可以通过已知用于制备分散体的任何常规方法来制备包含有机液体的组合物。因此,固体、有机介质和分散剂可以以任何顺序混合,然后对混合物进行机械处理以将固体颗粒减小至合适的尺寸,例如通过高速混合、球磨、篮式碾磨、玻珠碾磨、砾石碾磨、砂磨、摩擦研磨、两辊或三辊碾磨、塑料碾磨直至形成分散体。可选地,可以单独或与有机介质或分散剂混合处理固体以减小其粒度,然后加入其它一种或多种成分,并搅拌混合物以提供组合物。组合物还可通过将干燥的固体与分散剂一起研磨或碾磨,然后添加液体介质或在颜料冲洗过程中将固体与分散剂在液体介质中混合来制备。
[0076]
本发明的组合物尤其适合于液体分散体。在一个实施例中,此类分散体组合物包括:
[0077]
a)0.5到80份的颗粒固体;
[0078]
b)0.1到79.6份的式i的聚合物/分散剂;和
[0079]
c)19.9到99.4份的有机液体。
[0080]
其中所有相对份数均按重量计并且量(a) (b) (c)=100。
[0081]
在一个实施例中,组分a)包括0.5至30份的颜料,并且此类分散体可用作(液体)油墨、涂料和漆浆。
[0082]
如果需要包括干燥形式的颗粒状固体和式1的分散剂的组合物,则有机液体通常是挥发性的,因此可以通过简单的分离手段(诸如蒸发)将其容易地从颗粒状固体中去除。在一个实施例中,组合物包括有机液体。
[0083]
如果干燥组合物基本上由式i的分散剂和颗粒状固体组成,则基于颗粒状固体的重量计,其通常含有至少0.2%、至少0.5%或至少1.0%的式i的分散剂。在一个实施例中,基于颗粒固体的重量计,干燥组合物包含不大于100重量%、不大于50重量%、不大于20重量%或不大于10重量%的式1的分散剂。
[0084]
如本文所公开的,本发明的组合物适合于制备漆浆,其中将颗粒状固体在式1的化合物存在下在有机液体中碾磨。
[0085]
因此,根据本发明的另一方面,提供一种漆浆,其包含颗粒状固体、有机液体和式(1)的聚合物。
[0086]
通常,按漆浆的总重量计,漆浆包含20重量%至70重量%的颗粒状固体。在一个实施例中,颗粒固体不少于研磨浆的10重量%或不少于20重量%。这类研磨浆可任选地包含在碾磨之前或碾磨之后添加的黏结剂。
[0087]
在一个实施例中,黏结剂是能够在有机液体挥发时结合组合物的聚合材料。
[0088]
黏结剂是包括天然和合成材料的聚合材料。在一个实施例中,黏结剂包括聚(甲基)丙烯酸酯、聚苯乙烯、聚酯、聚氨酯、醇酸树脂、多糖,如纤维素、硝化纤维素和天然蛋白质(如酪蛋白)。黏结剂可为硝化纤维素。在一个实施例中,以颗粒状固体的量计,黏结剂以大于100%、大于200%、大于300%或大于400%的量存在于组合物中。
[0089]
研磨浆中可选黏结剂的量可以在较宽的范围内变化,但通常不小于研磨浆连续/液相重量的10%,通常不小于20%。在一个实施例中,黏结剂的量不大于50重量%或不大于40重量%的研磨浆的连续/液相。
[0090]
在研磨浆中的分散剂的量取决于颗粒固体的量,但是通常为研磨浆重量的0.5重量%到5重量%。
[0091]
由本发明的组合物制备的分散体和研磨浆特别适合用于非水和无溶剂配制物,其中能量可固化系统(紫外线、激光、红外、阳离子、电子束、微波)与存在于配制物中的单体、低聚物等或组合物一起采用。它们尤其适用于涂料,如油漆、清漆、油墨、其它涂料材料和塑料。合适的实例包括其在低、中和高固体涂料中使用,包括烘烤的一般工业涂料,两种组分和金属涂层,如线圈和罐头涂层、粉末涂层、可紫外线固化涂层、木器清漆;油墨,如弹性印刷、凹版印刷、胶印、平版印刷、凸版印刷或浮雕、丝网印刷和用于包装印刷的印刷用油墨、非冲击油墨,如包括连续喷墨的喷墨油墨和包括热、压电和静电的按需喷墨,相变油墨和热熔蜡油墨,用于喷墨打印机的油墨和印刷清漆,如复印清漆;多元醇和增塑溶胶分散体;非水相陶瓷工艺,特别是流延法、凝胶注模、刮刀法、挤压和注塑成型工艺,进一步实例是制备用于等静压制的干陶瓷粉末;复合材料,如片状模塑料和块状模塑料、树脂传递模塑、挤压成型、手糊成型和喷涂工艺、匹配的合模模塑;建筑材料,比如铸模树脂,化妆品、个人护理,比如指甲油、防晒霜,粘结剂,调色剂,比如液体调色剂,塑料材料和电子材料,如用于包括有机发光二极管(oled)装置的显示器中的彩色滤光片体系的涂料配制物、液晶显示器和电泳显示器,玻璃涂层,其包括光纤涂层、反射涂层或抗反射涂层、导电和磁性油墨及涂层。它们可用于颜料和填料的表面改性,以改善上述应用中使用的干粉的分散性。涂料材料的另
外的实例在bodo muller,ulrich poth,lackformulierungund lackrezeptur,lehrbuch fr ausbildung und praxis,vincentz verlag,汉诺威(hanover)(2003)和p.g.garrat,strahlenhartung,vincentz verlag,汉诺威(1996)中给出。印刷油墨配制物的实例在e.w.flick《印刷油墨和叠印清漆配制物
‑
最新进展(printing ink and overprint varnish formulations
‑
recent developments)》,诺伊斯出版物,帕克里奇新泽西州,(1990)和后续版本中给出。
[0092]
在一个实施例中,本发明的组合物进一步包括一种或多种额外已知的分散剂。
[0093]
以下实施例提供了本发明的说明。这些实施例不是详尽的,并不旨在限制本发明的范围。
[0094]
使用的试剂
[0095]1‑
十二醇——来自西格玛奥德里奇公司(sigma aldrich)
[0096]
isofol
tm
‑
36——来自康德亚化学公司(condea chemie gmbh)
[0097]
ε
‑
己内酯——来自柏斯托公司(perstorp)
[0098]
磷酸二苯酯——来自西格玛奥德里奇公司(sigma aldrich)
[0099]1‑
丁醇——来自飞世尔科技(fisher scientific)
[0100]
mpeg 750
–
聚(乙二醇)甲基醚(mw 750)——来自西格玛奥德里奇公司(sigma aldrich)
[0101]
丁醇锆(iv)溶液(80重量%的1
‑
丁醇溶液)——来自西格玛奥德里奇公司(sigma aldrich)
[0102]
mpeg 500
–
聚(乙二醇)甲基醚(mw 500)——来自西格玛奥德里奇公司(sigma aldrich)
[0103]
δ
‑
戊内酯——来自巴斯夫(basf)
[0104]
buo ppg 1000
–
聚(丙二醇)丁醚(mw 1000)——来自西格玛奥德里奇公司(sigma aldrich)
[0105]
l
‑
丙交酯
–
puralact b3级——来自科碧恩公司(corbion)
[0106]
surfonamine
tm b60——来自亨斯迈公司(huntsman)
[0107]
surfonamine l100——来自亨斯迈公司(huntsman)
[0108]
琥珀酸酐——来自西格玛奥德里奇公司(sigma aldrich)
[0109]
戊二酸酐——来自梯西爱公司(tci)
[0110]
十六烯基琥珀酸酐——来自凡特鲁斯公司(vertellus)
[0111]
十八烯基琥珀酸酐——来自凡特鲁斯公司(vertellus)
[0112]
高邻苯二甲酸酐——来自acros organics公司
[0113]
甲苯——来自飞世尔科技
[0114]
mpeg 1000
–
聚(乙二醇)甲基醚(mw 1000)——来自英力士(ineos)
[0115]
mpeg 350
–
聚(乙二醇)甲基醚(mw 350)——来自西格玛奥德里奇公司
[0116]
synalox
tm 50
‑
30b
‑
聚(乙二醇
‑
ran
‑
丙二醇)单丁醚(mw 1000)——来自陶氏化学(dow),
[0117]
正磷酸溶液——来自sigma aldrich,85重量%的水溶液
[0118]
由c12
‑
c15醇引发的丙氧基化醇(propoxylated alcohol)1
–
24摩尔当量的环氧丙
烷(mw 1600)——来自路博润公司
[0119]
由c12
‑
c15醇引发的丁氧基化醇1
–
20摩尔当量的环氧丁烷(mw 1700)——来自路博润公司(lubrizol)
[0120]
乙酸酐——来自西格玛奥德里奇公司
[0121]
epomin
tm sp200聚乙烯亚胺——来自日本触媒公司,mw 10000
[0122]
epomin
tm sp018聚乙烯亚胺——来自日本触媒公司,mw 1800
[0123]
epomin
tm sp006聚乙烯亚胺——来自日本触媒公司,mw 600
[0124]
己二酸——来自西格玛奥德里奇公司
[0125]
1,4
‑
丁二醇——来自西格玛奥德里奇公司
[0126]6‑
氨基己酸——来自西格玛奥德里奇公司
[0127]
正磷酸——来自西格玛奥德里奇公司
[0128]
硫酸二甲酯——来自西格玛奥德里奇公司
[0129]
聚异丁烯基琥珀酸酐550(mw 550)
‑
来路博润公司
[0130]
步骤1
–
醇封端的聚合物的合成
[0131]
醇封端的聚合物1:将1
‑
十二醇(100.85份)和ε
‑
己内酯(802.98份)装入反应容器并在氮气下加热至70℃。在该温度下,装入磷酸二苯酯(2.71份)。在4小时之后,反应停止,得到白色蜡状固体。这是醇封端的聚合物1。
[0132]
醇封端的聚合物2:将ε
‑
己内酯(410.01份)装入反应容器并在氮气下加热至110℃。1小时后,将温度降至70℃。一旦达到温度,装入1
‑
丁醇(88.75份)和磷酸二苯酯(1.50份)。在3小时之后,反应停止,得到透明无色液体。这是醇封端的聚合物2。
[0133]
醇封端的聚合物3:将mpeg 750(111.80份)和ε
‑
己内酯(141.23份)装入反应容器并在氮气下加热至120℃。11/2小时后,装入丁醇锆溶液(0.95份),并将温度升高至180℃。在20小时之后,反应停止,得到黄色糊状物(paste)。这是醇封端的聚合物3。
[0134]
醇封端的聚合物4:将mpeg 500(60.00份)、ε
‑
己内酯(46.62份)、δ
‑
戊内酯(48.10份)和l
‑
丙交酯(51.89份)装入反应容器并在氮气下加热至120℃。11/2小时后,装入丁醇锆溶液(0.77份),并将温度升高至180℃。在19小时之后,反应停止,得到清澈的棕色液体。这是醇封端的聚合物4。
[0135]
醇封端的聚合物5:将buo ppg 1000(431.04份)和l
‑
丙交酯(310.63份)装入反应容器并在氮气下加热至120℃。11/2小时后,装入丁醇锆溶液(2.23份),并将温度升至180℃。在19小时之后,反应停止,得到棕色糊状物。这是醇封端的聚合物5。
[0136]
醇封端的聚合物6:将mpeg 500(65.02份)、ε
‑
己内酯(81.61份)和δ
‑
戊内酯(78.10份)装入反应容器并在氮气下加热至70℃。装入正磷酸溶液(0.68份)并将温度升高至120℃。在8小时之后,反应停止,得到透明无色液体。这是醇封端的聚合物6。
[0137]
醇封端的聚合物7:将1
‑
十二醇(25.41份)、ε
‑
己内酯(70.00份)、δ
‑
戊内酯(68.22份)和l
‑
丙交酯(68.75份)装入反应容器并在氮气下加热至120℃。11/2小时后,装入丁醇锆溶液(0.87份),并将温度升至180℃。在8小时之后,反应停止,得到混浊的黄色溶液。这是醇封端的聚合物7。
[0138]
醇封端的聚合物8:将isofol
tm
‑
36(70.04份)和ε
‑
己内酯(152.81份)装入反应容器并在氮气下加热至70℃。当反应温度达到70℃时装入正磷酸(0.72份)并将温度升至120℃。
8小时后,反应停止,在室温下得到灰白色固体。这是醇封端的聚合物8。
[0139]
醇封端的聚合物9:将surfonamine
tm b60(60份)、ε
‑
己内酯(99.4份)和原磷酸(0.1g)装入到反应容器中并在氮气气氛下在120℃下搅拌数小时。获得淡黄色液体(157份)。这是醇封端的聚合物9。
[0140]
醇封端的聚合物10:将surfonamine
tm l100(60份)和ε
‑
己内酯(12.8份)装入反应容器并在氮气下搅拌并加热至120℃。装入正磷酸(0.1份)并在120℃下搅拌8小时。反应停止,得到淡黄色糊状物。这是醇封端的聚合物10。
[0141]
醇封端的聚合物11:将mpeg350(100份)、ε
‑
己内酯(63.6份)、δ
‑
戊内酯(38.6份)和o
‑
磷酸(0.2份)加入反应容器中并在氮气气氛下搅拌16小时并加热至120℃。反应停止,得到无色液体。这是醇封端的聚合物11。
[0142]
醇封端的聚合物12:重复美国专利4518435中试剂j的步骤,制备聚醚加合物,该加合物通过将2
‑
二乙氨基乙醇与10摩尔环氧乙烷缩合,然后与20摩尔环氧丙烷缩合来制备。这是醇封端的聚合物12。
[0143]
醇封端的聚合物13:将己二酸(81.09份)、癸醇(12.56份)和1,4
‑
丁二醇(150.15份)装入反应容器中并在氮气下搅拌并加热至130℃。装入正磷酸(0.42份)并在130℃下搅拌49.5小时。反应停止,得到白色固体。这是醇封端的聚合物13。
[0144]
醇封端的聚合物14:将辛胺(11.32份)和ε
‑
己内酯(140份)装入反应容器中加热至90℃并在氮气下搅拌。3.5小时后,温度升至120℃,搅拌30分钟。装入丁醇锆(0.46份)并将温度升至180℃。将反应在180℃下搅拌18小时。反应停止,得到白色固体。这是醇封端的聚合物14。
[0145]
醇封端的聚合物15:将来自2
‑
萘酚的聚醚形式和10摩尔的环氧乙烷(69.42份)和ε
‑
己内酯(134.75份)装入反应容器并在氮气下搅拌并加热至70℃。装入正磷酸(0.61份),温度升至120℃。将反应在120℃搅拌18.5小时。反应停止,得到米黄色蜡状固体。这是醇封端的聚合物15。
[0146]
醇封端的聚合物16:将6
‑
氨基己酸(70.13份)和ε
‑
己内酯(127.02份)装入反应容器中加热至180℃并在氮气下搅拌1.5小时。此后,温度降低至120℃,保持0.75小时。然后加入癸醇(20.77),5分钟后加入丁醇锆(0.43份)。将温度升至180℃并在此温度下搅拌17.5小时。反应停止,得到米色固体。这是醇封端的聚合物16。
[0147]
步骤2
–
醇封端的聚合物与环状酸酐反应生成酸封端的聚合物
[0148]
酸封端的聚合物1:将醇封端的聚合物1(843.81份)装入反应容器并在氮气下加热至70℃。在该温度下,加入琥珀酸酐(50.53份),并将温度升至130℃。20小时后,反应停止,得到酸值为34mg koh/g的白色蜡状固体。这是酸封端的聚合物1。
[0149]
酸封端的聚合物2:将醇封端的聚合物2(450.00份)和甲苯(22.37份)装入配备冷凝器(condenser)的反应容器中并在氮气下加热至70℃。在该温度下,装入琥珀酸酐(108.13份),并将温度升至130℃。18小时后,反应停止并冷却至60℃。用旋转蒸发仪除去甲苯,得到酸值为116mg koh/g的微混浊的淡黄色液体。这是酸封端的聚合物2。
[0150]
酸封端的聚合物3:将醇封端的聚合物3(211.77份)装入反应容器并在氮气下加热至70℃。在该温度下,装入琥珀酸酐(12.46份),并将温度升至130℃。71/2小时后,反应停止,得到酸值为34mg koh/g的淡黄色糊状物。这是酸封端的聚合物3。
[0151]
酸封端的聚合物4:将醇封端的聚合物4(180.00份)装入反应容器并在氮气下加热至70℃。在该温度下,装入琥珀酸酐(10.44份),并将温度升至130℃。121/2小时后,反应停止,得到酸值为44mg koh/g的澄清的棕色液体。这是酸封端的聚合物4。
[0152]
酸封端的聚合物5:将醇封端的聚合物5(180.00份)装入反应容器并在氮气下加热至70℃。在该温度下,装入琥珀酸酐(10.52份),并将温度升至130℃。31小时后,反应停止,得到酸值为34mg koh/g的粘稠的琥珀色液体。这是酸封端的聚合物5。
[0153]
酸封端的聚合物6:将mpeg 1000(300.00份)装入反应容器并在氮气下加热至70℃。在该温度下,装入琥珀酸酐(30.01份),并将温度升至130℃。5小时后,反应停止,得到酸值为54mg koh/g的白色蜡状糊状物。这是酸封端的聚合物6。
[0154]
酸封端的聚合物7:将buo ppg 1000(100.00份)装入反应容器并在氮气下加热至70℃。在该温度下,装入琥珀酸酐(10.04份),并将温度升至130℃。在18小时之后,反应停止,得到酸值为45mg koh/g的黄色液体。这是酸封端的聚合物7。
[0155]
酸封端的聚合物8:将synalox
tm 30
‑
50b(245.03份)和正磷酸溶液(0.97份)装入反应容器并在氮气下加热至70℃。在该温度下,装入琥珀酸酐(24.52份),并将温度升至130℃。9小时后,反应停止,得到酸值为61mg koh/g的澄清的无色液体。这是酸封端的聚合物8。
[0156]
酸封端的聚合物9:将丙氧基化醇1(300.00份)装入反应容器并在氮气下加热至70℃。在该温度下,装入琥珀酸酐(18.76份),并将温度升至130℃。26小时后,反应停止,得到酸值为36mg koh/g的澄清的黄色液体。这是酸封端的聚合物9。
[0157]
酸封端的聚合物10:将醇封端的聚合物6(200.00份)装入反应容器并在氮气下加热至70℃。在该温度下,装入琥珀酸酐(11.57份),并将温度升至130℃。41/2小时后,反应停止,得到酸值为42mg koh/g的澄清的无色液体。这是酸封端的聚合物10。
[0158]
酸封端的聚合物11:将醇封端的聚合物7(200.00份)装入反应容器并在氮气下加热至70℃。在该温度下,装入琥珀酸酐(11.74份),并将温度升至130℃。16小时后,反应停止,得到酸值为41mg koh/g的混浊的黄色液体。这是酸封端的聚合物11。
[0159]
酸封端的聚合物12:将醇封端的聚合物8(188.10份)装入反应容器并在氮气下加热至70℃。在该温度下,装入琥珀酸酐(11.40份),并将温度升至130℃。8.5小时后,反应停止,在室温下得到酸值为40mg koh/g的灰白色固体。这是酸封端的聚合物12。
[0160]
酸封端的聚合物13:将醇封端的丙氧基化醇1(140.60份)装入反应容器并在氮气下加热至70℃。在该温度下,装入戊二酸酐(9.40份),并将温度升至130℃。18小时后,反应停止以,室温下得到酸值为36.10mg koh/g的澄清液体。这是酸封端的聚合物13。
[0161]
酸封端的聚合物14:将醇封端的丙氧基化醇1(150.08份)装入反应容器并在氮气下加热至70℃。在该温度下,装入等重量(30.54份)的十六碳烯基琥珀酸酐和十八碳烯基琥珀酸酐的混合物并将温度升高至130℃。21.5小时后,反应停止,室温下为酸值为41.09mg koh/g的淡黄色澄清液体。这是酸封端的聚合物14。
[0162]
酸封端的聚合物15:将醇封端的丙氧基化醇1(119.98份)装入反应容器并在氮气下加热至70℃。在该温度下,装入高邻苯二甲酸酐(10.79份),并将温度升至130℃。23小时后,反应停止,在室温下得到酸值为39.88mg koh/g的澄清液体。这是酸封端的聚合物15。
[0163]
酸封端的聚合物16:将醇封端9(150.06份)装入反应容器并在氮气下加热至70℃。在该温度下,装入琥珀酸酐(9.12份),并将温度升至130℃。4.5小时后,反应停止,在室温下
得到酸值为46.45mg koh/g的灰白色蜡。这是酸封端的聚合物16。
[0164]
酸封端的聚合物17:将丁氧基化醇1(283份)装入反应容器,在氮气气氛下搅拌并加热至70℃。在该温度下,装入琥珀酸酐(13.4份),并将温度升至120℃。20小时后,反应停止,得到酸值为25.3mg koh/g的无色液体。这是酸封端的聚合物17。
[0165]
酸封端的聚合物18:将醇封端的聚合物10(72.8份)装入反应容器并在氮气氛下加热至80℃。在该温度下,装入琥珀酸酐(5.6份),并将温度升至120℃。8小时后,反应停止,得到酸值为46.1mg koh/g的淡黄色蜡状固体。这是酸封端的聚合物18。
[0166]
酸封端的聚合物19:将醇封端的聚合物11(202.2份)装入反应容器并在氮气氛下加热至80℃。在该温度下,加入琥珀酸酐(28.5份)并在80℃下搅拌12小时。反应停止,得到酸值为72.3mg koh/g的淡黄色液体。这是酸封端的聚合物19。
[0167]
酸封端的聚合物20:将丙氧基化醇1(200份)装入反应容器并在氮气下加热至70℃。在该温度下,装入琥珀酸酐(11.1份),并将温度升至120℃。20小时后,反应停止,得到酸值为34mg koh/g的无色液体。这是酸封端的聚合物20。
[0168]
酸封端的聚合物21:将醇封端的聚合物12(153份)装入反应容器并在氮气下加热至70℃。在该温度下,装入琥珀酸酐(8.7份),并将温度升至120℃。在10小时之后,反应停止,得到酸值为31.9mg koh/g的淡黄色、混浊的液体。这是酸封端的聚合物21。
[0169]
酸封端的聚合物22:将丙氧基化醇1(59.5份)和聚异丁烯琥珀酸酐550(36.06份)加入反应容器并在氮气下加热至70℃。在该温度下,装入正磷酸(0.84份),并将温度升至130℃。50小时后,反应停止,在室温下得到酸值为31.25mg koh/g的澄清的黄色液体。这是酸封端的聚合物22。
[0170]
酸封端的聚合物23:将醇封端的聚合物13(55.1份)装入反应容器并在氮气下加热至70℃。在该温度下,装入琥珀酸酐(3.1份),并将温度升至130℃。4.5小时后,反应停止,在室温下得到酸值为38.38mg koh/g的白色固体。这是酸封端的聚合物23。
[0171]
酸封端的聚合物24:将醇封端的聚合物14(140.13份)装入反应容器并在氮气下加热至70℃。在该温度下,装入琥珀酸酐(8.11份),并将温度升至130℃。2.5小时后,反应停止,在室温下得到酸值为32.58mg koh/g的澄清液体。这是酸封端的聚合物24。
[0172]
酸封端的聚合物25:将醇封端的聚合物15(185.04份)装入反应容器并在氮气下加热至70℃。在该温度下,装入琥珀酸酐(10.80份),并将温度升至130℃。20小时后,反应停止,在室温下得到酸值为35.74mg koh/g的米黄色固体。这是酸封端的聚合物25。
[0173]
酸封端的聚合物26:将醇封端的聚合物16(115.26份)装入反应容器并在氮气下加热至70℃。在该温度下,装入琥珀酸酐(7.04份),并将温度升至130℃。3.75小时后,反应停止,在室温下得到酸值为35.15mg koh/g的米黄色固体。这是酸封端的聚合物26。
[0174]
步骤3
–
酸封端的聚合物与非环状酸酐反应生成聚合酸酐
[0175]
聚合酸酐1:将酸封端的聚合物1(420.00份)和乙酸酐(30.94份)装入安装有迪安
·
斯达克分水器的反应容器中,并在氮气下加热至120℃。6小时之后,将温度升高至150℃。再过4小时后,反应停止,得到白色蜡状固体。这是聚合酸酐1。
[0176]
聚合酸酐2:将酸封端的聚合物2(120.00份)和乙酸酐(30.30份)装入安装有迪安
·
斯达克分水器的反应容器中,并在氮气下加热至120℃。6小时之后,将温度升高至150℃。又过16个小时后,去除迪安
·
斯达克分水器,留下一个开口。再过1小时后,反应停止,得
到澄清的淡黄色液体。这是聚合酸酐2。
[0177]
聚合酸酐3:将酸封端的聚合物3(140.00份)和乙酸酐(9.53份)装入安装有迪安
·
斯达克分水器的反应容器中,并在氮气下加热至120℃。6小时之后,将温度升高至150℃。又过18个小时后,去除迪安
·
斯达克分水器,留下一个开口。再过1小时后,反应停止,得到浅棕色糊状物。这是聚合酸酐3。
[0178]
聚合酸酐4:将酸封端的聚合物4(99.99份)和乙酸酐(6.73份)装入装有迪安
·
斯达克分水器的反应容器中,并在氮气下加热至120℃。6小时之后,将温度升高至150℃。又过19个小时后,去除迪安
·
斯达克分水器,留下一个开口。再过1小时后,反应停止,得到澄清的深棕色液体。这是聚合酸酐4。
[0179]
聚合酸酐5:将酸封端的聚合物5(99.97份)和乙酸酐(6.73份)装入装有迪安
·
斯达克分水器的反应容器中,并在氮气下加热至120℃。6小时之后,将温度升高至150℃。再过19小时后,反应停止,得到粘稠的棕色液体。这是聚合酸酐5。
[0180]
聚合酸酐6:将酸封端的聚合物6(90.00份)和乙酸酐(10.02份)装入装有迪安
·
斯达克分水器的反应容器中,并在氮气下加热至120℃。6小时之后,将温度升高至150℃。又过171/2个小时后,去除迪安
‑
斯达克分水器,留下一个开口。再过1小时后,反应停止,得到深棕色蜡状固体。这是聚合酸酐6。
[0181]
聚合酸酐7:将酸封端的聚合物7(40.00份)和乙酸酐(3.94份)装入安装有迪安
·
斯达克分水器的反应容器中,并在氮气下加热至120℃。6小时之后,将温度升高至150℃。又过16个小时后,去除迪安
·
斯达克分水器,留下一个开口。再过1小时后,反应停止,得到澄清的淡黄色液体。这是聚合酸酐7。
[0182]
聚合酸酐8:将酸封端的聚合物8(150.00份)和乙酸酐(16.71份)装入安装有迪安
·
斯达克分水器的反应容器中,并在氮气下加热至120℃。6小时之后,将温度升高至150℃。又过16个小时后,去除迪安
·
斯达克分水器,留下一个开口。再过1小时后,反应停止,得到深棕色液体。这是聚合酸酐8。
[0183]
聚合酸酐9:将酸封端的聚合物9(90.00份)和乙酸酐(6.49份)装入安装有迪安
·
斯达克分水器的反应容器中,并在氮气下加热至120℃。6小时之后,将温度升高至150℃。又过171/2个小时后,去除迪安
‑
斯达克分水器,留下一个开口。再过1小时后,反应停止,得到澄清的棕色液体。这是聚合酸酐9。
[0184]
聚合酸酐10:将酸封端的聚合物10(120.00份)和乙酸酐(8.03份)装入安装有迪安
·
斯达克分水器的反应容器中,并在氮气下加热至120℃。6小时之后,将温度升高至150℃。再过23小时后,反应停止,得到澄清的深棕色液体。这是聚合酸酐10。
[0185]
聚合酸酐11:将酸封端的聚合物11(120.01份)和乙酸酐(8.15份)装入安装有迪安
·
斯达克分水器的反应容器中,并在氮气下加热至120℃。6小时之后,将温度升高至150℃。又过20个小时后,去除迪安
·
斯达克分水器,留下一个开口。再过1小时后,反应停止,得到澄清的橙色液体。这是聚合酸酐11。
[0186]
聚合酸酐12:将酸封端的聚合物12(100.18份)和乙酸酐(6.96份)装入安装有迪安
·
斯达克分水器的反应容器中,并在氮气下加热至120℃。6小时之后,将温度升高至150℃。又过9个小时后,去除迪安
·
斯达克分水器,留下一个开口。再过1小时后,反应停止,在室温下得到浅棕色固体。这是聚合酸酐12。
[0187]
聚合酸酐13:将酸封端的聚合物13(69.98份)和乙酸酐(4.73份)装入安装有迪安
·
斯达克分水器的反应容器中,并在氮气下加热至120℃。6小时之后,将温度升高至150℃。又过12.75个小时后,去除迪安
·
斯达克分水器,留下开口。再过1小时后,反应停止,在室温下得到澄清液体。这是聚合酸酐13。
[0188]
聚合酸酐14:将酸封端的聚合物14(86.04份)和乙酸酐(5.19份)装入安装有迪安
·
斯达克分水器的反应容器中,并在氮气下加热至120℃。6小时之后,将温度升高至150℃。又过16个小时后,去除迪安
·
斯达克分水器,留下一个开口。再过1小时后,反应停止,在室温下得到淡黄色澄清的液体。这是聚合酸酐14。
[0189]
聚合酸酐15:将酸封端的聚合物15(65.01份)和乙酸酐(4.02份)装入安装有迪安
·
斯达克分水器的反应容器中,并在氮气下加热至120℃。6小时之后,将温度升高至150℃。又过16.5个小时后,去除迪安
·
斯达克分水器,留下一个开口。再过1小时后,反应停止,在室温下得到黄色澄清的液体。这是聚合酸酐15。
[0190]
聚合酸酐16:将酸封端的聚合物16(60.00份)和乙酸酐(4.26份)装入安装有迪安斯达克分水器的反应容器中,并在氮气下加热至120℃。6小时之后,将温度升高至150℃。又过15个小时后,去除迪安
·
斯达克分水器,留下一个开口。再过1小时后,反应停止,在室温下得到金色澄清的液体。这是聚合酸酐16。
[0191]
聚合物酐17:将酸封端的聚合物17(102份)和乙酸酐(12份)装入安装有迪安
‑
斯达克分水器的反应容器中,并在氮气气氛下搅拌并加热至120℃。10小时后,将温度升至150℃。再过4小时后,反应停止,得到淡黄色液体。这是聚合酸酐17。
[0192]
聚合酸酐18:将酸封端的聚合物18(78份)和乙酸酐(10份)装入安装有迪安
·
斯达克分水器的反应容器中,并在氮气氛下加热至120℃。6小时后,将温度升至150℃以除去过量的乙酸酐和残留的乙酸。再过4小时后,反应停止,得到淡琥珀色蜡状固体。这是聚合酸酐18。
[0193]
聚合酸酐19:将酸封端的聚合物18(230份)和乙酸酐(35份)装入安装有迪安
·
斯达克分水器的反应容器中,并在氮气氛下加热至120℃。6小时后,将温度升至150℃以除去过量的乙酸酐和残留的乙酸。再过4小时后,反应停止,得到淡黄色液体。这是聚合酸酐19。
[0194]
聚合酸酐20:将酸封端的聚合物20(101份)和乙酸酐(10份)装入安装有迪安
·
斯达克分水器的反应容器中,并在氮气氛下加热至120℃。10小时后,将温度升至150℃。再过10小时后,反应停止,得到淡黄色液体。这是聚合酸酐20。
[0195]
聚合酸酐21:将酸封端的聚合物21(52份)和乙酸酐(6份)装入安装有迪安
·
斯达克分水器的反应容器中,并在氮气氛下加热至120℃。6小时后,将温度升至150℃以除去过量的乙酸酐和残留的乙酸。再过4小时后,反应停止,得到深琥珀色液体。这是聚合酸酐21。
[0196]
聚合酸酐22:将酸封端的聚合物22(85.04份)和乙酸酐(3.87份)装入安装有迪安
·
斯达克分水器的反应容器中,并在氮气氛下加热至120℃。6小时之后,将温度升高至150℃。再过7小时后,反应停止,得到棕色粘稠的液体。这是聚合酸酐22。
[0197]
聚合酸酐23:将酸封端的聚合物23(50.03份)和乙酸酐(3.2份)装入安装有迪安
·
斯达克分水器的反应容器中,并在氮气氛下加热至120℃。6小时之后,将温度升高至150℃。再过13.25小时后,反应停止,得到棕色固体。这是聚合酸酐23。
[0198]
聚合酸酐24:将酸封端的聚合物24(130.05份)和乙酸酐(8.72份)装入安装有迪
安
·
斯达克分水器的反应容器中,并在氮气氛下加热至120℃。6小时之后,将温度升高至150℃。再过12.75小时后,反应停止,得到淡米黄色固体。这是聚合酸酐24。
[0199]
聚合酸酐25:将酸封端的聚合物25(60.04份)和乙酸酐(4.04份)装入安装有迪安
·
斯达克分水器的反应容器中,并在氮气氛下加热至120℃。6小时之后,将温度升高至150℃。再过9小时后,反应停止,得到米黄色蜡状固体。这是聚合酸酐25。
[0200]
聚合酸酐26:将酸封端的聚合物26(60.08份)和乙酸酐(4.33份)装入安装有迪安
·
斯达克分水器的反应容器中,并在氮气氛下加热至120℃。6小时之后,将温度升高至150℃。再过26.5小时后,反应停止,得到棕色固体。这是聚合酸酐26。
[0201]
步骤4
–
聚合酸酐与多胺反应生成分散剂。
[0202]
分散剂1:将聚合酸酐1(50.01份)装入反应容器中,并加热至70℃,然后装入epomin
tm sp018(3.86份,已经预热至70℃)。1小时后,反应停止,得到酸值为44mg koh/g且碱当量为1060的淡黄色蜡状固体。这是分散剂1。
[0203]
分散剂2:将聚合酸酐1(45.01份)和聚合酸酐2(15.03份)装入反应容器并加热至70℃,然后装入epomin
tm sp018(4.61份,已预热至70℃)。1小时后,反应停止,得到酸值为56mg koh/g且碱当量为1221的棕黄色蜡状固体。这是分散剂2。
[0204]
分散剂3:将聚合酸酐3(129.75份)装入反应容器中并加热至70℃,然后装入epomin
tm sp018(10.00份,已预热至70℃)。1小时后,反应停止,得到酸值为16mg koh/g且碱当量为1053的棕色糊状物。这是分散剂3。
[0205]
分散剂4:将聚合酸酐4(40.02份)装入反应容器中并加热至70℃,然后装入epomin
tm sp018(3.08份,已预热至70℃)。1小时后,反应停止,得到酸值为27mg koh/g且碱当量为1246的混浊的深棕色液体。这是分散剂4。
[0206]
分散剂5:将聚合酸酐5(40.00份)装入反应容器中并加热至70℃,然后装入epomin
tm sp018(3.09份,已预热至70℃)。1小时后,反应停止,得到酸值为14mg koh/g且碱当量为1228的混浊的粘稠淡棕色液体。这是分散剂5。
[0207]
分散剂6:将聚合酸酐6(50.01份)装入反应容器中并加热至70℃,然后装入epomin
tm sp018(3.86份,已预热至70℃)。1小时后,反应停止,得到酸值为26mg koh/g且碱当量为993的深棕色蜡状固体。这是分散剂6。
[0208]
分散剂7:将聚合酸酐7(34.98份)装入反应容器中并加热至70℃,然后装入epomin
tm sp018(2.69份,已预热至70℃)。1小时后,反应停止,得到酸值为18mg koh/g且碱当量为958的澄清的淡黄色液体。这是分散剂7。
[0209]
分散剂8:将聚合酸酐8(130.01份)装入反应容器中并加热至70℃,然后装入epomin
tm sp018(10.01份,已预热至70℃)。1小时后,反应停止,得到酸值为32mg koh/g且碱当量为1008的深棕色液体。这是分散剂8。
[0210]
分散剂9:将聚合酸酐9(50.00份)装入反应容器中并加热至70℃,然后装入epomin
tm sp018(3.85份,已预热至70℃)。1小时后,反应停止,得到酸值为16mg koh/g且碱当量为1071的澄清的棕色液体。这是分散剂9。
[0211]
分散剂10:将聚合酸酐1(70.04份)装入反应容器中并加热至70℃,然后装入epomin
tm sp018(3.93份,已预热至70℃)。1小时后,反应停止,得到酸值为49mg koh/g且碱当量为1946的棕黄色蜡状固体。这是分散剂10。
[0212]
分散剂11:将聚合酸酐1(50.00份)装入反应容器中并加热至70℃,然后装入epomin
tm sp018(5.56份,已预热至70℃)。1小时后,反应停止,得到酸值为50mg koh/g和碱当量为634的淡黄色蜡状固体。这是分散剂11。
[0213]
分散剂12:将聚合酸酐1(60.00份)装入反应容器中并加热至70℃,然后装入epomin
tm sp006(4.61份,已预热至70℃)。1小时后,反应停止,得到酸值为43mg koh/g且碱当量为1145的淡黄色固体。这是分散剂12。
[0214]
分散剂13:将聚合酸酐10(60.00份)装入反应容器中并加热至70℃,然后装入epomin
tm sp018(4.62份,已预热至70℃)。1小时后,反应停止,得到酸值为28mg koh/g且碱当量为1119的澄清的深棕色粘稠液体。这是分散剂13。
[0215]
分散剂14:将聚合酸酐11(60.01份)装入反应容器中并加热至70℃,然后装入epomin
tm sp018(4.63份,已预热至70℃)。1小时后,反应停止,得到酸值为19mg koh/g且碱当量为1221的混浊的粘稠棕色液体。这是分散剂14。
[0216]
分散剂15:将聚合酸酐9(60.00份)装入反应容器中并加热至70℃,然后装入琥珀酸酐(0.94份)和epomin
tm sp018(4.62份,已预热至70℃)。1小时后,反应停止,得到酸值为24mg koh/g且碱当量为1104的混浊的棕色液体。这是分散剂15。
[0217]
分散剂16:将聚合物酸酐12(70.01份)装入反应容器中并加热至70℃,然后装入epomin
tm sp018(5.37份,已预热至70℃)。1小时后,反应停止,在室温下得到酸值为32mg koh/g且碱当量为910的深棕色固体。这是分散剂16。
[0218]
分散剂17:将聚合酸酐13(50.02份)装入反应容器中并加热至70℃,然后装入epomin
tm sp018(3.83份,已预热至70℃)。1小时后,反应停止,在室温下得到酸值为18.25mg koh/g且碱当量为1152.11的混浊的黄色液体。这是分散剂17。
[0219]
分散剂18:将聚合酸酐14(70.05份)装入反应容器中并加热至70℃,然后装入epomin
tm sp018(5.37份,已预热至70℃)。1小时后,反应停止,在室温下得到酸值为28.27mg koh/g且碱当量为1013.35的金黄色液体。这是分散剂18。
[0220]
分散剂19:将聚合酸酐15(43.98份)装入反应容器中并加热至70℃,然后装入epomin
tm sp018(3.38份,已预热至70℃)。1小时后,反应停止,在室温下得到酸值为29.89mg koh/g且碱当量为1068.52的棕色液体。这是分散剂19。
[0221]
分散剂20:将聚合酸酐16(49.99份)装入反应容器中并加热至70℃,然后装入epomin
tm sp018(3.84份,已预热至70℃)。1小时后,反应停止,在室温下得到酸值为30.64mg koh/g且碱当量为1158.4的橘黄色粘稠澄清液体。这是分散剂20。
[0222]
分散剂21:将聚合酸酐17(51份)装入反应容器中并在氮气气氛下搅拌并加热至70℃,然后装入epomin
tm sp018(3份,已预热至70℃)。1小时后,反应停止,得到酸值为12.6mg koh/g且碱当量为1516的淡黄色液体。这是分散剂21。
[0223]
分散剂22:将聚合酸酐18(75份)装入反应容器中并加热至70℃,然后装入epomin
tm sp018(6.5份,已预热至70℃)。1小时后,反应停止,得到酸值为22.7mg koh/g且碱当量为1083的浅棕色蜡状固体。这是分散剂22。
[0224]
分散剂23:将聚合酸酐19(50份)装入反应容器并加热至70℃,然后装入epomin sp200(5份,已预热至70℃)。1小时后,反应停止,得到酸值为44.5mg koh/g且碱当量为930的琥珀色液体。这是分散剂23。
[0225]
分散剂24:将聚合酸酐19(50份)装入反应容器并加热至70℃,然后装入epomin
tm sp018(5份,已预热至70℃)。1小时后,反应停止,得到酸值为43.1mg koh/g且碱当量为962的琥珀色液体。这是分散剂24。
[0226]
分散剂25:将聚合酸酐20(51份)装入反应容器并加热至70℃,然后装入epomin
tm sp200(4份,已预热至70℃)。1小时后,反应停止,得到酸值为19.2mg koh/g且碱当量为1203的淡琥珀色液体。这是分散剂25。
[0227]
分散剂26:将聚合酸酐20(45份)装入反应容器并加热至70℃,然后装入epomin
tm sp200(5份,已预热至70℃)。1小时后,反应停止,得到酸值为25mg koh/g且碱当量为753的淡琥珀色液体。这是分散剂26。
[0228]
分散剂27:将分散剂18(39.99份)加入反应容器中,并在氮气下加热至70℃,然后装入己内酯(0.81份)。一小时后,停止反应,得到酸值为27.45mg koh/g且碱当量为1257.93的粘性液体/糊状物。这是分散剂27。
[0229]
分散剂28:将分散剂16(40.17份)装入反应容器中,并在氮气下加热到70℃,然后装入正磷酸(85%w/w,0.82份)和甲苯(40.96份)。一小时后,停止反应,得到酸值为24.13mg koh/g且碱当量为1174.43的粘性液体/糊状物。这是分散剂28。
[0230]
分散剂29:将分散剂19(30.24份)装入反应容器中,并在氮气下加热至70℃,然后装入丙烯酸丁酯(0.57份)。一小时后,停止反应,得到酸值为25.79mg koh/g且碱当量为1384.03的粘性液体/糊状物。这是分散剂29。
[0231]
分散剂30:将分散剂1(35.09份)装入反应容器中,并在氮气下加热至70℃,然后装入硫酸二甲酯(0.7份)。一小时后,停止反应,得到酸值为49.56mg koh/g且碱当量为1535.18的粘性液体/糊状物。这是分散剂30。
[0232]
分散剂31:将分散剂3(50.03份)装入反应容器中,并在氮气下加热至70℃,然后装入已预热至70℃的美国6197877的实例198(1.00份)。一小时后,反应停止,得到酸值为16.13mg koh/g且碱当量为1240.25的粘稠的液体/糊状物。这是分散剂31。
[0233]
分散剂32:将聚合酸酐21(52份)装入反应容器中并加热至70℃,然后装入epomin
tm sp018(3.8份,已预热至70℃)。1小时后,反应停止,得到酸值为15.9mg koh/g且碱当量为679的深琥珀色液体。这是分散剂32。
[0234]
分散剂33:将聚合酸酐22(70.02份)装入反应容器中并加热至70℃,然后装入epomin
tm sp018(5.42份,已预热至70℃)。1小时后,反应停止,在室温下得到酸值为25.23mg koh/g且碱当量为1025.32的棕色粘稠液体。这是分散剂33。
[0235]
分散剂34:将聚合酸酐23(40.03份)装入反应容器并加热至70℃,然后装入epomin
tm sp018(3.08份,已预热至70℃)。1小时后,反应停止,在室温下得到酸值为24.95mg koh/g且碱当量为990.76的棕色固体。这是分散剂34。
[0236]
分散剂35:将聚合酸酐24(100.14份)装入反应容器并加热至70℃,然后装入epomin
tm sp018(7.66份,已预热至70℃)。1小时后,反应停止,得在室温下到酸值为18.85mg koh/g且碱当量为1184.82的米黄色固体。这是分散剂35。
[0237]
分散剂36:将聚合酸酐25(50.03份)装入反应容器并加热至70℃,然后装入epomin
tm sp018(3.87份,已预热至70℃)。1小时后,反应停止,在室温下得到酸值为22.75mg koh/g且碱当量为1123.03的米色固体。这是分散剂36。
[0238]
分散剂37:将聚合酸酐26(40.01份)装入反应容器并加热至70℃,然后装入epomin sp018(3.11份,已预热至70℃)。1小时后,反应停止,在室温下得到酸值为22.58mg koh/g且碱当量为899.5的棕色固体。这是分散剂37。
[0239]
分散剂38:将聚合酸酐9(47.09份)和聚合酸酐1(47份)装入反应容器并加热至70℃,然后装入epomin
tm sp018(7.27份,已预热至70℃)。1小时后,反应停止,在室温下得到酸值为46.21mg koh/g且碱当量为1064.50的棕色液体。这是分散剂38。
[0240]
比较实例
[0241]
以下实例基于文献中的教导,即酸封端的聚合物可以很容易地与多官能聚胺(尤其是pei)反应,因此在每个比较实例中,我们都采用了相同的酸封端的聚合物作为中间体,在每种情况下创建最接近的可能的比较实例。
[0242]
所用的反应条件是将酸封端的聚合物与多官能团聚胺(尤其是pei)在120℃下搅拌6小时,其为制备基于聚酯的pei分散剂的us 6,197,877分散剂1至29(实例30至59)中使用的反应条件。与制备基于聚醚的pei分散剂的us 7,767,750(wo2005/010109a2)分散剂1至28中使用的反应条件相同。
[0243]
比较实例1:将酸封端的聚合物1(30.05份)装入反应容器中并加热至70℃,然后装入epomin
tm sp018(2.31份,已预热至70℃),并将温度升至120℃。6小时后,反应停止,得到酸值为26mg koh/g且碱当量为1392的棕橙色蜡状固体。这是比较实例1。
[0244]
比较实例2:将酸封端的聚合物3(60.01份)装入反应容器中并加热至70℃,然后装入epomin
tm sp018(4.62份,已预热至70℃),并将温度升至120℃。6小时后,反应停止,得到酸值为19mg koh/g且碱当量为1505的棕色糊状物。这是比较实例2。
[0245]
比较实例3:将酸封端的聚合物4(60.02份)装入反应容器中并加热至70℃,然后装入epomin
tm sp018(4.62份,已预热至70℃),并将温度升至120℃。6小时后,反应停止,得到酸值为31mg koh/g且碱当量为1882的混浊的深棕色液体。这是比较实例3。
[0246]
比较实例4:将酸封端的聚合物5(60.01份)装入反应容器中并加热至70℃,然后装入epomin
tm sp018(4.64份,已预热至70℃),并将温度升至120℃。6小时后,反应停止,得到酸值为30mg koh/g且碱当量为1791的混浊的粘稠浅棕色液体。这是比较实例4。
[0247]
比较实例5:将酸封端的聚合物6(50.00份)装入反应容器中并加热至70℃,然后装入epomin
tm sp018(3.87份,已预热至70℃),并将温度升至120℃。6小时后,反应停止,得到酸值为20mg koh/g且碱当量为1745的固体和混浊液体的非均相混合物。这是比较实例5。
[0248]
比较实例6:将酸封端的聚合物7(50.02份)装入反应容器中并加热至70℃,然后装入epomin
tm sp018(3.85份,已预热至70℃),并将温度升至120℃。6小时后,反应停止,得到酸值为26mg koh/g且碱当量为1369的浑浊的棕色液体。这是比较实例6。
[0249]
比较实例7:将酸封端的聚合物8(80.00份)装入反应容器中并加热至70℃,然后装入epomin
tm sp018(6.15份,已预热至70℃),并将温度升至120℃。6小时后,反应停止,得到酸值为35mg koh/g且碱当量为1502的乳黄色液体。这是比较实例7。
[0250]
比较实例8:将酸封端的聚合物9(50.01份)装入反应容器中并加热至70℃,然后装入epomin
tm sp018(3.85份,已预热至70℃),并将温度升至120℃。6小时后,反应停止,得到酸值为15mg koh/g且碱当量为1452的澄清的橙色液体。这是比较实例8。
[0251]
比较实例9:将酸封端的聚合物10(60.01份)装入反应容器中并加热至70℃,然后
装入epomin
tm sp018(4.62份,已预热至70℃),并将温度升至120℃。6小时后,反应停止,得到酸值为25mg koh/g且碱当量为1558的澄清的橘黄色液体。这是比较实例9。
[0252]
比较实例10:将酸封端的聚合物11(60.00份)装入反应容器中并加热至70℃,然后装入epomin
tm sp018(4.64份,已预热至70℃),并将温度升至120℃。6小时后,反应停止,得到酸值为30mg koh/g且碱当量为1900的粘稠的棕色液体。这是比较实例10。
[0253]
比较实例11:将酸封端的聚合物12(50.00份)装入反应容器中并加热至70℃,然后装入epomin
tm sp018(3.87份,已预热至70℃),并将温度升至120℃。6小时后,反应停止,在室温下得到酸值为24mg koh/g且碱当量为1409的黄色固体。这是比较实例11。
[0254]
比较实例12:将酸封端的聚合物13(50.51份)装入反应容器中并加热至70℃,然后装入epomin
tm sp018(3.98份,已预热至70℃),并将温度升至120℃。6小时后,反应停止,在室温下得到酸值为27.01mg koh/g且碱当量为1298.10的混浊的橘黄色粘稠液体。这是比较实例12。
[0255]
比较实例13:将酸封端的聚合物14(65.98份)装入反应容器中并加热至70℃,然后装入epomin
tm sp018(5.06份,已预热至70℃),并将温度升至120℃。6小时后,反应停止,在室温下得到酸值为20.89mg koh/g且碱当量为1131.20的澄澈的棕色液体。这是比较实例13。
[0256]
比较实例14:将酸封端的聚合物15(45.13份)装入反应容器中并加热至70℃,然后装入epomin
tm sp018(3.59份,已预热至70℃),并将温度升至120℃。6小时后,反应停止,在室温下得到酸值为18.71mg koh/g且碱当量为2690.50的不透明的浅棕色液体。这是比较实例14。
[0257]
比较例15:将酸封端的聚合物17(51份)装入反应容器中并在氮气氛下搅拌加热至70℃,然后装入epomin
tm sp018(3份,已预热至70℃)。加热至120℃并在氮气氛下在搅拌。10小时后,反应停止,得到酸值为9.2mg koh/g且碱当量为1998的浅黄色混浊液体。这是比较实例15。
[0258]
比较例16:将酸封端的聚合物20(39份)装入反应容器中并在氮气气氛下搅拌加热至70℃,然后装入epomin
tm sp200(3份,已预热至70℃)。加热至120℃并在氮气氛下在搅拌。6小时后,反应停止,得到酸值为9.8mg koh/g且碱当量为1586的深琥珀色液体。这是比较实例16。
[0259]
比较例17:将酸封端的聚合物21(52份)装入反应容器中并在氮气气氛下搅拌加热至70℃,然后装入epomin
tm sp018(4份,已预热至70℃)。加热至120℃并在氮气氛下在搅拌。6小时后,反应停止,得到酸值为12.3mg koh/g且碱当量为789的黄色液体。这是比较实例17。
[0260]
应用测试
[0261]
应用测试试剂
[0262]
dowanol mpa
–
来自西格玛奥德里奇
[0263]
甲苯——来自飞世尔科技
[0264]
甲苯——来自飞世尔科技
[0265]
乙酸乙酯——来自飞世尔科技
[0266]
exxol d140——来自埃克森美孚(exxonmobil)
[0267]
酞菁蓝l7101f颜料(heliogen blue l7101f)——来自巴斯夫
[0268]
宝石红d4240颜料(irgalite rubine d4240)——来自巴斯夫
[0269]
symular carmine 6b400s——太阳化学(sun chemicals)有限公司
[0270]
拜耳乐130m(bayferrox 130m)——来自朗盛
[0271]
3毫米玻璃珠——来自犀利玻璃珠(sigmund lindner)制造公司
[0272]
应用结果
[0273]
将下表2
‑
5中所示的每种分散剂(0.25份)加入到8德拉姆小瓶中,并加入溶剂(8.25份)。然后根据需要通过振荡和加热使分散剂溶解。一旦溶解,添加3mm玻璃珠(17份),随后添加酞菁蓝l7101f颜料(1.50份)。然后将小瓶密封并在水平振荡器上振荡16小时。然后使用a到e(流动的到粘稠的)的视觉表征等级(visual characterization scale)评估所得分散体的流动性:
[0274]
a
–
玻璃珠自由运动(流动的)
[0275]
b
–
晃动后运动1分钟
[0276]
c
–
晃动后运动10秒
[0277]
d
–
晃动时运动
[0278]
e
–
无运动(胶凝的)
[0279]
表1.颜料分散结果。溶剂:dowanol mpa
[0280]
分散剂流动性等级分散剂流动性等级比较实例6d分散剂7b比较实例7d分散剂8c/b
[0281]
表2.颜料分散结果。溶剂:甲苯
[0282][0283]
表3.颜料分散结果。溶剂:1﹕1乙醇/乙酸乙酯
[0284]
分散剂流动性等级分散剂流动性等级比较实例5d分散剂6a比较实例8d分散剂9a
[0285]
表4.颜料分散结果。溶剂:4﹕1乙醇/乙酸乙酯
[0286]
分散剂流动性等级分散剂流动性等级比较实例5d分散剂6a比较实例8d分散剂9a
[0287]
将下表6
‑
9中所示的每种分散剂(0.40份)加入到8德拉姆小瓶中,并加入溶剂(7.60份)。然后根据需要通过振荡和加热使分散剂溶解。溶解后,加入3mm玻璃珠(17份),然后加入宝石红d4240颜料(2.00份)。然后将小瓶密封并在水平振荡器上振荡16小时。然后使用a到e(流动的到粘稠的)的视觉表征等级(visual characterization scale)评估所得分散体的流动性:
[0288]
a
–
玻璃珠自由运动(流动的)
[0289]
b
–
晃动后运动1分钟
[0290]
c
–
晃动后运动10秒
[0291]
d
–
晃动时运动
[0292]
e
–
无运动(胶凝的)
[0293]
表5.颜料分散结果。溶剂:乙醇
[0294][0295]
表6.颜料分散结果。溶剂:甲苯
[0296]
分散剂流动性等级分散剂流动性等级比较实例3c分散剂4b/a比较实例8d分散剂9b/a比较实例9c分散剂13a
[0297]
表7.颜料分散结果。溶剂:exxol d140
[0298][0299]
表8.颜料分散结果。溶剂:2.5﹕1二甲苯/丁醇
[0300]
分散剂流动性等级分散剂流动性等级比较实例1d/e分散剂34a比较实例11d分散剂35a
[0301]
将下表10中所示的每种分散剂(0.40份)加入到8德拉姆小瓶中,并加入溶剂(7.60份)。然后根据需要通过振荡和加热使分散剂溶解。溶解后,加入3mm玻璃珠(17份),然后加入symuler carmine 6b400s(2.00份)。然后将小瓶密封并在水平振荡器上振荡16小时。然后使用a到e(流动的到粘稠的)的视觉表征等级(visual characterization scale)评估所得分散体的流动性:
[0302]
a
–
玻璃珠自由运动(流动的)
[0303]
b
–
晃动后运动1分钟
[0304]
c
–
晃动后运动10秒
[0305]
d
–
晃动时运动
[0306]
e
–
无运动(胶凝的)
[0307]
表9.颜料分散结果。溶剂:4﹕1乙醇/乙酸乙酯
[0308][0309]
将下表11中所示的每种分散剂(0.40份)加入到8德拉姆小瓶中,并加入溶剂(7.60份)。然后根据需要通过振荡和加热使分散剂溶解。溶解后,加入3mm玻璃珠(17份),然后加入宝石红颜料(2.00份)。然后将小瓶密封并在水平振荡器上振荡16小时。然后使用a至e(流动的到粘稠的)的视觉表征等级评估所得分散体的流动性。
[0310]
a
–
玻璃珠自由运动(流动的)
[0311]
b
–
晃动后运动1分钟
[0312]
c
–
晃动后运动10秒
[0313]
d
–
晃动时运动
[0314]
e
–
无运动(胶凝的)
[0315]
表10:颜料分散体结果。溶剂:1﹕1乙醇/乙酸乙酯
[0316]
分散剂流动性等级分散剂流动性等级比较实例12c分散剂17a
[0317]
将下表12中所示的每种分散剂(0.10份)加入到8德拉姆小瓶中,并加入溶剂(4.90份)。然后根据需要通过振荡和加热使分散剂溶解。溶解后,加入3mm玻璃珠(17份),然后加入拜耳乐130m(5.00份)。然后将小瓶密封并在水平振荡器上振荡16小时。然后使用a到e(流动的到粘稠的)的视觉表征等级(visual characterization scale)评估所得分散体的流动性:
[0318]
a
–
玻璃珠自由运动(流动的)
[0319]
b
–
晃动后运动1分钟
[0320]
c
–
晃动后运动10秒
[0321]
d
–
晃动时运动
[0322]
e
–
无运动(胶凝的)
[0323]
表11.颜料分散结果。溶剂:甲苯
[0324][0325]
通过将各分散剂实例21和实例25以及比较实例16和17(0.4份)分别溶解在4﹕1乙醇﹕乙酸乙酯(v﹕v)(7.6份)中来制备分散体。然后将3mm玻璃珠(17份)和宝石红d4240颜料
(2.0份,颜料红57.1exbasf)添加到每个溶液中,并将内容物在水平振荡器上研磨16个小时。通过确定玻璃珠在整个研磨基料中移动的自由度来评估粘度。在所有情况下,除非不存在任何试剂,否则颜料会变湿并形成均匀的分散体。所得分散体的粘度使用从a到e(好到差)的视觉表征等级评估。下面给出的结果清楚地说明本发明的分散剂产生更优异的流体分散体。每种分散体的粒度通过取研磨分散体样品(0.04份)并在4﹕1乙醇﹕乙酸乙酯(v﹕v)(8份)中稀释,并在nanotrac dls粒度分析仪上测量粒度来获得。得到的结果为:
[0326]
表12.宝石红颜料的分散结果
[0327]
实例粘度等级粒度nm d
50
/d
90
对照(无分散剂)e胶凝的比较实例15d497/1351分散剂实施例21b308/419比较实例16d329/451分散剂实例25b213/345比较实例17d330/582分散剂实施例32a163/289
[0328]
粒度分析:从上表2
‑
12中选择的分散体在适当的溶剂中稀释(按体积计约1:50)。对下表9
‑
10中所示的每种分散体进行粒度分析。d50和d90值从基于强度的分布获得。
[0329]
表13.粒度分析结果。颜料:酞菁蓝l7101f颜料。溶剂:甲苯
[0330][0331]
表14.粒度分析结果。颜料:宝石红d4240。溶剂:甲苯
[0332][0333]
表15.粒度分析结果。颜料:宝石红d4240。溶剂:乙醇
[0334]
分散剂d50/nmd90/nm分散剂d50/nmd90/nm比较实例13479706分散剂18304498
[0335]
表16.粒度分析结果。颜料:宝石红d4240。溶剂:exxol d140
[0336][0337]
表17.粒度分析结果。颜料:宝石红d4240。溶剂:1﹕1乙醇﹕乙酸乙酯
[0338]
分散剂d50/nmd90/nm分散剂d50/nmd90/nm比较实例12331557分散剂17242327
[0339]
表18粒度分析结果。颜料:宝石红d4240。溶剂:2.5﹕1二甲苯/丁醇
[0340][0341]
粘度测量:使用流变仪测量上表2
‑
12中选定的分散体的粘度。选择了两种剪切速率(shear rate)进行数据比较——40s
‑1和100s
‑1。
[0342]
表19.粘度数据。颜料:酞菁蓝l7101f颜料。溶剂:甲苯
[0343][0344]
表20.粘度数据。颜料:宝石红d4240。溶剂:甲苯
[0345][0346]
如本文所使用的,与“包括(including)”、“含有(containing)”或“特征在于(characterized by)”同义的过渡术语“包含(comprising)”是包括性的或开放式的,并且不排除另外的、未叙述的要素或方法步骤。然而,在本文中对“包括”的每一次叙述中,所述术语也旨在作为替代实施例包括短语“基本上由
……
组成”和“由
……
组成”,其中“由
……
组成”排除了未指定的任何要素或步骤,而“基本上由
……
组成”允许包括不实质性影响所考虑的组合物或方法的基本和新颖特征的其它未叙述的要素或步骤。
[0347]
尽管已经针对本发明的优选实施例对本发明进行了说明,但是应当理解,对本领域技术人员而言,在阅读说明书后,其各种修改将变得显而易见。因此,应当理解,本文公开的发明旨在覆盖落入所附权利要求的范围内的这种修改。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。