一种检测新型冠状病毒alpha和delta突变体试剂盒及应用
技术领域
1.本发明涉及病毒检测试剂盒技术领域,具体涉及一种检测新型冠状病毒 alpha和delta突变体试剂盒及应用。
背景技术:
2.目前,新型冠状病毒sars
‑
cov
‑
2的突变体在pango系统中分别属于b.1.1.7 (英国株,alpha)和b.1.617.2(印度株,delta)谱系,在世卫组织命名系统中 称为alpha突变体和delta突变体。据报道,alpha突变体传播力最强,delta突 变体致死率更高,传播力仅次于的alpha突变体。下一代高通量测序技术(ngs), 由于其具有获取新冠病毒全长基因组的能力在此次大流行的病毒突变体基因组 检测中体现了其强大性能。但是ngs测序需要一定成本的试剂、耗材,需要接 受培训的操作人员及熟练的生物信息学分析能力。这使得ngs测序在此次大流 行病诊断中仍然具有短板。
3.因为目前alpha突变体和delta突变体在都在全球引起了严重广泛传播,如 何在sars
‑
cov
‑
2阳性样本中快速、低成本地区分是否是这两种突变体是及时 调整卫生防疫非常迫切的需求。
4.本发明不仅关注sars
‑
cov
‑
2在临床样本中的阴阳性检出情况,还关注 sars
‑
cov
‑
2阳性的样本中是否含有这两种突变体。由于ngs测序技术成本高, 无法实时检测变异,且对于核酸含量低的样本得到的序列的覆盖度较低,难以 准确分析出其突变株类型。
技术实现要素:
5.本发明旨在提供一种灵敏、快速、低成本的新型冠状病毒alpha和delta突 变体筛查试剂盒,结合生物信息学分析挖掘出alpha和delta突变体的保守特征 突变,从而针对性地设计了能同时检测sars
‑
cov
‑
2阴阳性和是否存在以上两 种突变体的荧光定量pcr的引物探针及试剂盒。该试剂盒共包含4对引物探针, 分别在两个反应中进行检测。为筛查这两种高传播力的突变体提供技术支持。
6.突变体特异性引物设计要点,通过生物信息学算法挖掘设计突变体保守特 征引物。该引物只能特异性有效地扩增含有突变体携带的特征突变所在核酸。 特异性靶向突变体的特征突变引物需要保证该引物只与对应突变体的保守特征 突变匹配。由于碱基序列组成及空间位置差异和非特异性扩增,并不能随机选 择一个特征突变位点作为检测靶标。需要对生物信息学分析的两个突变体的全 部保守特征突变位点进行引物设计,选择效果最好的位点作为区分对应突变体 的靶标。经过优化以确定最佳的突变体检测引物和探针。
7.具体地,本发明的方案如下:
8.一种检测新型冠状病毒alpha和delta突变体试剂盒,包括特异性引物组和 荧光探针,特异性引物组包括第一引物对、第二引物对、宿主内参引物对以及 病毒内参引物对,荧光探针包括第一探针、第二探针、宿主内参探针以及病毒 内参探针;所述第一引物对的碱基序列如seq id no:1
‑
2所示;所述第二引物 对的碱基序列如seq id no.4
‑
5所示;第一
探针的碱基序列如seq id no:3 所示,第二探针的碱基序列如seq id no:6所示。
9.根据本发明的实施例,所述宿主内参引物对的碱基序列如seq id no:7
‑
8 所示,所述病毒内参引物对的碱基序列如seq id no:10
‑
11所示;所述病毒内 参探针的的碱基序列如seq id no:9所示,所述病毒内参探针的碱基序列如 seq id no:12所示。
10.根据本发明的实施例,所述试剂盒荧光探针的荧光报告基团为fam/hex 或hex/rox。
11.根据本发明的实施例,还包括rt
‑
pcr缓冲液、dna聚合酶、逆转录酶和 rna酶抑制剂。
12.根据本发明的实施例,所述特异性引物组在反应体系中的终浓度为10pm, 荧光探针在反应体系中的终浓度为5pm。
13.根据本发明的实施例,还包含阳性对照,所述阳性对照由检测基因的重组 质粒制备获得。
14.本发明还提供以上所述试剂盒在制备sars
‑
cov
‑
2检测产品中的应用,所 述检测产品可检测sars
‑
cov
‑
2并同时鉴定alpha和delta突变体。
15.相比现有技术,本发明的有益效果为:
16.1.本发明提供的检测试剂盒可实现灵敏、快速地筛查新型冠状病毒alpha 和delta突变体,两管内两重rt
‑
qpcr实现诊断新冠感染已经鉴别感染毒株 alpha和delta突变体,可以达到1copy/l的灵敏度。
17.2.本发明提供的试剂盒选取其中alpha突变株b.1.1.7的a570d的特征突变 位点,以及delta突变株b.1.617.2的特征突变位点t19r为对象设计引物探针。 这两者能检出相应突变株的比例分别为99.83%和99.90%。
附图说明
18.为了更清楚地说明本发明实施例的技术方案,下面将对实施例中所需要使 用的附图作简单地介绍,应当理解,以下附图仅示出了本发明的某些实施例, 因此不应被看作是对范围的限定,对于本领域普通技术人员来讲,在不付出创 造性劳动的前提下,还可以根据这些附图获得其他相关的附图。
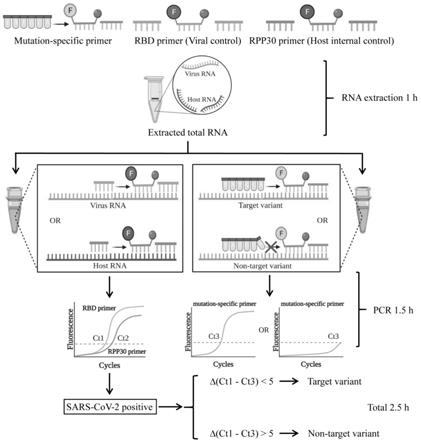
19.图1是本发明所述试剂盒检测原理示意图。
20.图2是本发明sars
‑
cov
‑
2的alpha突变株b.1.1.7和delta突变株b.1.617.2 在基因组水平上的常见突变情况示意图。
具体实施方式
21.以下实例用于说明本发明,但不限制本发明的范围。在不背离本发明精神 和实质的前提下,对本发明的方法、步骤或条件所作的修改或替换,均属于本 发明的范围。
22.因此本发明创新地利用生物信息学方法分析数百万公共数据库 sars
‑
cov
‑
2基因组,挖掘了alpha和delta突变体的特征突变信息,并根据这 些特征突变信息设计了sars
‑
cov
‑
2阴阳性检测和突变株检测的荧光定量pcr 引物探针,开发了检测这两种目前较关注的突变体的试剂盒。
23.现有sars
‑
cov
‑
2的检测试剂盒都是针对每个突变株的多个突变位点,而 这些突
变检测的试剂盒检测灵敏度和特异性都不太好,并且多个位点检测费用 也高。我们通过分析比对发现了sars
‑
cov
‑
2的alpha和delta突变株的特征突 变,各利用一个位点的突变就能检测相应的突变株。
24.一个实施方式的sars
‑
cov
‑
2突变株的基因组分析比对包括:
25.首先从gisaid数据库下载sars
‑
cov
‑
2全部基因组。使用自编的软件将下 载的全部基因组进行质量控制,过滤掉基因组中含有超过5%简并碱基的基因组 (简并碱基含量多意味着这些基因组测序深度低,覆盖度可能低,不属于高质 量基因组)。保留剩余基因组,视为高质量基因组。将sars
‑
cov
‑
2wiv04 (genome accession:nc_045512.2)作为参考基因组。分别以下载的高质量基因组 和参考基因组进行两两全局比对。通过自主编写的变异信息提取程序提取目标 序列相对于参考基因组的突变,包括点突变(point mutation),插入(insertion), 缺失(deletion)。同时以参考基因组的基因信息注释文件(文件格式gff)为辅 助信息,根据全基因组的点突变结果和基因注释信息计算对应的氨基酸突变。 同时在公共数据库pango系统中下载sars
‑
cov
‑
2每个序列对应的谱系信息。结 合每个序列的突变信息与谱系信息,计算出每个谱系的突变信息。然后,为了 计算每个谱系的常见突变,每个包含100个以上毒株的谱系的每个突变被计算 谱系内突变频率。该突变频率的计算方式为:某个谱系的某个突变在该谱系中 的频率=某谱系的此突变一共出现的毒株基因组数/某谱系的全部毒株基因组数。 选择突变频率大于50%的突变作为此谱系的常见突变。获得每个谱系的常见突 变信息后,利用数学中图论的模型,将谱系与常见突变分别进行连线。如果某 个常见突变只与一个谱系存在连线,那么这个常见突变则被视为该谱系的特征 突变。如果两个以上的突变都有同一个常见突变,那么这个常见突变则与这两 个谱系分别有连线。利用发明人编写的程序对谱系与常见突变的关系进行分析。 分析结果使用cytoscape软件进行可视化。根据可视化结果直接筛选出分别属于 alpha突变体和delta突变体的特征突变。如图2所示,显示了sars
‑
cov
‑
2的 alpha突变株b.1.1.7和delta突变株b.1.617.2在基因组水平上的常见突变。进 一步将sars
‑
cov
‑
2的alpha突变株b.1.1.7和delta突变株b.1.617.2的特征突 变进行归纳整理,得到如表1所示的两种突变株的各三种突变,选取其中alpha 突变株b.1.1.7的a570d的特征突变位点,以及delta突变株b.1.617.2的特征突 变位点t19r为对象设计引物探针。这两者能检出相应突变株的比例分别为 99.83%和99.90%。
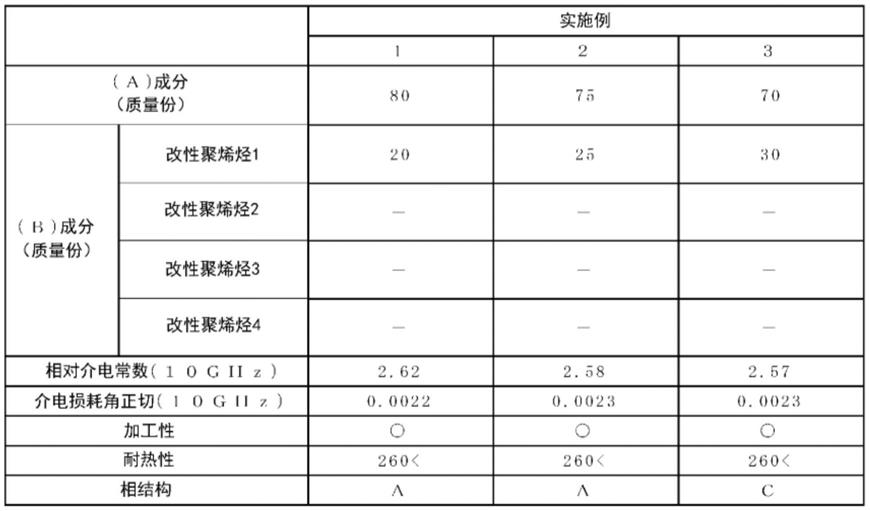
26.表1:基于gsaid上1,240,000个sars
‑
cov
‑
2的基因组序列得到的结果
[0027][0028]
一个实施方式的sars
‑
cov
‑
2突变株alpha和delta的试剂盒的引物和 taqman探针序列包括:
[0029]
一种快速灵敏检测新型冠状病毒(sars
‑
cov
‑
2)alpha和delta突变体的引物及taqman探针,其特征在于,所述引物的上游引物3’末端的碱基与该突变体的特征突变碱基匹配,而与非该突变体的碱基错配,因此导致qpcr扩增的不同效率,由此判断突变株是否存在。
[0030]
所述的引物探针由4对引物探针组成,包括检测alpha和delta突变体的特异性引物探针以及检测宿主内参(ic)和病毒内参(sars2)的引物探针。
[0031]
(1)检测alpha突变体的特异性引物探针:
[0032]
alpha
‑
f:5
’‑
caacaatttggcagagacattgt
‑3’
(seqidno:1)
[0033]
alpha
‑
r:5
’‑
ccaagtaggagtaagttga
‑3’
(seqidno:2)
[0034]
alpha
‑
p:5
’‑
hex
‑
tccacagacacttgagattcttgaca
‑
bhq1
‑3’
(seqidno:3)
[0035]
(2)检测delta突变体的特异性引物探针:
[0036]
delta
‑
f:5
’‑
gtcagtgtgttaatcttat
‑3’
(seqidno:4)
[0037]
delta
‑
r:5
’‑
gaaccaagtaacattggaa
‑3’
(seqidno:5)
[0038]
delta
‑
p:5
’‑
rox
‑
acattcaactcaggacttgttcttacc
‑
bhq2
‑3’
(seqidno:6)
[0039]
(3)检测宿主基因的引物探针:
[0040]
ic
‑
f:5
’‑
agtgcatgcttatctctgacag
‑3’
(seqidno:7)
[0041]
ic
‑
r:5
’‑
gcagggctatagacaagttca
‑3’
(seqidno:8)
[0042]
ic
‑
p:5
’‑
hex
‑
tttcctgtgaaggcgattgaccga
‑
bhq1
‑3’
(seqidno:9)
[0043]
(4)检测sars
‑
cov
‑
2的保守引物探针:
[0044]
sars2
‑
f:5
’‑
caatggtttaacaggcacagg
‑3’
(seqidno:10)
[0045]
sars2
‑
r:5
’‑
ctcaagtgtctgtggatcacg
‑3’
(seqidno:11)
[0046]
sars2
‑
p:5
’‑
fam
‑
acagcatcagtagtgtcagcaatgtctc
‑
bhq1
‑3’
(seqidno:12)
[0047]
一个实施方式的sars
‑
cov
‑
2突变株alpha和delta的试剂盒包括:
[0048]
所述试剂盒包括上述4套引物和探针,ic、sars、alpha、delta分别对应检测编码核糖核酸p蛋白亚基p30(rpp30)的人类基因的引物和探针作为人的内参,新型冠状病毒s基因上rbd的保守性片段的引物和探针作为病毒内参,以及sars
‑
cov
‑
2的alpha突变株和delta突变株。检测病毒内参和人的内参的两组引物探针在一个反应中,分别检测两种突变株的两组引物探针在另一个反应中。进一步地,所述引物的工作终浓度均为0.4μm,探针浓度均为0.1μm。进一步地,所述试剂盒采用taqman实时荧光定量pcr反应体系,总体系为20μl,包括采用vazyme(codeno.q222
‑
01)mix10μl,1μlenzymemix,0.8μl10μm上游引物,0.8μl10μm下游引物,0.2μl10μm探针,2.2μl的无核酸酶的水,最后加入提取的rna模板5μl。将反应体系混匀后短暂离心,在bioradcfx96荧光定量pcr运行,反应条件为逆转录50℃30min,预变性95℃30s,以95℃10s,57℃30s,扩增40个循环并采集荧光信号。
[0049]
采用印度株(delta)、英国株(alpha)、武汉株的rna样本对试剂盒的灵敏度进行了表征,对该试剂盒的检测效果进行评价,最终得到反转录荧光定量pcr的结果如表2所示。可以看出检测突变株的引物探针能够有效地扩增相应的突变株的核酸,并且ct值与使用病毒内参的引物探针扩增rbd保守片段的ct值很接近,但是对非目标突变株或者武汉株的扩增效率很低或者不扩增,因此可以根据这种ct值的差异分析是否存在突变株。
[0050]
表2:各样本分别10倍稀释、100倍稀释和1000倍稀释的检测结果
[0051][0052]
本发明创新性地利用生信技术对gisaid数据库中大规模的sars
‑
cov
‑
2 基因组高质量的测序数据进行分析,挖掘出sars
‑
cov
‑
2alpha和delta突变体 的保守的特异性突变位点,基于这两种突变位点,把扩增阻滞突变系统 (amplification refractory mutation system,(arms))与反转录qpcr结合, 设计了一种快速灵敏检测这两种突变体的引物探针及试剂盒,大大提高了突变 株的检测效率和检测速度。
[0053]
一个实施方式的sars
‑
cov
‑
2突变株alpha和delta的试剂盒的灵敏度包括:
[0054]
进一步评价该试剂盒的灵敏度,分别将印度株、英国株的rna进行梯度稀 释,检测试剂盒的灵敏度。最终得到如表3所示的荧光定量pcr的ct值的结果。 能够被检测到的最低样本浓度对应的拷贝数即为检测该突变株的检测限。从结 果看出,该试剂盒的最低检测限为1copy/μl。
[0055]
表3:试剂盒对delta和alpha灵敏度检测结果
[0056][0057]
一个实施方式的sars
‑
cov
‑
2突变株alpha和delta的试剂盒应用于临床样 本检测包括:
[0058]
将所述试剂盒用于80个临床样本检测,检测的结果如表4所示。80个临床 样本中,检测出2个sars
‑
cov
‑
2的alpha突变株,35个sars
‑
cov
‑
2的delta 突变株,43个非sars
‑
cov
‑
2的alpha突变株、非sars
‑
cov
‑
2的delta突变株 或阴性样本。这些突变株经ngs或一代测序验证。从表4的结果可以看出,对 于核酸含量很低的样本(ct值38以上),用所述试剂盒也能检测出其是否为目 标突变株,说明了所述试剂盒的灵敏性和特异性。而对于有些核酸含量高的样 本(ct值<29),某些突变株能检测出较高的ct值(>35),对这些核酸含量高 的样本,所述试剂盒有很弱的非特异性扩增,因此在实际实施过程中,我们采 用突变株检测ct值与病毒本身(sars2)所检测的ct值的差值在5以上,说明 无目标突变株存在。
[0059]
表4:试剂盒应用于80个临床样本中sars
‑
cov
‑
2突变型的鉴定结果
[0060]
[0061]
[0062][0063]
本发明并不仅仅限于说明书和实施方式中所描述,因此对于熟悉领域的人 员而言可容易地实现另外的优点和修改,故在不背离权利要求及等同范围所限 定的一般概念的精神和范围的情况下,本发明并不限于特定的细节、代表性的 设备和这里示出与描述的图示示例。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。