1.本技术属于基因工程技术领域,尤其涉及一种抗肿瘤重组胶原蛋白及其制备方法和应用。
背景技术:
2.胶原蛋白是哺乳动物中最重要和最丰富的蛋白质之一,在人体的皮肤、结缔组织和骨骼以及其它组织中发现的结构蛋白。在人体内胶原蛋白的含量约为总蛋白质的30%。胶原蛋白的结构是三螺旋,由命名为gly
‑
x
‑
y的重复的三联体氨基酸序列组成,x和y可以是任何氨基酸。重组胶原蛋白具有良好的水溶性、无病毒感染风险、低排异性、生物相容性等优点,在生物医药、组织工程、食品、化妆品等领域有着广泛的应用。
3.胶原蛋白可以给予肌肤必需的养分,改善皮肤细胞生存环境和促进组织的新陈代谢。目前,已有研究表明胶原蛋白寡肽是改善皮肤水分含量的功能因子,保持皮肤纤维结构的完整性,通过补充胶原蛋白合成所需的营养物质,起到修补受损细胞作用。同时,也有报道证实人胶原xv
‑
α1具有改善睡眠效果,人胶原iv
‑
α3具有诱导细胞凋亡作用。因此,在特定领域,通过特定的氨基酸替代、氨基酸序列修饰可精确构建胶原蛋白,可在疾病控制和治疗方面起到更有效的作用,也将会是一种更安全更高效的选择。
技术实现要素:
4.本技术的目的在于提供了一种抗肿瘤重组胶原蛋白,所述抗肿瘤重组胶原蛋白能有效支持细胞粘附、提高皮肤抗氧化损伤能力、显著抑制肿瘤细胞增殖。可广泛应用于食品、保健品、生物医药等领域。
5.本技术的具体技术方案如下:
6.1、一种抗肿瘤重组胶原蛋白,其特征在于,其氨基酸序列如seq id no.1所示。
7.2、一种核酸分子,其特征在于,其编码项1所述的重组胶原蛋白。
8.3、根据项2所述的核酸分子,其特征在于,其序列如seq id no.2所示。
9.4、一种宿主细胞,其特征在于,其包含项2所述核酸分子。
10.5、根据项4所述的宿主细胞,其特征在于,所述宿主细胞选自毕赤酵母、酿酒酵母、大肠杆菌、枯草芽孢杆菌中的任意一种。
11.6、一种制备项1所述重组胶原蛋白的方法,其特征在于,其包括下述步骤:
12.利用项4或5所述的宿主细胞进行表达,然后进行分离纯化得到。
13.7、根据项6所述的方法,其特征在于,所述分离纯化的方法包括盐析法、超滤法、亲和层析法和凝胶过滤层析法。
14.8、项1所述的重组胶原蛋白,或项2或3所述的核酸分子所编码的重组胶原蛋白,或由项4或5所述的宿主细胞生产的重组胶原蛋白在制备具有抗氧化、抑制肿瘤生长的食品、化妆品、保健品及药物组合物中的应用。
15.9、一种抗肿瘤药物组合物,其特征在于,其包括项1所述的重组胶原蛋白,或项2或
3所述的核酸分子所编码的重组胶原蛋白,或由项4或5所述的宿主细胞生产的重组胶原蛋白。
16.发明的效果
17.1.本技术的重组胶原蛋白是全新的序列,长度远小于天然人胶原蛋白基因,且其翻译的蛋白分子量小,容易制备。
18.2.本技术制备的重组胶原蛋白由毕赤酵母工程菌表达而得,该蛋白无内毒素隐患,且该蛋白携带组氨酸标记,可通过特异性亲和进行纯化,纯化步骤简单。
19.3.本技术的方法所制备的基因重组胶原蛋白,能有效促进哺乳动物抗氧化能力提升、抑制肿瘤细胞生长的作用。
具体实施方式
20.下面结合实施例进一步说明本技术,应当理解,实施例仅用于进一步说明和阐释本技术,并非用于限制本技术。
21.除非另外定义,本说明书中有关技术的和科学的术语与本领域内的技术人员所通常理解的意思相同。虽然在实验或实际应用中可以应用与此间所述相似或相同的方法和材料,本文还是在下文中对材料和方法做了描述。在相冲突的情况下,以本说明书包括其中定义为准,另外,材料、方法和例子仅供说明,而不具限制性。以下结合具体实施例对本技术作进一步的说明,但不用来限制本技术的范围。
22.如本文所使用的,术语“多肽”、“肽”、“蛋白”、“蛋白质”在本文中互换使用以意指氨基酸残基的聚合物。即,针对多肽的描述同样适用于描述肽和描述蛋白质,且反之亦然。所述术语适用于天然产生氨基酸聚合物以及其中一个或一个以上氨基酸残基为非天然编码氨基酸的氨基酸聚合物。如本文中所使用,所述术语涵盖任何长度的氨基酸链。
23.如本文所使用的,术语“核酸分子”可以包括包含天然和/或非天然存在的核苷酸和碱基的那些,例如包括具有骨架修饰的那些,所述核酸分子指的是核苷酸的聚合物,核苷酸的此类聚合物可以含有天然和/或非天然核苷酸,并且包括但不限于dna、rna和pna。核苷酸序列指的是构成核酸分子的线性序列。
24.在一些情况下,核酸分子含有cdna,在一些情况下,可以修饰核酸分子以用于本技术所述的构建体中,如用于密码子优化。在一些情况下,出于克隆到载体的目的,可以将序列设计为含有末端限制性位点序列。
25.在一些情况下,核酸分子可以从多种来源获得,如通过一种或多种给定细胞内的或从所述一种或多种给定细胞中分离的编码核酸的聚合酶链式反应(pcr)扩增获得。
26.如本文所使用的,术语“多核苷酸”或“核苷酸”意指单股或双股形式的脱氧核糖核苷酸、脱氧核糖核苷、核糖核苷或核糖核苷酸及其聚合物。除非特定限制,否则所述术语涵盖含有天然核苷酸的已知类似物的核酸,所述类似物具有类似于参考核酸的结合特性并以类似于天然产生的核苷酸的方式进行代谢。除非另外特定限制,否则所述术语也意指寡核苷酸类似物,其包括pna(肽核酸)、在反义技术中所用的dna类似物(硫代磷酸酯、磷酰胺酸酯等)。除非另外指定,否则特定核酸序列也隐含地涵盖其保守修饰的变异体(包括(但不限于)简并密码子取代)和互补序列以及明确指定的序列。
27.如本文所使用的,术语“载体”用于描述可以被工程化以含有可以在宿主细胞中扩
增的克隆的一种多核苷酸或多种多核苷酸的核酸分子。载体包括但不限于:单链,双链或部分双链的核酸分子;包含一个或多个游离末端,没有游离末端(例如环状)的核酸分子;包含dna,rna或两者的核酸分子;以及本领域已知的其它多核苷酸种类。一种类型的载体是“质粒”,其是指可以插入额外dna片段的环状双链dna环,例如通过标准分子克隆技术。某些载体能够在引入它们的宿主细胞中自主复制(例如,具有细菌复制起点的细菌载体和游离型哺乳动物载体)。其它载体(例如,非游离型哺乳动物载体)在引入宿主细胞后整合到宿主细胞的基因组中,从而与宿主基因组一起复制。此外,某些载体能够指导它们可操作地连接的那些基因的表达。此类载体在本文中称为“表达载体”。重组表达载体可以包含适于在宿主细胞中表达核酸的形式的本技术的核酸,这意味着重组表达载体包括一种或多种调节元件,其可以基于用于表达的、可以与待表达的核酸序列可操作地连接的宿主细胞来选择。
28.如本文所使用的,术语“表达”包括变体产生所涉及的任何步骤,包括但不限于转录、转录后修饰、翻译、翻译后修饰和分泌。
29.如本文所使用的,术语“表达载体”意指直链或环状的dna分子,其包含编码变体的多核苷酸,并可操作地连接于提供其表达的其它核苷酸。
30.如本文所使用的,术语“宿主细胞”意指任何细胞类型,其易受包含本技术的多核苷酸的核酸构建体或表达载体的转化、转染、转导等。术语“宿主细胞”涵盖亲本细胞的任何后代,其由于复制过程发生的突变与亲本细胞不完全相同。宿主细胞可以是在本技术的重组类人胶原蛋白生产中有用的任何细胞。
31.如本文所使用的,术语“重组胶原蛋白”是指通过重组技术产生的胶原蛋白,其中通常将编码表达的蛋白质的dna或rna插入合适的表达载体中进而用于转化宿主细胞以产生蛋白质。在一些示例性实施方案中,将编码表达的蛋白质的dna或rna通过同源重组或本领域公知的其它方式插入宿主染色体,并因此用于转化宿主细胞以产生蛋白质。
32.本技术提供一种抗肿瘤重组胶原蛋白,其氨基酸序列如seq id no.1所示:
33.gapgapgsqgapglqgapgapgsqgapglqvsigyllvkhsqtdqepmcpvgmnklwsgysllyfegqekahnqdlglagsclarfstmpflycnpgdvcyyasrndksywlsttaplpmmpvaedeikpyisrcsvceapaiaiavhsqdvsiphcpagwrslwigysflmhtaagdegggqslvspgscledfratpfiecnggrgtchyyankysfwlttipeqsfqgspsadtlkaglirthisrcqvcmknlgapgapgsqgapglqgapgapgsqgapglqhhhhhh(seq id no.1)。
34.本技术还提供一种核酸分子,其编码上述抗肿瘤重组胶原蛋白。
35.在一个具体的实施方式中,所述核酸分子的核苷酸序列如seq id no.2所示:
36.ggagcaccaggagctcctggtagtcaaggtgctccaggattacaaggtgctcctggagctccaggttctcaaggcgcccctggtctgcaggtttccatcggatacttgttggttaagcactctcagacagaccaggaaccaatgtgcccagttggtatgaacaagctttggtctggttactctctgttgtactttgaaggacaagagaaggctcacaaccaagatctaggcttggccggttcatgtttggctcgtttcagtacaatgccatttctgtactgtaatcccggcgacgtgtgttactatgcttcaagaaatgacaaatcttactggttgtctactactgcacctttgcctatgatgccagtcgctgaggacgaaattaaaccttatatctctcgttgttctgtctgcgaggcccctgctatcgctatcgccgttcactcacaggatgtgtctattcctcactgtcctgctggctggagatctttgtggattggatacagttttttgatgcataccgctgccggtgatgaaggtggtggtcagtcattggtgtcacctggatcatgcttagaggattttagagctaccccatttatcgaatgcaacggtggtagaggtacatgtcactactacgctaacaagtatagtttttggcttactactatcccag
aacaatcttttcaaggctccccttcagctgatacattgaaagccggtcttattcgtacccacatttcccgttgccaagtgtgtatgaagaatcttggagcccctggagctccaggatctcagggagctccaggtttgcaaggtgctccaggtgccccaggtagtcaaggagctccaggattgcagcaccaccatcatcatcac(seq id no.2)。
37.本技术提供一种表达载体,其包含上述核酸分子。
38.例如,将编码上述重组胶原蛋白的一种或多种核酸克隆到合适的一种或多种表达载体中,表达载体可以是任何合适的重组表达载体,并且可以用于转化或转染任何合适的宿主。合适的载体包括设计用于繁殖和扩增或用于表达或用于两者的那些,如质粒和病毒。
39.所述载体可以含有调节序列(如转录和翻译起始和终止密码子),其对待引入载体的宿主的类型(例如,细菌、真菌、植物或动物)具有特异性,酌情并考虑载体是基于dna还是基于rna。
40.在一个具体的实施方式中,所述表达载体为ppic9k。
41.本技术提供一种宿主细胞,其包含上述核酸分子。
42.为了产生重组胶原蛋白,可以将编码重组胶原蛋白的核酸分离,并且将其插入一种或多种载体中,以在宿主细胞中进一步克隆/或表达。可以使用常规技术(例如,通过使用能够与编码重组胶原蛋白的基因特异性结合的寡核苷酸探针)容易地分离和测序这种核酸。
43.所述宿主细胞是指已引入外源核酸的细胞,包括此类细胞的后代。宿主细胞包括转化体和转化细胞,其包括原代转化细胞和源自其的后代,不考虑传代次数。后代在核酸含量上可能与亲代细胞不完全相同,但可能含有突变。
44.对于载体导入宿主细胞中的方法是公知的,例如使用电转化将载体导入宿主细胞中。
45.在一个具体的实施方式中,所述宿主细胞选自毕赤酵母、酿酒酵母、大肠杆菌、枯草芽孢杆菌中的任意一种。
46.在一个具体的实施方式中,所述宿主细胞为毕赤酵母。
47.本技术提供一种制备前述任一种重组胶原蛋白的方法,其包括如下步骤:
48.利用上述的宿主细胞进行表达,然后进行分离纯化得到。
49.所述将宿主细胞进行表达指的将宿主细胞进行培养,培养基和培养条件对于本领域技术人员来说是公知的。
50.在一个具体的实施方式中,所述宿主细胞为毕赤酵母,得到毕赤酵母基因工程菌后,具体的培养条件如下:将毕赤酵母基因工程菌接种于ypd培养基中,于30℃,220rpm条件下培养22~24h,至od
600
=18~20作为上罐种子液,将种子液扩培后按10%接种量接入初始体积为12l的nbs 415
‑
19.2l发酵罐中,培养温度为28~30℃,ph=5.0~6.0,溶氧控制在20%~30%,待甘油耗尽,开始进入甘油补料培养,至菌体湿重达到180g/l以上时,开始进行诱导培养。
51.对于表达方式,本技术不作任何限制,其可以根据需要进行确认,例如表达为诱导表达,对于诱导表达,其诱导剂甲醇。
52.在一个具体的实施方式中,流加甲醇进行诱导培养,诱导阶段温度为28℃,ph为5.0,诱导48h放罐。
53.对于分离纯化的方法,本技术不作任何限制,其可以根据进行确定,例如可以使用
盐析法、超滤法、亲和层析法和凝胶过滤层析法。
54.本技术还提供上述的重组胶原蛋白,或上述核酸分子所编码的重组胶原蛋白,或上述表达载体所表达的重组胶原蛋白,或上述宿主细胞生产的重组胶原蛋白在制备具有抗氧化、抑制肿瘤生长的食品、化妆品、保健品及药物组合物中的应用。
55.本技术还提供一种抗肿瘤药物组合物,其包括上述的重组胶原蛋白,或上述核酸分子所编码的重组胶原蛋白,或上述表达载体所表达的重组胶原蛋白,或上述宿主细胞生产的重组胶原蛋白。
56.实施例
57.实施例1
58.表达工程菌ppic9k
‑
cola
‑
6his/毕赤酵母gs115的构建和表达
59.化学合成本技术的重组胶原蛋白基因(核苷酸序列如seq id no.2所示)。合成时在5'端和3'分别加入了eco r i和not i识别位点和组氨酸标签,经限制性内切酶sal i线性化后克隆至表达载体ppic9k中,以毕赤酵母gs115为表达宿主菌,通过电转化将获得的ppic9k
‑
cola
‑
6his克隆质粒线性化后转化到gs115中。以g418梯度法挑选高拷贝阳性克隆,30℃培养72h得到毕赤酵母基因工程菌。
60.将上述得到的毕赤酵母基因工程菌接种于ypd培养基,培养至od
600
=19.2时按10%接种量接入初始体积为12l的nbs 415
‑
19.2l发酵罐中,培养温度为30℃,ph=5.5,溶氧控制在20%~30%,待甘油耗尽,开始进入甘油补料培养,至菌体湿重达到190g/l以上时,开始流加甲醇进行诱导培养,诱导阶段温度为28℃,ph为5.0,诱导48h放罐,离心收集上清液。
61.实施例2
62.重组胶原蛋白的纯化
63.(1)将离心收集的上清液超滤至初始体积的50%时,加入3~5倍体积的纯水,再经超滤浓缩至初始体积的5%;
64.(2)将浓缩后的上清液加入60%饱和硫酸铵,常温下搅拌30min,9000rpm离心10min后收集沉淀,将得到的沉淀溶解于500ml0.05m,ph为7.0的pbs后经0.45μm滤膜过滤;
65.(3)取20ml过滤后的粗蛋白溶液上样ni
‑
nat柱,流速为1ml/min,采用50mm ph 7.4的pbs缓冲液冲洗30ml;
66.(3)用30ml,100mm的咪唑缓冲液(50mm ph 7.4的pbs 0.5m nacl)洗脱目标蛋白,流速为2.0ml/min;
67.(4)收集洗脱下的目标蛋白,经sephadex g25柱(ge healthcare,xk26/20;柱体积50ml)脱盐,再经超滤浓缩至初始体积的20
‑
30%,然后置于
‑
20℃冰箱预冻4h,然后转入真空冷冻干燥机中进行冻干,48h后收集冻干后蛋白。
68.实施例3
69.抗氧化性试验
70.重组胶原蛋白清除超氧阴离子自由基能力的测定采用邻苯三酚自氧化法测定样品清除超氧阴离子自由基的活性:空白组中加入9ml tris
‑
hcl缓冲液(50mmol/l ph 8.2)和20μl邻苯三酚溶液,在325nm,25℃条件下监测吸光度的变化,调节邻苯三酚的加入量使其自氧化的速率约为0.07od/min。实验组是在上述体系下加入不同量的重组胶原蛋白,同
样方法在325nm,25℃条件下测定吸光值。
71.重组胶原蛋白对pr自氧化抑制率依据下式计算:
72.抑制率i=(δa0
‑
δa)/δa0
×
100%
73.其中,δa0为邻苯三酚自氧化的速率,δa为重组胶原蛋白抑制的邻苯三酚自氧化的速率。活力单位定义:在反应温度为25℃、邻苯三酚的终浓度为0.1mm、tris
‑
hcl缓冲液ph值为8.2的条件下,使每毫升反应液自氧化速率抑制50%的抑制剂量为1个活力单位(u)。结果见表1。
74.表1 不同浓度重组胶原蛋白对邻苯三酚自氧化作用的抑制率
[0075][0076]
从表1可以看出,本技术方法制备的重组胶原蛋白有非常显著的抗氧化活性,且呈现一定的浓度依赖关系。其原因可能是重组胶原蛋白中侧链带电基团可以强烈地增加邻苯三酚溶液的极性,而邻苯三酚在极性条件下更易分解自氧化,从而产生更多的o2,最终表现出促进邻苯三酚自氧化的性质。
[0077]
实施例4
[0078]
人乳腺癌细胞抑制肿瘤细胞实验
[0079]
将每孔接种1.5
×
106人乳腺癌细胞的96孔培养板放到co2培养箱中培养24h(饱和湿度、37℃、5%co2),空白组为正常细胞培养液,实验组为重组胶原蛋白,每个浓度设置3个平行孔,培养时间为24h、48h、72h,据培养结束约4小时,每孔加入20μl mtt溶液后继续培养,培养结束采用mtt测定细胞抑制率。结果采用spss 16.0统计软件进行统计学分析,实验数据用均值
±
标准差表示。实验结果见表2所示。
[0080]
抑制率(%)=(对照组od值
‑
实验组od)/对照组od值
[0081]
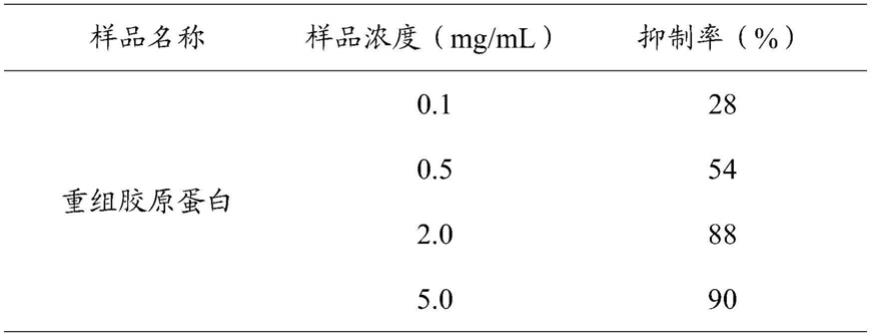
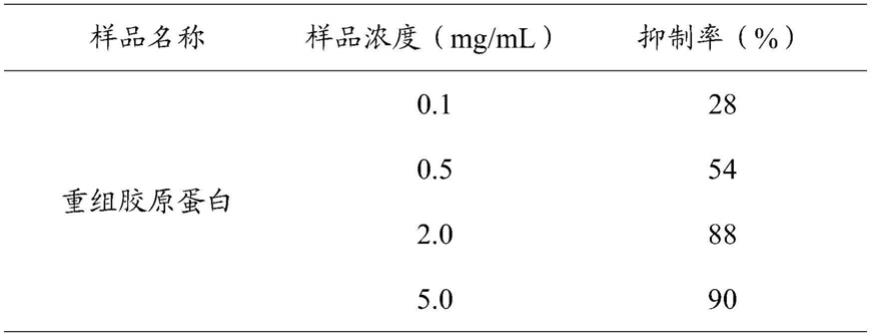
表2 不同浓度重组胶原蛋白对人乳腺癌细胞的抑制率
[0082][0083]
由表2结果可知,重组胶原蛋白在浓度为20mg/l、40mg/l、60mg/l、80mg/l、100mg/l时均能抑制人乳腺癌细胞的增殖,其中胶原蛋白在浓度为60mg/l时,对人乳腺癌细胞的抑制率达到最大。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。