1.本技术属于光热材料技术领域,具体涉及一种复合光热材料及其制备方法和应用。
背景技术:
2.癌症,又称恶性肿瘤,一直以来严重影响人类的生命健康。据统计,到2030年癌症新发病例将从每年1400万上升到每年2200万,目前我国每分钟有6人被诊断为癌症,每7
‑
8人中就有1人死于癌症,癌症正成为人类生命健康最主要的残酷杀手之一。据深圳市慢性病防治中心公布的最新肿瘤监测数据显示,2018年深圳市共报告常住人口新发肿瘤病例25587例,其中男性11399例,女性14188例,女性数量多于男性。肺癌依旧位居全部及男性恶性肿瘤榜首,乳腺癌位居女性恶性肿瘤首位。
3.目前,治疗癌症的方法通常以手术治疗和化疗为主。然而传统的手术治疗很难将癌变组织完全清除干净,也不能克服由于恶性肿瘤的高转移性导致的复发。化疗手段虽然能实现全身治疗,但是目前化疗药物给药效率低,毒副作用大,在杀死癌细胞的同时也将大量的正常体细胞杀死。另外,现有的化疗手段很难有效跟踪药物分子,无法实时判断药效,从而无法实现癌症的精准给药治疗。因此研发具有光控释放和精准给药的高效抗癌药物已成为当今医学研究领域的热门课题。
4.当前,光热治疗作为新型的肿瘤治疗方法正受到越来越多的关注,其治疗特点一方面通过近红外光照射使肿瘤区域形成过高温环境,促进肿瘤细胞的凋亡;另一方面通过高温可以促进肿瘤部位的药物可控释放,达到精准给药和协同促进杀伤肿瘤细胞的效果。其中,二维材料因其具有良好的生物相容性和较高的光热转换效率被广泛用于肿瘤的光热治疗。例如,旧金山加利福尼亚大学的huang xiaohua通过调控生长液中ag
浓度合成了一系列不同尺寸的金纳米棒(aunrs),筛选了最佳光热转换效率的aunrs,并用于转移癌细胞的光热治疗。中科院理化所geng jianxin报道了应用表面功能化的石墨烯(go)作为光热剂在肿瘤治疗中表现出增强的光热效应,其增强机理主要是光生能量从表面聚合物分子转移到石墨烯表面使其光热转换效率达到约25%。深圳大学zhang han制备出二维黑磷量子点(bpqds)作为光热剂用于肿瘤的光热治疗,其光热转换效率达到28.4%并表现出良好的生物兼容性。然而当前的二维材料诸如金纳米棒、石墨烯等作为光热剂仍然面临着光热转换效率低和稳定性差等缺点。探索高光热转换效率和高稳定性的新型二维材料光热剂仍然是肿瘤光热治疗研究的关键。
5.此外,随着药理、病理和诊疗手段的日益改进,单一功能的抗癌药物或者治疗方法已经不能满足科研和应用的要求。联合治疗成为当前癌症治疗的新策略。将两种或者多种不同作用机理的抗癌药物或者治疗方法有效结合能够发挥协同增效作用,以达到更好抑制肿瘤生长的目的。尤其通过近红外光的调控来实现纳米复合药物的精准给药和肿瘤联合高效治疗具有重要的研究价值和应用前景。虽然目前有公开报道联合治疗所取得的进展,如目前公开的介孔氧化硅包覆的氧化石墨烯为载体负载阿霉素(dox)比单一的功能的抗癌药
物对细胞毒性效果要好,但是当前联合治疗药物也存在一定的不足。具体的如光热转化效率较低,常用的光热剂如金纳米壳(13%)、金纳米棒(21%)、石墨烯氧化物(25%)、cu2‑
xse纳米颗粒(22%)、mos2‑
peg纳米片(27.6%)、bpqd(28.4%)、bi2s3纳米棒(28.1%)或bi2s3纳米球形海绵(31.1%)等光热效率不高,导致光热治疗效果不理想。
技术实现要素:
6.本技术的目的在于克服现有技术的上述不足,提供一种复合光热材料及其制备方法和应用,以解决现有光热剂光热转换效率低和稳定性不理想和联合治疗药物存在疗效不理想的技术问题。
7.为了实现上述申请目的,本技术的第一方面,提供了一种复合光热材料。本技术复合光热材料包括二维光热材料基体,二维光热材料基体为二维锑烯,在二维锑烯上负载有纳米银颗粒。
8.进一步地,二维锑烯的厚度为0.5nm~1μm。
9.进一步地,二维锑烯的平面面积为50nm2~3000nm2。
10.进一步地,纳米银颗粒是原位生长在二维锑烯上。
11.进一步地,纳米银颗粒为亚纳米银簇。
12.进一步地,纳米银颗粒的粒径为0.5nm~100nm。
13.进一步地,二维锑烯与纳米银颗粒的摩尔比为1:0.05~1:0.5。
14.进一步地,还包括靶向剂,靶向剂结合在二维锑烯和/或纳米银颗粒上。
15.更进一步地,靶向剂包括靶向多肽、生长因子、靶向药剂中的至少一种。
16.更进一步地,二维锑烯与靶向剂的摩尔比为1:0.05~1:0.2。
17.具体地,靶向多肽包括rgd
‑
peg
‑
pla靶向多肽、dspe
‑
peg
‑
otc生长抑索受体靶向多肽、温度响应性类弹性蛋白多肽、富精氨酸多肽、dspe
‑
peg5000
‑
rgd|磷脂
‑
peg
‑
靶向肽、紫杉醇csnrdarrc
‑
pcl
‑
pga/tpgs多肽中的至少一种。
18.具体地,生长因子包括特异性靶向vegfr2。
19.具体地,靶向药剂包括依维莫斯靶向试剂、t
‑
dm1乳癌靶向药中的至少一种。
20.进一步地,还包括表面活性剂,表面活性剂修饰结合在二维锑烯上。
21.更进一步地,表面活性剂包括聚乙二醇、聚乙烯吡咯烷酮、吐温中的至少一种;和/或
22.更进一步地,二维锑烯与表面活性剂的摩尔比为1:0.2~1:2。
23.本技术的第二方面,提供了一种复合光热材料的制备方法。本技术复合光热材料的制备方法包括如下步骤:
24.提供二维锑烯;
25.在二维锑烯上形成纳米银颗粒,使得纳米银颗粒负载在二维锑烯上,得到复合光热材料。
26.进一步地,在二维锑烯上形成纳米银颗粒的方法包括如下步骤:
27.将经表面活性剂改性的二维锑烯配制成二维锑烯分散液;
28.向二维锑烯分散液中加入银盐和还原剂,进行混合处理和还原反应,在二维锑烯上原位沉积纳米银颗粒。
29.进一步地,还包括如下步骤:
30.将复合光热材料配合成分散液,将分散液与靶向剂进行混合处理,在二维锑烯和/或纳米银颗粒上结合靶向剂。
31.更进一步地,二维锑烯分散液与银盐是按照二维锑烯:银离子的摩尔比为1:0.05~1:0.5的比例进行混合处理。
32.更进一步地,银盐为银离子配合物。
33.更进一步地,分散液与靶向剂的混合比例保证在制备的复合光热材料上,二维锑烯:靶向剂的摩尔比为1:0.05~1:0.2。
34.本技术的第三方面,提供了本技术的应用方法。本技术复合光热材料在光热剂、药物载体、光热催化、光热治疗剂或光热发电材料中的应用。
35.与现有技术相比,本技术具有如下技术效果:
36.本技术第一方面提供的复合光热材料以二维锑烯作为双功能响应平台的基体,一方面发挥锑烯作为光热剂引导的光热治疗,另一方面发挥利用锑烯光热转换效应促使其负载的纳米银颗粒解离引导的光动力治疗,进而通过近红外光调控实现光热/光动力协同治疗的作用,达到显著治疗癌症的效果。
37.本技术第二方面提供的复合光热材料制备方法将纳米银颗粒形成在二维锑烯上,实现二维锑烯负载纳米银颗粒,从而赋予制备的复合光热材料具有上述本技术复合光热材料所具有的能够通过近红外光调控实现光热/光动力协同治疗作用特性,而且本技术复合光热材料制备方法工艺步骤和条件可控,制备的复合光热材料具有光热/光动力协同治疗作用的性能稳定,而且制备方法的效率高,降低了经济成本。
38.本技术第三方面提供的复合光热材料的应用中,由于本技术具有能够通过近红外光调控实现光热/光动力协同治疗的作用,因此,有效增强了本技术复合光热材料的应用效果和领域。
附图说明
39.为了更清楚地说明本技术具体实施方式或现有技术中的技术方案,下面将对具体实施方式或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图是本技术的一些实施方式,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
40.图1为本技术实施例复合光热材料的结构示意图;
41.图2为图1所示本技术实施例复合光热材料含有靶向剂的结构示意图;
42.图3为图2所示含有靶向剂的本技术实施例复合光热材料在靶向位点起到光热/光动力协同治疗癌症的原理示意图;
43.图4为本技术实施例复合光热材料的制备方法流程框图;
44.图5为本技术实施例复合光热材料的制备方法流程示意图;
45.本技术实施例复合光热材料通过其负载的靶向剂达到靶向位点后,复合光热材料通过细胞壁并在光照如红外光照射后,
46.图6为对比例1中二维锑烯水分散液在光照下温度变化图;其中,a图为对比例1中的不同二维锑烯水分散液随着近红外光照射时间的温度变化曲线图;b图为对比例1中二维
锑烯水分散液随着激光开启和关闭的温度变化曲线图;
47.图7为实施例1、对比例1和空白组的分散液在808nm近红外激光照射下ros量的变化曲线图。
具体实施方式
48.为了使本技术要解决的技术问题、技术方案及有益效果更加清楚明白,以下结合实施例,对本技术进行进一步详细说明。应当理解,此处所描述的具体实施例仅仅用以解释本技术,并不用于限定本技术。
49.本技术中,术语“和/或”,描述关联对象的关联关系,表示可以存在三种关系,例如,a和/或b,可以表示:单独存在a,同时存在a和b,单独存在b的情况。其中a,b可以是单数或者复数。字符“/”一般表示前后关联对象是一种“或”的关系。
50.本技术中,“至少一个”是指一个或者多个,“多个”是指两个或两个以上。“以下至少一项(个)”或其类似表达,是指的这些项中的任意组合,包括单项(个)或复数项(个)的任意组合。例如,“a,b,或c中的至少一项(个)”,或,“a,b,和c中的至少一项(个)”,均可以表示:a,b,c,a
‑
b(即a和b),a
‑
c,b
‑
c,或a
‑
b
‑
c,其中a,b,c分别可以是单个,也可以是多个。
51.应理解,在本技术的各种实施例中,上述各过程的序号的大小并不意味着执行顺序的先后,部分或全部步骤可以并行执行或先后执行,各过程的执行顺序应以其功能和内在逻辑确定,而不应对本技术实施例的实施过程构成任何限定。
52.在本技术实施例中使用的术语是仅仅出于描述特定实施例的目的,而非旨在限制本技术。在本技术实施例和所附权利要求书中所使用的单数形式的“一种”、“所述”和“该”也旨在包括多数形式,除非上下文清楚地表示其他含义。
53.本技术实施例说明书中所提到的相关成分的重量不仅仅可以指代各组分的具体含量,也可以表示各组分间重量的比例关系,因此,只要是按照本技术实施例说明书相关组分的含量按比例放大或缩小均在本技术实施例说明书公开的范围之内。具体地,本技术实施例说明书中所述的质量可以是μg、mg、g、kg等化工领域公知的质量单位。
54.第一方面,本技术实施例提供了一种复合光热材料。本技术实施例复合光热材料包括二维光热材料基体和纳米银颗粒。其结构如图1和图2所示,包括二维光热材料基体1和负载在二维光热材料基体1上的纳米银颗粒2。
55.其中,本技术实施例复合光热材料所含的二维光热材料基体1为二维锑烯。这样,本技术实施例复合光热材料以二维锑烯作为光热材料也即是以二维光热材料基体1作为双功能响应平台的基体,其能够有效吸收红外光能并将其转换热能,实现对病灶病毒或癌细胞进行杀灭作用,实现光热治疗作用。与此同时,当复合光热材料作为载体负载有药物活性时,那么二维锑烯的光热转换效应还能够促使病灶如肿瘤部位的药物可控释放。另外,二维锑烯负载的纳米银颗粒2能够起到导电子助剂的作用,将二维锑烯在发挥光热转换效应过程中产生的电子传导进行传到纳米银颗粒2并促使纳米银颗粒2和二维锑烯产生活性氧物以实现对病灶病毒或癌细胞进行杀灭作用,以实现复合光热材料同时具备光动力治疗作用。因此,本技术实施例复合光热材料通过二维锑烯基体和其负载的纳米银颗粒2之间的协同增效作用,赋予本技术实施例复合光热材料同时具有光热/光动力协同治疗的作用,达到增强治疗癌症的作用和效果。
56.实施例中,本技术实施例复合光热材料所含的二维锑烯与纳米银颗粒的摩尔比为1:0.05~1:0.5。通过控制两者的比例,提高两者的协同增效作用,从而提高本技术实施例复合光热材料同时具备的光热/光动力协同治疗作用,进一步增强其治疗癌症的作用和效果。
57.实施例中,本技术实施例复合光热材料所含的二维光热材料基体1也即是二维锑烯的厚度为0.5nm~1μm,进一步为0.5nm~10nm,具体可以为0.5nm、1nm、2nm、3nm、4nm、5nm、6nm、7nm、8nm、9nm、10nm、50nm、100nm、200nm、300nm、400nm、500nm、600nm、700nm、800nm、900nm、1000nm等典型但非限制性的厚度。通过对二维锑烯厚度的控制,间接对二维锑烯的层数进行优化控制,从而使得二维锑烯具有更丰富的活性位以具有相对高的光热效应和提高其促使的光动力效果。
58.实施例中,二维锑烯的平面面积为50nm2~3000nm2,进一步为50nm2~200nm2,具体可以为50nm2、100nm2、150nm2、200nm2、500nm2、1500nm2、2000nm2、2500nm2、3000nm2等典型但非限制性的面积。通过对二维锑烯平面面积的选择和调节,能够控制复合光热材料的尺寸,从而能够增强本技术实施例复合光热材料的应用性能,提高其同时具有的光热/光动力协同治疗作用。
59.本技术实施例复合光热材料所含的纳米银颗粒2如上文所述的,其能够起到导电子助剂的作用,将二维锑烯在发挥光热转换效应过程中产生的电子传导进行传到纳米银颗粒2并促使纳米银颗粒2和二维锑烯产生活性氧物以实现对病灶病毒或癌细胞进行杀灭作用,以实现复合光热材料同时具备光动力治疗作用。实施例中,纳米银颗粒2是原位生长在二维锑烯上。这样,不仅能够增强纳米银颗粒2负载的稳定性,提高本技术实施例复合光热材料的结构稳定性,而且提高了纳米银颗粒2与二维锑烯之间的电导性率,从而能够提高了二维锑烯在光热效应过程中产生的电子传到至纳米银颗粒2,从而提高纳米银颗粒2和二维锑烯产生活性氧物的量以提高对病灶病毒或癌细胞进行杀灭效果。
60.实施例中,纳米银颗粒2为亚纳米银簇,在进一步实施例中,该纳米银颗粒的粒径为0.5nm~100nm,进一步为0.5nm~5nm,具体可以为0.5nm、1nm、2nm、3nm、4nm、5nm、6nm、7nm、8nm、9nm、10nm、20nm、30nm、40nm、50nm、60nm、70nm、80nm、90nm、1000nm等典型但非限制性的粒径。发明人在研究中发现,将纳米银颗粒2的粒径控制在亚纳米银簇,进一步在0.5nm~100nm,进一步为0.5nm~5nm范围,纳米银颗粒2发挥上段所述发挥纳米银颗粒2和二维锑烯在光热效应中产生活性氧物的量以对病灶病毒或癌细胞进行杀灭效果更优异。
61.在进一步实施例中,上述各实施例中本技术实施例复合光热材料还包括靶向剂,具体的如图2所示的靶向剂3。该靶向剂3是结合在二维锑烯1和/或纳米银颗粒2上。通过在靶向剂3,能够使得本技术实施例复合光热材料同时具备的光热/光动力协同治疗作用的基础上,同时具备靶向性,从容实现本技术实施例复合光热材料精准靶向给药并发挥光热/光动力协同治疗作用,或进一步实现精准靶向给药,释放活性药物成分。具体如图3所示,本技术实施例复合光热材料通过其负载的靶向剂达到靶向位点后,复合光热材料通过细胞壁并在光照如红外光照射后,复合光热材料起到光热/光动力协同治疗的作用,实现治疗癌症的作用和效果。
62.实施例中,二维锑烯与靶向剂3的摩尔比为1:0.05~1:0.2,具体可以为1:0.05、1:0.06、1:0.07、1:0.08、1:0.09、1:0.1、1:0.11、1:0.12、1:0.13、1:0.14、1:0.15、1:0.16、1:
0.17、1:0.18、1:0.19、1:0.2等典型但非限制性的摩尔比,通过对本技术实施例复合光热材料负载靶向剂3的含量,提高靶向剂3的靶向效果,从而提高本技术实施例复合光热材料的精准靶向光热/给药。
63.实施例中,靶向剂3包括靶向多肽、生长因子、靶向药剂、光热催化、光热治疗剂或光热发电材料中的至少一种。具体实施例中,靶向多肽包括rgd
‑
peg
‑
pla靶向多肽、dspe
‑
peg
‑
otc生长抑索受体靶向多肽、温度响应性类弹性蛋白多肽、富精氨酸多肽、dspe
‑
peg5000
‑
rgd|磷脂
‑
peg
‑
靶向肽、紫杉醇csnrdarrc
‑
pcl
‑
pga/tpgs多肽中的至少一种。生长因子包括但不仅仅为特异性靶向vegfr2。靶向药剂包括依维莫斯靶向试剂、t
‑
dm1乳癌靶向药中的至少一种。该些种类的靶向剂3赋予复合光热材料精准的靶向性,而且可以根据需要进行选择,实现不同靶向精准给药或光热治疗。
64.在进一步实施例中,上述各实施例中本技术实施例复合光热材料还包括表面活性剂(图1和图2未显示)。该表面活性剂修饰结合在二维锑烯上,当然也可以结合在纳米银颗粒2上,或同时接枝在二维锑烯和纳米银颗粒2上。通过在本技术实施例复合光热材料接枝表面活性剂,提高本技术实施例复合光热材料的分散性能,提高其光热/光动力协同治疗的作用。在具体实施例中,表面活性剂包括聚乙二醇(peg)、聚乙烯吡咯烷酮(pvp)、吐温中的至少一种。该些表面活性剂能够有效增强本技术实施例复合光热材料的分散性能,而且不影响其光热/光动力协同治疗作用的发挥。
65.第二方面,本技术实施例提供了上文复合光热材料的制备方法。本技术实施例复合光热材料的制备方法工艺流程如图4和图5所示,包括如下步骤:
66.s01:提供二维锑烯;
67.s02:在二维锑烯上形成纳米银颗粒,使得纳米银颗粒负载在二维锑烯上,得到复合光热材料。
68.这样,本技术实施例复合光热材料制备方法将纳米银颗粒形成在二维锑烯上,实现二维锑烯负载纳米银颗粒,构成复合结构的复合光热材料,使得制备的复合光热材料具有光热/光动力协同治疗作用的性能稳定。而且其制备方法的效率高,降低了经济成本。
69.其中,步骤s01中的二维锑烯为上文复合光热材料所含的二维光热材料基体1,也即是二维锑烯。因此,该步骤s01中的二维锑烯的厚度、面积等均如上文复合光热材料所含的二维锑烯的厚度、面积等。为了节约篇幅,在此不再对步骤s01中的二维锑烯做赘述。
70.二维锑烯可以按照现有方法制备获得,如采用超声辅助的液相剥离法制备获得。
71.实施例中,步骤s01中的二维锑烯的表面修饰结合有表面活性剂。该表面活性剂为上文复合光热材料所含的表面活性剂。因此,该表面活性剂的种类和其结合在二维锑烯的量均如上文复合光热材料所含的表面活性剂的种类和修饰结合量。通过在二维锑烯表面修饰结合表面活性剂,以提高二维锑烯配制的分散液中其分散性和分散的稳定性,这样能够提高步骤s02中的纳米银颗粒负载的均匀性。
72.实施例中,二维锑烯的表面修饰结合有表面活性剂的方法可以将二维锑烯与表面活性剂于溶剂中进行混合处理进行表面修饰。也可以在制备二维锑烯的过程中,如采用超声辅助的液相剥离法制备二维锑烯的过程中,采用含表面活性剂的溶液进行超声剥离二维锑烯,直接获得表面修饰结合有表面活性剂的二维锑烯。
73.步骤s02中,在二维锑烯上形成的纳米银颗粒为上文复合光热材料所含的纳米银
颗粒2。因此,该步骤s02中的纳米银颗粒的相关性能参数如形貌和粒径等均如上文复合光热材料所含的纳米银颗粒2的相关性能参数等。为了节约篇幅,在此不再对步骤s02中的纳米银颗粒做赘述。
74.实施例中,在二维锑烯上形成纳米银颗粒的方法包括如下步骤:
75.s021:将经表面活性剂改性的二维锑烯配制成二维锑烯分散液;
76.s022:向二维锑烯分散液中加入银盐和还原剂,进行混合处理和还原反应,在二维锑烯上原位沉积纳米银颗粒;
77.其中,步骤s021中的表面活性剂和二维锑烯分别如上文所述的表面活性剂和二维锑烯。其二维锑烯分散液的浓度可以根据实际情况配制和调节,以保证二维锑烯充分分散为前提。
78.步骤s022中的二维锑烯分散液与银盐的混合比例应该保证生长的纳米银颗粒满足上文所述的二维锑烯与银离子的摩尔比为1:0.05~1:0.5。实施例中,该银盐是以银配合物的形式添加,如该配合物应该是能够与银盐形成银配合物的任何配合物,如可以但不仅仅为银氨络合溶液。将银盐以银配合物的形式添加,能够有效控制沉淀形成的纳米银颗粒形貌和尺寸,如控制沉积形成的纳米银颗粒为亚纳米银簇形貌,进步控制亚纳米银簇的粒径为0.5nm~100nm。
79.实施例中,步骤s022中的还原剂包括硼氢化钠、水合肼、醛类、氢气等中的至少一种。该还原剂的添加量应该保证银离子全部被还原生成银单质以沉淀,也即是还原剂应该是相对银离子是过量的,如实施例中,银盐与还原剂的按照质量比为100:1~100:20的比例进行添加混合。
80.进一步地,上述各实施例复合光热材料的制备方法还包括如下步骤,如图4中的步骤s03:
81.将复合光热材料配合成分散液,将分散液与靶向剂进行混合处理,在二维锑烯和/或纳米银颗粒上结合靶向剂。
82.在该步骤s03中,靶向剂与步骤s02中的复合光热材料进行混合处理过程中,靶向剂会吸附并结合在二维锑烯和/或纳米银颗粒上,如可以但不仅仅形成靶向剂包覆层,该包覆层可以是连续的,也可以是非连续的,具体可以根据实际的吸附结合靶向剂的量而定。这样,由于靶向剂的存在,使得制备的复合光热材料在具有光热/光动力协同治疗作用的基础上,还具有精准的靶向性。
83.另外,步骤s03中的靶向剂为上文复合光热材料所含的靶向剂3。因此,该步骤s03中的靶向剂的种类和负载量等均如上文复合光热材料所含的靶向剂3。为了节约篇幅,在此不再对步骤s02中的靶向剂做赘述。如实施例,分散液与靶向剂的混合比例保证在制备的复合光热材料上,二维锑烯与靶向剂的摩尔比为1:0.05~1:0.2。通过对靶向剂在复合光热材料上负载量的控制和优化,提高复合光热材料的靶向性。
84.因此,上述各实施例中复合光热材料制备方法能够有效制备上文复合结构复合光热材料,而且能够通过对制备条件的控制,实现对制备的复合光热材料粒径、负载纳米银颗粒的形貌、粒径和负载量等进行控制,提高制备的复合光热材料的光热/光动力协同治疗作用。或进一步地,对靶向剂的种类和与负载纳米银颗粒的二维锑烯复合光热材料混合比例进行控制,从而控制靶向剂在制备的复合光热材料上的负载量,以赋予并提高复合光热材
料精准的靶向性,实现并提高不同靶向精准给药或光热治疗。
85.第三方面,本技术实施例提供上文复合光热材料的应用。基于上文本技术实施例复合光热材料所含的组分和各组分形成的结构,赋予上文复合光热材料具有光热/光动力协同治疗作用或进一步具有精准的靶向性,从而有效增强了本技术实施例复合光热材料的应用效果和领域。如本技术实施例复合光热材料可以直接作为光热剂,实现对病灶病毒或癌细胞进行杀灭作用,实现光热和光动力治疗作用作用。本技术实施例复合光热材料还可以作为某种活性药物的药物载体,实现活性药物的精准靶向给药,从而实现活性药物与光热和光动力治疗的协同治疗作用和效果。当然基于本技术实施例复合光热材料的结构和特性,其还可以作为光热催化或光热发电材料中的应用。
86.以下通过多个具体实施例来举例说明本技术实施例复合光热材料及其制备方法等。
87.实施例1
88.本实施例提供一种复合光热材料及其制备方法。复合光热材料包括二维锑烯和原位生长在二维锑烯上的亚纳米银簇。
89.复合光热材料的制备方法包括如下步骤:
90.s1.利用超声辅助的液相剥离法制备锑烯纳米片:
91.将锑金属块放入研钵中粉碎,加入仲丁醇并沿同一方向均匀研磨1个小时,使其充分剥离。然后将其移入到超声瓶中,冰水浴中探头超声处理6小时得到含有锑烯和表面活性剂的混合液;随后5000rpm离心10分钟去除块状的金属锑和大尺寸的锑烯,并将滤液在10000rpm离心20分钟得到小尺寸的表面活性剂表面改性的锑烯,将锑烯用去离子水多次洗涤后分散到去离子水中,得到锑烯分散液;
92.s2.在锑烯纳米片上负载亚纳米银簇:
93.将硝酸银水溶液与正丁胺以摩尔比1:2比例充分混合形成银氨络合溶液,将银氨络合溶液按比例加入到锑烯分散液中充分混合,然后加入过量的甲醛溶液后继续搅拌,由于剥离后的锑烯表面有很多活性位点,还原后的银原子会持续不断地沉积到锑烯表面的活性位点处,形成较强的化学键,在二维锑烯上沉积亚纳米银簇。
94.经检测,二维锑烯也即是锑烯纳米片的平均厚度为500nm,平均面积为1500nm2;亚纳米银簇的平均粒径为50nm,二维锑烯与亚纳米银簇的摩尔比平均为1:0.2。
95.实施例2
96.本实施例提供一种复合光热材料及其制备方法。复合光热材料包括二维锑烯和原位生长在二维锑烯上的亚纳米银簇,在二维锑烯和亚纳米银簇上还结合有rgd多肽。
97.复合光热材料的制备方法包括如下步骤:
98.s1.按照实施例1中的步骤s1制备锑烯纳米片;
99.s2.按照实施例1中的步骤s1在锑烯纳米片上负载亚纳米银簇:
100.s3.将合成的纳米复合物离心洗涤后重新分散到去离子水中,加入靶向试剂rgd多肽并不断搅拌过夜,使其充分包裹纳米复合物;最后将产物离心洗涤后得到最终的复合光热材料。
101.经检测,二维锑烯和亚纳米银簇以及两者之间的摩尔含量均如实施例1,二维锑烯与rgd多肽的摩尔比平均为1:0.1。
102.实施例3
103.本实施例提供一种复合光热材料及其制备方法。复合光热材料包括二维锑烯和原位生长在二维锑烯上的亚纳米银簇,在二维锑烯和亚纳米银簇上还结合有vegfr2靶向剂。
104.本实施例复合光热材料的制备方法参照实施例2中的制备方法制备。不同在于,通过控制锑烯纳米片、亚纳米银簇制备条件和负载的靶向剂条件控制,使得制备的复合光热材料所含的
105.二维锑烯也即是锑烯纳米片的平均厚度为900nm,平均面积为2500nm2;亚纳米银簇的平均粒径为1nm,二维锑烯与亚纳米银簇的摩尔比平均为1:0.1。
106.实施例4
107.本实施例提供一种复合光热材料及其制备方法。复合光热材料包括二维锑烯和原位生长在二维锑烯上的亚纳米银簇,在二维锑烯和亚纳米银簇上还结合有t
‑
dm1乳癌靶向药。
108.本实施例复合光热材料的制备方法参照实施例2中的制备方法制备。不同在于,通过控制锑烯纳米片、亚纳米银簇制备条件和负载的靶向剂条件控制,使得制备的复合光热材料所含的
109.二维锑烯也即是锑烯纳米片的平均厚度为1nm,平均面积为100nm2;亚纳米银簇的平均粒径为0.6nm,二维锑烯与亚纳米银簇的摩尔比平均为1:0.5
110.对比例1
111.本对比例提供二维锑烯。与实施例1相比不同在于不含亚纳米银簇,也即是二维锑烯上不负载亚纳米银簇。
112.复合光热材料的相关性质实验
113.将上述各实施例1至实施例4提供的复合光热材料和对比例1提供的光热材料分别按照如下方法进行相关性质实验:
114.1.基于锑烯的光热效应研究:
115.(1)光热性能实验:
116.将实施例1至实施例4和对比例1中的二维锑烯分布配制以二维锑烯质量计的浓度为2μg/ml、5μg/ml、10μg/ml不同浓度的水分散溶液,并以水作为空白试验组(二维锑烯浓度为0μg/ml),分别取不同浓度的水分散溶液2ml加入到32孔板中,然后在808nm近红外激光照射,每隔30秒记录水分散溶液的温度,连续记录30分钟后关闭激光照射,马上记录水分散溶液冷却温度与时间的变化,最后得到不同浓度下的水分散溶液的温度变化随着近红外光照射时间的变化曲线。其中,对比例1中的不同二维锑烯水分散液随着近红外光照射时间的温度变化曲线如图6中a图所示。由6中a图可知,二维锑烯具有优异的光热性能。另外,实施例1至实施例4的不同复合光热材料水分散液随着近红外光照射时间的温度变化曲线基本与图6中a图相同。由此说明,本技术实施例复合光热材料具有良好的光热效应,而且负载的亚纳米银簇和靶向剂几乎不影响二维锑烯的光热性能的发挥。
117.(2)光热稳定性实验:
118.待(1)中光热性能试验完后,再次打开激光进行照射,并重复3到5次,记录水分散液升温和降温曲线。其中,对比例1中的5μg/ml浓度的二维锑烯水分散液随着激光开启和关闭的温度变化曲线如图6中b图所示,由6中b图可知,二维锑烯具有优异的光热灵敏度,且光
热效应稳定性好。实施例1至实施例4的不同水分散液随着激光的开启和关闭的温度变化曲线基本与图6中b图相同。由此说明,本技术实施例复合光热材料具有优异的光热灵敏度,且光热效应稳定性好,同样而且负载的亚纳米银簇和靶向剂几乎不影响二维锑烯的光热性能的发挥。
119.2.复合光热材料光控释放以及解离产生的ros研究:
120.将实施例1至实施例4的复合光热材料和对比例1中的二维锑烯分别配制相同浓度的分散液,并在808nm近红外激光照射,不同照射时间取出定量样品离心,将滤液进行icp检测确定光照解离的银簇的量随光照时间的变化曲线。
121.利用1,3
‑
二苯基异苯并呋喃(dpbf)来研究银簇解离产生的ros的变化。具体方法为:将上述配制的分散液并同dpbf充分混合,于808nm近红外激光照射,每分钟取定量溶液离心后测定滤液的uv
‑
vis吸收光谱,研究光照条件下银簇解离产生的ros量的变化曲线。同时以空白溶液作为空白组。其中,实施例1、对比例1和空白组的ros量的变化曲线如图7所示。由图7可知,实施例1提供的复合光热材料在光照条件下银簇解离产生的ros量随着时间显著增加,而对比例1中的二维锑烯和空白组基本保持不变,也即是在光照条件下几乎没有产生的ros。另外,对其他实施例提供的复合光热材料在光照条件下银簇解离产生的ros量与实施例1趋势相同,具随着时间延长ros量显著增加。
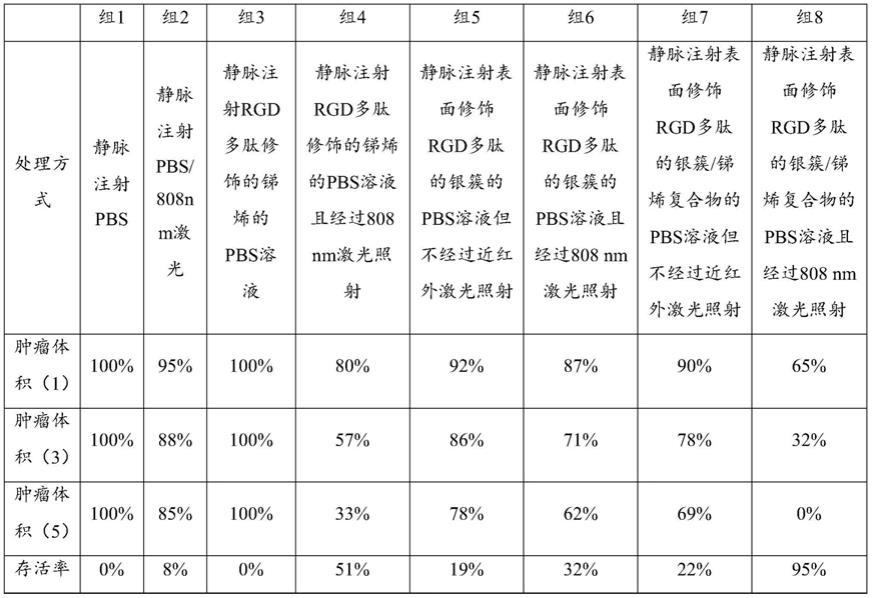
122.3.复合光热材料用于体内肿瘤治疗研究。
123.将成瘤裸鼠随机分为8组,分别经以下方式处理:
124.组1:静脉注射pbs;
125.组2:静脉注射pbs且经过808nm激光照射;
126.组3:静脉注射表面修饰rgd多肽的锑烯(相对实施例2复合光热材料,不含银簇)的pbs溶液但不经过近红外激光照射;
127.组4:静脉注射表面修饰rgd多肽的锑烯(相对实施例2复合光热材料,不含银簇)的pbs溶液且经过808nm激光照射;
128.组5:静脉注射表面修饰rgd多肽的银簇(相对实施例2复合光热材料,不含二维锑烯)的pbs溶液但不经过近红外激光照射;
129.组6:静脉注射表面修饰rgd多肽的银簇(相对实施例2复合光热材料,不含二维锑烯)的pbs溶液且经过808nm激光照射;
130.组7:静脉注射表面修饰rgd多肽的银簇/锑烯复合物(实施例2复合光热材料)的pbs溶液但不经过近红外激光照射;
131.组8:静脉注射表面修饰rgd多肽的银簇/锑烯复合物(实施例2复合光热材料)的pbs溶液且经过808nm激光照射。
132.各组之间给药量、激光源和照射时间均相同,每3天静脉给药一次,总共给药3
‑
5次。肿瘤体积每3天测量一次,小鼠体重每3天称一次,并每天记录小鼠的存活率,直至pbs对照组小鼠全部死亡为止。停止给药一周后,每组选出一只代表性的小鼠,将其处死并摘取肿瘤测量其体积大小来评价肿瘤治疗的情况。实验结果如表1所示:
133.表1
[0134][0135]
由表1可知,组8与组7相比可知,本技术复合光热材料在红外激光照射下,能够有效起到二维锑烯和银簇能够起到光热/光动力协同治疗作用,实现对肿瘤细胞有效杀灭作用。如组8的杀灭效果明显高于组7。
[0136]
组8与组6、组4相比可知,虽然组6中单独银簇和组4中单独锑烯分别在红外激光照射下也呈现一定的杀灭肿瘤细胞的作用,但是组6和组4对肿瘤细胞有效杀灭作用显著的低于组8,因此,有效说明在本技术实施例复合光热材料中锑烯和银簇之间有效起到了协同增效作用,起到了发挥光热/光动力协同治疗作用,显著提高了复合光热材料。其中,复合光热材料所负载的靶向剂能够进一步实现精准靶向给药,释放活性药物成分。
[0137]
以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,均应包含在本发明的保护范围之内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。