增强治疗急性卒中之抗血小板药物之递送方法及其组合物
1.本技术是申请日为2014年7月28日,申请号为201410362859.7,发明名称为“增强治疗急性卒中之抗血小板药物之递送方法及其组合物”的申请的分案申请。
技术领域
2.本发明系提供一种医药组合物之递送方法,特别系一种能增强治疗急性卒中之医药组合物之递送方法。
背景技术:
3.脑血管疾病(cerebrovascular disease)为全世界十大死因之一,同时也造成存活者残障的主要原因,而这些急性或慢性脑血管疾病的患者之医疗照顾也成为社会的一大负担,急性卒中的症状包含有突发性晕眩、恶心、呕吐、平衡失调、走路不稳、突然剧烈头痛、颈部不适或暂时性失去知觉,系为卒中急性期(即卒中初期或一周内)。依研究表明,积极地治疗脑卒中不旦可减少死亡率,并能改善存活者的失能程度,因此,美国国家卒中学会(national stroke association)的暂时性脑缺血综合症治疗准则,建议使用抗血小板药物来预防非心因性暂时性脑缺血综合症之后续发作的二次卒中,主要的药物有阿司匹林 (aspirin)、氯吡格雷(clopidogrel)、双嘧达莫(dipyridamole)、噻氯匹定(ticlopidine)及西洛他唑(cilostazol)等等(《台湾脑中风防治指引2008》.缺血性中风的血小板药物治疗指引)。
4.目前,已核准治疗急性缺血性脑卒中之适应症之药物为重组组织型纤溶酶原激活剂 (recombinant
‑
type plasminogen activator,rt
‑
pa),此为急性发作的三个小时用药,但此药的禁忌繁多,因为rt
‑
pa具有时间的依赖性与会使患者发生高度出血之风险,必须仅慎地筛选病人,因此,在临床实务中,仅约3%急性卒中患者到院时符合使用rt
‑
pa药物之治疗方针而给予rt
‑
pa,但仍无法避免高度出血而造成死亡之风险(《台湾脑中风防治指引2008》.缺血性中风的血小板药物治疗指引)。
5.有关预防卒中复发的抗血小板药物,过去已知单独使用clopidogrel在预防非心因性暂时性脑缺血综合症后发生的卒中上可能较aspirin稍佳;对于非心因性暂时性缺血性卒中病患亦表明联合使用aspirin和长效dipyridamole比单独使用aspirin或单独使用 dipyridamole更为有效。研究表明虽然aspirin加上长效dipyridamole复方比clopidogrel 有较多的出血事件及较高的颅内出血机率,但在整体之风险与效益评估,aspirin加上长效dipyridamole复方与clopidogrel在卒中复发或出血事件上是相似的(《台湾脑中风防治指引2008》.缺血性中风的血小板药物治疗指引)。
6.而预防二次卒中的用药之抗血小板药物dipyridamole在活体外(in vitro)及活体内(invivo)的研究表明,dipyridamole可抑制红血球、血小板及内皮细胞对腺核苷(adenosine) 的再摄取,此种作用使得局部作用于血小板a2受体(platelet a2
‑
receptor)之腺核苷的浓度增加,刺激血小板之腺核环状(platelet adenylate cyclase),导致血小板环腺苷酸(camp) 的浓度增加。dipyridamole亦可抑制血小板中的磷酸二酯酶
(phosphodiesterase),造成血小板中camp与环鸟苷酸(cgmp)浓度增加,进一步抑制血小板活化因子(plateletactivating factor)、胶原(collagen)、二磷酸腺苷(adp)等所引起的血小板凝集作用。此外,腺核苷具有血管扩张的作用,此亦为dipyridamole产生血管扩张作用的机制之一,且已证实静脉注射100mg/kg dipyridamole对于老鼠卒中梗死面积的降低具有良好功效,但同时也发现静脉注射100mg/kg的dipyridamole会引起低血压状态而使老鼠在卒中模式中增加死亡率。虽然dipyridamole在动物模式上具有治疗急性卒中的潜力,但需要极高剂量(80mg/kg
‑
200mg/kg),但由于dipyridamole之血管扩张作用,可能会造成低血压、热潮红与心搏加速之副作用,如此高剂量便会引发dipyridamole之副作用产生,特别是低血压的状态,会造成卒中急性期(即卒中初期或一周内)的死亡率增加(aldandashi,s.,r. noor,et al.(2007).“combination treatment with dipyridamole,aspirin,and tpa in anembolic model of stroke in rats.”exp neurol 205(2):563
‑
568.melani,a.,s.cipriani,et al. (2010).;"effect of intravenous administration of dipyridamole in a rat model of chroniccerebral ischemia."ann n y acad sci 1207:89
‑
96.garcia
‑
bonilla,l.,v.sosti,et al.(2011).;及"effects of acute post
‑
treatment with dipyridamole in a rat model of focal cerebralischemia."brain res 1373:211
‑
220)。
7.zhu等人(2006)揭示用于双嘧达莫之血管周围递送的持续释放系统,以预防具血管通道接驳管植入物的渗析病患中由血管内膜增生引起的再狭窄及阻塞,其系利用聚乳酸共聚羟基乙酸(plga)微球与(一种可注射的共聚物)之组合(见j.biomed.mater. res.part b:appl.biomater.77b:135
‑
143)。chen等人(2013)揭示聚乳酸共聚羟基乙酸
‑ꢀ
聚乙二醇
‑
聚乳酸共聚羟基乙酸(plga
‑
peg
‑
plga)纳米微粒的表面修饰(界面活性剂涂层)对于抗疼痛药物洛哌丁胺(loperamide)穿过血脑障壁之递送功效的影响(见"j. biomater.appl.27(7):909
‑
922)。
8.并未有任何先前公开文献教示或建议使用可降低血浆蛋白结合率之载体,诸如 plga
‑
peg
‑
plga,用于递送抗血小板药物(例如,双嘧达莫)以治疗急性卒中。
技术实现要素:
9.有鉴于此,本发明系提供一种增强治疗急性卒中之抗血小板药物之递送方法,包含把含有一有效剂量之(a)低剂量之抗血小板药物以及(b)一可降低血浆蛋白结合率之载体的组合物递送,使得该低剂量抗血小板药物能于一段有效时间达成治疗急性卒中之功效,其中该组合物之有效剂量系为30
‑
100毫克,该抗血小板药物系为一磷酸二酯酶(phosphodiesterase)抑制剂,且该可降低血浆蛋白结合率之载体系为一高分子载体或一脂质体,且该低剂量之抗血小板药物与该可降低血浆蛋白结合率之载体形成纳米微粒,该高分子载体系由聚乳酸共聚羟基乙酸
‑
聚乙二醇
‑
聚乳酸共聚羟基乙酸(plga
‑
peg
‑
plga) 形成。
10.在本发明之ㄧ实施例中,其中该抗血小板药物系为双嘧达莫(dipyridamole)。
11.在本发明之ㄧ实施例中,其中该组合物进一步包含一血栓溶解剂,且该血栓溶解剂系为重组组织型纤溶酶原激活剂(recombinant
‑
type plasminogen activator,rt
‑
pa)。
12.本发明另提供一种增强治疗急性卒中之医药组合物,包含(a)低剂量之抗血小板
药物以及(b)一可降低血浆蛋白结合率之载体,其中该医药组合物之有效剂量系为30
‑
100毫克,且该可降低血浆蛋白结合率之载体系为一高分子载体或一脂质体,或将药物进行化学修饰,该抗血小板药物系为一磷酸二酯酶抑制剂,且该高分子载体系为聚乳酸共聚羟基乙酸
‑
聚乙二醇
‑
聚乳酸共聚羟基乙酸(plga
‑
peg
‑
plga),该抗血小板药物与该高分子载体之重量比系为1:5至1:15。
13.在本发明又一实施例中,其中该抗血小板药物系为双嘧达莫(dipyridamole)。
14.在本发明再一实施例中,其中该医药组合物进一步包含重组组织型纤溶酶原激活剂 (rt
‑
pa)。
15.本发明系提供有效增强治疗急性卒中之医药组合物,其系以一可降低血浆蛋白结合率之载体及一抗血小板药物形成之抗血小板药物纳米粒子进行传输,进而达到该抗血小板药物控制释放的目的,可避免为减少大脑卒中梗死面积而给予较高剂量抗血小板药物,因而引起低血压之副作用。本发明能大幅减少抗血小板药物的使用剂量,且药物浓度能保持在稳定范围内,让抗血小板药物发挥治疗急性卒中之高度療效。
16.本发明亦关于治疗急性卒中之方法,包含对罹患急性卒中之个体投与本发明之医药组合物。
附图说明
17.图1系为聚乳酸共聚羟基乙酸
‑
聚乙二醇
‑
聚乳酸共聚羟基乙酸 ((poly(lacitide
‑
co
‑
glycolide))
‑
(ethylene glycol)
‑
(poly(lacitide
‑
co
‑
glycolide), plga
‑
peg
‑
plga,pep)高分子进行核磁共振光谱分析结果。
18.图2系为plga
‑
peg
‑
plga高分子进行傅立叶变换红外光谱仪分析结果。
19.图3系为本发明plga
‑
peg
‑
plga高分子与dipyridamile所形成之纳米粒子进行x 雷射粒径分析仪分析数据图。
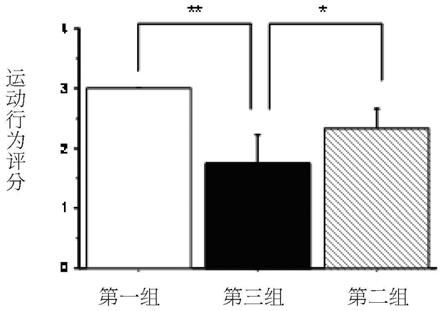
20.图4系为小鼠大脑中动脉梗死模型后以三组药物试验治疗7天后之神经行为测试结果(*p<0.05**p<0.01);第一组系为100μl plga
‑
peg
‑
plga高分子载体控制组 (vehicle control)、第二组系为10mg/kg(2mg/ml)重组组织型纤溶酶原激活剂 (recombinant
‑
type plasminogen activator,rt
‑
pa)及第三组系为10mg/kg(2mg/ml)本发明之 dipyridamile纳米粒子。
21.图5系为小鼠大脑中动脉梗死模型后以三组药物试验治疗15天后之神经行为测试结果(*p<0.05**p<0.01);第一组系为100μl plga
‑
peg
‑
plga高分子载体控制组(vehicle control)、第二组系为10mg/kg(2mg/ml)重组组织型纤溶酶原激活剂 (recombinant
‑
type plasminogen activator,rt
‑
pa)及第三组系为10mg/kg(2mg/ml)本发明之 dipyridamile纳米粒子。
22.图6系为小鼠大脑中动脉梗死模型后以三组药物试验治疗15天后之脑组织尼氏染色法结果;a.为第一组plga
‑
peg
‑
plga高分子载体控制组之脑组织尼氏染色法结果; b.为第二组10mg/kg(2mg/ml)重组的组织血纤维蛋白溶酶原活化剂之脑组织尼氏染色法结果;c.为第三组本发明之dipyridamile纳米粒子之脑组织尼氏染色法结果。
23.图7系为小鼠大脑中动脉梗死模型后以三组药物试验治疗15天后之脑梗死体积百分比:第一组plga
‑
peg
‑
plga高分子载体控制组;第二组10mg/kg(2mg/ml)重组的组织血纤
维蛋白溶酶原活化剂;第三组系为10mg/kg(2mg/ml)本发明之dipyridamile纳米粒子;第四组系为20mg/kg本发明之dipyridamile纳米粒子;第五组10mg/kg本发明之dipyridamile纳米粒子与重组组织型纤溶酶原激活剂(rt
‑
pa)结合之组合物。
24.本发明之特征及优点可由下述详细说明而更清楚了解,然而,应了解该详细说明及特定实施例,虽然指出本发明较佳之实施态样,然其仅提供做为说明之用,因为由此详细说明,熟习此艺者将可轻易了解在本发明之精神及范围中之各种改变及修饰。
具体实施方式
25.本发明提供一种有效增强治疗急性卒中之医药组合物,其系利用抗血小板药物与可降低血浆蛋白结合率之载体所形成之抗血小板药物纳米粒子,藉由控制药物释放而达到增加药效、减少药物毒性及副作用、增加病患对药物的耐受度、及增加便利性之目的。控制药物释放则是利用高分子载体包载或吸收药物,在药物给予人体时不会被人体内之消化液破坏,达到投药部位时可缓慢释放,并且可控制药物释放比例。此外,本发明之可降低血浆蛋白结合率之载体可使用之聚乳酸共聚羟基乙酸
‑
聚乙二醇
‑
聚乳酸共聚羟基乙酸((poly(lacitide
‑
co
‑
glycolide))
‑
(ethylene glycol)
‑
(poly(lacitide
‑
co
‑
glycolide), plga
‑
peg
‑
plga)高分子载体系为生物可降解性及非毒性。
26.根据本发明,有效治疗急性卒中之抗血小板药物量为约30至100毫克,较佳为约 40至80毫克,且更佳为约37.5至46毫克。
27.根据本发明,可降低血浆蛋白结合率之载体系为聚合性载体或脂质体。
28.相较于传统赋型剂,一般生物可降解高分子就来源不同可分为天然高分子与人工合成高分子,天然生物可降解高分子来源取得不易,因此人工合成可降解高分子逐渐被开发。人工合成的生物可降解高分子可分成聚酰胺(poly(amides))、聚氨基酸(poly(aminoacids))、聚氰基丙烯酸烷基酯(poly(alkyl
‑
α
‑
cyano acrylates))、聚酯(poly(esters))、聚原酸酯(poly(orthoesters))、聚氨基甲酸乙酯(poly(urethanes))和聚丙烯酰胺(poly(acrylamides)),其中因为聚酯类高分子(polyesters)具有良好的生物兼容性、生物可降解性和低毒性,常被用来做为组织细胞支架或是药物载体;其中聚乳酸(polylacitide1,pla)、聚乙醇酸 (polyglycolide,pga)及其共聚物(poly(lacitide
‑
co
‑
glycolide),plga)已被美国食品药物管理局(fda)认可,能于体内使用的合成聚合物。pla和pga具有類似化学结构,当pga 主链上的氢原子被甲基取代,即为pla。pla具有兩种立体異构物,分别为l型和d 型,依聚合单体不同,可分为l型
‑
聚乳酸(poly
‑
l
‑
lactic acid,plla)、d型
‑
聚乳酸 (poly
‑
d
‑
lactic acid,pdla)和d,l
‑
聚乳酸(poly
‑
dl
‑
lactic acid,pdlla),前兩者具有高规律性的聚合物链段,为半结晶性(semi
‑
crystalline)的聚合物,后者则因为聚合物链段结构不规则,为无定型(amorphous)的聚合物。生物体内之乳酸为l型,故生物医学应用上,多半为plla与pdlla;而plga则是将pga链段导入pla中,而成为pla 和pga之共聚物。pla、pga及plga于生物体内水解之产物为乳酸(lactide acid)和乙醇酸(glycolide acid),水解产物再经由克氏循环(krebs cycle)代谢成二氧化碳和水分子后排出体外。因此pla、pga及plga之裂解产物最终将被生物体代谢或排泄作用除去,无毒性残留之疑虑。
29.plga虽具有良好的生物可降解性和生物兼容性,但此种材料的疏水性限制其应用于药物载体之发展;而乙二醇单体能聚合成聚乙二醇poly(ethylene glycol,peg)无毒性、
无免疫原性、无抗原性、亲水性佳且生物可兼容性,其为良好且常見的生医材料。因此,本发明plga与peg,使其成为plga
‑
peg
‑
plga高分子复合材料,利用 plga
‑
peg
‑
plga高分子当载体时具有的特性,改善药物释放行为。
30.本发明之药物通过降低血浆蛋白结合率,进而达到降低dipyridamole剂量,由于在急性卒中状态下,血脑障壁会受损而造成通透性改变以及开启,而dipyridamole具高亲脂性与容易过bbb之分子量(504.63),因此在bbb受损时可轻易穿过bbb,其降低药物剂量所使用之主因非通过提高进入bbb比率或缓释所造成之作用,在dipyridamole 小鼠梗死性中风试验中,dipyridamole因中风导致bbb受损,而可进入大脑中,且剂量具治疗意义;而plga
‑
peg
‑
plga高分子载体,为一三嵌段共聚物,利用其aba高分子结构,可降低血浆蛋白结合率。
31.此外,本发明之可降低血浆蛋白结合率之载体可使用脂质体(liposome),其系由磷脂双层所构成,中间包载水溶液的球状粒子。脂质体的膜由磷脂质构成,脂质具有亲脂端与亲水端,利用亲水性的部份,脂质体可与水相互作用自行组装(self
‑
assemble)形成胶体粒子(colloidal particles)。脂质体之横截面,亲水性的头部朝向具有水的空腔,亲脂性尾端则远离,形成双层膜的构造。脂质体独特的构造,可同时做为亲水性与疏水性药物的载体。其具有生物兼容性(biocompatibility)、生物可分解性(biodegradability)且安全无毒,其应用范围从药物和基因传送(gene delivery)到诊断、化妆品和食品工业。
32.根据本发明,可降低血浆蛋白结合率之载体系为聚合性载体,其由选自pla、pga、 plga及peg及其任何组合之聚合性材料所组成,于一较佳实施态样中,该聚合性载体为plga
‑
peg
‑
plga聚合性载体。
33.关于降低血浆蛋白结合率的方法,在高分子载体设计时,可通过不同高分子的聚合,包含aba,bab的tri
‑
block copolymers形式以及plla
‑
peg、plga
‑
peg、pla
‑
peg、 plla
‑
mpeg、plga
‑
mpeg、pla
‑
mpeg等block copolymers形式,并设计出如星状、l型等各种形状如peg
‑
(plga)8、peg
‑
(plla)8与peg
‑
(pdla)8star等blockcopolymers;亦可透过peglated修饰任何载体如高分子与脂质体而达到降低血浆蛋白结合率的效果(park j,fong pm,lu j,russell ks,booth cj,saltzman wm,fahmy tm. pegylated plga nanoparticles for the improved delivery of doxorubicin.nanomedicine. 2009dec;5(4):410
‑
8.doi:10.1016/j.nano.2009.02.002;l
ü
ck m,pistel kf,li yx,blunk t, m
ü
ller rh,kissel t.plasma protein adsorption on biodegradable microspheres consisting ofpoly(d,l
‑
lactide
‑
co
‑
glycolide),poly(l
‑
lactide)or aba triblock copolymers containingpoly(oxyethylene).influence of production method and polymer composition.j controlrelease.1998nov 13;55(2
‑
3):107
‑
20;及sempf k,arrey t,gelperina s,schorge t,meyer b, karas m,kreuter j.adsorption of plasma proteins on uncoated plga nanoparticles.eur j pharm biopharm.2013sep;85(1):53
‑
60)。
34.此外,为达降低血浆蛋白结合率,亦可对dipyridamole进行化学修饰,其修饰方法包括改变其结构如成盐修饰、成酯及成酰胺、具羰基药物、开环、成环修饰以及接合高分子等方式,如pegylation;研究表明,药物透过接合peg可提高其水溶性与稳定度;而peg本身具疏水透特性可降低与血液中血浆蛋白结合比率,而小分子药物与peg连结的方式除直接
连接外,还可透过连结臂方式连接。
35.于本文中使用之抗血小板药物一词,系表示会抑制血小板功能之药剂,例如藉由抑制血小板之凝集、黏连或粒状分泌。抗血小板药物包括磷酸二酯酶(phosphodiesterase) 抑制剂,及其药学上可接受之盐或前体药物。dipyridamole有分成立即释放型(低剂量 25或75毫克)和缓释型(高剂量200毫克),由于低剂量的生物可利用率低,血液中浓度低,无法达到有效抑制血小板效果,所以,其实效果不佳,高剂量缓释型大多数是联合低剂量aspirin使用,主要是使用在脑卒中次级预防上。
36.于本文中使用之抗血小板药物,用于急性梗死卒中治疗时,其药理为大脑神经保护作用,非藉由抗血小板凝集而达成治疗目的。dipyridamole已被证实具有抗发炎、抗氧化与抗mmps效果,且于大脑中具有抑制微胶细胞活化效果;而在急性梗死卒中小鼠研究表明,其治疗卒中药理为抑制mmp
‑
9,mip
‑
1α等神经保护机转。
37.现已一般性地描述本发明,其可透过参照下述实施例而更清楚地了解,该等实施例系提供制备本发明医药组合物及其用于增强急性卒中之例示性方法。该等实施例系仅提供做为说明目的,且不欲在任何方面限制本发明之范围,申请人已尽力确保所使用的数值(例如数量、温度等等)之正确性,但某些实验误差及偏差当然应被容许。
38.实施例1.合成聚乳酸共聚羟基乙酸
‑
聚乙二醇
‑
聚乳酸共聚羟基乙酸((poly(lacitide
‑
co
‑
glycolide))
‑
(ethylene glycol)
‑
(poly(lacitide
‑
co
‑
glycolide), plga
‑
peg
‑
plga,pep)高分子及与双嘧达莫(dipyridamole)之纳米粒子(nanoparticale) 载体
39.1.1合成聚乳酸共聚羟基乙酸
‑
聚乙二醇
‑
聚乳酸共聚羟基乙酸(plga
‑
peg
‑
plga)
40.将乳酸(lactide,la)、乙二醇(glycolide,ga)和聚乙二醇2000(peg2000)之单体,其系购自sigma(steinheim,germany),如下反应式i所示,分别加入至250ml烧瓶密闭并通入氮气后,放入140℃油浴中加热搅拌,当加入之单体完全溶解后加入0.005wt%的辛酸亚锡(stannous octoate),加热搅拌反应8小时后,静置冷却。将反应物加入去离子水,置于5℃下搅拌溶解。当完全溶解形成水溶液后,以水浴加热至70℃至80℃,搅拌该水溶液直到白色沉淀物出现,静置冷却后将上层液倒出,再加入去离子水搅拌溶解,重复此程序2次至3次,去除未反应的乳酸、乙二醇和peg单体。最后将 plga
‑
peg
‑
plga高分子产物取出进行抽取真空干燥。
[0041][0042]
反应式i
[0043]
1.2plga
‑
peg
‑
plga高分子进行核磁共振光谱(nuclear magnetic resonance,nmr) 分析
[0044]
使用500mhz nmr等级以上(400mhz bruker分析仪)之取样管,取约3mgplga
‑
peg
‑
plga高分子并加入7μl含重氢的二甲基亚砜(deuterated dimethylsulfoxide, d
‑
dmso)及四甲基硅烷(tetramethylsilane,tms)之混合溶剂,将样品与溶剂充份混合为均匀相。
[0045]
plga
‑
peg
‑
plga高分子进行核磁共振光谱分析结果,如图1所示,tms为内标, dmso为溶剂,在δ=1.21
‑
1.46ppm的范围为乳酸的
‑
ch3存在,δ=5.0
‑
5.21ppm的范围为乳酸的
‑
ch2存在,δ=3.4
‑
3.5,4.07
‑
4.20ppm的范围为聚乙二醇的
‑
ch2存在,δ= 4.7
‑
4.9ppm的范围为乙二醇的
‑
ch2存在。因此,藉由核磁共振光谱分析可证实 plga
‑
peg
‑
plga高分子之合成。
[0046]
1.3plga
‑
peg
‑
plga高分子进行傅立叶变换红外光谱(fourier transform infrared spectroscopy,ftir)分析
[0047]
将样品加入溴化钾中制成薄片,置入于傅立叶变换红外线光谱仪(horiba ft/ir
‑
720 光谱分析仪(kyoto,japan))中进行分析。
[0048]
其结果如图2所示,在1100cm
‑
1处之波峰为较宽的吸收峰为醚中的c
‑
o键的不对称振动峰;在3000cm
‑
1处之波峰为pla段中ch3的特征吸收峰;在2800cm
‑
1处之波峰为peg段中ch2的特征峰;在1200cm
‑
1处之波峰为co
‑
o
‑
c的特征峰;在3500cm
‑
1 处之波峰为oh
‑
团的特
征峰,证明其含有端羟基;在1700cm
‑
1处为酯中c=o的特征锋;而在935cm
‑
1和650cm
‑
1处无明显吸收峰,其表明乳酸的残留很少。因此,藉由傅立叶变换红外线光谱可证实plga
‑
peg
‑
plga高分子之合成。
[0049]
1.4形成plga
‑
peg
‑
plga高分子与dipyridamole之纳米粒子
[0050]
取40mg之plga
‑
peg
‑
plga高分子与4mg之dipyridamile(sigma(steinheim, germany))溶于10ml之dmso中,并使其均匀混合,再以真空抽气方式去除dmso,并加入1ml的水后进行超音处理(sonication)以形成本发明之dipyridamile纳米粒子;故本发明之最佳实施例中,dipyridamile与plga
‑
peg
‑
plga之比重为1:5至1:15。
[0051]
实施例2.分析plga
‑
peg
‑
plga高分子与dipyridamile所形成之纳米粒子之包载率及粒径分布
[0052]
利用高效液相色谱法(high
‑
performance liquid chromatography,hplc)(荧光侦测器 (shimadzu,japan))分析以0.45μm之滤膜过滤本发明之dipyridamile纳米粒子,以确保dipyridamile保持一定的大小以控制包载药物的粒径;膜过滤前dipyridamile浓度为ctotal;膜过滤后dipyridamile浓度为c,包载率(%)之计算公式为c/ctotal
×
100%。计算出plga
‑
peg
‑
plga高分子与dipyridamile所形成之纳米粒子包载率约为50%, dipyridamile之含量约为2.0mg/ml。
[0053]
x雷射光散仪(zetasizer,型号3000has,厂牌melven,英国),分析本发明之 dipyridamile纳米粒子粒径分布,如图3所示,实验结果表明其粒径为155nm以及多分散性为0.18,代表粒子大多均匀分布。
[0054]
实施例3.缺血脑梗死模型建立
[0055]
为模拟人类脑卒中,本实验采用血管内栓线阻断法建立小鼠大脑中动脉梗死(middlecerebral artery occlusion,mcao)模型。在实验前将小鼠秤体重并且开始纪录直肠体温,接着以4%氟烷(halothane)混入100%o2将小鼠深度麻醉,接着以0.5
‑
1%氟烷混合70% n2o与30%o2维持小鼠麻醉状态。依据tamura氏方法(focal cerebral ischemia in the rat: 1.description of technique and early neuropathological consequences following middlecerebral artery occlusion.j cereb blood flow metab.1981;1(1):53
‑
60.tamura a,graham di, mcculloch j,teasdale gm)建立小鼠脑中动脉梗死模型,将小鼠俯卧以手术刀将头颈部及腹侧颈部割开使右总颈动脉露出,并且将中大脑动脉(middle cerebral artery,mca)灼蚀以达到缺血目的,手术完成后将手术部位的表皮切口稍加缝合,让小鼠从麻醉中苏醒,暂时移到有烤灯照射保温的饲养笼中以完成永久性大脑梗死的模型。
[0056]
实施例4.药物剂量试验
[0057]
于小鼠于卒中后5小时,所有药物之给予采从小鼠大脑中动脉梗死模型之尾巴静脉注射,药物试验组别与药量如下:第一组系为100μl plga
‑
peg
‑
plga高分子载体控制组(vehicle control)、第二组系为10mg/kg(2mg/ml)重组组织型纤溶酶原激活剂 (recombinant
‑
type plasminogen activator,rt
‑
pa)及第三组系为10mg/kg(2mg/ml)本发明之 dipyridamile纳米粒子。
[0058]
实施例5.神经功能行为学评估
[0059]
将上述三组药物试验之小鼠体重与神经学检查同时进行量测与评估,目的是比较
以三组药物治疗之小鼠神经行为之差异。手术后7天及15天分别进行一次检查所使用的神经学评估系统之运动的神经学检查,因卒中后第15天已过了急性卒中时期,本发明比较在急性卒中时期内治疗及急性卒中时期过后治疗小鼠,评估小鼠在运动方面的状态,评估方式如表一(middle cerebral artery occlusion in the rat by intraluminal suture. neurological and pathological evaluation of an improved model.belayev l,alonso of, busto r,zhao w,ginsberg md.stroke.1996sep;27(9):1616
‑
22;discussion 1623),因此分数愈高,代表行动愈不便:
[0060]
表一、运动神经行为检查评估表
[0061]
评分动作状态0无显着行动上缺陷1前肢屈曲2前肢屈曲,且较不能抵抗侧边的推力3前肢屈曲,较不能抵抗侧边的推力,且身躯绕同一侧旋转4前肢屈曲,且较难或无法行走
[0062]
小鼠大脑中动脉梗死模型后以三组药物试验治疗7天之神经行为测试结果,如图4 所示,第一组plga
‑
peg
‑
plga高分子载体控制组之运动神经行为评估为3分;第二组10mg/kg(2mg/ml)重组的组织血纤维蛋白溶酶原活化剂之运动神经行为评估为2.3分;第三组本发明之dipyridamile纳米粒子之运动神经行为评估为1.7分。小鼠大脑中动脉梗死模型后以三组药物试验治疗15天之神经行为学结果,如图5所示,第一组 plga
‑
peg
‑
plga高分子载体控制组之运动神经行为评估为3分;第二组10mg/kg (2mg/ml)重组组织型纤溶酶原激活剂之运动神经行为学评估为2.6分;第三组本发明之dipyridamile纳米粒子之运动神经行为学评估为1.5分。其结果表明出使用本发明之 dipyridamile纳米粒子治疗之大脑中动脉梗死模型之小鼠神经功能行为学评分明显较佳,同时,急性卒中时期过后治疗小鼠比在急性卒中时期内治疗之小鼠神经功能行为能力佳。
[0063]
实施例6.神经元灰质的局灶缺血伤害之评估
[0064]
在大脑中动脉梗死模式后以三组药物试验治疗第15天将小鼠牺牲,取得小鼠脑部检体,采用尼氏染色法(nissl stain)以甲酚紫(cresyl violet)为染料对小鼠大脑神经元灰质的局灶缺血伤害进行评估。尼氏染色法步骤流程如下:先将干燥的玻片浸入装有0.5%甲酚紫避光的玻璃染色缸中约4至6小时,再以干净的去离子水将玻片冲洗浸泡2分钟,接着进入脱水步骤,将玻片依序浸入75%、85%、与95%的酒精中各约2分钟,接连着浸入三缸100%无水酒精各30秒以脱水完全,再连续浸入三缸的二甲苯(xylene)中,各约2分钟,最后以油性胶(entellan)将盖玻片(24
×
50mm)覆上,完成封片,并于室温下风干保存。
[0065]
如图6所示,a.为第一组plga
‑
peg
‑
plga高分子载体控制组之脑组织尼氏染色法结果;b.为第二组10mg/kg(2mg/ml)重组的组织血纤维蛋白溶酶原活化剂之脑组织尼氏染色法结果;c.为第三组本发明之dipyridamile纳米粒子之脑组织尼氏染色法结果。将预先决定之冠状高度(2mm)切片上所计算而得的梗死区域接着汇编成每个脑的梗死体积(infarction),单位为立方毫米,计算方式如下:
[0066]
(1)脑部梗死的体积是用间接方法计算得来,因脑部梗死后的病情恶化,常常都是因为脑组织中由于液体过多囤积而形成脑水肿,所以将计算出的整个对侧左脑半球正常未
受损范围减去整个同(患)侧右脑半球未受损区域,再以对侧左脑半球的百分比来表示,这是为了要补偿同侧右脑水肿所造成的误差。公式如下:
[0067]
右脑梗死体积百分比=[左脑正常体积-右脑未受损体积]
÷
左脑正常体积
×
100%
[0068]
(2)在同侧(右)半球所引起的脑水肿,其计算方式是将每一个脑切片的右脑半球体积增加的总和,再除以对侧半球的脑部体积,这样就可以得知同侧半球脑水肿体积占对侧半球脑部体积的百分比。计算公式如下:
[0069]
右脑水肿体积百分比={σ[右脑切片-左脑切片]
×
体积}
÷
左脑半球体积
×
100%
[0070]
梗死体积的计算结果,如图7所示,第一组plga
‑
peg
‑
plga高分子载体控制组之脑梗死体积约为14%;第二组10mg/kg(2mg/ml)重组的组织血纤维蛋白溶酶原活化剂之脑梗死体积约为18%;第三组系为10mg/kg(2mg/ml)本发明之dipyridamile纳米粒子之脑梗死体积约为7%;此外,
[0071]
此外,本实施例另进行第四组及第五组实验,第四组系为小鼠于卒中后5小时注射 20mg/kg本发明之dipyridamile纳米粒子,而第五组系为为小鼠卒中后5小时注射 10mg/kg本发明之dipyridamile纳米粒子以及10mg/kg之重组组织型纤溶酶原激活剂 (rt
‑
pa)结合之组合物。结果表明,第四组系小鼠之脑梗死体积约为5%,以及第五组小鼠之脑梗死体积约为6%。
[0072]
小鼠大脑中动脉梗死模式后以五组药物试验治疗第15天将老鼠牺牲,在卒中后第 15天已过了急性卒中时期,并由于威利斯环(the circle of wills)所造成因血管伤害所导致的神经行为之代偿作用,尼氏染色法之结果表明缺血不明显且无脑水肿。但若根据梗死体积百分比公式可发现,永久性卒中小鼠模式第15天后,给予第一组 plga
‑
peg
‑
plga高分子载体控制组与第二组10mg/kg(2mg/ml)rt
‑
pa的小鼠之大脑有萎缩的现象,同时,于过去研究表明,rt
‑
pa在永久性梗死且施打时间超过卒中发生3 小时后,对于大脑有害而增加梗死面积(pfefferkorn t,rosenberg ga.closure of theblood
‑
brain barrier by matrix metalloproteinase inhibition reduces rtpa
‑
mediated mortality incerebral ischemia with delayed reperfusion.stroke.2003aug;34(8):2025
‑
30.;wang ymf, tsirka se,strickland s,stieg pe,soriano sg,lipton sa(1998)tissue plasminogenactivator(tpa)increases neuronal damage after focal cerebral ischemia in wild
‑
type andtpa
‑
deficient mice.nat med 4:228
–
231;tsirka se,gualandris a,amaral dg,strickland s (1995)excitotoxin
‑
induced neuronal degeneration and seizure are mediated by tissueplasminogen activator.nature 377:340
–
344)。
[0073]
本实验数据跟文献所描述相符;而给予第三组本发明之dipyridamile纳米粒子的小鼠脑组织尼氏染色法结果则可有效预防萎缩(相较于第一组与第二组,p<0.01),似乎五组药物试验皆无脑水肿,但第三组的本发明可预防脑萎缩。
[0074]
目前,若以临床应用之口服预防卒中的剂量而言,患者每日需口服高剂量200毫克的dipyridamile两次,若换算静脉注射之等效剂量约2分之1到3分之1则为每日66.6mg 至100mg两次。根据本发明,小鼠所需剂量仅为10mg/kg,而一般估计成人所需剂量约为小鼠的
13分之1到16分之1,其所需剂量为0.625mg/kg至0.769mg/kg,若以成人60公斤而言则为37.5mg至46mg之间;与临床核子医学心脏血流灌注造影所用剂量 0.56mg/kg相当,且低于目前预防卒中每日所需剂量的4分之1,因此,证实本发明在临床上具可用性。
[0075]
本发明系提供有效增强治疗急性卒中之医药组合物及其递送方法,其系以一可降低血浆蛋白结合率之载体及一抗血小板药物所形成之抗血小板药物纳米粒子进行传输,进而达到该抗血小板药物控制释放的目的。将抗血小板药物和可降低血浆蛋白结合率之载体结合使药物可以增加药物与细胞的兼容性,利用降低其高血浆蛋白结合率以达到增加有效药物浓度于大脑中的剂量,进而能大幅减少治疗的使用剂量,且药物浓度能保持在稳定范围内,让抗血小板药物有效进入患部,达到抗发炎、抗氧化与抗脑水肿的神经保护效果,并能减少给予大剂量抗血小板药物时所造成的血压降低等副作用产生。
[0076]
如上述说明性实施例所载之发明的各种修饰及变异对熟习此艺者系可预期发生,因此,只有所附申请专利范围中的限制条件应被加诸在所请发明上。
[0077]
符号说明
[0078]
无。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。