rubicon run结构域的苏氨酸166和丝氨酸189作为lrrk2激酶抑制靶点
相关申请的交叉引用
1.本技术要求于2019年3月7日提交的新加坡专利申请号10201902046s 的优先权,其内容通过引用并入本文。
技术领域
3.本发明一般涉及用于诊断和/或提供治疗与富含亮氨酸重复激酶2(lrrk2)相关的疾病,特别是诊断和/或提供治疗帕金森病(pd)的方法、抗体、抑制剂和试剂盒。
背景技术:
5.以下对本发明背景的讨论旨在促进对本发明的理解。应当理解,该讨论不是确认或承认在本发明的优先权日期所提及的任何材料,已在任何司法管辖区出版、已知或属于本领域技术人员的公知常识的一部分。
6.富含亮氨酸重复激酶2(lrrk2)是一种丝氨酸/苏氨酸激酶。lrrk2突变与帕金森病(pd)、慢性炎症,如克罗恩病和分枝杆菌感染有关。lrrk2突变是常染色体显性和散发性pd的最常见原因,在某些人群中占pd病例的40%。 g2019s是最普遍的lrrk2突变体,据报道与野生型lrrk2相比,其激酶活性增强。亚洲lrrk2变体如n551k、r1398h、r1628p和g2385r已被报道,但突变的功能影响尚不清楚,因为这些变体尚未被完全描述。家族性 lrrk2相关pd与特发性pd有很大的重叠,这表明阐明lrrk2功能可能会提供对家族性和特发性pd的见解。尽管lrrk2相关毒性与其激酶功能有关,但由于缺乏真正的lrrk2底物,其生理功能仍然未知。因此,对lrrk2 底物的探索和lrrk2激酶抑制剂的开发引起了人们的兴趣,因为它们可能引导对lrrk2相关疾病(如pd)的治疗干预。
7.pd是一种中枢神经系统的长期退行性疾病,主要影响运动系统。pd是一种全球性疾病,无法治愈,治疗主要针对改善症状。迄今为止,还没有诊断分析来帮助pd的临床诊断。当前的pd临床诊断依赖于运动症状和脑部扫描。
8.作为beclin
‑
1相互作用和富含半胱氨酸的run结构域蛋白(rubicon)是一种已知参与自噬、吞噬作用和免疫反应的蛋白质。
9.在诊断和/或提供帕金森病治疗方面,至少需要减轻一些困难。
技术实现要素:
11.可以预见,描述的方法、抗体、抑制剂和试剂盒将用于诊断和/或提供治疗与富含亮氨酸重复激酶2(lrrk2)相关的疾病,特别是诊断和/或提供治疗帕金森病(pd)。
12.相应地,本发明的一个方面提供了一种检测rubicon蛋白磷酸化的体外方法,包括:从样品中分离蛋白质;将分离的蛋白质与抗体接触,该抗体与rubicon 蛋白的166位处的磷酸化苏氨酸杂交以形成复合物;检测所述复合物,其中检测到与预定值不同的复合物表明样品来自患有与富含亮氨酸重复激酶2(lrrk2) 相关的疾病的受试者。
13.本发明的另一方面提供了一种能够结合在苏氨酸166位磷酸化的rubicon 的抗体。
14.本发明另一方面提供了一种如上文所描述的抗体,用于诊断或治疗与富含亮氨酸重复激酶2(lrrk2)相关的疾病。
15.本发明的另一方面提供了一种rubicon与富含亮氨酸重复激酶2(lrrk2)相互作用的抑制剂,其包含一种能够阻断lrrk2与rubicon蛋白的苏氨酸166相互作用的化合物。
16.本发明的另一方面提供了一种如上文所描述的抑制剂,用于治疗与富含亮氨酸重复激酶2(lrrk2)相关的疾病。
17.本发明另一方面提供了一种如上文所描述的抗体或如上文所描述的抑制剂,在制备用于治疗与富含亮氨酸重复激酶2(lrrk2)相关的疾病的药物中的用途。
18.本发明的另一方面提供了治疗有患有与富含亮氨酸重复激酶2(lrrk2)相关的疾病的需要的受试者的方法,包括:施用能够阻断lrrk2与rubicon蛋白的苏氨酸166和/或丝氨酸189相互作用的化合物。
19.本发明的另一方面提供了一种试剂盒,其包含上文所描述的抗体或上文所描述的抑制剂,以及用于检测与富含亮氨酸重复激酶2(lrrk2)相关的疾病的检测试剂。
20.结合附图阅读以下对本发明具体实施例的描述后,本发明的其他方面和特征对本领域普通技术人员将变得显而易见。
21.附图简要说明
22.在仅通过非限制性示例的方式说明的附图中,本发明的实施例可包括,
23.图1.lrrk2和rubicon相互作用。(a)lrrk2和rubicon在尸检 (post
‑
mortem)的人pd大脑中的共定位。对尸检的人黑质脑组织进行内源性 lrrk2和rubicon表达染色。imaris软件分析共聚焦图像以生成2d直方图和共定位统计数据(表1)。(b)lrrk2和rubicon的免疫共沉淀。用过度表达人lrrk2
‑
gfp和/或rubicon
‑
flag的hek裂解物进行免疫共沉淀。
24.图2.lrrk2特异性rubicon磷酸化位点(phosphosite)的鉴定。野生型或突变型lrrk2激酶测定以野生型或无磷突变体rubicon作为底物进行。所得磷酸化rubicon信号以条形图的形式制成表格,并使用针对野生型rubicon 的学生t检验(student’s t
‑
test)计算统计显着性。*p<0.05,**p<0.01,***p<0.001。
25.图3.lrrk2特异性rubicon磷酸化位点的验证。(a)使用野生型或无磷突变体rubicon作为底物进行lrrk2 adp激酶测定,测量激酶反应生成的adp。使用针对野生型rubicon的学生t检验计算统计显着性;*p<0.05。(b)使用elisa分析内源性lrrk2敲低或过表达lrrk2的人神经元细胞的内源性 pt166 rubicon表达。使用学生t检验针对对照计算统计显着性,且*p<0.05, **p<0.01。
26.图4.果蝇攀爬试验和寿命研究。评估过表达人类lrrk2
±
rubicon的果蝇的攀爬能力和寿命。每10天进行一次攀爬试验,直到第60天,并将得到的攀爬指数制成表格。寿命研究每7天记录一次,直到所有苍蝇都死亡。每条果蝇线的最后一天都标在条形图上方。使用多重比较与tukey
‑
kramer事后检验进行统计分析。*p<0.05,***p<0.001(表2和3)。
27.图5.果蝇酪氨酸羟化酶(th)表达。年老的转基因果苍蝇大脑在五个区域 (ppl1、ppl2、ppm1/2、ppm3、pal)中被染色为th阳性神经元簇并计数。结果计数制成表格,并在调整多重比较后使用学生t检验分析统计显着性(表 4)。
28.图6.果蝇酪氨酸羟化酶(th)表达。通过th elisa分析年老的苍蝇脑裂解物,并使用学生t检验进行统计显着性,其中*p<0.05和**p<0.01。
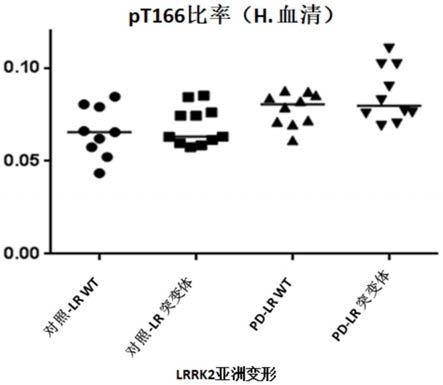
29.图7.使用人血清样品验证pt166 rubicon夹心elisa(sandwich elisa)。通过pt166 rubicon夹心elisa分析携带lrrk2变异突变的本地pd队列的人血清。每个类别中的10个样本表示为带有各自中位数的点图。使用 mann
‑
whitney检验和显著性数字分析统计显着性,其中p<0.05以粗体表示(表 5)。
30.图8.lrrk2和rubicon在小胶质细胞和巨噬细胞中的内源性表达。 (a)lrrk2和rubicon在人神经元细胞和小胶质细胞中的内源蛋白表达。 (b)rubicon在小鼠巨噬细胞中过表达,细胞裂解物通过pt166 rubicon夹心 elisa进行分析。使用多个t检验分析统计显着性,使用holm
‑
sidak方法对多重比较进行校正。当p<0.05时达到统计显着性(表6)。
31.图9.使用人脑样品验证pt166 rubicon夹心elisa。一组年老匹配的非pd 脑(左)和pd脑(右)在人尸检黑质脑切片中的共定位lrrk2和rubicon染色。通过pt166 rubicon夹心elisa 分析尸检人脑样本。人脑组织被均质化并分离成可溶性蛋白和膜相关蛋白。每个类别有四个样品,它们各自的平均值用条形图表示。使用单向方差(one
‑
way anova)分析统计显着性,当p<0.05 时达到统计显着性(表7)。
具体实施方式
33.在本文件中,除非另有相反说明,否则术语“包括”、“包括”、“具有”等应解释为非详尽无遗,或换句话说,其含义为“包括但不限于。
34.进一步,在整个文件中,除非上下文另有要求,否则“包括”一词或“包括”或“包括”等变体将被理解为包含规定的整数或整数组,但不排除任何其他整数或整数组。
35.除非另有定义,否则本文中使用的所有其他技术和科学术语的含义与本文主题所属技术人员通常理解的含义相同。
36.观察到lrrk2激酶与rubicon run结构域相互作用。lrrk2是一种丝氨酸/苏氨酸激酶,rubicon run结构域包含12个丝氨酸残基和3个苏氨酸残基。克隆了单个丝氨酸/苏氨酸残基被丙氨酸取代的rubicon无磷突变体,以描绘对lrrk2功能至关重要的run结构域残基。利用野生型或突变型 lrrk2进行lrrk2激酶分析,系统地筛选lrrk2特异性磷酸化位点。鉴定出的共有rubicon磷酸化位点为苏氨酸166(t166)和丝氨酸189(s189)。如果 rubicon通过lrrk2激酶活性介导lrrk2诱导的毒性,则rubicon无磷突变体 t166a和/或s189a将拯救lrrk2诱导的毒性。
37.识别lrrk2底物是阐明lrrk2生理功能的关键。在这里,报道了一种新的lrrk2底物rubicon,并鉴定了lrrk2特异性磷位点。
38.相应地,在各种实施例中,一种检测rubicon蛋白磷酸化的体外方法,包括:从样品中分离蛋白质;使分离的蛋白质与抗体接触,该抗体与rubicon蛋白质的166位磷酸化苏氨酸杂交以形成复合物;检测复合物,其中检测到与预定值不同的复合物表明样品来自与富含亮氨酸的重复激酶2(lrrk2)有关的受试者。
39.可以量化并易于使用最少的患者样本进行的诊断测定的可行性将增强pd 临床诊断的确定性。在各种实施例中,在临床环境中使用灵敏的elisa检测很容易实现。在各种实施例中,血液样本(如血清样本或单核细胞组分样本)的使用进一步增强了临床环境中实施
的便利性。
40.如本文所用,术语“样品”是指从受试者(如动物或患者)处获得的样品。在各种实施例中,所述样品从患者处获得,并且可以是例如血液、体液或组织样品。在各种实施例中,所述样品为血液或血液衍生样品。即,所述样品可以是从患者处获得的全血,或者可以是从自患者处获得的一定量的血液。在一些实施例中,来自血液的样品可以是来自受试者血液的一定量的血浆或血清。在一些实施例中,来自血液的样品可以是来自受试者血液的单核细胞部分或患者来源的巨噬细胞系。
41.在各种实施例中,所述样品可能是肺液。在各种实施例中,所述样品可以是组织,例如肺组织、胃肠组织或脑组织。在各种实施例中,所述样品可以是脑组织。
42.在各种实施例中,一份样品从疑似患有与富含亮氨酸重复激酶2(lrrk2)相关的疾病的患者处获得。在各种实施例中,与富含亮氨酸重复激酶2(lrrk2)相关的疾病包括但不限于帕金森病(pd)、慢性炎症,如克罗恩病和分枝杆菌感染,如肺结核。
43.在各种实施例中,所述方法包括从受试者处获得样品的步骤。在各种实施例中,所述样品可以被获得并随后被储存,例如在
‑
80℃。可以根据本发明的方法解冻和分析所述储存的样品。
44.在各种实施例中,一份样品获得自与富含亮氨酸重复激酶2(lrrk2)相关疾病的拟定或同期治疗过程相关的预定时间点的患者处。在各种实施例中,在与富含亮氨酸重复激酶2(lrrk2)相关疾病的拟定或同期治疗过程相关的多个时间点从患者处获取样品。
45.在各种实施例中,患有与富含亮氨酸重复激酶2(lrrk2)相关的疾病的受试者用能够阻断lrrk2与rubicon蛋白的苏氨酸166和/或丝氨酸189相互作用的化合物进行治疗。阻断相互作用可防止rubicon蛋白的苏氨酸166和/或丝氨酸 189磷酸化,从而减缓运动技能的退化和/或延长寿命。在各种实施例中,患有与富含亮氨酸重复激酶2(lrrk2)相关的疾病的受试者用能够阻断lrrk2 与rubicon蛋白的磷酸化的苏氨酸166相互作用的化合物进行治疗。阻断 rubicon蛋白的苏氨酸166和/或丝氨酸189磷酸化后的相互作用也将具有减缓运动技能退化和/或延长寿命的作用。在各种实施例中,所述化合物包含一种治疗抗体。在各种实施例中,所述治疗抗体是一种单克隆抗体。在各种实施例中,所述治疗抗体是一种嵌合人源化抗体。在各种实施例中,患有与富含亮氨酸重复激酶2(lrrk2)相关的疾病的受试者用能够阻断lrrk2与rubicon蛋白的磷酸化苏氨酸166相互作用的化合物进行治疗。
46.在各种实施例中,样品是或已经在治疗所述疾病的治疗干预前1天、2天、 3天、4天、5天、6天、7天、8天、9天、10天、11天、12天、13天、2周、 3周、4周、2个月、3个月、4个月、5个月、6个月或1年内,从患者处获得。
47.在各种实施例中,所述样品是或已经在治疗所述疾病的治疗干预过程中从患者处获得。在各种实施例中,所述样品是或已经在开始治疗所述疾病的治疗干预后从患者处获得。
48.在各种实施例中,样品是或已经在治疗所述疾病的治疗干预后(例如在开始后,即第一次给药,治疗干预)的1天、2天、3天、4天、5天、6天、7天、 8天、9天、10天、11天、12天、13天、2周、3周、4周、2个月、3个月、4 个月、5个月、6个月或1年内,从患者处获得。在各种实施例中,所述样品是或已经在治疗所述疾病的治疗干预后(例如在治疗干预开始后,即首次给药后) 不超过1年、6个月、5个月、4个月、3个月、2个月、4周、3周、2周、13 天、12天、11天、10
天、9天、8天、7天、6天、5天、4天、3天、2天或1 天内,从患者处获得。
49.在各种实施例中,所述样品是或已经在完成治疗所述疾病的治疗性干预过程时或之后从患者处获得。在各种实施例中,所述样品是或完成治疗所述疾病的治疗干预过程后,最多1天、2天、3天、4天、5天、6天、7天、8天、9天、 10天、11天、12天、13天、2周、3周、4周、2个月、3个月、4个月、5个月、6个月或1年,从患者处获得。在各种实施例中,所述样品是或完成治疗所述疾病的治疗干预过程后,不超过1年、6个月、5个月、4个月、3个月、 2个月、4周、3周、2周、13天、12天、11天、10天、9天、8天、7天、 6天、5天、4天、3天、2天或1天,从患者处获得。在各种实施例中,所述样品是从患者尸体解剖获得。
50.如本文所用,术语“rubicon蛋白”是指作为beclin
‑
1相互作用且富含半胱氨酸的run结构域蛋白。在各种实施例中,rubicon蛋白具有seq id no.1 中所述的氨基酸序列或其功能变体,其保留rubicon的一个或多个已知功能,例如与beclin
‑
1相互作用、与vps34相互作用、与uvrag相互作用,与rab7相互作用或抑制自噬并参与吞噬和免疫反应。一个功能性变体可具有对seq idno.1的一个或多个取代、删除或附加氨基酸,以保留rubicon的一个或多个已知功能。在各种实施例中,一个功能变体包含与seq id no.1具有60%或70%或80%或90%或95%或96%或97%或98%或99%序列同源性的序列。如本文所用,166位的苏氨酸指序列seq id no.1的第166个氨基酸中的苏氨酸或功能变体的第166个氨基酸附近某处的苏氨酸。189位丝氨酸是指序列seq id no.1 第189位氨基酸中的丝氨酸或功能变体第189位氨基酸附近的丝氨酸。
51.如本文所用,术语“与富含亮氨酸重复激酶2(lrrk2)相关的疾病”是指已将seq id no.3的lrrk2鉴定为风险因素的任何疾病。在多个实施例中,与lrrk2相关的疾病选自帕金森病;如克罗恩病或溃疡性结肠炎的慢性炎症,;以及如分枝杆菌感染的细菌感染。在各种实施例中,与lrrk2相关的疾病是帕金森病。在各种实施例中,与lrrk2相关的疾病可包含完整的lrrk2,表示为seq id no.3中所述的氨基酸序列。在各种其他实施例中,与lrrk2相关的疾病可包括序列seq id no.3的lrrk2蛋白质的添加、删除或替换的突变。
52.在各种实施例中,所述抗体为一种单克隆抗体。在各种实施例中,所述抗体为一种嵌合人源化抗体。
53.在各种实施例中,可以通过本领域熟知的各种方法检测和/或测量抗体
ꢀ‑
rubicon复合物,例如通过蛋白质印迹、免疫组织化学、免疫细胞化学、流式细胞术、elisa、elispot、基于报告的方法(reporter
‑
based methods)等。在各种实施例中,用酶联免疫吸附测定(elisa)检测抗体
‑
rubicon复合物。在各种实施例中,elisa检测可以通过允许计算绝对量的直接elisa进行。在各种实施例中,elisa检测可以通过间接elisa。在各种实施例中,elisa检测可以通过夹心elisa,其可以提供更具体的定量。在各种实施例中,elisa检测可以通过允许检测抗体
‑
rubicon复合物的任何方法进行。
54.在各种实施例中,预定值是没有与富含亮氨酸重复激酶2(lrrk2)相关的疾病的健康个体的正常范围的阈值,其中与预定值的变化表明存在疾病。在各种实施例中,预定值是seq id no.1中的苏氨酸166处磷酸化的rubicon蛋白相对于样品中rubicon蛋白总量的百分比或比率。在各种实施例中,检测高于预定值的复合物表明样品来自具有与富含亮氨酸重复激酶2(lrrk2)相关疾病的受试者。在各种其他实施例中,检测低于预定值的复合物表明样品来自患有与富含亮氨酸重复激酶2(lrrk2)相关的疾病的受试者。
55.在各种实施例中,所述体外方法还包括在将分离的蛋白质与抗体接触之前去除封闭蛋白质。在各种实施例中,所述封闭蛋白可包含白蛋白。在各种实施例中,所述封闭蛋白可通过过滤、离心、标记沉淀或本领域已知的去除特定蛋白质的任何方法去除。有利的是,该方法具有足够的灵敏度和特异性,可检测所有血液样本中苏氨酸166磷酸化的rubicon蛋白。通常,然而,从血清样本中去除白蛋白可在使用血清样本时增强检测。
56.在各种实施例中,提供了一种能够结合在苏氨酸166磷酸化的rubicon的抗体。
57.在各种实施例中,所述抗体包含至少一个可变区,所述可变区并入选自氨基酸序列i)至vi)的cdr:i)lc
‑
cdr1:rssqslvhsngntylh(seqid no.4);ii)lc
‑
cdr2:klsnrfs(seq id no.5);iii)lc
‑
cdr3:sqsthvplt(seq id no.6);iv)hc
‑
cdr1:nygvs(seq id no.7);v)hc
‑
cdr2:tinsnggskyypdsvkg(seq id no.8);vi)hc
‑
cdr3:dvwlrrqwyfdv(seq id no.9);以及一个与氨基酸序列i)至vi)中的任一个具有99%氨基酸序列同一性的功能性变体。
58.在各种实施例中,所述抗体包含氨基酸序列:i)lc
‑
cdr1:rssqslvhsngntylh(seq id no.4);ii)lc
‑
cdr2:klsnrfs(seq id no.5);iii)lc
‑
cdr3:sqsthvplt(seq id no.6);iv)hc
‑
cdr1:nygvs(seq id no.7);v)hc
‑
cdr2:tinsnggskyypdsvkg(seq id no.8);vi)hc
‑
cdr3:dvwlrrqwyfdv(seq id no.9);或一个与氨基酸序列i)至vi) 中的任一个具有99%氨基酸序列同一性的功能性变体。
59.在各种实施例中,所述抗体包含seq id no.12和seq id no.13中规定的氨基酸序列或与seq id no.12和seq id no.13具有99%氨基酸序列同一性的功能性变体。
60.在各种实施例中,所述功能性变体包括能够以至少1:30的上清液稀释度与在苏氨酸166磷酸化的rubicon结合的抗体。在各种实施例中,所述功能性变体包括能够以至少1:90的上清液稀释度与在苏氨酸166磷酸化的rubicon结合的抗体。在各种实施例中,所述功能性变体包含能够以至少1:270的上清液稀释度结合在苏氨酸166磷酸化的rubicon的抗体。在各种实施例中,所述功能性变体包含能够以至少1:810的上清液稀释度结合在苏氨酸166磷酸化的rubicon的抗体。在各种实施例中,所述功能性变体包含能够以至少1:2430的上清液稀释度结合在苏氨酸166磷酸化的rubicon的抗体。在各种实施例中,所述功能性变体包含能够以1:8和1:2500之间的上清液稀释度结合在苏氨酸166磷酸化的 rubicon的抗体。在各种实施例中,所述功能性变体包含能够以1:10和1:2500 之间的上清液稀释度结合在苏氨酸166磷酸化的rubicon的抗体。在各种实施例中,所述功能性变体包含能够以1:20和1:2500之间的上清液稀释度结合在苏氨酸166磷酸化的rubicon的抗体。在各种实施例中,所述功能性变体包含能够以 1:80和1:2500之间的上清液稀释度结合在苏氨酸166磷酸化的rubicon的抗体。在各种实施例中,所述功能性变体包含能够以1:250和1:2500之间的上清液稀释度结合在苏氨酸166磷酸化的rubicon的抗体。在各种实施例中,所述功能性变
体包含能够以1:800和1:2500之间的上清液稀释度结合在苏氨酸166磷酸化的rubicon的抗体。
61.多克隆抗体
62.在各种实施例中,所述抗体可包括多克隆抗体。制备多克隆抗体的方法是本领域技术人员已知的。可以在哺乳动物中产生多克隆抗体,例如,通过注射一次或多次免疫制剂和(如果需要)佐剂。
63.通常,将通过多次皮下或腹膜内注射将免疫剂制剂和/或佐剂注射到哺乳动物中。反应的强度由几个因素决定,包括免疫原分子的大小、化学特性以及它与动物自身蛋白质的不同程度。大多数天然免疫原是分子量高于5kda的蛋白质,其来源在系统发育上与宿主动物相距甚远(即将人类蛋白质注射到兔子或山羊中)。使用高度纯化的蛋白质作为免疫原是可取的,因为动物会产生针对甚至少量存在的杂质以及主要成分的抗体。抗体反应随着免疫原的反复接触而增加,因此需要定期进行一系列注射以实现高水平的抗体产生和高亲和力的抗体。
64.在各种实施例中,所述抗体与苏氨酸166处磷酸化的rubicon蛋白(rubiconprotein phosphorylated at threonine 166)连结、杂交或结合。在各种实施例中,所述抗体与rubicon蛋白的苏氨酸166处连结、杂交或结合。在各种实施例中,所述抗体与rubicon蛋白磷酸化的苏氨酸166处(rubicon protein atphosphorylated threonine 166)连结、杂交或结合。在各种实施例中,将从rubicon 蛋白中约117至189的区域中选择氨基酸序列。来自seq id no.1区域中的至少5、6、7、8、9、10、15、20、25、30个氨基酸序列通常将用于产生这些抗体。在各种实施例中,所述氨基酸序列为seq id no.2。理想地,所选序列将产生特异性干扰rubicon和lrrk2结合的抗体。
65.然而,并非所有免疫原性分子都能产生所需的抗体水平。为了增加免疫反应的强度,免疫原与称为佐剂的复杂混合物结合。佐剂是天然或合成化合物的混合物,当与抗原一起服用时,可增强免疫反应。佐剂用于(1)刺激对非固有免疫原性抗原的免疫反应,(2)增加免疫反应的强度,(3)优先刺激细胞或体液反应(即防止疾病与抗体产生相比(protection from disease versus antibodyproduction))。可使用的佐剂的实例包括弗氏完全佐剂(freund's completeadjuvant)和mpl
‑
tdm佐剂(单磷酰脂质a,合成海藻酸盐 (trehalosedicorynomycolate))。
66.如果免疫原仍然无法产生可接受的反应,则可能与更具免疫原性的载体蛋白结合。小分子,如药物、有机化合物、分子量小于2
‑
5kda的肽和低聚糖,例如 seq id no.2,即使在有佐剂的情况下给药,通常也不具有免疫原性。为了产生对这些化合物的免疫反应,有必要将它们连接到蛋白质或其他化合物上,称为具有免疫原性的载体。当连接到载体蛋白时,小分子免疫原被称为半抗原。半抗原也与载体蛋白结合,用于免疫分析。载体蛋白提供将半抗原连接到固体载体的方法,例如微量滴定板或硝酸纤维素膜。当连接到琼脂糖时,它们可用于纯化抗
‑
半抗原抗体。它们也可用于制造多价抗原,将能够形成大的抗原
‑
抗体复合物。在选择载体蛋白时,请记住,动物会形成针对载体蛋白以及附着的半抗原的抗体。因此,选择与分析样品中可能发现的蛋白质无关的免疫载体蛋白是相关的。如果半抗原被结合用于免疫和检测,则两种载体蛋白应尽可能不同。这允许使用抗血清,而不必从抗
‑
载体抗体中分离抗
‑
半抗原抗体。
67.在各种实施例中,所述免疫制剂是与已知在被免疫哺乳动物中具有免疫原性的蛋白质结合的seq id no.2。
68.此类免疫原性蛋白质的示例包括但不限于钥孔血蓝蛋白(klh)、血清白蛋白、牛甲状腺球蛋白、大豆胰蛋白酶抑制剂和类毒素,例如破伤风类毒素。
69.klh是一种在软体动物中发现的呼吸蛋白。它的大尺寸使其具有很强的免疫原性,并且大量赖氨酸残基可用于接合,使其作为半抗原的载体非常有用。哺乳动物和软体动物之间的系统发育分离增加了免疫原性,并降低了抗klh载体的抗体与哺乳动物样本中天然存在的蛋白质之间交叉反应的风险。
70.klh以其天然形式提供,用于通过胺进行共轭,以及琥珀酰化,用于通过羧基进行共轭。琥珀酰化的klh可以与含有胺基(例如肽)的半抗原进行共轭,其通过在klh的新引入的羧基和半抗原胺基之间与碳二亚胺交联实现。半抗原与载体蛋白质共轭的方案在本领域是已知的。
71.本领域技术人员无需过多实验即可选择免疫方案。用于制备免疫原、动物免疫和抗血清收集的方案可以在本领域技术人员可获得的参考材料中找到。
72.单克隆抗体
73.在各种实施例中,抗体可以是或者是单克隆抗体。可以使用杂交瘤方法制备单克隆抗体,例如由kohler and milstein(1975),nature,256:495描述的那些。在杂交瘤方法中,小鼠、仓鼠或其他合适的宿主动物进行免疫,以诱导产生或能够产生将特异性结合到免疫剂的抗体的淋巴细胞。或者,淋巴细胞可以在体外免疫。
74.通常,如果需要人类来源的细胞,则使用外周血淋巴细胞(“pbl”),如果需要非人类哺乳动物来源,则使用脾细胞或淋巴结细胞。然后使用合适的融合剂(例如聚乙二醇)将淋巴细胞与永生化细胞系融合以形成杂交瘤细胞。永生化细胞系通常是转化的哺乳动物细胞,尤其是啮齿动物、牛和人类来源的骨髓瘤细胞。通常采用大鼠或小鼠骨髓瘤细胞系。所述杂交瘤细胞可在合适的培养基中培养,该培养基优选包含抑制未融合的永生化细胞的生长或存活的一种或多种物质。例如,如果亲代细胞缺乏次黄嘌呤鸟嘌呤磷酸核糖转移酶(hgprt 或hprt),则杂交瘤的培养基通常包括次黄嘌呤、氨基蝶呤和胸苷(“hat 培养基”),这些物质会阻止hgprt缺陷细胞的生长。
75.首选的永生化细胞系是那些高效融合、通过支持所选抗体产生细胞稳定高水平表达抗体、并且对培养基(如hat培养基)敏感的细胞系。更优选的永生化细胞系是小鼠骨髓瘤系,可从例如加利福尼亚州圣地亚哥的索尔克研究所细胞分布中心(salk institute cell distribution center)和美国马纳萨斯的美国典型培养物保藏中心(american type culture collection)获得,人骨髓瘤和小鼠
‑
人异骨髓瘤细胞系也被描述用于生产人单克隆抗体。
76.然后,可以分析培养杂交瘤细胞的培养基中是否存在针对苏氨酸166磷酸化的rubicon蛋白的单克隆抗体。
77.在确定所需杂交瘤细胞后,可通过限制稀释过程对克隆进行亚克隆,并通过标准方法进行生长。用于此目的的合适培养基包括,例如,dulbecco's modifiedeagle's培养基和rpmi
‑
1640培养基。或者,杂交瘤细胞可以在哺乳动物体内以腹水的形式生长。
78.亚克隆分泌的单克隆抗体可通过常规免疫球蛋白纯化程序从培养基或腹水中分
是指已将seq id no.3的lrrk2认定为一种风险因子的任何疾病。在各种实施例中,与lrrk2相关的疾病选自帕金森病;如克罗恩病或溃疡性结肠炎的慢性炎症;在各种实施例中,与lrrk2相关的疾病是帕金森病。
91.在各种实施例中,与富含亮氨酸重复激酶2(lrrk2)相关的疾病为帕金森病。
92.在各种实施例中,提供了一种rubicon与富含亮氨酸重复激酶2(lrrk2) 相互作用的抑制剂,其包含一种能够阻断lrrk2与rubicon蛋白的苏氨酸166 相互作用的化合物。
93.目前的lrrk2抑制剂直接靶向lrrk2激酶,且在体内模型测试时会产生不良副作用。阻断或靶向lrrk2底物rubicon蛋白的特定磷酸化位点对激酶有间接影响。由于抑制作用仅限于lrrk2和rubicon之间的相互作用以及与这种相互作用相关的通路,而不是单独影响lrrk2的通用功能,因此这会施加更多控制。
94.在各种实施例中,所述抑制剂化合物包含抗体。在各种实施例中,所述化合物包含嵌合人源化抗体。在各种实施例中,所述化合物包含单克隆抗体。
95.在各种实施例中,可提供上文所述的抑制剂用于治疗与富含亮氨酸重复激酶 2(lrrk2)相关的疾病。
96.如上所述,在各种实施例中,术语“与富含亮氨酸重复激酶2(lrrk2)相关的疾病”是指已将seq id no.3的lrrk2认定为一种风险因素的任何疾病。在各种实施例中,与lrrk2相关的疾病选自帕金森病;如克罗恩病或溃疡性结肠炎的慢性炎症;如分枝杆菌感染的细菌感染。在各种实施例中,所述抑制剂用于治疗作为帕金森病的与富含亮氨酸重复激酶2(lrrk2)相关的疾病。
97.在各种实施例中,使用上文所述的抗体或上文所述的抑制剂制造用于治疗与富含亮氨酸重复激酶2(lrrk2)相关疾病的药物。。
98.如上所述,在各种实施例中,术语“与富含亮氨酸重复激酶2(lrrk2)相关的疾病”是指已将seq id no.3的lrrk2认定为一种风险因素的任何疾病。在各种实施例中,与lrrk2相关的疾病选自帕金森病;如克罗恩病或溃疡性结肠炎的慢性炎症;以及如分枝杆菌感染的细菌感染。在各种实施例中,在制造用于治疗与富含亮氨酸重复激酶2(lrrk2)相关的疾病的药物中使用抗体或抑制剂,用于帕金森病。
99.在各种实施例中,一种治疗有患有与富含亮氨酸重复激酶2(lrrk2)相关疾病的需要的受试者的方法,包括:施用能够阻断lrrk2与rubicon蛋白的苏氨酸166和/或丝氨酸189相互作用的化合物。
100.在各种实施例中,所述化合物能够阻断lrrk2与rubicon蛋白磷酸化的苏氨酸166和/或丝氨酸189相互作用。在rubicon蛋白的苏氨酸166和/或丝氨酸189磷酸化之前或之后阻断相互作用将具有减缓运动技能退化和/或延长寿命的效果。
101.在各种实施例中,所述方法中使用的化合物包含上文所述的抗体。在各种实施例中,所述抗体是上文所述的嵌合人源化抗体。在各种实施例中,所述抗体是上文所述的单克隆抗体。
102.在各种实施例中,以本领域已知的任何适当方式施用该化合物。在各种实施例中,所述化合物通过注射给药。在各种实施例中,所述化合物通过直接注射到lrrk2与负责引起与富含亮氨酸重复激酶2(lrrk2)相关疾病的rubicon 蛋白的苏氨酸166和/或丝氨酸189相互作用的部位来施用。
103.在各种实施例中,提供了包含上文描述的抗体和用于检测与富含亮氨酸重复激酶2(lrrk2)相关的疾病的检测试剂的试剂盒。
104.在各种实施例中,检测试剂是用于酶联免疫吸附试验(elisa)的试剂。在各种实施例中,检测试剂是用于直接elisa的试剂。在各种实施例中,检测试剂是用于间接elisa的试剂。在各种实施例中,检测试剂是用于夹心elisa 的试剂。在各种实施例中,检测试剂是用于允许检测抗体
‑
rubicon复合物的任何方法的试剂。在各种实施例中,根据所使用的方法,检测试剂可从以下任一种中选择:覆盖微量滴定板的抗原;封闭未结合部位的试剂,以防止假阳性;抗igg结合酶;与酶反应以允许通过颜色变化、荧光或本领域已知的任何其他方式进行检测的底物;其他试剂,如洗涤缓冲液、停止溶液、稳定剂;及其任何组合。
105.在各种实施例中,所述试剂盒可包括预涂有上文所述抗体的微量滴定板。这将有助于更快速的检测,并减少污染的机会。
106.如上所述,在各种实施例中,术语“与富含亮氨酸重复激酶2(lrrk2) 相关的疾病”是指已将seq id no.3的lrrk2认定为一种风险因素的任何疾病。在各种实施例中,与lrrk2相关的疾病选自帕金森病;如克罗恩病或溃疡性结肠炎的慢性炎症;如分枝杆菌感染的细菌感染。
107.在各种实施例中,与富含亮氨酸重复激酶2(lrrk2)相关的疾病为帕金森病。
108.示例
109.尸检对人黑质脑组织进行内源性lrrk2(绿色荧光)和rubicon(红色荧光)表达染色。通过共聚焦显微镜分析lrrk2和rubicon共定位(黄色荧光)的范围,共定位统计显示lrrk2和rubicon之间存在高度相关性(图1,表1)。lrrk2和rubicon相互作用通过免疫共沉淀得到证实。
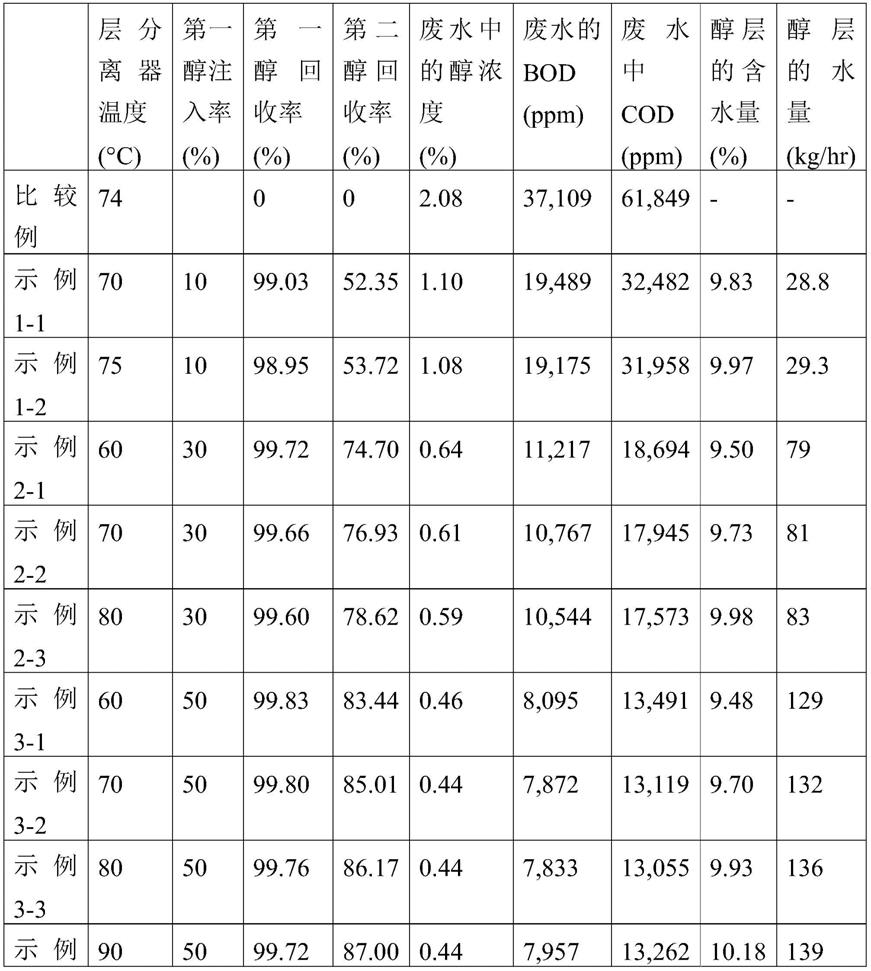
110.表1lrrk2和rubicon的共定位分析共定位统计数值解释皮尔逊系数0.7286强相关性
111.使用两种lrrk2激酶分析方法筛选rubicon无磷突变体。第一种方法通过lrrk2激酶量化了rubicon磷酸化程度,并将t166和s189确定为一致的 lrrk2特异性磷酸位点(图2)。第二种方法量化了作为lrrk2激酶活性副产物的产生的adp的量,并显示rubicon突变体的117
‑
189个氨基酸显著降低 lrrk2激酶活性(图3a)。肽分析表明lrrk2更喜欢苏氨酸残基作为磷酸化位点,因此产生了一种针对磷
‑
t166(pt166)rubicon的定制单克隆抗体,以验证所识别的磷酸化位点。与对照组相比,内源性lrrk2被敲除的人类神经元 pt166
‑
rubicon减少32.4%;与对照组相比,瞬时过度表达野生型(wt)lrrk2 或突变型lrrk2
‑
g2019s的人类神经元pt166
‑
rubicon分别增加12%和26%(图 3b)。
112.因此,通过在果蝇中共表达人lrrk2和rubicon来研究lrrk2和 rubicon的体内作用。产生基于先前识别的磷酸位点的rubicon突变体系: t166a、s189a、t166a s189a果蝇rubicon突变体(dm)和缺失117
‑
189 (del)。t166a在两条染色体上尝试三个插入位点后未产生转化子,s189a产生转化子,但经western blotting验证缺乏蛋白质表达。因此,在确认蛋白表达后,所有后续研究均采用wt、dm和del
‑
rubicon系进行。与人类的情况类似,果蝇多巴胺能(da)系统也参与运动控制。由于在成年果蝇大脑中可检测到通过阳性酪氨酸羟化酶(th)染色确定的不同da神经元簇,因此根据攀爬能力、寿命和th阳性表达评估了果蝇的生
存能力。首先,rubicon突变体的共表达显着提高了wt
‑
lrrk2和lrrk2
‑
g2019s果蝇攀爬的能力,直到第50天。此后,果蝇模型的特征表现为性能急剧下降(图4,表2)。接下来,rubicon突变体的共表达显着延长了wt
‑
lrrk2果蝇的寿命>25%,而rubicon的共表达显着延长了lrrk2
‑
g2019s果蝇的寿命>35%(图4,表3)。最后,老化的苍蝇大脑的五个区域被染色为th阳性神经元簇并计数(图5)。rubicon突变体的共表达显着增加了wt
‑
lrrk2果蝇中>2个区域和lrrk2
‑
g2019s果蝇中>3个区域的th计数(表4)。
113.表2中的果蝇攀爬试验统计分析采用tukey事后试验的多重比较。当p<0.05 (粗体值)时,达到统计学显著性。
114.表2a:lrrk2
‑
wt攀爬试验统计分析
115.表2b:g2019s攀爬试验统计分析
116.果蝇寿命统计分析采用tukey
‑
kramer方法进行多重比较。当p<0.05(粗体值)时,达到统计显著性。
117.表3a:lrrk2
‑
wt寿命统计分析
118.表3b:g2019s寿命统计分析g2019s寿命统计分析
119.表4:果蝇酪氨酸羟化酶(th)神经元染色在老年转基因果蝇中的统计学意义。对老龄(60天)转基因苍蝇大脑五个区域(ppl1、ppl2、ppm1/2、ppm3、 pal)的th神经元簇进行染色并计数。经多重比较调整后,使用student’s t检验分析统计显著性。
非配对t检测统计显著下降统计显著增加
120.在证明rubicon t166和s189无磷突变体能够在体内挽救lrrk2诱导的毒性后,接下来使用本文所述的定制pt166 rubicon夹心elisa研究了pt166 rubicon在人pd样品中的重要性。首先,分析了来自具有亚洲lrrk2 突变的本地pd队列的人血清。与健康对照组相比,无论是野生型还是突变型 lrrk2,pd患者血清中pt166 rubicon的表达均显著高于健康对照组(图7和表5)。接下来,使用所述的定制pt166 rubicon夹心elisa检测巨噬细胞中 pt166 rubicon的表达。首先,lrrk2和rubicon在神经元和小胶质细胞中具有相当的内源性表达,类似于脑巨噬细胞(图8a)对内源性lrrk2基因敲除的小鼠巨噬细胞进行pt166 rubicon表达分析(图8b,表6)。缺乏lrrk2的巨噬细胞内源性pt166 rubicon减少30%,过度表达的pt166 rubicon减少60%。
121.尸检后的人脑样本分为可溶性和膜相关蛋白组分,随后分析pt166 rubicon 表达。对尸检后人脑切片的lrrk2和rubicon进行染色显示,与对照脑相比, pd脑的总体表达较低(图9)。与对照组相比,pd脑在细胞质和膜相关部分的 pt166 rubicon表达显著降低(表7)。尽管检查的外周和中枢神经系统样本(即血清与大脑)之间存在差异,但这两个系统都显著改变了pt166 rubicon的表达。
122.表5:通过pt166 rubicon夹心elisa分析来自具有lrrk2变异突变的新加坡pd队列的人血清的统计显着性。使用mann
‑
whitney检验分析统计显着性。使用单向方差(kruskal
‑
wallis检验)的全表统计分析:p=0.0168
123.表6:lrrk2巨噬细胞elisa统计分析
ꢀ
过表达rubicon内源性rubicon多重t
‑
检验p=0.0154p=0.0227
124.表7:通过pt166 rubicon夹心elisa分析来自尸检的人脑样本的统计显着性。使用单向方差分析分析统计显着性,当p<0.05时达到统计显着性。 胞质pt166 rubicon膜pt166 rubicon单向方差p=0.022p=0.0004
125.与健康对照相比,pd血清和尸检pd大脑中pt166 rubicon的表达改变显示了其作为pd诊断生物标志物的潜力。
126.在体内,rubicon无磷突变体的共表达能够挽救lrrk2诱导的毒性。这表明rubicon磷酸位点t166和s189可能是lrrk2相关疾病的药物靶点。许多药物具有脱靶效应,因此针对lrrk2特异性底物位点的变构抑制剂将提高精确度并最小化不良的脱靶效应。
127.使用与钥孔血蓝蛋白(klh)共轭的合成肽 dahv{pthr}amlqcleave(seq id no.2)形成抗体,并且所得免疫原肽用于在哺乳动物中产生磷特异性抗体。
128.迄今为止,很少有真正的lrrk2底物被鉴定出来。其中,有条不紊地筛选lrrk2特异性磷酸位点的并不多。
129.使用与钥孔血蓝蛋白(klh)共轭的合成肽dahv{pthr}amlqcleave (seq id no.2)在3只balb/c小鼠和3只c57小鼠中开发多克隆抗体。在用肽共轭物进行第3次和第5次免疫接种后取试验血。为了测试抗体的滴度和特异性,98孔板涂有seq id no.2:dahv{pthr}amlqcleef或seq idno.14:dahvtalqcleef抗原表位,其中围绕seq id no.1的rubicon蛋白t166的序列被磷酸化或未磷酸化。然后,将第3次和第5次免疫后收集的预免疫血清和抗血清样本用于磷酸盐缓冲盐水(ph 7.4)中进行间接elisa分析,以检测一系列上清液稀释液中的磷酸化抗原seq id no.2或非磷酸化抗原seq idno.14。二抗为过氧化物酶亲和纯(peroxidase
‑
affinipure)山羊抗鼠igg,fcγ片段特异性(min x hu,bov hrs sr prot)。结果列于表8中。稀释范围扩大到 1:512000,但未列出整个稀释范围的结果。
130.表8:多克隆抗体的elisa结果
131.针对目标位点开发了单克隆抗体,并选择了5个初级克隆,为每个克隆建立了2个单克隆细胞系。为了测试抗体的滴度和特异性,98孔板涂布有seq idno.2:dahv{pthr}amlqcleave或seq id no.14:dahvtamlqcleave 抗原表位,其中围绕seq id no.1的
rubicon蛋白t166的序列被磷酸化或未磷酸化。然后在ph为7.4的磷酸盐缓冲盐水中对所有10个抗体细胞系进行间接 elisa分析,以检测一系列上清液稀释液中的磷酸化抗原seq id no.2或非磷酸化抗原seq id no.14。二抗为过氧化物酶亲和纯(peroxidase
‑
affinipure)山羊抗鼠igg,fcγ片段特异性(min x hu,bovhrs sr prot)。结果列于表9。
132.表9:杂交瘤培养上清液elisa结果杂交瘤培养上清液elisa结果
133.定制了针对已识别靶点的特异性单克隆抗体,并开发了使用定制pt166 rubicon抗体的夹心elisa。所述pt166 rubicon夹心elisa用人pd血清和脑样本进行验证。所述开发的pt166 rubicon夹心elisa可用于pd的诊断分析。
134.对产生的单克隆抗体进行测序。按照试剂的技术手册,从杂交瘤细胞中分离总rna。然后按照primescripttm第一链cdna合成试剂盒 (primescripttm 1st strand cdna synthesis kit)的技术手册,使用同型特异性反义引物或通用引物将总rna反转录成cdna。根据genscript的cdna末端快速扩增(race)标准操作程序(sop)扩增重链和轻链抗体片段。将扩增的抗体片段分别克隆到标准克隆载体中。进行菌落pcr以筛选具有正确大小插入片段的克隆。下面提供了共有序列。筛选的所有5个克隆具有至少99%的氨基酸序列同一性。类似地,分析发现重链(96.53%核苷酸同一性)和轻链(98.64%核苷酸同一性)中至少有96%的序列同一性。
135.重链:cdna序列(420bp)
136.信号序列
‑
fr1
‑
cdr1
‑
fr2
‑
cdr2
‑
fr3
‑
cdr3
‑
fr4,seq id no.10:
137.轻链:dna序列(393bp)
138.信号序列
‑
fr1
‑
cdr1
‑
fr2
‑
cdr2
‑
fr3
‑
cdr3
‑
fr4,seq id no. 11:11:
139.轻链:氨基酸序列(131aa)
140.信号肽
‑
fr1
‑
cdr1
‑
fr2
‑
cdr2
‑
fr3
‑
cdr3
‑
fr4,seq id no.12:
141.重链:氨基酸序列(140aa)
142.信号肽
‑
fr1
‑
cdr1
‑
fr2
‑
cdr2
‑
fr3
‑
cdr3
‑
fr4,seq id no.13:
143.确定了lrrk2特异性rubicon磷酸化位点t166和s189,lrrk2相关毒性能够在体内挽救,突出了磷酸化位点作为药物靶点的潜力。
144.目前的工作旨在将pt166 rubicon作为pd的诊断生物标志物。这是通过使用开发的pt166 rubicon夹心elisa 检测少量患者血清蛋白(2μg)实现的。
145.患者血清中pt166 rubicon的定量表达将根据预设阈值确定分析样本属于健康对照组还是pd组。理想情况下,如果pt166 rubicon表达在短病程(<5 年)和长病程(>5年)之间变化,量化的pt166 rubicon表达将能够揭示pd是早期还是晚期。
146.在各种实施例中,rubicon是由seq id no.1所表示的氨基酸序列:
147.其中磷酸位点t166和s189表示为粗体带下划线的氨基酸。
148.seq id no.2:dahv{pthr}amlqcleave
149.seq id no.3:masgscqgceedeetlkklivrlnnvqegkqietlvqiledllvftyserasklfqgknihvpllivldsy mrvasvqqvgwsllcklievcpgtmqslmgpqdvgndwevlgvhqlilkmltvhnasvnlsviglktl dllltsgkitllildeesdifmlifdamhsfpandevqklgckalhvlfervseeqltefvenkdymillsa ltnfkdeeeivlhvlhclhslaipcnnvevlmsgnvrcynivveamkafpmseriqevsccllhrltlgn ffnilvlnevhefvvkavqqypenaalqisalsclalltetiflnqdleeknenqenddegeedklfwlea cykaltwhrknkhvqeaacwalnnllmyqnslhekigdedghfpahrevmlsmlmhssskevfqasa nalstlleqnvnfrkillskgihlnvlelmqkhihspevaesgckmlnhlfegsntsldimaavvpkiltv mkrhetslpvqlealrailhfivpgmp
eesredtefhhklnmvkkqcfkndihklvlaalnrfignpgiq kcglkvissivhfpdalemlslegamdsvlhtlqmypddqeiqclglsligylitkknvfigtghllakil vsslyrfkdvaeiqtkgfqtilailklsasfskllvhhsfdlvifhqmssnimeqkdqqflnlcckcfakva mddylknvmleracdqnnsimvecllllgadanqakegsslicqvcekesspklvelllnsgsreqdvr kaltisigkgdsqiislllrrlaldvannsiclggfcigkvepswlgplfpdktsnlrkqtniastlarmvir yqmksaveegtasgsdgnfsedvlskfdewtfipdssmdsvfaqsddldsegsegsflvkkksnsisvgef yrdavlqrcspnlqrhsnslgpifdhedllkrkrkilssddslrssklqshmrhsdsisslasereyitsld lsanelrdidalsqkccisvhlehleklelhqnaltsfpqqlcetlkslthldlhsnkftsfpsyllkmsci anldvsrndigpsvvldptvkcptlkqfnlsynqlsfvpenltdvvekleqlilegnkisgicsplrlkelk ilnlsknhisslsenfleacpkvesfsarmnflaampflppsmtilklsqnkfscipeailnlphlrsldmss ndiqylpgpahwkslnlrellfshnqisildlsekaylwsrveklhlshnklkeippeigclenltsldvsy nlelrsfpnemgklskiwdlpldelhlnfdfkhigckakdiirflqqrlkkavpynrmklmivgntgsgk ttllqqlmktkksdlgmqsatvgidvkdwpiqirdkrkrdlvlnvwdfagreefysthphfmtqralyl avydlskgqaevdamkpwlfnikarassspvilvgthldvsdekqrkacmskitkellnkrgfpairdy hfvnateesdalaklrktiineslnfkirdqlvvgqlipdcyvelekiilserknvpiefpvidrkrllqlvr enqlqldenelphavhflnesgvllhfqdpalqlsdlyfvepkwlckimaqiltvkvegcpkhpkgiisrr dvekflskkrkfpknymsqyfkllekfqialpigeeyllvpsslsdhrpvielphcenseiiirlyempyfpm gfwsrlinrlleispymlsgreralrpnrmywrqgiylnwspeayclvgsevldnhpesflkitvpscrk gcillgqvvdhidslmeewfpglleidicgegetllkkwalysfndgeehqkillddlmkkaeegdllvn pdqprltipisqiapdliladlprnimlnndelefeqapefllgdgsfgsvyraayegeevavkifnkhtslr llrqelvvlchlhhpslisllaagirprmlvmelaskgsldrllqqdkasltrtlqhrialhvadglrylh samiiyrdlkphnvllftlypnaaiiakiadygiaqyccrmgiktsegtpgfrapevargnviynqqadvy sfglllydilttggriveglkfpnefdeleiqgklpdpvkeygcapwpmveklikqclkenpqerptsaqv fdilnsaelvcltrrillpknvivecmvathhnsrnasiwlgcghtdrgqlsfldlntegytseevadsril clalvhlpvekeswivsgtqsgtllvintedgkkrhtlekmtdsvtclycnsfskqskqknfllvgtadg klaifedktvklkgaaplkilnignvstplmclsestnsternvmwggcgtkifsfsndftiqklietrtsq lfsyaafsdsniitvvvdtalyiakqnspvvevwdkkteklcglidcvhflrevmvkenkeskhkmsysg rvktlclqkntalwigtggghillldlstrrlirviynfcnsvrvmmtaqlgslknvmlvlgynrknte gtqkqkeiqscltvwdinlphevqnlekhievrkelaekmrrtsve
150.本领域技术人员还应该理解,上述特征的变化和组合,不是替代或替代,可以组合以形成落入本发明的预期范围内的更进一步的实施例。
151.本领域技术人员可以理解,每个实施例可以与其他实施例或多个实施例组合使用。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。