用于治疗神经变性障碍的组合物和方法
1.相关申请
2.本技术要求2018年12月28日提交的美国临时专利申请顺序号62/785,903的权益和优先权,其通过引用整体并入本文。
技术领域
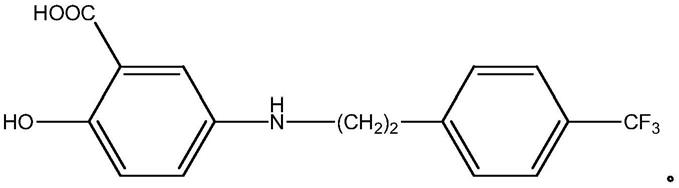
3.本公开内容涉及用于治疗衰老的伴侣动物的认知障碍的药物组合物,其包含式(i)的5
‑
苄基氨基水杨酸化合物或其药学上可接受的盐;和适合用于口服施用的药学上可接受的赋形剂。本公开内容涉及用于治疗认知衰退的方法,所述认知衰退包括犬科动物cds、心境恶劣、退化性抑郁症(involutive depression)和精神错乱综合征。
背景技术:
4.世界范围内的伴侣动物数量正在稳步增加。排名前20位的国家的家养的狗和猫数量估计分别为大约2.56亿只和大约2.36亿只。由于营养的改善、疾病治疗以及出色的兽医和宠物主人护理,如今家养的狗和猫的寿命要长得多。因此,人们对伴侣动物年龄相关疾病的治疗越来越感兴趣。
5.许多年老或衰老的狗和猫患有由神经系统疾病引起的认知损害,包括cds、心境恶劣、退化性抑郁症和精神错乱综合征。认知损害被定义为在记忆、学习新事物、注意力集中或做出可能影响日常生活的决定方面存在困难。cds是狗和猫中的与年龄相关的退行性脑疾病。据报道,8岁以上狗的cds患病率为14%
‑
60%[1
‑
4]。其他报告显示,11
‑
16岁的伴侣狗中有62%患有cds,其中患病率随着年龄的增长而显著增加[5]。因此,大量的狗患有cds,这会恶化人与动物的关系,降低动物的生活质量,并从而缩短动物的寿命[6
‑
8]。
[0006]
犬科动物cds中看到的病理生理学改变包括大脑皮质和基底神经节萎缩;脑室大小增加;脱髓鞘;神经胶质细胞的大小和数量增加;神经元丢失,尤其是在海马皮层区域;轴索变性;β
‑
淀粉样斑块的蓄积[6,9,10]。患有cds的猫还伴有神经元数量减少、β淀粉样蛋白沉积和类似于犬科动物cds的神经胶质细胞增加。与人的阿尔茨海默病(ad)相反,在患有cds的狗和猫的脑中尚未发现ad中广泛存在的神经原纤维缠结,这启示狗和猫的cds可与ad区分开来[11]。
[0007]
诊断为cds的狗和猫在认知和神经功能方面表现出进行性损害。它们表现出各种行为问题,诸如在家里迷路,白天活动较少,不再向家人或其他熟悉的动物打招呼,点名时没有反应,绕圈子或在不寻常的地方排尿[10,12
‑
15]。
[0008]
尽管最近观察到患有cds的狗和猫的数量迅速增长,但cds仍然是未满足的医疗需求。司来吉兰是单胺氧化酶b(mao
‑
b)的选择性不可逆抑制剂,其为唯一被fda批准用于治疗cds的药物[16]。先前的报道表明,司来吉兰增强认知功能并改善行为功能。然而,近期数据表明,其有益作用并不能长期维持,显示司来吉兰疗法只是症状学治疗。例如,cds狗中的认知功能在司来吉兰治疗后的前2周内得到改善,但大多数狗中的有益效果在治疗后的8周消失[17
‑
19]。此外,一项涉及474只8岁以上患有cds的狗的大型临床试验得出结论:应在临床
症状发作的早期施用司来吉兰治疗[19]。
[0009]
许多非药理学疗法已经是可用的,包括膳食补充抗氧化剂、l
‑
肉碱和ω
‑
3脂肪酸,这些疗法只是为了通过缓解焦虑和支持认知功能来改善狗的福利(welfare)。为获得最佳结果,此类膳食补充剂应在犬科动物cds的早期阶段开始。由于犬科动物和猫科动物的cds无法治愈,因此需要开发可以阻止或减缓cds进展的缓解疾病的(disease
‑
modifying)化合物和方法。
[0010]
2002年至2012年间进行了超过400项用于治疗ad的临床试验,但美金刚(一种低至中等亲和力的n
‑
甲基
‑
d
‑
天冬氨酸受体拮抗剂)是唯一被批准用于ad的症状学治疗的药物,这基于如下发现:它在中度至重度ad中显示在心理功能和进行日常活动的能力方面略有改善。此后,靶向β淀粉样蛋白、炎症或氧化应激的药物的大量iii期临床试验均已针对ad进行,但均未能显示出有益效果,这使得情况更为恶化。然而,在分别过表达家族性ad突变基因、突变淀粉样前体蛋白(app)或app和早老素的两种标准ad小鼠模型tg2576和app/ps1中,几乎所有失败的药物都减少了淀粉样斑块负担并改善了认知功能。因此,在ad的临床前期动物模型中证明的候选药物的药理功效并未转化为用于在人中的ad的治疗。
[0011]
发明详述
[0012]5‑
苄基氨基水杨酸化合物或其药学上可接受的盐已经被用于治疗ad和神经变性疾病(美国专利号6,964,982)。在先前的研究中,2
‑
羟基
‑5‑
[2
‑
(4
‑
三氟甲基
‑
苯基)乙基氨基]苯甲酸被证实为在纳摩尔浓度下有效的自旋捕获分子和微粒体前列腺素e(2)合酶
‑
1(mpges
‑
1)抑制剂,其不仅能阻断神经元死亡、轴突病和自体吞噬体形成,还能在肌萎缩侧索硬化小鼠模型中增加运动功能活动和寿命[20]。
[0013]
探究5
‑
苄基氨基水杨酸化合物或其药学上可接受的盐用于治疗伴侣动物的cds。令人惊奇地,口服施用2
‑
羟基
‑5‑
[2
‑
(4
‑
三氟甲基
‑
苯基)乙基氨基]苯甲酸超过4周显著改善了患有严重cds的年老伴侣狗的认知和神经行为功能。此外,在最后一次施用后2
‑
羟基
‑5‑
[2
‑
(4
‑
三氟甲基
‑
苯基)乙基氨基]苯甲酸的有益作用维持至少4周。因此,启示2
‑
羟基
‑5‑
[2
‑
(4
‑
三氟甲基
‑
苯基)乙基氨基]苯甲酸可以为用于通过抑制氧化应激和炎症治疗cds的潜在治疗选择。在一些实施方案中,本公开内容涉及包含式(i)的5
‑
苄基氨基水杨酸化合物或其药学上可接受的盐的组合物和方法,其用于治疗伴侣动物的例如神经系统疾病中的认知和/或神经行为损害。
[0014]
技术问题
[0015]
因此,本公开内容提供了用于治疗伴侣动物的例如神经系统疾病中的认知和/或神经行为损害(诸如cds、心境恶劣、退化性抑郁症和精神错乱综合征)的药物组合物和方法。
[0016]
技术方案
[0017]
本公开内容提供了用于治疗伴侣动物的例如神经系统疾病中的认知和/或神经行为损害的式(i)的化合物:
[0018][0019]
其中
[0020]
x选自co、so2和(ch2)
n
;
[0021]
r1选自氢、c1‑
c6烷基和c1‑
c6烷酰基;
[0022]
r2选自氢和c1‑
c6烷基;
[0023]
r3选自氢和c1‑
c5乙酰基;且
[0024]
r4选自苯基、苯氧基和5
‑
至10
‑
元芳基,其未被取代或被一个或多个取代基取代,所述取代基各自独立地选自硝基、卤素、c1‑
c6烷基、c1‑
c6卤代烷基、c1‑
c5烷氧基和c1‑
c5卤代烷氧基;
[0025]
n为1
‑
5的整数,包括1和5在内;
[0026]
或其药学上可接受的盐。
[0027]
本公开内容提供了治疗例如神经系统疾病中的认知和/或神经行为损害的方法,包含对有此需要的伴侣动物施用式(i)的化合物:
[0028][0029]
其中,
[0030]
x选自co、so2和(ch2)
n
;
[0031]
r1选自氢、c1‑
c6烷基和c1‑
c6烷酰基;
[0032]
r2选自氢和c1‑
c6烷基;
[0033]
r3选自氢和c1‑
c5乙酰基;且
[0034]
r4选自苯基、苯氧基和5
‑
至10
‑
元芳基,其未被取代或被一个或多个取代基取代,所述取代基各自独立地选自硝基、卤素、c1‑
c6烷基、c1‑
c6卤代烷基、c1‑
c5烷氧基和c1‑
c5卤代烷氧基;
[0035]
n为1
‑
5的整数,包括1和5在内;
[0036]
或其药学上可接受的盐。
[0037]
在一些实施方案中,已经制备并且评价了多种式(i)的化合物。在一些实施方案中,所述组合物和方法包含式(i)的5
‑
苄基氨基水杨酸化合物或其药学上可接受的盐。
[0038]
在一些实施方案中,5
‑
苄基氨基水杨酸化合物为5
‑
苄基氨基水杨酸自身。
[0039]5‑
苄基氨基水杨酸化合物的优选实例包括、但不限于2
‑
羟基
‑5‑
苯乙基氨基
‑
苯甲酸(化合物1)、2
‑
羟基
‑5‑
[2
‑
(4
‑
三氟甲基
‑
苯基)
‑
乙基氨基]
‑
苯甲酸(化合物2)、2
‑
羟基
‑5‑
[2
‑
(3
‑
三氟甲基
‑
苯基)
‑
乙基氨基]
‑
苯甲酸(化合物3)、5
‑
[2
‑
(3,5
‑
双
‑
三氟甲基
‑
苯基)
‑
乙
基氨基]
‑2‑
羟基
‑
苯甲酸(化合物4)、2
‑
羟基
‑5‑
[2
‑
(2
‑
硝基
‑
苯基)
‑
乙基氨基]
‑
苯甲酸(化合物5)、5
‑
[2
‑
(4
‑
氯
‑
苯基)
‑
乙基氨基]
‑2‑
羟基
‑
苯甲酸(化合物6)、5
‑
[2
‑
(3,4
‑
二氟
‑
苯基)
‑
乙基氨基]
‑2‑
羟基
‑
苯甲酸(化合物7)、5
‑
[2
‑
(3,4
‑
二氯
‑
苯基)
‑
乙基氨基]
‑2‑
羟基
‑
苯甲酸(化合物8)、5
‑
[2
‑
(4
‑
氟
‑2‑
三氟甲基
‑
苯基)
‑
乙基氨基]
‑2‑
羟基
‑
苯甲酸(化合物9)、5
‑
[2
‑
(2
‑
氟
‑4‑
三氟甲基
‑
苯基)
‑
乙基氨基]
‑2‑
羟基
‑
苯甲酸(化合物10)、2
‑
羟基
‑5‑
[2
‑
(4
‑
甲氧基
‑
苯基)
‑
乙基氨基]
‑
苯甲酸(化合物11)、2
‑
羟基
‑5‑
(2
‑
邻
‑
甲苯基
‑
乙基氨基)
‑
苯甲酸(化合物12)、2
‑
羟基
‑5‑
(3
‑
苯基
‑
丙基氨基)
‑
苯甲酸(化合物13)、2
‑
羟基
‑5‑
[3
‑
(4
‑
三氟甲基
‑
苯基)
‑
丙基氨基]
‑
苯甲酸(化合物14)、5
‑
[3
‑
(4
‑
氟
‑
苯基)
‑
丙基氨基]
‑2‑
羟基
‑
苯甲酸(化合物15)、5
‑
[3
‑
(3,4
‑
二氯
‑
苯基)
‑
丙基氨基]
‑2‑
羟基
‑
苯甲酸(化合物16)、2
‑
羟基
‑5‑
(3
‑
对
‑
甲苯基
‑
丙基氨基)
‑
苯甲酸(化合物l7)、2
‑
乙酰氧基
‑5‑
[2
‑
(4
‑
三氟甲基
‑
苯基)
‑
乙基氨基]
‑
苯甲酸(化合物18)、5
‑
[2
‑
(2
‑
氯
‑
苯基)
‑
乙基氨基]
‑2‑
羟基
‑
苯甲酸(化合物19)、5
‑
苄基氨基水杨酸(化合物20)、5
‑
(4
‑
硝基苄基)氨基水杨酸(化合物21)、5
‑
(4
‑
氯苄基)氨基水杨酸(化合物22)、5
‑
(4
‑
三氟甲基苄基)氨基水杨酸(化合物23)、5
‑
(4
‑
氟苄基)氨基水杨酸(化合物24)、5
‑
(4
‑
甲氧基苄基)氨基水杨酸(化合物25)、5
‑
(2,3,4,5,6
‑
五氟苄基)氨基水杨酸(化合物26)、乙基苯甲酸5
‑
(4
‑
硝基苄基)氨基
‑2‑
羟基酯(化合物27)、乙基苯甲酸5
‑
(4
‑
硝基苄基)
‑
n
‑
乙酰氨基
‑2‑
羟基酯(化合物28)、乙基苯甲酸5
‑
(4
‑
硝基苄基)
‑
n
‑
乙酰氨基
‑2‑
乙酰氧基酯(化合物29)、5
‑
(4
‑
硝基苯甲酰基)氨基水杨酸(化合物30)、5
‑
(4
‑
硝基苯磺酰基)氨基水杨酸(化合物31)、5
‑
[2
‑
(4
‑
硝基苯基)
‑
乙基]氨基水杨酸(化合物32)和5
‑
[3
‑
(4
‑
硝基
‑
苯基)
‑
正
‑
丙基]氨基水杨酸(化合物33)。在某些优选的实施方案中,式(i)的化合物为化合物2,即2
‑
羟基
‑5‑
[2
‑
(4
‑
三氟甲基
‑
苯基)乙基氨基]苯甲酸,或其药学上可接受的盐。在一些实施方案中,式(i)的化合物具有如下结构:
[0040][0041]
本公开内容的5
‑
苄基氨基水杨酸化合物或其药学上可接受的盐可以通过美国专利号6,573,402中有代表性的反应方案制备,但不限于此。
[0042]
在一些实施方案中,所述认知和/或神经行为损害为cds、心境恶劣、退化性抑郁症或精神错乱综合征。在一些实施方案中,式(i)的化合物治疗伴侣动物中的认知和/或神经行为损害。在一些实施方案中,所述认知和/或神经行为损害为cds。
[0043]
在一些实施方案中,治疗认知和/或神经行为损害通过氧化应激和炎症的并发药理学抑制来进行。在一些实施方案中,治疗认知和/或神经行为损害通过抑制氧化应激和前列腺素e2合成来进行。在一些实施方案中,治疗认知和/或神经行为损害通过抑制氧化应激和微粒体前列腺素e合酶
‑
1来进行。
[0044]
在一些实施方案中,伴侣动物表现出涉及行为改变的症状,其选自食欲、饮行为、发声、排泄行为(elimination behavior)、睡眠模式、漫无目的行为、适应能力、社交行为、感知能力、定向障碍和记忆力。在一些实施方案中,伴侣动物表现出涉及行为改变的症状,其选自发声、排泄行为、睡眠模式、漫无目的行为、社交行为、感知能力、定向障碍和记忆力。
在一些实施方案中,伴侣动物表现出涉及行为改变的症状,其选自睡眠模式、社交行为、定向障碍和记忆力。在一些实施方案中,伴侣动物表现出涉及记忆力改变的症状。在一些实施方案中,伴侣动物表现出涉及行为改变的症状,其选自定向(例如茫然地盯着和在家中迷路)、记忆力(例如不认识主人和弄脏房子)、冷漠(例如减少活动时间和避免与主人接触)、嗅觉损害(例如难以找到食物)和运动。
[0045]
在一些实施方案中,伴侣动物表现出涉及行为改变的症状,其选自空间定向、社交互动、睡眠
‑
觉醒周期和弄脏房屋。
[0046]
在一些实施方案中,伴侣动物表现出病理生理学改变。在一些实施方案中,病理生理学改变选自大脑皮质萎缩;基底神经节萎缩;脑室大小增加;脱髓鞘;神经胶质细胞大小增加;神经胶质细胞数量增加;神经元丢失,尤其是在海马皮层区域;轴索变性;以及β
‑
淀粉样斑块蓄积。在一些实施方案中,病理生理学改变改变选自神经胶质细胞大小增加;神经胶质细胞数量增加;神经元丢失;以及β
‑
淀粉样蛋白沉积增加。
[0047]
在一些实施方案中,伴侣动物选自猫、毛丝鼠、狗、雪貂、沙鼠、豚鼠、仓鼠、刺猬、小鼠、家兔和大鼠。在某些优选的实施方案中,伴侣动物为猫或狗。在一些实施方案中,伴侣动物为犬科动物或猫科动物。
[0048]
定义
[0049]
如下所述的术语定义适用于该术语自身的应用或与另一术语组合使用。
[0050]
术语“乙酰氧基”是指由通式烃基c(o)o
‑
、优选烷基c(o)o
‑
表示的基团。
[0051]
术语“乙酰基”是指由通式ch3c(o)
‑
表示的基团。
[0052]“烷基”基团(包括卤代烷基的
‘
烷基’)或“烷”为完全饱和的直链或支链非芳族烃。典型地,直链或支链烷基基团具有1
‑
约20个碳原子,优选1
‑
约10个,另有定义的除外。c1‑
c6直链或支链烷基基团也被称为“低级烷基”基团。在一些实施方案中,烷基为c1‑
c5烷基、更优选为c1‑
c3烷基。更具体地,优选的烷基基团包括但不限于:甲基、乙基、丙基、异丙基、丁基、仲丁基和叔丁基。
[0053]
此外,术语“烷基”(或“低级烷基”)如在整个说明书、实施例和权利要求中使用的,旨在包括“未取代的烷基”和“取代的烷基”,后者是指具有替代烃主链的一个或多个碳上的氢的取代基的烷基部分。如果没有另外指明,则这样的取代基可以包括,例如,卤素、羟基、羰基(诸如羧基、烷氧基羰基、甲酰基或酰基,诸如烷基c(o))、硫代羰基(诸如硫酯、硫代乙酸酯或硫代甲酸酯)、烷氧基、磷酰基、磷酸酯、膦酸酯、次膦酸酯、氨基、酰氨基、脒、亚胺、氰基、硝基、叠氮基、甲硅烷基醚、巯基、烷硫基、硫酸酯、磺酸酯、氨磺酰基、磺酰氨基、磺酰基、杂环基、芳烷基或芳族或杂芳族部分。本领域技术人员将理解,如果适合,烃链上被取代的部分本身可以被取代。例如,取代的烷基的取代基可以包括以下取代和未取代形式:氨基、叠氮基、亚氨基、酰氨基、磷酰基(包括膦酸酯和次膦酸酯)、磺酰基(包括硫酸酯、磺酰氨基、氨磺酰基和磺酸酯)以及甲硅烷基和醚、烷基硫醇、羰基(包括酮、醛、羧酸酯和酯)、
‑
cf3、
‑
cn等。示例性取代的烷基描述如下。环烷基可以进一步被烷基、烯基、烷氧基、烷硫基、氨基烷基、羰基
‑
取代的烷基、
‑
cf3、
‑
cn等取代。
[0054]
术语“c
x
‑
y”在与化学部分诸如酰基、酰氧基、烷基、烯基、炔基或烷氧基结合使用时是指包括链中含有x
‑
y个碳的基团。例如,术语“c
x
‑
y
烷基”是指取代或未取代的饱和烃基,包括链中含有x
‑
y个碳的直链烷基和支链烷基基团,包括卤代烷基基团,诸如三氟甲基和2,2,
2
‑
三氟乙基等。c0烷基表示氢,其中该基团位于末端位置,如果c0是内部的,则c0表示键。术语“c2‑
y
‑
烯基”和“c2‑
y
‑
炔基”是指取代或未取代的不饱和脂族基团,其长度和可能的取代与上述烷基相似,但分别含有至少一个双键或三键。
[0055]
术语“烷酰基”是指由通式烃基
‑
c(o)
‑
、优选烷基
‑
c(o)
‑
表示的基团。
[0056]
术语“烷氧基”(包括卤代烷氧基的
‘
烷氧基’)是指连接有氧的烷基基团,优选低级烷基基团。在一些实施方案中,优选地,烷氧基为c
l
‑
c5烷氧基,更优选为c
l
‑
c3烷氧基。更具体地,优选的烷氧基包括但不限于,甲氧基、乙氧基和丙氧基。卤素包括但不限于氟化物、氯化物、溴化物和碘化物。优选地,烷酰基为c2‑
c
10
烷酰基,更优选c3‑
c5烷酰基。更具体地,优选的烷酰基包括但不限于乙酰基、丙酰基和环己烷羰基。
[0057]
术语“胺”和“氨基”为本领域公认的并且是指未取代的和取代的胺及其盐,例如可以由如下表示的部分:
[0058][0059]
其中r
10
各自独立地表示氢或烃基,或两个r
10
与所连接的n原子一起得到环结构中具有4
‑
8个原子的杂环。
[0060]
如本文所用,术语“芳基”包括取代或未取代的单环芳族基团,其中环的每个原子均为碳。优选地,该环是5
‑
至10
‑
元环,更优选6
‑
至10
‑
元环或6
‑
元环。术语“芳基”还包括具有两个或更多个环的多环系统,其中两个或更多个碳是两个相邻环共有的,其中环的至少一个为芳族的,例如其他环可以是环烷基、环烯基、环炔基,芳基、杂芳基和/或杂环基。芳基基团包括苯、萘、菲、苯酚、苯胺等。芳基基团上的示例性取代可以包括例如卤素,卤代烷基诸如三氟甲基,羟基,羰基(诸如羧基、烷氧基羰基、甲酰基或酰基诸如烷基c(o)),硫代羰基(诸如硫酯、硫代乙酸酯、或硫代甲酸酯),烷氧基,磷酰基,磷酸酯,膦酸酯,次膦酸酯、氨基,酰氨基,脒,亚胺,氰基,硝基,叠氮基,甲硅烷基醚、巯基,烷硫基,硫酸酯,磺酸酯,氨磺酰基,磺酰氨基,磺酰基,杂环基,芳烷基或芳族或杂芳族部分。
[0061]
如本文所用,术语“卤代”和“卤素”是指卤素,且包括氯、氟、溴和碘。
[0062]
术语“低级”当与化学部分诸如酰基、酰氧基、烷基、烯基、炔基或烷氧基结合使用时,意指包括在取代基中存在十个或更少、优选六个或更少的非氢原子的基团。例如,“低级烷基”是指含有十个或更少、优选六个或更少的碳原子的烷基基团。在某些实施方案中,本文定义的酰基、酰氧基、烷基、烯基、炔基或烷氧基取代基分别为低级酰基、低级酰氧基、低级烷基、低级烯基、低级炔基或低级烷氧基,无论它们单独出现还是与其他取代基组合出现,诸如在叙述中的羟基烷基和芳烷基(在这种情况下,例如,在计数烷基取代基中的碳原子时,芳基基团中的原子不计数在内)中。
[0063]
术语“取代的”是指具有替代主链的一个或多个碳原子上的氢的取代基的部分。应当理解,“取代”或“被取代”包括隐含的条件,即这种取代符合被取代原子和取代基的允许价态,并且该取代产生稳定的化合物,例如它不会自发地发生转化诸如通过重排、环化、消除等发生转化。如本文所用,术语“取代的”预期包括有机化合物的所有允许的取代基。在广泛的方面,允许的取代基包括有机化合物的无环和环状、支链和无支链、碳环和杂环、芳族和非芳族取代基。对于适合的有机化合物,允许的取代基可以是一个或多个并且可以相同
或不同。出于本发明的目的,杂原子诸如氮可以具有氢取代基和/或满足杂原子化合价的本文所述的有机化合物的任何允许的取代基。取代基可包括本文所述的任何取代基,例如,卤素、卤代烷基、羟基、羰基(诸如羧基、烷氧基羰基、甲酰基或酰基)、硫代羰基(诸如硫酯、硫代乙酸酯或硫代甲酸酯)、烷氧基、磷酰基、磷酸酯、膦酸酯、次膦酸酯、氨基、酰氨基、脒、亚胺、氰基、硝基、叠氮基、巯基、烷硫基、硫酸酯、磺酸酯、氨磺酰基、磺酰氨基、磺酰基、杂环基、芳烷基或芳族或杂芳族部分。本领域技术人员将理解,如果适合,取代基本身可以被取代。除非特别说明为“未取代”,否则本文提及的化学部分应理解为包括取代的变体。例如,提及“芳基”基团或部分隐含地包括取代和未取代的变体。
[0064]
本公开内容的术语“药学上可接受的盐”是指由无毒或几乎无毒的酸或碱生产的盐。在本公开内容的化合物为酸性的情况下,本公开内容的化合物的碱加成盐可以通过使化合物的游离碱与足量的所需碱和足够的惰性溶剂反应来制备。药学上可接受的碱加成盐包括但不限于钠、钾、钙、铵、镁或有机氨基形成的盐。在本公开内容的化合物为碱性的情况下,该化合物的酸加成盐可以通过使该化合物的游离碱与足量的所需酸和足够的惰性溶剂反应来制备。药学上可接受的酸加成盐包括但不限于丙酸、异丁酸、草酸、苹果酸、丙二酸、苯甲酸、琥珀酸、辛二酸、富马酸、扁桃酸、邻苯二甲酸、苯磺酸、对
‑
甲苯磺酸、柠檬酸、酒石酸、甲磺酸、盐酸、溴酸、硝酸、碳酸、一氢
‑
碳酸(monohydrogen
‑
carbonic acid)、磷酸、一氢
‑
磷酸、二氢
‑
磷酸、硫酸、一氢
‑
硫酸、碘化氢和亚磷酸。此外,本公开内容的药学上可接受的盐包括但不限于氨基酸的盐(如精氨酸盐)和有机酸的类似物(如葡糖醛酸类似物或半乳糖醛酸类似物)。
[0065]
例如,2
‑
羟基
‑5‑
[2
‑
(4
‑
三氟甲基
‑
苯基)
‑
乙基氨基]
‑
苯甲酸(化合物2)的药学上可接受的盐,即本公开内容的一个优选实例可以通过下列反应方案1制备。然而,通过示例提供下列反应方法,且并不预期限制本公开内容的范围。
[0066]
<反应方案1>
[0067][0068]
在方案1中,m为药学上可接受的金属或碱性有机化合物,诸如二乙胺、锂、钠和钾。
[0069]
更详细地,可以通过将化合物溶于醇,滴加二乙胺,搅拌混合物,真空蒸馏,并通过加入乙醚使残余物结晶来制备二乙胺盐。碱金属盐可通过用无机试剂如氢氧化锂、氢氧化钠、氢氧化钾在如醇、丙酮、乙腈这样的溶剂中制备期望的盐,然后冷冻干燥而制成。另外,根据类似方法,锂盐可以用醋酸锂制备,钠盐可以用2
‑
乙基己酸钠或醋酸钠制备,而钾盐可以用醋酸钾制备。
[0070]
本公开内容的一些化合物可以是水合形式并且可以溶剂化或非溶剂化形式存在。根据本公开内容的部分化合物以晶体形式或无定形形式存在,且任何物理形式均包括在本公开内容的范围中。此外,本公开内容的一些化合物可以含有一个或多个不对称碳原子或双键,且由此以两种或更多种立体异构形式存在,如外消旋体、对映异构体、非对映异构体、
几何异构体等。本公开内容包括所述化合物的这些单独的立体异构体。
[0071]
组合物
[0072]
本公开内容还提供了组合物,其包含由上述化学式(i)表示的5
‑
苄基氨基水杨酸衍生物或其药学上可接受的盐;和药学上可接受的赋形剂或添加剂。本公开内容的上述化学式(i)表示的5
‑
苄基氨基水杨酸衍生物或其药学上可接受的盐可以被单独施用。在一些实施方案中,包含式(i)的化合物的组合物与任意便利的载体、稀释剂等一起被施用。
[0073]
在一些实施方案中,所述组合物包含约1mg
‑
约1,000mg的式(i)的化合物。在一些实施方案中,所述组合物包含约10mg
‑
约1,000mg的式(i)的化合物。在一些实施方案中,所述组合物包含约1mg
‑
约500mg的式(i)的化合物。在一些实施方案中,所述组合物包含约1mg
‑
约100mg的式(i)的化合物。在一些实施方案中,所述组合物包含约2mg
‑
约50mg的式(i)的化合物。
[0074]
在一些实施方案中,用于施用的制剂可以为单剂量单位或多剂量单位。在一些实施方案中,该组合物包含单剂量单位。在一些实施方案中,该组合物包含多剂量单位。
[0075]
可以将本公开内容的用于口服施用的组合物配制成固体或液体形式。固体制剂包括但不限于粉末、颗粒剂、片剂、胶囊剂、栓剂等。此外,固体制剂还可包括但不限于稀释剂、矫味剂、粘合剂、防腐剂、崩解剂、润滑剂、填充剂、增塑剂等。液体制剂包括但不限于溶液诸如水溶液和丙二醇溶液、悬浮液、乳液等,并且可以通过添加适合的添加剂来制备,所述添加剂诸如着色剂、矫味剂、稳定剂、增稠剂等。在一些实施方案中,该组合物以选自胶囊、片剂、粉末和溶液的形式被施用。在一些实施方案中,该组合物通过与膳食补充剂混合被施用。在一些实施方案中,该组合物作为膳食补充剂被施用。在一些实施方案中,该组合物通过与食物混合被施用。在一些实施方案中,该组合物作为食品组合物被施用。在一些实施方案中,该组合物通过溶于水中被施用。在一些实施方案中,该组合物作为胶囊与水一起被施用。在一些实施方案中,该组合物作为咀嚼片被施用。
[0076]
例如,通过将本公开内容的5
‑
苄基氨基水杨酸衍生物与如乳糖、淀粉、微晶纤维素这样的药学上可接受的赋形剂简单混合制成粉末。颗粒剂可以如下制备:将化合物、药学上可接受的赋形剂混合。在一些实施方案中,药学上可接受的赋形剂包含稀释剂和/或药学上可接受的粘合剂。在一些实施方案中,所述粘合剂为聚乙烯吡咯烷酮、羟丙基纤维素等。
[0077]
在一些实施方案中,该组合物通过用如水、乙醇、异丙醇等这样足够的溶剂湿法制粒形成。在一些实施方案中,该组合物通过使用压缩力直接压制形成。此外,可以通过将颗粒与药学上可接受的润滑剂诸如硬脂酸镁混合并将混合物压片来制备片剂。
[0078]
本公开内容的药物组合物可以以但不限于口服制剂、可注射制剂(例如,肌内、腹膜内、静脉内、输注、皮下、植入)、可吸入、鼻内、阴道、直肠、舌下、经皮、局部等形式施用,这取决于待治疗的障碍和动物的状况。可以将本公开内容的组合物配制在包含药学上可接受的和无毒的载体、添加剂和/或媒介物的适合的剂量单位中,它们通常都在本领域中使用,这取决于施用途径。能够在期望的时间内连续释放药物的贮库型制剂也被包括在本公开内容的范围内。
[0079]
在一些实施方案中,所述组合物为胶囊,其包含:
[0080]
约1mg
‑
约1000mg的式(i)的化合物;
[0081]
约50%w/w
‑
约70%w/w的乳糖一水合物;
[0082]
约2%w/w
‑
约8%w/w的交联羧甲基纤维素钠;
[0083]
约0.1%w/w
‑
约1%w/w的硬脂酸镁;和
[0084]
约0.1%w/w
‑
约2%w/w的十二烷基硫酸钠。
[0085]
在一些实施方案中,所述组合物为胶囊,其包含:
[0086]
约1mg
‑
约1000mg的式(i)的化合物;
[0087]
约60%w/w的乳糖一水合物;
[0088]
约5%w/w的交联羧甲基纤维素钠;
[0089]
约0.5%w/w的硬脂酸镁;和
[0090]
约1%w/w的十二烷基硫酸钠。
[0091]
在一些实施方案中,所述组合物为食品组合物,其包含:
[0092]
约1mg
‑
约1000mg的式(i)的化合物;
[0093]
约30%w/w
‑
约50%w/w的淀粉;
[0094]
约15%w/w
‑
约25%w/w的粗蛋白质;
[0095]
约10%w/w
‑
约20%的粗脂肪;
[0096]
约0.1%w/w
‑
约5%w/w的粗纤维;
[0097]
约1%w/w
‑
约10%w/w的粗灰分;
[0098]
约0.1%w/w
‑
约5%w/w的精氨酸;
[0099]
约0.1%w/w
‑
约2.5%w/w的钙;
[0100]
约0.1%w/w
‑
约3%w/w的赖氨酸;
[0101]
约0.1%w/w
‑
约3%w/w的甲硫氨酸 胱氨酸;和
[0102]
约0.1%w/w
‑
约2.5%w/w的磷。
[0103]
在一些实施方案中,所述组合物为食品组合物,其包含:
[0104]
约1mg
‑
约1000mg的式(i)的化合物;
[0105]
约42.7%w/w的淀粉;
[0106]
约21.0%w/w的粗蛋白质;
[0107]
约14%w/w的粗脂肪;
[0108]
约1.9%w/w的粗纤维;
[0109]
约6.1%w/w的粗灰分;
[0110]
约1.4%w/w的精氨酸;
[0111]
约0.75%w/w的钙;
[0112]
约1.1%w/w的赖氨酸;
[0113]
约1.18%w/w的甲硫氨酸 胱氨酸;和
[0114]
约0.5%w/w的磷。
[0115]
在一些实施方案中,所述组合物为膳食补充剂,其包含:
[0116]
约1mg
‑
约1000mg的式(i)的化合物;
[0117]
约5%w/w
‑
约20%w/w的粗蛋白质;
[0118]
约0.1%w/w
‑
约5%w/w的粗脂肪;
[0119]
约0.1%w/w
‑
约5%w/w的粗纤维;
[0120]
约0.1%w/w
‑
约5%w/w的粗灰分;
[0121]
约0%w/w
‑
约1%w/w的钙;
[0122]
约0%w/w
‑
约2%w/w的钾;和
[0123]
约60%w/w
‑
约95%w/w的水。
[0124]
在一些实施方案中,所述组合物为膳食补充剂,其包含:
[0125]
约1mg
‑
约1000mg的式(i)的化合物;
[0126]
约12.0%w/w的粗蛋白质;
[0127]
约1.5%w/w的粗脂肪;
[0128]
约0.4%w/w的粗纤维;
[0129]
约1.5%w/w的粗灰分;
[0130]
约0.02%w/w的钙;
[0131]
约0.1%w/w的钾;和
[0132]
约78.0%w/w的水。
[0133]
在一些实施方案中,所述组合物为咀嚼片,其包含:
[0134]
约1mg
‑
约1000mg的式(i)的化合物;
[0135]
约0.1%w/w
‑
约5%w/w的二氧化硅;
[0136]
约0%w/w
‑
约2%w/w的苯甲酸;
[0137]
约0%w/w
‑
约1%w/w的山梨酸;
[0138]
约0.1%w/w
‑
约10%w/w的硬脂酸镁;
[0139]
约10%w/w
‑
约30%w/w的纤维素;
[0140]
约30%w/w
‑
约50%w/w的鸡肉源(chicken source);
[0141]
约0.1%w/w
‑
约5%w/w的干酵母;和
[0142]
约10%w/w
‑
约30%w/w的葡萄糖。
[0143]
在一些实施方案中,所述组合物为咀嚼片,其包含:
[0144]
约1mg
‑
约1000mg的式(i)的化合物;
[0145]
约3%w/w的二氧化硅;
[0146]
约0.05%w/w的苯甲酸;
[0147]
约0.01%w/w的山梨酸;
[0148]
约5%w/w的硬脂酸镁;
[0149]
约20%w/w的纤维素;
[0150]
约40%w/w的鸡肉粉;
[0151]
约3%w/w的干酵母;和
[0152]
约19%w/w的葡萄糖。
[0153]
本公开内容还提供了5
‑
苄基氨基水杨酸衍生物或其药学上可接受的盐用于治疗动物的认知衰退的用途。即本公开内容提供了用于治疗动物的认知衰退的药物组合物,其包含由上述化学式(i)表示的5
‑
苄基氨基水杨酸衍生物或其药学上可接受的盐。更具体地,5
‑
苄基氨基水杨酸衍生物或其药学上可接受的盐可以用于治疗动物的认知衰退,包括认知功能障碍综合征(例如犬科动物认知功能障碍综合征)、心境恶劣、退化性抑郁症和精神错乱综合征。在一些实施方案中,所述认知衰退由cds导致。
[0154]
在一些实施方案中,所述组合物被用于制备治疗伴侣动物的认知功能障碍综合征
(cds)的药剂。在一些实施方案中,所述组合物被用于制备通过氧化应激和炎症的并发药理学抑制治疗cds的药剂。在一些实施方案中,所述组合物被用于制备通过抑制氧化应激和前列腺素e2合成治疗cds的药剂。在一些实施方案中,所述组合物被用于制备通过抑制氧化应激和微粒体前列腺素e合酶
‑
1治疗cds的药剂。然而,根据本公开内容的5
‑
苄基氨基水杨酸衍生物或其药学上可接受的盐的用途不限于上述具体疾病名称。
[0155]
本公开内容提供了5
‑
苄基氨基水杨酸衍生物或其药学上可接受的盐在制备药物产品中的用途,所述药物产品用于治疗认知和/或神经行为损害,诸如减轻或减缓社交互动的衰退,减少与年龄相关的行为改变,增加训练能力,改善注意力,保持脑功能健康,减少记忆力减退和治疗伴侣动物(诸如犬科动物或猫科动物)的认知衰退。在一些实施方案中,伴侣动物表现出涉及行为改变的症状,其选自食欲、饮行为、发声、排泄行为、睡眠模式、漫无目的行为、适应能力、社交行为、感知能力、定向障碍和记忆力。在一些实施方案中,伴侣动物表现出涉及行为改变的症状,其选自发声、排泄行为、睡眠模式、漫无目的行为、社交行为、感知能力、定向障碍和记忆力。在一些实施方案中,伴侣动物表现出涉及行为改变的症状,其选自睡眠模式、社交行为、定向障碍和记忆力。在一些实施方案中,伴侣动物表现出涉及记忆力中的改变的症状。在一些实施方案中,伴侣动物表现出涉及行为改变的症状,其选自定向(例如茫然地盯着和在家中迷路)、记忆力(例如不认识主人和弄脏房屋)、冷漠(例如减少活动时间和避免与主人接触)、嗅觉损害(例如难以找到食物)和运动。
[0156]
在一些实施方案中,伴侣动物表现出涉及行为改变的症状,其选自空间定向、社交互动、睡眠
‑
觉醒周期和弄脏房屋。
[0157]
在一些实施方案中,伴侣动物表现出病理生理学改变。在一些实施方案中,病理生理学改变选自大脑皮质萎缩;基底神经节萎缩;脑室大小增加;脱髓鞘;神经胶质细胞大小增加;神经胶质细胞数量增加;神经元丢失,尤其是在海马皮层区域;轴索变性;以及β
‑
淀粉样斑块蓄积。在一些实施方案中,病理生理学改变选自神经胶质细胞大小增加;神经胶质细胞数量增加;神经元丢失;和β
‑
淀粉样蛋白沉积增加。
[0158]
为了治疗猫科伴侣动物的认知衰退,本公开内容的化合物可以以大约0.01mg/kg
‑
大约200mg/kg、优选大约0.1mg/kg
‑
大约30mg/kg的剂量每日施用。在一些实施方案中,将式(i)的化合物以约0.1mg/千克体重
‑
约10mg/千克体重的剂量施用。然而,剂量可根据动物的状况(年龄、性别、体重等)、有此需要的动物的疾病严重程度、所用的有效成分、饮食等而改变。本公开内容的化合物如有必要可每天施用一次或以分次剂量一天施用几次。在一些实施方案中,将式(i)的化合物每天施用1、2或3次。在一些实施方案中,将式(i)的化合物每天施用1次。
实施例
[0159]
将化合物2即2
‑
羟基
‑5‑
[2
‑
(4
‑
三氟甲基
‑
苯基)乙基氨基]苯甲酸用作有代表性的化合物。此后,相当详细地描述了本公开内容以有助于本领域技术人员理解本公开内容。然而,通过示例提供下列实施例,而不预期用于限制本公开内容的范围。显而易见的是,可以在不脱离本公开内容精神和范围或牺牲其所有实质性优势(material advantage)的情况下进行各种改变。
[0160]
1.研究设计和受试者
[0161]
在初步数据中,在以2.5mg/kg的剂量口服施用化合物2后,在ad的动物模型(app/ps1小鼠)和肌萎缩侧索硬化的动物模型(g93a小鼠)中显示最大程度的有益作用,诸如认知和运动功能改善。
[0162]
在小鼠中以2.5mg/kg的剂量口服施用化合物2后,将c
max
(平均最大血浆浓度)和auc(血浆水平
‑
时间曲线下的面积)分别测量为5.19
±
0.96μg/ml和9.61
±
1.38μg
·
hr/ml。
[0163]
在剑桥郡,英格兰的大型非临床合同研究组织huntington life science中研究了化合物2在比哥犬中的全身毒性潜能。三组各自包含三个雄性和三个雌性,接受化合物2的剂量为20、65或200mg/kg/天,持续13周。对比哥犬每日口服施用化合物2引起肝和肾中的适应性改变和甲状腺中的继发性发现。尽管接受治疗的动物在给药施用时倾向于挣扎,但是没有毒性证据。主要的治疗相关发现均显示在4周的恢复期内至少部分恢复,其中大多数显示完全恢复。因此,200mg/kg/天被视为狗的未观察到不良作用水平(noael)。
[0164]
在药代动力学研究中,口服施用20mg/kg/天化合物2后,比哥犬的c
max
和auc分别为10.6μg/ml和75.1μg
·
hr/ml。基于化合物2的安全性和药代动力学特性,选择10mg/kg/天的剂量来研究化合物2在犬科动物cds中的安全性和功效。
[0165]
在稳定性试验中,化合物2在25℃下稳定至少60个月。此外,化合物2的胶囊剂和咀嚼剂在25℃下分别稳定至少24和12个月。
[0166]
在本研究中测试的伴侣动物为22只被诊断患有cds的老年狗(12
‑
19岁)。实施例的受试者如表1中所示。参加本研究的每只狗均符合以下标准:体重<12kg(不分性别)、与主人一起生活至少90天的狗、能够口服药物的狗、研究人员诊断患有cds的狗(犬科动物认知功能障碍评分(ccdr)量表≥50分)和获得主人知情同意的狗。妊娠或哺乳、对水杨酸衍生物过敏或患有基础疾病(即肾功能不全、视力丧失、心力衰竭或肾衰竭)的狗被排除在外。此外,在90天内已经参加过任何其他临床试验的狗或不仅患有cds还患有其他神经变性疾病的狗被排除在外。
[0167]
本研究是一项随机、盲法、安慰剂对照的临床试验,以研究化合物2在患有cds的狗中的功效和安全性。为了研究化合物2的功效,评价了两种问卷调查:ccdr量表和犬科动物痴呆量表(cades)。为了测量化合物2的安全性,不仅研究了狗中不良事件的发生,而且还对狗进行了生命体征、体格检查和血液测试。开据化合物2以10mg/kg口服施用的处方,每天一次给药持续8周。经主要研究者批准,受试者3和4额外接受化合物2持续4周。代替化合物2,受试者18
‑
22接受安慰剂持续8周。在本研究中,我们允许以多种方式向狗施用化合物2:与膳食补充剂混合(受试者1和3)、与食物混合(受试者2和6)、溶于水(受试者4)、或与水一起的胶囊(受试者5)或与水一起的咀嚼片(受试者7
‑
22)。
[0168][0169]
表1.实施例的受试者
[0170]
2.患有cds的狗的问卷调查
[0171]
评分量表是用于cds诊断、分期、评估和谨慎监测疾病症状以及用于评价治疗策略的功效的基本工具。在过去十年中已经开发了几种评分量表,例如ccdr量表[21
‑
24]。为了评估本研究中cds的严重程度,口服施用化合物2之前和之后由兽医进行两次问卷调查(ccdr量表和cades)。问卷调查包括测量食欲、饮行为、吠叫、排泄行为、昼/夜睡眠模式、漫无目的行为、适应能力、社交行为、感知能力、定向障碍和记忆力的广泛项目。
[0172]
2.1根据ccdr量表的检查
[0173]
ccdr量表由基于cds症状的13个项目组成(表2)。13种行为包括与定向(茫然地盯着、在家中迷路)、记忆(缺乏对主人的认识、弄脏房屋)、冷漠(减少活动时间、避免与主人接触)、嗅觉损害(难以找到食物)和运动相关的各种问题。这些问题会影响狗的生活质量和狗
‑
主人之间的关系[25,26]。ccdr评分≥50表明老年狗(12
‑
19岁的年龄)出现cds。在本研究中,我们比较了在患有cds的狗中施用化合物2之前和之后的ccdr评分。
[0174]
[0175][0176]
表2.犬科动物认知功能障碍评分(ccdr)量表
[0177]
尽管在本研究中启动了总计22只患有cds的伴侣狗,但17只伴侣狗接受了8周的用化合物2的治疗,并且受试者1和2在施用后7周时经历了衰老依赖性肾毒性和自然死亡。即使在口服施用化合物2后4周,大多数患有cds的伴侣狗在ccdr量表上表现出显著减少的行为倾向,表明接受化合物2治疗的狗在4周内表现出接近正常的认知功能(表3)。此外,大多数狗的异常行为频率降低,且其社交互动得到改善。观察到施用化合物2后改善的ccdr评分长达8周。
[0178][0179]
表3.施用化合物2后受试者的ccdr评分
[0180]
为了确定在药物治疗中断后化合物2的有益作用是否可以维持,在6只伴侣狗中进行了后续研究。在接受用化合物2的8或12周治疗的受试者3、4、7、8、10和11中,在最后一次施用药物后的4或8周内观察到化合物2的有益作用(表4和5)。重要地,社交互动、适当排泄和睡眠
‑
觉醒活动周期中的改变得到显著改善。这意味着化合物2可用于通过改善认知缺陷和减缓疾病进展来治疗cds。
[0181][0182][0183]
表4.施用和中断化合物2后受试者的ccdr评分
[0184][0185]
表5.施用和中断化合物2后受试者的ccdr评分
[0186]
2.2根据cades的检查
[0187]
为了确保和证实ccdr量表,我们使用了额外的问卷调查cades,它含有分布在四个区域中的17个项目,与狗的行为改变相关:空间定向、社交互动、睡眠
‑
觉醒周期和弄脏房屋(表6)[3]。根据认知损害的不同阶段,可将其分为轻度、中度和重度认知损害。众所周知,cades也适合用于长期评估犬科动物认知损害的进展,并可能作为治疗的功效读数。
[0188]
[0189]
[0190][0191]
表6.犬科动物痴呆量表(cades)
[0192]
空间定向和变化的评分在表7中给出。在施用后4周时,17只伴侣狗中有10只(59%)表现出其空间定向障碍得到改善。受试者3、4和10在空间定向项目中表现出几乎正常的行为。在15只伴侣狗中的9只(60%)中,在口服施用化合物2后的8周时观察到有益效果。总之,这些结果表明化合物2改善了患有cds的狗的空间定向能力。
[0193][0194][0195]
表7.施用化合物2后的0、4和8周时受试者空间定向(项目1
‑
5)的cades评分
[0196]
cades中的社交互动评分如表8中所示。在施用化合物2持续4周后,除了受试者5、
8、11、12、14和17外,大多数参与的狗的社交互动显著改善。尽管3只狗(受试者3、4和10)在用化合物2治疗前已经表现出严重的异常社交行为,但在治疗后4周时它们的社交行为与正常老年狗几乎相似。此外,大多数狗在化合物2治疗后8周时表现出改善的社交活动。更重要地,与施用化合物2后4周时的改善相比,在施用化合物2后8周时15只伴侣狗中有8只(53%)表现出进一步的社交互动改善。总之,这些结果表明化合物2改善了患有cds的狗的社交互动活动。
[0197][0198][0199]
表8.施用化合物2后的0、4和8周时受试者社交互动(项目6
‑
10)的cades评分
[0200]
表9中量化了cades中睡眠
‑
觉醒周期的改变。在施用化合物2之前,除受试者14外,所有狗在睡眠
‑
觉醒周期(项目11)方面均存在严重的异常行为,但在施用化合物2后的8周
时,15只伴侣狗中有10只(67%)具有显著性改善。同时,在17只伴侣狗中的14只(82%)中观察到从失眠转变为嗜睡(项目12),但施用化合物2后所述异常改变几乎消失。
[0201][0202][0203]
表9.施用化合物2后的0、4和8周时受试者睡眠
‑
觉醒周期(项目11
‑
12)的cades评分
[0204]
弄脏房屋的频率如表10中所示。在化合物2施用8周后,除受试者4、12、13和17外,所有受试者的弄脏房屋行为均减少。特别是,受试者3、5和10在施用化合物2后8周时未表现出弄脏行为。
[0205][0206][0207]
表10.施用化合物2后的0、4和8周时受试者弄脏房屋(项目13
‑
17)的cades评分
[0208]
总cades评分显示在表11中。该评分揭示出,除受试者9外,所有患有cds的伴侣狗的认知功能障碍行为均在施用化合物2后逐步减轻。在口服施用化合物2后8周时,观察到认知功能由重度到中度、弱或正常水平的显著改善。
[0209][0210]
表11.施用化合物2后的0、4和8周时受试者的总cades评分
[0211]
甚至在中断施用后的接下来的4或8周内观察到化合物2在6只伴侣狗(受试者3、4、7、8、10和11)中的有益作用(表12和13)。用化合物2治疗后,睡眠模式、弄脏房屋、社交互动和行为活动得到显著性改善。此外,受试者对其主人变得更加顺从,并且表现出攻击性降低。这些结果暗示可以施用化合物2以在犬科动物cds中减轻认知损害和减缓疾病进展。
[0212][0213]
表12.施用和中断化合物2后受试者的总cades评分
[0214][0215]
表13.施用和中断化合物2后受试者的总cades评分
[0216]
2.3接受安慰剂的狗中ccdr和cades的结果
[0217]
为了阐明化合物2对认知损害的影响,5只患有cds的狗(受试者18
‑
22)接受安慰剂。大多数接受安慰剂的狗的ccdr和cades评分在安慰剂治疗后的8周时未显示显著性改变或增加,表明安慰剂治疗不影响认知功能。总之,强烈暗示可以施用化合物2来减轻犬科动物cds的认知损害。
[0218][0219][0220]
表14.施用安慰剂后受试者的ccdr评分
[0221][0222]
表15.施用安慰剂后受试者的总cades评分
[0223]
3.患有cds的狗中的安全性评估
[0224]
在本研究期间,在每次访视时评价化合物2在患有cds的狗中的安全性。作为结果,在血液毒性试验中没有观察到显著性改变,也没有发生与治疗相关的不良事件。
[0225]
4.结论
[0226]
使用两个问卷调查来评价化合物2对患有cds的伴侣狗的认知功能的影响。在ccdr量表中,化合物2的施用实质上改善了认知功能,认知功能几乎恢复到正常评分。与ccdr量表一致,在患有cds的狗中的重度认知和神经行为损害在施用化合物2后8周内显著缓解。在完成化合物2的8或12周施用后,这些有益效果在4或8周内得以维持。此外,在本研究期间没有观察到不良事件或毒性。另一方面,安慰剂组中没有显著改善。综上所述,这些发现强烈暗示化合物2可用于治疗犬科动物和猫科动物中的cds。
[0227]
工业实用性
[0228]
本公开内容提供了包含化合物2的组合物和施用治疗有效量的化合物2用于治疗犬科动物或猫科动物的神经系统疾病中的认知和神经行为损害的方法,所述神经系统疾病中的认知和神经行为损害包括cds、心境恶劣、退化性抑郁症和精神错乱综合征。本公开内容的组合物和方法对于减轻或减缓犬科动物或猫科动物与年龄相关的神经系统疾病中的认知和神经行为损害非常有用。
[0229]
其他出版物
[0230]
1.azkona,g.等人,prevalence and risk factors of behavioural changes associated with age
‑
related cognitive impairment in geriatric dogs.j small anim pract,2009.50(2):p.87
‑
91.
[0231]
2.neilson,j.c.等人,prevalence of behavioral changes associated with age
‑
related cognitive impairment in dogs.j am vet med assoc,2001.218(11):p.1787
‑
91.
[0232]
3.madari,a.等人,assessment of severity and progression of canine cognitive dysfunction syndrome using the canine dementia scale(cades).appl anim behav sci.,2015.171:p.138
‑
45.
[0233]
4.salvin,h.e.等人,under diagnosis of canine cognitive dysfunction:a cross
‑
sectional survey of older companion dogs.the veterinary journal,2010.184(3):p.277
‑
281.
[0234]
5.hart,b.l.和l.a.hart,selecting,raising,and caring for dogs to avoid problem aggression.journal of the american veterinary medical association,1997.210(8):p.1129.
[0235]
6.landsberg,g.m.,j.nichol和j.a.araujo,cognitive dysfunction syndrome:a disease of canine and feline brain aging.vet clin north am small anim pract,2012.42(4):p.749
‑
68,vii.
[0236]
7.landsberg,g.m.,t.deporter和j.a.araujo,clinical signs and management of anxiety,sleeplessness,and cognitive dysfunction in the senior pet.vet clin north am small anim pract,2011.41(3):p.565
‑
90.
[0237]
8.gonzalez
‑
martinez,a.等人,effect of age and severity of cognitive dysfunction on two simple tasks in pet dogs.vet j,2013.198(1):p.176
‑
81.
[0238]
9.cummings,b.j.等人,β
‑
amyloid accumulation correlates with cognitive dysfunction in the aged canine.neurobiology of learning and memory,1996.66(1):p.11
‑
23.
[0239]
10.cummings,b.j.等人,β
‑
amyloid deposition and other measures of neuropathology predict cognitive status in alzheimer's disease.neurobiology of aging,1996.17(6):p.921
‑
933.
[0240]
11.cummings,b.j.等人,diffuse plaques contain c
‑
terminal aβ42 and not aβ40:evidence from cats and dogs.neurobiology of aging,1996.17(4):p.653
‑
659.
[0241]
12.ozawa,m.等人,the relation between canine cognitive dysfunction and age
‑
related brain lesions.j vet med sci,2016.78(6):p.997
‑
1006.
[0242]
13.rofina,j.等人,cognitive disturbances in old dogs suffering from the canine counterpart of alzheimer's disease.brain research,2006.1069(1):p.216
‑
226.
[0243]
14.head,e.等人,visual
‑
discrimination learning ability and β
‑
amyloid accumulation in the dog.neurobiology of aging,1998.19(5):p.415
‑
425.
[0244]
15.tapp,p.d.等人,frontal lobe volume,function,and β
‑
amyloid pathology in a canine model of aging.journal of neuroscience,2004.24(38):p.8205
‑
8213.
[0245]
16.druce,k.,canine cognitive dysfunction
–
recognition and treatment.veterinary nursing journal,2014.29(8):p.268
‑
270.
[0246]
17.ruehl,w.等人,canine cognitive dysfunction as a model for human age
‑
related cognitive decline,dementia and alzheimer's disease:clinical presentation,cognitive testing,pathology and response to 1
‑
deprenyl therapy,in progress in brain research.1995,elsevier.p.217
‑
225.
[0247]
18.head,e.等人,spatial learning and memory as a function of age in the dog.behavioral neuroscience,1995.109(5):p.851.
[0248]
19.campbell,s.,a.trettien和b.kozan,a noncomparative open
‑
label study evaluating the effect of selegiline hydrochloride in a clinical setting.vet ther,2001.2(1):p.24
‑
39.
[0249]
20.shin,j.h.等人,concurrent blockade of free radical and prostaglandin e synthase
‑1‑
mediated pge2 production improves safety and efficacy in a mouse model of amyotrophic lateral sclerosis.journal of neurochemistry,2012.122(5):p.952
‑
961.
[0250]
21.colle,m.a.等人,vascular and parenchymal abeta deposition in the aging dog:correlation with behavior.neurobiol aging,2000.21(5):p.695
‑
704.
[0251]
22.pugliese,m.等人,severe cognitive impairment correlates with higher cerebrospinal fluid levels of lactate and pyruvate in a canine model of senile dementia.prog neuropsychopharmacol biol psychiatry,2005.29(4):p.603
‑
10.
[0252]
23.schneider,b.m.和m.h.erhard,[canine cognitive dysfunction syndrome:prevalence,diagnosis and therapeutic measures].tierarztl prax ausg k kleintiere heimtiere,2010.38(2):p.113
‑
8.
[0253]
24.salvin,h.e.等人,the canine cognitive dysfunction rating scale
(ccdr):a data
‑
driven and ecologically relevant assessment tool.vet j,2011.188(3):p.331
‑
6.
[0254]
25.hughes,c.p.等人,a new clinical scale for the staging of dementia.br j psychiatry,1982.140:p.566
‑
72.
[0255]
26.swan,g.e.和d.carmelli,impaired olfaction predicts cognitive decline in nondemented older adults.neuroepidemiology,2002.21(2):p.58
‑
67.
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。