自顶向下抗体分析中的背景减少
1.相关申请
2.本技术要求于2019年5月13日提交的美国临时申请第62/847,130号的优先权的权益,该申请的全部内容通过引用并入本文。
技术领域
3.本发明涉及在完整抗体的质谱分析中利用电子捕获解离(ecd)的方法和装置。
背景技术:
4.质谱法(ms)是一种用于确定测试物质的元素组分的分析技术,其具有定量应用和定性应用二者。例如,ms能够用于识别未知化合物和/或通过观察特定化合物的碎裂来确定其结构。最近,由于ms策略在表征和识别肽和蛋白质方面的速度、特异性和灵敏度,ms在蛋白质组学中发挥了越来越重要的作用。
5.在基于ms的蛋白质组学中表征蛋白质的一种策略是“自底向上”方法,其中感兴趣的(一种或多种)蛋白质经受酶消化(例如,通过胰蛋白酶、lysc等)并在使肽片段经受ms分析(ms1)或串联ms/ms分析(ms2)之前经受一次或多次分离(例如,多维lc)。在“自底向上”的ms2工作流程中,碰撞诱导解离(cid)通常用于将在第一个ms阶段中选择的前体肽片段进一步解离为产物离子片段。然后可以从产物离子片段的质量推导出前体肽离子的氨基酸序列。在cid中,电离的前体离子与惰性中性气体和/或氮分子之间的高能碰撞会振动并最终解离(裂解)主链酰胺键,从而产生b型(n端)和y型(c端)产物离子。通过识别几种产物离子肽,可以确定原始蛋白质(例如,通过参照蛋白质或基因组数据库中的已知序列)。然而,由于cid反应通常只发生在最弱的肽酰胺键处,因而沿肽主链的不完全碎裂会使肽序列的完全重建困难。在蛋白质组学中使用cid的另一个关键限制是解离期间翻译后修饰(ptm)的丢失。通常仅微弱结合到肽主链的ptm(例如,磷酸化或硫酸化的官能团)会在碎裂期间从肽剥离,从而阻止在ms2谱中检测和表征ptm。
6.与上述“自底向上”方法相反,替代的基于ms的蛋白质组学策略利用“自顶向下”分析,其中完整蛋白质代为经受质谱仪中的利用例如离子
‑
离子相互作用的解离。虽然传统cid通常解离太少位点而无法提供完全信息来表征完整蛋白质的整个氨基酸序列,但离子
‑
离子相互作用可由于肽主链的更完全碎裂而对于完整蛋白质的“自顶向下”测序更有效。然而,“自顶向下”方法的一个可能障碍是电离后各种多电荷前体的质量的广泛分布以及ms2谱的复杂性。此外,真实世界的应用涉及复杂的未知样品,这会进一步增加ms2谱分析的模糊性。
7.因此,仍然需要用于利用自顶向下方法对抗体进行质谱分析的改进的方法和装置。
技术实现要素:
8.根据本教导的各种方面,本文提供了用于执行抗体的自顶向下的基于ms的分析的
方法和系统。在某些方面中,该方法包括利用离子源从包含至少一种完整抗体的样品产生多种离子,并在对四极杆组施加rf信号的同时并且在不存在分辨dc电压的情况下将所述多种离子传输通过四极杆组,以便优先将具有比约1500m/z的低质量截止大的m/z值的前体离子从四极杆组传输到ecd单元。然后在ecd单元中对前体离子执行ecd反应,并检测来自ecd反应的反应产物。在各种实施方式中,四极杆组包括三重四极中的q1。在某些方面中,调整rf信号的幅度和/或频率以使得低质量截止为约1700m/z。可替代的,调整rf信号的幅度和/或频率以使得低质量截止为约2000m/z。在一些方面中,反应产物的至少一部分具有低于低质量截止的m/z。
9.在一些实施方式中,执行ecd反应包括在传输所述前体离子通过ecd单元的同时将电子引入到ecd单元中。
10.在某些方面中,多种前体抗体离子包括多种电荷态。例如,在某些方面中,多种前体抗体离子可以包括抗体物种相同但表现出在从约2000至约4000的范围内的至少两个不同m/z的抗体。
11.在本教导的各种方面中,提供了一种质谱仪系统,该质谱仪系统包括:离子源,用于从包含完整抗体的样品产生多种离子;四极杆组,沿中心纵轴延伸并被配置为通过入口端从所述离子源接收所述多种离子并通过出口端传输所述离子的至少一部分,四极杆组包括围绕并平行于中心纵轴设置的第一对伸长杆和第二对伸长杆;ecd单元,用于接收从四极杆组传输的离子,并且从四极杆组接收的所述离子在ecd单元内与电子反应以从其产生产物离子;以及检测器,用于检测所述产物离子。电耦接到四极杆组的电力系统被配置为在不存在分辨dc电压的情况下向四极杆组提供rf信号,以便基本上阻止具有比约1500m/z的低质量截止小的m/z值的离子从四极杆组传输到ecd单元。在一些实施方式中,低质量截止可以高于1500m/z。例如,在一些实施方式中,电力系统被配置为在不存在分辨dc电压的情况下向四极杆组提供rf信号,以便基本上阻止具有比约1700m/z的低质量截止小的m/z值的离子从四极杆组传输到ecd单元。在其他实施方式中,电力系统被配置为在不存在分辨dc电压的情况下向四极杆组提供rf信号,以便基本上阻止具有比约2000m/z的低质量截止小的m/z值的离子从四极杆组传输到ecd单元。此外,该系统可以包括控制器以调整低质量截止。例如,在一些实施例中,控制器被配置为增加rf信号的幅度以增加低质量截止。在各种实施方式中,rf信号的幅度在从约0.1kv
p
‑
p
到约10kv
p
‑
p
的范围内。
12.在一些实施方式中,四极杆组包括q1。另外,在一些方面中,四极杆组被容纳在维持在小于约1
×
10
‑4托的压强处的腔室内。系统中包括电子源,用于将电子引入到ecd单元中。
13.在各种方面中,完整抗体可以具有在从约2000至约4000的范围内的m/z。另外,在一些实施方式中,所述产物离子的至少一部分具有低于所述低质量截止的m/z。
14.上述特征中的每一个可以以各种方式与所描述的具体实施例配对和/或组合和/或去除,以得到应被认为在本教导的范围内的替代实施例。
15.申请人的教导的这些和其他特征在本文中被阐述。
附图说明
16.参照附图,通过以下进一步的描述,将更充分地理解本发明的前述和其他目的和
优点。本领域技术人员将理解,以下描述的附图仅用于说明目的。附图不旨在以任何方式限制申请人的教导的范围。
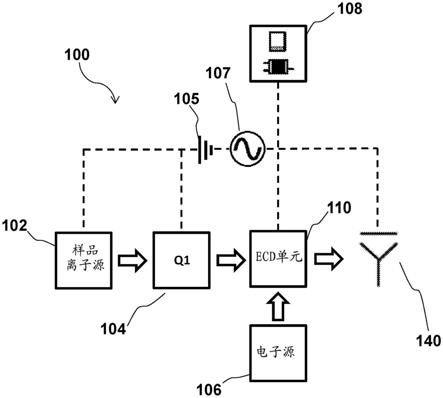
17.图1示意性地描绘了根据申请人的教导的各种方面的示例性ecd
‑
质谱仪系统。
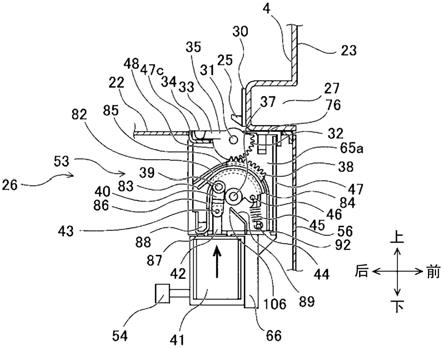
18.图2示意性地描绘了根据本教导的各种方面的适合于在图1的系统中使用的示例性四极。
19.图3示意性地描绘了根据本教导的各种方面的以仅rf模式操作的图2的示例性四极。
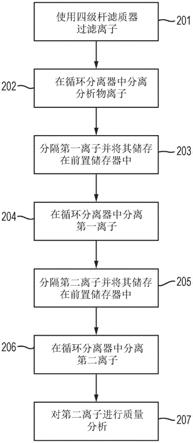
20.图4描绘了根据本教导的各种方面的用于执行抗体的基于ecd的自顶向下分析的示例性方法的流程图。
21.图5a
‑
图5c描绘了根据本教导的待分析的包含抗体的样品的示例性质谱。
具体实施方式
22.将理解,为了清楚起见,以下讨论将说明申请人的教导的实施例的各种方面,同时在任何方便或适当的地方省略某些具体细节。例如,在替代实施例中对相似或类似特征的讨论可以有所简化。为简洁起见,也可以不详细讨论众所周知的想法或概念。本领域技术人员将认识到,申请人的教导的一些实施例可以不需要在每个实施方式中的某些具体描述的细节,在本文中阐述这些细节只是为了提供对实施例的透彻理解。类似地,将清楚的是,所描述的实施例可以易于根据公知常识而改变或变化,而不脱离本公开的范围。以下对实施例的详细描述不应被视为以任何方式限制申请人的教导的范围。如本文所用的,术语“约”和“基本上相等”是指例如通过以下而可能发生的数值量的变化:真实世界中的测量或处理过程;这些过程中的疏忽错误;组合物或试剂的制造、来源或纯度的差异等。通常,如本文所用的术语“约”和“基本上”意指比所述值或值的范围大或小所述值的1/10,例如
±
10%。例如,约30%或基本上等于30%的浓度值可表示介于27%和33%之间的浓度。该术语还指本领域技术人员将认识到是等效的变化,只要这样的变化不包括现有技术实践的已知值。
23.在各种方面中,本文提供了用于分析离子以便能够对完整抗体进行基于ecd的自顶向下分析的方法和系统。基于ms的蛋白质组学的常规方法可由于干扰物种以及不同电荷态的多电荷前体离子的存在而导致复杂和/或不准确的数据,而本教导可导致不太复杂的质谱,同时利用ecd的高解离效率产生抗体离子的完全序列。如下文详细讨论的,本文公开的方法和系统的各种方面选择性地阻止表现出低于低质量截止(lmco)的m/z的离子进入ecd单元,并允许由完整抗体形成的离子的传输,而不管它们的电荷态如何。
24.虽然本文描述的系统、设备和方法可以与具有比所描绘的部件更少、更多或不同的部件的许多不同的质谱仪系统结合使用,但是在图1中示意性地图示了根据本教导使用的示例性质谱仪系统100。如图1中描绘的示例性实施例所示,质谱仪系统100通常包括:样品离子源102,用于电离包含或怀疑包含一种或多种感兴趣抗体的样品,从而从其产生多种前体离子;以及四极杆组104,用于从离子源102接收所产生的离子,然后将所产生的离子的一部分传输到ecd反应单元110。ecd单元110包括相互作用区域,在该相互作用区域内前体阳离子与由电子源106产生的电子相互作用以将前体离子解离成由检测器140检测的多种产物离子。如图1所示,示例性质谱仪系统100另外包括一个或多个电源(例如,dc电源105和rf电源107),电源由控制器108控制以便施加具有rf、ac和/或dc分量的电势至各种部件的
电极,从而以协调方式和/或针对各种不同的操作模式配置质谱仪系统100的元件。如下文详细讨论的,在本教导的示例性实施方式中,施加到四极杆组104的电信号被设置和/或调整以优先将具有大于lmco(例如,约1500m/z)的m/z值的那些前体离子传输到ecd单元110。在特定实施方式中,表现出幅度和频率的rf信号被施加到四极杆组的各个杆,并且在这些杆没有dc分辨电压的情况下,选择该幅度和该频率以便基本上阻止具有低于lmco的m/z值的离子被传输到下游元件,从而消除这些低m/z离子以防干扰在抗体前体离子在ecd单元110中反应后通过检测产物离子产生的ms2谱的后续分析和/或解释。
25.离子源102可以具有各种配置,但通常被配置为从包含在样品中的抗体产生离子(例如,阳离子)。在某些实施方式中,根据本教导使用的合适的样品源被配置为包含样品(例如,包含或怀疑包含感兴趣的抗体的溶液)和/或将样品引入至离子源102,例如,经由流体耦接以便通过一个或多个导管、通道、管、管道、毛细管等将液体样品传输到离子源102。作为非限制性示例,样品源包括待分析的样品的储存器或通过其注入样品的输入端口。在一些方面中,例如,样品源包括用于使样品连续流入离子源102的输液泵(例如,注射泵)。可替代地,同样作为非限制性示例,待分析的液体样品是以来自在线液相色谱柱的洗脱液的形式,但在某些方面中,一个或多个样品制备步骤(例如,多维lc分离、电泳、二硫键还原等)可以离线执行。
26.在本教导的一些示例性方面中,离子源102包括与样品源直接或间接流体连通的导管,该导管终止于至少部分地延伸到电离腔室中的出口端。在液体样品从出口端排放到电离腔室中(例如,作为多个微滴)时,包含在微滴内的抗体(和其他干扰分析物)被离子源102电离(即,带电)。在液滴内的液体(例如,溶剂)蒸发时,离子被释放并被拉向并穿过孔以传输至四极杆组104和ecd单元110。将理解,本领域中已知并根据本文的教导修改的多种不同设备可以用作离子源102。作为非限制性示例,离子源102可以是电喷雾电离设备、雾化器辅助电喷雾设备、化学电离设备、雾化器辅助原子化设备、光电离设备、激光电离设备、热喷雾电离设备、声波喷雾电离设备。
27.如图1的实施方式中所示,系统100包括ecd单元110,在该单元中由四极杆组104传输的前体离子可以经受ecd反应。ecd反应通常涉及多质子化分子m与自由电子相互作用以形成带奇数个电子的自由基物种:
28.[m nh]
n
e
‑
→
[m nh]
(n
‑
1)
·
→
ecd片段
[0029]
向前体抗体阳离子的不完全分子轨道添加电子释放结合能,该结合能如果足以超过解离阈值则会如本领域已知的那样引起电子受体离子的碎裂。一旦前体离子在ecd单元110内发生反应,片段或产物离子就可以在检测器110检测ecd产物离子之前被转移到一个或多个质量分析器以进行进一步分析。例如,设置在ecd单元110和检测器140之间的质量分析器可以包括任何合适的质谱仪模块,包括但不限于例如飞行时间(tof)质谱模块、四极质谱模块、线性离子阱(lit)模块等,用于从中扫描产物离子。作为非限制性示例,ecd反应可以在名称为“inline ion reaction device cell and method of operation”的pct公开第wo2014191821号中描述的ecd设备中进行,该pct公开的教导通过引用而整体并入。为符合向ecd单元110提供电子以进行ecd反应的需要,系统100另外包括电子源106。本领域技术人员将理解,适用于质谱仪系统以提供用于离子
‑
离子反应的电子并根据本教导修改的任何电子源可用于系统100中。作为非限制性示例,电子可以由灯丝(例如钨、钍钨等)或另一
电子发射器(例诸如y2o3阴极)产生。在示例性操作中,可以施加1至3a的电流来加热电子源,电子源产生1至10w的热功率以产生电子。将理解的是,在一些方面中,电子源106可以另外与磁场发生器(例如,永久钕磁体或电磁体,未示出)相关联以控制ecd单元110内的电子的路径,以及与冷却机制(例如,散热器、主动冷却)相关联以保持磁体(如果存在)的温度低于其居里温度(在居里温度处永磁体的磁化丧失)。也可以利用冷却磁体的其他已知方法。
[0030]
如图所示,系统100包括检测器140(例如,飞行时间质量分析器,离子阱质量分析器,法拉第杯或其他离子电流测量设备)以有效地检测从ecd单元110传输的前体和/或产物离子。检测到的离子数据可以存储在存储器中并由计算机或计算机软件分析。
[0031]
如本领域技术人员将理解的,系统100可以另外包括设置在四极杆组104和ecd单元110的上游或下游的任何数量的附加质量分析器元件或离子光学元件,以用于进一步的离子处理、操纵和/或质量分析。举例来说,离子可以被运输通过一个或多个附加的差分泵送真空级(例如,维持在大约2.3托的压强处的第一级,维持在大约6毫托的压强处的第二级,以及维持在大约10
‑5托的压强处的第三级,其中第三个单元包含检测器140和两个或多个四极质量分析器,并且ecd单元110位于其间)。例如,在一个实施例中,四极杆组104代表q1(维持在小于约1
×
10
‑4托的压强处)并且ecd单元110代表或替代q
‑
q
‑
q三重四极质谱仪内的q2(参见例如baba等人,“electron capture dissociation in a radio frequency ion trap,”anal.chem.2004年8月1日;76(15):4263
‑
6,以及名称为“inline ion reaction device cell and method of operation”的pct公开第wo2014191821号,这些描述ecd设备的示例性参考文献中的每一个的教导都通过引用而整体并入)。
[0032]
如图所示,所描绘的系统100另外包括控制器108,该控制器108可操作地耦接到系统100的元件中的一个或多个以控制其操作。举例来说,控制器108可以包括用于处理信息的处理器、用于存储质谱数据和要执行的指令的数据存储装置。如下文详细讨论的以及如本领域公知并根据本教导修改的,举例来说,控制器108可以控制样品离子源102产生离子和电子源106产生电子和/或经由将一个或多个rf/dc电压施加到四极杆组104和ecd单元110的电极来控制离子移动进入并通过四极杆组104和ecd单元110。将理解,虽然控制器108被描绘为单个部件,但是一个或多个控制器(无论是本地的还是远程的)可以被配置为使质谱仪系统100根据本文所述的任何方法进行操作。此外,在一些实施方式中,控制器108可以可操作地与诸如显示器(例如,用于向计算机用户显示信息的阴极射线管(crt)或液晶显示器(lcd))之类的输出设备以及/或者包括字母数字和其他键和/或光标控制以向处理器传送信息和命令选择的输入设备相关联。与本教导的某些实施方式一致,控制器108执行例如包含在数据存储装置中或者从诸如存储设备(例如,盘)之类的另一计算机可读介质读入存储器中的一个或多个指令的一个或多个序列。一个或多个控制器可以采用硬件或软件的形式,例如,控制器108可以采用其中存储有计算机程序的适当编程的计算机的形式,该计算机程序被执行以使质谱仪系统100如本文中另外描述的那样操作,但是本教导的实施方式不限于硬件电路和软件的任何特定组合。例如,与控制器108相关联的各种软件模块可以执行可编程指令以执行下面参照图4描述的示例性方法。
[0033]
如上所述,示例性质谱仪系统100包括一个或多个电源,该一个或多个电源由控制器108控制以便将具有rf、ac和/或dc分量的电势施加到各种部件的电极以将质谱仪系统100的元件配置为协调的方式和/或用于各种不同的操作模式,如本文另外讨论的。现在参
照图2,示例性四极杆组104包括围绕并平行于从入口端(例如,朝向离子源)延伸到出口端(例如,朝向ecd单元)的中心纵轴(z)设置的四个杆104a
‑
104d。杆104a
‑
104d包括与中心轴(z)等距设置的具有圆柱形形状(即,半径为r的圆形横截面,如图2所示)的杆,其中杆104a
‑
104d中的每个杆在尺寸和形状方面彼此相同。杆104a
‑
104d中的每个杆与中心轴(z)之间的最小距离由距离r0定义,使得每个初级杆104a
‑
104d的最内表面和其杆对中的另一个杆的最内表面跨中心纵轴(z)分离2r0的最小距离。在一些示例性实施方式中,杆组104的r0在约从3mm至约10mm的范围内。将理解,虽然杆104a
‑
104d被描绘为圆柱形,但是杆104a
‑
104d的横截面形状、尺寸和/或相对间距可以如本领域已知的那样变化。例如,在一些方面中,杆104a
‑
104d可以根据公式表现出径向内部双曲表面,其中r0(场半径)是电极之间的内切圆的半径以便产生四极场。
[0034]
杆104a
‑
104d是导电的(即,它们可以由诸如金属或合金之类的任何导电材料制成)并且可以耦接到电力系统(包括图1的一个或多个电源105、107)以使得一个或多个电信号可以被单独或组合地施加到每个杆104a
‑
104d。特别地,杆104a
‑
104d通常包括两对杆(例如,包括杆104a和104c的第一对以及包括杆104b和104d的第二对),其中每对杆设置在中心轴(z)的相对侧上并且可以对每对杆施加相同的电信号。例如,在如图2所示的一些方面中,电力系统可以包括:电耦接到第一对杆104a、104c的电源106a以便向第一对杆104a、104c施加相同的电势;以及电耦接到第二对杆104b、104d的电源106b以便向第二对杆104b、104d施加不同的电信号。如图2所示,在一些实施方式中,示例性电力系统可以向第一对杆104a、104c施加[u
‑
vcosωt]的电势,其中u是dc电信号的量值,v是ac信号或rf信号的零到峰幅度,ω是ac信号或rf信号的频率,并且t是时间。类似地,示例性电力系统可以向第二对杆104b、104d施加
‑
[u
‑
vcosωt]的电势。在该示例性配置中,施加到第一对杆104a、104c的电信号和施加到第二对杆104b、104d的电信号的不同在于dc信号的极性(即u的符号),同时电信号的rf部分将彼此异相180
°
。因此本领域技术人员将理解,四极杆组104在一些方面中可以被认为是四极质量过滤器,其能够通过dc/rf比的合适选择来选择性地传输所选m/z范围的离子。例如,考虑单独施加到四个初级杆104a
‑
104d的dc电信号(即,
±
u),如图2所示注入到四极杆组104中的阳离子将基于向第一对电极104a、104c施加正dc电压而受到在x
‑
z平面中的稳定力(朝向中心轴z),同时阳离子将基于向第二对电极104b、104d施加负dc电压而受到在y
‑
z平面中的去稳定力。单独考虑rf信号的影响,当施加到杆对的rf信号随时间变化时,阳离子将依次被各个杆对104a、104c和104b、104d吸引和排斥。因为低m/z的阳离子更容易能够跟随场的交替分量,所以低m/z阳离子将倾向于更多地与rf信号保持同相,从场中获得能量,并以越来越大的幅度振荡,直到它们遇到杆104a
‑
104d中的一个并放电。现在,考虑到组合的dc信号和rf信号的影响,将理解,x
‑
z平面中的场将用作高通质量过滤器,因为只有高m/z的离子将被传输到四极的另一端而不撞击第一对电极104a、104c。另一方面,在y
‑
z平面中,由于负dc电压的散焦/吸引效应,因而高m/z的阳离子将不稳定,但是如果rf分量的幅度被设置为无论何时阳离子的偏差增加都校正轨迹则一些较低m/z的离子可以被rf分量稳定。因此,可以说y
‑
z平面中的场用作低通质量过滤器,因为只有较低m/z的离子将被传输到四极杆组104的另一端而不会撞击第二对杆104b、104d。
[0035]
通过施加到四极杆组104的电信号的rf/dc比的合适选择,在x
‑
z平面中和y
‑
z平面中的上述两个效应一起提供能够分辨个别原子质量的质量过滤器,如在以下参数的示例性
内插mathieu稳定性图中描述的:
[0036][0037][0038]
其中e是电子上的电荷,u是dc电压的幅度,v是施加的零到峰rf电压,m是离子的质量,r0是杆104a
‑
104d之间的有效半径,并且ω是施加的rf频率。应当注意的是,参数a和q分别与dc电压u和rf电压v成比例,并且在mathieu稳定性图中的稳定性边界处q=0.908。
[0039]
如上所述,示例性质谱仪系统100包括一个或多个电源,该一个或多个电源由控制器108控制以便将具有rf、ac和/或dc分量的电势施加到各种部件的电极以将质谱仪系统100的元件配置为协调的方式和/或用于各种不同的操作模式,如本文另外讨论的。虽然图2描绘了在质量过滤器实施期间将dc信号(即,
±
u)和rf信号(即,
±
[u
‑
vcosωt])二者均施加到四极杆组104的杆104a
‑
104d(例如,通过斜升u和v),但本教导提供了其中在建立lmco和高于lmco m/z的离子的优先传输的时段期间在没有dc分辨电压的情况下将电信号施加到四极杆组104的各个杆的系统和方法。现在参照图3,四极杆组104以这样的仅rf配置示出,其中具有大于lmco的m/z的那些离子被优先传输到ecd单元110用于进一步处理,如本文另外讨论的。即,如图3所示,dc信号(u)被设置为0v,使得公式(1)中的参数a变为零。在其中表现出峰到峰幅度(v)和频率(ω)的仅rf信号被施加到各个杆104a
‑
104d的这些条件下,如图3的内插mathieu稳定性图所示,质量扫描线变为水平,使得进入四极杆组104且在q
max
=0.908处及以下稳定的离子被选择性地传输到ecd110。换言之,通过重新布置上述公式(2)并用0.908代替q,根据下式的m/e
lmco
代表由四极杆组104传输的最低质荷比的离子:
[0040][0041]
通过根据本教导的各种方面适当选择施加到四极杆组104的rf幅度(v)和频率(ω),可以设置和/或调整lmco以基本上阻止低m/z离子被传输到下游元件,从而消除了对通过在ecd单元110中较高m/z抗体前体离子的反应之后对产物离子的检测产生的谱的后续分析和/解释的干扰。在一些方面中,例如,rf信号的幅度和频率可以设置成使得表现出大于1500、大于1700或大于2000的m/z的离子可以被四极杆组104选择性地传输。v和ω的示例性组合包括在从约0.1kv
p
‑
p
至约10kv
p
‑
p
的范围内的rf幅度和/或在从约0.8mhz至约3mhz的范围内的rf频率,其中例如根据上述公式(3)例如基于四极的有效场半径和期望的lmco来选择值。在一个示例性实施方式中,为获得等于约1500m/z的lmco,场半径(r0)可以是0.4mm,rf幅度可以是6.4kv,并且rf频率可以是约1.2mhz。本领域技术人员将理解,根据本教导的rf幅度的这样的值可以显著大于四极离子阱通常以窄带通质量过滤器模式操作的那些值(例如,如图2中所示)。
[0042]
现在参照图4,描绘了根据本教导的各种方面的用于操作图1的质谱仪系统的示例性方法400。如步骤401所示,方法400可以始于将包含抗体的样品递送到离子源104,由此样品内的分子被电离。一旦样品(包括抗体)内的分子被电离,这些离子例如通过一个或多个离子透镜、质量分析器和/或差分泵送真空级(例如,q0或q
jet
)而被传输到四极杆组104,如步骤402所示。当离子被传输进入并通过四极杆组104时,如图3所示各个杆104a
‑
104d上施
加有rf信号,使得rf幅度(v)和频率(ω)的组合使低于与该rf信号相关联的lmco的离子不稳定并被放电,同时允许高于lmco的那些离子(包括相对高m/z的抗体离子)被传输到ecd单元中(步骤403)。根据本教导,将理解,以这种仅rf模式操作四极杆组104可以在即使抗体离子表现出不同的电荷态(例如,相同物种的抗体,其中一种分子带单电荷,而另一种分子带双电荷)的情况下也允许感兴趣的抗体的离子传输到ecd单元110。在步骤404中,传输到ecd单元110的这些前体抗体离子然后经受ecd反应(例如,经由与在步骤405中在ecd单元110内捕获的或通过ecd单元110传输的电子的相互作用),从而导致产物离子的形成。在步骤406中,ecd产物离子然后由检测器110检测以生成ecd产物离子谱,其可以如本领域已知的那样被分析以在“自顶向下”分析中重建抗体结构。
[0043]
参照以下示例和图5a
‑
图5c中呈现的数据可以更充分地理解申请人的教导,提供图5a
‑
图5c是用于展示但不限制本教导。如下所述,本文公开的方法和系统选择性地阻止表现出低于低质量截止(lmco)的m/z的离子传输到下游ecd单元。
[0044]
示例1
[0045]
制备包括从nist获得的人源化单克隆igg抗体(nist
‑
mab)的样品。利用脱盐lc柱(水)使样品经受脱盐和lc分离,然后使用研究级四极
‑
tof系统(sciex)使样品经受电喷雾电离和质谱分析,该研究级四极
‑
tof系统(sciex)被修改为包括如发表在anal.chem.87(1):785
‑
792中的名称为“electron capture dissociation in a branched radio
‑
frequency ion trap”的文章(其通过引用整体并入)中描述的ecd单元。ecd单元安装在质谱仪系统的q1和q2之间。典型的电子束照射时间为10ms,并调节电子束强度以获得适当的解离效率。tof
‑
ms的质量分辨率为35000
‑
47000,其分辨高达z~30 的片段的同位素模式。图5a描绘了由电离的样品产生的谱,其中rf幅度被选择为在400v
p
‑
p
处允许基本上所有离子传输通过。图5a的谱包括表现出小于500的m/z的离子的显著信号以及在约m/z1520处的几个显著峰。现在参照图5b,将施加到四极杆组的rf信号的幅度增加到5kv
p
‑
p
(分辨dc电压被设置为0v),并且再次检测由q1传输的离子(未进行ecd反应)。如将通过比较图5a和图5b所观察到的,通过增加rf信号的幅度,q1阻止了那些表现出小于约1700的m/z的离子的传输。图7描绘了在图5b的条件下在对从q1传输的前体离子执行ecd后检测到的离子。表现出小于约2000的m/z的低强度峰代表ecd后的产物离子片段。比较图5a和5c将会理解,如果没有根据本教导去除低m/z离子,那么在图5c中观察到的那些产物离子峰中的许多峰将被混淆,从而使抗体的自顶向下分析更具挑战性。
[0046]
本领域技术人员将知道或能够仅使用常规实验来确定本文描述的实施例和实践的许多等同物。举例来说,各种部件的尺寸和应用于各种部件的特定电信号的确切值(例如,幅度、频率等)仅是示例性的并且不旨在限制本教导的范围。因此,将理解本发明不限于本文公开的实施例,而是应从以下权利要求中理解,权利要求应在法律允许的范围内被宽泛地解释。
[0047]
本文使用的章节标题仅用于组织目的并且不应被解释为限制。尽管结合各种实施例描述了申请人的教导,但并不意图使申请人的教导限于这些实施例。相反,如本领域技术人员将理解的,申请人的教导包含各种替代、修改和等同方案。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。