1.本发明涉及评估癌症患者是处于高死亡风险还是低死亡风险的方法,以及预测癌症患者对抗癌疗法的治疗应答的方法。本发明的方法可应用于例如选择临床试验患者、选择用抗癌疗法治疗的患者、在用抗癌疗法治疗期间监测癌症患者以及评估抗癌疗法的临床试验的结果。
背景技术:
2.影响预期寿命的因素在公共卫生中非常重要(ganna&ingelsson,2015)。在肿瘤学中,预测患者生存有助于优化患者管理(halabi&owzar,2010)。通过了解哪些变量对结果具有预后性,有可能深入了解疾病生物学,可以对患者进行个性化治疗,并且也许能够改进临床试验的设计、实施和数据分析。
3.目前对肿瘤学预后和预测因素的研究主要基于小样品量。因此,主要是一次针对一个风险因素来研究与死亡的关联(banks等人.,2013;hu等人,2004;mcgee等人.,1999;thun等人,1997;tota
‑
maharaj等人,2012)。甚至现有的预后评分,例如皇家马斯登医院评分(rmhs)(nieder&dalhaug,2010)、国际预后指数(ipi)(n.engl.j.med.,329:987
–
94,1993)、格拉斯哥预后评分(gps)或改进的格拉斯哥预后评分(mgps)(kinoshita等人,2013;nozoe等人,2014;jin等人,2017;grose等人,2014),由通常少于五个的少数风险因素构建而成。这些小样品量不允许同时评估多个因素(altman&simon,1994;graf等人,1999)。文献和研究结果中提出了许多生物标志物作为癌症患者死亡过程的预后指标,并且报告的研究的弱点(例如小样品量,特别是相对于正在评估的参数数量而言,以及正在进行的单变量而不是多变量分析)在reid等人.,2017中进行了总结。尽管报告了一些生物标志物的高等级证据,但reid等人.,2017没有提供证据表明可以根据此类生物标志物准确预测死亡,并且没有描述可用于进行此预测的模型。
4.因此,需要更大样品量以能够得到增加临床决策的信心的更准确的预测的需求,这种需求未得到满足。最近的英国生物银行倡议(sudlow等人,2015)是对可得数据的重要补充,并被ganna和ingelsson(2015)使用以在约500,000名参与者的人口样本中调查预期寿命,并构建优于查尔森合并症指数的死亡风险评分(charlson等人,1987)。然而,鉴于癌症对公共卫生的高度影响(stock等人,2018),本领域仍然需要更准确的测试来预测癌症患者的死亡和治疗应答,以尤其改善患者的治疗,以及临床试验的设计、实施和数据分析。
技术实现要素:
5.本发明人开发了一种基于多个参数评估癌症患者的死亡风险,或预测癌症患者对抗癌疗法的治疗应答的新方法。该方法源于以下发现:包括大量受试者的常规测量参数的训练数据可用于形成一个模型,该模型产生比目前已知的评分更可靠的死亡风险和治疗应答指标。
6.具体地,本发明人使用来自flatiron health数据库的数据对来自12个不同群组
(ropro1)的99,249人和来自15个不同群组(ropro2)的110,538人进行了生存分析,群组由肿瘤类型定义,并验证了在两项独立的临床研究中的结果。以真实的死亡作为终点,检查了人口统计学和临床变量(关注常规收集的临床和实验室数据)、诊断和治疗(curtis等人.,2018),并评估了第一线治疗的生存时间。如上所述,重点是在临床实践中常规收集的参数,这使得该方法可以应用于各种环境,而无需专门为分析收集患者参数数据。与依赖于在临床中未经常规测量的参数的测量的评分相比,这是一个优势。
7.确定了总共26个参数(ropro1)和29个参数(ropro2),这些参数是癌症患者经常规测量的,并且表明能够预测患有多种癌症的患者的死亡风险,其准确性远高于皇家马斯登医院评分(rmhs),如在i期研究(bp29428)中更准确性地预测患者停留时间长度所证明的,该研究调查了依米妥珠单抗(emactuzumab)和阿特珠单抗在患有选择的局部晚期或转移性实体瘤的患者中的安全性、药代动力学和初步抗肿瘤活性。本发明人已进一步表明,使用ropro1的26个参数中的13个允许以接近使用所有26个参数所达到的准确性预测死亡风险,并且使用少至26个参数中的4个足以以明显高于rmhs的准确性预测患者的死亡风险。本发明人已类似地表明,使用ropro2的29个参数中的13个允许以接近使用所有29个参数所达到的准确性预测死亡风险并且使用少至29个参数中的4个足以以明显高于rmhs的准确性预测患者的死亡风险。
8.具体地,本发明人已表明,当包含分别对应于少至4个选自以下(i)至(xxvi)或(i)至(xxix)列出的参数的患者信息用于计算ropro1(前4个参数:r2=0.15;前5个参数:r2=0.16;前10个参数:r2=0.17;前13个参数:r2=0.19;其中前4、前5、前10和前13分别指表15中列出的ropro1的排名编号为1
‑
4、1
‑
5、1
‑
10和1
‑
13的参数)或ropro2(前4个参数:r2=0.174;前5个参数:r2=0.184;前10个参数:r2=0.288;前13个参数:r2=0.299;其中,前4、前5、前10和前13分别指表15中列出的ropro2的排名编号为1
‑
4、1
‑
5、1
‑
10和1
‑
13的参数)时,ropro1和ropro2在与死亡时间(死亡风险)的相关性方面明显优于rmhs。
9.因此,对应于至少四个选自以下参数(i)至(xxvi)或(i)至(xxix)的参数的任意组合的数据适合形成有用的评分。例如,至少五个、至少六个、至少七个、至少八个、至少九个、至少十个、至少十一个、至少十二个、至少十三个、至少十四个、至少十五个、至少十六个、至少十七个、至少十八个、至少十九个、至少二十个、至少二十一个、至少二十二个、至少二十三个、至少二十四个、至少二十五个、至少二十六个、至少二十七个、至少二十八个或二十九个选自参数(i)至(xxvi)或(i)至(xxix)的参数可以使用。
10.在优选实施例中,选择对应于以下所有十三个参数(i)至(xiii)的数据。
11.本发明的第一方面提供了一种评估癌症患者的死亡风险的方法,所述方法包括将癌症患者信息输入模型以生成指示癌症患者死亡风险的评分。
12.患者信息可以包含对应于以下参数中的每一个参数的数据:
13.(i)血清或血浆中的白蛋白水平;
14.(ii)东部肿瘤协作组(ecog)体力状况;
15.(iii)血液中淋巴细胞与白细胞的比率;
16.(iv)吸烟状况;
17.(v)年龄;
18.(vi)恶性肿瘤分期的tnm分类;
19.(vii)心率;
20.(viii)血清或血浆中的氯化物或钠水平,优选血清或血浆中的氯化物水平;
21.(ix)血清或血浆中的尿素氮水平;
22.(x)性别;
23.(xi)血液中的血红蛋白或血细胞比容水平,优选血液中的血红蛋白水平;
24.(xii)血清或血浆中的天冬氨酸转氨酶酶活性水平;和
25.(xiii)血清或血浆中的丙氨酸转氨酶酶活性水平。
26.本发明人已进一步表明,使用26个参数或29个参数或其子集适用于预测癌症患者对抗癌疗法的治疗应答。
27.因此,本发明的第二方面提供了一种预测癌症患者对抗癌疗法的治疗应答的方法,所述方法包括将癌症患者信息输入模型以生成指示癌症患者治疗应答的评分。患者信息可以包含对应于以下参数中的每一个参数的数据:
28.(i)血清或血浆中的白蛋白水平;
29.(ii)东部肿瘤协作组(ecog)体力状况;
30.(iii)血液中淋巴细胞与白细胞的比率;
31.(iv)吸烟状况;
32.(v)年龄;
33.(vi)恶性肿瘤分期的tnm分类;
34.(vii)心率;
35.(viii)血清或血浆中的氯化物或钠水平,优选血清或血浆中的氯化物水平;
36.(ix)血清或血浆中的尿素氮水平;
37.(x)性别;
38.(xi)血液中的血红蛋白或血细胞比容水平,优选血液中的血红蛋白水平;
39.(xii)血清或血浆中的天冬氨酸转氨酶酶活性水平;和
40.(xiii)血清或血浆中的丙氨酸转氨酶酶活性水平。
41.所述方法可以进一步包括选择预测受益于用抗癌疗法治疗的患者进行抗癌疗法治疗,或用抗癌疗法治疗预测受益于用抗癌疗法进行治疗的患者。
42.还提供了一种用抗癌疗法治疗癌症患者的方法,所述方法包括:
43.(i)预测癌症患者对抗癌疗法的治疗应答;或
44.(ii)对预测癌症患者对抗癌疗法的治疗应答的方法的测试结果进行排序;
45.其中所述方法包括将癌症患者信息输入模型以生成指示癌症患者的治疗应答的评分。患者信息可以包含对应于以下参数中的每一个参数的数据:
46.(i)血清或血浆中的白蛋白水平;
47.(ii)东部肿瘤协作组(ecog)体力状况;
48.(iii)血液中淋巴细胞与白细胞的比率;
49.(iv)吸烟状况;
50.(v)年龄;
51.(vi)恶性肿瘤分期的tnm分类;
52.(vii)心率;
53.(viii)血清或血浆中的氯化物或钠水平,优选血清或血浆中的氯化物水平;
54.(ix)血清或血浆中的尿素氮水平;
55.(x)性别;
56.(xi)血液中的血红蛋白或血细胞比容水平,优选血液中的血红蛋白水平;
57.(xii)血清或血浆中的天冬氨酸转氨酶酶活性水平;和
58.(xiii)血清或血浆中的丙氨酸转氨酶酶活性水平;和
59.向预测对抗癌疗法有应答的患者施用药学有效量的抗癌疗法。
60.进一步提供了一种用于治疗患者癌症的方法中的抗癌疗法,所述方法包括预测癌症患者对抗癌疗法的治疗应答,所述方法包括将癌症患者信息输入模型以生成指示癌症患者治疗应答的评分。患者信息可以包含对应于以下参数中的每一个参数的数据:
61.(i)血清或血浆中的白蛋白水平;
62.(ii)东部肿瘤协作组(ecog)体力状况;
63.(iii)血液中淋巴细胞与白细胞的比率;
64.(iv)吸烟状况;
65.(v)年龄;
66.(vi)恶性肿瘤分期的tnm分类;
67.(vii)心率;
68.(viii)血清或血浆中的氯化物或钠水平,优选血清或血浆中的氯化物水平;
69.(ix)血清或血浆中的尿素氮水平;
70.(x)性别;
71.(xi)血液中的血红蛋白或血细胞比容水平,优选血液中的血红蛋白水平;
72.(xii)血清或血浆中的天冬氨酸转氨酶酶活性水平;和
73.(xiii)血清或血浆中的丙氨酸转氨酶酶活性水平;和
74.向预测对抗癌疗法有应答的患者施用药学有效量的抗癌疗法。
75.在本公开的一些实施例中,患者信息可以包含对应于多于四个选自参数(i)至(xiii)的参数,但少于所有参数(i)至(xiii)的数据或由其组成。例如,患者信息可以包含对应于五个、六个、七个、八个、九个、十个、十一个或十二个选自参数(i)至(xiii)的参数的数据或由其组成。或者,患者信息可以包含对应于所有十三个选自参数(i)至(xiii)的参数的数据或由其组成。优选地,患者信息包含或对应于至少五个、至少六个、至少七个、至少八个、至少九个、至少十个、至少十一个、至少十二个或所有十三个选自参数(i)至(xiii)的参数的数据或由其组成。更优选地,患者信息包含对应于至少五个、至少六个、至少七个、至少八个或至少九个选自参数(i)至(xiii)的参数的数据或由其组成。例如,患者信息可以包含对应于至少五个选自参数(i)至(xiii)的参数的数据或由其组成。或者,患者信息可以包含对应于至少六个选自所述参数(i)至(xiii)的参数的数据或由其组成。作为进一步地选择,患者信息可以包含对应于至少七个选自所述参数(i)至(xiii)的参数的数据或由其组成。作为仍进一步地选择,患者信息可以包含对应于至少八个选自所述参数(i)至(xiii)的参数的数据或由其组成。作为另一个选择,患者信息可以包含对应于至少九个选自所述参数(i)至(xiii)的参数的数据或由其组成。
76.例如,患者信息可以包含对应于参数(i)至(v)中的全部参数的数据或由其组成。
发明人已经发现选择这些参数可以提高死亡风险评估的准确性。
77.或者,患者信息可以包含对应于参数(i)至(xi)以及(xii)和(xiii)之一或两者中的全部参数的数据或由其组成。
78.癌症患者对抗癌疗法的治疗应答可以是完全应答、无进展存活、部分应答或癌症进展。完全应答(完全缓解)可以指患者体内没有可检测的疾病(癌症)。无进展存活可以指患者生存一段时间,在此期间疾病(癌症)没有恶化。部分应答可以指肿瘤尺寸的减小或癌症在患者体内扩散的减少。完全应答(也称为完全缓解)可以指患者体内没有可检测的疾病。癌症进展可以指疾病(癌症)的恶化,例如肿瘤尺寸的增加和/或患者体内肿瘤数量的增加。检测癌症患者应答抗癌疗法的完全应答、部分应答、无进展存活和癌症进展的方法是本领域公知的。
79.除非上下文另有要求,本文所指的抗癌疗法可以是所讨论的癌症的已知抗癌疗法,例如放射疗法、化学疗法、免疫疗法、激素疗法和/或手术。例如,抗癌疗法可以是晚期非小细胞肺癌(nsclc)、膀胱癌、慢性淋巴细胞白血病(cll)、弥漫性大b
‑
细胞淋巴瘤(dlbcl)、肝细胞癌(hcc)、转移性乳腺癌、转移性结直肠癌(crc)、转移性肾细胞癌(rcc)、多发性骨髓瘤、卵巢癌、小细胞肺癌(sclc)的已知抗癌疗法。抗癌疗法可以替代地是滤泡性淋巴瘤、胰腺癌或头颈部癌的已知抗癌疗法。
80.本文所指的患者优选为人类患者。在所述方法包括预测对抗癌疗法的治疗应答的情况下,除非上下文另有要求,否则患者可以是之前未接受过所述抗癌疗法治疗的患者。
81.患者信息可以进一步包含对应于选自以下的一个或多个参数的数据:
82.(xiv)收缩压或舒张压,优选收缩压;
83.(xv)血清或血浆中的乳酸脱氢酶酶活性水平;
84.(xvi)体质量指数;
85.(xvii)血清或血浆中的蛋白质水平;
86.(xviii)血液中的血小板水平;
87.(xix)转移部位的数量;
88.(xx)血液中嗜酸性粒细胞与白细胞的比率;
89.(xxi)血清或血浆中的钙水平;
90.(xxii)动脉血中的氧饱和度水平;
91.(xxiii)血清或血浆中的碱性磷酸酶酶活性水平;
92.(xxiv)血液中的中性粒细胞与淋巴细胞的比率(nlr);
93.(xxv)血清或血浆中的总胆红素水平;和
94.(xxvi)血液中的白细胞水平。
95.此外或可选地,患者信息可以进一步包含对应于选自以下的一个或多个参数的数据:
96.(xxvii)血液中的淋巴细胞水平;
97.(xxviii)血液中的二氧化碳水平;和
98.(xxix)血液中的单核细胞水平。
99.在一些实施例中,患者信息可以包含对应于多于一个选自参数(xiv)至(xxvi)和/或(xxvii)至(xxix)的参数的数据。例如,患者信息可以附加地或替代地包含对应于至少两
个、至少三个、至少四个、至少五个、至少六个、至少七个、至少八个、至少九个、至少十个、至少十一个、至少十二个或全部十三个选自参数(xiv)至(xxvi)的参数和/或至少一个、至少两个或全部三个选自参数(xxvii)至(xxix)的参数的数据。在一些实施例中,除了(i)至(xxvi)或(i)至(xxix)之外的参数也可以纳入患者信息和训练数据。
100.例如,患者信息可以包含对应于至少四个选自参数(i)至(xiii)的参数,和至少两个另外的选自参数(i)至(xxvi)或(i)至(xxix)的参数的数据或由其组成。
101.或者,患者信息可以包含对应于至少七个个选自参数(i)至(xxix)的参数的数据,其中至少一个参数选自参数(xxvii)至(xxix)。
102.例如,癌症患者信息可以包含对应于至少八个、至少九个、至少十个、至少十一个、至少十二个、至少十三个、至少十四个、至少十五个、至少十六个、至少十七个、至少十八个、至少十九个、至少二十个、至少二十一个、至少二十二个、至少二十三个、至少二十四个、至少二十五个、至少二十六个、至少二十七个或至少二十八个选自参数(i)至(xxix)的参数的数据,其中至少一个参数选自参数(xxvii)至(xxix)。
103.从参数(xxvii)至(xxix)选择参数,优选地是或包括参数(xxvii)(血液中的淋巴细胞水平)。
104.作为进一步的选择,患者信息可以包括对应于参数(xxvii)和五个或更多个选自参数(i)、(ii)、(iii)、(v)、(vi)、(vii)、(viii)、(ix)、(xi)、(xviii)和(xxiii)的参数的数据。
105.例如,癌症患者信息可以包含对应于参数(xxvii)和至少六个、至少七个、至少八个、至少九个、至少十个、至少十一个、至少十二个、至少十三个、至少十四个、至少十五个、至少十六个、至少十七个、至少十八个、至少十九个、至少二十个、至少二十一个、至少二十二个、至少二十三个、至少二十四个、至少二十五个、至少二十六个、至少二十七个、至少二十八个或所有二十九个选自参数(i)至(xxix)的参数的数据,其中至少一个参数选自参数(xxvii)至(xxix)。
106.患者信息可以包含对应于参数(i)至(xxvi)中的全部参数的数据或由其组成。发明人已经表明,所有这些参数都对模型具有独立的贡献。这样的评分与死亡时间相关性很好(示例数据集上的r2=0.24)并且明显优于rmhs(同一示例数据集上的r2=0.02)。优选地,患者信息包含对应于参数(i)至(xxix)中的全部参数的数据或由其组成。发明人已经表明,所有这些参数都对模型具有独立的贡献。这样的评分表明与死亡时间的相关性有所改善(示例数据集上的r2=0.30)并且再次明显优于rmhs(同一示例数据集上的r2=0.04)。
107.通常,使用更多的参数(i)至(xiii)、(i)至(xxvi)或(i)至(xxix)从而导致更准确的模型和评分,但实际上可能难以获得一个或多个参数的患者信息和/或训练数据,因此模型和评分的准确性可以与实际约束相平衡。
108.所述模型可以通过对训练数据进行统计显著性分析来形成,所述训练数据包括为多个受试者选择的参数。统计显著性分析可以包括多变量cox回归分析。在一些实施例中,可以使用一种或多种其他统计分析技术。
109.训练数据还可包括指示受试者死亡风险的信息。例如,训练数据可以包括总体存活、生存时间、受试者的第一线治疗和最后记录的联系之间的时间的指示或每个受试者的死亡风险的其他指示。训练数据可以包括表明从第一线治疗到患者最后一次与其诊所联系
的日期所经过的时间的截尾随访时间。最后一次联系可以是最后一次就诊、药物施用、样本采集或其他联系。
110.选择使用参数(i)至(xxvi)或(i)至(xxix)是有利的,因为这些参数是经常规测量的和/或在临床中可用的。因此,该评分易于使用,因为参数(i)至(xxvi)或(i)至(xxix)的数据可用于大多数癌症患者,同时还提供高准确性的预测。
111.即使并非所有参数都可用于患者,也可以获得有用的评分。因此,为患者信息选择的参数数量可能少于训练数据中纳入的参数数量。例如,如果使用包括所有参数(i)至(xxvi)或(i)至(xxix)的训练数据形成模型,则患者信息可以包括少于所有这些参数,并且仍然可以产生具有相似准确性的评分。例如,可以将来自列表(i)到(xxvi)或(i)至(xxix)的13个、14个、15个或16个参数输入到包括所有参数(i)至(xxvi)或(i)至(xxix)的模型中。这增加了该方法的易用性,因为该方法仍然可以评估缺少患者信息的患者。
112.训练数据可以从数据库获得,所述数据可以来自电子健康记录数据。例如,flatiron health数据库。数据库和/或训练数据可以包括结构化和/或非结构化数据。训练数据中的受试者可以是癌症患者。可以基于癌症类型从训练数据中纳入或排除受试者。例如,为了针对患有第一种癌症类型的患者定制方法,训练数据可以排除没有患有第一种癌症类型的受试者。
113.可以基于参数在训练数据和/或患者数据中的可用性来选择参数以在模型中使用。例如,在一些实施例中,可以仅选择对数据库中至少75%的患者可用的参数用于模型,或者可以仅选择对数据库中超过25%的患者可用的参数用于模型。为了改进训练数据,可以从训练数据中排除缺少治疗信息的患者。可以输入缺失的数据以改进训练数据。这可以使用合适的算法来执行,例如,missforest r包。
114.为了改进训练数据,可以排除外围数据。例如,对于连续参数,可以排除与平均值相差超过4个标准差的观测值。
115.可以筛选数据,以便从模型中排除无关紧要的参数。发明人已经发现参数(i)至(xxvi)和(i)至(xxix)在死亡风险的评估和对抗癌疗法的治疗应答的预测中具有重要意义,其中采用参数(i)至(xxix)的模型优于采用参数(i)至(xxvi)的模型。筛选可以包括使用bonferroni校正分析每个参数并排除p值大于阈值的参数。例如,可以从训练数据中排除p值为0.05的参数除以考虑的参数数量或更大的参数。参数可以在筛选期间按照其重要性(预测值)的顺序纳入模型中。
116.ropro1中参数(i)至(xxvi)的预测值在表15中详述,其中排名(1)表示预测性最高的参数(白蛋白),排名(26)表示该模型中参数(i)至(xxvi)中预测性最低的参数(白细胞水平)。ropro2中参数(i)至(xxix)的预测值也在表15中详述,其中排名(1)再次表示预测性最高的参数(白蛋白),排名(29)表示该模型中参数(i)至(xxix)中预测性最低的参数(二氧化碳水平)。因此,表15中参数的排名编号越低,患者信息就越优选包含对应于所述参数的数据。
117.由于发明人已经发现,在ropro1中,参数(i)至(xxvi)在上述(i)至(xxvi)中列出的参数的编号顺序(对应于表15中所示的排序)中很重要,可以通过以该顺序纳入从参数(i)至(xxvi)选择的参数来形成模型。
118.在优选实施例中,患者信息因此可以包含对应于如表15所示的ropro1中具有排名
1至4、1至5、1至6、1至7、1至8、1至9、1至10、1至11、1至12、1至13、1至.14、1至15、1至16、1至17、1至.18、1至19、1至20、1至21、1至22、1至23、1至24、1至25或1至26的参数的数据或由其组成,其中ropro1中排名1至4的参数对应于血清或血浆中的白蛋白水平、ecog体力状况、血液中淋巴细胞与白细胞的比率和吸烟状况。
119.由于发明人已经发现参数(i)至(xxix)在表15中所示的ropro2的排序中很重要,并且这样的模型比基于参数(i)至(xxvi)的模型更准确地预测os,在一个优选实施例中,可以通过按照表15所示的排序纳入从参数(i)至(xxix)中选择的参数来形成模型。
120.因此,在一个更优选实施例中,患者信息可以包含对应于如表15所示的ropro2中具有排名1至4、1至5、1至6、1至7、1至8、1至9、1至10、1至11、1至12、1至13、1至.14、1至15、1至16、1至17、1至.18、1至19、1至20、1至21、1至22、1至23、1至24、1至25、1至26、1至27、1至28或1至29的参数的数据或由其组成,其中ropro2中排名1至4的参数对应于血清或血浆中的白蛋白水平、血液中的淋巴细胞水平、ecog体力状况、血液中的白细胞水平。
121.因此,本公开提供:
122.[1]如本文所述,一种方法或在方法中使用的抗癌疗法,其中所述方法包括将癌症患者信息输入到模型以生成评分,所述患者信息包含对应于四个或更多个参数的数据。
[0123]
[2]根据[1]所述的方法或在方法中使用的抗癌疗法,其中所述参数包括患者血清或血浆中的白蛋白水平。
[0124]
[3]根据[1]或[2]所述的方法或在方法中使用的抗癌疗法,其中所述参数包括患者的ecog体力状况。
[0125]
[4]根据[1]至[3]中任一项所述的方法或在方法中使用的抗癌疗法,其中所述参数包括患者血液中淋巴细胞与白细胞的比率。
[0126]
[5]根据[1]至[4]中任一项所述的方法或在方法中使用的抗癌疗法,其中所述参数包括患者的吸烟状况。
[0127]
[6]根据[1]至[5]中任一项所述的方法或在方法中使用的抗癌疗法,其中所述参数包括患者的年龄。
[0128]
[7]根据[1]至[6]中任一项所述的方法或在方法中使用的抗癌疗法,其中所述参数包括患者恶性肿瘤分期的tnm分类。
[0129]
[8]根据[1]至[7]中任一项所述的方法或在方法中使用的抗癌疗法,其中所述参数包括患者的心率。
[0130]
[9]根据[1]至[8]中任一项所述的方法或在方法中使用的抗癌疗法,其中所述参数包括患者血清或血浆中的氯化物或钠水平,优选患者的血清或血浆中的氯化物水平。
[0131]
[10]根据[1]至[9]中任一项所述的方法或在方法中使用的抗癌疗法,其中所述参数包括患者血清或血浆中的尿素氮水平。
[0132]
[11]根据[1]至[10]中任一项所述的方法或在方法中使用的抗癌疗法,其中所述参数包括患者的性别。
[0133]
[12]根据[1]至[11]中任一项所述的方法或在方法中使用的抗癌疗法,其中所述参数包括患者血液中的血红蛋白或血细胞比容水平,优选血液中的血红蛋白水平。
[0134]
[13]根据[1]至[12]中任一项所述的方法或在方法中使用的抗癌疗法,其中所述参数包括患者血清或血浆中的天冬氨酸转氨酶酶活性水平。
[0135]
[14]根据[1]至[13]中任一项所述的方法或在方法中使用的抗癌疗法,其中所述参数包括患者血清或血浆中的丙氨酸转氨酶酶活性水平。
[0136]
[15]根据[1]至[14]中任一项所述的方法或在方法中使用的抗癌疗法,其中所述参数包括患者的收缩压或舒张压,优选收缩压。
[0137]
[16]根据[1]至[15]中任一项所述的方法或在方法中使用的抗癌疗法,其中所述参数包括患者血清或血浆中的乳酸脱氢酶酶活性水平。
[0138]
[17]根据[1]至[16]中任一项所述的方法或在方法中使用的抗癌疗法,其中所述参数包括患者的体质量指数。
[0139]
[18]根据[1]至[17]中任一项所述的方法或在方法中使用的抗癌疗法,其中所述参数包括患者血清或血浆中的蛋白质水平。
[0140]
[19]根据[1]至[18]中任一项所述的方法或在方法中使用的抗癌疗法,其中所述参数包括患者血液中的血小板水平。
[0141]
[20]根据[1]至[19]中任一项所述的方法或在方法中使用的抗癌疗法,其中所述参数包括患者体内转移部位的数量。
[0142]
[21]根据[1]至[20]中任一项所述的方法或在方法中使用的抗癌疗法,其中所述参数包括患者血液中嗜酸性粒细胞与白细胞的比率。
[0143]
[22]根据[1]至[21]中任一项所述的方法或在方法中使用的抗癌疗法,其中所述参数包括患者血清或血浆中的钙水平。
[0144]
[23]根据[1]至[22]中任一项所述的方法或在方法中使用的抗癌疗法,其中所述参数包括患者动脉血中的氧饱和度水平。
[0145]
[24]根据[1]至[23]中任一项所述的方法或在方法中使用的抗癌疗法,其中所述参数包括患者血清或血浆中的碱性磷酸酶酶活性水平。
[0146]
[25]根据[1]至[24]中任一项所述的方法或在方法中使用的抗癌疗法,其中所述参数包括患者血液中的nlr。
[0147]
[26]根据[1]至[25]中任一项所述的方法或在方法中使用的抗癌疗法,其中所述参数包括患者血清或血浆中的总胆红素水平。
[0148]
[27]根据[1]至[26]中任一项所述的方法或在方法中使用的抗癌疗法,其中所述参数包括患者血液中的白细胞水平。
[0149]
[28]根据[1]至[27]中任一项所述的方法或在方法中使用的抗癌疗法,其中所述参数包括患者血液中的淋巴细胞水平。
[0150]
[29]根据[1]至[28]中任一项所述的方法或在方法中使用的抗癌疗法,其中所述参数包括患者血液中的二氧化碳水平。
[0151]
[30]根据[1]至[29]中任一项所述的方法或在方法中使用的抗癌疗法,其中所述参数包括患者血液中的单核细胞水平。
[0152]
[31]根据[1]至[30]中任一项所述的方法或在方法中使用的抗癌疗法,其中患者信息包括对应于四个或更多、五个或更多、六个或更多、七个或更多、八个或更多、九个或更多、十个或更多、十一个或更多、十二个或更多、十三个或更多、十四个或更多、十五个或更多、十六个或更多、十七个或更多、十八个或更多、十九个或更多、二十个或更多、二十一个或更多、二十二个或更多、二十三个或更多、二十四个或更多、二十五个或更多、二十六个或
更多、二十七个或更多、二十八个或更多、或二十九个选自[2]至[30]列出的参数的参数的数据。
[0153]
上述(i)至(xxix)列出的一个或更多个参数可以用与相关参数相关的合适的替代参数来替代。表15列出了合适的替代参数。例如,血清或血浆中的氯化物水平可以用血清或血浆中的钠水平代替,血液中的血红蛋白水平可以用血液中的血细胞比容水平替代,血清或血浆中的丙氨酸氨基转移酶(alt)酶活性水平可以是用血清或血浆中的天冬氨酸转氨酶(ast)酶活性水平替代,和/或收缩压可以用舒张压替代。
[0154]
用于测量或评估上述参数(i)至(xxix)以及本文提及的替代参数的方法是本领域已知的并且在临床环境中常规测量。因此,测量这些参数完全在技术人员的能力范围内。给定参数的测量方法优选在被分析的癌症患者和任何训练或验证数据集之间是一致的。必要时,可以对来自不同测量方法的结果进行标准化,以允许在从所述方法获得的数据之间进行比较。
[0155]
用于测量上述参数(i)至(xxix)以及本文提及的替代参数的示例性方法在表15中详述。在可用的情况下,表15还列出了本文提及的参数的loinc代码(2.65版;2018年12月14日发布)。可以从以下检索存储在其loinc代码下的给定参数的信息,包括适用的测量方法:https://search.loinc.org/searchloinc/.
[0156]
肿瘤的tnm分期可根据来自https://www.uicc.org/8th
‑
edition
‑
uicc
‑
tnm
‑
classification
‑
malignant
‑
tumors
‑
published的第8版恶性肿瘤的uicc tnm分类[2019年3月27日检索]确定。本文提及的参数的测量可以采用任何合适的测量单位,例如表15列出的这些参数的测量单位。给定参数的测量单位优选在被分析的癌症患者和任何训练或验证数据集之间是一致的。必要时,可以将不同的测量单位转换为通用的测量单位。
[0157]
上述参数(i)至(xxix),以及本文提及的替代参数,可以在任何合适的时间点测量。
[0158]
例如,在包括评估癌症患者的死亡风险的方法,例如选择癌症患者纳入临床试验的方法或用抗癌疗法进行治疗的方法的背景下,参数可以分别在临床试验开始或向患者施用第一剂抗癌疗法之前测量。在临床试验开始或对患者施用第一剂抗癌疗法前不久,例如6个月或更短、3个月或更短、或1个月或更短进行测量。
[0159]
当所述方法是预测癌症患者对抗癌疗法的治疗应答的方法时,可以在对患者施用第一剂抗癌疗法之前测量参数。或者,可以在对患者施用抗癌疗法之后测量参数以预测治疗期间对抗癌疗法的治疗应答。在一个实施例中,可以在第一时间点和第二时间点测量参数,其中第一时间点可以在对患者施用第一剂抗癌疗法之前,第二时间点可以在向患者施用抗癌疗法之后,其中与第一时间点相比在第二时间点预测的治疗应答的改善表明患者对抗癌疗法有应答,并且与第一时间点相比在第二时间点预测的治疗应答恶化表明患者对抗癌治疗没有应答或已对抗癌疗法产生抗药性。
[0160]
在所述方法包括通过对训练数据执行多变量cox回归分析来形成模型的情况下,训练数据可以包括患者信息,所述患者信息包括多个受试者的参数数据。多个受试者可以包括至少10000个受试者。使用大量受试者可以提高模型的准确性。例如,多个受试者可以包括至少15000个、20000个、30000个、40000个、50000个、60000个、70000个、80000个或90000个受试者。
[0161]
形成模型可以包括为选自多个受试者的列表的相应参数中的每一个相应参数分配相应均值m,并且为选自列表的相应参数中的每一个相应参数分配相应权重w,并且其中所述模型的输出是根据以下公式由选择的参数的总和给出的:输出=σw(输入
‑
m)。因此评分可以0为中心。
[0162]
根据任何公开的实施例的评估癌症患者的死亡风险的方法可以包括将由模型生成的评分与一个或多个预定阈值进行比较,或将生成的评分与同一组中其他癌症患者的生成的评分进行比较,以评估死亡风险。例如,所述方法可以包括确定生成的评分是高于还是低于预先确定的阈值或在两个不同的预先确定的阈值之间的值范围内。
[0163]
根据任何公开的实施例的预测癌症患者对抗癌疗法的治疗应答的方法可以包括将由模型生成的评分与一个或多个预定阈值进行比较,或将生成的评分与同一组中其他癌症患者的生成的评分进行比较,以获得治疗应答的预测。例如,所述方法可以包括确定生成的评分是高于还是低于预先确定的阈值或在两个不同的预先确定的阈值之间的值范围内。
[0164]
死亡风险可被评估为高风险或低风险。例如,如果患者的评分高于0、或高于1、或高于1.05,则可将患者评估为处于高死亡风险。如果患者的评分低于0或低于
‑
1或低于
‑
1.19,则可将患者评估为处于低死亡风险。如果ropro评分高于1.13,则死亡风险可能被评估为非常高的风险。如果ropro评分低于1.13,则死亡风险可能会被评估为较低。对于晚期nsclc特异性ropro评分,如果ropro评分高于0.81,则死亡风险可能被评估为非常高。对于晚期黑色素瘤特异性ropro评分,如果ropro评分高于1.06,则死亡风险可能被评估为非常高。对于膀胱癌特异性ropro评分,如果ropro评分高于0.99,则死亡风险可能被评估为非常高。对于cll特异性ropro评分,如果ropro评分高于1.16,则死亡风险可能被评估为非常高。对于dlbcl特异性ropro评分,如果ropro评分高于1.17,则死亡风险可能被评估为非常高。对于hcc特异性ropro评分,如果ropro评分高于1.11,则死亡风险可能被评估为非常高。对于转移性乳腺癌特异性ropro评分,如果ropro评分高于1.00,则死亡风险可能被评估为非常高。对于转移性crc特异性ropro评分,如果ropro评分高于0.94,则死亡风险可能被评估为非常高。对于rcc特异性ropro评分,如果ropro评分高于1.22,则死亡风险可能被评估为非常高。对于多发性骨髓瘤特异性ropro评分,如果ropro评分高于1.02,则死亡风险可能被评估为非常高。对于卵巢癌特异性ropro评分,如果ropro评分高于1.04,则死亡风险可能被评估为非常高。对于sclc特异性ropro评分,如果ropro评分高于0.89,则死亡风险可能被评估为非常高。对于头颈部癌特异性ropro评分,如果ropro评分高于0.75,则死亡风险可能被评估为非常高。对于滤泡癌特异性ropro评分,如果ropro评分高于1.60,则死亡风险可能被评估为非常高。对于胰腺癌特异性ropro评分,如果ropro评分高于0.87,则死亡风险可能被评估为非常高。
[0165]
或者,患者可以是一组患者中的一个,并且可以为该组中的每个患者生成评分。然后,如果患者的评分处于组中评分最高的50%或最高的10%或最高的5%,则可将其评估为处于高死亡风险。如果患者的评分处于组中评分最低的50%或最低的10%或最低的5%,则可将其评估为处于低死亡风险。基于患者的评分与训练数据中受试者的评分的比较,患者的死亡风险可以被评估为高或低。可以为训练数据中的多个受试者生成评分,并且可以将患者的评分与训练数据中的评分分布进行比较。如果患者的评分处于多个受试者的评分的最高的50%或最高的10%或最高的5%的范围内,则可将患者评估为处于高死亡风险。如果
患者的评分处于多个受试者的评分的最低50%或最低的10%或最低的5%,则可将患者评估为处于低死亡风险。
[0166]
如本文所用,术语比率可指缩放比率。例如,血液中淋巴细胞与白细胞的比率可以是每100个白细胞中淋巴细胞的数量。类似地,血液中嗜酸性粒细胞与白细胞的比率可以是每100个白细胞中嗜酸性粒细胞的数量。
[0167]
评估癌症患者是处于高死亡风险还是低死亡风险的方法可用于许多不同的情况。
[0168]
例如,在进行临床试验时,例如对于抗癌疗法,仅选择那些可能在整个试验期间生存的患者纳入临床试验是有利的。从进行临床试验的角度来看,这都是有益的,因为因死亡而退出试验的患者的数据在许多情况下不能用于例如针对安全性或有效性评估抗癌疗法,从而增加临床试验的成本和完成试验所需的时间。此外,在临床试验中纳入具有高死亡风险的患者可能会掩盖对低死亡风险或较低死亡风险患者的治疗效果,因为高死亡风险患者的健康受到损害而无法从治疗中获益。此外,将具有高死亡率的患者排除在临床试验之外对患者有益,因为不太可能从被测试的抗癌疗法中受益的个体不会暴露于不必要的治疗以及任何伴随的副作用。
[0169]
因此,在一个实施例中,本发明提供了一种选择癌症患者纳入临床试验(例如用于抗癌疗法)的方法,所述方法包括使用如本文所述的方法评估癌症患者是处于高死亡风险还是低死亡风险,并选择被评估为处于低死亡风险的患者纳入临床试验。
[0170]
对于临床试验结果的评估,接受测试的抗癌疗法组中的患者和作为治疗组的对照组的接受安慰剂或无治疗的组中的患者匹配良好是很重要的,即具有与使用本文所述的方法评估的相同的死亡风险,以确保在治疗组中看到的任何效果都是待测试的抗癌疗法的结果,而不是由不同患者组之间的差异引起的。例如,如果安慰剂组的死亡风险显著高于治疗组,这可能错误地表明治疗对患者生存有积极影响,反之亦然。
[0171]
在另一个实施例中,本发明因此提供了一种评估对癌症患者进行的临床试验(例如用于抗癌疗法)的结果的方法,所述方法包括使用本文所述的方法评估参加临床试验的癌症患者是处于高死亡风险还是低死亡风险。
[0172]
在一个进一步的实施例中,本发明涉及一种选择癌症患者纳入临床试验(例如用于抗癌疗法)的方法,所述方法包括使用本文所述的方法确定具有相同死亡风险的第一癌症患者和第二癌症患者,并且将所述患者纳入临床试验。第一癌症患者可以接受抗癌疗法,而第二癌症患者可以不接受抗癌疗法。在这种情况下,第二癌症患者充当第一癌症患者的对照,从而允许例如待评估的抗癌疗法的安全性或有效性。优选地,第一和第二患者都具有低死亡风险。
[0173]
如果患者都被评估为具有低风险或都被评估为具有高风险,则可以判断患者具有相同的死亡风险。或者,如果患者的评分在彼此相同的分位数内,则可以判断患者具有相同的风险。例如,一组患者可以根据他们的评分分为10%或5%的分位数。组中评分前5%的两名患者可能被判断为具有相同的风险。第二个(5
‑
10%)分位数中的两名患者可能被判断为具有相同的风险。
[0174]
本发明还提供了一种分别将第一癌症患者或癌症患者群组与第二癌症患者或癌症患者群组进行比较的方法,所述方法包括使用如本文所述的方法评估患者或第一群组和第二群组中的患者是否是处于高死亡风险或低死亡风险。
[0175]
如上所述,处于高死亡风险的患者不太可能从抗癌疗法中受益。在治疗之前确定这样的患者是有利的,因为它避免将患者暴露于最终证明无效的疗法以及与之相关的任何副作用。鉴于许多抗癌疗法也与高成本有关,在治疗前确定此类患者的能力也减少了医疗保健系统的成本负担。
[0176]
在另一个实施例中,本发明因此涉及一种选择癌症患者进行抗癌疗法治疗的方法,所述方法包括使用本文所述的方法评估癌症患者是处于高死亡风险还是低死亡风险,并选择被评估为处于低死亡风险的癌症患者用抗癌疗法进行治疗。所述方法可以进一步包括用抗癌疗法治疗被评估为处于低死亡风险的癌症患者。
[0177]
还提供了一种用抗癌疗法治疗癌症患者的方法,所述方法包括使用如本文所述的方法评估癌症患者是否处于高死亡风险或低死亡风险中,并向评估为处于低死亡风险的患者施用药学有效量的抗癌疗法。
[0178]
进一步提供了一种用于用抗癌疗法治疗癌症患者的方法中的抗癌疗法,所述方法包括使用如本文所述的方法评估癌症患者是否处于高死亡风险或低死亡风险中,并向评估为处于低死亡风险的患者施用药学有效量的抗癌疗法。
[0179]
类似地,患者在癌症治疗期间的死亡风险预计将指示患者是否正在受益或将从疗法中受益。
[0180]
因此,还提供了一种在用抗癌疗法治疗期间监测癌症患者的方法,其中患者可以任选地显示疾病进展,所述方法包括使用本文所述的方法评估癌症患者是处于高死亡风险还是低死亡风险,其中选择被评估为处于低死亡风险的癌症患者继续用抗癌疗法进行治疗,并且选择被评估为处于高死亡风险的癌症患者停止用抗癌疗法进行治疗。
[0181]
用于预测特定癌症类型预后的参数是本领域已知的,测量或评估这些参数的方法也是如此。本发明人已经表明,在评估例如癌症患者的死亡风险时,或预测癌症患者对抗癌疗法的治疗应答时,进一步纳入患者信息中的一种或多种癌症类型特异性参数(例如用于预测晚期非小细胞肺癌(nsclc)、膀胱癌、慢性淋巴细胞白血病(cll)、弥漫性大b
‑
细胞淋巴瘤(dlbcl)、肝细胞癌(hcc)、转移性乳腺癌、转移性结直肠癌(crc)、转移性肾细胞癌(rcc)、多发性骨髓瘤、卵巢癌、小细胞肺癌(sclc)、头颈部癌或胰腺癌),与单独使用参数(i)至(xxvi)或(i)至(xxix)相比,死亡风险评分更准确。因此,评估癌症患者的死亡风险的方法中的患者信息可进一步包含对应于一个或多个选自已知指示晚期nsclc、膀胱癌、cll、dlbcl、hcc、转移性乳腺癌、转移性crc、转移性rcc、多发性骨髓瘤、卵巢癌、sclc、头颈部癌和胰腺癌,例如表15中列出的那些预后的参数的参数的数据。这些癌症特异性参数可以在与所述方法中采用的其他参数相同的时间点或不同的时间点测量。
[0182]
因此,本发明进一步提供:
[0183]
[32]如本文所述,一种方法或在方法中使用的抗癌疗法,其中癌症患者是晚期nsclc患者,并且其中所述方法包括将癌症患者信息输入到模型以生成评分,所述患者信息包含对应于四个或更多个上述[2]至[30]列出的参数和一个或多个nsclc特异性参数的数据。
[0184]
[33]根据[32]所述的方法或在方法中使用的抗癌疗法,其中nsclc特异性参数是患者中鳞状细胞癌的存在或不存在。
[0185]
[34]根据[32]或[33]所述的方法或在方法中使用的抗癌疗法,其中nsclc特异性
参数是患者原发肿瘤的阳性或阴性pd
‑
l1表达状况。
[0186]
[35]根据[32]至[34]中任一项所述的方法或在方法中使用的抗癌疗法,其中nsclc特异性参数是患者肿瘤中alk重排的存在或不存在。
[0187]
[36]根据[32]至[35]中任一项所述的方法或在方法中使用的抗癌疗法,其中nsclc特异性参数是患者肿瘤中egfr突变的存在或不存在。
[0188]
[37]根据[32]至[36]中任一项所述的方法或在方法中使用的抗癌疗法,其中nsclc特异性参数是患者肿瘤中kras突变的存在或不存在。
[0189]
[38]如本文所述,一种方法或在方法中使用的抗癌疗法,其中癌症患者是膀胱癌患者,并且其中所述方法包括将癌症患者信息输入到模型以生成评分,所述患者信息包含对应于四个或更多个上述[2]至[30]列出的参数和一个或多个膀胱癌特异性参数的数据。
[0190]
[39]根据[38]所述的方法或在方法中使用的抗癌疗法,其中膀胱癌特异性参数是患者存在或不存在膀胱切除术史。
[0191]
[40]根据[38]或[39]所述的方法或在方法中使用的抗癌疗法,其中膀胱癌特异性参数是患者在初始诊断时肿瘤的n分期。
[0192]
[41]根据[38]至[40]中任一项所述的方法或在方法中使用的抗癌疗法,其中膀胱癌特异性参数是患者初次诊断时的肿瘤的t分期。
[0193]
[42]如本文所述,一种方法或在方法中使用的抗癌疗法,其中癌症患者是cll患者,并且其中所述方法包括将癌症患者信息输入到模型以生成评分,所述患者信息包含对应于四个或更多个上述[2]至[30]列出的参数和一个或多个cll特异性参数的数据。
[0194]
[43]根据[42]所述的方法或在方法中使用的抗癌疗法,其中cll特异性参数是患者每体积血液中的血细胞比容百分比。
[0195]
[44]根据[42]或[43]所述的方法或在方法中使用的抗癌疗法,其中cll特异性参数是血液中单核细胞与白细胞的比率,优选患者血液中单核细胞与100个白细胞的比率。
[0196]
[45]根据[42]至[44]中任一项所述的方法或在方法中使用的抗癌疗法,其中cll特异性参数是患者肿瘤中17p缺失的存在或不存在。
[0197]
[46]如本文所述,一种方法或在方法中使用的抗癌疗法,其中癌症患者是dlblc患者,并且其中所述方法包括将癌症患者信息输入到模型以生成评分,所述患者信息包含对应于四个或更多个上述[2]至[30]列出的参数和患者骨髓中cd5的阳性或阴性表达状况的数据。
[0198]
[47]如本文所述,一种方法或在方法中使用的抗癌疗法,其中癌症患者是hcc患者,并且其中所述方法包括将癌症患者信息输入到模型以生成评分,所述患者信息包含对应于四个或更多个上述[2]至[30]列出的参数,和患者体内是否存在腹水,优选在向患者施用抗癌疗法(例如全身性抗癌疗法)之前的60天或之内存在或不存在腹水的数据。
[0199]
[48]如本文所述,一种方法或在方法中使用的抗癌疗法,其中癌症患者是转移性乳腺癌患者,并且其中所述方法包括将癌症患者信息输入到模型以生成评分,所述患者信息包含对应于四个或更多个上述[2]至[30]列出的参数和一个或多个转移性乳腺癌特异性参数的数据。
[0200]
[49]根据[48]所述的方法或在方法中使用的抗癌疗法,其中转移性乳腺癌特异性参数是患者肿瘤的阳性或阴性er状况。
[0201]
[50]根据[48]或[49]所述的方法或在方法中使用的抗癌疗法,其中转移性乳腺癌特异性参数是患者肿瘤的阳性或阴性pr状况。
[0202]
[51]根据[48]至[50]中任一项所述的方法或在方法中使用的抗癌疗法,其中转移性乳腺癌特异性参数是患者肿瘤的阳性或阴性her2状况。
[0203]
[52]根据[48]至[51]中任一项所述的方法或在方法中使用的抗癌疗法,其中转移性乳腺癌特异性参数是患者血液中粒细胞与白细胞的比率,优选患者血液中的粒细胞与100个白细胞的比率。
[0204]
[53]如本文所述,一种方法或在方法中使用的抗癌疗法,其中癌症患者是转移性crc患者,并且其中所述方法包括将癌症患者信息输入到模型以生成评分,所述患者信息包含对应于四个或更多个上述[2]至[30]列出的参数和一个或多个转移性crc特异性参数的数据。
[0205]
[54]根据[53]所述的方法或在方法中使用的抗癌疗法,其中转移性crc特异性参数是患者肿瘤中braf突变的存在或不存在。
[0206]
[55]根据[53]或[54]所述的方法或在方法中使用的抗癌疗法,转移性crc特异性参数是患者肿瘤中kras突变或重排的存在或不存在。
[0207]
[56]根据[53]至[55]中任一项所述的方法或在方法中使用的抗癌疗法,其中转移性crc特异性参数是在患者的原发肿瘤中微卫星不稳定性(msi
‑
h)的存在或不存在,和mmr蛋白表达缺失或mmr蛋白表达正常。
[0208]
[57]如本文所述,一种方法或在方法中使用的抗癌疗法,其中癌症患者是转移性rcc患者,并且其中所述方法包括将癌症患者信息输入到模型以生成评分,所述患者信息包含对应于四个或更多个上述[2]至[30]列出的参数和一个或多个转移性rcc特异性参数的数据。
[0209]
[58]根据[57]所述的方法或在方法中使用的抗癌疗法,其中转移性rcc特异性参数是患者的肾切除术史的存在或不存在。
[0210]
[59]根据[57]或[58]所述的方法或在方法中使用的抗癌疗法,其中转移性rcc特异性参数是患者中透明细胞rcc的存在或不存在,或患者中主要透明细胞rcc的存在或不存在,其中患者中透明细胞rcc的存在或不存在任选地通过组织学确定。
[0211]
[60]如本文所述,一种方法或在方法中使用的抗癌疗法,其中癌症患者是多发性骨髓瘤患者,并且其中所述方法包括将癌症患者信息输入到模型以生成评分,所述患者信息包含对应于四个或更多个上述[2]至[30]列出的参数和一个或多个多发性骨髓瘤特异性参数的数据。
[0212]
[61]根据[60]所述的方法或在方法中使用的抗癌疗法,其中多发性骨髓瘤特异性参数是患者肿瘤中异常的存在或不存在,其中异常的存在或不存在任选地使用fish或染色体组型分析确定。
[0213]
[62]根据[60]或[61]所述的方法或在方法中使用的抗癌疗法,其中多发性骨髓瘤特异性参数是免疫球蛋白iga类的骨髓瘤(m)蛋白的存在或不存在。
[0214]
[63]根据[60]至[62]中任一项所述的方法或在方法中使用的抗癌疗法,其中多发性骨髓瘤特异性参数是免疫球蛋白igg类的m蛋白的存在或不存在。
[0215]
[64]根据[60]至[63]中任一项所述的方法或在方法中使用的抗癌疗法,多发性骨
髓瘤特异性参数是κ轻链骨髓瘤的存在或不存在。
[0216]
[65]根据[60]至[64]中任一项所述的方法或在方法中使用的抗癌疗法,多发性骨髓瘤特异性参数是λ轻链骨髓瘤的存在或不存在。
[0217]
[66]如本文所述,一种方法或在方法中使用的抗癌疗法,其中癌症患者是卵巢癌患者,并且其中所述方法包括将癌症患者信息输入到模型以生成评分,所述患者信息包含对应于四个或更多个上述[2]至[30]列出的参数和卵巢癌特异性参数,其中卵巢癌特异性参数是透明细胞卵巢癌的存在或不存在。
[0218]
[67]如本文所述,一种方法或在方法中使用的抗癌疗法,其中癌症患者是sclc患者,并且其中所述方法包括将癌症患者信息输入到模型以生成评分,所述患者信息包含对应于四个或更多个上述[2]至[30]列出的参数和sclc特异性参数,其中sclc特异性参数是初始诊断时广泛性疾病或局限性疾病的存在或不存在。
[0219]
[68]如本文所述,一种方法或在方法中使用的抗癌疗法,其中癌症患者是头颈部癌患者,并且其中所述方法包括将癌症患者信息输入到模型以生成评分,所述患者信息包含对应于四个或更多个上述[2]至[30]列出的参数和头颈部癌特异性参数,其中头颈部癌特异性参数是人乳头瘤病毒(hpv)状况。
[0220]
[69]如本文所述,一种方法或在方法中使用的抗癌疗法,其中癌症患者是胰腺癌患者,并且其中所述方法包括将癌症患者信息输入到模型以生成评分,所述患者信息包含对应于四个或更多个上述[2]至[30]列出的参数和胰腺癌特异性参数,其中胰腺癌特异性参数是通过手术切除原发性胰腺肿瘤。
[0221]
上文提及的癌症类型特异性参数是本领域众所周知的,测量这些参数的方法也是如此。示例性方法在表15中列出。因此,测量这些参数完全在技术人员的能力范围内。例如,如果癌症类型特异性参数是生物标志物(例如alk重排的存在或不存在、egfr突变的存在或不存在等),则关于生物标志物存在或不存在的信息包含在患者的电子健康记录中(ehr)。确定生物标志物存在或不存在的方法包括:测序,例如下一代测序、荧光原位杂交(fish)和免疫组织化学(ihc)。
[0222]
基于其确定了上述ropro1的26个参数的来自flatiron health数据库的数据集由99,249名患有以下癌症类型之一的患者组成:晚期黑色素瘤、晚期非小细胞肺癌(nsclc)、膀胱癌、慢性淋巴细胞白血病(cll)、弥漫性大b
‑
细胞淋巴瘤(dlbcl)、肝细胞癌(hcc)、转移性乳腺癌、转移性结直肠癌(crc)、转移性肾细胞癌(rcc)、多发性骨髓瘤、卵巢癌或小细胞肺癌(sclc)。此外,本发明人已经表明,包含对应于上述(i)至(xxvi)中列出的参数的数据的患者信息可用于预测这些癌症类型的死亡风险。因此,本文提及的癌症可以是选自由以下项组成的组的癌症:黑色素瘤(例如晚期黑色素瘤)、nsclc(例如晚期nsclc)、膀胱癌、cll、dlbcl、hcc、转移性乳腺癌、转移性crc、转移性rcc、多发性骨髓瘤、卵巢癌和sclc。
[0223]
基于其确定了上述ropro 2的29个参数的来自flatiron health数据库的数据集由111,538名患有以下癌症类型之一的患者组成:晚期黑色素瘤、晚期nsclc、膀胱癌、cll、dlbcl、hcc、转移性乳腺癌、转移性crc、转移性rcc、多发性骨髓瘤、卵巢癌、sclc、滤泡性淋巴瘤、胰腺癌或头颈部癌。此外,本发明人已经表明,包含对应于上述(i)至(xxix)中列出的参数的数据的患者信息可用于预测这些癌症类型的死亡风险。因此,本文提及的癌症可以是选自由以下项组成的组的癌症:黑色素瘤(例如晚期黑色素瘤)、nsclc(例如晚期nsclc)、
膀胱癌、cll、dlbcl、hcc、转移性乳腺癌、转移性crc、转移性rcc、多发性骨髓瘤、卵巢癌、sclc、滤泡性淋巴瘤、胰腺癌和头颈部癌。
附图说明
[0224]
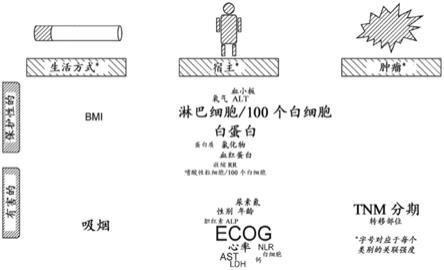
图1a和1c:分别显示ropro1和ropro2的风险比(hr)估计值和相应的置信区间(ci)(在标准正态参数尺度内)。2b和2d:分别显示ropro1和ropro2参数的“wordle”图:大字体对应于参数的高相关性。参数由参数类别生活方式、宿主和肿瘤显示。指示了保护和风险参数。保护参数的hr低于1,表明该参数的较高水平是有益的。有害参数的hr高于1,意味着参数值越高风险越高。参数缩写参见表20。
[0225]
图2a:显示了与参加临床1期研究bp29428的患者相比,flatiron health数据库中患者的ropro 1的概率密度函数图,该研究在实体瘤患者中调查了依米妥珠单抗和阿特珠单抗。结果表明bp29428中患者群体略右移,表明预后不良的患者比例较高。图2b:显示了与临床1期研究bp29428相比,flatiron health数据库中ropro1的概率密度函数图,两者均仅限于原发性膀胱癌。结果表明bp29428中患者群体向右移,表明预后不良的患者比例较高,在这种情况下,可能反映了先前治疗线数量的差异。
[0226]
图3a和3b显示了oak 3期临床研究中应答组对ropro1的纵向监测。x轴对应不同的时间点。第一线治疗(lot)的开始是最左边的点,结果事件发生的日期是最右边的点。在两者之间,以11天为步长显示事件之前的时间点。y轴对应于ropro1(组平均值)。每条曲线代表5个结果组之一。a:曲线从最上面的曲线依次向下表示:死亡患者、进展患者、病情稳定患者、和部分应答患者、完全应答患者。b:曲线从图右侧最上面的曲线依次向下表示:死亡患者、进展患者、病情稳定患者、部分应答患者、和完全应答患者。置信区间显示为每条曲线周围的阴影带。图3显示ropro1与治疗应答相关。
[0227]
图4a和4d显示为高和低rmhs患者绘制的km生存曲线。上图显示了在第一线治疗开始后,生存概率随时间(以天为单位)的变化(上下曲线分别代表具有高rmhs和低rmhs的患者)。下图显示了在第一线治疗开始后,具有高rmhs和低rmhs的患者数量随时间(以天为单位)的变化。图4b和4e分别显示了为具有高和低ropro1和ropro2的患者绘制的km生存曲线。上图显示了在第一线治疗开始后,生存概率随时间(以天为单位)的变化(下曲线代表具有ropro1或ropro2前5%的患者,而下曲线代表具有ropro1或ropro2剩余95%的患者)。下图显示了在第一线治疗开始后,具有高和低ropro1或ropro2的患者数量随时间(以天为单位)的变化。图4c和4f分别显示了由ropro 1和ropro2十分位数为患者绘制的km生存曲线。上图显示了在第一线治疗开始后,生存概率随时间(以天为单位)变化的。曲线从最上面的曲线向下依次表示:十分位数1到10。下图表示第一线治疗开始后,每个十分位数中的患者数量随的时间的变化(y轴;从顶部:十分位数1到10)。
[0228]
图5a
‑
d显示了ropro2在纵向监测中识别事件发生的能力。a:显示在相应事件(死亡、进展、应答)前几天内死亡患者(顶部曲线)、进展患者(中间曲线)或具有部分或完全应答的患者(底部曲线)的ropro2评分。对于死亡患者,ropro2评分朝着事件显著恶化(p=6.50
×
10
‑
14,图5b),基线时平均评分为0.09(sd 0.50),死亡前最后一次测量为0.30(sd0.54)。进展患者的ropro2评分也表现出显著但不太明显(图5c)的恶化(p=3.90x10
‑
11,图5c)。部分(n=191)和完全(n=11)应答者的ropro2评分朝着应答事件没有显著变化
(图5d)。
具体实施方式
[0229]
现在将描述形成模型和评分的示例性方法。应当理解,可以利用用于分析参数对死亡风险的贡献的替代统计技术以形成模型。示例包括参数(i)至(xxvi)或(i)至(xxix)中的全部参数,但如上所述,该方法可适用于仅选择这些参数和/或分别纳入除(i)至(xxvi)或(i)至(xxix)之外的参数。
[0230]
现在将模型和评分的两个示例描述为罗氏预后评分(ropro)1和2。ropro1是患者数据与相应参考参数平均值之差的26个参数(i)至(xxvi)的加权总和,而ropro 2是患者数据与相应参考参数平均值之差的29个参数(i)至(xxix)的加权总和。较高的ropro表示较高的死亡危险和较高的死亡风险,较低的ropro表示较低的死亡危险和较低的死亡风险。
[0231]
ropro的通用公式是∑
i
ln(hr(x
i
))(m
ij
‑
m
i
),其中hr(x
i
)是为参数i估计的hr,mi
i
是flatiron health数据库数据集中的参数平均值,m
ij
是参数i,i∈i时患者j的值。hr加权参数对评分的贡献,参数平均值的减法使评分集中在零附近。
[0232]
使用此方法生成的所有适应症的通用ropro1公式示例如下:
[0233]
‑
0.0364(白蛋白
‑
38.79) 0.278(ecog
‑
0.78) 0.00035(ldh
‑
273.99)
‑
0.00921(淋巴细胞/100个白细胞
‑
25.83)
‑
0.0427(血红蛋白
‑
12.28) 0.00034(alp
‑
108.93) 0.0549(nlr
‑
0.57)
‑
0.0265(氯化物
‑
101.58) 0.00603(心率
‑
83.37) 0.00373(ast
‑
25.98) 0.0103(年龄
‑
66.36) 0.0112(尿素氮
‑
17.33)
‑
0.0162(氧气
‑
96.42) 0.109(tnm分期
‑
2.98)
‑
0.0067(蛋白质
‑
69.7)
‑
0.00296(收缩rr
‑
129.58)
‑
0.0302(嗜酸性粒细胞/100个白细胞
‑
2.32) 0.0621(胆红素
‑
0.51) 0.07228(钙
‑
9.37) 0.16482(性别
‑
0.48)
‑
0.0075(bmi
‑
28.25) 0.256(吸烟
‑
0.36)
‑
0.00048(血小板
‑
272.01) 0.0531(转移部位的数量
‑
0.44)
‑
0.00334(alt
‑
24.63) 0.00082(白细胞
‑
12.78)。
[0234]
使用此方法生成的所有适应症的通用ropro2公式示例如下:
[0235]
0.01012(年龄
‑
66.695) 0.12264(性别
‑
0.502) 0.20044(吸烟
‑
0.581) 0.06476(转移部位的数量
‑
0.163) 0.23399(ecog
‑
0.834) 0.09786(nlr
‑
0.583)
‑
0.00801(bmi
‑
27.838)
‑
0.04095(氧气
‑
96.607)
‑
0.00303(收缩rr
‑
128.707) 0.00521(心率
‑
83.246)
‑
0.04637(hgb_t0
‑
12.092) 0.00927(白细胞
‑
11.077) 0.01108(尿素氮
‑
17.53) 0.11564(钙
‑
9.314)
‑
0.00078(血小板
‑
272.168)
‑
0.00623(淋巴细胞与白细胞的比率
‑
23.786) 0.00285(ast
‑
26.729) 0.00117(alp
‑
111.233)
‑
0.00978(蛋白质
‑
69.034)
‑
0.00252(alt
‑
25.152)
‑
0.04085(白蛋白
‑
37.798) 0.17365(胆红素
‑
0.523)
‑
0.01713(淋巴细胞
‑
3.683)
‑
0.00467(二氧化碳
‑
25.768)
‑
0.02951(氯化物
‑
101.369) 0.1176(单核细胞
‑
0.729)
‑
0.03171(嗜酸性粒细胞与白细胞的比率
‑
2.225) 0.00022(ldh
‑
286.624) 0.08136(肿瘤分期
‑
3.101)。
[0236]
表15显示了上述公式中参数的描述以及如何在ropro模型中测量和评估这些参数的示例。应当理解,在其他实施例中,可以以任何其他合适的方式测量参数并且可以使用不同的单位。分配给非数字参数的值,例如性别和吸烟史,可以自由选择,只要它们在训练数据和输入到患者评分的数据中一致使用即可。在上述公式所示的示例中,女性被赋予值0,男性被赋予值1。但是,如果在整个训练数据和患者数据中,女性被赋予值1,男性被赋予值
0,因为生成的权重值(ln(hr(x
i
))具有相反的符号,所以该参数对评分的贡献将保持不变,则为患者生成等同的评分。术语性别(gender/sex)在本文中可互换使用。该原则也适用于可以在不影响产生的评分的情况下进行数字缩放的所有参数,只要这种缩放在训练数据和患者输入数据上是一致的。
[0237]
在上面的公式中,ecog水平直接输入到模型中。使用了0、1、2、3和4的ecog水平。ecog值为5的受试者不包括在训练数据中。如公式所示,ecog水平训练数据的平均值为0.78。
[0238]
进一步,可以使用来自患有特定癌症适应症的受试者的数据,通过重新估计特定群组中的权重(hr(xi
i
))来产生针对每个癌症适应症的特定ropro公式。出于以下解释的验证的目的,在独立的临床研究中应用了通用评分,无需重新估计参数权重。
[0239]
为了计算患者的评分,将患者的26或29个参数(白蛋白、ecog、ldh等)的测量值输入到公式中。将患者每个参数的测量值插入公式中,以代替相应的参数标签。用于生成评分的flatiron health数据库中患者的患者ropro1范围为
‑
4.06至3.72,其中99%位于(
‑
2.12;2.00)。稍后将更详细地讨论flatiron health数据库。表15中讨论了用于每个参数的值。例如,对于“性别”参数,如果患者是男性,则赋予值1,如果患者是女性,则赋予值0。
[0240]
26个因素(i)至(xxvi),以及类似的29个因素(i)至(xxix),独立地贡献于定量预后风险评分,即“ropro”。
[0241]
ropro1和ropro2在两项独立的临床研究(1期和3期)中得到验证。此处发现与患者早期退出研究(不到3天)、无进展存活和总存活密切相关。ropro随时间的变化预示着随后的进展和死亡。
[0242]
在ropro1的开发中,发明人发现了39个与总存活(os)显著相关的参数,其中参数(i)至(xxvi)在多变量建模中独立贡献(表1a、图1a和1b)。由此产生的模型与死亡时间相关(r2=0.24),显著优于rmhs(在相同数据上r2=0.02)。
[0243]
在ropro2的开发中,发明人类似地发现参数(i)至(xxix)在多变量建模中独立贡献(表1b、图1c和1d)。由此产生的模型与死亡时间(r2=0.30)相关,甚至比ropro1更优于rmhs(在相同数据上r2=0.02)。
[0244]
表1a:最终ropro1 cox回归模型(os)和ropro参数描述。
[0245]
[0246][0247]
*对于连续变量:正常尺度内每1个标准偏差(sd)的风险比(hr),即根据标准
‑
正态转换参数估计。
[0248]
**tailhr:与具有特定低值(等于2.5%分位数)的人相比,具有特定高参数值(等于97.5%分位数)的患者的hr。针对其他模型参数进行了调整。
[0249]
平均值
[0250]
48.3%的患者为男性
[0251]
36.0%的患者有明确的吸烟史
[0252]
表1b:最终ropro2 cox回归模型(os)和ropro参数描述。
[0253][0254]1按变量尺度的危险比率(=每个测量单位),以及95%置信区间
[0255]2具有平均值 2sd的参数值的患者与具有平均值
‑2sd的值的患者的危险比率
[0256]3flatiron health数据中的平均值
[0257]4flatiron health数据的标准偏差
[0258]5编码1=男性,0=女性
[0259]6编码1=吸烟史,0=无吸烟史或未知
[0260]7如果nlr>3编码为1,如果nlr<=3编码为0
[0261]8编码细节可以在在线补充表1中找到
[0262]
在用于形成ropro1和ropro2模型的数据中,分别为每个受试者计算了ropro1和ropro2以及rmhs。图4a和4b显示了为ropro1和rmhs绘制的生存曲线。根据图4a中的低/高rmhs,存在明显的生存曲线分离hr 2.22(2.15;2.28)。图4b中ropro1的图显示了更好的生存曲线分离(hr4.72(4.57;4.87),表明高ropro1与死亡时间的相关性比高rmhs更强。此外,生存曲线可以以细粒度显示:样本可分为10个大小相同但增加ropro1(10%分位数)的子组。相应的kaplan
‑
meyer曲线有明显的分离,即,使用ropro1不仅可以剖析高风险和低风险患者,而且可以指定可很好区分的死亡风险等级。中位生存期在分位数上明显分开,最低分位数的中位生存期为2286天,而最高分位数为147天。与最低风险组(ropro<
‑
1.19)相比,来自最高风险组(ropro>1.05)的患者的hr为20.48(19.47
‑
21.55),p<2.23x10
‑
308
。
[0263]
ropro1和rmhs分别应用于flatiron health数据库中的每个数据群组。在所有群组中,通用ropro1在死亡时间的预后方面明显优于rmhs。对于cll,看到了群组特异性ropro1的最强性能改进(对于通用ropro1r2=0.11,对于cll特异性ropro1 r2=0.17)。对于转移性乳腺癌,我们通过纳入激素受体状况、her2neu状况和粒细胞/白细胞比率,获得了与死亡时间(从r2=0.10到r2=0.17)相关性的特别强的改善。
[0264]
ropro1评分在应用于独立数据集(不是来自flatiron health数据库的集)时表现良好。与具有低ropro1的患者(低于10%)相比,具有ropro1升高(高于10%)的晚期非小细胞肺癌患者的死亡风险增加了6.32倍(95%ci 5.95
‑
6.73)(p<2.23x10
‑
308)。
[0265]
与已建立的预后评分,如皇家马斯登医院评分(rmhs)(r2=0.001
‑
0.033,依赖于群组)相比,ropro1显示出与死亡时间的强相关性(r2=0.155
‑
0.239,依赖于群组),有了显著的改善。
[0266]
个体患者ropro2评分(通过将29个变量的每个的测量值输入公式得出)范围从
‑
3.22到3.61,其中99%的范围在
‑
2.33和2.22之间。较高的评分表明os的预后较差。
[0267]
图4d、4e和4f呈现了基于rmhs或ropro2的预后风险评分的比较。图4d显示了根据高/低rmhs(hr 2.37;95%ci 2.32
‑
2.43)的生存曲线的清晰分离。图4e描绘了具有最高10%ropro2评分的患者与其余90%的患者。根据ropro2的该分析显示,生存曲线的分离度(hr 4.66;95%ci4.56
‑
4.77)比rmhs更好,表明高ropro2评分与死亡时间的相关性比高rmhs更强。此外,将样本细分为十个大小相同但增加的ropro2评分(十分位数)的亚组显示各自的kaplan
‑
meier生存曲线明显分离,反映了较高风险亚组中较差的os(图4f)。中位生存期在十分位数上明显分开,其中最低十分位数的中位生存期为2,975天,而最高十分位数为118天。与最低风险组(评分<
‑
1.26)相比,最高风险患者(ropro2评分>1.13)的hr为25.79(95%ci 24.58
‑
27.06),p<2.23
×
10
‑
308。
[0268]
当ropro2和rmhs单独应用于群组时,通用ropro2公式在所有群组的所有性能指标方面再次明显优于rmhs。
[0269]
下面解释了ropro1和ropro2对临床试验数据的验证结果的更多示例。在这两项独立临床研究的验证分析中,评分显示与早期退出研究(3天内)、pfs和os的强相关性。
[0270]
应用于1期研究
[0271]
在早期肿瘤学临床试验中彻底了解患者群体对于结论性的数据解释和开发决策非常重要。ropro1和ropro2被回顾性地应用于1期首次人体研究bp29428(nct02323191)的患者,该研究调查了在患有不适合标准治疗的选择的局部晚期或转移性实体瘤的参与者
中,依米妥珠单抗和阿特珠单抗组合施用的安全性、药代动力学和初步抗肿瘤活性。
[0272]
ropro1和ropro2分别用于给bp29428研究中的患者一个ropro1和ropro2值,并将每个患者的ropro1和ropro2值与患者在研究中的结果进行比较,以确定ropro1和ropro2用于确定患者的预后的准确性。
[0273]
flatiron health数据集中的患者和参加bp29428的患者的ropro1近似正态分布,平均值约为0(图2a)。参与bp29428的患者的ropro1分布倾向于更多地向右延伸,表明bp29428中特定高风险患者的比例增加(图2a)。
[0274]
具有高ropro1的患者死亡风险更高,hr=4.99(2.59;9.63),p=1.5x10
‑6,与rmhs,hr=3.38(1.79;6.38),p=1.72x10
‑4)相比提供改进的区分。此外,ropro1可用于识别早期的退出研究。具有最高5%ropro1(n=11)的患者在研究中平均仅保持3天(表16),而这种区分对于rmhs是不可能的。如表4a和4b所示,ropro1分位数比rmhs更有效地表明研究的时间长度。
[0275]
在bp29428中,原发性膀胱癌诊断构成了最大的亚组(n=62)。与用于构建ropro1(所有阶段的混合)的flatiron health数据库中的膀胱群组相比,该亚组的晚期患者比例较高,平均有1.76( /
‑
1.00)条既往治疗线。因此,bp29428的ropro1分布向右移动(图2b),即bp29428膀胱亚组中有更多具有高ropro的患者。尽管如此,在该亚组中,ropro1也与os(p=4.86x10
‑7)密切相关。此外,来自最高ropro1 10%分位数(n=6)的所有患者在研究中仅保持1天(表17),表明即使先前治疗线的数量分布偏离flatiron health发现数据,ropro1也是有用的。
[0276]
ropro2与os的相关性在i期研究bp29428中得到复制(n=217,p=4.56x10
‑
14,r2=0.22,c
‑
指数=0.80)。
[0277]
具有ropro2>1.13(flatiron health中截止值等于90%分位数,n=11)的患者的os预后较差(hr 16.36;95%ci 7.95
‑
33.66),与rmhs相比提供了更好的区分(hr 3.38;95%ci 1.79
‑
6.38)。
[0278]
ropro2应用潜力的一个示例是它能够指示早期退出研究。具有ropro2>1.13(n=11,参见上面的截止值定义)的患者由于疾病进展或死亡全部早期退出研究(研究的平均时间为29天)。只有一名患者留在研究中直到第二个治疗周期。值得注意的是,按照研究方案,所有患者的ecog均为1。使用rmhs不可能有类似的区分水平(见表18)。
[0279]
应用于3期研究
[0280]
对3期研究结果进行了回顾性分析,以评估使用ropro1和ropro2作为排除标准的影响,并调查ropro1和ropro2随时间的变化是否指示后续事件。
[0281]
oak iii期研究(rittmeyer a,等人,2017)(nct02008227)在含铂化疗失败后的患有局部晚期或转移性nsclc参与者(n=1187)中评估了阿特珠单抗与多西他赛相比的疗效和安全性。
[0282]
ropro1和ropro2分别用于给nct02008227研究中的患者一个ropro1或ropro2值,并将每个患者的ropro1和ropro2值与患者在研究中的结果进行比较,以确定ropro1和ropro2用于确定患者的预后的准确性。
[0283]
再次,ropro1(r2=0.20,p=1.09x10
‑
59
)在对死亡时间的预后方面明显优于rmhs(r2=0.06,p=2.80x10
‑
18
)(表2)。此外,ropro1还与无进展存活相关(r2=0.06,p=
1.06x10
‑
17
)。
[0284]
我们评估了使用预后评分对治疗组之间os比较的潜在影响(表2)。在未调整的分析中,根据已发表的结果(graf e等人,1999),我们观察到阿特珠单抗与对照的hr为0.794(0.690;0.913)。使用ropro1作为协变量,效果估计值提高到0.780(0.678;0.898),而用rmhs调整稍微削弱了信号(0.801[0.692;0.922])。通过从最高的10%ropro1中排除患者,也观察到hr的改善(0.766[0.659;0.891])。尽管样品量减少,但与整个数据的分析(p=0.0012)相比,我们获得了更高的显著性(p=0.0006)。
[0285]
表2:在oak 3期临床研究的后验分析中使用预后评分对hr估计的影响
[0286][0287][0288]1与死亡时间的相关性(来自cox回归的rsq(r
‑
平方;r2))。
[0289]2999个复制数据集的中位数
[0290]
ropro2与os生存的相关性在iii期研究oak中复制(n=1,187,p=3.65x10
‑
56,r2=0.19,c
‑
指数=0.68)。具有ropro2>0.81(flatiron health中针对专用晚期nsclc ropro2的截止值等于90%分位数,n=76)的患者的os预后较差(hr 3.62;95%ci 2.82
‑
4.65),与rmhs相比再次提供了更好的区分(hr 1.97;95%ci 1.79
‑
2.31)。曲线下面积值再次优于rmhs。来自高ropro2类别的患者在研究中平均仅停留4.8个月(中位数为2.4个月)(参见表19)。
[0291]
还评估了使用预后评分比较治疗组之间的os的潜在影响。在未经调整的分析中,根据已发表的结果,观察到阿特珠单抗与多西他赛的hr为0.794(95%ci 0.690
–
0.913,p=
0.0012)。20通过排除ropro2>0.81的患者,观察到较低的hr(0.785;95%ci 0.678
–
0.909)。尽管导致样品量损失,但与整个数据集的分析(p=0.0012)相比,显著性水平(p=0.0012)几乎相同。
[0292]
如图3所示,还显示ropro1能够在纵向监测中区分事件组。死亡患者在死亡前99天的ropro1升高,平均ropro1为0.32(sd 0.45),并且朝着事件评分显著(p=8.78x10
‑
15
)增加,死亡前最后一次测量的平均ropro1为0.77(sd 0.48)。进展(黑色)患者在进展前66天开始显示显著增加(p=4.62x10
‑6),从平均ropro1为0.02(sd 0.45)到事件发生时平均ropro1为0.15(sd 0.46)。部分(n=191名患者)和完全应答者(n=11名患者)以低ropro1(平均值为
‑
0.10,sd 0.40)开始,其朝着应答事件没有显著变化(p=0.46)。
[0293]
最后,评估了ropro2在纵向监测中区分事件发生的能力(图5)。对于死亡的患者(顶部曲线),评分朝着事件显著恶化(p=6.50
×
10
‑
14,图5a、5b),基线时的平均评分为0.09(sd 0.50),死亡前最后一次测量为0.30(sd 0.54)。进展患者(中间曲线)也显示出显著但不太明显(图5a)的增加(p=3.90
×
10
‑
11,图5c)。部分(n=191)和完全(n=11)应答者(底部曲线)朝着应答事件并没有显著变化(图5a,5d)。
[0294]
如上所述,ropro1和ropro2在两个独立的临床研究(1期和3期)中验证,这两个研究都调查了免疫治疗。我们在研究bp29428(依米妥珠单抗和阿特珠单抗的组合治疗,nct02323191)中的分析表明,评分不仅与os相关,而且与特定的早期退出研究(少于3天之内)相关,如表16中ropro1所示。因此,使用ropro 1或ropro2排除非常高风险的患者可能有助于保护患者免受不必要的研究程序负担和潜在不良事件的影响。它还可以支持快速研究进行和降低试验成本,同时不会显著阻碍招募,因为可能只需要排除少数患者。同样,与化疗对照组相比,在nsclc的单药阿特珠单抗的oak 3期试验中排除10%具有最高ropro1或ropro2的患者确实增加了治疗效果,表明这些高风险患者从干涉中受益较少。我们的数据表明,ropro1和ropro2能够更准确地区分考虑到身体健康状况不佳的高退出风险患者和仍可从研究治疗中受益的患者。还可以定义患者排除/纳入标准的先验截止值,以便排除预先指定的患者部分(例如5%)。调查ropro1随着时间的变化,我们发现随后进展或死亡的患者呈稳步增加的趋势,而我们无法确定ropro1的过程与应答之间的明确相关性。但是,更大的患者数量可能会导致相应的发现。
[0295]
ropro1和ropro2易于使用,尽管它们使用大量参数,但大多数参数是经常规测量的和/或在临床常规中可用。这些参数组合在一个易于使用的简单评分中。进一步,对于计算患者的ropro,可以容忍缺失的参数,这意味着即使患者信息不完整,仍然可以生成评分。例如,当患者数据缺少模型中纳入的5
‑
10个参数时,仍然可以生成有用的评分。
[0296]
进一步,ropro1和ropro2可以应用于各种癌症适应症,由ropro1和ropro2在bp29428中的良好表现证实,其中40%的患者患有除用于建立评分的12种以外的癌症类型。癌症特异性模型可以仅使用来自患有特定癌症类型的受试者的数据生成,并且这些模型的示例在下面详细描述。癌症特异性模型可以优于通用模型,例如对于cll和转移性乳腺癌,但通用模型仍然可以产生有用的结果。
[0297]
易用性、跨癌症适应症的适用性和增加的预后能力进一步鼓励使用ropro1和ropro2进行群组比较,例如在fih研究中的剂量递增期间或用于解释与如bp29428所示的现实世界设置相比的研究结果,其中ropro1和ropro2分布与flatiron health群组不同。确定
了特定高危患者的存在,有助于解释整体研究结果。进一步,持续监测ropro1随着时间的变化,可能通过治疗出现的不良事件或超出肿瘤进展来增加治疗决策的信心。我们在oak中的分析表明,评分随时间恶化的高风险患者不会从治疗中受益。观察稳定的评分或甚至略微改进的评分可能表明治疗益处,并且可以
‑
除了其他考虑因素
‑
用于做出继续治疗的决定。
[0298]
当将ropro1或ropro2应用于二线或后线群组时,评分的附加参数可以包括先前治疗方案的数量和类型。正如我们对临床研究的分析所证实的那样,即使先前治疗线的数量在各组之间存在差异,ropro1和ropro2也非常有用。模型和评分中纳入的其他可选参数可能包括尿液、血液、(表观)遗传生物标志物和自我报告的健康(sudlow c等人,2015)和精细分析,例如与无进展存活(pfs)的关联。
[0299]
ropro1和ropro2证实了分析大型患者数据集的价值,导致以前不可能实现的粒度。尽管在回顾性现实世界数据分析中通常会遇到不确定性和不准确性(kahn mg等人,2016),但发明人的发现表明偏见已被克服。这得到了与文献结果的高度一致性、评分的跨群组适用性以及成功应用于独立临床研究数据的支持,这些数据产生了与flatiron health数据集相当的模型拟合质量。
[0300]
ropro1是通过在cox比例风险框架内评估131个人口统计学、临床和常规血液参数获得的。99,249名患者来自由肿瘤类型(非小细胞肺、小细胞肺、黑色素瘤、膀胱、乳腺、结直肠、肾细胞、卵巢、肝细胞、多发性骨髓瘤、慢性淋巴细胞白血病、弥漫性大b细胞淋巴瘤)定义的12个不同群组。包括所有治疗方案。
[0301]
训练数据从flatiron health数据库获得,该数据库源自包括超过210万名活跃美国癌症患者的280多个癌症诊所的电子健康记录(ehr)数据(https://flatiron.com/real
‑
world
‑
evidence/),[12
‑
2018]。flatiron health数据库具有纵向、人口统计学和地理多样性,这可能有利于形成广泛适用的模型。参数可以是数字的(例如年龄),也可以是非数字的(例如性别是女性或男性)。非数字参数被分配一个数值用于建模。如上所讨论,用于ropro1和ropro2模型中每个参数的值在表15中进行了讨论。例如,对于“性别”参数,如果患者是男性,则赋予值1,如果患者是女性,则赋予值0。分配给非数字参数的值,例如性别和吸烟史,可以自由选择,只要它们在训练数据和输入到患者评分的数据中一致使用即可。进一步,可以在不影响产生的评分的情况下缩放数值,只要这种缩放在输入到评分中的所有训练数据和患者数据上是一致的。
[0302]
该数据库包括结构化数据(例如,实验室值和处方药)和非结构化数据,例如,通过从医生的笔记和其他非结构化文档(例如,生物标志物报告)中通过技术支持的图表抽象收集的数据。
[0303]
数据库可以根据由癌症类型定义的群组进行组织:肝细胞癌(hcc)、晚期黑色素瘤、晚期非小细胞肺癌(nsclc)、小细胞肺癌(sclc)、膀胱癌、转移性肾细胞癌(rcc)、转移性结直肠癌(crc)、弥漫性大b
‑
细胞淋巴瘤(dlbcl)、卵巢癌、转移性乳腺癌、多发性骨髓瘤、慢性淋巴细胞白血病(cll)和任选的滤泡性淋巴瘤、胰腺癌和头颈部癌。在flatiron health数据库中,根据来自2014[国立癌症研究所。seer*stat软件,版本8.3.4。http://seer.cancer.gov/seerstat2018年2月9日访问]的监测、流行病学和最终结果数据中疾病流行率的估计,患者在年龄、性别和种族/民族方面与美国黑色素瘤、nsclc和rcc患者人群相似,但在本发明的其他实施例中,可以使用包括具有替代特征的患者的数据库。这在针对
特定人群定制模型方面可能是有利的。在flatiron health数据库中,所有群组数据集都包括人口统计数据、临床数据(例如癌症类型、疾病分期和合并症)、药物处方数据和常规血液生物标志物数据。
[0304]
flatiron health在2018年12月发布的数据,包括人口统计学、临床数据(如癌症类型、疾病分期和合并症)、药物处方数据和常规血液生物标志物数据被用于形成示例ropro1。总共有来自12个群组的99,249名患者可供分析:晚期黑色素瘤(n=3,543)、晚期非小细胞肺癌(nsclc)(n=33,575)、膀胱癌(n=4,570)、慢性淋巴细胞白血病(cll)(n=8,904)、弥漫性大b
‑
细胞淋巴瘤(dlbcl)(n=3,396)、肝细胞癌(hcc)(n=1,028)、转移性乳腺癌(n=12,425)、转移性结直肠癌(crc)(n=14,487)、转移性肾细胞癌(rcc)(n=4,057)、多发性骨髓瘤(n=5,345)、卵巢癌(n=3,713)、小细胞肺癌(sclc)(n=4,206)。对于最终分析,可得42个通用测量值和89个其他的群组特异性生物标志物。表1a中包括了对各自患者特征的描述。中位随访时间为23.3个月( /
‑
21.4sd),中位生存时间为20.4个月(95%ci 20.13至20.70)。
[0305]
flatiron health在2019年5月发布的数据,包括人口统计学、临床数据(如癌症类型、疾病分期和合并症)、药物处方数据和常规血液生物标志物数据被用于形成示例ropro2。总共有来自15个群组的110,538名患者可供分析:晚期黑色素瘤、晚期非小细胞肺癌(nsclc)、膀胱癌、慢性淋巴细胞白血病(cll)、弥漫性大b
‑
细胞淋巴瘤(dlbcl)、肝细胞癌(hcc)、转移性乳腺癌、转移性结直肠癌(crc)、转移性肾细胞癌(rcc)、多发性骨髓瘤、卵巢癌、小细胞肺癌(sclc)、滤泡性淋巴瘤、胰腺癌和头颈部癌。对于最终分析,可得45个通用测量值和99个其他的群组特异性生物标志物。表1b中包括了对各自患者特征的描述。中位生存时间为18.7个月(95%置信区间[ci]18.5
‑
18.9)。
[0306]
仅使用了超过25%的患者可用的参数,并排除了缺少第一线治疗信息的患者。
[0307]
为了形成模型,使用cox比例风险模型(cox dr,journal of the royal statistical society series b(methodological)vol.34)研究了训练数据中患者的总存活(os)。生存时间是从患者的第一线治疗开始(定义为t0)到“死亡”事件开始计算的,如真实世界死亡率表(curtis md等人,2018)中所编码。对于仅包括晚期/转移性患者的群组,第一线是第一个晚期/转移性治疗线。截尾随访时间计算为从t0到患者最后一次记录在案的(就诊、药物施用、样本采集等)与其诊所接触的日期之间的天数。对于用于建模的训练数据,我们使用了患者在t0之前的最后可用测量值。
[0308]
对于全部连续参数,排除与平均值相差超过4个标准差的观测值。使用missforest r包为每个群组单独输入缺失数据。(r core team,2013)。对于敏感性分析,重复分析,其中用群组参数平均值代替缺失的患者数据。
[0309]
可以对数据进行筛选,以便仅将重要参数纳入模型中。在形成示例模型时,作为初步筛选,每个参数都单独进行了分析。p值小于α1α=0.05/45=0.0011(bonferroni校正)的参数被认为适合建模并保留在训练数据中。参数按照它们在筛选分析中的重要性给定的顺序纳入模型中。为了将参数保留在模型中,需要纳入产生显著的模型改进的参数(p≤α1)。由于纳入另一个参数而失去重要性的参数从模型中去除。通过构建,该程序将家庭错误率控制在α=0.05,即所有参数在多次测试调整后均显著。
[0310]
对于连续变量,cox模型产生风险比(hr),其是每单位调查参数给出的:对于年龄,
例如,hr是每个1年的年龄差异的hr。因此,对于具有高绝对值的参数,尽管有压倒性的统计证据,但hr估计值的相关性似乎可以忽略不计。因此,也使用“tailhr”。tailhr是与具有特定低值(等于2.5%分位数)的人相比,具有特定高参数值(等于97.5%分位数)的患者的hr。然而,统计检验是基于完整的定量模型。
[0311]
修改的ropros
[0312]
如上所讨论,可以通过纳入其他参数或修改训练数据,例如,仅包括具有特定癌症类型的患者,来修改ropro1和ropro2模型和评分。针对所讨论的癌症类型,与上面讨论的通用ropro1和ropro2相比,特定模型和评分可以提高准确性。
[0313]
具有群组协变量的通用ropro1评分
[0314]
该评分由以下公式给出:
[0315]
‑
0.03644(白蛋白
‑
38.79) 0.27834(ecog
‑
0.78) 0.00035(ldh
‑
273.99)
‑
0.00921(淋巴细胞/100个白细胞
‑
25.83)
‑
0.04271(血红蛋白
‑
12.28) 0.00034(alp
‑
108.93) 0.05494(nlr
‑
0.57)
‑
0.02653(氯化物
‑
101.58) 0.00603(心率
‑
83.37) 0.00373(ast
‑
25.98) 0.01032(年龄
‑
66.36) 0.01123(尿素氮
‑
17.33)
‑
0.01622(氧气
‑
96.42) 0.1092(tnm分期
‑
2.98)
‑
0.00672(蛋白质
‑
69.7)
‑
0.00296(收缩压rr
‑
129.58)
‑
0.03019(嗜酸性粒细胞/100个白细胞
‑
2.32) 0.06207(胆红素
‑
0.51) 0.07228(钙
‑
9.37) 0.16482(性别
‑
0.48)
‑
0.0075(bmi
‑
28.25) 0.25569(吸烟
‑
0.36)
‑
0.00048(血小板
‑
272.01) 0.05308(转移部位的数量
‑
0.44)
‑
0.00334(alt
‑
24.63) 0.00082(白细胞
‑
12.78) 0.16954(晚期nsclc
‑
0.34) 0.20866(晚期黑色素瘤
‑
0.04) 0.33719(膀胱
‑
0.05)
‑
0.69241(cll
‑
0.09)
‑
1.28587(dlbcl
‑
0.03) 0.58248(hcc
‑
0.01)
‑
0.04801(转移性乳腺癌
‑
0.13)
‑
0.0726(转移性rcc
‑
0.04)
‑
0.76472(多发性骨髓瘤
‑
0.05)
‑
0.47683(卵巢
‑
0.04) 0.20785(sclc
‑
0.04)
[0316]
该评分通过在评分中纳入癌症类型的附加参数来考虑癌症类型。
[0317]
具有群组协变量的通用ropro2评分
[0318]
该评分由以下公式给出:0.00942(年龄
‑
66.695) 0.13976(性别
‑
0.502) 0.2006(吸烟
‑
0.581) 0.07037(转移部位的数量
‑
0.163) 0.22798(ecog
‑
0.834) 0.09204(nlr
‑
0.583)
‑
0.00734(bmi
‑
27.838)
‑
0.0393(氧气
‑
96.607)
‑
0.00283(sbp
‑
128.707) 0.00526(心率
‑
83.246)
‑
0.04512(hgb
‑
12.092) 0.00864(白细胞
‑
11.077) 0.01171(尿素氮
‑
17.53) 0.10861(钙
‑
9.314)
‑
0.00066(血小板
‑
272.168)
‑
0.00614(淋巴细胞与白细胞的比率
‑
23.786) 0.00342(ast
‑
26.729) 0.00095(alp
‑
111.233)
‑
0.00885(蛋白质
‑
69.034)
‑
0.00432(alt
‑
25.152)
‑
0.04085(白蛋白
‑
37.798) 0.09984(胆红素
‑
0.523)
‑
0.01623(淋巴细胞
‑
3.683)
‑
0.00467(二氧化碳
‑
25.768)
‑
0.02848(氯化物
‑
101.369) 0.10973(单核细胞
‑
0.729)
‑
0.02952(嗜酸性粒细胞与白细胞的比率
‑
2.225) 0.00055(ldh
‑
286.624) 0.0806(肿瘤分期
‑
3.101) 0.24079(晚期nsclc
‑
0.309) 0.17555(晚期黑色素瘤
‑
0.032) 0.23156(膀胱
‑
0.043)
‑
0.82379(cll
‑
0.079)
‑
1.32362(dlbcl
‑
0.033) 0.68852(hcc
‑
0.011)
‑
0.09865(转移性乳腺癌
‑
0.107) 0.06371(转移性rcc
‑
0.036)
‑
0.78937(多发性骨髓瘤
‑
0.057)
‑
0.50345(卵巢
‑
0.035) 0.28493(sclc
‑
0.04) 0.33059(头颈
‑
0.039)
‑
1.79085(滤泡
‑
0.004) 0.91282(胰腺
‑
0.045)。该评分通过在评分中纳入癌症类型的附加参数来考虑癌症类型。
[0319]
当应用于独立群组时,通过特定变量扩展ropro可能会很有趣,这些变量可能适用
于该群组。在这种情况下,可以通过在群组数据上拟合cox模型,使用原始ropro和新变量x作为参数来构建扩展的ropro。根据与用于构建ropro公式本身相同的原理,这会产生形式为ln(hr(ropro))*(roproj
–
平均(ropro)) ln(hr(x))*(xj
‑
平均(x))的公式。在该公式中,ropro和x的平均值是研究中观察到的平均值。对于ropro项,使用通用公式,即不重新估计根本的29个变量的权重。仅从数据中估计ropro本身的权重ln(hr(ropro)),以确定ropro和附加变量x的正确平衡。然后可以将扩展的ropro公式后验应用于新样本或先验于另一个样本。
[0320]
ropro分布可以在具有特定纳入标准的样本中偏移。典型情况可能是研究设计,其中要求所有患者对ropro变量xi取特定值z。在这种情况下,ropro分布可能会偏移wi(z
‑
mi),其中mi是训练数据中xi的平均值,wi是cox模型中的变量权重in(hr)。ropro截止值可以偏移wi(z
‑
mi)以使用ropro患者排除标准。例如,如果一项研究要求所有患者的ecog为1,则与训练数据(其平均ecog为0.83)相比,平均ropro2可能偏移1.264*(1
‑
0.82)~0.12。因此,ropro2截止值1.13应替换为1.25。作为另一个示例,her2阳性转移性乳腺癌患者的亚群组比其他转移性乳腺癌患者的预后要好得多,尽管已知her2过表达是乳腺癌发展的危险因素。这个悖论是众所周知的,并且可以通过专用靶向疗法的可用性和系统应用来解释。在ropro2应用中,对于阳性her_状况的患者,ropro公式(补充表7)的相应项
‑
0.708*(her2_状况
‑
0.206)给出值
‑
0.56。因此,在这种情况下,将ropro截止值偏移
‑
0.56可能是合适的。应该注意的是,her2变量不同于通用ropro变量,因为它直接影响治疗决策。在ropro训练数据中,绝大多数her2 患者接受靶向治疗(曲妥珠单抗、帕妥珠单抗等)。对于未接受靶向治疗的her2 患者,相应的ropro项将被缺少指定。通常,由于her2状况与治疗的相互作用,在疗效比较中,可根据实际研究设计决定ropro中是否适当纳入her2项。
[0321]
癌症特异性模型
[0322]
下面讨论的特定癌症模型和评分的创建方式与上述通用ropro1和ropro2模型相同,不同之处在于仅包括来自适当癌症类型的训练数据。
[0323]
特定于晚期黑色素瘤的ropro1评分由以下公式给出:
[0324]
‑
0.03255(白蛋白
‑
39.83) 0.28838(ecog
‑
0.7) 0.00046(ldh
‑
286.82)
‑
0.00931(淋巴细胞/100个白细胞
‑
21.7)
‑
0.03681(血红蛋白
‑
13.26) 0.00119(alp
‑
90.46) 0.13144(nlr
‑
0.61)
‑
0.02788(氯化物
‑
102.07) 0.00564(心率
‑
80.06) 0.00412(ast
‑
24.45) 0.00595(年龄
‑
65.15) 0.0086(尿素氮
‑
17.68)
‑
0.04493(氧气
‑
96.89) 0.12968(tnm分期
‑
3.03)
‑
0.017(蛋白质
‑
69.04)
‑
0.00271(收缩rr
‑
131.2)
‑
0.04086(嗜酸性粒细胞/100个白细胞
‑
2.53) 0.00564(胆红素
‑
0.56) 0.06153(钙
‑
9.34) 0.14823(性别
‑
0.67)
‑
0.00581(bmi
‑
29.07)
‑
0.00021(血小板
‑
255.36)
‑
0.02629(转移部位的数量
‑
0.99)
‑
0.0009(alt
‑
25.6) 0.00519(白细胞
‑
8.2)。
[0325]
表3:晚期黑色素瘤ropro1的最终ropro cox回归模型(os)。
[0326][0327]1hr=原始尺度的危险比
[0328]
特定于晚期nsclc的ropro1评分由以下公式给出:
[0329]
‑
0.028(白蛋白
‑
37.92)0.24063(ecog
‑
0.89)0.00065(ldh
‑
265.82)
‑
0.01143(淋巴细胞/100个白细胞
‑
18.89)
‑
0.03854(血红蛋白
‑
12.51) 0.00059(alp
‑
105.95) 0.06241(nlr
‑
0.78)
‑
0.02719(氯化物
‑
100.81) 0.0056(心率
‑
85.61) 0.00315(ast
‑
22.29) 0.00746(年龄
‑
67.64) 0.0103(尿素氮
‑
16.64)
‑
0.02669(氧气
‑
95.74) 0.12445(tnm分期
‑
3.31)
‑
0.00811(蛋白质
‑
68.83)
‑
0.00285(收缩rr
‑
127.43)
‑
0.02494(嗜酸性粒细胞/100个白细胞
‑
2.35) 0.08866(胆红素
‑
0.47) 0.0813(钙
‑
9.36) 0.19274(性别
‑
0.53)
‑
0.00726(bmi
‑
27.1) 0.17495(吸烟
‑
0.87)
‑
0.00033(血小板
‑
294.59) 0.08169(转移部位的数量
‑
0.44)
‑
0.00399(alt
‑
23.17) 0.01166(白细胞
‑
9.29) 0.05736(鳞状细胞
‑
0.26)
‑
0.23384(原发部位肿瘤_pdl1
‑
0.28)
‑
0.47035(alk
‑
0.03)
‑
0.38758(egfr
‑
0.14) 0.08973(kras
‑
0.3)
[0330]
表4:晚期nsclc ropro1的最终ropro cox回归模型(os)。
[0331]
参数单位hr1[95%ci]p值白蛋白g/l0.972[0.969;0.976]1.07e
‑
48
ecog无1.272[1.243;1.302]1.62e
‑
92ldhu/l1.001[1.001;1.001]1.43e
‑
21淋巴细胞/100个白细胞%0.989[0.986;0.991]6.87e
‑
18血红蛋白g/dl0.962[0.954;0.971]1.75e
‑
17alpu/l1.001[1.000;1.001]3.87e
‑
12nlr无1.064[1.019;1.112]5.34e
‑
03氯化物mmol/l0.973[0.969;0.977]4.11e
‑
39心率bpm1.006[1.005;1.006]1.90e
‑
38astu/l1.003[1.001;1.005]2.84e
‑
04年龄无1.007[1.006;1.009]1.26e
‑
20尿素氮mg/dl1.010[1.008;1.013]2.53e
‑
21氧气%0.974[0.967;0.980]6.02e
‑
15tnm分期无1.133[1.113;1.153]1.09e
‑
42蛋白质g/l0.992[0.989;0.994]2.29e
‑
10收缩rrmmhg0.997[0.996;0.998]3.87e
‑
14嗜酸性粒细胞/100个白细胞%0.975[0.967;0.984]6.55e
‑
08胆红素mg/dl1.093[1.023;1.167]7.92e
‑
03钙mg/dl1.085[1.058;1.112]9.13e
‑
11性别无1.213[1.180;1.247]1.21e
‑
42bmikg/m20.993[0.991;0.995]1.81e
‑
12吸烟无1.191[1.141;1.243]1.05e
‑
15血小板10*9/l1.000[1.000;1.000]1.92e
‑
05转移部位的数量无1.085[1.068;1.103]1.08e
‑
23altu/l0.996[0.995;0.997]7.26e
‑
10白细胞10*9/l1.012[1.009;1.015]2.57e
‑
13squamouscell2无1.059[1.027;1.092]2.83e
‑
04primarysitetumor_pdl13无0.791[0.710;0.883]2.64e
‑
05alk4无0.625[0.558;0.700]5.38e
‑
16egfr5无0.679[0.643;0.716]7.37e
‑
45kras6无1.094[1.034;1.158]1.92e
‑
03
[0332]1hr=原始尺度的危险比
[0333]2鳞状细胞癌与非鳞状细胞癌
[0334]3原发肿瘤中的pdl1状况
[0335]4存在alk重排,血液、肿瘤部位和转移部位的评估一致
[0336]5egfr突变的存在,血液、肿瘤部位和转移部位的评估一致
[0337]6kras突变的存在,血液、肿瘤部位和转移部位的评估一致
[0338]
特定于膀胱癌的ropro1评分由以下公式给出:
[0339]
‑
0.03776(白蛋白
‑
38.24) 0.31113(ecog
‑
0.86)
‑
0.0000006(ldh
‑
207.51)
‑
0.01648(淋巴细胞/100个白细胞
‑
19.98)
‑
0.05865(血红蛋白
‑
11.79) 0.00199(alp
‑
102.19)
‑
0.02476(nlr
‑
0.75)
‑
0.02689(氯化物
‑
101.84) 0.0067(心率
‑
81.99) 0.01477(ast
‑
20.89) 0.00582(年龄
‑
70.66) 0.00883(尿素氮
‑
21.95)
‑
0.01548(氧气
‑
96.77)
‑
0.05903(tnm分期
‑
3.12)
‑
0.01324(蛋白质
‑
69.3)
‑
0.00097(收缩rr
‑
129.7)
‑
0.0303(嗜酸性粒细胞/100个白细胞
‑
2.66) 0.16313(胆红素
‑
0.45) 0.20268(钙
‑
9.35) 0.14791(性别
‑
0.74)
‑
0.0055(bmi
‑
27.56) 0.03807(吸烟
‑
0)
‑
0.00046(血小板
‑
291.95) 0.08332(转移部位的数量
‑
0.38)
‑
0.00943(alt
‑
19.7) 0.00372(白细胞
‑
8.57)
‑
0.29635(手术
‑
0.5)
‑
0.09292(n分期
‑
0.87) 0.0882(t分期
‑
2.5)
[0340]
表5:膀胱癌ropro1的最终ropro cox回归模型(os)。
[0341][0342][0343]1hr=原始尺度的危险比
[0344]2表明患者是否进行了膀胱切除术或其他相关手术
[0345]3初诊时的n分期
[0346]4初诊时的t分期
[0347]
特定于cll的ropro1评分由以下公式给出:
[0348]
‑
0.03867(白蛋白
‑
41.27) 0.41112(ecog
‑
0.61) 0.00035(ldh
‑
257.53)
‑
0.00048(淋巴细胞/100个白细胞
‑
67.49) 0.00858(血红蛋白
‑
11.9) 0.00322(alp
‑
86.29) 0.003(nlr
‑
0.16)
‑
0.0278(氯化物
‑
103.45) 0.00728(心率
‑
77.61) 0.00348(ast
‑
24.35) 0.05572(年龄
‑
69.71) 0.00942(尿素氮
‑
20.19)
‑
0.07428(氧气
‑
96.72) 0.01033(tnm分期
‑
1.38)
‑
0.00604(蛋白质
‑
65.51)
‑
0.00352(收缩rr
‑
129.82) 0.01924(嗜酸性粒细胞/100个白细胞
‑
1.18) 0.0243(胆红素
‑
0.64) 0.04474(钙
‑
9.26) 0.28007(性别
‑
0.62)
‑
0.01238(bmi
‑
29.11) 1.28681(吸烟
‑
0.01)
‑
0.00108(血小板
‑
165.63) 0.6591(转移部位的数量
‑
0.01)
‑
0.00752(alt
‑
22.11)
‑
0.00108(白细胞
‑
57.72)
‑
0.02779(血细胞比容
‑
36.55) 0.01526(mono_leuko
‑
6.81) 0.4047(17pdel状况
‑
0.09)
[0349]
表6:cll ropro1的最终ropro1 cox回归模型(os)。
[0350][0351]
[0352]1hr=原始尺度的危险比
[0353]217p缺失的患者状况
[0354]
特定于dlbcl的ropro1评分由以下公式给出:
[0355]
‑
0.01324(白蛋白
‑
38.76) 0.41084(ecog
‑
0.78) 0.00051(ldh
‑
330)
‑
0.00259(淋巴细胞/100个白细胞
‑
21.57)
‑
0.02629(血红蛋白
‑
12.33) 0.00246(alp
‑
94.94)
‑
0.14718(nlr
‑
0.67)
‑
0.01611(氯化物
‑
101.62) 0.00186(心率
‑
83.71) 0.00324(ast
‑
27.74) 0.03897(年龄
‑
65.41) 0.0115(尿素氮
‑
18.02)
‑
0.08422(氧气
‑
97.03) 0.11178(tnm分期
‑
2.8)
‑
0.01996(蛋白质
‑
67.65) 0.00247(收缩rr
‑
129.35) 0.03503(嗜酸性粒细胞/100个白细胞
‑
2.42)
‑
0.0067(胆红素
‑
0.6)
‑
0.08837(钙
‑
9.45) 0.21277(性别
‑
0.54)
‑
0.01197(bmi
‑
29.21)
‑
0.32111(吸烟
‑
0)
‑
0.00116(血小板
‑
264.91) 0.01659(转移部位的数量
‑
0.64)
‑
0.00427(alt
‑
25.71) 0.01014(白细胞
‑
8.06) 0.48816(bm_cd5
‑
0.19)
[0356]
表7:dlcbl ropro1的最终ropro1 cox回归模型(os)。
[0357][0358]1hr=原始尺度的危险比
[0359]2ihc或流式细胞术报告的骨髓中的cd5表达状况
[0360]
特定于hcc的ropro1评分由以下公式给出:
[0361]
‑
0.04636(白蛋白
‑
34.77) 0.09009(ecog
‑
0.85)
‑
0.00024(ldh
‑
242.97)
‑
0.00747(淋巴细胞/100个白细胞
‑
21.85)
‑
0.03135(血红蛋白
‑
12.56) 0.0009(alp
‑
190.83) 0.01655(nlr
‑
0.66)
‑
0.01749(氯化物
‑
101.53) 0.00797(心率
‑
79.59) 0.00375(ast
‑
81.06) 0.00472(年龄
‑
66.35) 0.01482(尿素氮
‑
16.98)
‑
0.05141(氧气
‑
97.04) 0.24331(tnm分期
‑
3.33) 0.00045(蛋白质
‑
71.86) 0.00075(收缩rr
‑
128.81)
‑
0.04362(嗜酸性粒细胞/100个白细胞
‑
2.55) 0.10363(胆红素
‑
1.23) 0.07832(钙
‑
9.13) 0.13751(性别
‑
0.8) 0.00405(bmi
‑
27.52)
‑
0.87098(吸烟
‑
0.01) 0.00044(血小板
‑
194.03) 0.02497(转移部位的数量
‑
0.2)
‑
0.00273(alt
‑
56.13) 0.0234(白细胞
‑
6.53) 0.34357(isascites
‑
0.25)
[0362]
表8:hcc ropro1的最终ropro 1 cox回归模型(os)。
[0363]
参数单位hr1[95%ci]p值白蛋白g/l0.955[0.936;0.974]6.05e
‑
06ecog无1.094[0.964;1.242]1.64e
‑
01ldhu/l1.000[0.999;1.001]6.18e
‑
01淋巴细胞/100个白细胞%0.993[0.980;1.006]2.59e
‑
01血红蛋白g/dl0.969[0.923;1.018]2.10e
‑
01alpu/l1.001[1.000;1.002]1.30e
‑
02nlr无1.017[0.825;1.253]8.77e
‑
01氯化物mmol/l0.983[0.96;1.006]1.43e
‑
01心率bpm1.008[1.003;1.013]4.08e
‑
03astu/l1.004[1.002;1.006]7.55e
‑
05年龄无1.005[0.996;1.013]2.62e
‑
01尿素氮mg/dl1.015[1.005;1.025]3.32e
‑
03氧气%0.950[0.897;1.006]7.67e
‑
02tnm分期无1.275[1.134;1.435]5.05e
‑
05蛋白质g/l1.000[0.989;1.012]9.38e
‑
01收缩rrmmhg1.001[0.996;1.005]7.39e
‑
01嗜酸性粒细胞/100个白细胞%0.957[0.908;1.009]1.06e
‑
01胆红素mg/dl1.109[1.019;1.207]1.67e
‑
02钙mg/dl1.081[0.911;1.285]3.72e
‑
01性别无1.147[0.945;1.394]1.66e
‑
01bmikg/m21.004[0.991;1.018]5.55e
‑
01吸烟无0.419[0.154;1.139]8.83e
‑
02血小板10*9/l1.000[0.999;1.001]3.61e
‑
01转移部位的数量无1.025[0.903;1.165]7.01e
‑
01altu/l0.997[0.994;1.000]5.48e
‑
02白细胞10*9/l1.024[0.982;1.068]2.75e
‑
01isascites2%1.410[1.172;1.696]2.70e
‑
04
[0364]1hr=原始尺度的危险比
[0365]2表明患者是否在开始全身疗法前60天或之内有记录的腹水证据
[0366]
特定于转移性乳腺癌的ropro1评分由以下公式给出:
[0367]
‑
0.03505(白蛋白
‑
40.26) 0.27677(ecog
‑
0.65) 0.00036(ldh
‑
279.9)
‑
0.02201(淋巴细胞/100个白细胞
‑
25.19)
‑
0.05064(血红蛋白
‑
12.57) 0.0005(alp
‑
116.55)0.0224(nlr
‑
0.39)
‑
0.00573(氯化物
‑
102.11) 0.00426(心率
‑
84.54) 0.00453(ast
‑
30.73) 0.00347(年龄
‑
62.48) 0.0056(尿素氮
‑
15.74)
‑
0.00592(氧气
‑
96.52)
‑
0.05314(tnm分期
‑
2.79)
‑
0.00482(蛋白质
‑
69.92)
‑
0.00228(收缩rr
‑
132.42)
‑
0.04465(嗜酸性粒细胞/100个白细胞
‑
2.18) 0.00263(胆红素
‑
0.48) 0.07961(钙
‑
9.47)
‑
0.06088(性别
‑
0.01)
‑
0.00505(bmi
‑
29.66) 0.30504(吸烟
‑
0)
‑
0.00041(血小板
‑
259.77) 0.01433(转移部位的数量
‑
0.65)
‑
0.00285(alt
‑
26.76)
‑
0.01321(白细胞
‑
7.11)
‑
0.00912(粒细胞_白细胞
‑
65.19)
‑
0.66376(状况_er
‑
0.75)
‑
0.32253(状况_pr
‑
0.21)
‑
0.64684(状况_her2
‑
0.58)
[0368]
表9:转移性乳腺癌ropro1的最终ropro1 cox回归模型(os)。
[0369]
[0370][0371]1hr=原始尺度的危险比
[0372]2雌激素受体状况
[0373]3孕激素受体状况
[0374]4ihc或流式细胞术报告的人表皮生长因子受体2
[0375]
特定于转移性crc的ropro1评分由以下公式给出:
[0376]
‑
0.04114(白蛋白
‑
38.65) 0.31521(ecog
‑
0.7) 0.00027(ldh
‑
321.84)
‑
0.01522(淋巴细胞/100个白细胞
‑
22.63)
‑
0.01996(血红蛋白
‑
12.03) 0.00019(alp
‑
141.96) 0.02894(nlr
‑
0.49)
‑
0.02129(氯化物
‑
101.75) 0.00589(心率
‑
82.9) 0.00545(ast
‑
30.64) 0.01066(年龄
‑
63.59) 0.01004(尿素氮
‑
15.01)
‑
0.02764(氧气
‑
97.15) 0.11828(tnm分期
‑
3.48)
‑
0.00019(蛋白质
‑
70.32)
‑
0.0026(收缩rr
‑
130.17)
‑
0.00342(嗜酸性粒细胞/100个白细胞
‑
2.81) 0.11769(胆红素
‑
0.55) 0.05607(钙
‑
9.31) 0.08277(性别
‑
0.56)
‑
0.00752(bmi
‑
28.13) 0.0168(吸烟
‑
0)
‑
0.00067(血小板
‑
298.33) 0.05164(转移部位的数量
‑
0.51)
‑
0.00523(alt
‑
27.14)
‑
0.00154(白细胞
‑
8.04) 0.50779(状况_braf
‑
0.11) 0.17346(状况_kras
‑
0.45) 0.2077(msimod_primary
‑
0.06)
[0377]
表10:转移性crc ropro1的最终ropro1 cox回归模型(os)。
[0378]
[0379][0380]1hr=原始尺度的危险比
[0381]2存在braf突变
[0382]3存在kras突变
[0383]4在初生组织中评估,msi
‑
h和缺失mmr蛋白表达归入一类
[0384]
特定于转移性rcc的ropro1评分由以下公式给出:
[0385]
‑
0.04107(白蛋白
‑
38.71) 0.22807(ecog
‑
0.81) 0.00066(ldh
‑
239.9)
‑
0.0166(淋巴细胞/100个白细胞
‑
21.81)
‑
0.03591(血红蛋白
‑
12.34) 0.00042(alp
‑
102.79)
‑
0.07151(nlr
‑
0.59)
‑
0.04034(氯化物
‑
101.67) 0.00675(心率
‑
80.99) 0.01167(ast
‑
21.98) 0.00478(年龄
‑
65.5) 0.01264(尿素氮
‑
20.71)
‑
0.00236(氧气
‑
96.65) 0.10591(tnm分期
‑
3.11)
‑
0.01258(蛋白质
‑
70.59)
‑
0.00152(收缩rr
‑
130.68)
‑
0.03656(嗜酸性粒细胞/100个白细胞
‑
2.54)
‑
0.08249(胆红素
‑
0.5) 0.05246(钙
‑
9.46)
‑
0.01377(性别
‑
0.7)
‑
0.00665(bmi
‑
30.17)
‑
0.04439(吸烟
‑
0.57)
‑
0.00052(血小板
‑
286.2) 0.03115(转移部位的数量
‑
0.71)
‑
0.01082(alt
‑
23.41) 0.03307(白细胞
‑
8.02)
‑
0.40166(肾切除术
‑
0.68)
‑
0.37353(透明细胞
‑
0.7)
[0386]
表11:转移性rcc ropro1的最终ropro1 cox回归模型(os)。
[0387]
参数单位hr1[95%ci]p值白蛋白g/l0.960[0.949;0.971]3.52e
‑
12
ecog无1.256[1.166;1.354]2.27e
‑
09ldhu/l1.001[1.000;1.001]3.81e
‑
03淋巴细胞/100个白细胞%0.984[0.976;0.991]2.45e
‑
05血红蛋白g/dl0.965[0.938;0.993]1.35e
‑
02alpu/l1.000[0.999;1.001]3.71e
‑
01nlr无0.931[0.832;1.041]2.11e
‑
01氯化物mmol/l0.960[0.948;0.973]4.05e
‑
09心率bpm1.007[1.004;1.010]6.23e
‑
06astu/l1.012[1.007;1.016]5.35e
‑
07年龄无1.005[1.000;1.009]4.25e
‑
02尿素氮mg/dl1.013[1.007;1.018]3.35e
‑
06氧气%0.998[0.971;1.025]8.63e
‑
01tnm分期无1.112[1.054;1.173]1.00e
‑
04蛋白质g/l0.988[0.980;0.995]1.44e
‑
03收缩rrmmhg0.998[0.996;1.001]2.08e
‑
01嗜酸性粒细胞/100个白细胞%0.964[0.933;0.996]2.64e
‑
02胆红素mg/dl0.921[0.764;1.109]3.85e
‑
01钙mg/dl1.054[0.980;1.133]1.56e
‑
01性别无0.986[0.899;1.082]7.71e
‑
01bmikg/m20.993[0.988;0.999]1.94e
‑
02吸烟无0.957[0.879;1.041]3.04e
‑
01血小板10*9/l0.999[0.999;1.000]4.48e
‑
02转移部位的数量无1.032[0.993;1.071]1.05e
‑
01altu/l0.989[0.986;0.993]1.74e
‑
08白细胞10*9/l1.034[1.015;1.053]3.79e
‑
04肾切除术2无0.669[0.598;0.748]2.01e
‑
12透明细胞3无0.688[0.628;0.754]1.55e
‑
15
[0388]1hr=原始尺度的危险比
[0389]2患者是否进行过肾切除术
[0390]3透明细胞癌是/否
[0391]
特定于多发性骨髓瘤的评分由以下公式给出:
[0392]
‑
0.03132(白蛋白
‑
37.7) 0.40645(ecog
‑
0.83) 0.00093(ldh
‑
203.06)
‑
0.00781(淋巴细胞/100个白细胞
‑
29.79)
‑
0.04835(血红蛋白
‑
10.98) 0.00219(alp
‑
82.55)
‑
0.07473(nlr
‑
0.3)
‑
0.01956(氯化物
‑
102.06) 0.00436(心率
‑
80.65) 0.00191(ast
‑
24.06) 0.03613(年龄
‑
68.6) 0.01272(尿素氮
‑
22.03)
‑
0.01123(氧气
‑
97.07) 0.23461(tnm分期
‑
1.97)
‑
0.00372(蛋白质
‑
82.13)
‑
0.00398(收缩rr
‑
134.69)
‑
0.04269(嗜酸性粒细胞/100个白细胞
‑
2.42) 0.30565(胆红素
‑
0.5) 0.01936(钙
‑
9.44) 0.13929(性别
‑
0.54)
‑
0.00452(bmi
‑
29.26) 0.9616(吸烟
‑
0)
‑
0.00132(血小板
‑
223.01) 0.05053(转移部位的数量
‑
0.09)
‑
0.00309(alt
‑
23.53) 0.00522(白细胞
‑
6.95) 0.3403(确定的异常
‑
0.26)
‑
0.23267(m蛋白iga
‑
0.19)
‑
0.23776(m蛋白igg
‑
0.54)
‑
0.45875(轻链κ
‑
0.56)
‑
0.32882(轻链λ
‑
0.34)
[0393]
表12:多发性骨髓瘤ropro1的最终ropro1 cox回归模型(os)。
[0394][0395][0396]1hr=原始尺度的危险比
[0397]2测试基因是否确定为异常
[0398]3患者m蛋白的免疫球蛋白分类是否为iga
[0399]4患者m蛋白的免疫球蛋白分类是否为igg5患者涉及的轻链是否为κ6患者涉及的轻链是否为λ
[0400]
特定于卵巢癌的ropro1评分由以下公式给出:
[0401]
‑
0.03337(白蛋白
‑
38.74) 0.35052(ecog
‑
0.77) 0.00022(ldh
‑
261.65)
‑
0.00104(淋巴细胞/100个白细胞
‑
23.59)
‑
0.01649(血红蛋白
‑
11.84) 0.0017(alp
‑
92.92)0.0684(nlr
‑
0.49) 0.00501(氯化物
‑
101.92) 0.00396(心率
‑
84.27) 0.00725(ast
‑
23.74) 0.01471(年龄
‑
64.54) 0.02218(尿素氮
‑
15.47)
‑
0.00578(氧气
‑
96.68) 0.46146(tnm分期
‑
3.13)
‑
0.00401(蛋白质
‑
69.42)
‑
0.00307(收缩rr
‑
128.24)
‑
0.06112(嗜酸性粒细胞/100个白细胞
‑
2.53)
‑
0.11501(胆红素
‑
0.4) 0.07324(钙
‑
9.38) 0.00015(性别
‑
0) 0.58224(bmi
‑
28.63)
‑
0.00098(吸烟
‑
0) 0.06139(血小板
‑
333.29)
‑
0.00837(转移部位的数量
‑
0.21) 0.01713(alt
‑
21.46)
‑
0.3742(白细胞
‑
0.82) 0.41366(透明细胞
‑
0.07)
[0402]
表13:卵巢癌ropro1的最终ropro1 cox回归模型(os)。
[0403][0404][0405]1hr=原始尺度的危险比
[0406]2患者初步诊断为卵巢癌的手术治疗后的减瘤程度
[0407]3透明细胞癌是/否
[0408]
特定于sclc的ropro1评分由以下公式给出:
[0409]
‑
0.01875(白蛋白
‑
38.7) 0.14992(ecog
‑
0.94) 0.00018(ldh
‑
349.5)
‑
0.00919(淋巴细胞/100个白细胞
‑
21.1)
‑
0.01399(血红蛋白
‑
12.88)
‑
0.00014(alp
‑
112.17) 0.00145(nlr
‑
0.7)
‑
0.01345(氯化物
‑
99.97) 0.00372(心率
‑
85.7) 0.00486(ast
‑
29.1) 0.01048(年龄
‑
66.8) 0.01096(尿素氮
‑
16.02)
‑
0.00712(氧气
‑
95.65) 0.28747(tnm分期
‑
3.55)
‑
0.00597(蛋白质
‑
68.55)
‑
0.0045(收缩rr
‑
128.2)
‑
0.02105(嗜酸性粒细胞/100个白细胞
‑
1.99)
‑
0.07518(胆红素
‑
0.5) 0.00318(钙
‑
9.36) 0.16448(性别
‑
0.48)
‑
0.01073(bmi
‑
27.94) 0.11721(吸烟
‑
0.98)
‑
0.00127(血小板
‑
274.14) 0.02463(转移部位的数量
‑
0.38)
‑
0.00172(alt
‑
27.89)
‑
0.00026(白细胞
‑
9) 0.58755(sclc分期
‑
0.65)
[0410]
表14:sclc ropro1的最终ropro1 cox回归模型(os)。
[0411]
参数单位hr1[95%ci]p值白蛋白g/l0.981[0.970;0.993]1.13e
‑
03ecog无1.162[1.093;1.235]1.45e
‑
06ldhu/l1.000[1.000;1.000]4.73e
‑
02淋巴细胞/100个白细胞%0.991[0.985;0.997]3.43e
‑
03血红蛋白g/dl0.986[0.963;1.010]2.56e
‑
01alpu/l1.000[0.999;1.000]5.83e
‑
01nlr无1.001[0.899;1.115]9.79e
‑
01氯化物mmol/l0.987[0.978;0.996]4.27e
‑
03心率bpm1.004[1.001;1.006]3.31e
‑
03astu/l1.005[1.002;1.008]4.17e
‑
04年龄无1.011[1.006;1.015]1.04e
‑
05尿素氮mg/dl1.011[1.005;1.017]4.16e
‑
04氧气%0.993[0.971;1.015]5.28e
‑
01tnm分期无1.333[1.223;1.453]6.12e
‑
11蛋白质g/l0.994[0.986;1.002]1.26e
‑
01收缩rrmmhg0.996[0.993;0.998]1.31e
‑
05嗜酸性粒细胞/100个白细胞%0.979[0.947;1.012]2.12e
‑
01胆红素mg/dl0.928[0.807;1.067]2.91e
‑
01钙mg/dl1.003[0.916;1.098]9.45e
‑
01性别无1.179[1.090;1.275]3.70e
‑
05bmikg/m20.989[0.984;0.995]1.83e
‑
04吸烟无1.124[0.871;1.452]3.69e
‑
01血小板10*9/l0.999[0.998;0.999]8.66e
‑
09转移部位的数量无1.025[0.978;1.074]3.00e
‑
01altu/l0.998[0.996;1.001]1.76e
‑
01白细胞10*9/l1.000[0.989;1.010]9.60e
‑
01sclc分期2无1.800[1.594;2.032]2.34e
‑
21
[0412]1hr=原始尺度的危险比
[0413]2通过临床评估获得的广泛疾病与局限性疾病
[0414]
群组特定的ropro2模型显示,群组之间变量相关性的一致性通常很高。对于慢性淋巴细胞白血病(cll),看到了群组特异性重新估计变量权重的最强性能改进(对于通用ropro2,r2=0.12,c
‑
指数=0.70,3个月auc=0.81;对于cll特定的ropro2,r2=0.17,c
‑
指数=0.74,3个月auc=0.83)。通过纳入癌症特异性生物标志物(激素受体状况和人类表皮生长因子受体2[her2]
‑
neu状况),转移性乳腺癌模型显示最大的改进(对于通用ropro2,r2=0.12,c
‑
指数=0.66,3个月auc=0.83;对于特定ropro2,r2=0.21,c
‑
指数=0.72,3个月auc=0.83)。
[0415]
特定于晚期nsclc的ropro2评分由以下公式给出:0.00653(年龄
‑
67.981) 0.16544(性别
‑
0.537) 0.29991(吸烟
‑
0.877) 0.12237(转移部位的数量
‑
0.174) 0.19453(ecog
‑
0.922) 0.02572(nlr
‑
0.766)
‑
0.00725(bmi
‑
26.899)
‑
0.03658(氧气
‑
95.996)
‑
0.00259(sbp
‑
126.983) 0.00518(心率
‑
85.716)
‑
0.04524(hgb
‑
12.327) 0.00529(白细胞
‑
9.807) 0.01222(尿素氮
‑
17.129) 0.14336(钙
‑
9.323)
‑
0.00051(血小板
‑
298.177)
‑
0.01381(血液中淋巴细胞/100个白细胞
‑
16.727) 0.00251(ast
‑
22.414) 0.00144(alp
‑
102.824)
‑
0.01326(蛋白质
‑
68.696)
‑
0.00416(alt
‑
23.117)
‑
0.03692(白蛋白
‑
37.062) 0.18286(胆红素
‑
0.467) 0.01683(淋巴细胞
‑
1.465)
‑
0.00542(二氧化碳
‑
26.047)
‑
0.03064(氯化物
‑
100.545) 0.11354(单核细胞
‑
0.672)
‑
0.03235(血液中嗜酸性粒细胞/100个白细胞
‑
2.07) 0.00055(ldh
‑
280.888) 0.10307(肿瘤分期
‑
3.465) 0.05508(鳞状细胞
‑
0.269)
‑
0.18049(原发部位肿瘤_pdl1
‑
0.278)。
[0416]
特定于晚期黑色素瘤的ropro2评分由以下公式给出:0.0062(年龄
‑
65.539) 0.1059(性别
‑
0.68)
‑
0.13496(吸烟
‑
0.352)
‑
0.01106(转移部位的数量
‑
0.368) 0.2725(ecog
‑
0.758) 0.10207(nlr
‑
0.594)
‑
0.00161(bmi
‑
28.896)
‑
0.03303(氧气
‑
97.009)
‑
0.0029(sbp
‑
130.345) 0.00699(心率
‑
79.392)
‑
0.02029(hgb
‑
13.099)
‑
0.00206(白细胞
‑
8.308) 0.01633(尿素氮
‑
18.031) 0.08373(钙
‑
9.297)
‑
0.00025(血小板
‑
258.758)
‑
0.01065(血液中淋巴细胞/100个白细胞
‑
21.258) 7e
‑
04(ast
‑
24.439) 0.00058(alp
‑
94.702)
‑
0.01989(蛋白质
‑
68.102) 0.00155(alt
‑
25.62)
‑
0.04059(白蛋白
‑
38.916) 0.03968(胆红素
‑
0.564) 0.0433(淋巴细胞
‑
1.674) 1e
‑
04(二氧化碳
‑
25.859)
‑
0.02939(氯化物
‑
102.027) 0.09766(单核细胞
‑
0.624)
‑
0.0515(血液中嗜酸性粒细胞/100个白细胞
‑
2.692) 0.00068(ldh
‑
313.076) 0.13055(肿瘤分期
‑
3.017)。
[0417]
特定于膀胱癌的ropro2评分由以下公式给出:0.00347(年龄
‑
71.109) 0.07937(性别
‑
0.748) 0.05865(吸烟
‑
0.73) 0.14505(转移部位的数量
‑
0.144) 0.23068(ecog
‑
0.895) 0.023(nlr
‑
0.692)
‑
0.00651(bmi
‑
27.624)
‑
0.00666(氧气
‑
96.81)
‑
7e
‑
04(sbp
‑
128.949) 0.00511(心率
‑
81.449)
‑
0.04131(hgb
‑
11.637) 0.0192(白细胞
‑
8.918) 0.01188(尿素氮
‑
22.192) 0.16766(钙
‑
9.292)
‑
0.00095(血小板
‑
286.043)
‑
0.01657(血液中淋巴细胞/100个白细胞
‑
18.953) 0.01467(ast
‑
22.276) 0.00247(alp
‑
106.899)
‑
0.01493(蛋白质
‑
68.58)
‑
0.00939(alt
‑
20.732)
‑
0.04466(白蛋白
‑
37.235) 0.00392(胆红素
‑
0.464) 0.00895(淋巴细胞
‑
1.524)
‑
0.01209(二氧化碳
‑
24.819)
‑
0.02813(氯化物
‑
101.957) 0.06395(单核细胞
‑
0.661)
‑
0.02002(血液中嗜酸性粒细胞/100个白细胞
‑
2.567)
‑
3e
‑
05(ldh
‑
233.144)
‑
0.07393(肿瘤分期
‑
3.532)
‑
0.26819(手术
‑
0.504) 0.11056
(t分期
‑
2.465)。
[0418]
特定于cll(慢性淋巴细胞白血病)的ropro2评分由以下公式给出:0.05779(年龄
‑
69.951) 0.26067(性别
‑
0.626) 0.71525(吸烟
‑
0.35) 0.70923(转移部位的数量
‑
0.008) 0.39314(ecog
‑
0.622)
‑
0.22371(nlr
‑
0.077)
‑
0.00915(bmi
‑
28.769)
‑
0.01203(氧气
‑
96.811)
‑
0.00232(sbp
‑
129.642) 0.00826(心率
‑
77.465)
‑
0.07827(hgb
‑
11.767) 0.00096(白细胞
‑
40.123) 0.00878(尿素氮
‑
20.195) 0.01911(钙
‑
9.216)
‑
0.00137(血小板
‑
160.155)
‑
0.00201(血液中淋巴细胞/100个白细胞
‑
67.021) 0.00313(ast
‑
24.08) 0.00352(alp
‑
87.048)
‑
0.00622(蛋白质
‑
65.126)
‑
0.00792(alt
‑
21.752)
‑
0.03883(白蛋白
‑
40.74) 0.0879(胆红素
‑
0.621)
‑
0.00713(淋巴细胞
‑
28.523) 0.01213(二氧化碳
‑
25.898)
‑
0.03209(氯化物
‑
103.766) 0.05868(单核细胞
‑
1.885) 0.03505(血液中嗜酸性粒细胞/100个白细胞
‑
1.16) 0.00037(ldh
‑
273.307)
‑
0.00708(肿瘤分期
‑
1.392)。
[0419]
特定于dlbcl(弥漫性大b细胞癌)的ropro2评分由以下公式给出:0.038(年龄
‑
66.079) 0.22192(性别
‑
0.547)
‑
0.22649(吸烟
‑
0.351) 0.11979(转移部位的数量
‑
0.012) 0.31201(ecog
‑
0.784) 0.00719(nlr
‑
0.631)
‑
0.01538(bmi
‑
28.581)
‑
0.02739(氧气
‑
96.915) 0.00373(sbp
‑
128.501) 0.00047(心率
‑
83.492)
‑
0.02201(hgb
‑
12.038)
‑
0.01588(白细胞
‑
7.943) 0.02116(尿素氮
‑
18.144)
‑
0.007(钙
‑
9.344)
‑
0.00098(血小板
‑
260.621)
‑
0.01131(血液中淋巴细胞/100个白细胞
‑
21.008) 0.00335(ast
‑
26.771) 0.00298(alp
‑
95.829)
‑
0.01163(蛋白质
‑
66.364)
‑
0.01085(alt
‑
24.473)
‑
0.02293(白蛋白
‑
37.656) 0.17582(胆红素
‑
0.563) 0.10388(淋巴细胞
‑
1.589) 0.00502(二氧化碳
‑
25.833)
‑
0.01428(氯化物
‑
101.524) 0.22388(单核细胞
‑
0.638) 0.00275(血液中嗜酸性粒细胞/100个白细胞
‑
2.293)
‑
6e
‑
04(ldh
‑
329.933) 0.06839(肿瘤分期
‑
2.791) 0.44252(bm_cd5
‑
0.168)。
[0420]
特定于hcc(肝细胞癌)的ropro2评分由以下公式给出:0.00592(年龄
‑
66.277) 0.12226(性别
‑
0.807)
‑
19.43777(吸烟
‑
0.352)
‑
0.00323(转移部位的数量
‑
0.094) 0.10789(ecog
‑
0.922) 0.15643(nlr
‑
0.592) 0.00388(bmi
‑
27.783)
‑
0.01924(氧气
‑
97.2)
‑
0.00132(sbp
‑
128.568) 0.00801(心率
‑
80.125)
‑
0.01479(hgb
‑
12.489) 0.06616(白细胞
‑
6.7) 0.02277(尿素氮
‑
16.886) 0.10928(钙
‑
9.092) 0.00019(血小板
‑
195.961)
‑
0.00532(血液中淋巴细胞/100个白细胞
‑
21.082) 0.00517(ast
‑
68.984) 0.00093(alp
‑
189.229)
‑
0.00514(蛋白质
‑
71.962)
‑
0.00396(alt
‑
50.691)
‑
0.04574(白蛋白
‑
34.109) 0.36517(胆红素
‑
1.154)
‑
0.0059(淋巴细胞
‑
1.339)
‑
0.03001(二氧化碳
‑
24.955)
‑
0.02278(氯化物
‑
101.52)
‑
0.28334(单核细胞
‑
0.591)
‑
0.05039(血液中嗜酸性粒细胞/100个白细胞
‑
2.729) 0.00134(ldh
‑
306.135) 0.15332(肿瘤分期
‑
3.111)。
[0421]
特定于转移性乳腺癌的ropro2评分由以下公式给出:0.00269(年龄
‑
62.989) 0.01453(性别
‑
0.011) 0.1938(吸烟
‑
0.351) 0.00116(转移部位的数量
‑
0.339) 0.2144(ecog
‑
0.76) 0.13996(nlr
‑
0.449)
‑
0.00682(bmi
‑
29.567)
‑
0.03728(氧气
‑
96.722)
‑
0.00404(sbp
‑
131.38) 0.0038(心率
‑
85.049)
‑
0.05297(hgb
‑
12.364)
‑
0.02052(白细胞
‑
7.427) 0.00939(尿素氮
‑
15.999) 0.10216(钙
‑
9.434)
‑
0.00071(血小板
‑
266.78)
‑
0.00192(血液中淋巴细胞/100个白细胞
‑
23.863) 0.00719(ast
‑
31.774) 0.00065(alp
‑
120.469)
‑
0.00802(蛋白质
‑
69.839)
‑
0.00303(alt
‑
28.294)
‑
0.0403(白蛋白
‑
39.387)
‑
0.03278(胆红素
‑
0.49)
‑
0.0146(淋巴细胞
‑
1.686)
‑
0.00091(二氧化碳
‑
25.745)
‑
0.01655(氯化物
‑
101.831) 0.34615(单核细胞
‑
0.532)
‑
0.03497(血液中嗜酸性粒细胞/100个白细胞
‑
2.15) 0.00051(ldh
‑
302.721)
‑
0.05209(肿瘤分期
‑
2.853) 0.00353(n24_t0
‑
66.322)
‑
0.67362(状况_er
‑
0.752)
‑
0.31455(状况_pr
‑
0.576)
‑
0.70817(状况_her2
‑
0.206)。
[0422]
特定于转移性crc(结肠直肠癌)癌症的ropro2评分由以下公式给出:0.01002(年龄
‑
63.765) 0.05288(性别
‑
0.558) 0.01467(吸烟
‑
0.351) 0.04867(转移部位的数量
‑
0.184) 0.2995(ecog
‑
0.724) 0.12341(nlr
‑
0.561)
‑
0.00452(bmi
‑
28.025)
‑
0.04628(n28_t0
‑
97.301)
‑
0.00216(sbp
‑
129.373) 0.00387(心率
‑
82.507)
‑
0.00925(hgb
‑
11.801)
‑
0.00807(白细胞
‑
8.157) 0.01254(尿素氮
‑
15.177) 0.07242(钙
‑
9.242)
‑
0.00045(血小板
‑
294.471)
‑
0.00861(血液中淋巴细胞/100个白细胞
‑
21.651) 0.00332(ast
‑
31.853) 0.00074(alp
‑
139.89)
‑
0.00212(蛋白质
‑
69.152)
‑
0.00485(alt
‑
26.673)
‑
0.04476(白蛋白
‑
37.617) 0.22807(胆红素
‑
0.539)
‑
0.02575(淋巴细胞
‑
1.635)
‑
0.01573(二氧化碳
‑
25.449)
‑
0.03205(氯化物
‑
101.807) 0.1334(单核细胞
‑
0.647)
‑
0.004(血液中嗜酸性粒细胞/100个白细胞
‑
2.868) 0.00044(ldh
‑
339.711) 0.09735(肿瘤分期
‑
3.496) 0.53129(状况_braf
‑
0.107) 0.18914(状况_kras
‑
0.451)。
[0423]
特定于转移性rcc(肾细胞癌)的ropro2评分由以下公式给出:0.00638(年龄
‑
66.118)
‑
0.01476(性别
‑
0.699) 0.00179(吸烟
‑
0.572) 0.06387(转移部位的数量
‑
0.272) 0.16002(ecog
‑
0.86) 0.05433(nlr
‑
0.575)
‑
0.01004(bmi
‑
29.805)
‑
0.0425(n28_t0
‑
96.707)
‑
0.00266(sbp
‑
130.368) 0.00795(心率
‑
81.061)
‑
0.00346(hgb
‑
12.161) 0.04464(白细胞
‑
8.072) 0.0106(尿素氮
‑
21.186) 0.04739(钙
‑
9.416)
‑
0.00033(血小板
‑
286.676)
‑
0.00984(血液中淋巴细胞/100个白细胞
‑
21.154) 0.00739(ast
‑
22.983) 0.00049(alp
‑
109.25)
‑
0.01171(蛋白质
‑
69.997)
‑
0.01121(alt
‑
24.263)
‑
0.05349(白蛋白
‑
37.749)
‑
0.0202(胆红素
‑
0.499)
‑
0.04447(淋巴细胞
‑
1.578)
‑
0.00319(二氧化碳
‑
25.558)
‑
0.03636(氯化物
‑
101.488)
‑
0.0937(单核细胞
‑
0.626)
‑
0.03918(血液中嗜酸性粒细胞/100个白细胞
‑
2.579) 0.00121(ldh
‑
261.093) 0.0851(肿瘤分期
‑
3.145)
‑
0.31275(肾切除术
‑
0.66)
‑
0.37341(透明细胞_rcc
‑
0.695)。
[0424]
特定于多发性骨髓瘤的ropro2评分由以下公式给出:0.03943(年龄
‑
68.434) 0.14741(性别
‑
0.542)
‑
0.09141(吸烟
‑
0.351) 0.10112(转移部位的数量
‑
0.037) 0.32641(ecog
‑
0.901)
‑
0.05074(nlr
‑
0.267)
‑
0.00195(bmi
‑
29.017)
‑
0.02522(氧气
‑
97.041)
‑
0.00427(sbp
‑
133.73) 0.00449(心率
‑
80.919)
‑
0.0559(hgb
‑
10.824)
‑
0.00576(白细胞
‑
6.364) 0.01195(尿素氮
‑
21.864) 0.00914(钙
‑
9.33)
‑
0.00135(血小板
‑
220.519)
‑
0.00925(血液中淋巴细胞/100个白细胞
‑
28.37) 0.00706(ast
‑
23.754) 0.00196(alp
‑
84.221)
‑
0.00472(蛋白质
‑
78.166)
‑
0.00766(alt
‑
23.431)
‑
0.03242(白蛋白
‑
36.515) 0.26533(胆红素
‑
0.493) 0.02637(淋巴细胞
‑
1.75)
‑
0.003(二氧化碳
‑
24.927)
‑
0.0161(氯化物
‑
101.955) 0.19518(单核细胞
‑
0.507)
‑
0.02945(血液中嗜酸性粒细胞/100个白细胞
‑
2.3) 0.00071(ldh
‑
216.938) 0.17142(肿瘤分期
‑
1.987)
‑
0.12075(m蛋白igg
‑
0.542)
‑
0.46168(轻链κ
‑
0.572)
‑
0.38144(轻链λ
‑
0.337)。
[0425]
特定于卵巢癌的ropro2评分由以下公式给出:0.00998(年龄
‑
65.176) 1.02303(吸烟
‑
0.35) 0.11866(转移部位的数量
‑
0.082) 0.25502(ecog
‑
0.778) 0.21763(nlr
‑
0.555)
‑
0.00348(bmi
‑
28.264)
‑
0.05212(氧气
‑
96.969)
‑
0.00274(sbp
‑
128.397) 0.00062(心率
‑
84.888)
‑
0.02728(hgb
‑
11.746) 0.01832(白细胞
‑
7.828) 0.02424(尿素氮
‑
15.932) 0.00599(钙
‑
9.323)
‑
0.00101(血小板
‑
332.437) 0.01093(血液中淋巴细胞/100个白细胞
‑
21.544) 0.00837(ast
‑
23.971) 0.00353(alp
‑
91.691)
‑
0.01219(蛋白质
‑
68.922)
‑
0.01376(alt
‑
21.587)
‑
0.03487(白蛋白
‑
37.78) 0.32377(胆红素
‑
0.412)
‑
0.03305(淋巴细胞
‑
1.526) 0.01351(二氧化碳
‑
25.341)
‑
0.01256(氯化物
‑
102.004) 0.05714(单核细胞
‑
0.539)
‑
0.03722(血液中嗜酸性粒细胞/100个白细胞
‑
2.117) 0.00109(ldh
‑
288.609) 0.40066(肿瘤分期
‑
3.108)。
[0426]
特定于sclc(小细胞肺癌)的ropro2评分由以下公式给出:0.00891(年龄
‑
67.252) 0.22435(性别
‑
0.481) 0.10511(吸烟
‑
0.985) 0.01216(转移部位的数量
‑
0.13) 0.13932(ecog
‑
0.983) 0.00473(nlr
‑
0.645)
‑
0.00942(bmi
‑
27.722)
‑
0.03779(氧气
‑
95.68)
‑
0.00509(sbp
‑
127.436) 0.00184(心率
‑
85.411)
‑
0.02368(hgb
‑
12.674) 0.0187(白细胞
‑
9.25) 0.00619(尿素氮
‑
16.446) 0.04426(钙
‑
9.3)
‑
0.00107(血小板
‑
282.204)
‑
0.00278(血液中淋巴细胞/100个白细胞
‑
19.709) 0.0059(ast
‑
31.42) 0.00047(alp
‑
114.166)
‑
0.00912(蛋白质
‑
67.956)
‑
0.00551(alt
‑
29.195)
‑
0.02229(白蛋白
‑
37.454)
‑
0.06248(胆红素
‑
0.52)
‑
0.02092(淋巴细胞
‑
1.707)
‑
0.00089(二氧化碳
‑
26.303)
‑
0.01935(氯化物
‑
99.666)
‑
0.03149(单核细胞
‑
0.704)
‑
0.0199(血液中嗜酸性粒细胞/100个白细胞
‑
1.961) 0.00069(ldh
‑
365.223) 0.23314(肿瘤分期
‑
3.549) 0.47876(sclc分期
‑
0.648)。
[0427]
特定于头颈部癌的ropro2评分由以下公式给出:0.00518(年龄
‑
64.674) 0.12697(性别
‑
0.772)
‑
0.02112(吸烟
‑
0.805) 0.09328(转移部位的数量
‑
0.111) 0.16008(ecog
‑
0.894)
‑
0.04024(nlr
‑
0.775)
‑
0.00764(bmi
‑
24.671)
‑
0.03521(氧气
‑
96.753)
‑
0.00198(sbp
‑
125.17) 0.00672(心率
‑
81.443)
‑
0.05918(hgb
‑
12.345) 0.01424(白细胞
‑
8.344) 0.00502(尿素氮
‑
17.085) 0.17451(钙
‑
9.441)
‑
8e
‑
05(血小板
‑
276.764)
‑
0.01363(血液中淋巴细胞/100个白细胞
‑
16.982) 0.00467(ast
‑
23.164) 0.00271(alp
‑
87.966)
‑
0.00349(蛋白质
‑
69.592)
‑
0.00565(alt
‑
20.505)
‑
0.03886(白蛋白
‑
38.568)
‑
0.00106(胆红素
‑
0.483)
‑
0.01571(淋巴细胞
‑
1.269) 0.0089(二氧化碳
‑
26.889)
‑
0.02273(氯化物
‑
99.978) 0.10163(单核细胞
‑
0.613)
‑
0.02502(血液中嗜酸性粒细胞/100个白细胞
‑
2.252) 0.00084(ldh
‑
209.625)
‑
0.08805(肿瘤分期
‑
3.5)
‑
0.22453(hpv状况
‑
0.472)。
[0428]
特定于滤泡的ropro2评分由以下公式给出:0.0468(年龄
‑
66.416) 0.70266(性别
‑
0.516) 1.06061(转移部位的数量
‑
0.012) 0.06024(ecog
‑
0.556) 0.26978(nlr
‑
0.493)
‑
0.02437(bmi
‑
29.51)
‑
0.17142(氧气
‑
96.821) 0.00584(sbp
‑
129.754) 0.01086(心率
‑
78.578)
‑
0.05796(hgb
‑
12.858)
‑
0.01222(白细胞
‑
7.63) 0.02537(尿素氮
‑
17.532) 0.01785(钙
‑
9.334)
‑
0.00083(血小板
‑
227.01)
‑
0.00522(血液中淋巴细胞/100个白细胞
‑
24.463) 0.01112(ast
‑
22.11) 0.00406(alp
‑
83.673) 0.01715(蛋白质
‑
67.455)
‑
0.03429(alt
‑
20.377)
‑
0.07823(白蛋白
‑
39.938)
‑
0.58047(胆红素
‑
0.566)
‑
0.04803(淋巴细胞
‑
2.253) 0.11677(二氧化碳
‑
26.334) 0.11495(氯化物
‑
102.349) 0.42239(单核细胞
‑
0.602) 0.20839(血液中嗜酸性粒细胞/100个白细胞
‑
2.822) 0.00141(ldh
‑
240.005)
‑
0.14411(肿瘤分期
‑
3.034)。
[0429]
特定于胰腺癌的ropro2评分由以下公式给出:0.00638(年龄
‑
67.378) 0.05687
(性别
‑
0.541)
‑
0.62763(吸烟
‑
0.35) 0.00541(转移部位的数量
‑
0.093) 0.22063(ecog
‑
0.894) 0.03629(nlr
‑
0.667)
‑
0.00469(bmi
‑
26.238)
‑
0.02826(氧气
‑
97.09)
‑
0.00141(sbp
‑
126.099) 0.00776(心率
‑
82.714)
‑
0.0175(hgb
‑
11.903) 0.00485(白细胞
‑
8.717) 0.01408(尿素氮
‑
15.205) 0.10756(钙
‑
9.203)
‑
0.00054(血小板
‑
257.947)
‑
0.00733(血液中淋巴细胞/100个白细胞
‑
19.318) 0.00386(ast
‑
37.701) 0.00114(alp
‑
185.199)
‑
0.00548(蛋白质
‑
66.673)
‑
0.00654(alt
‑
37.784)
‑
0.04763(白蛋白
‑
36.334) 0.03451(胆红素
‑
0.777)
‑
0.10421(淋巴细胞
‑
1.539) 0.00822(二氧化碳
‑
25.679)
‑
0.02157(氯化物
‑
100.587) 0.26008(单核细胞
‑
0.696)
‑
0.00193(血液中嗜酸性粒细胞/100个白细胞
‑
2.499) 0.00048(ldh
‑
259.294) 0.00544(肿瘤分期
‑
3.522)
‑
0.29951(issurgery
‑
0.2)。
[0430]
所有分析均使用统计分析包(r core team,2013)进行。应当理解,附加地或替代地,可以采用其他包进行分析。
[0431]
上述实施例的系统和方法可以在计算机系统中(特别是在计算机硬件或计算机软件中)实现。
[0432]
术语“计算机系统”包括硬件、软件和数据存储设备,用于实现系统或执行根据上述实施例的方法。例如,计算机系统可以包含中央处理单元(cpu)、输入装置、输出装置和数据存储器。优选地,计算机系统具有监视器以提供视觉输出显示(例如在业务流程的设计中)。数据存储器可以包含ram、磁盘驱动器或其他计算机可读介质。计算机系统可以包括通过网络连接并且能够在该网络彼此通信的多个计算设备。
[0433]
上述实施例的方法可以作为计算机程序或作为计算机程序产品或承载计算机程序的计算机可读介质提供,该计算机程序被布置为在计算机上运行时执行上述方法。
[0434]
术语“计算机可读介质”包括但不限于可由计算机或计算机系统直接读取和访问的任何非暂时性介质或介质。所述介质可以包括但不限于磁存储介质,如软盘、硬盘存储介质和磁带;光存储介质,例如光盘或cd
‑
rom;电子存储介质,例如存储器,包括ram、rom和闪存;以及上述的混合和组合,例如磁/光存储介质。
[0435]
除非上下文另有说明,否则上述特征的描述和定义不限于本发明的任何特定方面或实施例并且同样适用于所描述的所有方面和实施例。
[0436]
在本文中使用的“和/或”将被视为两个特定特征或部件中的每一个的具体公开,其中包含或不包含另一个。例如,“a和/或b”将被视为(i)a、(ii)b和(iii)a和b中每一个的具体公开,就好像每一个在本文中单独列出一样。
[0437]
必须注意的是,如在本说明书和所附权利要求中所用,单数形式“一个”、“一种”和“所述”包括复数指代物,除非上下文另外明确规定。范围在本文中可以表示为从“约”一个特定值和/或到“约”另一个特定值。当表达这样的范围时,另一个实施例包括从一个特定值和/或到另一个特定值。类似地,当值表示为近似值时,通过使用先行词“约”,将理解特定值形成另一个实施例。与数值相关的术语“约”是任选的并且意味着例如 /
‑
10%。
[0438]
在整个说明书,包括随后的权利要求中,除非上下文另有要求,否则词语“包括”和“包含”以及诸如“包含”(comprises和comprising)和“包括”的变体应被理解为暗示包括所陈述的整数或步骤或整数或步骤组,但不排除任何其他整数或步骤或整数或步骤组。
[0439]
本发明的其他方面和实施例提供上述方面和实施例,其中术语“包含”被术语“由
……
组成”或“基本上由
……
组成”代替,除非上下文另有说明。
[0440]
前述说明书公开的特征,或以下权利要求中,以其特定形式表达或实施公开功能的方式方面,或用于获得公开结果的方法或过程,这些特征可以其多种形式适当地单独使用,或以任何组合的形式使用,以实现本发明。
[0441]
虽然已经结合上述示例性实施例描述了本发明,但是当给出本公开时,许多等效修改和变化对于本领域技术人员来说将是显而易见的。因此,上述本发明的示例性实施例被认为是说明性的而非限制性的。在不脱离本发明的精神和范围的情况下,可以对所描述的实施例进行各种改变。
[0442]
为避免任何疑问,本文提供的任何理论解释都是为了改进读者的理解。发明人不希望受任何这些理论解释的束缚。
[0443]
此处使用的任何章节标题仅用于组织目的,不应被解释为限制所描述的主题。
[0444]
表15提供了罗氏预后评分1(ropro1)中纳入的26个参数和ropro2中纳入的29个参数的详细信息,可以替代ropro1或ropro2中纳入的参数的参数,以及特定癌症类型的已知参数。本文所述方法中采用的癌症患者信息可包含对应于如本文别处公开的表15中所列的一个或多个参数的数据。
[0445]
[0446]
[0447]
[0448]
[0449]
[0450]
[0451]
[0452]
[0453]
[0454]
[0455]
[0456]
[0457][0458]
表16通过rmhs和ropro1 5%分位数显示了研究bp29428的平均患者时间。还显示了每组低rmhs、高rmhs和每个ropro1分位数中的患者数量(n)。表单元格通过rmhs(组平均值)和ropro1 5%分位数分类(运行组平均值)显示研究bp29428的患者时间(天)。对于ropro1,明确给出了5%分位数的数字边界。
[0459][0460][0461]
表17通过rmhs和ropro1 10%分位数显示了初步诊断为膀胱癌的患者在研究
bp29428的平均患者时间。还显示了每组低rmhs、高rmhs和每个ropro1分位数中的患者数量(n)。表单元格通过rmhs(组平均值)和ropro1 10%分位数分类(运行组平均值)显示研究bp29428的患者时间(天)。对于ropro1,明确给出了10%分位数的数字边界。由于样品量较小,此表中使用10%而不是5%的分位数。
[0462]
rmhs研究天数(平均)患者数量(n)高7821低146415%分位数的ropro1研究天数(运行平均)患者数量(n)>1.2116[0.80;1.21]257[0.66;0.80]516[0.50;0.66]1066[0.41;0.50]1026[0.28;0.41]946[0.21;0.28]956[0.07;0.21]1006[
‑
0.08;0.07]1216<
‑
0.081237
[0463]
表18通过rmhs和ropro2 10%分位数显示了患者在研究bp29428的平均患者时间。还显示了每组低rmhs、高rmhs和每个ropro2十分位数中的患者数量(n)。表单元格通过rmhs(组平均值)和ropro2 10%分位数分类(运行组平均值)显示研究bp29428的患者时间(天)。对于ropro2,明确给出了10%分位数的数字边界。
[0464][0465][0466]
表19通过rmhs和ropro2 10%分位数显示了患者在iii期研究oak的平均患者时间。还显示了每组低rmhs、高rmhs和每个ropro2十分位数中的患者数量(n)。表单元格通过rmhs(组平均值)和ropro2 10%分位数分类(运行组平均值)显示研究的患者时间(天)。对于ropro2,明确给出了10%分位数的数字边界。
[0467]
rmhs研究天数(平均值)患者数量低372884高244303ropro(十分位数)研究天数(平均值)患者数量[
‑
1.94;
‑
0.74]471105[
‑
0.74;
‑
0.52]45291[
‑
0.52;
‑
0.35]439111[
‑
0.35;
‑
0.19]395143[
‑
0.19;
‑
0.05]377139[
‑
0.05;0.11]324122[0.11;0.29]314153[0.29;0.5]248134[0.5;0.81]201113[0.81;2.94]14876
[0468]
表20:缩写列表
[0469]
participants:a prospective population
‑
based study.the lancet 386:533
–
540,2015
[0481]
graf e,schmoor c,sauerbrei w,et al.:assessment and comparison of prognostic classification schemes for survival data.stat med 18:2529
–
2545,1999
[0482]
halabi s,owzar k:the importance of identifying and validating prognostic factors in oncology.semin oncol 37:e9
–
e18,2010
[0483]
hu fb,willett wc,li t,et al.:adiposity as compared with physical activity in predicting mortality among women.n engl j med 351:2694
–
2703,2004
[0484]
jin j,hu k,zhou y,li w:clinical utility of the modified glasgow prognostic score in lung cancer:a meta
‑
analysis.plos one 12(9):e0184412,2017.
[0485]
kahn mg,callahan tj,barnard j,et al.:a harmonized data quality assessment terminology and framework for the secondary use of electronic health record data.egems gener evid methods improve patient outcomes 4:18,2016
[0486]
kinoshita a,onoda h,imai n,et al.:the glasgow prognostic score,an inflammation based prognostic score,predicts survival in patients with hepatocellular carcinoma.bmc cancer 52,2013
[0487]
mcgee dl,liao y,cao g,et al.:self
‑
reported health status and mortality in a multiethnic us cohort.am j epidemiol 149:41
–
46,1999
[0488]
nieder c,dalhaug a:a new prognostic score derived from phase i study participants with advanced solid tumours is also valid in patients with brain metastasis.anticancer res.977
–
9,2010
[0489]
r core team(2013).r:a language and environment for statistical computing.r foundation for statistical computing,vienna,austria.url http://www.r
‑
project.org/.
[0490]
reid vl,mcdonald r,nwosu ac,mason sr,probert c,ellershaw je,coyle s:a systematically structured review of biomarkers of dying in cancer patients in the last months of life;an exploration of the biology of dying.plos one 12(4),2017
[0491]
rittmeyer a,barlesi f,waterkamp d,et al.:atezolizumab versus docetaxel in patients with previously treated non
‑
small
‑
cell lung cancer(oak):a phase 3,open
‑
label,multicentre randomised controlled trial.lancet 389:255
–
265,2017
[0492]
stock c,mons u,brenner h:projection of cancer incidence rates and case numbers until 2030:a probabilistic approach applied to german cancer registry data(1999
‑
2013).cancer epidemiol.57:110
–
119,2018
[0493]
sudlow c,gallacher j,allen n,et al.:uk biobank:an open access resource for identifying the causes of a wide range of complex diseases of middle and old age.plos med.12:e1001779,2015
[0494]
tadahiro nozoe,rumi matono,hideki ijichi,takefumi ohga,takahiro ezaki:glasgow prognostic score(gps)can be a useful indicator to determine prognosis of patients with colorectal carcinoma.int.surg.99:512
–
517,2014.
[0495]
thun mj,peto r,lopez ad,et al.:alcohol consumption and mortality among middle
‑
aged and elderly u.s.adults.n.engl.j.med.337:1705
–
1714,1997
[0496]
tota
‑
maharaj r,blaha mj,mcevoy jw,et al.:coronary artery calcium for the prediction of mortality in young adults<45 years old and elderly adults>75years old.eur.heart j.33:2955
–
2962,2012.
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。