1.本发明属于疫苗生产工艺技术领域,具体涉及一种包载抗原的阳离子纳米乳佐剂、及其制备方法和应用。
背景技术:
2.感染性疾病当前仍然严重威胁着全球人类健康,接种疫苗是预防和控制传染病最经济有效的措施。传统疫苗主要有减毒疫苗、灭活疫苗,其主要用毒性弱或灭活的病原微生物及代谢产物作为抗原,其免疫原性强,但存在毒力恢复的风险。随着生物技术的发展,具有更高安全性的亚单位疫苗、合成肽疫苗、重组蛋白疫苗、多糖结合疫苗诞生,这些新型疫苗纯度高、成分明确、安全性好,但其免疫原性弱,单独使用难以诱导机体产生有效的免疫应答,因此添加佐剂以提升其免疫应答效果极为重要。
3.目前可供临床使用的佐剂数量十分有限,主要有铝盐佐剂、天然免疫刺激物和纳米乳佐剂,临床研究和追踪证明水包油型纳米乳佐剂相对于另两类佐剂具有更高的安全性和可靠性。水包油型纳米乳佐剂能诱导单核细胞、中性粒细胞及嗜酸性粒细胞等在注射部位快速聚集和增殖,增强抗原的免疫效应和免疫保护。
4.虽然水包油型纳米乳佐剂的有效性、安全性已在临床得到验证,但常用水包油型纳米乳佐剂仍然存在一定的缺陷。一般情况下,水包油型纳米乳由非离子型或者阴离子型乳化剂结合适宜的油相制备,使纳米乳表面带较高的负电荷,不易直接装载多肽、蛋白抗原。传统的水包油型纳米乳佐剂只能与抗原形成简单的混合物,其抗原和佐剂处于相互分离的状态,这导致佐剂与抗原在免疫接种后,抗原和佐剂分布在不同的区域,两者具有不同的动力学“行为”,最终致使佐剂发挥效应不足,疫苗免疫应答水平降低。此外,负电荷的纳米乳佐剂与体内生物膜相互作用弱甚至存在静电斥力,因此,现有的负电荷水包油型纳米乳佐剂不能克服天然的生理屏障,致使其免疫途径极大受限;更重要的是,现有的负电荷纳米乳佐剂仅能促进体液免疫,而对细胞免疫的增强效果并不明显,难以清除细胞内的感染的病原体。
5.鉴于上述缺陷,有必要提出一种新型的纳米乳佐剂,以提高纳米乳佐剂对抗原的包封率,实现抗原和佐剂的协同地送,消除抗原与佐剂免疫激活中时间和空间上的分离,充分发挥佐剂效应,进而提高抗原的免疫效力;同时使纳米乳佐剂可以克服生理屏障,拓宽纳米乳佐剂的免疫途径,充分发挥疫苗免疫保护作用。为了解决上述问题,本发明提供了一种阳离子纳米乳佐剂及其制备方法,实现了蛋白抗原的包载,同时克服了黏膜屏障,而此内容目前还未见报道。
技术实现要素:
6.本发明的目的之一是针对现有纳米乳佐剂技术的不足,提供一种能包载抗原的阳离子纳米乳佐剂,实现了抗原和佐剂的共载和协同递送。
7.本发的目的之二是针对现有纳米乳佐剂技术的不足,提供一种能包载抗原的阳离
子纳米乳佐剂的制备方法,通过高压均质、超声、高速搅拌等方法制备阳离子纳米乳佐剂,阳离子纳米乳佐剂能够通过静电作用、范德华力、氢键等作用力包载带负电的核酸、多肽、蛋白等抗原。
8.本发的目的之三是针对现有纳米乳佐剂技术的不足,提供一种能包载抗原的阳离子纳米乳佐剂,其阳离子性质增加抗原的生物膜粘附性和渗透性,促进抗原摄取,提升疫苗免疫应答能力,并拓宽纳米乳佐剂的免疫应用途径。
9.为实现上述目的之一,本发明采取的技术方案是提供:
10.一种能包载抗原的阳离子纳米乳佐剂,其中所述阳离子纳米乳佐剂包括双亲性阳离子材料和水包油纳米乳;所述双亲性阳离子材料包括疏水端和亲水端,所述疏水端不带电荷,亲水端为带正电荷的聚合物;所述纳米乳为水包油型乳剂,包括油相、水相和乳化剂。同时,该阳离子纳米乳佐剂由水包油型纳米乳和双亲性阳离子材料融合制备,其中所述水包油型纳米乳包括油相和乳化剂,其中各组分重量百分比为:油相0.01%
‑
50%、乳化剂0.001%
‑
10%,双亲性阳离子材料10%
‑
0.0001%,余量为水。各组分重量优选百分比为:油相0.5%
‑
10%、乳化剂0.1%
‑
2.5%,双亲性阳离子材料0.1%
‑
2.5%,所述的水包油型纳米乳中油相可以是任何药物上可接受的油。优选的油相为动物油、植物油、天然油、合成油、烃油、硅油、其半合成衍生物及其组合物。
11.进一步优选油包括但不限于矿物油、角鲨烯油、c6
‑
c30脂肪及其芳香酸及醇类、大豆油、中链甘油三酯、硬脂酸异丙酯、硬脂酸丁酯、棕榈酸辛酯、棕榈酸十六酯、贝氏酸三癸酯、己二酸二异丙酯、癸二酸二辛酯、邻苯二甲酸薄荷酯、辛酸十六酯、水杨酸辛酯、肉豆蔻酸异丙酯、新戊二醇二乙酸十六醇、油酸癸酯、己二酸二异丙酯,c12
‑
15烷基乳酸酯、乳酸十六酯、乳酸月桂酯、新戊酸异硬脂酯、肉豆蔻酯、硬脂酸异硬脂酯、硬脂酸辛酯、烃类油、异戊二烯、异十二烷、油酸、亚油酸、异硬脂醇、甲基苯基聚硅氧烷、西米硅酮、二甲基硅氧烷、苯基三甲基硅氧烷(或其有机改性版本)、聚合硅氧烷的烷基化衍生物、十六烷基二甲基硅氧烷、十二烷基三甲基硅氧烷、聚合硅氧烷的羟基化衍生物、挥发性硅油、环和线性硅油、环甲基852.5硅油、环甲基硅油、六甲基环三硅油、十甲基环戊烷硅油、挥发性线性二甲基硅油、异十六烷、异二十烷、聚异丁烯、异辛烷、异十二烷半合成衍生物或其组合物。特别优选的油相为角鲨烯,大豆油,中链甘油三酯,油酸的一种或一种以上的组合物。
12.所述的纳米乳为水包油型纳米乳,其中水相可以包括任何类型的水相,包括但不限于水(例如水、蒸馏水、纯化水、注射用水、去离子水、自来水)和溶液(例如hepes溶液),水相可进一步优选为无菌且无热原,优选水相为注射用水。
13.所述的水包油型纳米乳中乳化剂包括但不限于非离子性表面活性剂、阴离子表面活性剂、两性表面活性剂。优选但不限于c6
‑
c30脂肪及其芳香酸、油酸、亚油酸、聚乙二醇
‑
二硬脂酰乙醇胺(dspe
‑
peg)、吐温80、吐温40、司盘85、异四乙酸、百里酚。最优选为吐温80、和司盘85的一种或其组合。
14.所述的双亲性阳离子材料是指既有亲水头部基团,又有疏水尾部的聚合物,其中所述疏水端不带电荷,亲水端带正电荷,优选的其中所述亲水端为带正电的合成线性聚合物、交联聚合物或支化共聚物,特别优选的双亲性阳离子材料包括但不限于聚已内酯
‑
聚乙烯亚胺及衍生物、硬脂酸
‑
聚乙烯亚胺及衍生物、聚精氨酸
‑
硬脂酸及衍生物、聚精氨酸
‑
聚乳酸
‑
羟基乙酸及衍生物、聚赖氨酸
‑
硬脂酸及衍生物。最优选的双亲性阳离子材料为聚已
内酯
‑
聚乙烯亚胺聚合物、聚乳酸
‑
羟基乙酸
‑
聚精氨酸共聚物的一种或其组合。
15.所述聚已内酯
‑
聚乙烯亚胺聚合物(pcl
‑
pei),疏水端pcl分子量优选在1k~10k之间,进一步优选在1k~5k之间;亲水端pei分子量优选在1k~25k之间,进一步优选在1.8k~5k之间。pcl
‑
pei结构式如下,最优选的pcl
‑
pei的pcl分子量为3.57k,pei分子量为2k。
16.所述聚乳酸
‑
羟基乙酸
‑
聚精氨酸共聚物的亲水端聚精氨酸单元优选在8~30之间,疏水端聚乳酸
‑
羟基乙酸共聚物分子量优选在1k~20k之间,进一步优选在1k~5k之间,优选的聚乳酸
‑
羟基乙酸
‑
聚精氨酸到的聚精氨酸单元优选为3.14k,聚乳酸
‑
羟基乙酸共聚物的分子量为5k。聚精氨酸
‑
聚乳酸
‑
羟基乙酸结构式如下:
17.为实现上述目的之二,本发明提供了一种能包载抗原的阳离子纳米乳佐剂的制备方法,包含以下步骤:(1)将亲油相乳化剂溶于油相中,将亲水性乳化剂溶于水相中,二者混合形成初乳,初乳再经充分混合,例如高压均质、超声或高速搅拌等混合方法制备纳米乳佐剂;(2)称取双亲性阳离子材料,在涡旋、搅拌、超声条件下,或者通过微量注射泵加入双亲性阳离子材料到步骤(1)制备的纳米乳中,混匀至完全溶解,得到阳离子纳米乳佐剂;(3)取步骤(2)制备的阳离子纳米乳稀释,在涡旋、搅拌、超声条件下,或者通过微量注射泵加入抗原,混合均匀,阳离子纳米乳佐剂即成功包载抗原。
18.作为本发明优选的实施方案,步骤(1)以最终体积为40ml时计算:其中,步骤(1)所述处方中的亲油相乳化剂质量比为0.5%,亲水性乳化剂质量比为0.5%,油相优选质量比1.25
‑
5%。
19.作为本发明优选的实施方案,步骤(2)以最终体积为1ml时计算:其中,步骤(2)所稀释的纳米乳体积为25μl~500μl,所用稀释液为注射用水,包括但不仅限于磷酸盐缓冲液、hepes缓冲液。其中,步骤(2)所述的双亲性阳离子材料的量为0.1mg~10mg。其中,步骤(3)所述包载抗原量为0.05mg~5mg。
20.根据本发明按上述步骤制备出的阳离子纳米乳佐剂中,双亲性阳离子材料疏水端插入纳米乳的油相,正电性的亲水端则分布在纳米乳表面,其粒径均一、性质稳定。
21.根据本发明按上述步骤制备出的阳离子纳米乳佐剂成品粒径为500nm~10nm,进一步地优选为300~50nm,更优选为150nm~80nm;表面电荷为正电荷,优选为 40mv~ 5mv,进一步地优选为 20mv~ 5mv,更优选为 10mv~ 5mv。
22.根据本发明按上述步骤制备出的阳离子纳米乳佐剂包载带负电的抗原后,其粒径为600nm~20nm,进一步地优选为300~40nm,更优选为200nm~80nm;表面为正电荷或负电荷,优选表面电荷为 30mv~
‑
20mv,进一步地优选为 15mv~
‑
10mv,更优选为 10mv~
‑
5mv。
23.为实现上述目的之三,本发明提供一种能包载抗原的阳离子纳米乳佐剂,其通过静电、氢键、范德华力的一种或者多种作用力实现抗原的包载。
24.如上所述的抗原可以选自:蛋白类抗原包括乙型肝炎表面抗原hbsag、幽门螺杆菌重组b亚单位抗原ureb、重组pres1、pres2、重组核心蛋白、丙型肝炎病毒抗原、戊型肝炎病毒抗原、炭疽毒素结合蛋白、肺炎链球菌蛋白、a群m蛋白、链球菌c5a肽酶、牵连蛋白结合蛋白、丝氨酸羧酸酯酶、b型脑膜炎球菌外膜蛋白omp、鸡卵清白蛋白、苍白密螺旋体表面脂蛋白、牛血清白蛋白、溶菌酶、转铁蛋白、胰岛素、乳白蛋白、肌白蛋白、豆白蛋白、麦白蛋白、肌红蛋白、胶原蛋白、纤层蛋白;或类毒素类如白喉类毒素、破伤风类毒素、霍乱毒素,或多糖类如a群多糖、荚膜多糖、肺炎球菌多糖、伤寒多糖、脑膜炎球菌多糖,或病毒样颗粒如人乳头瘤病毒、轮状病毒,或灭活或减毒类疫苗抗原如百日咳毒素、甲型肝炎病毒、乙型脑炎病毒、狂犬病毒、脊髓灰质炎索尔克株病毒抗原、流感病毒、巨细胞病毒、喷鼻流感抗原、水痘—带状胞疹病毒、腮腺炎抗原、风疹病毒、天花病毒、麻疹、水痘、黄热病、脊髓灰质炎噻宾株、呼吸道合胞病毒;或减弱、杀灭的菌类如或肺结核活分枝杆菌、白喉棒状杆菌、百日咳博得特氏菌、a组链球菌、脑膜炎奈瑟氏球菌、侵肺军团菌、霍乱弧菌、铜绿假单胞菌、肺炎链球菌、苍白密螺旋体;或多糖
‑
蛋白复合物如肺炎球菌多糖结合物、脑膜炎球菌多糖
‑
蛋白结合物;或核酸、单链和双链核酸、超螺旋质粒dna、线性质粒dna、粘粒、细菌人工染色体、酵母人工染色体、哺乳动物人工染色体、rna;或合成的多肽类抗如:a组链球菌m肽、trp2、hgp100、p15e、铜绿假单胞菌合成肽、风疹病毒合成肽;或肿瘤细胞裂解液抗原,细菌裂解液抗原,肿瘤全细胞抗原中的一种或一种以上组合物。
25.本发明提供一种能包载抗原的阳离子纳米乳佐剂,还可加入不同的佐剂联合进一步提高免疫反应,所述附加佐剂包括但不限于:toll样受体激动剂:肽聚糖、脂磷壁酸、mpla、咪喹莫特、瑞喹莫特、cpg
‑
odn、细菌鞭毛蛋白、poly i:c;rig
‑
i样受体激动剂:3prna、短的双链rna、nod样受体激动剂、胞壁酰二肽(mdp)、n一乙酰葡萄糖胺;c
‑
型凝集素受体:β
‑
葡聚糖、海藻糖二硼酸盐;sting激动剂:cgamp;细菌毒素及其衍生物:霍乱毒素(ct)、大肠杆菌不耐热肠毒素(lt)、霍乱毒素b亚单位;皂苷类:qs21、番茄苷、quil
‑
a;细胞因子:gm
‑
csf、il
‑
2、il
‑
12、il
‑
6、ifn
‑
γ、flt
‑
3、淋巴细胞趋化因子;其他佐剂包括:热激蛋白、a151、gtp
‑
gdp、氟化钠、烷基聚丙烯酯多聚体、二甲基双十八烷基季胺溴化物(dda)的一种或一种以上组合物。优选的附加佐剂为cpg 1826、a151的一种或一种以上组合物。
26.本发明提供一种能包载抗原的阳离子纳米乳佐剂,其中双亲性材料不仅能够提供静电作用、氢键、范德华力等作用力包载抗原,同时还能通过其正电性增加生物粘膜粘附性以及提高抗原摄取的能力。可以应用于皮下、皮内、鼻腔黏膜和阴道粘膜进行免疫。
27.相比于现有技术,本发明的优点在于:(1)通过涡旋、搅拌使双亲性阳离子材料的疏水端插入乳剂的油相中,正电性的亲
水端则分散在乳剂表面,获得阳离子纳米乳佐剂,其可以通过静电吸附、范德华力、氢键等作用包载抗原,提供了一种制备纳米乳佐剂包载抗原的普适性方法。(2)双亲性阳离子材料修饰于纳米乳表面后,纳米乳佐剂分散性好,稳定性高,粒径可控范围大,可包载大剂量的大分子抗原,并实现高效的抗原提呈。(3)亲水性抗原和疏水性抗原可同时包载于该阳离子纳米乳佐剂中,实现不同性质的多种抗原的共递送,同时还能通过阳离子纳米乳佐剂正电性增加生物粘膜粘附性以及提高抗原摄取的能力。可以应用于皮下、皮内、鼻腔黏膜和阴道粘膜进行免疫,诱导机体产生针对病原体的全面、有效的免疫应答。(4)本发明制备方法简单迅速,条件温和,无有机试剂的加入,不会造成抗原蛋白的变性,可以有效地保持抗原蛋白的构象和活性,同时有利于大规模生产,具有广阔的应用和市场前景。
附图说明
图1.pcl
‑
pei的1h nmr图谱;图2.plga
‑
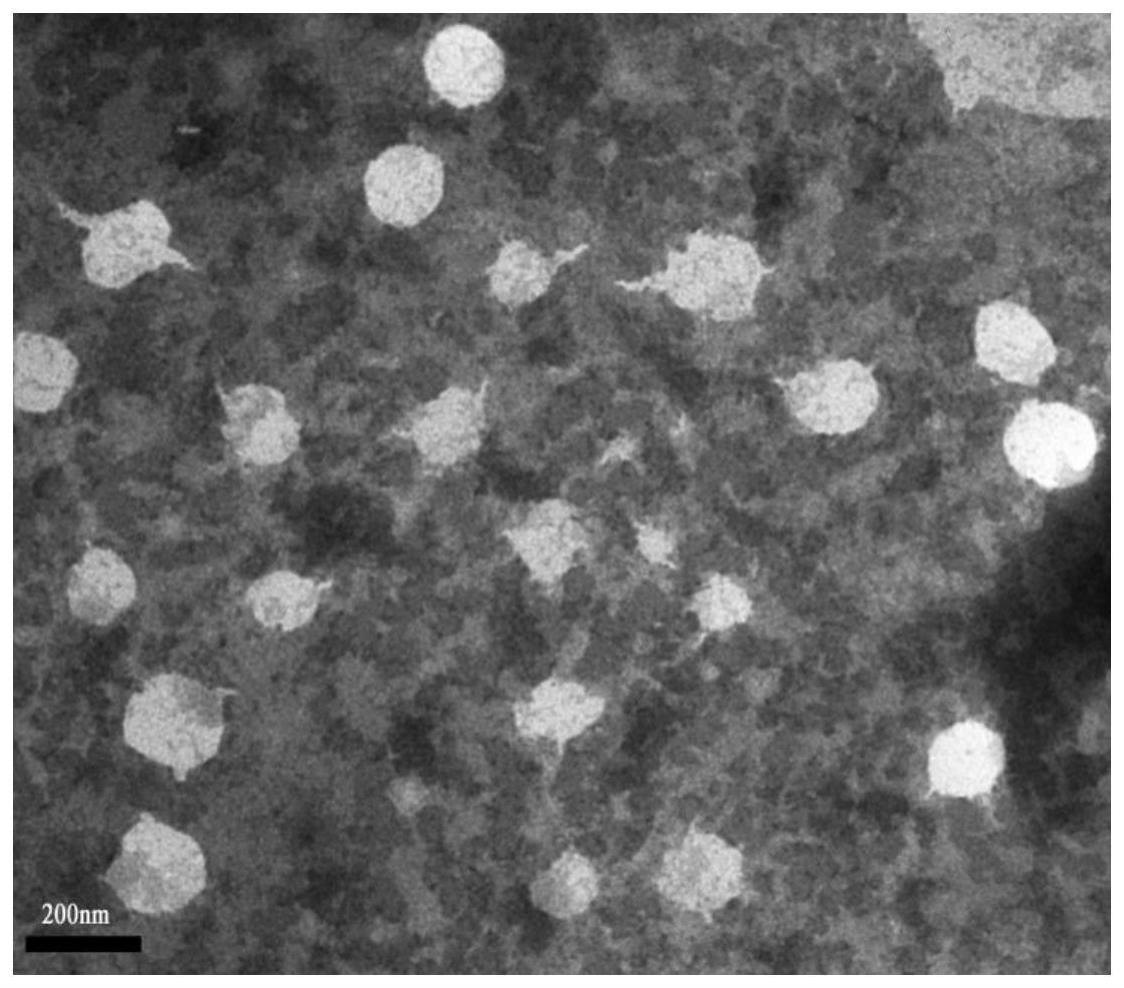
r20的1h nmr图谱;图3.未修饰纳米乳的电镜图;图4.双亲性材料pcl
‑
pei修饰的阳离子纳米乳佐剂电镜图;图5.包载模型抗原ova的阳离子纳米乳佐剂电镜图;图6.包载幽门螺杆菌重组尿素酶b亚单位疫苗rureb的阳离子纳米乳佐剂电镜图;图7.阳离子纳米乳佐剂显著延长抗原ova在鼻腔的滞留时间;图8.包载抗原ova的阳离子纳米乳佐剂皮下免疫小鼠提高血清中lgg、lgg1和lgg2a抗体水平;图9.包载抗原ova的阳离子纳米乳佐剂鼻腔免疫后提高xueqinglgg、lgg1、lgg2a、lga抗体水平;图10.包载抗原ova的阳离子纳米乳佐剂鼻腔免疫小鼠后,第7
‑
75天血清中lgg、lgg1、lgg2a抗体和鼻腔灌洗液中iga的抗体水平的变化;图11.包载抗原rureb的阳离子纳米乳佐剂鼻腔免疫后提高lgg、lgg1、lgg2a、lga抗体水平。
具体实施方式
28.以下实施例是对本发明的进一步说明,但绝不是对本发明范围的限制。下面参照实施例进一步详细阐述本发明,但是本领域技术人员应当理解,本发明并不限于这些实施例以及使用的制备方法。而且,本领域技术人员根据本发明的描述可以对本发明进行等同替换、组合、改良或修饰,但这些都将包括在本发明的范围内。
29.实施例1双亲性阳离子材料聚已内酯
‑
聚乙烯亚胺聚合物(pcl
‑
pei)的合成:以苯甲醇为引物,二乙基己酸亚锡为催化剂使ε
‑
己内酯开环,发生聚合反应生成pcl
‑
oh。以pcl
‑
oh为起始物,选用低毒的pei 2k与pcl
‑
oh室温搅拌反应24h,然后置于透析袋透析,除去未反应底物,冷冻干燥得到pcl
‑
pei。合成路线如下,pcl
‑
pei经1h nmr验证结构如图1所示,经凝胶渗透
色谱(gpc)测定pcl
‑
pei分子量为10224,其中疏水端pcl分子量为6495,占比63.5%,亲水端pei分子量为3729,占比36.4%。
30.实施例2双亲性阳离子材料聚乳酸
‑
羟基乙酸
‑
聚精氨酸共聚物(plga
‑
r20)的合成:以plga
‑
cooh为引物,加2.19mg edci,1.32mg nhs反应3h,再加30mg r20,反应22h。透析2天、冻干,得plga
‑
r20双亲性材料。plga
‑
r20经1h nmr验证结构如图2所示,经凝胶渗透色谱(gpc)测定plga
‑
r20分子量为15440,其中疏水端plga分子量为5k,占比47.89%,亲水端20分子量为3729,占比67.61%。
31.实施例3阳离子纳米乳佐剂的制备:将0.1g油酸、0.2g司盘85溶解在0.5g角鲨烯中,将0.2g吐温80溶于注射用水中,混合形成初乳,初乳经高压均质(876bar;15min)得到纳米乳(nanoemulsion,ne),加超纯水定容至40ml。取纳米乳125ul,称取双亲性阳离子材料实施例1中合成的pcl
‑
pei 0.5mg,加入乳液中,涡旋1min至完全溶解,加注射用水定容至1ml,即得阳离子纳米乳(cationic nanoemulsion,cne)佐剂。
32.实施例4阳离子纳米乳佐剂的制备:将0.35g蛋黄卵磷脂与0.01g吐温80溶于注射用水中,与0.5g角鲨烯混合形成初乳,初乳经高压均质(876bar;15min)得到纳米乳,加超纯水定容至40ml。取纳米乳125μl,称取双亲性阳离子材料实施例2中合成的plga
‑
r
20 0.5mg,加入乳液中,涡旋1min至完全溶解,加注射用水定容至1ml,即得阳离子纳米乳佐剂。
33.实施例5阳离子纳米乳佐剂用于包载模型抗原鸡卵清白蛋白(ova):取实施例3制备的阳离子纳米乳佐剂300μl,称取ova冻干粉末2mg溶于200μl注射用水中,涡旋状态下缓慢滴加到阳离子纳米乳中,涡旋30s,即得。
34.实施例6阳离子纳米乳佐剂用于包载模型抗原ova:取实施例4制备的阳离子纳米乳佐剂300μl,称取ova冻干粉末2mg溶于200μl注射用水中,涡旋状态下缓慢滴加到阳离子纳米乳中,涡旋30s,即得。
35.实施例7阳离子纳米乳佐剂用于包载幽门螺杆菌重组尿素酶b亚单位蛋白(ureb):取实施例3制备的阳离子纳米乳佐剂300μl,称取rureb冻干粉末1mg溶于100μl注射用水中,涡旋状态下缓慢滴加到阳离子纳米乳中,涡旋30s,即得。
36.实施例8阳离子纳米乳佐剂用于包载模型抗原ureb:取实施例4制备的阳离子纳米乳佐剂300μl,称取rureb冻干粉末1mg溶于100μl注射用水中,涡旋状态下缓慢滴加到阳离子纳米乳中,涡旋30s,即得。
37.实施例9粒径测定:使用zetasizer nano zs90激光粒度分析仪测定纳米粒的粒径分布。分别取实施例3和实施例4中制备的阳离子纳米乳佐剂25μl,用超纯水稀释至1ml,分别将上述样品放入样品池内检测,测定温度设为25℃。同时取实施例5、6、7和8中制备的载抗原阳离
子纳米乳佐剂500μl,用超纯水稀释至1ml,分别将上述样品放入样品池内检测,测定温度设为25℃。上述各实施例所制备样品粒径在160
‑
230nm之间,pdi小于0.3,分布均一,具体粒径结果如表1所示。表1.阳离子纳米乳佐剂和载抗原的阳离子纳米乳佐剂的粒径分布及电位。
38.实施例10阳离子纳米乳佐剂和载抗原的阳离子纳米乳佐剂的形态观察:取实施例2中制备的纳米乳、实施例3中制备的阳离子纳米乳佐剂以及实施例5和6中制备的载抗原阳离子纳米乳佐剂滴加于铜网上,静置3min,然后用2%磷钨酸染色2min,并用滤纸吸走铜网上多余的染液,室温晾干样品,在200kv条件下观察样品,透射电镜观察。其中图3为实施例2中纳米乳电镜图;图4为实施例3中pcl
‑
pei修饰后的阳离子纳米乳佐剂透射电镜图;图5为实施例5中载模型抗原ova的阳离子纳米乳佐剂的透射电镜图;图6为实施例6中载抗原rureb的阳离子纳米乳佐剂的透射电镜图。
39.实施例11阳离子纳米乳佐剂增加抗原粘膜粘附性:荧光染料cy5标记的抗原ova,按照实施例5制备包载cy5
‑
ova的阳离子纳米乳佐剂,用1%戊巴比妥钠溶液对balb/c小鼠进行腹腔麻醉后,避光,各组取等量cy5
‑
ova 10μg,采取垂直体位给药,分组为游离抗原组(cy5
‑
ova)、未修饰纳米乳和ova的混合液(ne cy5
‑
ova)组、载抗原ova的阳离子纳米乳佐剂(cne
‑
cy5
‑
ova)组,将制备好的制剂滴入小鼠鼻腔,同时将未进行任何处理的同批次正常小鼠设为空白组。给药完毕后,利用活体成像仪分别在给药后0min、30min、60min、120min和150min对小鼠进行活体成像拍摄,观察鼻腔中cy5
‑
ova的荧光强度。结果显示如图7所示,游离cy5
‑
ova溶液组荧光60min时基本消失,表明游离cy5
‑
ova在鼻腔的滞留时间较短;ne cy5
‑
ova组在鼻腔的滞留时间延长至120min,但到150min时荧光完全消失;而cne
‑
cy5
‑
ova滞留时间显著延长,150min后仍有荧光滞留鼻腔,表明阳离子纳米乳佐剂利用表面正电性质显著增加抗原在鼻腔的粘附和滞留时间。
40.实施例12小鼠皮下免疫实验:按照实施例5制备包载ova阳离子纳米乳佐剂(cne
‑
ova),取鼠龄在6~8周的babl/c小鼠20只,随机分成4组:空白组、游离ova溶液组、ne ova组、cne
‑
ova组,各组等量ova 5μg免疫,于第0天初次免疫后,在第7天加强免疫一次,分别在初次免疫后第35天眼眶静脉取血,收集血清,稀释105后,elisa法测定血清中lgg、lgg1和lgg2a抗体水平。结果图8所示,包载抗原的阳离子纳米乳佐剂cne
‑
ova免疫小鼠后,血清中lgg、lgg1抗体水平相对于游离ova和ne ova组均有显著差异(数据分析采用单因素方差法进行各组之间均值的比较,**:p<0.1;***:p<0.01;****:p<0.001);上述结果表明双亲性阳离子材料
修饰后的阳离子纳米乳佐剂增强皮下接种疫苗免疫应答能力优于单一的纳米乳佐剂。
41.实施例13小鼠鼻腔免疫实验:按照实施例5制备包载ova阳离子纳米乳疫苗制剂(ne
‑
ova),取鼠龄在6~8周的babl/c小鼠20只,随机分成4组:空白组、游离ova溶液组、ne ova组、cne
‑
ova组,用1%戊巴比妥钠溶液对babl/c小鼠进行腹腔麻醉后,各组取等量ova 10μg,于第0天初次免疫后,在第7天加强免疫一次,在初次免疫后第35天眼眶静脉取血,收集血清,elisa法测定血清中lgg、lgg1和lgg2a抗体水平。结果如图9所示,血清稀释至107滴度后,cne
‑
ova免疫组小鼠血清中抗原特异性igg与igg1抗体水平显著高于其他组(数据分析采用单因素方差法进行各组之间均值的比较,****:p<0.0001);血清稀释至106滴度后,cne
‑
ova免疫组小鼠血清中抗原特异性igg2a与其他组具有显著性差异(数据分析采用单因素方差法进行各组之间均值的比较,****:p<0.0001),上述结果表明,双亲性阳离子材料修饰后的阳离子纳米乳佐剂增强了鼻腔疫苗的体液免疫应答。此外,取鼻腔灌洗液,elisa测定iga抗体水平,结果如图9所示,cne
‑
ova免疫组鼻腔灌洗液中iga抗体水平,显著高于其他组(数据分析采用单因素方差法进行各组之间均值的比较,****:p<0.0001)。上述结果表明阳离子纳米乳佐剂能够诱导黏膜(呼吸道)部位产生较高水平的黏膜抗体水平。考察免疫小鼠第7天至第75天血清阴道灌洗液中抗体水平情况,结果如图10所示,cne
‑
ova组lgg、lgg1、lgg2a、lga抗体水平均显著高于空白对照组、游离ova组和ne ova组。cne
‑
ova组lgg抗体水平从初次免疫后第7天开始上升,在第21~35天到达峰值,在第42天开始下降,至75天抗体水平逐渐接近空白对照组小鼠抗体水平。lgg1与lgg变化趋势一致,且抗体水平相当,lgg1下降趋势比lgg稍缓。cne
‑
ova组lgg2a抗体水平在第7天上升,在28天到达峰值,其峰值时间较短,35天开始下降,至65天接近空白对照组小鼠抗体水平。阴道灌洗液中lga抗体水平从第7天到第75天具有缓慢上升和缓慢下降的过程,35天到达峰值。上述总体结果表明,阳离子纳米乳佐剂能够不仅能够增强鼻腔疫苗的系统性免疫应答,同时也显著提高疫苗的粘膜免疫应答能力,后者对于粘膜感染性疾病尤其重要。
42.实施例14载rureb的阳离子纳米乳佐剂的免疫效果:按照实施例6制备包载rureb的阳离子纳米乳制剂(ne
‑
rureb)。取鼠龄在6~8周的babl/c小鼠20只,随机分成4组:空白对照组、游离rureb组、纳米乳和rureb的混合液组(ne rureb)、制剂组ne
‑
rureb,用1%戊巴比妥钠溶液对小鼠进行腹腔麻醉后,各组取等量rureb 20μg,采取垂直体位,将制备好的制剂溶液滴入小鼠鼻腔,于第0天初次免疫后,在第7天加强免疫一次,在初次免疫后第28天取血清和鼻腔灌洗液,用elisa法测定阴道灌洗液中抗体水平。结果如图11所示,ne
‑
rureb鼻腔免疫后iga、lgg、lgg1和lgg2a抗体水平均显著高于其他实验组(数据分析采用单因素方差法进行各组之间均值的比较,*:p<0.05,**:p<0.01,***:p<0.001),上述结果表明阳离子纳米乳佐剂能够提高多种疫苗的粘膜免疫效力。
43.以上所述实施例证明,本发明提供一种阳离子纳米乳佐剂,其性质稳定性,分散均一,能够成功包载抗原。阳离子纳米乳佐剂能够显著提升皮下接种疫苗免疫效力,还能克服粘膜免疫屏障,显著提升粘膜接种疫苗的免疫应答能力,可见本发明所提供的阳离子纳米乳佐剂能够弥补现有技术的不足,并具有一定的临床应用潜力。
44.以上所述仅是本发明的优选实施例而已,并非对本发明做任何形式上的限制,虽
然本发明已以优选实施例揭露如上,然而并非用以限定本发明,任何熟悉本专业的技术人员,在不脱离本发明技术方案的范围内,当可利用上述揭示的技术内容做出些许更动或修饰为等同变化的等效实施例,但凡是未脱离本发明技术方案的内容,依据本发明的技术实质对以上实施例所做的任何简单修改、等同变化与修饰,均仍属于本发明技术方案的范围内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。